É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Preparação Facile de derivados de quinazolina 4-substituída
Neste Artigo
Resumo
A protocol for facile preparation of 4-substituted quinazoline derivatives from 2-aminobenzophenones, thiourea and dimethyl sulfoxide is presented.
Resumo
Relatado no presente documento é um método muito simples para a preparação directa de derivados de quinazolina 4-substituída a partir de uma reacção entre o composto 2-aminobenzof enonas e tioureia na presença de sulfóxido de dimetilo (DMSO). Este é um sistema de reacção complementar único, no qual tioureia sofre decomposição térmica para formar carbodiimida e sulfureto de hidrogénio, em que os antigos reage com 2-aminobenzofenona para formar 4-fenilquinazolina-2 (1H) -imine intermédia, enquanto que o sulfureto de hidrogénio reage com DMSO para dar metanotiol ou outra molécula que contém enxofre, o qual, em seguida, funciona como um agente redutor para reduzir complementar 4-fenilquinazolina-2 (1H) -imine intermédio em 4-fenil-1,2-di-hidroquinazolin-2-amina. Subsequentemente, a eliminação de amoníaco a partir de 4-fenil-1,2-di-hidroquinazolin-2-amina proporciona derivado de quinazolina substituídos. Esta reacção geralmente dá derivado de quinazolina como um único produto resultante a partir de 2-aminobenzofenona como monitorizada por CG / EManálise, juntamente com uma pequena quantidade de moléculas contendo enxofre tais como dissulfureto de dimetilo, trissulfureto de dimetilo, etc. A reacção geralmente completa em 4-6 horas a 160 ºC em escala pequena, mas pode durar mais de 24 horas quando efectuada em larga escala. O produto da reacção pode ser facilmente purificado por meio de lavagem com água fora DMSO seguido por cromatografia em coluna ou cromatografia em camada fina.
Introdução
Quinazolinas substituídas, como um único tipo de heterociclos, foram conhecidas para uma variedade de actividades biológicas, incluindo a antibiótico, um antidepressivo, 2 anti-inflamatório, anti-hipertensiva 3,4, 3 antimalárico, 5 e anti-tumoral, 6 entre outros . O que é quinazolinas mais, 4-substituídos, por exemplo, 4-aril-quinazolinas, com actividade anti-plasmodial 7 foram reconhecidas como inibidores do receptor do factor de crescimento epidérmico (EGFR) de tirosina cinase, 8 depressores do SNC, 9 e antibióticos contra o Staphylococcus aureus resistente à meticilina aureus e Enterococcus faecalis resistentes a vancomicina. 10 Devido ao seu largo espectro de actividades biológicas, os métodos sintéticos para quinazolinas substituídas têm sido amplamente explorados. Como um exemplo, mais de 25 métodos sintéticos já têm sido relatados para a preparação de 4-phenylquinazolines. 11 Repmétodos sentante incluem a formação de 4-phenylquinazolines partir de 2-aminobenzof enonas e formamida na presença de eterato de trifluoreto de boro (BF3 Et2O) 12 ou ácido fórmico, 13 ou a partir da reacção de 2-aminobenzofenonas com urotropine e bromoacetato de etilo, 14 ou a reacção com o aldeído e acetato de amónio na presença de um agente oxidante. 15
Diferente das reacções acima, utilizando o reagente sensível à humidade (por exemplo, BF3 Et2O) ou reagente caro (por exemplo, urotropine e bromoacetato de etilo), um método fácil, que possa facilmente converter 2-aminobenzofenonas na correspondente 4-phenylquinazolines em sulfóxido de dimetilo ( DMSO), na presença de tioureia tem sido explorado. Estudos mecanicistas extensivamente nesta reacção indicar que é uma reacção na qual complementar tioureia sofre decomposição térmica para formar e carbodiimidasulfureto de hidrogénio, em que carbodiimida reage com 2-aminobenzofenona para formar 4-fenilquinazolina-2 (1H) -imine intermédia, enquanto DMSO é usado não apenas como um solvente, mas também o reagente para gerar um reagente redutor quando reage com hidrogénio sulfurado- sulfureto (também resultantes da tioureia). Em seguida, os agentes redutores contendo enxofre reduzir o 4-fenilquinazolina-2 (1H) -imine intermediário para formar 4-fenil-1,2-di-hidroquinazolin-2-amina que é submetido a eliminação do amoníaco para formar 4-fenilquinazolina. Esta reacção é geralmente levada a cabo à temperatura 135-160 ° C, e pode ser facilmente realizada por meio de aquecimento do banho de óleo tradicional em placa de aquecimento ou sob irradiação de microondas. Esta reacção é geralmente ilustrado na Figura 1 abaixo.
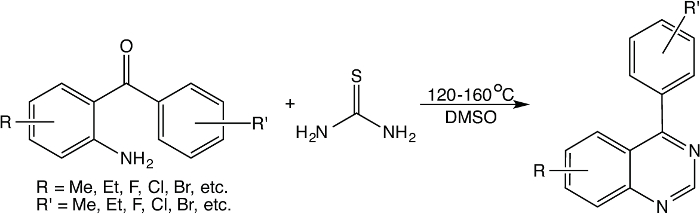
Figura 1: A reacção geral entre 2-aminobenzofenona etioureia em DMSO. Por favor clique aqui para ver uma versão maior desta figura.
Protocolo
Cuidado: Por favor, consulte todas as folhas de dados de segurança pertinentes (MSDS) antes do uso. Enquanto 2-aminobenzofenonas são inodoras, algumas moléculas contendo enxofre são geradas nesta reacção. Portanto, deve sempre ser usado em bom estado de ventilação. Por favor, use toda a prática de segurança adequado ao realizar as reacções à temperatura mais elevada do que 140 ° C, como a pressão pode ir acima de 5 bares como registrado sob irradiação de microondas. Quando a temperatura é regulada a 160 ° C, a pressão é mais elevada registada barras 21, que é quase o limite superior do reactor de microondas pode manipular. Embora a pressão não é um problema quando a reacção é realizada em banho de óleo sob refluxo, uma boa ventilação deve ser sempre utilizado.
1. Preparação de 4-fenilquinazolina em pequena escala Sob irradiação de microondas
- Preparação da Mistura de Reacção
- Adicionar uma barra de agitação magnética compatível a um tubo de reacção de 2-5 ml de microondas.
- Use balança analítica e pesa 0,0866 g de 2-aminobenzofenona (pó amarelo), 0,0988 g de tioureia (cristais brancos, 3 equivalentes) para dentro do tubo de reacção acima.
Nota: A relação ideal entre 2-aminobenzofenona e tioureia é de 1: 3. - Transferência de 5 ml de DMSO ao tubo de reacção.
Nota: A quantidade de DMSO é bastante flexível, 5 ml de DMSO é apenas sobre o suficiente para atender a exigência mínima do volume para a absorção correta de microondas de acordo com o manual do fabricante. Contudo, sob condição térmica, muito menos solvente é necessário para a reacção deste escala. - Selar o tubo de reacção com uma tampa de alumínio compatível contendo borracha de entrada de septo.
- Agitar vigorosamente o tubo em um agitador por 1-2 min para dissolver os reagentes.
Nota: A tioureia pode não se dissolvem completamente em DMSO à temperatura ambiente, mas que se dissolvem completamente quando o calor é aplicado. - Utilize uma micro-seringa para retirar 5 ul de mistura reaccional para um copo de 2 ml sampling tubo contendo 0,35 ml de acetato de etilo (EtOAc) para cromatografia em fase gasosa / espectroscopia de massa (GC / MS) de análise antes de iniciada a reacção.
- A formação de 4-fenilquinazolina Sob irradiação de microondas
- Ligue reactor de microondas, coloque o tubo de reacção de microondas em um dos oito titulares de tubo.
- Configuração de reacção por meio de parâmetros de ecrã táctil, tal como a localização do tubo (por exemplo, a partir do poço 1 a 8), tipo de tubo (por exemplo, 2-5 mL), temperatura de reacção (a 150 ° C), a duração pré-agitação (1 min), o nível de absorção de microondas (elevado), velocidade de agitação (600 rpm), e tempo de reacção (5 horas).
- Uma vez que todos os parâmetros estão configurados corretamente, clique no botão "Run", o robô irá automaticamente pegar o tubo de reacção do titular do tubo (ou bem) e colocá-lo dentro do buraco de aquecimento. Em seguida, o reactor de microondas irá executar a reacção de acordo com os parâmetros definidos anteriormente.
- Quando irradiação de microondas completa, wait até que a temperatura cai para cerca de 30 ºC, o robô vai pegar o tubo de reacção e colocá-lo de volta para o titular original.
- Use micro-seringa para retirar 5 ul de mistura reaccional (solução amarela límpida, nenhuma substância insolúvel observado) e adicioná-lo a um outro tubo de amostragem de vidro de 2 ml contendo 0,35 ml de EtOAc para análise por GC / MS.
- Como a análise por CG / EM indica que a reacção está apenas metade completa, configurar a reacção de microondas ao mesmo tubo durante mais 5 h à mesma temperatura.
Nota: O tempo de reacção varia dependendo da quantidade de material de partida utilizado, a concentração da solução de reacção, os grupos substituintes no grupo 2-aminobenzof enonas, e mais importante ainda, a temperatura de reacção. Por exemplo, uma reacção de 0,3 g de 2-aminobenzofenona em 3 ml de DMSO vai completar em 6 h a 160 ° C, mas mais dura do que 14 h a 140 ° C, sob irradiao com microondas, tanto de aquecimento e placa de aquecimento. Recomenda-se também para monitorar a reação periodically com GC ou análise GC / MS. Pessoas sem acesso a GC ou GC / MS deve então usar cromatografia em camada delgada (TLC) para monitorar a reação, embora não seja a melhor ferramenta.
- GC / MS Análise de Mistura de Reacção
- Certifique-se de GC / MS está configurado corretamente de acordo com o protocolo do fabricante.
- Coloque os tubos de amostragem de vidro no tabuleiro amostrador automático.
- Clique em "GCMS_3" atalho no monitor para iniciar o programa de aquisição de dados que controla e coordena as funções de injector, GC e espectrômetro de massa. Carregar um método adequado clicando no "Método" no menu drop-down e destacando "Método de carga." O método selecionado contém todos os parâmetros necessários para as qualidades GC e espectrômetro de massa quádruplo para analisar as amostras-alvo. Se não existe tal método, criar um método necessário.
- Para uma nova amostra, se modificar alguns dos parâmetros de GC para atender a uma determinada amostra, realce o "Editar entire Método ", clicando em" Método "do menu drop-down e alterar os parâmetros relevantes em conformidade. Os parâmetros de GC que muitas vezes são alterados são a temperatura inicial ea duração para manter essa temperatura, a taxa de aumento da temperatura, a temperatura final ea duração para manter a temperatura, a quantidade de injecção, as vezes para lavar a agulha de injecção, antes e após a injecção, o tempo de equilíbrio e pós correr do tempo, e a temperatura de pós de execução.
- Para esta experiência, ajustar a temperatura inicial GC em 70 ° C (1 min), com uma taxa de aumento da temperatura a 20 ° C / min, e a temperatura final a 250 ° C (5 min). Use um tempo total de 15 minutos. Utilizar um volume de injecção de 2 mL, com 4 de pré-lavagem e depois 4-lavagens de agulha. Use hélio puro como gás de transporte utilizado sob esta condição.
Nota: Um método para a análise GC / MS contém os parâmetros pré-definidos para executar tanto instrumentos MS GC e. Os parâmetros foR GC incluem a temperatura inicial do forno para aquecer a coluna de GC e o número de minutos, para reter essa temperatura, a taxa para elevar a temperatura do forno, a temperatura final do forno e o número de minutos para manter a temperatura final antes do A análise por CG completa; a quantidade de amostra injectada; a taxa de divisão do gás portador; o número de vezes para lavar a agulha antes da amostra é injectado; e o número de vezes para lavar a agulha depois de a amostra é injectada; etc. A escolha de temperaturas iniciais e finais, bem como a taxa de aumento da temperatura depende da natureza da amostra analisada. Em geral, as moléculas não-polares de baixos pontos de ebulição são analisadas a temperaturas relativamente baixas inicial.
- Sintonize o Espectrômetro de Massa De acordo com o protocolo do fabricante.
- Depois de um método de execução é selecionado, clique em "Instrument" no topo do menu drop-down e selecione "Tune MSD." Em seguida, outra janelaaparece na frente da janela de aquisição de dados. Pode-se escolher qualquer um "Tune MSD" ou "QuickTune" e clique no botão "OK" para iniciar o processo de ajuste de espectrômetro de massa. A opção "QuickTune" leva cerca de 3 minutos para ser concluída, enquanto que a opção "Tune MSD" corre cerca de 10 min. Sob circunstâncias normais, a opção "QuickTune" é bom o suficiente para calibrar o espectrômetro de massa com uma precisão até 0,1 Dalton. O processo de sintonização vai medir a abundância relativa do pico de 69, 219 e 502 de perfluorotributilamina (PFTBA), bem como a quantidade de N 2, O 2, H 2 O, CO 2, etc.
Nota: O espectrómetro de massa deve ser calibrado em cada dois dias, a fim de ter uma medição precisa da massa. A afinação é para ajustar os parâmetros para o espectrómetro de massa para funcionar correctamente, tais como a tensão de quádruplo, vácuo de um detector de massa, o ruído de fundo, os picos do padrão para medir o espectrómetro de massa,etc Pode-se escolher o modo sintonia manual de auto-ajuste ou para calibrar o espectrômetro de massa, ou seja, selecionando "QuickTune" ou opção "Tune MSD".
- Depois de um método de execução é selecionado, clique em "Instrument" no topo do menu drop-down e selecione "Tune MSD." Em seguida, outra janelaaparece na frente da janela de aquisição de dados. Pode-se escolher qualquer um "Tune MSD" ou "QuickTune" e clique no botão "OK" para iniciar o processo de ajuste de espectrômetro de massa. A opção "QuickTune" leva cerca de 3 minutos para ser concluída, enquanto que a opção "Tune MSD" corre cerca de 10 min. Sob circunstâncias normais, a opção "QuickTune" é bom o suficiente para calibrar o espectrômetro de massa com uma precisão até 0,1 Dalton. O processo de sintonização vai medir a abundância relativa do pico de 69, 219 e 502 de perfluorotributilamina (PFTBA), bem como a quantidade de N 2, O 2, H 2 O, CO 2, etc.
- Adquirir o GC / MS de dados
- Editar sequência de aquisição de dados. Clique no botão "Sequence" no topo do menu drop-down para realçar "Editar Seqüência", e uma nova janela aparece, em que as informações sobre as amostras devem ser de entrada, tais como o tipo de amostra (amostra, em branco, calibração, QC , etc.), a localização do frasco de amostras (de 1 a 100), nome da amostra, o nome do arquivo de dados, comentários de amostra, etc. Quando todas as informações da amostra foi de entrada, clique no botão "OK". Em seguida, clique no botão "Sequence" no topo do menu drop-down para realçar "Guardar sequência como .." e insira o nome da seqüência em uma pasta adequada.
- Obter os dados GC / MS. Clique no botão "Sequence" no topo do menu drop-down para realçar "Run Sequence", escolhaum "directório de arquivo de dados" adequada para salvar os dados adquiridos e, em seguida, clique no botão "Run Sequence" para iniciar o processo de aquisição de dados.
- Analisar os GC / MS Resultados
Nota: As moléculas podem ser caracterizados pelos minutos eles são eluídos a partir da coluna GC, chamado o tempo de retenção. Sob a mesma condição GC (isto é, os parâmetros acima mencionados GC), o tempo de retenção de uma molécula particular, é muito reprodutível. O composto pode ainda ser confirmada pelo seu espectro de massa. Pode-se facilmente identificar um composto, em termos de tempo de retenção e o espectro de massa, e verificar a pureza de um composto bem.- Dê um duplo clique no atalho "Análise de Dados GCMS_3" no monitor para abrir o software que, deliberadamente, processa os dados adquiridos a partir do GC máquina / MS.
- Durante o processo de aquisição de dados, para ver o resultado imediato da amostra analisada, clique em "Arquivo" no menu suspenso e highlig baixoht "Take Snapshot" para obter o espectro de GC sincronizada de amostra. Muitas vezes, as pessoas vão processar os dados após o processo de aquisição seja concluída. Neste caso, clique em "Arquivo" no menu drop-down para realçar "Carregar arquivo de dados" e selecione o arquivo de dados correto, ou navegue na lista de dados e clique duas vezes no arquivo de dados, para mostrar todo o espectro GC da amostra. Uma linha vertical aparece na posição onde o mouse é apontado para dentro da janela do espectro GC.
- Mova o mouse para o centro de um pico onde a linha vertical atinge o ponto mais alto do pico, e dê um duplo clique no botão direito do mouse para abrir o espectro de massa da amostra em uma nova janela abaixo da janela do espectro GC. Pode-se aumentar o espectro de massa, segurando o botão esquerdo e selecione a região para aumentar para o detalhe de espectro de massa.
- Identificar os compostos com um duplo clique no botão direito do rato dentro da janela espectro de massa para obter duas novas janelas. O pequenojanela da frente com um nome de "PBM Resultados da Pesquisa: C: Database W8N08.L" traz 20 moléculas do banco de dados que provavelmente coincide com o espectro de massa analisados, e classifica as 20 moléculas, a fim de suas semelhanças. A grande janela traseira contém dois painéis, dos quais o painel superior exibe o espectro de massa inicial do pico analisados dentro do espectro de GC, eo painel inferior mostra o espectro de massa da molécula seleccionada da lista de pequena janela da frente. Muitas vezes, os compostos orgânicos comuns pode ser confirmada por comparação do seu espectro de massa com o espectro de massa padrão recolhidas na base de dados. Embora os novos compostos ou moléculas não recolhidas na base de dados não podem ser confirmadas directamente, as suas identidades podem ser obtidos através da comparação do peso molecular esperado e os fragmentos possíveis com as suas estruturas.
- Identificar o mesmo composto em diferentes amostras por comparação do seu tempo de retenção no espectro de GC. Sob a mesma condição de acqu de dadosisition, o mesmo composto deve aparecer com o mesmo tempo de retenção no espectro GC.
- Analisar a pureza da amostra clicando no botão "Cromatograma" no menu drop-down, com destaque para qualquer um "Integrar" ou "AutoIntegrate", e selecionando "Relatório por cento".
- Imprimir ambos espectro de GC e de massa correspondente aos picos dentro do espectro de GC no formato retrato ou paisagem, selecionando "Configuração da impressora" quando um clique em "Arquivo" no menu drop-down. Além disso, imprimir os espectros diretamente em formato pdf, selecionando um conversor de pdf.
- Extracção de Mistura de Reacção
Nota: O processo de isolamento foi realizado no exaustor de fumos, como pequena quantidade de moléculas contendo enxofre com cheiro desagradável são geradas nesta reacção.- Abrir o tubo reaccional de microondas com o fabricante fornecida alicate, e transferir a mistura reaccional para uma ampola de decantação de 125 ml. UMAdd 20 ml de EtOAc para este funil seguido por 10 ml de água.
Nota: Se a solução de reacção é deixada à temperatura ambiente durante um dia, os cristais de forma longa agulha pode aparecer na solução, dependendo da concentração da solução. Assim, é aconselhável deixar a mistura de reacção em grande escala, à temperatura ambiente para formar cristais e isolar o produto de cristal directamente se o tempo não é um factor. - Agitar a ampola de decantação vigorosamente, e drenar a camada aquosa inferior. Em seguida, adicione mais 10 ml de água para a ampola de decantação, e repita este processo.
- Concentra-se a solução de EtOAc restante para baixo para cerca de 1 mL por evaporação rotatória.
- Abrir o tubo reaccional de microondas com o fabricante fornecida alicate, e transferir a mistura reaccional para uma ampola de decantação de 125 ml. UMAdd 20 ml de EtOAc para este funil seguido por 10 ml de água.
- Purificação de 4-fenilquinazolina por TLC preparativa
- Transferir a solução EtOAc foi concentrada com uma pipeta de Pasteur a 20 cm x 20 cm de placa de CCF preparativa de uma maneira tal que a faixa de amostra na placa de TLC é inferior a 1 cm de largura e é de cerca de 1 cm do bordo. Mergulhe esta placa a uma ABLSS câmara contendo 150 ml de hexano e EtOAc (2: 1). Observar o movimento da fronteira solvente se aproximando do topo da placa de TLC, e tirar a placa quando fronteira solvente é de cerca de 1 cm da borda superior.
- Desenhe duas linhas retas na placa TLC com lápis para marcar o local antes da amostra é carregada. Além disso, mergulhar a placa de TLC em câmara de vidro de tal maneira que a faixa de amostra é, na parte inferior, mas ainda de cerca de 2 mm acima do nível de solvente.
- Sob ultra-violeta (UV), use um lápis para marcar a banda com fluorescência verde e raspe a banda marcada na placa de TLC com um papel de pesagem (com uma mobilidade relativa de R f = 0,68, hexano / AcOEt = 2 : 1).
Nota: Devido à alta sensibilidade da absorção de UV, pode-se observar várias bandas fracas na placa. No entanto, as principais bandas muito frequentemente correspondem a moléculas contendo enxofre, como dissulfureto de dimetilo, trissulfureto de dimetilo; Outras bandas abaixo de 4 fenilquinazolina são visiblE, mas a sua quantidade é demasiado pequena para ser isolado e caracterizado. - Para uma pipeta de vidro preenchido com lã de vidro, a transferência do pó de gel de sílica riscado à pipeta dobrando o papel de pesagem diagonalmente para permitir que o pó de gel de sílica desce para a pipeta, e toque da pipeta contra uma superfície dura para embalar o gel de sílica apertado . Lava-se a pipeta com acetona (8-15 ml) para um frasco de cintilação de 2-cilindro.
- Transferir 0,35 ml da solução de acetona eluída a um outro tubo de amostragem de 2 ml de vidro para a análise de GC / MS, e secar directamente a solução de acetona restante num evaporador rotativo. Colocar todo o frasco de cintilação contendo o composto purificado em exsicador de vácuo para posterior secagem.
Nota: Até este passo, o produto é purificado e pode ser utilizado para a caracterização adicional (por exemplo, a ressonância magnética nuclear (RMN)) ou transformações adicionais.
- Transferir a solução EtOAc foi concentrada com uma pipeta de Pasteur a 20 cm x 20 cm de placa de CCF preparativa de uma maneira tal que a faixa de amostra na placa de TLC é inferior a 1 cm de largura e é de cerca de 1 cm do bordo. Mergulhe esta placa a uma ABLSS câmara contendo 150 ml de hexano e EtOAc (2: 1). Observar o movimento da fronteira solvente se aproximando do topo da placa de TLC, e tirar a placa quando fronteira solvente é de cerca de 1 cm da borda superior.
2. Preparação de 4-fenilquinazolina in Pequena Escala via Hotplate Aquecimento
Nota: Os procedimentos para a análise de GC / MS da mistura reaccional, extracção da mistura de reacção, e a purificação do produto da reacção são muito semelhantes aos descritos na secção 1 (1.1.1-1.3.4, 1.4.1-1.4.3 , e 1.5.1-1.5.5, respectivamente), de modo que a maior parte destas etapas podem ser omitidas abaixo.
- Preparação da mistura de reacção para o aquecimento placa de aquecimento
- Pesar 0,0240 g de 2-aminobenzofenona e 0,0280 g de tioureia em um frasco de vidro de 2 ml, em seguida, transferir 0,5 mL de DMSO para o mesmo frasco, e fechar o frasco com uma tampa de rosca.
Nota: A quantidade de DMSO utilizada sob esta condição é muito menor do que aquela sob irradiação de microondas. Devido à pequena dimensão da presente reacção, sob agitação magnética não é mais necessário, portanto, para a agitação da solução vortex para dissolver os reagentes. No entanto, numa escala de reacção relativamente grande, por exemplo, em 2 de tambor frasco de cintilação ou frasco de fundo redondo, de agitação magnéticaainda é necessário.
- Pesar 0,0240 g de 2-aminobenzofenona e 0,0280 g de tioureia em um frasco de vidro de 2 ml, em seguida, transferir 0,5 mL de DMSO para o mesmo frasco, e fechar o frasco com uma tampa de rosca.
- Preparação de 4-fenilquinazolina através Placa eléctrica de aquecimento
- Dentro exaustor, colocar um bloco de aquecimento em cima do fogão, e a temperatura ajustada para 160 ° C.
- Quando a temperatura atinge 160 ° C, inserir o frasco de vidro em um dos poços em bloco de aquecimento. Com cerca de meia hora de intervalo, levar para fora do frasco e mão agitá-lo durante 2-3 segundos, e colocá-lo de volta para o bem novamente. Após 6 horas, retirar do frasco e deixá-lo no interior do exaustor para esfriar.
- Transferência de 5 ul da mistura reaccional para outro tubo de amostragem de vidro de 2 ml contendo 0,35 ml de EtOAc, e submeter a amostra para análise por GC / MS.
- Uma vez que a reacção completa, exercitar-se o produto como descrito no capítulo 1. Veja os detalhes na seção 1.1.1-1.3.4, 1.4.1-1.4.3 e 1.5.1-1.5.5 para análise por CG / MS, extracção da mistura de reacção, e a purificação do produto, respectivamente.
Resultados
A análise por GC da mistura da reacção antes da reacção, após 5 h de reacção sob irradiação de microondas, e 10 h após a reacção sob irradiação de micro-ondas a 150 ° C são apresentados na Figura 2, que ilustra claramente o processo desta reacção limpo. Os espectros de massa de 2-aminobenzofenona e 4-fenilquinazolina são apresentados na Figura 3 e Figura 4, respectivamente. Um mecanis...
Discussão
Esta reacção limpo (como mostrado na Figura 2) aparece muito intrigante no início como o peso molecular do produto é aumentado apenas por 9 no que diz respeito ao do material de partida (como se mostra na Figura 3 e Figura 4). Isso parece impossível, porque o peso atómico do carbono é 12. Muito provavelmente, a introdução de um átomo de carbono numa molécula irá aumentar o peso molecular de, pelo menos 12, se o átomo de hidrogénio de acompanhamento (s) nã...
Divulgações
Except for the contents described in patent (pending), the authors have nothing else to disclose.
Agradecimentos
The financial support from the National Science Foundation (NSF, grant number 0958901), the Robert Welch Foundation (Welch departmental grant BC-0022 and the Principal Investigator grant BC-1586), and the University of Houston-Clear Lake (FRSF grant) are greatly appreciated.
Materiais
| Name | Company | Catalog Number | Comments |
| 2-Aminobenzophenone | Alfa Aesar | A12580 | 98% purity, with tiny impurity as seen on Figure 1(A) in the manuscript. |
| Thiourea | Acros | 138910010 | 1 kg package, 99%, extra pure |
| Dimethyl Sulfoxide | Acros | 326880010 | Methyl sulfoxide, 99.7+%, Extra Dry, AcroSeal® |
| N,N-Dimethylformamide | Acros | 348430010 | N,N-Dimethylformamide, 99.8%, Extra Dry over Molecular Sieve, AcroSeal® |
| Ethyl Acetate | Acros | 610170040 | Ethyl acetate, used as solvent for GC/MS analysis |
| Preparative TLC plate | Sigma-Aldrich | Z740216 SIGMA | PTLC (Preparative TLC) Glass Plates from EMD/Merck KGaA |
| Rotavapor | Buchi | Rotavapor R-205 | Use to dry solvent |
| Microwave Reactor | Biotage | Initiator+ | Use to carry out chemical reaction under microwave irradiation |
| Hotplate | IKA | RCT basic | use to carry out thermal chemical reaction |
Referências
- Kamal, A., Reddy, K. L., Devaiah, V., Shankaraiah, N., Rao, M. V. Recent Advances in the Solid-Phase Combinatorial Synthetic Strategies for the Quinoxaline, Quinazoline and Benzimidazole Based Privileged Structures. Mini-Rev. Med. Chem. 6 (1), 71-89 (2006).
- Spirkova, K., Stankovsky, S. Some Tricyclic Annelated Quinazolines. Khim. Geterotsikl. Soedin. (10), 1388-1389 (1995).
- Connolly, D. J., Cusack, D., O'Sullivan, T. P., Guiry, P. J. Synthesis of Quinazolinones and Quinazolines. Tetrahedron. 61 (43), 10153-10202 (2005).
- Baba, A., et al. Studies on Disease-Modifying Antirheumatic Drugs: Synthesis of Novel Quinoline and Quinazoline Derivatives and Their Anti-Inflammatory Effect. J. Med. Chem. 39 (26), 5176-5182 (1996).
- Gama, Y., Shibuya, I., Simizu, M. Novel and Efficient Synthesis of 4-Dimethylamino-2-Glycosylaminoquinazolines by Cyclodesulfurization of Glycosyl Thioureas with Dimethylcyanamide. Chem. Pharm. Bull. 50 (11), 1517-1519 (2002).
- Wakeling, A. E., et al. Specific Inhibition of Epidermal Growth Factor Receptor Tyrosine Kinase by 4-Anilinoquinazolines. Breast Cancer Res Treat. 38 (1), 67-73 (1996).
- Verhaeghe, P., et al. Synthesis and Antiplasmodial Activity of New 4-Aryl-2-Trichloromethylquinazolines. Bioorg. Med. Chem. Lett. 18 (1), 396-401 (2008).
- Kitano, Y., Suzuki, T., Kawahara, E., Yamazaki, T. Synthesis and Inhibitory Activity of 4-Alkynyl and 4-Alkenylquinazolines: Identification of New Scaffolds for Potent Egfr Tyrosine Kinase Inhibitors. Bioorg. Med. Chem. Lett. 17 (21), 5863-5867 (2007).
- Goel, R. K., Kumar, V., Mahajan, M. P. Quinazolines Revisited: Search for Novel Anxiolytic and Gabaergic Agents. Bioorg. Med. Chem. Lett. 15 (8), 2145-2148 (2005).
- Parhi, A. K., et al. Antibacterial Activity of Quinoxalines, Quinazolines, and 1,5-Naphthyridines. Bioorg. Med. Chem. Lett. 23 (17), 4968-4974 (2013).
- Brown, D. J. . Chemistry of Heterocyclic Compounds, Volume 55: Quinazolines, Supplement I. , (1996).
- Yang, C. -. H., et al. Color Tuning of Iridium Complexes for Organic Light-Emitting Diodes: The Electronegative Effect and -Conjugation Effect. J. Organomet. Chem. 691 (12), 2767-2773 (2006).
- Byford, A., Goadby, P., Hooper, M., Kamath, H. V., Kulkarni, S. N. O-Aminophenyl Alkyl/Aralkyl Ketones and Their Derivatives. Part V. An Efficient Synthetic Route to Some Biologically Active 4-Substituted Quinazolines. Ind. J. Chem. B. 27 (4), 396-397 (1988).
- Blazevic, N., Oklobdzija, M., Sunjic, V., Kajfez, F., Kolbah, D. New Ring Closures of Quinazoline Derivatives by Hexamine. Acta Pharmaceut. Jugo. 25 (4), 223-230 (1975).
- Panja, S. K., Saha, S. Recyclable, Magnetic Ionic Liquid Bmim[Fecl4]-Catalyzed, Multicomponent, Solvent-Free, Green Synthesis of Quinazolines. RSC Adv. 3 (34), 14495-14500 (2013).
- Wang, Z. D., Eilander, J., Yoshida, M., Wang, T. Mechanistic Study of a Complementary Reaction System That Easily Affords Quinazoline and Perimidine Derivatives. Eur. J. Org. Chem. (34), 7664-7674 (2014).
- Wang, D. Z., Yoshida, M., George, B. Theoretical Study on the Thermal Decomposition of Thiourea. Comput. Theoret. Chem. 1017, 91-98 (2013).
- Zhang, P., et al. Inhibitory Effect of Hydrogen Sulfide on Ozone-Induced Airway Inflammation, Oxidative Stress, and Bronchial Hyperresponsiveness. Am. J. Respir. Cell Mol. Biol. 52 (1), 129-137 (2015).
- Yan, J., et al. One-Pot Synthesis of Cdxzn1-Xs-Reduced Graphene Oxide Nanocomposites with Improved Photoelectrochemical Performance for Selective Determination of Cu2+. RSC Adv. 3 (34), 14451-14457 (2013).
- Keith, J. D., Pacey, G. E., Cotruvo, J. A., Gordon, G. Experimental Results from the Reaction of Bromate Ion with Synthetic and Real Gastric Juices. Toxicology. 221 (2-3), 225-228 (2006).
- Timchenko, V. P., Novozhilov, A. L., Slepysheva, O. A. Kinetics of Thermal Decomposition of Thiourea. Russ. J. Gen. Chem. 74 (7), 1046-1050 (2004).
- Wang, S., Gao, Q., Wang, J. Thermodynamic Analysis of Decomposition of Thiourea and Thiourea Oxides. J. Phys. Chem. B. 109 (36), 17281-17289 (2005).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados