Method Article
Flash NanoPrecipitation para o encapsulamento de compostos hidrofóbicos e hidrofílicos em nanopartículas poliméricas
Neste Artigo
Resumo
Flash NanoPrecipitation (FNP) é uma abordagem dimensionável para produzir nanopartículas poliméricas de núcleo-casca. Formulações de laboratório-escala para o encapsulamento de hidrofóbico ou hidrofílico terapêuticas são descritas.
Resumo
A formulação de um composto terapêutico em nanopartículas (NPs) pode lhes conferem propriedades únicas. Para drogas pouco solúveis em água, formulações de NP podem melhorar a biodisponibilidade e modificar a distribuição de drogas dentro do corpo. Para drogas hidrofílicas como peptídeos ou proteínas, encapsulamento dentro NPs também pode fornecer proteção contra os mecanismos naturais de apuramento. Existem algumas técnicas para a produção de polímero NPs que são escaláveis. Flash NanoPrecipitation (FNP) é um processo que usa engenharia mistura geometrias para produzir NPs com distribuições de tamanho estreito e tamanhos ajustáveis entre 30 e 400 nm. Este protocolo fornece instruções sobre a produção em escala laboratorial de nanopartículas poliméricas de núcleo-casca de um tamanho de destino usando a FNP. O protocolo pode ser implementado para encapsular compostos hidrofílicos ou hidrofóbicos, com apenas pequenas modificações. A técnica pode ser facilmente empregada em laboratório em escala miligrama para formulações de tela. Sucessos de chumbo diretamente podem ser escalados a escala grama e quilograma. Como um processo contínuo, escala envolve mais mistura tempo de processo executado em vez de tradução de novos navios de processo. Produzido pela FNP o NPs são altamente carregado com terapêutica, apresentam um pincel denso de polímero estabilizador e têm uma reprodutibilidade de tamanho de ± 6%.
Introdução
Desde a década de 1990, tem havido um aumento constante no número de ensaios clínicos empregando nanomateriais1,2. O crescente interesse reflete a promessa de nanomateriais para melhorar a biodisponibilidade de fármacos hidrofóbicos e habilitar o direcionamento preferencial dentro do corpo3. Nanopartículas poliméricas (referidas como nanopartículas ou NPs aqui) representam uma parte crescente desta classe de materiais2. O NPs tem atraído interesse porque eles têm propriedades altamente sintonizáveis como tamanho, composição e superfície functionalization4. Quando aplicado à administração de drogas pouco solúveis, NPs frequentemente têm um núcleo-estrutura onde a terapêutica é encapsulada no núcleo hidrofóbico e o shell é composto por uma escova de polímeros hidrofílicos. Uma maneira simples para gerar essa estrutura emprega um copolímero de diblock anfifílica (BCP) que consiste de um bloco hidrofóbico degradável, que faz parte do núcleo das partículas, e bloquear um poly(ethylene glycol) hidrofílico (PEG), que constitui o pincel de polímero e transmite o impedimento estérico4,5.
Nanoprecipitation é uma técnica comum de fabricação de nanopartículas poliméricas porque é simples e não de energia intensiva6. Em sua forma mais simples, nanoprecipitation envolve a adição com uma pipeta de componentes de NP em um solvente orgânico como a acetona, para um volume adicional de água mexido. A mudança de solvente de uma solução aquosa diluída resultados para a precipitação do componente núcleo insolúvel. O estabilizador monta nesta superfície crescente da partícula, dirigido por adsorção do bloco hidrofóbico recolhido8,7,9,10. Uma distribuição granulométrica uniforme é obtida quando o solvente e a água misturam rapidamente para formar uma solução homogênea. Que mistura é mais lenta que a nucleação e montagem dos resultados de componentes em uma maior, mais população de partículas polydisperse. Embora prontamente acessível para um teste simples, a abordagem do lote mexido resulta em grande variabilidade devido à inconsistência de mistura e não é passível de aumentar6,11. Microfluídica têm emergido como uma outra avenida para produção de NP que pode ser executada continuamente. Este meio de produção foi recentemente revisado por Ding et al 11 . Uma abordagem comum usa fluxo laminar com foco para reduzir a escala de comprimento de solvente para valores de submícron. Mistura do antisolvent ocorre por difusão, portanto, dimensões de pequeno fluxo são cruciais para garantir o uniforme de partículas11,12. Paralelização de múltiplas câmaras microfluidic para aumentar é problemática para volumes de grande produção.
As condições de mistura rápidas que favorecem nanoprecipitation uniforme em microfluídica, alternadamente, podem ser produzidas em confinados, escoamentos turbulentos. Flash NanoPrecipitation (FNP) emprega especiais mistura geometrias para alcançar essas condições sob maior caudal volumétrico que possível com microfluídica. Fluxos de entrada Introduza uma câmara de mistura em condições turbulentas que levam à geração de vórtices, lamelas de solvente/anti-co-solventes formam a escala de comprimento de difusão11,13. Assim, a mistura uniforme em uma escala de tempo mais curta do que a nucleação e crescimento da terapêutica é alcançado. A geometria confinada do mixer não permite fluxo ignorando da região onde ocorre dissipação de energia turbulenta, e o mesmo processo histórico13de experiências de todo o sistema. Nucleação ocorre uniformemente na câmara de mistura e crescimento de partícula continua até interrompida pela Assembleia do BCP sobre a superfície de9,14. O fluxo misto contendo partículas estáveis pode então ser diluído com antisolvent adicional para suprimir Ostwald amadurecimento do partículas15,16,17.
Um misturador colidindo confinados do jato (CIJ) é o mais simples projeto de misturador para FNP e permite a mistura de dois fluxos de forma escalável e contínuo, como mostrado na figura 1A13. Um mixer de entrada multi vórtice (MIVM) foi desenvolvido para permitir até quatro entradas de fluxo diferentes e ainda alcançar a rápida micromixing necessário para a formação de partículas uniformes, como mostrado na figura 1B18. FNP permite o rastreio de formulação simples que pode ser facilmente traduzido para produção em escala comercial. Devido à natureza contínua do processo, tamanhos de lotes maiores não exigem novos navios, mas prefiro mais tempos de execução, permitindo a simples tradução para produção em escala quilograma no mesmo comboio equipamentos.
Hidrofílicos compostos como peptídeos e proteínas ('biológicos') também podem ser encapsulados em um processo denominado inverso Flash NanoPrecipitation (iFNP). A técnica requer uma anfifílica BCP onde um quarteirão é hidrofóbico e o outro é um poliácida19. A etapa inicial envolve a mistura rápida de um fluxo de dimetil sulfóxido (DMSO) contendo o biológico e o BCP contra um solvente lipofílico como diclorometano ou clorofórmio. Isso resulta na formação de partículas estabilizado com o pincel de bloco hidrofóbicas. Aqui, tal uma arquitetura vai ser denominada um NP 'invertida'. O núcleo contém a poliácida, que é então ionically quitosana usando um cátion multivalentes. Isto estabiliza as partículas para a transformação em um ambiente aquoso, sob a forma de micropartículas ou nanopartículas PEG-revestido por técnicas que têm sido relatadas na literatura19,20,21.
Este protocolo pode ser empregado para a produção de lab-escala de poliméricas núcleo-casca nanopartículas encapsulando compostos hidrofóbicos ou hidrofílicos. As subseções do protocolo fornecem instruções sobre o uso de ambas as classes de misturador - a CIJ e o MIVM. O leitor deve ser capaz de adaptar o protocolo para componentes principais romance e gerar reproducibly nanopartículas de um tamanho desejado usando o misturador apropriado para as entradas de fluxo. Três formulações de exemplo usando a FNP e iFNP são apresentadas abaixo. Dois empregam o misturador da CIJ e requer o MIVM15,22. A primeira formulação demonstra o encapsulamento de um modelo hidrofóbico composto pela FNP. A segunda formulação demonstra o encapsulamento de um modelo hidrófilo composto por iFNP em um misturador CIJ. A formulação final fornece um exemplo de encapsulamento de proteína por iFNP usando um MIVM. O protocolo para esta formulação terceiro descreve o uso de um MIVM em pequena escala, de mão, denominado o 'μMIVM'. O projeto de misturador é menor para permitir o rastreio de formulação simplificada, mas o comportamento de dimensionamento é bem compreendido e a batedeira não é um dispositivo de microfluidic22. A seção final do protocolo inclui algumas notas sobre escala de formulações de chumbo identificadas na triagem. Estas formulações são destinadas a fornecer pontos de acesso para o processo de aprendizagem e consequentemente usar não-degradáveis poli (estireno)-com base em polímeros. Estabilizadores alternativos têm sido descritos na literatura, com um número de opções comerciais biocompatível disponível14,23,24.
Protocolo
1. encapsulação de compostos hidrofóbicos em polímero NPs usando um misturador CIJ
- Preparar e limpar o equipamento.
- Adquirir e validar um misturador da CIJ.
Nota: Ver Informações complementares seção 1 para orientação de construção. Arquivos CAD também estão disponíveis como Informação suplementar . - Antes de cada utilização, certifique-se de que todos os encaixes na mesa de mixagem CIJ são confortáveis e o tubo de saída não é dobrado ou amassado.
- Em uma coifa, anexe uma seringa de fecho luer 5ml contendo 2-3 mL de solvente para cada adaptador de entrada. Selecione um solvente (por exemplo, acetona) que irá limpar quaisquer compostos usados recentemente na batedeira.
Nota: As seleções típicas são acetona ou tetrahidrofurano (THF). Só uso polipropileno seringas para evitar problemas de compatibilidade de solvente como a lixiviação. Não utilize seringas com êmbolos de vedação o-ring de borracha. - Defina o assembly da CIJ sobre um recipiente de resíduos.
Nota: Um frasco com uma abertura menor do que o corpo da CIJ funciona bem como isso suporta o mixer e permite operação fácil das seringas. - Pressione firmemente os êmbolos de seringa para esvaziar o conteúdo através da câmara de mistura durante alguns segundos. Retire as seringas.
Nota: As seringas podem ser retidas e reutilizadas para várias rodadas de limpeza entre as execuções FNP. - Seca a parte interna do misturador CIJ usando um fluxo de2 N. Um adaptador luer macho na extremidade de uma linha de2 N é eficaz.
Nota: Se o solvente de limpeza não é volátil (por exemplo, DMSO), repita as etapas 1.1.3-1.1.5 com acetona ou THF antes de prosseguir para a etapa 1.1.6. É crucial remover o solvente residual para consistência de execução para execução.
- Adquirir e validar um misturador da CIJ.
- Prepare-se fluxos de solventes e antisolvent em composições de alvo.
- Dissolva o composto hidrofóbico (ou seja, vitamina E) em THF instabilizado em 10 mg/mL em quantidade suficiente para completar o número desejado de FNP é executado. Prepare-se ligeiramente mais do que o necessário por execução.
Nota: Outros solventes podem ser usados nessas etapas, sujeita as restrições na seção de discussão. Se empregando THF, solvente livre de estabilizador é recomendado porque butil-hidroxitolueno tem baixa solubilidade na água. Tome cuidado para evitar o acúmulo de peróxido (incluindo teste de peróxido) e estar ciente de que baixos níveis de peróxidos podem interferir com determinadas aplicações de NP (por exemplo, o branqueamento de corantes). - Misture a solução de vitamina E no vortex até dissolver.
Nota: Para alguns compostos, sonication banho por 1-2 min pode ser úteis para gerar uma solução dissolvida. É importante que todos os componentes de NP são molecularmente dissolvidos. - Dissolver o estabilizador de copolímero de bloco (ou seja, poly(styrene) -b- poly(ethylene glycol), PS1,6 k-b-PEG5 k) em THF em 10 mg/mL em aproximadamente o mesmo volume como na etapa 1.2.1 para formar a solução de polímero.
Nota: Outros solventes podem ser usados, sujeitos as restrições detalhadas na seção de discussão. - Misture a solução de polímero com um misturador do vortex até dissolver. Se for necessário, coloque a solução em um banho de sonication para 1-2 min auxiliar na dissolução de sólidos.
Nota: O polímero não pode estar em uma forma micélica. Difusão dinâmica da luz (DLS) pode ser uma ferramenta útil para determinar se uma nova composição de fluxo atende a este critério. - Crie o fluxo de entrada de solvente contendo 5 mg/mL de vitamina E e o estabilizador (50% vitamina E carregamento) pelos primeiros pipetagem 0,25 mL da solução de vitamina E em um tubo de centrífuga de 1,5 mL. Em seguida Pipete 0,25 mL da solução de polímero para o mesmo tubo.
Nota: Volumes superiores a 0,5 mL por execução são viáveis com tamanhos diferentes de seringa. Acima do volume de entrada de 10 mL, é prático usar uma bomba de seringa. - Misture bem no Vortex para 5-10 s. opcionalmente, centrifugar o tubo a 1000 x g por 5-10 s para recuperar qualquer líquido preso ao PAC, que melhora a reprodutibilidade entre execuções CIJ.
- Pipete 0,525 mL de água desionizada para um segundo tubo de centrífuga de 1,5 mL, como o fluxo antisolvent.
Nota: É melhor ter antisolvent em excesso, o que garante que o fluxo de solvente nunca entra a câmara de mistura sem antisolvent presente. Em alguns casos onde não é limitar a solubilidade de sal na mistura solvente/antisolvent, podem ser usados em sistemas aquosos em buffer. - Pipete 4 mL de água desionizada para um frasco de cintilação de 20 mL ou outro recipiente adequado como um banho de retardamento. Coloque uma barra de agitação magnética pequena no frasco.
Nota: O banho de retardamento reduz o Ostwald amadurecimento, reduzindo o teor de solvente final de 10% por volume15,17. Este volume pode ser ajustado para restrições de endereço processo e pode ser escalado diretamente com volume de fluxo de entrada.
- Dissolva o composto hidrofóbico (ou seja, vitamina E) em THF instabilizado em 10 mg/mL em quantidade suficiente para completar o número desejado de FNP é executado. Prepare-se ligeiramente mais do que o necessário por execução.
- Produzir NPs por FNP usando o misturador da CIJ.
- Posicione o frasco do banho aberto quench abaixo o misturador CIJ limpo em uma placa de agitação em uma coifa. Uma configuração prática usa um bloco de cremalheira do tubo de ensaio de 50ml para apoiar o misturador CIJ com o frasco abaixo e a tubagem de saída dirigido dentro do frasco. Ver figura 1A para orientação.
- Begin, agitando o retardamento de banho através de barra de agitação magnética em torno de 75% de velocidade máxima.
- Usando uma seringa de 1 mL de polipropileno equipada com uma agulha de ponta sem corte, retire todo o volume do tubo antisolvent.
Nota: Não utilize seringas que contêm um selo o-ring de borracha para evitar preocupações de compatibilidade. Para volumes maiores de entrada, use uma seringa de fecho luer de tamanho apropriado. Saída da seringa deve ser centralizada no eixo de seringa ou será instável durante a depressão. - Cuidadosamente, remova todas as bolhas de ar da seringa e retire a agulha de ponta romba, descarte em um recipiente de objectos cortantes.
- Prime o êmbolo de modo que o fluxo vem apenas para a abertura da seringa. Ligue a seringa a um dos encaixes de entrada da CIJ.
- Repita as etapas 1.3.3-1.3.5 para a solução solvente.
- Rápido, suave e uniformemente deprimi as seringas ao mesmo tempo, colocando a bola de mão, a palma da mão ou um polegar cada nos topos dos êmbolos dependendo da preferência pessoal. Recolha o efluente no frasco do banho de têmpera.
Nota: Um 0,5 mL de entrada deve ser pressionado em menos de 0,5 s. - Reserve a CIJ misturador com as seringas ainda ligadas. Retirar a barra de agitação e tampa do frasco, que agora contém a dispersão de NP com uma estrutura de partícula núcleo-casca (Figura 1).
- Mantenha a batedeira sobre um recipiente de resíduos de solução e retire as seringas. O volume de assalto (cerca de 0,25 mL) então irá drenar para fora. Descartar as seringas usadas e repita a etapa de limpeza 1.1 antes da FNP próximo julgamento.
Nota: Não permitem o volume Mantenha-se ao vazio dentro do frasco que contém o NPs como isso afetará negativamente uniformidade da amostra.
- Realize análise e pós-processamento de dispersão de NP.
- Para caracterizar o tamanho de NP usando DLS, Pipetar 100 μL de dispersão em uma cubeta plástica NP e adicionar 900 μL do solvente de banho de têmpera (por exemplo, água).
Nota: Volumes menores podem ser utilizados para cubetas de baixo volume. Uma diluição de 10 vezes é geralmente suficiente. - Misture bem pipetando para cima e para baixo ou por agitação suave. Siga as instruções específicas do instrumento para analisar a amostra.
Observação: Técnicas de caracterização alternativa tais como análise de potencial zeta ou microscopia eletrônica pode ser efectuada como necessário. A dispersão de NP pode ser processada conforme ditado pelo aplicativo e revista na seção de discussão.
- Para caracterizar o tamanho de NP usando DLS, Pipetar 100 μL de dispersão em uma cubeta plástica NP e adicionar 900 μL do solvente de banho de têmpera (por exemplo, água).
2. encapsulamento de compostos hidrofílicos no NPs invertido usando um misturador CIJ
- Preparar o solvente, antisolvent e saciar a soluções na coifa.
- Conclua os procedimentos de limpeza e preparação descritos na etapa 1.1, usando DMSO como um solvente de limpeza e aderindo à nota na etapa 1.1.6 para completar uma segunda lavagem com THF.
- Dissolver o composto hidrofílico (i.e., maltodextrina (MD) com dextrose equivalente (DE) de 4-7, peso molecular médio = 3.275 g/mol, "3 k MD") em DMSO a 10 mg/mL em volume suficiente para completar o número desejado de FNP é executado.
Nota: Outros solventes podem ser usados, sujeito às restrições descritas na seção de discussão. - Misture a solução de maltodextrina com um misturador do vortex até dissolver. Se for necessário, coloque a solução em um banho de sonication para 1-2 min auxiliar na dissolução de sólidos.
- Criar um estabilizador de copolímero de bloco (ou seja, poly(styrene) -b- poli (ácido acrílico), PS5 k-b- PAA4,8 k) solução em THF em 11,1 mg/mL em aproximadamente o mesmo volume como na etapa 2.1.2 para formar a solução de polímero .
Nota: Outros solventes e concentrações de estabilizador podem ser usadas. DMSO prontamente pode ser usado como um solvente no lugar de THF. - Misture a solução de polímero com um misturador do vortex até dissolver. Se for necessário, coloque a solução em um banho de sonication para 1-2 min auxiliar na dissolução de sólidos.
Nota: A entrada de polímero não pode estar em uma forma micélica. DLS pode ser usado para determinar se uma nova composição de fluxo atende a este critério. - Preparar a entrada do fluxo de solvente (0,5 mL), combinando o seguinte, na ordem, num tubo de centrífuga 1,5 mL: 0,250 mL da solução de 3 k MD, 0,225 mL de solução de polímero e 0,025 mL de água desionizada.
Nota: O conteúdo de água de fluxo tem um forte impacto no tamanho do NP e polidispersividade. Geralmente é melhor operar no 2.5-10 vol % intervalo20. Valores na parte alta da gama podem ajudar a encapsulação de compostos de peso molecular maiores. - Misturar bem no Vortex para 5-10 s.
- Opcionalmente, centrifugar o tubo a 1000 x g por 5-10 s para recuperar qualquer líquido preso ao PAC, que melhora a reprodutibilidade entre execuções CIJ.
- Prepare uma solução de agente reticulante de cloreto de cálcio (CaCl2) dihidrato em metanol a 25,0 mg/mL.
Nota: O agente reticulante será adicionado na proporção de 1:1 carga aos grupos ácidos no bloco PAA. Ajuste a concentração em conformidade, se for usado um agente reticulante diferente ou se uma PAA bloco tamanho ou polímero concentração diferente é utilizado20,21. - Prepare o fluxo de antisolvent por pipetagem 0,5 mL de clorofórmio e 0,05 mL da solução de agente reticulante (0,55 mL total) em um tubo de microcentrifugadora.
Nota: Outros antisolvents aceitáveis são ditadas pela escolha de copolímero de bloco e tipicamente incluem diclorometano ou acetona. O agente reticulante em vez disso pode ser adicionado ao banho de retardamento, com envelhecimento adicional de dispersão para permitir a formação de ligação cruzada20NP. - Misturar bem no Vortex para 5-10 s.
- Opcionalmente, centrifugar o tubo a 1000 x g por 5-10 s para recuperar qualquer líquido preso ao PAC, que melhora a reprodutibilidade entre execuções CIJ.
- Adicione 4 mL da antisolvent (ou seja, clorofórmio) para um frasco de cintilação de 20 mL para formar o banho de retardamento. Coloque uma barra de agitação magnética pequena no frasco.
Nota: Este volume pode ser ajustado para restrições de processo de endereço.
- Complete o protocolo para formação de NP conforme descrito na etapa 1.3.
- Realize análise e pós-processamento de dispersão de NP.
- Para caracterizar o tamanho de NP usando DLS, Pipetar 100 μL de dispersão NP em uma cubeta de vidro e adicionar 900 μL do solvente usado para o banho de retardamento.
- Misture bem pipetando para cima e para baixo ou por agitação leve da cubeta. Siga as instruções de software para analisar a amostra.
Nota: Reticulação do NPs pode ser avaliada qualitativamente por DLS usando um bom solvente como DMSO ou dimetilformamida (DMF) como diluente de DLS20. As partículas que são estàvel quitosana irão expor uma função de autocorrelação no solvente, com mínima alteração no tamanho de partícula. Partículas de quitosana mal incham e apresentam uma função de autocorrelação fraco e dispersão força21. - Opcionalmente, adicione uma base, tais como amônia, conduzir complexação iônica e reforçar a reticulação do núcleo da partícula.
- Opcionalmente, prepare uma solução de 3,48 mg/mL de amoníaco em metanol por gravimetria utilizando a solução de hidróxido de amônio (normalmente, 30 amônia % wt). Adicione 50 μL (ou seja, 0,6 equivalentes no que diz respeito os grupos ácidos sobre o polímero) gota a gota, agitando.
Nota: Os equivalentes podem ser ajustados, se desejado, variando também a concentração ou o volume adicionado25. - Opcionalmente, idade não inferior a 30 min com agitação suave para reticulação ocorrer.
- Opcionalmente, prepare uma solução de 3,48 mg/mL de amoníaco em metanol por gravimetria utilizando a solução de hidróxido de amônio (normalmente, 30 amônia % wt). Adicione 50 μL (ou seja, 0,6 equivalentes no que diz respeito os grupos ácidos sobre o polímero) gota a gota, agitando.
- Processo a dispersão de NP para produzir micropartículas ou revestido NPs conforme descrito na literatura19,20,21.
3. encapsulamento de ovalbumina no NPs invertido usando um μMIVM
- Prepare soluções de solventes e antisolvent.
- Prepare uma solução de 50 mg/mL de ovalbumina em água desionizada ("OVA").
- Prepare 0,75 mL da solução A em um tubo de centrífuga de 1,5 mL, diluindo 75 μL da solução de óvulos com 0,675 mL de DMSO para gerar uma solução de 5 mg/mL de óvulos em DMSO contendo 10% de água em volume. Misture bem e centrifugue brevemente, conforme descrito anteriormente.
Nota: Consulte a etapa 2.1.6 sobre efeitos de água. Como em seções anteriores, os volumes de solução podem ser escalados acima ou para baixo para ajustar necessidades materiais. - Preparar a solução B dissolvendo o estabilizador de copolímero de bloco (ou seja, poly(styrene) -b- poli (ácido acrílico), PS5 k-b- PAA4,8 k) em DMSO a 6 mg/mL. Misture bem e proceda à sonicação para dissolver se necessário. Pipete 0,75 mL para um tubo de centrífuga de 1,5 mL.
- Pipete 0,75 mL de THF (solução C) para um tubo de centrifugação de 1,5 mL.
- Pipete 1,85 mL de clorofórmio (solução D) para um frasco de cintilação.
- Prepare um 60,0 mg/mL de cloreto de cálcio dihidratado crosslinker solução em metanol. Misture usando um misturador do vortex.
- Prepare um 4,17 mg/mL solução de amônia em metanol, conforme descrito na etapa 2.3.4.
- Adicione 5,25 mL de clorofórmio para um tubo de centrífuga de 15 mL, como o banho de retardamento.
- Preparar a montagem do misturador e ficar.
- Reunir o receptor inferior, mistura de geometria de disco, o disco superior, a chave de boca e um-Ring. Consulte a Figura 2 para o diagrama de componentes e terminologia de carrinho do misturador.
Nota: Detalhes na construção de MIVM podem ser encontradas na Informação suplementar (seção 1) e na literatura22. Arquivos CAD também estão disponíveis como Informação suplementar . - Coloque o anel-o na ranhura, garantindo que ele se encaixa bem e que não há sinais de desgaste ou danos.
Nota: Funcionamento Normal levará para anéis desgastados ou solvente-inchado. Se o-Ring aparece esticada ou deformada, deixe-o ar seco durante a noite antes do uso. Se a forma não recupera durante a noite, elimine o-Ring. Manter um grande estoque, pois esta é uma parte consumível. - Cuidadosamente, alinhe os orifícios de disco mistura com os pegs no disco superior e empurrar juntos. Certifique-se de que o-ring não se tornar deslocado, verificando que as duas peças se sentar flush.
- Inverter as duas peças e montar manualmente com o receptor de fundo. Certifique-se de que o encaixe de tubulação de saída tem sido afrouxado para que não interfira com aperto completa do disco.
Nota: Se a segmentação das capturas durante a montagem, cuidadosamente desmonte e aplicar um grau alimentício ou farmacêutico-anti-agarrador de rosca para evitar escoriação. - Após o aperto manual, ajuste a chave de boca nos pinos do disco superior e aperte firmemente o assembly. Em seguida aperte o tubo tomada encaixe para que senta-se firmemente contra a face inferior da geometria da mistura. Certifique-se de que os encaixes de seringa no disco superior são confortáveis.
- Coloque o misturador montado no suporte do misturador para que o tubo de saída se estende abaixo da placa de apoio. Suporte a placa móvel, para que este é suspenso do caminho o espaço de trabalho.
- Opcionalmente, para verificar o alinhamento do batente mecânico, primeiro encaixe as seringas de vidro vazio as entradas do misturador.
Nota: O caudal volumétrico é variado usando seringas de barril de diferentes diâmetros, desde que as seringas são deprimidas simultaneamente na mesma velocidade linear. A altura vertical inicial e final deve ser o mesmo para todas as seringas e pode ser ajustada usando parafusos grampeados o êmbolo eixo22. O mecânico para garantir que não ocorra danos excessivos para as seringas de vidro.- Opcionalmente, menor a placa móvel é isso que vem para descansar durante as paradas de mecânicas. Certifique-se de que estes estejam alinhados para que a placa também vem repousar imediatamente antes de entrar em contato com as seringas vazias (como visto na Figura 2).
- Opcionalmente, afrouxe o mecânica para e reposição, se necessário. Retire as seringas de vidro e redefinir a placa móvel fora do caminho.
Nota: Para operação com seringas de plástico, as paragens mecânicas não são necessárias.
- Coloque o banho de retardamento aberta abaixo ao tubo de saída para recolher o efluente.
- Desenhe a solução A uma seringa de 1 mL estanques ao gás usando uma agulha de ponta romba. Remover todas as bolhas de ar e elimine-o da agulha. Prime a solução para o fim do encaixe seringa luer. Repita este processo para soluções B e C.
- Desenhe a solução D uma seringa hermética de 2,5 mL, usando uma agulha de ponta romba. Remover todas as bolhas de ar e elimine-o da agulha. Prime a solução para o fim do encaixe seringa luer.
Nota: Estes volumes foram selecionados para que as alturas de êmbolo de seringa iniciais são os mesmos. Se os volumes forem alterados, eles ainda devem atender este requisito de altura. - Monte as quatro seringas para o misturador no sentido horário em ordem alfabética. Ver figura 1B para seringa orientação esquemática e aparência final.
Nota: Verifique se não há altura da seringa é significativamente diferente das outras e solucionar problemas conforme necessário.
- Reunir o receptor inferior, mistura de geometria de disco, o disco superior, a chave de boca e um-Ring. Consulte a Figura 2 para o diagrama de componentes e terminologia de carrinho do misturador.
- Execute operação de misturador e limpeza.
- Aperto a carcaça de rolamento de ambos os lados da placa móvel. Não coloque os dedos na face inferior da caixa porque este é uma pitada de perigo contra o mecânico para. Abaixe lentamente a placa móvel, para que fique apoiada uniformemente mas mal tocando as seringas.
- Continuamente e suavemente aperte a placa, com o objetivo de concluir a operação em cerca de 0.5-1 s para estes stream volumes22.
- Remover e tampar o tubo de banho de retardamento que agora contém a dispersão de NP.
- Leve a batedeira com as seringas ainda ligadas e mantenha sobre um recipiente de resíduos. Retire as seringas, permitindo que o volume Mantenha-se escoe para o recipiente. Segure o conjunto misturador de cabeça e desmontar o mixer usando a chave de boca.
- Usando um frasco de spray, lave o tubo de saída com alguns mililitros de solvente (por exemplo, acetona) e seque com ar ou nitrogênio.
- Enxágue a geometria mistura com um bom solvente (por exemplo, água deionizada, água ou DMSO) e em seguida enxaguar com acetona, usando vários mililitros de um frasco de spray. Seco com um fluxo de ar ou nitrogênio.
- Enxágue o-ring em um fluxo de água desionizada e secar.
- Lave o disco superior completamente com vários mililitros de acetona, usando um frasco de solvente até visualmente limpo. Seque com um fluxo de ar ou nitrogênio, tanto a superfície e os encaixes de seringa.
- Lave cada seringa com vários mililitros de um bom solvente (por exemplo, água deionizada, água ou acetona) de um frasco de solvente. Aplicar uma lavagem final de vários mililitros de acetona e ar seco antes da próxima utilização.
- Realize pós-processamento e análise.
- Adicionar 50 μL da solução de cloreto de cálcio dihidratado crosslinker gota a gota, agitando em cerca de 75% velocidade máxima.
- Adicione 50 μL da solução de amônia gota a gota, agitando a velocidade máxima de 75%. Idade pelo menos 30 min.
- Caracteriza o tamanho NP conforme descrito nas etapas 2.3.1 e 2.3.2.
- Processo a dispersão de NP para produzir micropartículas ou revestido NPs conforme descrito na literatura19,20,21.
4. modificações para formulação de Scale-up
- Prepare as soluções de solventes e antisolvent, conforme descrito nas etapas 1, 2 ou 3 na composição desejada e em volume suficiente para o tamanho necessário de formulação.
- Opcionalmente, se necessário, limpar e esterilizar o misturador no lugar usando um protocolo adequado antes da formação do NP.
Nota: Enxaguamentos sequenciais de CIP 100, água (pH neutro), CIP 200, água (pH neutro) e um solvente adequado têm sido empregados no passado. Além disso, filtros estéreis podem ser fixados nas entradas do misturador em instâncias onde granulometria final impede a esterilização por filtração. - Carregar as soluções em seringas estanques ao gás de volume adequado e anexar tubos de politetrafluoretileno (PTFE) com um adaptador luer montado na extremidade. Prime manualmente as soluções para a extremidade do tubo.
- Carregar as seringas em uma bomba de seringa e fixe as seringas para as entradas do misturador na CIJ ou o MIVM, conforme necessário.
Nota: Como alternativa, controladores de fluxo podem ser usados em laboratório ou em escala piloto para fornecer recursos de volumes maiores do que uma bomba de seringa. Operação bem sucedida requer fluxo constante e queda de pressão suficiente, que significa que os vasos pressurizados com medição de fluxo na saída são a seleção mais apropriada para a produção em larga escala.
- Carregar as seringas em uma bomba de seringa e fixe as seringas para as entradas do misturador na CIJ ou o MIVM, conforme necessário.
- Coloque um recipiente coleção que contém um retardamento de banho volume suficiente, se necessário, sob o tubo de saída.
- Definir as taxas de fluxo volumétrico para coincidir com aqueles obtidos manualmente (por exemplo, cerca de 30-60 mL/min por fluxo).
Nota: Se utilizar o CIJ, as taxas de fluxo da bomba devem ser idênticas. Se usando o MIVM, entradas diferentes podem ter taxas de fluxo diferentes. - Simultaneamente, começam as bombas. Coletar cerca de 5-10 mL de efluente como um resíduo em um pequeno frasco (este é um "volume de start-up") e então começar a coletar no banho de retardamento.
- Caracterizar e processo conforme descrito na seção de formulação correspondente acima.
Resultados
Rastreio de formulações de NP com a FNP é rápido e requer pequenas quantidades de material (da ordem de 1-10 mg). O protocolo FNP para encapsular compostos hidrofóbicos, como vitamina E (etapa 1) resulta em uma dispersão de NP estável, clara ou levemente opalescente. Difusão dinâmica da luz (DLS) fornece um meio robusto para caracterizar o tamanho de partícula. Como mostrado na Figura 3, o processo produz NPs com uma baixa polidispersividade de forma reproduzível. O índice de polidispersividade típico (PDI) é inferior a 0,20, indicando uma população de monodisperso relativamente. O PDI é obtido a partir da função de autocorrelação e geralmente é implementado no software do instrumento. É uma proporção do segundo para o primeiro momento, onde os valores de 0.1 geralmente são obtidos por monodisperso partículas26. Para a vitamina E quatro/PS-b-PEG formulação repetições relatado, o valor foi de 0,12 ± 0,02 e o diâmetro médio foi de 107 ± 7 nm. Um típico "misfire" devido a qualquer depressão desigual das seringas ou velocidade mais lenta de depressão também é relatado na Figura 3. A polidispersividade não foi afetada, mas o tamanho era um pouco maior (135 nm). Incluindo neste exemplo, as novas métricas para tamanho de partícula são 113 ± 14 nm. Uma falha resulta em períodos de tempo, onde a câmara contém apenas um tipo de fluxo único. É importante que o fluxo inteiro experimenta a mesma história de processo e volumes relativas dos fluxos orgânicos e aquosos dentro do misturador. Sem um estabilizador, uma solução opaca com agregados visíveis é produzida. A função de autocorrelação DLS para esta amostra é não-monotônicas e não decadência sem problemas, como visto em baixo-relevo a Figura 3 .
Controle de tamanho de partícula por FNP é demonstrado na Figura 4, onde variando os montantes relativos do material do núcleo – poly(styrene)1,8 k neste caso – e PS -b-PEG estabilizador resultou em tamanhos de partículas que variaram entre 49-152 nm. Estes tamanhos de partículas foram gerados com fluxos THF contendo uma concentração de massa total do núcleo e estabilizador de 20 mg/mL, onde 25%, 50% ou 75% da massa foi o material do núcleo poly(styrene). A polidispersividade das nanopartículas foi sempre inferior a 0,15. Ampla discussão de efeitos de parâmetro no tamanho de partícula, produzido pela FNP pode ser encontrado na literatura10. O carregamento pode ser ajustado mantendo constante do volume de solvente e variando os volumes relativos das soluções estoque núcleo e estabilizador. Da mesma forma, a concentração em massa total pode ser variada através da elaboração de soluções estoque em valores diferentes de 10 mg/mL. Sob certas condições, é possível observar uma população micelle vazio por DLS27. Isto não tem qualquer efeito prejudicial, além de ampliar a distribuição de tamanho de partículas medido. Quando os tamanhos são semelhantes, isto pode manifestar-se como um único pico amplo ao invés de dois picos separados.
O misturador CIJ a mesma também pode ser usado para encapsular compostos hidrófilos por iFNP, como exemplificado na etapa 2 do protocolo. As partículas produzidas na formulação relatada são em torno de 65 nm, com uma baixa polidispersividade de 0,08. A distribuição de tamanho pode ser vista na Figura 5A (linhas tracejadas). O efeito de reticulação os resíduos de ácido carboxílico PAA na estabilidade da partícula é demonstrado pela análise DLS em um solvente forte como DMSO, conforme mostrado na Figura 5B. A função de autocorrelação para partículas bem-quitosana deve começar perto de um valor de 1 e gota agudamente a 0 em um momento característico que está relacionado com o tamanho de partícula (linha contínua). Partículas que incham extensivamente ou dissolvem não são quitosana e mostram sinal mínimo autocorrelação (linha pontilhada). Para iFNP, ensaios falhados se manifestar de maneiras semelhantes conforme descrito por FNP acima. Agregados visíveis podem ser vistos ou forma de função de autocorrelação DLS pobre pode ser observada. O MIVM pode ser usado para a FNP ou iFNP quando mais de dois fluxos de entrada são necessários devido a restrições de sistema, tais como a solubilidade ou incompatibilidade química. Uma versão em escala reduzida do MIVM (o μMIVM), com stand mixer é mostrada na Figura 2. Tal como acontece com a CIJ, este misturador pode ser usado para encapsular compostos hidrofóbico ou hidrofílico22. Na etapa 3, um protocolo para o encapsulamento de uma proteína hidrofílico, óvulos, por iFNP foi descrito. A distribuição de tamanho de partícula é mostrada na Figura 5A (linha contínua). O tamanho é de cerca de 125 nm com um PDI de 0,16. Um protocolo geral para o funcionamento da bomba de seringa em escalas maiores é fornecido na etapa 4.
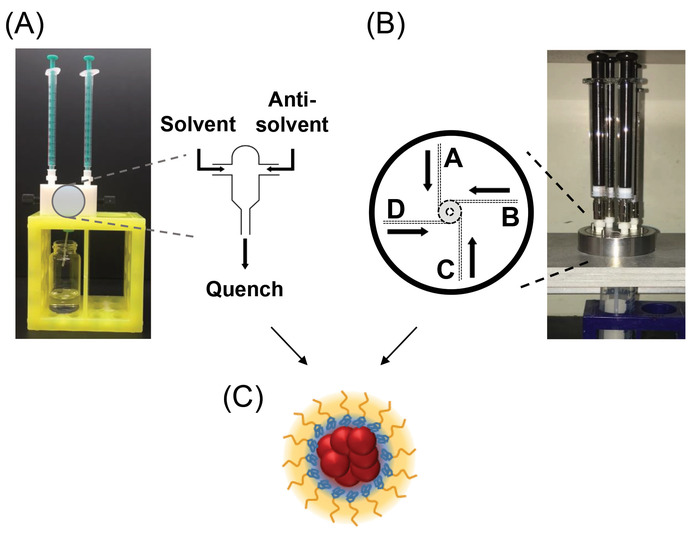
Figura 1: montagem do misturador e fluxo interno padrão esquemas. Misturador de jatos (CIJ) (A) os confinados colide com seringas anexadas está posicionado acima do banho de têmpera. Não imaginava são uma barra de agitação no frasco de banho de têmpera e uma placa de agitação. A geometria de mistura é retratada na visualização expandida mostrando as entradas de fluxo de dois que interfere no centro da câmara. (B) um vórtice de entrada multi mixer (o μMIVM) é mostrada com seringas de vidro e posicionado no stand acima de um banho de retardamento. A placa móvel e o mecânico para ter sido cortado da foto. A vista expandida mostra a câmara de vórtice e os canais de entrada esquematicamente. (C) A representação esquemática do núcleo-casca NPs produzido pela FNP. As esferas vermelhas representam a terapêutica que, combinado com o bloco de polímero recolhido azul, compõem o núcleo de NP. O bloco de polímero amarelo forma a camada de pincel transmitir estabilização estérica para o NPs. clique aqui para ver uma versão maior desta figura.

Figura 2: μMIVM terminologia e componentes para montagem. O μMIVM requer um stand mixer para permitir uniforme depressão de seringas de quatro. Neste caso, as alturas de êmbolo de seringa todos devem ser uniformes para assegurar uma mistura consistente. Alternativamente pode ser operado usando bombas de seringa. O stand mixer com componentes rotulados é mostrado à esquerda da figura. À direita está o misturador desmontado com o anel-o no lugar do disco mistura de geometria. Clique aqui para ver uma versão maior desta figura.
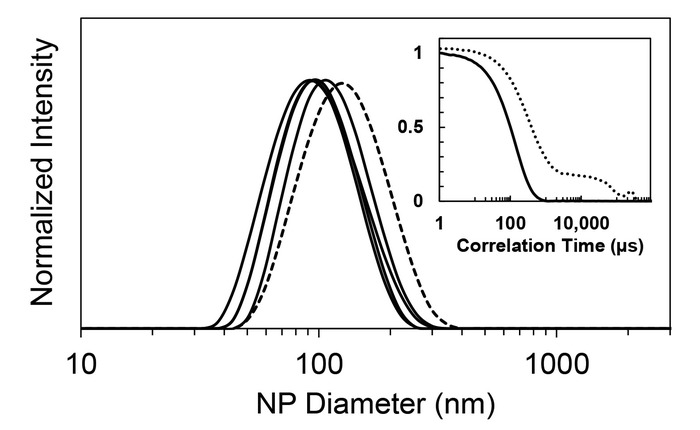
Figura 3: Distribuição de nanopartículas poliméricas contendo um núcleo de vitamina E de tamanho de partícula e estabilizada por PS -b-PEG. Difusão dinâmica da luz (DLS) fornece distribuições de tamanho de intensidade-tornada mais pesada que indicam a distribuição de diâmetro de NP. As curvas são a média de três vias análises para cada julgamento e tem sido redimensionadas para produzir alturas de pico máximo idêntico. As quatro repetições (linhas sólidas) indicam a alta reprodutibilidade do método (desvio padrão = 7 nm). Também está incluído um falhanço representativo (linha tracejada), tais como a velocidade mais lenta de seringa ou depressão desigual de duas seringas, que resulta em maior diâmetro de partícula. O desvio padrão do tamanho do NP, incluindo a falha de ignição foi 14 nm. (Inserir) Sem o PS -b-PEG estabilizador, formam-se grandes agregados de mícron-escala (ou gotas, no caso de um óleo de vitamina E). A função de autocorrelação DLS de uma corrida sem o estabilizador (linha pontilhada) é mostrada junto com uma representante autocorrelação de nanopartículas idêntico (linha contínua). A função de autocorrelação mostra um número de escalas de tempo característicos para a amostra de controle, indicando uma população polydisperse. Clique aqui para ver uma versão maior desta figura.
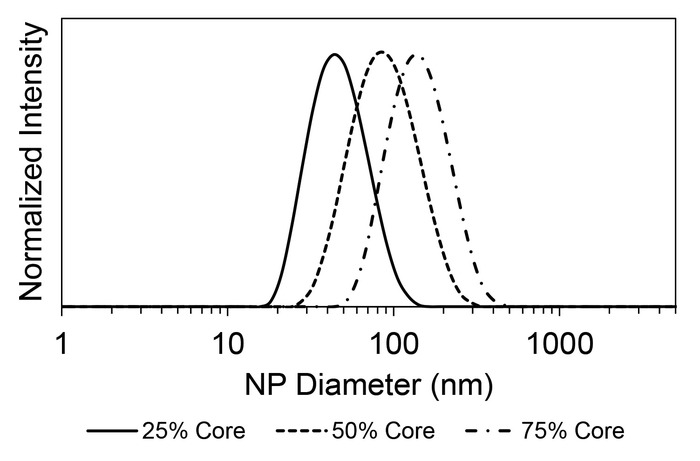
Figura 4: controle de tamanho de partícula por FNP através de variando relativos rácios do núcleo material para estabilizador. As distribuições de tamanho de intensidade ponderada de três formulações com um núcleo de poly(styrene) estabilizaram por PS -b-PEG são retratados. A concentração em massa total em THF foi de 20 mg/mL e o antisolvent era água. As formulações foram preparadas em um misturador da CIJ. A fração da massa composta de material do núcleo é listada na legenda. Por exemplo, amostra de 25% continha 5 mg/mL poly(styrene) e 15 mg/mL PS -b-PEG. Os tamanhos médios de 25% (linha contínua), 50% (linha tracejada) e cargas de núcleo de 75% (linha de traço misto) foram 49 nm, 96 nm e 152 nm, respectivamente. Todos os valores PDI foram inferiores a 0,15. Clique aqui para ver uma versão maior desta figura.
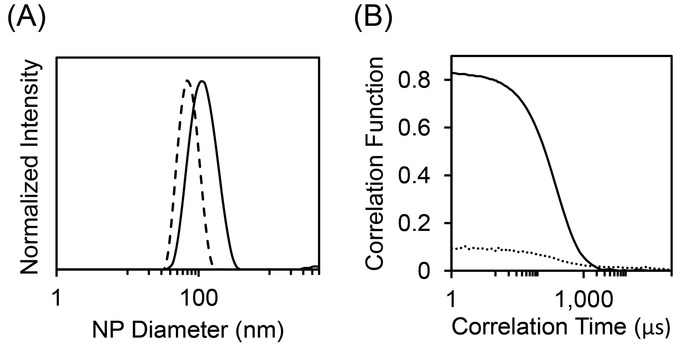
Figura 5: caracterização de NPs invertido em um misturador CIJ ou μMIVM. (A) DLS curvas são a média de três vias análises para cada formulação. Linha tracejada indica a distribuição de tamanho de partículas de MD 3 k feita na batedeira CIJ, enquanto a linha sólida é a distribuição de tamanho de partículas de óvulos no μMIVM. (B) a força de reticulação pode ser avaliada por DLS usando DMSO como o diluente. A função de autocorrelação DLS indica a força da reticulação através o valor inicial de autocorrelação e a observação de uma transição perfeita para um valor de zero. Linha tracejada mostra a função de autocorrelação para uma partícula com nenhum agente reticulante mostrando um fraco sinal inicial e um tempo de decaimento amplo. A linha sólida retrata a autocorrelação após a adição de um agente reticulante forte (no caso, tetraetilenopentamina), que mostra um forte sinal inicial e um calendário definido decadência. Clique aqui para ver uma versão maior desta figura.
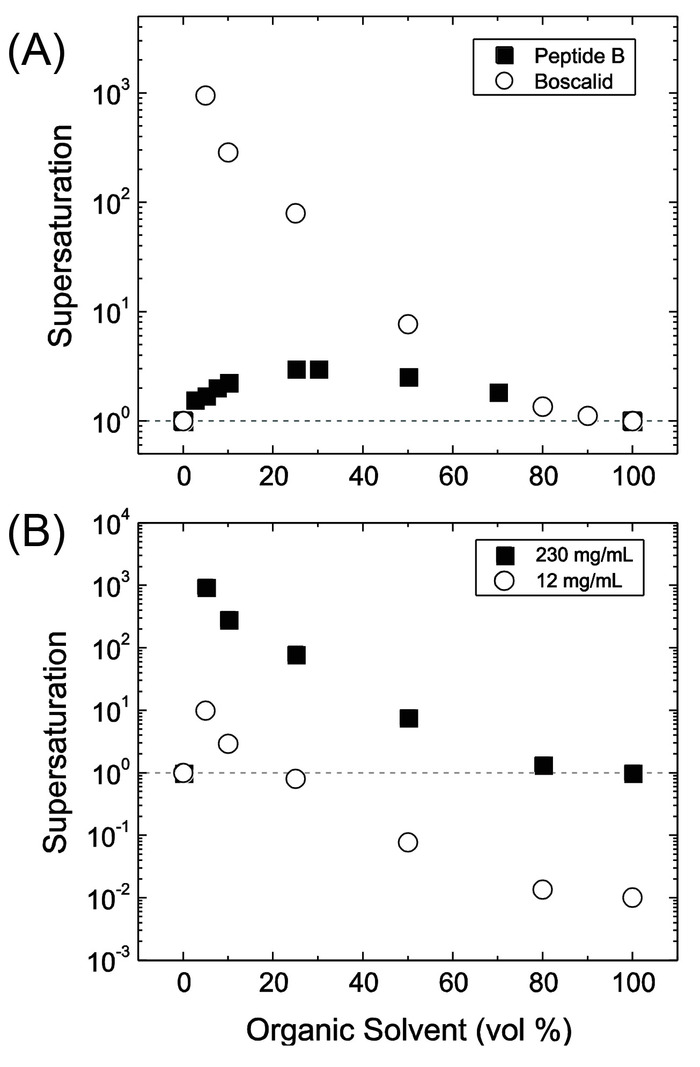
Figura 6: supersaturação, S, em função das relações de mistura relativas de solvente orgânico para água. (A) comparação de maior supersaturação atingível para (○) boscalide, um pesticida e (■) do peptide B, um peptídeo modelo sete-resíduo. O fluxo orgânico contém boscalide em uma concentração de 230 mg/mL e peptídeo B em 200 mg/mL, suas concentrações de saturação. Há uma máxima supersaturação que depende de cada ingrediente farmacêutico ativo (API) / solvente sistema. (B) quando a concentração de boscalide no fluxo orgânico é diminuída 20 vezes, as condições em que são alcançados supersaturação e nanoprecipitation tornar-se limitado. Esta figura é reproduzida com permissão da Elsevier9. Clique aqui para ver uma versão maior desta figura.
Discussão
O encapsulamento de compostos hidrofóbicos, como vitamina E, como na etapa 1 do protocolo, tem sido extensivamente descrito9,14,28. Relativamente monodisperso partículas são produzidas porque a escala de tempo para a mistura é menor do que a escala de tempo para a agregação e o crescimento das partículas. Especificamente, a solução solvente/antisolvent mista rapidamente se torna homogênea, que permite a nucleação ocorra uniformemente. Montagem do copolímero em bloco para a superfície da partícula então estérico que interrompe a partícula crescimento5. Desde o tempo de mistura na câmara (turbulência) é uma função das taxas de fluxo de entrada para a CIJ ou o MIVM, há uma taxa de entrada, que ocorre após a transição para a mistura turbulenta, onde o tamanho de partícula é essencialmente constante13. Isto fornece robustez adicional ao processo como alguns lotes de variação na vazão de entrada (ou seja, velocidade de depressão de seringa) pode ser tolerada sem impacto significativo para o tamanho final da NP, como pode ser visto da Figura 3. Velocidades de entrada mais lenta ou irregular podem resultar em partículas maiores ou mais polydisperse distribuições, como visto no exemplo de falha de ignição. FNP também foi estendido para encapsular compostos hidrofílicos em nanopartículas por inverso NanoPrecipitation Flash. Estes invertido nanopartículas pode então ser usados para criar micropartículas ou ser revestido com PEG para criar nanopartículas dispersáveis em água25. Os princípios subjacentes de montagem permanecem os mesmos, embora haja a complexidade adicional de reticulação, o núcleo da partícula. Isto é necessário para a estabilização da partícula em um ambiente aquoso. Em geral, uma proporção de 1:1 carga em comparação com o bloco de poliácida é suficiente, embora as interações ionic podem ser promovidas pelo ajuste do pH através da adição de uma base de19. Neste protocolo, tem sido descrito apenas o primeiro passo de processo para NPs de forma invertida.
Além de mistura rápida, formulação bem sucedida pela FNP ou iFNP é limitada aos casos onde várias condições podem ser met9,14. Primeiro, todo fluxo de entradas deve ser miscível. Enquanto emulsões têm sido usados para produzir o NPs, FNP requer uma fase de solução uniforme na batedeira. Em segundo lugar, o componente do núcleo deve ser quase insolúvel no solventes condições na batedeira (para a CIJ, uma mistura 50/50 por volume) para conduzir a nucleação rápida. Caso contrário, uma parcela significativa permanecerá desencapsulada ou irá precipitar após diluição mais com antisolvent. O MIVM pode permitir maior teor de antisolvent na câmara de mistura para limitações de solubilidade material de núcleo de endereço. Muitas vezes é útil gerar curvas de supersaturação de dados de solubilidade em função da composição solvente para orientar o processo de projeto9. A Figura 6 mostra as curvas representativas para dois compostos. Baixa supersaturação nos méritos de condições câmara misturadora operando em diferentes composições, tipicamente usando o MIVM. Maior supersaturação favorece a nucleação do componente núcleo sobre crescimento de partícula, mas uma incompatibilidade no tempo de montagem de material do núcleo e o estabilizador pode resultar em grandes agregados da terapêutica. D'Addio e Prud'homme tem revisto a aplicação de tais curvas de supersaturação em detalhe9. Finalmente, o BCP molecularmente deve ser dissolvido no fluxo de solvente e o fluxo de antisolvent deve ser seletivo para um quarteirão. O BCP deve ser suficientemente anfifílica para fornecer tanto um solvophobic motor do bloco recolhido para ancorar o estabilizador na superfície de partículas e para o bloco de solvated conferir estabilidade estérica para a partícula. Solventes diferentes dos descritos no protocolo podem ser utilizados enquanto se encontram essas restrições.
Prática com operação manual seringa pode melhorar a taxa de sucesso durante a triagem. Conforme observado acima, operação acima a transição para condições de mistura homogêneas, turbulentas, não significa que pequenas variações na taxa de fluxo são toleradas no processo28. Escala-se para resultados de bomba, controlada por computador fluxos em ganhos ainda maiores em consistência devido as taxas de fluxo de entrada pode ser reproduzido. Em qualquer momento durante o pós-processamento das partículas, inspeção visual ou DLS análise pode indicar a presença de grandes agregados, que pode ser devido à instabilidade incidental de poeira ou partículas. Quando necessário, o fluxo pode ser filtrado com um tamanho de poro de filtro apropriado. Na ausência de agregados, achamos que menos de 5% em massa é normalmente perdida quando nanopartículas PEG-revestido de filtragem se o tamanho do filtro nominal é maior do que a distribuição de tamanho de partícula. Quando a filtragem de agregados, determinação experimental da massa perdida durante o processo é necessária. Quantificação da perda de massa pode ser realizada de duas maneiras. A massa de sólidos totais em um determinado volume pode ser determinada por análise térmica química antes e depois da filtragem para identificar a extensão da mudança (consulte a seção de Informações suplementares 2). Alternativamente, as partículas podem ser recuperados (por exemplo, por liofilização) e dissolvido em um solvente bom. A concentração do material do núcleo pode então ser medida diretamente por uma técnica apropriada como espectrofotometria ultravioleta-visível ou cromatografia.
Para a FNP, o residual 10 vol % solvente orgânico (por exemplo, THF) deve ser retirado a dispersão aquosa. Isso pode ser feito por destilação por evaporação14,29, diálise30ou de31,de filtração tangencial fluxo32. Considerações práticas para cada etapa de processamento são descritas nas citações fornecidas. Para diálise, membranas típicas são kDa 3,5 ou 6-8 kDa cortes, embora maiores opções estão disponíveis. Este corte de peso molecular é suficiente para a remoção do solvente quando diálise para 24h usando várias mudanças de banho. O uso de filtração tangencial fluxo implica um processo de desenvolvimento como deve ter cuidado para evitar a indução de agregação devido à polarização de concentração na superfície da membrana. Nós achamos que reduzindo a composição de solvente orgânica abaixo de um valor dependente do sistema, geralmente 2-10 vol %, elimina a agregação na superfície da membrana. Após o processamento, a concentração de nanopartículas é prontamente determinada por análise térmica química (consulte a seção de Informações suplementares 2). Muitas vezes é desejável para transportar ou armazenar partículas em uma forma altamente estável. Dispersões aquosas podem simplesmente ser congeladas rapidamente usando uma mistura de gelo seco/acetona e em seguida, armazenado a-80 ° C. Alternativamente, pós secos podem ser obtidos por liofilização33,34 ou spray de secagem24. Frequentemente, um crioprotetor deve ser adicionado para reduzir a agregação de nanopartículas durante o congelamento ou secagem. Açúcares (sacarose, trealose, etc.), poly(ethylene glycol) ou ciclodextrinas podem ser rastreadas para eficácia sobre uma escala das concentrações por tamanho de monitoramento por DLS35,36,37,, 38. Problemas comuns de estabilidade NP durante processamento estão muitas vezes relacionados à solubilidade ou fase de separação no núcleo resultando em rearranjo em direção um estado de energia mais baixo em condições onde a mobilidade é maior. Uso dos materiais do núcleo co, estabilizadores alternativos ou composição solução externa modificada pode ajudar a melhorar a estabilidade14,16,17,39,40, 41.
Conforme observado acima, o MIVM permite maior teor de antisolvent na câmara de mistura quando necessário para alcançado alta supersaturação. Também pode permitir que a segregação física das espécies em mais de duas correntes quando restrições de reatividade ou solubilidade exigirem-lo. Um exemplo é a formação de nanopartículas de proteína estabilizada zein do antibiótico clofazimina24. A clofazimina hidrofóbica é introduzida em um fluxo de acetona; Zein é introduzida em um fluxo de 60% etanol aquoso; caseína, que complexos com zein, é trazida com um fluxo tampão aquosa, e o fluxo de quarto é buffer adicional para aumentar a taxa de água, a acetona e etanol. Dois córregos solventes são necessários desde clofazimina e zein não são solúveis em um solvente comum. Este processo não poderia ser feito em um misturador CIJ dois-jato. Esta formulação estabilizada proteína também demonstra que a FNP não é limitado aos estabilizadores do BCP. Partículas de Janus foram produzidas sem estabilizador42 e uma gama de estabilizadores de baixo custo tem sido demonstrada para aplicações oral24. Notavelmente, copolímeros como metilcelulose hidroxipropil podem ser usados no lugar de copolímeros de bloco24. Materiais do núcleo podem ser feitos mais hidrofóbicas por um número de técnicas. Emparelhamento hidrofóbico íon tem sido aplicada para encapsular uma ampla gama de compostos que têm solubilidade intermediária43,44,45. Exemplos extremamente hidrofóbicos tem sido gerado e então encapsulado46. Ácidos nucleicos foram encapsulados por complexação com lipídios catiônicos47. Importante, esses estudos têm demonstrado que a FNP pode produzir uma gama de produtos químicos de superfície de partícula. Têm sido utilizados estabilizadores mais, mistos, contendo uma fração do BCP que tenha sido modificado com um ligante direcionamento na extremidade da cadeia. Isso permite um controle preciso sobre o conteúdo do ligante na superfície, desde que a composição da partícula reflete o fluxo de entrada composição23,48. Da mesma forma, é possível incorporar vários componentes principais, bem como, incluindo corantes e nanopartículas inorgânicas3,8.
NanoPrecipitation flash é uma abordagem dimensionável de nanopartículas poliméricas, compostas por um núcleo hidrofílico ou um hidrofóbico. Se os critérios enumerados acima, geralmente mais 95% do material do núcleo é encapsulado em alta fração de massa na partícula. Os três exemplos aqui apresentados foram realizados em escala de bancada, exigindo alguns miligramas de material e cerca de 0,5 mL em cada fluxo de entrada. Isto permite a seleção rápida de condições de partícula para otimização de formulação. Aumentar de formulações de chumbo para maiores tamanhos de lote é uma questão de execução do processo por mais tempo, que pode ser facilmente realizado com o uso de bombas de seringa ou controladores de fluxo. Por outro lado, a aumentar de volume adição nanoprecipitation enfrenta desafios bem documentados em manutenção suficiente micromixing no ponto de adição e contabilizar o efeito da alteração de geometria do navio49. Este é um grande obstáculo, uma vez que é crucial para a fabricação de partículas de forma consistente para atender requisitos de FDA50. Microfluídica técnicas podem também produzir nanopartículas uniformes, pode ser reproduzidas, mas apenas permitir a produção na faixa de miligrama. Por exemplo, Karnik et al relataram taxas de produção de 0,25 mg/min. para uma liberação de drogas estudo51. Escala-se mais geralmente envolve paralelização no alto custo12de capital. Com a FNP, é simples de produzir 1 grama de nanopartículas em 600 mg/min com uma bomba de seringa e alguns acessórios para ligar o misturador nas entradas. Consequentemente, a FNP representa tanto uma ferramenta de triagem de laboratório acessível-escala, bem como uma abordagem dimensionável para produção de NP para trabalho translacional.
Divulgações
Os autores não têm nada para divulgar.
Agradecimentos
Este trabalho foi financiado por fundos da Optimeos Life Sciences, National Science Foundation (CBET 1605816), o Bill e Melinda Gates Foundation (BMGF, OPP1150755) e o nacional Science Foundation pós-graduação bolsa de pesquisa (DGE-1656466) atribuído a K.D.R.
Materiais
| Name | Company | Catalog Number | Comments |
| Confined Impinging Jets Mixer | NA | NA | See supplemental information for engineering drawings. Review text for new mixer validation |
| Luer fitting | Idex Health & Science | P-604 | Assemble on CIJ or MIVM mixer inlet with corresponding threads |
| Plug fitting | Idex Health & Science | P-309 | Assemble on CIJ mixer sides (seal access point from drilling) |
| Outlet fitting - CIJ | Idex Health & Science | P-205 | Assemble with ferrule and tubing on CIJ chamber outlet |
| Outlet ferrule - CIJ | Idex Health & Science | P-200 | Assemble with outlet fitting (large end flush with tubing) |
| Outlet tubing - CIJ | Idex Health & Science | 1517 | Use tubing cutter for clean ends. Ensure extra tubing doesn't protrodue into mixing chamber |
| Tetrahydrofuran (THF) | Fisher Scientific | T425-4 | Use stabilizer-free THF to avoid solubility limits of BHT. Peroxides may interfere in some applications. |
| Norm-ject syringe (3 ml) | VWR | 53548-017 | |
| Vitamin E (α-tocopherol) | Sigma-Aldrich | 90669-50G-F | Store cold |
| poly(styrene-b-ethylene glycol), PS1.6k-b-PEG5k | Polymer Source | P13141-SEO | Other block sizes acceptable depending on application |
| poly(styrene)1.8k | Polymer Source | P2275-S | Example hydrophobic core material |
| Scintillation vial | DWK Lifesciences | 74504-20 | |
| Luer-slip plastic syringes, 1ml (100 pk) | National | S7510-1 | |
| Maltodextrin DE 4-7 | Sigma-Aldrich | 419672-100G | |
| poly(styrene-b-acrylic acid), PS5k-b-PAA4.8k | Polymer Source | P5917-SAA | Other block sizes acceptable depending on application |
| Dimethyl Sulfoxide (DMSO) | Fisher Scientific | D159-4 | |
| Calcium chloride dihdyrate | Sigma-Aldrich | 223506-25G | Hygroscopic. |
| Methanol | Fisher Scientific | A452-4 | |
| Ammonium Hydroxide | Fisher Scientific | AC423300250 | |
| Albumin from chicken egg white (Ovalbumin, OVA) | Sigma-Aldrich | A5503-1G | |
| Multi-Inlet Vortex Mixer | NA | NA | See supplemental information for engineering drawings. Review text for new mixer validation |
| Outlet fitting - MIVM | Idex Health & Science | P-942 | Combination with ferrule |
| Outlet tubing - MIVM | NA | NA | Fit to ferrule ID. |
| O-ring (MIVM) | C.E. Conover | MM1.5 35.50 V75 | Order bulk - consumable part. Ensure solvent compatibility if using an alternative source. |
| Mixer stand | NA | NA | See Markwalter & Prud'homme for design.17 |
Referências
- Bobo, D., Robinson, K. J., Islam, J., Thurecht, K. J., Corrie, S. R. Nanoparticle-Based Medicines: A Review of FDA-Approved Materials and Clinical Trials to Date. Pharmaceutical Research. 33 (10), 2373-2387 (2016).
- D'Mello, S. R., et al. The evolving landscape of drug products containing nanomaterials in the United States. Nature Nanotechnology. 12 (6), 523-529 (2017).
- Gindy, M. E., Prud'homme, R. K. Multifunctional nanoparticles for imaging, delivery and targeting in cancer therapy. Expert Opinion on Drug Delivery. 6 (8), 865-878 (2009).
- Chen, G., Roy, I., Yang, C., Prasad, P. N. Nanochemistry and Nanomedicine for Nanoparticle-based Diagnostics and Therapy. Chemical Reviews. 116 (5), 2826-2885 (2016).
- Johnson, B. K., Prud'homme, R. K. Mechanism for Rapid Self-Assembly of Block Copolymer Nanoparticles. Physical Review Letters. 91 (11), 118302-118302 (2003).
- Schubert, S., Delaney, J. J. T., Schubert, U. S. Nanoprecipitation and nanoformulation of polymers: from history to powerful possibilities beyond poly(lactic acid). Soft Matter. 7 (5), 1581-1588 (2011).
- Lebouille, J. G. J. L., Stepanyan, R., Slot, J. J. M., Cohen Stuart, M. A., Tuinier, R. Nanoprecipitation of polymers in a bad solvent. Colloids and Surfaces A: Physicochemical and Engineering Aspects. , 225-235 (2013).
- Akbulut, M., et al. Generic method of preparing multifunctional fluorescent nanoparticles using flash nanoPrecipitation. Advanced Functional Materials. 19 (5), 718-725 (2009).
- D'Addio, S. M., Prud'homme, R. K. Controlling drug nanoparticle formation by rapid precipitation. Advanced Drug Delivery Reviews. 63 (6), 417-426 (2011).
- Pagels, R. F., Edelstein, J., Tang, C., Prud'homme, R. K. Controlling and Predicting Nanoparticle Formation by Block Copolymer Directed Rapid Precipitations. Nano Letters. 18 (2), 1139-1144 (2018).
- Ding, S., Anton, N., Vandamme, T. F., Serra, C. A. Microfluidic nanoprecipitation systems for preparing pure drug or polymeric drug loaded nanoparticles: an overview. Expert Opinion on Drug Delivery. 13 (10), 1447-1460 (2016).
- Valencia, P. M., Farokhzad, O. C., Karnik, R., Langer, R. Microfluidic technologies for accelerating the clinical translation of nanoparticles. Nature Nanotechnology. 7 (10), 623-629 (2012).
- Johnson, B. K., Prud'homme, R. K. Chemical processing and micromixing in confined impinging jets. AIChE Journal. 49 (9), 2264-2282 (2003).
- Saad, W. S., Prud'homme, R. K. Principles of nanoparticle formation by flash nanoprecipitation. Nano Today. 11 (2), 212-227 (2016).
- Han, J., et al. A simple confined impingement jets mixer for flash nanoprecipitation. Journal of Pharmaceutical Sciences. 101 (10), 4018-4023 (2012).
- Kumar, V., Wang, L., Riebe, M., Tung, H. H., Prud'homme, R. K. Formulation and stability of itraconazole and odanacatib nanoparticles: Governing physical parameters. Molecular Pharmaceutics. 6 (4), 1118-1124 (2009).
- Liu, Y., Kathan, K., Saad, W., Prud'homme, R. K. Ostwald Ripening of β -Carotene Nanoparticles. Physical Review Letters. 98 (3), 036102-036102 (2007).
- Liu, Y., Cheng, C., Liu, Y., Prud'homme, R. K., Fox, R. O. Mixing in a multi-inlet vortex mixer (MIVM) for flash nano-precipitation. Chemical Engineering Science. 63, 2829-2842 (2008).
- Pagels, R. F., Prud'homme, R. K. Polymeric nanoparticles and microparticles for the delivery of peptides, biologics, and soluble therapeutics. Journal of Controlled Release. 219, 519-535 (2015).
- Pagels, R. F., Prud'homme, R. K. Ch. 11. Control of Amphiphile Self-Assembling at the Molecular Level: Supra-Molecular Assemblies with Tuned Physicochemical Properties for Delivery Applications Vol. 1271 ACS Symposium Series. , 249-274 (2017).
- Markwalter, C. E., Prud'homme, R. K. Ch. 12. Control of Amphiphile Self-Assembling at the Molecular Level: Supra-Molecular Assemblies with Tuned Physicochemical Properties for Delivery Applications Vol. 1271 ACS Symposium Series. , 275-296 (2017).
- Markwalter, C. E., Prud'homme, R. K. Design of a Small-Scale Multi-Inlet Vortex Mixer for Scalable Nanoparticle Production and Application to the Encapsulation of Biologics by Inverse Flash NanoPrecipitation. Journal of Pharmaceutical Sciences. 107 (9), 2465-2471 (2018).
- Gindy, M. E., Ji, S., Hoye, T. R., Panagiotopoulos, A. Z., Prud'Homme, R. K. Preparation of poly(ethylene glycol) protected nanoparticles with variable bioconjugate ligand density. Biomacromolecules. 9 (10), 2705-2711 (2008).
- Zhang, Y., et al. Design and Solidification of Fast-Releasing Clofazimine Nanoparticles for Treatment of Cryptosporidiosis. Molecular Pharmaceutics. 14 (10), 3480-3488 (2017).
- Pagels, R. F. . Polymeric Nanoparticles and Microparticles for the Delivery of Hydrophobic and Hydrophilic Therapeutics. , (2018).
- Frisken, B. J. Revisiting the method of cumulants for the analysis of dynamic light-scattering data. Applied Optics. 40 (24), 4087-4091 (2001).
- Budijono, S. J., Russ, B., Saad, W., Adamson, D. H., Prud'homme, R. K. Block copolymer surface coverage on nanoparticles. Colloids and Surfaces A: Physicochemical and Engineering Aspects. 360 (1-3), 105-110 (2010).
- Johnson, B. K., Prud'homme, R. K. Flash NanoPrecipitation of Organic Actives and Block Copolymers using a Confined Impinging Jets Mixer. Australia Journal of Chemistry. 56, 1021-1024 (2003).
- Kumar, V., Prud'homme, R. K. Nanoparticle stability: Processing pathways for solvent removal. Chemical Engineering Science. 64 (6), 1358-1361 (2009).
- Shi, L., Shan, J., Ju, Y., Aikens, P., Prud'homme, R. K. Nanoparticles as delivery vehicles for sunscreen agents. Colloids and Surfaces A: Physicochemical and Engineering Aspects. , 122-129 (2012).
- Dalwadi, G., Benson, H. A. E., Chen, Y. Comparison of Diafiltration and Tangential Flow Filtration for Purification of Nanoparticle Suspensions. Pharmaceutical Research. 22 (12), 2152-2162 (2005).
- Pansare, V. J., Tien, D., Thoniyot, P., Prud'homme, R. K. Ultrafiltration of nanoparticle colloids. Journal of Membrane Science. 538, 41-49 (2017).
- D'Addio, S. M., et al. Novel Method for Concentrating and Drying Polymeric Nanoparticles: Hydrogen Bonding Coacervate Precipitation. Molecular Pharmaceutics. 7 (2), 557-564 (2010).
- Abdelwahed, W., Degobert, G., Stainmesse, S., Fessi, H. Freeze-drying of nanoparticles: Formulation, process and storage considerations. Advanced Drug Delivery Reviews. 58 (15), 1688-1713 (2006).
- Correa, S., et al. Highly Scalable, Closed-Loop Synthesis of Drug-Loaded, Layer-by-Layer Nanoparticles. Advanced Functional Materials. 26 (7), 991-1003 (2016).
- Figueroa, C. . Engineering Nanoparticles for Pharmaceutical Applications: Formulation and Freeze-drying Techniques. , (2014).
- Harada, A., Li, J., Kamachi, M. Preparation and properties of inclusion complexes of polyethylene glycol with alpha-cyclodextrin. Macromolecules. 26 (21), 5698-5703 (1993).
- Troiano, G., Song, Y. -. H., Zale, S., Wright, J., Van Geen Hoven, C. Stable Formulations for Lyophilizing Therapeutic Particles. United States patent. , (2013).
- Kumar, V., Adamson, D. H., Prud'homme, R. K. Fluorescent polymeric nanoparticles: Aggregation and phase behavior of pyrene and amphotericin B molecules in nanoparticle cores. Small. 6 (24), 2907-2914 (2010).
- Budijono, S. J., et al. Synthesis of stable block-copolymer-protected NaYF4:Yb3+, Er3+up-converting phosphor nanoparticles. Chemistry of Materials. 22 (2), 311-318 (2010).
- Chen, T., et al. Protected peptide nanoparticles: Experiments and brownian dynamics simulations of the energetics of assembly. Nano Letters. 9 (6), 2218-2222 (2009).
- Sosa, C., et al. Soft Multifaced and Patchy Colloids by Constrained Volume Self-Assembly. Macromolecules. 49 (9), 3580-3585 (2016).
- Pinkerton, N. M., et al. Formation of stable nanocarriers by in situ ion pairing during block-copolymer-directed rapid precipitation. Molecular Pharmaceutics. 10 (1), 319-328 (2013).
- Lu, H. D., Rummaneethorn, P., Ristroph, K. D., Prud'homme, R. K. Hydrophobic Ion Pairing of Peptide Antibiotics for Processing into Controlled Release Nanocarrier Formulations. Molecular Pharmaceutics. 15 (1), 216-225 (2018).
- Lu, H. D., et al. Encapsulation of OZ439 into Nanoparticles for Supersaturated Drug Release in Oral Malaria Therapy. ACS Infectious Diseases. 4 (6), 970-979 (2018).
- Ansell, S. M., et al. Modulating the Therapeutic Activity of Nanoparticle Delivered Paclitaxel by Manipulating the Hydrophobicity of Prodrug Conjugates. Journal of Medicinal Chemistry. 51 (11), 3288-3296 (2008).
- Gindy, M. E., et al. Mechanism of macromolecular structure evolution in self-assembled lipid nanoparticles for siRNA delivery. Langmuir. 30 (16), 4613-4622 (2014).
- D'Addio, S. M., et al. Optimization of cell receptor-specific targeting through multivalent surface decoration of polymeric nanocarriers. Journal of Controlled Release. 168 (1), 41-49 (2013).
- . . Perry's Chemical Engineers' Handbook. , 19-20 (2007).
- Torrice, M. Does nanomedicine have a delivery problem?. ACS Central Science. 2 (7), 434-437 (2016).
- Karnik, R., et al. Microfluidic Platform for Controlled Synthesis of Polymeric Nanoparticles. Nano Letters. 8 (9), 2906-2912 (2008).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados