Method Article
Análise automatizada da marcha para avaliar a recuperação funcional em roedores com lesão de contusão do nervo periférico ou da medula espinhal
Neste Artigo
Resumo
A análise automatizada da marcha é uma ferramenta viável para avaliar a recuperação funcional em modelos de roedores de lesão nervosa periférica e lesão de contusão medular. Embora exija apenas uma configuração para avaliar a função locomotor em vários modelos experimentais, o ajuste meticuloso e macio e o treinamento dos animais é altamente importante.
Resumo
Lesões periféricas e centrais do nervo são estudadas principalmente em roedores, especialmente ratos, dado o fato de que esses modelos animais são econômicos e muitos dados comparativos foram publicados na literatura. Isso inclui uma infinidade de métodos de avaliação para estudar a recuperação funcional após lesões nervosas e reparos. Além da avaliação da regeneração nervosa por meio de histologia, eletrofisiologia e outras técnicas de avaliação in vivo e in vitro, a recuperação funcional é o critério mais importante para determinar o grau de regeneração neural. A análise automatizada da marcha permite o registro de uma grande quantidade de parâmetros relacionados à marcha, como a Área de Impressão do Pata e a Velocidade de Balanço da Pata, bem como medidas de coordenação entre membros. Além disso, o método fornece dados digitais das patas dos ratos após danos neuronais e durante a regeneração nervosa, adicionando ao nosso entendimento de como lesões nervosas periféricas e centrais afetam seu comportamento locomotor. Além do modelo de lesão do nervo ciático predominantemente utilizado, outros modelos de lesão nervosa periférica, como o nervo femoral, podem ser estudados por meio deste método. Além das lesões do sistema nervoso periférico, podem ser avaliadas lesões do sistema nervoso central, por exemplo, contusão medular. A avaliação de dados válida e reprodutível depende fortemente do ajuste meticuloso das configurações de software e hard antes da aquisição de dados. Além disso, o treinamento adequado dos animais experimentais é de importância crucial. Este trabalho tem como objetivo ilustrar o uso da análise de marcha automatizada computadorizada para avaliar a recuperação funcional em diferentes modelos animais de lesão nervosa periférica, bem como lesão de contusão medular. Também enfatiza as limitações do método, por exemplo, a avaliação da regeneração nervosa em ratos com neurotmese do nervo ciático devido à recuperação funcional limitada. Portanto, este protocolo é pensado para ajudar pesquisadores interessados em lesões nervosas periféricas e centrais a avaliar a recuperação funcional em modelos de roedores.
Introdução
Lesões do sistema nervoso periférico e central são frequentemente estudadas em roedores, resultando em uma grande quantidade de dados comparativos sobre o curso de lesão nervosa, reparação ou neuroproteção para neutralizar novas lesões secundárias e regeneração1,2,3. O resultado de estratégias experimentais de tratamento em modelos de roedores pode ser avaliado por uma variedade de técnicas como histologia, imunohistoquímica, eletrofisiologia e técnicas de imagem, como microtomografia de raios-X (μCT), mas o critério mais importante para determinar o sucesso de um tratamento é , como em pacientes humanos , o grau de recuperação funcional4,5. Os primeiros estudos que investigam o desempenho locomotor em roedores datam dos anos 19406,7,8. Ratos e camundongos foram sujeitos a uma grande quantidade de estudos que investigam seu comportamento locomotor nas décadasseguintes 9,10,11. Atualmente, existem uma ampla gama de técnicas de avaliação para modelos de roedores de lesões periféricas e centrais nervosas, que vão desde a análise de pista de caminhada com tinta e papel12,13,14 sobre a tornozeleira e a cinemática de marcha15,16,17 até métodos aprimorados de aprendizado de máquina, que permitem a estimativa de complexo de marcha, membro e trajetória articulatória18,19.
A Análise Automatizada de Marcha (AGA) computadorizada é usada para avaliar a função locomotor após lesões nervosas periféricas e centrais e potencial tratamento experimental de tais lesões. O dispositivo consiste principalmente de uma passarela de vidro e uma fonte de luz que ilumina as impressões da pata do roedor em correlação com a pressão excedida por eles. Esses dados são então informatizados para calcular uma ampla gama de parâmetros estáticos e dinâmicos. Segundo Deumens, esses parâmetros podem ser subdivididos nas categorias de parâmetros gerais, parâmetros relacionados à dor, bem como parâmetros relacionados à coordenação da marcha20 (Tabela 1). A viabilidade da AGA para detectar alterações no comportamento da marcha tem sido comprovada em vários modelos animais de lesão nervosa periférica (PNI)21, como o nervo ciático20,nervo femoral22e nervo mediano23,24. Também é usado rotineiramente para avaliar a função locomotor em ratos com lesões nervosas centrais, por exemplo, lesão de curso25 ou contusão medular26. Os avanços do método residem na grande quantidade de dados comparáveis e na sua possibilidade de registrar uma infinidade de parâmetros relacionados à marcha27. Este artigo tem como objetivo fornecer aos pesquisadores interessados em modelos animais de PNI e lesão medular (SCI) uma diretriz detalhada e prática para avaliar a função locomotor nesses modelos.
| Categoria | Parâmetro | Descrição | |
| Parâmetros gerais da marcha | Área de impressão (unidade de distância) | Área da impressão da pata | |
| Comprimento de impressão (unidade de distância) | Comprimento da impressão da pata | ||
| Base de Suporte (BoS) (unidade de distância) | Distância entre as duas patas traseiras ou dianteiras | ||
| Comprimento do passo (unidade de distância) | Distância entre duas colocações consecutivas de uma pata | ||
| Parâmetros relacionados à dor da marcha | Tempo de swing (s) | Duração da fase de balanço | |
| Tempo de espera (s) | Duração da fase de postura | ||
| Intensidade média da impressão da pata (unidade arbitrária) | Significa iIntensity da impressão da pata durante a fase de postura | ||
| Parâmetros relacionados à coordenação da marcha | Padrões normais de sequência de passos (NSSP) | Sequências específicas de colocações de patas durante um ciclo de passos | |
| Dispersões de fase (%) | Diferenças temporais entre os ciclos de passo de duas patas específicas | ||
| Índice de Regularidade (RI) (%) | Quantificação da coordenação interlimb dividindo a quantidade de NSSP impecável vezes 4 pelo número total de colocação da pata durante um ciclo de passo | ||
Tabela 1: Parâmetros de marcha avaliados com a análise de marcha automatizada. As categorias em que os parâmetros são classificados são escolhidas de acordo com Deumens et al.20.
Protocolo
O protocolo experimental para todos os experimentos foi aprovado antecipadamente pelo Conselho de Revisão do Protocolo Animal da Prefeitura de Viena. Todos os procedimentos foram realizados em total conformidade com a Declaração de Helsinque sobre Direitos dos Animais e o Guia de Cuidado e Uso de Animais de Laboratório dos Institutos Nacionais de Saúde.
1. Habitação animal
- Casa de ratos machos (Lewis ou Sprague Dawley) pesando 250-300 g sob um ciclo claro/escuro de 12 horas com acesso ad libitum a alimentos e água.
- Controle tanto a temperatura ambiente (mantida em 20-22 °C) quanto a umidade (45%-65 %) para habitação animal adequada. Para este trabalho, foram utilizados ratos masculinos de Lewis (PNIs) e Sprague Dawley (SCI).
- Forneça uma gaiola nova e limpa duas vezes por semana. Abrigar ratos em grupos de dois ou três e acompanhar de perto seu comportamento social e interação. Permita aos ratos um período de aclimatação de pelo menos 1 semana antes de qualquer procedimento cirúrgico ou teste funcional.
NOTA: Os ratos exigem pelo menos 5 dias de treinamento diário no aparelho de análise de marcha antes da cirurgia, então calcule pelo menos 2 semanas entre a chegada dos ratos na instalação e os dados agendados para cirurgia experimental28.
2. Indução de lesão nervosa
NOTA: Use equipamentos de proteção individual, como um vestido cirúrgico, luvas e uma máscara. Caso um vestido cirúrgico estéril não esteja disponível, um jaleco limpo e lavado também é suficiente. A menos que esteja contaminado, o vestido ou casaco não precisa ser trocado entre animais, mas entre as sessões de cirurgia. Recomenda-se o uso de luvas cirúrgicas estéreis. Caso essas luvas não estejam disponíveis, luvas de exame também podem ser usadas, mas devem ser lavadas antes da cirurgia usando desinfetante cirúrgico. Luvas devem ser trocadas entre animais.
- No dia da cirurgia, tente minimizar qualquer estresse aos animais, pois isso pode interferir na anestesia, por exemplo, os animais exigirão doses mais altas de anestésicos.
- No dia da cirurgia, injete 0,05 mg de buprenorfina/kg de peso corporal em suspensão com 100-200 μL 0,9% NaCl subcutânea usando uma cânula de 25 G 1 h antes da cirurgia para fornecer analgesia pré e interoperatória. Se não for indicado de outra forma, o flanco do rato é o local preferido para injeção.
- Anestesiar os ratos colocando-os em uma câmara de indução de anestesia conectada a um vaporizador sevoflurano e um recipiente ativo de giz para absorver o CO2. Anestesiar o rato inundando a caixa de anestesia com 4%-5% de mistura de sevoflurano-oxigênio por cerca de 5 minutos usando um fluxo de oxigênio de 1,5 L/min (fase de iniciação). Conecte um clipe de oximetria de pulso a uma das patas para monitorar a saturação de oxigênio sanguíneo do roedor. Manter o estado da anestesia geral com 2,5% a 4,5% de mistura de sevoflurano-oxigênio.
NOTA: Para cirurgia experimental, a anestesia geral é obrigatória. Confirme a anestesia geral verificando a falta de resposta para beliscar estímulos da cauda ou patas. - Quando o rato entrar na anestesia geral, raspe o respectivo areal que será operado e desinfete a área deslizando-a alternadamente com álcool e desinfetante de pele. O último deslizar deve ser realizado com desinfetante de pele.
- Coloque-o em uma almofada de aquecimento ajustável na posição necessária (supina para o modelo de nervo femoral, propenso ao modelo ciático e SCI). Insira uma sonda de termômetro flexível no reto do rato para monitorar a temperatura do animal e mantendo-a em torno de 37 °C durante a cirurgia. Durante a anestesia, proteja os olhos do rato da profanação usando pomada ocular
3. Indução cirúrgica de lesão nervosa
- Ao realizar procedimentos cirúrgicos, adere estritamente aos sete princípios de Halsted29 da seguinte forma:
- Sempre manuseie os tecidos suavemente quando trabalhar com eles. Evite rasgar ou esmagar os tecidos.
NOTA: Sistemasretráteis auto-fabricados ou comercialmente disponíveis são úteis para manter os músculos e vasos fora do campo de operação. - Mantenha cuidadosamente a hemostase usando um hemostat elétrico para cauterizar vasos ou ligaduras para garantir hemostasia cuidadosa.
- Mantenha sempre o suprimento de sangue para os tecidos dissecando-os cuidadosamente e manuseando-os delicadamente.
- Mantenha a assepsia estrita usando uma máscara, um vestido e luvas estéreis.
- Evite a tensão nos tecidos aplicando suturas que não são muito apertadas nem muito soltas.
- Meticulosamente apagar os tecidos, unindo suas respectivas bordas sem qualquer sobreposição.
NOTA: Isso é particularmente importante no caso da neurorreféia epineurial ou perineurial. Realize todos os procedimentos microcirúrgicos sob ampliação de 6x-16x usando um microscópio operacional. Idealmente, o microscópio fornece dois pares de oculares para permitir a observação da operação por um assistente. - Evite a criação de espaços mortos suturando cuidadosamente as diferentes camadas teciduais.
- Sempre manuseie os tecidos suavemente quando trabalhar com eles. Evite rasgar ou esmagar os tecidos.
- Indução da neurotmese do nervo ciático da cetamina traseira direita
- Exponha o nervo ciático direito no nível médio realizando uma incisão de 5 cm de comprimento no lado dorsal do membro traseiro com uma lâmina de bisturi #10 conectada a uma alça de bisturi #3 e dissecando a musculatura sobrevasa e tecido mole. Coloque um retrátil dentro da ferida para manter a musculatura dissecada e a pele fora do situs. Exponha suavemente o nervo removendo o tecido circundante usando uma tesoura microcirúrgica curva.
- Remova um segmento nervoso longo de 8 mm do nervo ciático de 1 a 2 mm proximal à sua trifurcação com uma tesoura microcirúrgica reta.
- Gire o segmento nervoso 180°, coloque-o entre o toco proximal e distal do nervo ciático transeccionado e realize neurorrefáfia epineurial em cada local com duas suturas interrompidas 10-0 e um suporte de agulha microcirúrgica.
- Indução de neurotmese do nervo femoral na cetraça traseira direita
- Realize uma incisão longitudinal de 3 a 4 cm na virilha com uma lâmina de bisturi #10 conectada a uma alça de bisturi #3, a fim de expor o feixe neurovascular femoral direito. Use uma tesoura cirúrgica para dissecção contundente até que a bifurcação do nervo femoral seja exposta. Coloque um retrátil dentro da ferida para manter a musculatura dissecada e a pele fora do situs.
- Transecte os ramos motores e sensoriais expostos distal à bifurcação e extirpa um segmento nervoso de 6 mm de comprimento de cada ramo, respectivamente, utilizando uma tesoura microcirúrgica reta.
- Gire ambos os segmentos nervosos 180°, coloque-os entre o toco proximal e distal dos ramos do nervo femoral transectado e realize neurorrefáfilia epineurial em cada local com duas suturas interrompidas 11-0 e um suporte de agulha microsúrgica.
NOTA: Realize um enxerto nervoso autólogo homotítpico enxertando o enxerto motor no ramo motor original e o enxerto sensorial ao ramo sensorial original. Alternativamente, realize um enxerto nervoso autólogo heterotópico enxertando o enxerto motor no ramo sensorial original e vice-versa.
- Indução da contusão da medula espinhal torácica
- Realize uma incisão cutânea através da coluna vertebral torácica com uma #10 lâmina de bisturi conectada a uma alça de bisturi #3 seguida de duas incisões musculares paralelas aos processos espinhosos para facilitar a retração muscular. Coloque um retrátil dentro da ferida para manter a musculatura dissecada e a pele fora do situs.
- Identifique a vértebra torácica 11ª (Th) e exponha a lâmina do arco vertebral removendo tecido sobrelado, bem como o processo espinhoso usando um rongeur.
- Realize uma laminectomia usando uma micro broca e uma rebarba apropriada para perfurar um pequeno furo na lâmina, ligeiramente maior que a ponta do impactor. Para evitar danos à medula espinhal, apenas diminua a lâmina enquanto abre e amplia o orifício usando um rongeur. Se o periosteum ainda estiver intacto, remova-o cuidadosamente usando uma sonda pontiaguda afiada sem danificar a dura-máter.
- Depois de garantir que um buraco grande o suficiente seja feito sem desestabilizar a lâmina, mantenha a coluna vertebral do animal no lugar, fixando-a rostrally e caudally até Th11 com as fórceps estabilizadores do impactor. Usando as rodas de mão na frente e na lateral, posicione a haste de aço 3-5 mm acima do orifício de laminectomia. Finalmente, sujeitar todos os animais a um impacto com uma força definida de 150 quilodyne para induzir um grau leve a moderado de contusão medular4.
- Realize o fechamento da ferida em camadas anatômicas usando poliglactina 4-0 ou 5-0 e um suporte de agulha cirúrgica. Limpe a ferida bem limpando-a suavemente com uma almofada de gaze encharcada em NaCl 0,9% estéril.
- Após a cirurgia, devolva os animais para sua gaiola de origem e os proteja da exposição à luz e ao som. Monitore o comportamento dos animais de perto até o dia pós-operatório (DPO) 7 e garanta o consumo suficiente de alimentos e água. Se necessário, forneça fluido adicional por injeções subcutâneas (por exemplo, 10 ml NaCl 0,9%).
- Fornecer analgesia pós-operatória por um mínimo de 2 dias por meio de, por exemplo, opioides (0,05 mg/kg de peso corporal Buprenorfina subcutânea (s.c.)) e/ou antipiréticos (4 mg/kg de peso corporal Carprofen s.c.). Se necessário, e no caso do modelo SCI, também fornecer terapia antiaudiológica pós-operatória (7,5 mg/kg de peso corporal Enrofloxacin por os (p.o.)).
- Em caso de lesão medular, esvazie manualmente a bexiga do rato até que a urinação espontânea retorne.
4. Recuperação de intervenções cirúrgicas antes da análise da marcha
NOTA: Ratos com lesão no nervo ciático mostram a tendência de roer suas patas traseiras devido ao aparecimento de neuropatia dolorosa após lesão nervosa. Esta forma de automutilação pode resultar em autoamputação de dedo dos dedo ou partes da respectiva pata traseira. Prefira os ratos de Lewis em vez de outras cepas de ratos no caso de usar o modelo de lesão do nervo ciático, pois esta cepa de rato mostra uma tendência menor para a automutilação31. Ratos com lesão no nervo ciático também mostram a tendência de desenvolver contraturas do membro operado, o que pode resultar em sua exclusão do estudo devido à interferência na aquisição de dados. Tais eventos adversos ocorrem muito menos comuns em ratos com lesão femoral.
- Inspecione animais operados diariamente após a cirurgia com especial atenção sobre o estado de seus membros e patas, respectivamente.
NOTA: Em ratos com SCI, na altura de Th11, prolapso peniano ou retal pode ocorrer devido ao comprometimento da capacidade natural dos animais de urinar e defecar. Esses eventos são comumente definidos como pontos finais humanos do estudo e implicam a exclusão imediata do animal afetado do estudo. - Continue a analgesia pós-operatória até que os ratos deixem de apresentar qualquer sintoma relacionado à dor.
- Em caso de dor persistente, administre a gabapentina (30-120 mg/kg de peso corporal) p.o. para tratar dor neuropática.
5. Preparação antes de realizar análise automatizada da marcha
NOTA: A metodologia do sistema de análise de marcha baseia-se no registro dos animais de baixo enquanto cruza uma placa de vidro, que é iluminada por uma luz LED verde. Quando as patas dos animais entram em contato com o chão, a área da impressão da pata é iluminada e gravada por uma câmera de vídeo de alta velocidade. Esses dados são então enviados através de um cabo Ethernet para um computador executando o software de análise de marcha. Embora as pegadas individuais possam ser classificadas manualmente pelo experimentador, a versão mais recente do software também possui classificação automática de pegada.
- Realize todos os procedimentos de teste no escuro e na ausência de ruídos perturbadores. Uma vez que os ratos são capazes de perceber frequências supersônicas, também verificar que nenhuma fonte está emitindo tais sons.
NOTA: Realizar análises de marcha semanal ou quinzenalmente, mas não testar ratos com muita frequência, pois especialmente os ratos de Lewis tendem a perder o interesse em participar do procedimento ao longo do tempo quando são expostos a um determinado exercício com muita frequência. É, no entanto, necessário treinar ratos diariamente por 5 dias antes da cirurgia para aclimatá-los ao ambiente de testes e procedimento. - Durante as sessões de treinamento e no dia do teste, prepare a sala de teste comportamental desligando todas as fontes de luz, o que poderia interferir com a câmera do dispositivo de análise de marcha automatizada. Coloque a tela do computador necessária para a aquisição de dados longe da câmera para evitar que sua luz interfira com a câmera.
- Certifique-se de que o dispositivo está instalado em uma posição estável e de forma a evitar qualquer forma de vibração, pois isso interferirá seriamente no procedimento de aquisição de dados.
- Leve os ratos para a sala de testes comportamentais e aclimá-los em sua própria gaiola por pelo menos 30 minutos antes do teste.
NOTA: Sempre que manusear os animais, use equipamentos de proteção individual, como um vestido cirúrgico ou jaleco, luvas e uma máscara.
6. Realizar análise automatizada de marcha
- Sessões de treinamento
NOTA: Durante o treinamento, os animais passarão por uma curva de aprendizado, por isso é recomendado ajustar o cronograma de treinamento gradualmente. Use recompensas alimentares (por exemplo, 1-2 pedaços de cereal de café da manhã) para recompensar os animais após a conclusão bem sucedida de cada sessão de treinamento.- No primeiro dia de treinamento, levante suavemente o animal segurando-o debaixo do tronco e leve-o suavemente até a entrada da passarela.
- Coloque o animal na área de entrada e deixe explorar a abertura do corredor sem qualquer interferência da pessoa que realiza o procedimento de teste.
NOTA: Não grite, assopre, sopre ou cutuque o animal na tentativa de motivá-lo a atravessar a passarela. Todo esse comportamento irá estressar severamente o animal e complicar ainda mais o procedimento de aquisição de dados. - Espere até que o animal cruze voluntariamente a passarela para chegar à sua gaiola. Às vezes, especialmente em animais destreinados, isso pode levar até vários minutos. No primeiro dia de treinamento, o animal não é nem esperado nem necessário para fazer corridas ininterruptas com velocidade de caminhada uniforme. Em vez disso, deve aclimatar-se com o aparelho de teste e o procedimento.
- No segundo dia de treinamento, acostume os animais a entrar na passarela sem hesitar e, também, voltar para sua gaiola de origem sem hesitação. Alguns animais provavelmente já aprenderam a atravessar a passarela sem interrupções, mas isso ainda não é necessário no final do segundo dia.
- No terceiro dia de treinamento, garanta que os animais aprendam a atravessar a passarela sem hesitar, cheirar ou movimentos exploratórios. Certifique-se de que eles andam com velocidade uniforme.
- No quarto e quinto dia de treinamento, repita o exercício anterior para consolidar o procedimento de teste.
NOTA: Caso um animal não adquira a habilidade necessária para atravessar a passarela corretamente até o final do período de treinamento de 5 dias, adicione 2 dias adicionais de treinamento (por exemplo, o fim de semana). Além disso, considere realizar até 3 sessões de treinamento por dia, separadas por pelo menos 2h de descanso entre as sessões individuais. Em 95% dos casos, o animal terá adquirido a experiência de treinamento necessária ao final deste período de treinamento prolongado. No raro caso em que um animal ainda não adquiriu essa habilidade após 7 dias de treinamento, recomenda-se adiar a sessão de cirurgia experimental planejada por pelo menos 1 semana e repetir o referido regime de treinamento.
7. Aquisição de dados
NOTA: O sistema de análise de marcha visualiza cada impressão de pata enquanto o animal está andando e analisa automaticamente vários parâmetros de marcha, como Área de Impressão da Pata, Intensidade da Impressão da Pata, Tempo de Balanço da Pata e Velocidade de Balanço da Pata(Tabela 1). À medida que o sistema de análise de marcha registra todos os dados com base na intensidade gerada pelas impressões das patas dos animais, certifique-se de que as configurações da câmera sejam ajustadas de acordo com o peso e o tamanho dos ratos. Além disso, certifique-se de que a passarela está seca e limpa antes do registro de dados para evitar qualquer influência na aquisição de dados.
- Antes da aquisição de qualquer dado, limpe a passarela usando limpador de vidro comercial e um rodo. Pulverize a placa de vidro várias vezes e limpe-a com o rodo para remover quaisquer partículas de sua superfície. Além disso, limpe a parte de baixo. Certifique-se de remover qualquer fluido das extremidades da passarela, já que os animais poderiam pisar nela, o que afetaria os dados registrados.
- Repita o procedimento de limpeza sempre que necessário, por exemplo, contaminação da passarela e antes do registro dos dados de um rato de uma gaiola diferente. Acredita-se que isso impeça o animal de se distrair com o cheiro de seus conespecíficos.
- Antes da primeira aquisição de dados, ajuste as configurações da câmera que se encaixam no peso dos animais. Confirme isso colocando o animal mais leve e pesado na passarela e escolha uma configuração de câmera que permita boa qualidade de dados em ambos os casos. Ajuste o ganho da câmera, luz do teto vermelho, luz de passarela verde e limiar de intensidade verde (GIT) para garantir a detecção ideal de impressão da pata.
NOTA: Não altere as configurações escolhidas após o início da aquisição de dados, pois isso dificultará a comparabilidade dos dados adquiridos. Como exceção, o GIT pode ser alterado durante a classificação de dados, mas isso deve ser feito para todos os ensaios uniformemente. - Defina e calibrar a passarela usando a folha de calibração fornecida.
- Escolha uma câmera registrada listada na guia Configuração.
- Clique no botão Abrir aquisição que pode ser encontrado na guia Adquirir.
- Tire uma foto da passarela vazia e limpa, que será usada como referência durante o seguinte procedimento de aquisição de dados.
- Observe o status mudando de Esperar por Snapshot para Pronto para Aquisição.
- Clique no botão Iniciar Aquisição e observe a mudança de status de Ready for Acquisition para Waiting for Run to Start.
- Coloque um rato na passarela e siga o movimento do animal na tela do computador. Observe a mudança de status de Esperar por Correr para Começar a Gravar Run.
NOTA: O software classificará automaticamente as execuções que julgarem compatível de acordo com as características de execução predefinidas com um símbolo verde, enquanto as execuções não compatíveis serão marcadas com um símbolo vermelho. O software interrompe automaticamente a aquisição de dados quando três execuções em conformidade foram registradas, mas a aquisição de dados pode ser continuada clicando no botão Iniciar aquisição novamente.
8. Classificação de dados
NOTA: Consulte a Tabela 1 para obter uma lista de parâmetros de desfecho da AGA. Pelo menos três corridas compatíveis são necessárias nas quais o animal deve atravessar a passarela de forma constante sem hesitar27. Além disso, as velocidades de corrida devem corresponder nas mesmas categorias definidas na literatura30.
- Clique no botão Classificar na guia Explorador Experimental dos respectivos ensaios que devem ser classificados.
- Jogue a corrida adquirida com velocidade normal para ter uma impressão se os dados estão de acordo com os requisitos listados anteriormente.
- No canto superior esquerdo, clique no botão AutoClass para classificação automática de impressões de patas pelo software.
NOTA: Embora o software tenha uma alta taxa de classificação correta da pata, às vezes ele não atribui uma pata às impressões ou atribui a pata errada. Portanto, verifique sempre as impressões automáticas das patas depois. - Para o cálculo correto dos Padrões de Sequência de Passos Normais (NSSPs), certifique-se de que o algoritmo de classificação não seja confundido por impressões de patas não visíveis, levando a NSSP(Figura 1A)falhos . Portanto, inclua apenas as impressões da pata que são detectáveis enquanto a pata contralateral também é visível para cálculos NSSP, por exemplo, a pata dianteira esquerda (LF) e a pata traseira direita (RH) (Figura 1B).

Figura 1: Dados exemplares da AGA, demonstrando a necessidade de verificação manual dupla da classificação correta dos dados. No caso de uma colocação detectada de uma pata dianteira for bem sucedida pela colocação detectada de outra pata dianteira (A)o software AGA pode confundir isso com um padrão de caminhada descoordenado, uma vez que nenhuma pata traseira foi detectada. Portanto, recomenda-se sempre verificar duas vezes e selecionar uma impressão inicial da pata, que é detectada quando a pata contralateral também é visível (B). Clique aqui para ver uma versão maior desta figura.
9. Cálculo de estatísticas
NOTA: Para ajustar os dados de execução para mudanças relacionadas ao ganho de peso ao longo do tempo, é fortemente recomendado calcular uma razão da pata experimental com uma pata não experimental (por exemplo, controle). Além disso, calcule a razão para os valores pré-operatórios desta comparação pata-pata para considerar as diferenças individuais no uso da pata.
- Clique no botão Exibir Estatísticas para obter uma visão geral abrangente das estatísticas de execução.
- Selecione Arquivo e Exportação para exportar estatísticas ou estatísticas de ensaio em um software de planilha.
Resultados
12 ratos foram submetidos a cirurgia nervosa periférica experimental. A ressecção do nervo ciático(Figura 2A) foi realizada em 7 ratos, enquanto a neurotmese do nervo femoral(Figura 2B) foi induzida em 5 ratos. Em todos os animais, o defeito nervoso foi reconstruído por meio de um enxerto nervoso autólogo. Lesão por contusão medular(Figura 2C) no nível Th11 foi induzida em 6 ratos, resultando em um total de 18 ratos.
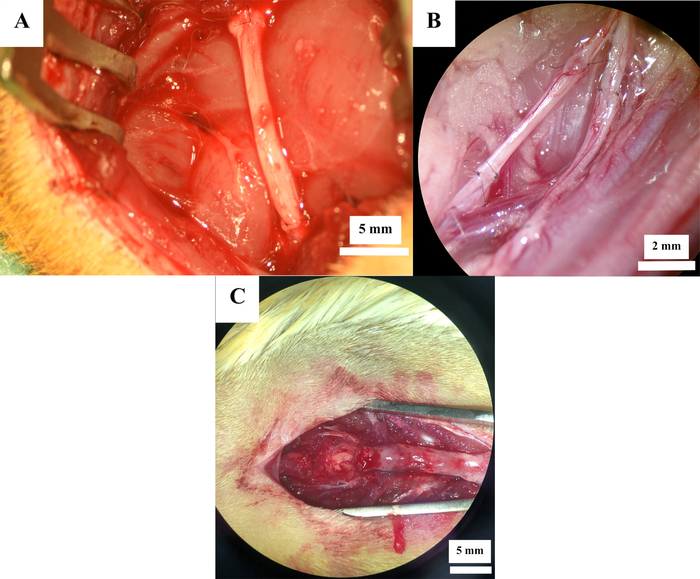
Figura 2: Locais operacionais após a reconstrução nervosa. Reconstrução nervosa com autoenxertos no nervo ciático(A) e nervo femoral(B)bem como após lesão de contusão medular(C). Clique aqui para ver uma versão maior desta figura.
Todos os animais se recuperaram bem da cirurgia e não houve casos de automutilação. Um animal do grupo de lesão do nervo ciático desenvolveu fortes contraturas da pata traseira direita durante o período de observação pós-operatória e teve que ser excluído da análise de dados posteriores.
Neurotmese do nervo ciático
Uma vez que o nervo ciático fornece inervação muscular e sensorial para a maioria da plataforma traseira, sua ressecção resulta em um grave comprometimento da função locomotor. Após a lesão, os ratos usam o calcanhar da pata apenas para suporte de peso(Figura 3B-E) e o membro é movido em um movimento circundutor varrendo. Portanto, as alterações locomotorizadas via AGA tornam-se aparentes por meio de uma área de impressão significativamente reduzida (Figura 4A) e significativamente aumentadas do Swing Time(Figura 4B). Ambos os parâmetros ainda foram significativamente alterados em comparação com as medições pré-OP como no final do período de observação. Notável, um animal desenvolveu fortes contraturas da pata traseira direita a partir da semana pós-operatória (WPO) 10. Isso resultou em um aumento da Área de Impressão da pata traseira direita para mais de 150% em comparação com a pata esquerda em WPO12(Figura 5). Por se trata de um extremo em comparação com todos os outros animais avaliados neste estudo, excluímos este animal da análise de dados em relação à Área Impressa.

Figura 3: Impressões representativas da pata antes e seguindo a ressecção de tamanho crítico do nervo ciático direito e reparo do autoenxerto. Note-se a forte diminuição na Área de Impressão após lesão nervosa(B)em relação ao pré-operatório(A). Apesar de um leve incremento na Área de Impressão durante o período de observação (C-E) as impressões da pata do membro traseiro direito permaneceram notavelmente alteradas das gravações da linha de base. Clique aqui para ver uma versão maior desta figura.

Figura 4: O curso de recuperação funcional após ressecção de tamanho crítico e reparo de autoenxerto do nervo ciático. A razão da área de impressão (A) e a Razão de Tempo de Oscilação(B)foram mudadas estatisticamente significativamente dos valores pré-OP imediatamente após a ressecção do nervo ciático. Embora a Área de Impressão tenha permanecido significativamente reduzida em comparação com a linha de base até wpo10, o Swing Time ainda foi significativamente aumentado para os valores pré-OP no WPO12. *: p < 0,05 em relação ao Pré-OP, **: p < 0,01 em relação ao Pré-OP. As barras de erro indicam ± erro padrão da média (SEM). Clique aqui para ver uma versão maior desta figura.

Figura 5: Boxplot do curso de Área de Impressão após lesão do nervo ciático. Note o extremo (elipse vermelha) no WPO12, o que é explicado pelo fato de que um animal desenvolveu fortes contraturas da pata traseira direita a partir de WPO10. O animal foi, portanto, excluído da análise estatística apresentada na Figura 4. Clique aqui para ver uma versão maior desta figura.
Neurotmese do nervo femoral
A ressecção do nervo femoral resulta na denervação do músculo quadríceps da coxa33,34. Em consequência, a extensão do joelho é prejudicada, resultando em hiperflexão da articulação do tornozelo com elevação consecutiva do calcanhar da pata. Portanto, a respectiva Área de Impressão da pata (Figura 6B), é fortemente reduzida após a cirurgia. A área de impressão da pata traseira esquerda é aumentada devido a uma mudança compensatória de peso para a esquerda. Isso deve ser mantido em mente, pois este fenômeno influencia diretamente a razão calculada entre a pata "experimental" e o "controle". A partir da reinervação do quadríceps WPO4 pelo nervo femoral regenerador leva à reversão dessas alterações, resultando no aumento da Área de Impressão da Pata da pata traseira direita(Figura 7A). Como o músculo quadríceps da coxa também desempenha um papel na fase de oscilação da respectiva pata, Swing Time (Figura 7B) é muito prolongado em ratos com lesão do nervo femoral. Espelhando o retorno da Área de Impressão, swing time diminui à medida que o nervo femoral regenerador atinge o músculo quadríceps da coxa. No WPO10, ambos os parâmetros da marcha voltaram à linha de base, sinalizando recuperação funcional completa.

Figura 6: Impressões de pata representativas. Impressões representativas da pata antes de (A) e seguinte(B-E) direita ressecção do nervo femoral e reparo de autoenxerto. A área de impressão de RH diminuiu fortemente no WPO2 (B),enquanto um aumento na Área de Impressão da pata traseira esquerda (LH) devido ao aumento da carga de peso tornou-se visível. A área de impressão rh começou a aumentar a partir de WPO6 (C) acompanhada por uma diminuição na área de impressão do LH. No WPO8(D) e WPO10(E) Área de Impressão de RH recuperou-se perto dos níveis pré-operatórios. (Adaptado com permissão da Heinzel et al.22, licenciado sob CC BY 4.0.) Clique aqui para ver uma versão maior desta figura.
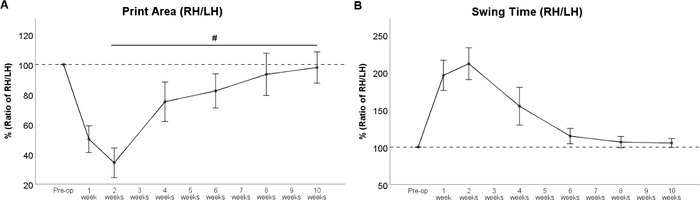
Figura 7: O curso de recuperação funcional após ressecção de 7 mm e reparo de autoenxerto do nervo femoral. O curso de Taxa de Área de Impressão (A) e Swing Time Ratio(B) revelou uma forte mudança imediatamente após a ressecção do nervo femoral, mas os valores se recuperaram de volta aos valores pré-operatórios no WPO8. #: p < 0,05. As barras de erro indicam ± SEM. (Adaptado com permissão da Heinzel et al.22, licenciado sob CC BY 4.0.) Clique aqui para ver uma versão maior desta figura.
Contusão medular
A análise da marcha revelou impressões de patas marcadamente alteradas após lesão de contusão na medula espinhal torácica(Figura 8),mais notável um decréscito na Área de Impressão e uma rotação interna marcada das patas traseiras no WPO2(Figura 8B). Vale ressaltar que a rotação da pata também é implementada como recurso de avaliação no BBB, ressaltando a aplicabilidade da análise informatizada da marcha para avaliar as alterações da marcha que foram originalmente avaliadas com testes de Campo Aberto. Quanto ao curso dos parâmetros individuais da marcha, a contusão da medula espinhal no nível de11 de dezembro resultou em diminuição da Relação de Área de Impressão (Figura 9A) e incremento da Razão de Tempo de Oscilação(Figura 9B). Ambos os parâmetros tendência para níveis de linha de base durante o curso posterior do período de observação, mas não houve alterações estatisticamente significativas observáveis. O Índice de Regularidade do parâmetro relacionado à coordenação (Figura 9C) também diminuiu no WPO2, mas o grau variou muito entre os animais. Também se voltou para valores pré-operatórios até wpo16. Base de Apoio das patas traseiras(Figura 9D),parâmetro geral de marcha segundo Deumens, mostrou um aumento acentuado, que foi estatisticamente significativo de WPO10 até WPO14. Ele tendênciau para os níveis de linha de base no WPO16 e não foi mais significativamente alterado a partir do valor Pré-OP neste momento.

Figura 8: Impressões de pata representativas das duas patas traseiras. A pata imprime no pré-operatório(A)e segue lesão de contusão na medula espinhal torácica(B-F). Observe a redução na área de impressão a partir de WPO2 (B) acompanhada de uma notável rotação interna das patas. Durante o período de observação (C–F) um incremento da Área de Impressão é observável, bem como o desobstrução da rotação interna. Clique aqui para ver uma versão maior desta figura.
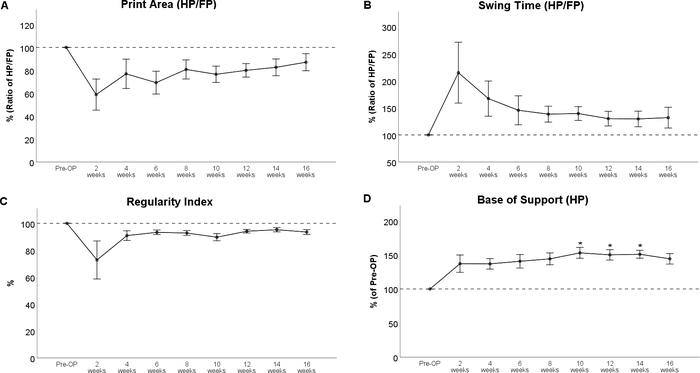
Figura 9: Contusão medular no nível th 11. A contusão da medula espinhal no dia 11 de dezembro resultou em alterações observáveis da Relação de Área de Impressão (A) e Tempo de Oscilação(B) e do Índice de Regularidade(C),mas essas alterações não foram estatisticamente significativas. Após a lesão, base de apoio das patas traseiras mostrou um aumento acentuado em relação à linha de base, o que foi estatisticamente significativo no WPO10 até WPO14. *: p < 0,05 em relação ao Pré-OP. As barras de erro indicam ± SEM. Clique aqui para ver uma versão maior desta figura.
Arquivo complementar 1: Detalhes de solução de problemas. Clique aqui para baixar este arquivo.
Discussão
A avaliação da recuperação funcional em modelos animais de PNI e SCI continua sendo desafiadora devido à grande variedade de métodos de avaliação, cada um com vantagens e desvantagens individuais. Apenas poucas abordagens foram testadas e validadas em múltiplos modelos de lesões nervosas periféricas e centrais, embora novas técnicas promissoras que combinem rastreamento de movimento e aprendizado de máquina podem potencialmente impulsionar a pesquisa neurobehavioral para o próximo nível de testes funcionais. Estamos convencidos de que métodos de ponta amplamente aplicáveis a uma grande variedade de modelos de animais e lesões surgirão em breve. À luz dessas considerações, uma das vantagens da AGA é a possibilidade de avaliar a recuperação funcional em múltiplos modelos de lesão nervosa usando apenas um dispositivo. Desde o início dos anos 2000, essa abordagem tem sido utilizada em modelos experimentais de PNI, como o ciático37, peroneal38, e o modelo de lesão do nervo femoral22, bem como após a avulsão raiz tanto doplexo lombar 39 quanto do plexo braquial40. Várias lesões nervosas centrais, incluindo lesão por contusão medular, também foram estudadas com o método41,42. Com este artigo, apresentamos um protocolo detalhado sobre como induzir três lesões nervosas comumente estudadas, bem como como avaliar a recuperação funcional posteriormente. Em nossa opinião, uma diretriz prática para pesquisadores interessados na área de lesão nervosa experimental, reparo e regeneração sobre como fazer o uso ideal das características vantajosas do método seria de grande ajuda.
Vários autores abordaram o potencial da AGA para avaliar a recuperação funcional em roedores, destacando a vantagem do método de avaliar simultaneamente parâmetros de marcha relacionados à reinervação motora e sensorial27,28. Além disso, a comparação dos dados de uma pata experimental, por exemplo, reconstruiu a lesão nervosa a uma pata não operada, como foi mostrado em ambos os modelos apresentados, permite a inclusão de um controle positivo intra-animal. Inversamente, uma pata operada sem reconstrução cirúrgica ou tratamento adicional poderia servir como um controle negativo intra-animal. Também foi demonstrado que é possível combinar AGA com abordagens de aprendizado de máquina43. Apesar das vantagens do método, também possui diversas limitações e desvantagens, como os esforços de treinamento demorados, que são obrigatórios para acostumar o animal ao procedimento de aquisição28,44. Outra limitação da AGA é o tamanho máximo dos animais elegíveis para testes devido às dimensões limitadas do aparelho. Portanto, o uso da AGA está atualmente limitado a animais do tamanho de roedores e furões45. Além disso, abordagens de avaliação neuroabameteral recentemente emergentes no campo do rastreamento de movimento capazes de aprender de máquina podem superar a AGA tanto na integralidade quanto nas possíveis aplicações18,19,46. Mais notável, mas de acordo com outros métodos de avaliação, parece que a recuperação funcional avaliada pela AGA é fortemente limitada — se mesmo ocorrendo — em modelos de neurotmese do nervo ciático47,48. Por outro lado, a AGA permite uma avaliação abrangente do curso de recuperação funcional após a neurotmese do nervo femoral, como mostrado por nossos dados. Com este trabalho, demonstramos que a Área de Impressão do Pata é um parâmetro de marcha representativo avaliado via AGA, o que é exemplar para o curso de recuperação funcional nos dois modelos de lesão nervosa periférica supracitados apresentados por nós. Enquanto o anúncio de recuperação funcional integrum era observável após a reparação do autoenxerto do nervo femoral, os parâmetros de AGA ainda foram significativamente alterados da linha de base no final do período de observação após a reparação do autoenxerto do nervo ciático. Vale ressaltar neste contexto que as contraturas de membros são um fenômeno comum em ratos com lesão do nervo ciático e é necessário cautela para não confundir esses sinais de desequilíbrio muscular e paralisia com a recuperação funcional em andamento32. Isso, por um lado, sublinha a incapacidade do método AGA de detectar recuperação funcional significativa após a lesão neurotmese neste modelo. Por outro lado, levanta a questão se é viável avaliar o modelo de lesão do nervo ciático do rato, que ainda é o modelo de reparação nervosa experimental mais utilizado, por meio da análise da marcha em geral, caso a lesão nervosa seja mais grave do que a axonotmesis48. Detalhes de solução de problemas são fornecidos no Arquivo Complementar 1.
Também fornecemos dados exemplares sobre o uso do método para avaliar a função locomotor em ratos com Lesão medular, o que é possível sem quaisquer alterações necessárias do procedimento de configuração ou aquisição de hardware. O mesmo princípio se aplica a outros modelos de roedores de lesão nervosa central (CNI)26,49,50 e lesão por avulsão raiz. Em contraste com as PNIs isoladas, as lesões da medula espinhal são muito mais complexas em suas consequências fisiodicosiológicas, pois uma infinidade de estruturas altamente importantes são danificadas, envolvendo vias efervescentes como os tratos corticospinal e rubrospinal e caminhos diferentes, como as colunas dorsais e os tratos fusotalâmicos35. O desafio de avaliar adequadamente essas mudanças patológicas se reflete no armamento abrangente de testes comportamentais, como a pontuação Basso, Beattie e Bresnahan (BBB)36. A base de apoio do parâmetro de marcha foi relatada para aumentar após lesões nervosas centrais, provavelmente para explicar uma marcha instável resultante. A Base de Suporte foi significativamente alterada da linha de base de WPO10 para WPO14 em nosso modelo, apoiando nossa presunção de que este parâmetro permite a avaliação do curso de recuperação funcional pela AGA após lesão de contusão na medula espinhal torácica.
Estamos convencidos de que a AGA é uma ferramenta viável para avaliar a recuperação funcional em roedores com lesões do sistema nervoso. No entanto, aconselhamos refletir as mudanças observadas da marcha cuidadosamente e minuciosamente em cada configuração experimental respectiva. Alterações nos parâmetros de marcha, por exemplo, um aumento na Área de Impressão após um decréscimo pós-operatório imediato ou uma diminuição no Tempo de Oscilação procedendo uma elevação pós-operatória imediata deste parâmetro, ao longo do período de observação não se relacionam inevitavelmente com a recuperação funcional. Em vez disso, essas mudanças também podem estar relacionadas a uma possível adaptação funcional para manter uma marcha discreta, uma vez que os ratos são uma espécie de presa e tentam evitar mostrar dor ou incapacidade para potenciais predadores51. Recomenda-se, portanto, a utilização da análise de marcha automatizada como ferramenta complementar para relacionar alterações da marcha a outras medidas de desfecho de lesão nervosa periférica e regeneração21. Como mencionado anteriormente, também acreditamos que deve ser cuidadosamente refletido se roedores com neurotmese do nervo ciático devem ser investigados por meio da AGA, pois nosso achado indica fortemente que a recuperação funcional é severamente limitada neste caso.
Como mostrado em nosso trabalho, o principal ativo da AGA é a possibilidade de estudar a reinervação motora e sensorial em uma infinidade de modelos PNI experimentais, bem como a CNI, exigindo apenas uma configuração. Portanto, o método é, em nossa opinião, uma ferramenta altamente valiosa para testes neuroviolíno abrangentes. Um dos ativos da AGA, que é a possibilidade de estudar a reinnervação motora e sensorial em vários modelos animais de PNI e CNI, exigindo apenas uma configuração, é, em nossa opinião, a principal vantagem do método em comparação com outros métodos de avaliação para estudar a recuperação funcional, como a análise de pista de caminhada52, von Frey testando53, ou cinemática marcha16. O potencial de avaliar simultaneamente mudanças de marcha que se correlacionam com resultados de investigações eletrofisiológicas do músculo reinnervado22 ou métodos de avaliação para função sensorial54 é promissor em relação às aplicações futuras do método. Por isso, recomendamos o uso da AGA para investigar a recuperação funcional em modelos de roedores de PNI de membro dianteiro, como o nervo ulnar, radial ou mediano, ou modelos experimentais de transferência de nervo55,que ainda não foram estudados com este método.
Fornecemos um protocolo detalhado sobre como usar a análise automatizada da marcha para estudar a recuperação funcional em três modelos de roedores de lesão nervosa. Embora o método exija uma cuidadosa consideração de vários aspectos-chave, como treinamento adequado e calibração meticulosa de software e força, é uma ferramenta complementar viável e valiosa para avaliar a regeneração nervosa em modelos de roedores de lesão nervosa central e periférica.
Divulgações
Os autores declaram que este trabalho foi apoiado pela Noldus Inc. pela cobertura da taxa de publicação de acesso aberto. Nenhum dos autores recebeu nenhum salário pessoal ou qualquer tipo de gratificação financeira. Os autores não têm outros interesses concorrentes para declarar.
Agradecimentos
Os autores gostariam de agradecer a Karin Brenner por sua cuidado apaixonada com os animais. Os autores também gostariam de agradecer Claudia Keibl, James Ferguson, Gabriele Leinfellner e Susanne Drechsler por sua ajuda durante as cirurgias experimentais.
Materiais
| Name | Company | Catalog Number | Comments |
| 0.9% Saline | B. Braun Austria | 3570410 | Vehicle for drug delivery |
| 1 ml syringe | B. Braun Austria | 9161708V | Injecting device |
| 10 ml syringe | B. Braun Austria | 4606728 V | Injecting device |
| 1-Propanol, 2-Propanol, Hexetidin | Gebro Pharma | N/A | Alcoholic skin disinfection |
| 23-gauge (G) canula | B. Braun Austria | 4657667 | Canula for s.c. injection |
| 26-gauge (G) canula | B. Braun Austria | 4657683 | Canula for s.c. injection |
| 5 ml syringe | B. Braun Austria | 4606710 V | Injecting device |
| Buprenorphine hydrochloride | Sigma | B9275 | Analgetic agent |
| Burrs for Micro Drill | F.S.T | 19007-29 | Drilling of a hole inside the lamina |
| Caprofen | Zoetis Austria | N/A | Analgetic agent |
| Catwalk Automated gait analysis system | Noldus | N/A | Automatic analysis software of animal gait |
| Cauterizer Kit | F.S.T | 18010-00 | Cauterization of vessels during surgery |
| Enrofloxacin | Bayer Austria | N/A | Antibiotic |
| Ethilon (10-0) | ETHICON | 2810G | Suture material for neurrorhaphy |
| Ethilon (11-0) | ETHICON | EH7465G | Suture material for neurrorhaphy |
| Eye ointment | Fresenius Kabi Austria | 4302436 | Eye protection during anesthesia |
| Friedman-Pearson Rongeurs | F.S.T | 16221-14 | Surgical instrument |
| Gabapentin | Wedgewood Pharmacy | N/A | Analgetic agent |
| Goldstein retractor | F.S.T | 17003-03 | Retraction of tissues during surgery |
| Hair trimmer | Aescular | N/A | Hair trimmer for shaving of the operation site prior to surgery |
| Heating Pad for rodents | ALA Scientific Instruments | N/A | Regulation of body temperature |
| Impactor | Precision Systems and Instrumentation | N/A | Induction of spinal cord contusion |
Lewis rat ( ) ) | Janvier | N/A | Experimental animal |
| Magnetic Fixator Retraction System | F.S.T | 18200-50 | Retraction of tissues during surgery |
| Metzenbaum Baby Scissors | F.S.T | 14019-13 | Surgical instrument |
| Micro Drill | Word Precision Instruments | 503599 | Instrument for bone drilling |
| Micro Needle holder | F.S.T | 12076-12 | Surgical instrument |
| Micro-scissors (curved) | F.S.T | 15023-10 | Surgical instrument |
| Micro-scissors (straight) | F.S.T | 15007-08 | Surgical instrument |
| Mirror Finish Forceps | F.S.T | 11251-23 | Surgical instrument |
| Needle holder | F.S.T | 12002-12 | Surgical instrument |
| Operating microscope | Leica | M651 MSD | Magnification of the operative site |
| Povidone Iod | B. Braun Melsungen | N/A | Non-alcoholic skin disinfectant |
| Pulse Oximeter | STARR Life Sciences | N/A | Surveillance of heart rate and oxygen saturation |
| Rodent thermometer | BIOSEB | BIO-TK8851 | Surveillance of body temperature |
| Scalpel blade | F.S.T | 10010-00 (#10) | Surgical instrument to make an incision |
| Scalpel handle | F.S.T | 10003-12 (#3) | Surgical instrument to make an incision |
| Sevoflurane Inhalation Vapour, Liquid (100%) | Baxter | HDG9117A | Anesthetic |
| Spatula & Probe | F.S.T | 10090-13 | Surgical instrument |
Sprague Dawley rat ( ) ) | Janvier | N/A | Experimental animal |
| Sterila gauze 5x5cm | EVAC MEDICAL | E010.03.00215 | Sterile gauze compress |
| Tissue Forceps | F.S.T | 11021-12 | Surgical instrument |
| Vicryl (4-0) | ETHICON | V3040H | Suture material for subcutaneous sutures |
| Vicryl (5-0) | ETHICON | V303H | Suture material for subcutaneous sutures |
| Vicryl cutting needle (4-0) | ETHICON | V392ZH | Suture material for skin sutures |
| Vicryl cutting needle (5-0) | ETHICON | V391H | Suture material for skin sutures |
Referências
- Mohanty, C. B., Bhat, D. I., Devi, B. I. Use of animal models in peripheral nerve surgery and research. Neurology India. 9, 100-105 (2019).
- Vela, F. J., et al. Animal models used to study direct peripheral nerve repair: a systematic review. Neural Regeneration Research. 15 (3), 491-502 (2020).
- Verma, R., Virdi, J. K., Singh, N., Jaggi, A. S. Animals models of spinal cord contusion injury. The Korean Journal of Pain. 32 (1), 12-21 (2019).
- de Medinaceli, L., Freed, W. J., Wyatt, R. J. An index of the functional condition of rat sciatic nerve based on measurements made from walking tracks. Experimental Neurology. 77 (3), 634-643 (1982).
- Navarro, X. Functional evaluation of peripheral nerve regeneration and target reinnervation in animal models: a critical overview. The European Journal of Neuroscience. 43 (3), 271-286 (2016).
- Sperry, R. W. The functional results of muscle transposition in the hind limb of the rat. The Journal of Comparative Neurology. 73 (3), 379-404 (1940).
- Sperry, R. W. The effect of crossing nerves to antagonistic muscles in the hind limb of the rat. The Journal of Comparative Neurology. 75 (1), 1-19 (1941).
- Sperry, R. W. Transplantation of motor nerves and muscles in the forelimb of the rat. The Journal of Comparative Neurology. 76 (2), 283-321 (1942).
- Zimmerman, E. A., Chambers, W. W., Liu, C. N. An experimental study of the anatomical organization of the Cortico-Bulbar System in the Albino Rat. The Journal of Comparative Neurology. 123, 301-323 (1964).
- Cohen, A. H., Gans, C. Muscle activity in rat locomotion: movement analysis and electromyography of the flexors and extensors of the elbow. Journal of Morphology. 146 (2), 177-196 (1975).
- Barnett, S. A. . The Rat: A Study in Behaviour. , (1963).
- Hare, G. M., et al. Walking track analysis: utilization of individual footprint parameters. Annals of Plastic Surgery. 30 (2), 147-153 (1993).
- Hare, G. M., et al. Walking track analysis: a long-term assessment of peripheral nerve recovery. Plastic and Reconstructive Surgery. 89 (2), 251-258 (1992).
- Bertelli, J. A., Mira, J. C. Behavioral evaluating methods in the objective clinical assessment of motor function after experimental brachial plexus reconstruction in the rat. Journa of Neuroscience Methods. 46 (3), 203-208 (1993).
- Varejao, A. S., Melo-Pinto, P., Meek, M. F., Filipe, V. M., Bulas-Cruz, J. Methods for the experimental functional assessment of rat sciatic nerve regeneration. Neurological Research. 26 (2), 186-194 (2004).
- Varejao, A. S., et al. Functional assessment of peripheral nerve recovery in the rat: gait kinematics. Microsurgery. 21 (8), 383-388 (2001).
- Varejao, A. S., et al. Ankle kinematics to evaluate functional recovery in crushed rat sciatic nerve. Muscle and Nerve. 27 (6), 706-714 (2003).
- Nath, T., et al. Using DeepLabCut for 3D markerless pose estimation across species and behaviors. Nature Protocols. 14 (7), 2152-2176 (2019).
- Mathis, A., et al. DeepLabCut: markerless pose estimation of user-defined body parts with deep learning. Nature Neuroscience. 21 (9), 1281-1289 (2018).
- Deumens, R., Jaken, R. J., Marcus, M. A., Joosten, E. A. The CatWalk gait analysis in assessment of both dynamic and static gait changes after adult rat sciatic nerve resection. Journal of Neuroscience Methods. 164 (1), 120-130 (2007).
- Heinzel, J., et al. Use of the CatWalk gait analysis system to assess functional recovery in rodent models of peripheral nerve injury - a systematic review. Journal of Neuroscience Methods. 345, 108889 (2020).
- Heinzel, J. C., Hercher, D., Redl, H. The course of recovery of locomotor function over a 10-week observation period in a rat model of femoral nerve resection and autograft repair. Brain and Behavior. , 01580 (2020).
- Chen, S. H., et al. Changes in GABA and GABA(B) receptor expressions are involved in neuropathy in the rat cuneate nucleus following median nerve transection. Synapse. 66 (6), 561-572 (2012).
- Chen, S. H., et al. Decreases of glycine receptor expression induced by median nerve injury in the rat cuneate nucleus contribute to NPY release and c-Fos expression. Life Sciences. 90 (7-8), 278-288 (2012).
- Hetze, S., Romer, C., Teufelhart, C., Meisel, A., Engel, O. Gait analysis as a method for assessing neurological outcome in a mouse model of stroke. Journal of Neuroscience Methods. 206 (1), 7-14 (2012).
- Sandner, B., et al. Systemic epothilone D improves hindlimb function after spinal cord contusion injury in rats. Experimental Neurology. 306, 250-259 (2018).
- Kappos, E. A., et al. Validity and reliability of the CatWalk system as a static and dynamic gait analysis tool for the assessment of functional nerve recovery in small animal models. Brain and Behavior. 7 (7), 00723 (2017).
- Deumens, R., Marinangeli, C., Bozkurt, A., Brook, G. A. Assessing motor outcome and functional recovery following nerve injury. Methods in Molecular Biology. 1162, 179-188 (2014).
- Webster, G. V. Halstedian principles in the practice of plastic and reconstructive surgery. Stanford Medical Bulletin. 13 (3), 315-316 (1955).
- Bozkurt, A., et al. A flexible, sterile, and cost-effective retractor system for microsurgery. Microsurgery. 31 (8), 668-670 (2011).
- Carr, M. M., Best, T. J., Mackinnon, S. E., Evans, P. J. Strain differences in autotomy in rats undergoing sciatic nerve transection or repair. Annals of Plastic Surgery. 28 (6), 538-544 (1992).
- Dellon, A. L., Mackinnon, S. E. Sciatic nerve regeneration in the rat. Validity of walking track assessment in the presence of chronic contractures. Microsurgery. 10 (3), 220-225 (1989).
- Jackson, C. M. Anatomy of the rat. Transactions of the American Philosophical Society, Philadelphia, New Series, Volume XXVII, 1935. The Anatomical Record. 65 (1), 127-129 (1936).
- Pena, M. C., Baron, J. Femoral nerve and rectus femoris muscle of the rat: a study in anatomy, histology, and histoenzymes. Annals of Plastic Surgery. 20 (6), 527-532 (1988).
- Kjell, J., Olson, L. Rat models of spinal cord injury: from pathology to potential therapies. Disease Models and Mechanisms. 9 (10), 1125-1137 (2016).
- Basso, D. M., Beattie, M. S., Bresnahan, J. C. A sensitive and reliable locomotor rating scale for open field testing in rats. Journal of Neurotrauma. 12 (1), 1-21 (1995).
- Bozkurt, A., et al. CatWalk gait analysis in assessment of functional recovery after sciatic nerve injury. Journal of Neuroscience Methods. 173 (1), 91-98 (2008).
- Godinho, M. J., et al. Immunohistochemical, ultrastructural and functional analysis of axonal regeneration through peripheral nerve grafts containing Schwann cells expressing BDNF, CNTF or NT3. PLoS One. 8 (8), 69987 (2013).
- Pajenda, G., et al. Spatiotemporally limited BDNF and GDNF overexpression rescues motoneurons destined to die and induces elongative axon growth. Experimental Neurology. 261, 367-376 (2014).
- Matsuura, Y., et al. The effect of anti-NGF receptor (p75 Neurotrophin Receptor) antibodies on nociceptive behavior and activation of spinal microglia in the rat brachial plexus avulsion model. Spine (Phila Pa 1976). 38 (6), 332-338 (2013).
- Hamers, F. P., Lankhorst, A. J., van Laar, T. J., Veldhuis, W. B., Gispen, W. H. Automated quantitative gait analysis during overground locomotion in the rat: its application to spinal cord contusion and transection injuries. Journal of Neurotrauma. 18 (2), 187-201 (2001).
- Koopmans, G. C., et al. The assessment of locomotor function in spinal cord injured rats: the importance of objective analysis of coordination. Journal of Neurotrauma. 22 (2), 214-225 (2005).
- Frohlich, H., Claes, K., De Wolf, C., Van Damme, X., Michel, A. A machine learning approach to automated gait analysis for the Noldus Catwalk system. IEEE Transaction on Bio-medical Engineering. 65 (5), 1133-1139 (2018).
- Batka, R. J., et al. The need for speed in rodent locomotion analyses. Anatomical Record (Hoboken, N. J). 297 (10), 1839-1864 (2014).
- Wood, T., et al. A ferret model of encephalopathy of prematurity. Developmental Neuroscience. 40 (5-6), 475-489 (2018).
- Abbas, W., Masip Rodo, D. Computer methods for automatic locomotion and gesture tracking in mice and small animals for neuroscience applications: a survey. Sensors. 19 (15), (2019).
- Irintchev, A. Potentials and limitations of peripheral nerve injury models in rodents with particular reference to the femoral nerve. Annals of Anatomy. 193 (4), 276-285 (2011).
- Haastert-Talini, K., Haastert-Talini, K., Assmus, H., Antoniadis, G. . Modern Concepts of Peripheral Nerve Repair. , 127-138 (2017).
- Lu, L., et al. Growth differentiation factor 11 promotes neurovascular recovery after stroke in mice. Frontiers in Cellular Neuroscience. 12, (2018).
- Caballero-Garrido, E., Pena-Philippides, J. C., Galochkina, Z., Erhardt, E., Roitbak, T. Characterization of long-term gait deficits in mouse dMCAO, using the CatWalk system. Behavioral Brain Research. 331, 282-296 (2017).
- Graham, D. M., Hampshire, V. Methods for measuring pain in laboratory animals. Lab Animal. 45 (3), 99-101 (2016).
- Monte-Raso, V. V., Barbieri, C. H., Mazzer, N., Yamasita, A. C., Barbieri, G. Is the sciatic functional index always reliable and reproducible. Journal of Neuroscience Methods. 170 (2), 255-261 (2008).
- Stossel, M., et al. Comparative evaluation of chitosan nerve guides with regular or increased bendability for acute and delayed peripheral nerve repair: a comprehensive comparison with autologous nerve grafts and muscle-in-vein grafts. Anatomical Record (Hoboken). 301 (10), 1697-1713 (2018).
- Vrinten, D. H., Hamers, F. F. CatWalk' automated quantitative gait analysis as a novel method to assess mechanical allodynia in the rat; a comparison with von Frey testing. Pain. 102 (1-2), 203-209 (2003).
- Aman, M., Sporer, M., Bergmeister, K., Aszmann, O. Animal models for selective nerve transfers of the upper extremity. Handchirurgie Mikrochirurgie Plastische Chirurgie. 51 (4), 319-326 (2019).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados