Method Article
Extração de Microtúbulos Modificados de Células de Mamíferos para Estudo de Complexos Microtúbulo-Proteína por Microscopia Crio-Eletrônica
Neste Artigo
Resumo
Aqui, descrevemos um protocolo para extrair tubulina endógena de células de mamíferos, que podem não possuir ou conter enzimas modificadoras de microtúbulos específicas, para obter microtúbulos enriquecidos para uma modificação específica. Em seguida, descrevemos como os microtúbulos extraídos podem ser decorados com proteínas purificadas de ligação a microtúbulos para preparar grades para microscopia crio-eletrônica.
Resumo
Os microtúbulos são uma parte importante do citoesqueleto e estão envolvidos na organização intracelular, divisão celular e migração. Dependendo das modificações pós-traducionais, os microtúbulos podem formar complexos com várias proteínas interagentes. Estes complexos microtúbulo-proteína estão frequentemente implicados em doenças humanas. O entendimento da estrutura de tais complexos é útil para elucidar seus mecanismos de ação e pode ser estudado por criomicroscopia eletrônica (crio-EM). Para a obtenção de tais complexos para estudos estruturais, é importante extrair microtúbulos contendo ou não modificações pós-traducionais específicas. Neste trabalho, descrevemos um protocolo simplificado para extração de tubulina endógena de células de mamíferos geneticamente modificadas, envolvendo polimerização de microtúbulos, seguida de sedimentação por ultracentrifugação. A tubulina extraída pode então ser usada para preparar grades de microscópios crio-eletrônicos com microtúbulos que estão ligados a uma proteína purificada de ligação a microtúbulos de interesse. Como exemplo, demonstramos a extração de microtúbulos totalmente tirosinados, de linhagens celulares projetadas para não possuir as três enzimas destirosinantes de tubulina conhecidas. Esses microtúbulos são então usados para fazer um complexo proteico com tubulina detirosinase associada a microtúbulos enzimaticamente inativos em grades crio-EM.
Introdução
Os microtúbulos são uma parte crucial do citoesqueleto; Eles estão envolvidos em diferentes funções, como migração e divisão celular, mas também contribuem para a organização intracelular. Para se adaptar a diferentes destinos funcionais, os microtúbulos interagem com uma variedade de proteínas associadas a microtúbulos (MAPs), enzimas e outras proteínas, que coletivamente chamaremos de "proteínas que interagem com microtúbulos". A ligação dos microtúbulos dessas proteínas pode ser guiada por diferentes modificações da tubulina, comumente referida como o "código da tubulina"1. Exemplos dessa preferência são a cinesina associada a centrômeros mitóticos (MCAK)2 e o domínio CAP-Gly dineína-dinactina de p1503, que se associam preferencialmente à tubulina tirosinada, enquanto os motores cinesina proteína E associada ao centrômero (CENP-E)4 e cinesina-25 preferem a tubulina que não possui a tirosina C-terminal.
Enquanto uma variedade de métodos pode ser empregada para estudar interações microtúbulo-proteína, a microscopia crioeletrônica (crio-EM) é frequentemente usada para estudar essas interações em resolução quase atômica 6,7. Nos últimos anos, estruturas crio-EM têm revelado grandes proteínas motoras como a dineína 8,9,10 e cinesina11, proteínas +TIP como EB312,13 e MCAK 14, outras proteínas como Tau 15,16 e até moléculas pequenas como paclitaxel, peloruside e zampanolide 17 interagem com microtúbulos. Para estudar as interações microtúbulo-proteína, os microtúbulos são tipicamente extraídos do cérebro suíno18. Em seguida, a maioria dos estudos in vitro, incluindo estruturas de microtúbulos crio-EM, é realizada usando tubulina cerebral suína. Os resultados desses estudos, portanto, obscurecem a importância da natureza heterogênea das modificações da tubulina19 entre tecidos e tipos celulares. Isso cria um problema particular ao investigar uma proteína que requer ou prefere uma modificação específica para se ligar aos microtúbulos. Isso pode ser ilustrado com tubulina tirosinada, o substrato para a microtúbulo detirosinase MATCAP.
A destirosinação é uma modificação da tubulina na qual o aminoácido C-terminal tirosina da α-tubulina está ausente, o qual está associado à função mitótica, cardíaca e neuronal20. Embora os microtúbulos totalmente tirosinizados sejam o substrato ideal para a MATCAP, esta está amplamente ausente nos microtúbulos comercialmente disponíveis do cérebro suíno devido à função das vasohibinas 21,22 e MATCAP 23 destirosinases nesse tecido 22,23,24,25,26. Embora a HeLa tubulina comercialmente disponível contenha principalmente microtúbulos tirosinados, a destirosinação pode ocorrer, e esta fonte de tubulina é, portanto, menos adequada para criar uma amostra uniforme para análise crio-EM.
Para estimular a ligação do MATCAP aos microtúbulos e criar uma amostra homogênea para análise estrutural, buscamos uma fonte de microtúbulos totalmente tirosinada. Para isso, foi criada uma linhagem celular deficiente em MATCAP e vasohibina, que foi usada para extrair microtúbulos totalmente tirosinados. O procedimento de extração foi baseado em protocolos bem estabelecidos que utilizam ciclos repetidos de polimerização e despolimerização dos microtúbulos para extrair tubulina do tecido cerebral ou das células 18,27,28,29,30, com apenas uma etapa de polimerização e centrifugação sobre um coxim de glicerol. Usando MATCAP como exemplo, demonstramos como esses microtúbulos podem ser usados para estudos de crio-EM. Para a preparação de grades crio-EM, um protocolo de aplicação em duas etapas com baixa concentração de sal é descrito. Os métodos neste artigo descrevem a extração de microtúbulos personalizáveis em quantidades e pureza suficientes para realizar análises crio-EM e fornecem um protocolo detalhado sobre como usar esses microtúbulos para criar complexos proteína-microtúbulos em grades crio-EM.
Protocolo
NOTA: Consulte a Tabela de Materiais para obter detalhes relacionados a todos os materiais e equipamentos utilizados neste protocolo.
1. Cultura celular
NOTA: Toda a cultura celular deve ser feita em uma capela de fluxo laminar estéril.
- Para seguir esse protocolo, primeiro descongele um frasco de células congeladas em banho-maria a 37 °C. Aqui, usamos uma linhagem celular HCT116 geneticamente modificada que não possui as três enzimas destirosinantes conhecidas, VASH1, VASH2 e MATCAP, para criar tubulina tirosinada.
- Preparar uma placa de Ø 10 cm contendo 10 mL do meio de cultura celular apropriado.
NOTA: Neste protocolo, DMEM (meio Dulbecco's modified Eagle) suplementado com 10% v/v FCS (soro fetal de bezerros) e antibiótico penicilina/estreptomicina (meio de cultura) foi utilizado para a linhagem celular HCT116 geneticamente modificada. - Conte as células e semeie ~2,5 × 106 células viáveis (~20% de confluência) na placa preparada de 10 cm. Agite a placa suavemente para distribuir uniformemente as células. Incubar a placa em uma estufa de cultura celular a 37 °C gaseificado com 5% (v/v) de CO2 até que as células atinjam 80%-90% de confluência.
NOTA: Normalmente, isso leva 3 dias para células HCT116, mas o tempo pode depender da densidade de semeadura específica e da linha celular usada. - Descarte o meio de cultura celular com pipeta ou aspirador a vácuo e lave a placa 2 x 5 mL de PBS.
NOTA: Tome cuidado para não dispensar o PBS com muita força na monocamada celular, pois isso poderia separar as células da placa. - Adicionar 1-2 mL de tripsina e incubar as células na incubadora por 2-5 min para desanexar as células.
- Adicionar 2 mL do meio de cultura à placa para extinguir a tripsina.
- Dividir a suspensão celular em três a cinco partes iguais e resemeá-las para expandir as células em meio de cultura até obter 6-12 placas confluentes de 15 cm.
2. Colheita
- Lave suavemente as células com 10 mL de PBS (1x) para remover qualquer meio de cultura celular.
- Separar as células das placas incubando-as por 5 min à temperatura ambiente com 3 mL de PBS gelado suplementado com EDTA 5 mM (estéril/filtrado) e, posteriormente, usando um raspador celular.
- Coletar as células em um tubo de 50 mL sobre gelo e girar para baixo (10 min, 250 × g).
- Observar o volume das células colhidas com a escala volumétrica no tubo de 50 mL.
NOTA: O volume esperado pode estar entre ~0,5 mL e 4 mL. PASSO DE PAUSA: Congele o pellet de célula em LN2 e armazene a -20 °C até o uso. Observe que o pellet de célula pode ser armazenado apenas por algumas semanas ou meses. Se o pellet for mantido por mais tempo, isso pode resultar em um rendimento diminuído ou nenhum microtúbulo.
- Observar o volume das células colhidas com a escala volumétrica no tubo de 50 mL.
3. Extração de microtúbulos
NOTA: Mantenha tudo para as etapas 3.1-3.5 no gelo; tudo a partir do passo 3.6 deve ser mantido aquecido (30-37 °C).
- Preparar 10 mL de tampão de lise gelada contendo 100 mM PIPES/KOH (pH 6,9), 2 mM EGTA/KOH, 1 mM MgCl2, 1 mM PMSF e um comprimido inibidor de protease (mini).
- Ressuspenda a pastilha de células colhidas em tampão de lise 1:1 v/v (em caso de dúvida sobre o volume exato, tome menos tampão de lise em vez de mais).
- Lise as células por sonicação: 15 s on, 45 s off, amp 30, quatro ciclos (determinar as condições experimentalmente, e mudar de acordo com o sonicator).
- Após a sonicação, coletar uma amostra para análise de SDS-PAGE: 2 μL de lisado + 18 μL de água + 5 μL de tampão de amostra 5x SDS.
NOTA: Verifique sob um microscópio de luz padrão se as células realmente lisaram completamente.
- Após a sonicação, coletar uma amostra para análise de SDS-PAGE: 2 μL de lisado + 18 μL de água + 5 μL de tampão de amostra 5x SDS.
- Pipetar as células lisadas para um tubo centrífugo. Gire por 1 h a 100.000 × g a 4 °C em um rotor ultracentrífugo para limpar o lisado.
NOTA: Certifique-se de que todos os bolsos do rotor estejam secos e limpos para garantir o balanceamento correto da centrífuga. - Use uma seringa para retirar o lisado limpo. Tome cuidado para não atrapalhar o pellet, bem como a camada flutuante na parte superior.
- Recolher uma amostra do lisado limpo: 2 μL de lisado + 18 μL de água + 5 μL de tampão de amostra 5x SDS.
- Enxágue cuidadosamente o pellet e retire um pouco do pellet girando uma ponta de pipeta P10 através do pellet; adicionar 200 μL de água e 50 μL de tampão SDS.
- Complementar o sobrenadante da etapa anterior com 1 mM de GTP e 20 μM de paclitaxel para polimerizar os microtúbulos; para um volume de 1 mL, adicionar 10 μL de 2 mM de paclitaxel e 10 μL de 100 mM de GTP.
CUIDADO: Paclitaxel pode causar irritação da pele, danos oculares graves, irritação respiratória, defeitos genéticos, danos ao feto e danos aos órgãos. A exposição prolongada ou repetida causa danos aos órgãos. Não respire, borrife ou polvilhe a substância de forma alguma. Use luvas de borracha nitrílica para evitar o contato com a pele. - Incubar o sobrenadante suplementado com GTP/paclitaxel durante 30 min a 37 °C para permitir a montagem dos microtúbulos.
- Durante esta etapa de incubação, deixe o rotor e a ultracentrífuga aquecerem até 30 °C.
- Prepare o tampão da almofada: Adicionar 0,6 mL de glicerol a 0,4 mL de tampão de lise e complementar a mistura com 20 μM de paclitaxel. Pré-aqueça o tampão da almofada a 37 °C.
- Adicionar 800 μL de tampão de almofada a um tubo de ultracentrífuga. Pipetar cuidadosamente o lisado suplementado com GTP/paclitaxel por cima do tampão da almofada.
NOTA: Evite a mistura do tampão da almofada e do lisado pipetando muito suavemente. - Gire por 30 min a 100.000 × g a 30 °C em um rotor ultracentrífugo. Marque a borda externa do tubo de centrifugação para reconhecer facilmente onde o pellet de microtúbulo deve se formar.
- Retire o tampão da almofada cuidadosamente usando uma pipeta, tomando cuidado para não perturbar o pellet de microtúbulo.
- Recolher uma amostra do tampão da almofada: 2 μL + 18 μL de água + 5 μL de tampão de amostra 5x SDS.
- Lave o pellet cuidadosamente 3x com tampão de lise morno para remover o glicerol. Distribua suavemente o tampão quente ao lado do pellet (não lavando o líquido diretamente sobre o pellet), gire o tubo algumas vezes para remover o máximo de glicerol possível do pellet e das paredes do tubo e, em seguida, aspirar e repetir.
NOTA: Se o glicerol não for lavado corretamente, a grade derreterá muito rapidamente sob a iluminação eletrônica. Isso pode ser evidenciado pelo alto movimento de partículas, criando imagens borradas. - Prepare o tampão de ressuspensão com os seguintes ingredientes: tubos de 100 mM/KOH (pH 6,9), 2 mM EGTA/KOH e 1 mM MgCl2 e aqueça o tampão a 37 °C.
- Ressuspenda o pellet lavado suavemente com uma ponta de corte em ~50 μL de tampão de ressuspensão pré-aquecido e mantenha o tubo a 37 °C.
- Coletar uma amostra da fração de pastilha ressuspensa: 2 μL + 18 μL de água + 5 μL de tampão de amostra 5x SDS.
DICA: A ponta de corte evita a quebra dos microtúbulos. Prepare um bloco de aquecimento metálico a 37 °C e guarde-o numa caixa de poliestireno para que os tubos de amostra possam ser transportados facilmente sem os arrefecer até à temperatura ambiente.
- Coletar uma amostra da fração de pastilha ressuspensa: 2 μL + 18 μL de água + 5 μL de tampão de amostra 5x SDS.
4. Preparação da grade Cryo-EM
- Prepare o dispositivo congelador de imersão instalando o papel mata-borrão. Aqueça o congelador de imersão até 30 °C e ajuste a umidificação a 100%. Deixe ~30 min para equilibrar a temperatura e umidade.
- Prepare as configurações do congelador de imersão para dois aplicativos e execute todo o programa uma vez para ter certeza de que as configurações estão definidas corretamente. Certifique-se de que o primeiro aplicativo tenha uma força de 10, 2 s de tempo de blot e 0 s de tempo de espera e que o segundo aplicativo tenha uma força de 10, 6,5 s de tempo de blot e 10 s de tempo de espera.
- Descarga de brilho das grades crio-EM a 30 mA por 60 s.
- Resfrie o conjunto do recipiente de poliestireno com LN2 e prepare o etano líquido em um copo de metal condensando o gás etano em um copo de metal frio.
- Preparar um tampão de diluição com os seguintes componentes: tubos de 100 mM/KOH (pH 6,9), 2 mM EGTA/KOH e 1 mM MgCl2 e aquecê-lo a 37 °C.
- Diluir a proteína de interação com microtúbulos 1:1 v/v com tampão de diluição imediatamente antes de aplicá-la nas grades para garantir que a concentração de sal seja reduzida (usamos uma concentração final de sal de 50 mM de NaCl). Manter a mistura a 37 °C.
- Pegue uma grade descarregada com pinça de mergulho e clique-as no congelador de imersão.
- Posicione o recipiente de poliestireno com etano líquido no congelador de imersão e percorra o programa preparado: primeiro aplique 3,5 μL de solução de microtúbulos na grade, deixe o congelador de imersão manchar a grade, em seguida, aplique imediatamente 3,5 μL de proteína recém-diluída e, por último, deixe o êmbolo manchar e mergulhe congelando a grade em etano líquido.
- Transfira as grades para uma caixa de armazenamento de grade e armazene-as em um dewar LN2 até a geração de imagens.
Resultados
Investigamos a tubulina destirosinase MATCAP ligada a microtúbulos tirosinados, por crio-EM. Para isso, extraímos microtúbulos totalmente tirosinados, de uma linhagem celular HCT116 geneticamente modificada, sem as três enzimas destirosinantes conhecidas, VASH1/2 e MATCAP. Foram utilizadas 6-12 placas confluentes de 15 cm para extrair os microtúbulos de aproximadamente 0,5-4 mL de pellet celular (Figura 1). Após a segunda etapa de centrifugação (etapa 3.11), obtém-se um pellet visível, porém pequeno e transparente (Figura 1I). O rendimento dos microtúbulos é tipicamente de ~75 μg. Se o pellet não estiver visível, isso pode indicar um problema em uma das etapas anteriores, como uma temperatura incorreta de polimerização de microtúbulos, problemas com a qualidade do GTP ou paclitaxel usados, ou a adição de muito tampão de lise, resultando em uma concentração de tubulina muito baixa para polimerização. Para avaliar a qualidade e concentração dos microtúbulos extraídos, analisamos amostras em gel de SDS corado com Coomassie (Figura 2A). Essas análises indicaram que os microtúbulos extraídos eram relativamente puros. A concentração de microtúbulos interpolados derivada da quantificação de BSA foi de ~1,4 mg/mL. Isso concorda bem com o número medido com espectrofotômetro (Figura 2B,C).
Os microtúbulos recém-extraídos podem ser usados diretamente para fazer amostras para crio-EM. Os microtúbulos devem parecer intactos e abundantes nas micrografias. Para uma análise mais aprofundada do crio-EM, é fundamental ter uma baixa densidade de microtúbulos por micrografia para evitar que os microtúbulos se cruzem entre si (Figura 3A). Microtúbulos quebrados ou que não são visíveis podem indicar que os microtúbulos despolimerizados (por exemplo, devido a uma baixa temperatura ou hidrólise de GTP) ou que os parâmetros de blotting e plunge freezing não foram ajustados corretamente. O fundo ao redor dos microtúbulos é denso, presumivelmente com tubulina não polimerizada.
O peso molecular do MATCAP é de 53 kDa, e ele tem um domínio catalítico globular logo abaixo do tamanho de um monômero de tubulina. A decoração do MATCAP no microtúbulo poderia, portanto, ser detectada visualmente. Os microtúbulos que não se ligaram ao MATCAP apresentaram bordas "lisas", enquanto os microtúbulos que se ligaram ao MATCAP apresentaram bordas "rugosas", caracterizadas por pontos elétron-densos na superfície dos microtúbulos (Figura 3B). Microtúbulos ligados a MATCAP e não ligados a MATCAP também puderam ser distinguidos nas classes 2D calculadas, embora devido à forma e tamanho, isso possa diferir para outras proteínas que interagem com microtúbulos (Figura 3C). Para confirmar que a densidade realmente pertence à proteína de interesse, pode-se tirar proveito de estruturas experimentalmente determinadas ou previstas. Também sugerimos fazer uma grade de controle que contenha microtúbulos apenas para comparação. Isso indica se os microtúbulos foram polimerizados e extraídos intactos em uma concentração suficientemente alta e se o processo de congelamento por imersão foi executado corretamente. Observou-se que a abundância de microtúbulos diminuiu nas grades com a segunda aplicação de MATCAP.
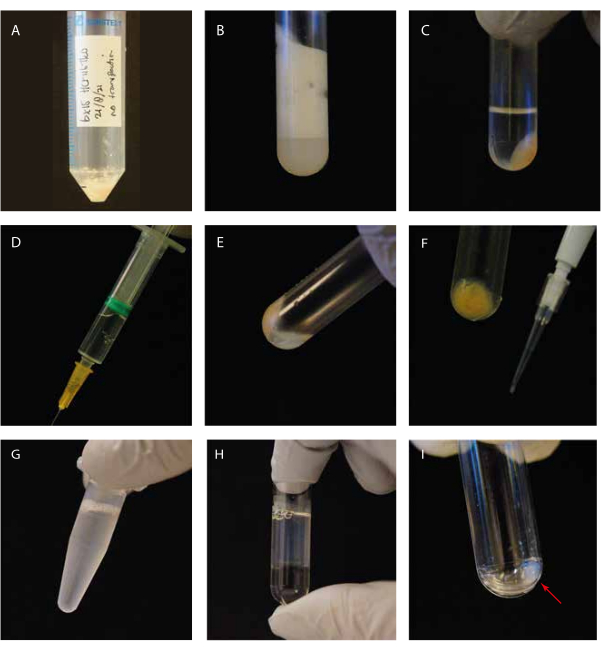
Figura 1: Orientação visual das etapas experimentais. (A) Pelotização celular antes da lise; (B) células sonicadas em tubo de ultracentrífuga antes da centrifugação; (C) células sonicadas em tubo de ultracentrífuga após centrifugação; (D) seringa com o sobrenadante limpo; (E) pellet residual após remoção do sobrenadante, incluindo uma "camada flutuante branca"; (F) Ponteira P10 com pellet de detritos celulares para o gel de Coomassie SDS; (G) Sobrenadante suplementado com GTP/paclitaxel antes da incubação; (H) sobrenadante incubado com GTP/paclitaxel sobre uma almofada de glicerol em um tubo de ultracentrífuga; (I) pastilha limpa de microtúbulos após a segunda etapa de centrifugação. Clique aqui para ver uma versão maior desta figura.
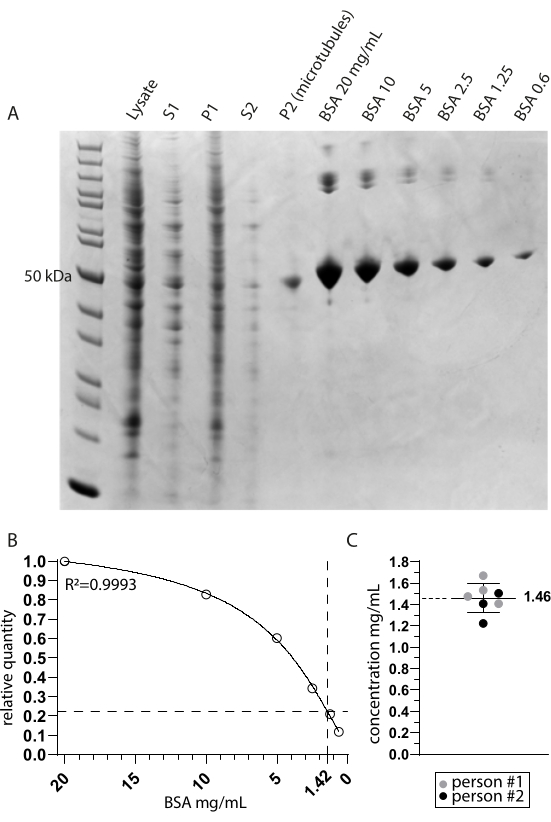
Figura 2: Determinação da pureza e concentração dos microtúbulos . (A) Gel de página SDS corado com Coomassie mostrando as amostras colhidas durante o protocolo de extração e uma comparação da concentração de BSA. S1 e P1 correspondem ao sobrenadante e ao pellet após a primeira etapa de centrifugação, respectivamente. S2 e P2 correspondem similarmente à segunda etapa de centrifugação. (B) Uma linha de regressão não linear das quantidades relativas de BSA derivadas de A. A interpolação da banda de microtúbulos em torno de 50 kDa na faixa P2 (microtúbulos) indica uma concentração final de 1,42 mg/mL. (C) A análise espectrofotométrica dos microtúbulos ressuspendidos (P2) medidos por duas pessoas e corrigidos pelo coeficiente de extinção combinado de TUBA1A e TUBB3 (0,971) indica uma concentração média e desvio padrão de 1,46 mg/mL ± 0,14 mg/mL. Clique aqui para ver uma versão maior desta figura.

Figura 3: Exemplo de micrografias. (A) Exemplo de micrografias mostrando microtúbulos ligados ao MATCAP. Os microtúbulos indicados por uma caixa verde estão intactos, decorados, e podem ser usados para a análise crio-EM. O microtúbulo indicado pela caixa laranja é um microtúbulo intacto e decorado, mas está posicionado próximo aos microtúbulos à esquerda dele; portanto, é menos adequado para incluir na análise crio-EM. Os microtúbulos na caixa vermelha estão cruzando e quebrados. Estes devem ser excluídos da análise crio-EM. (B) Uma visão ampliada do microtúbulo verde circundado do painel esquerdo. As pontas de seta vermelhas indicam os pontos pretos que só apareceram nos microtúbulos nas micrografias que tiveram aplicação de MATCAP e, portanto, provavelmente correspondem a MATCAP ligado ao microtúbulo. (C) Exemplo de classes 2D de partículas de microtúbulos escolhidas de A que mostraram alta e baixa decoração e uma classe 2D de um conjunto de dados diferente para o qual não observamos nenhuma decoração por MATCAP (painel mais à direita). Barras de escala = (A) 50 nm, (B) 25 nm, (C) 10 nm. Clique aqui para ver uma versão maior desta figura.

Figura 4: Análise imunoblot de microtúbulos derivados de células HCT116 HCT116 com deficiência de MATCAP e VASH1/2 com nocaute triplo (TKO), cérebro suíno comercial e tubulina HeLa. Abreviações: nocaute técnico = nocaute triplo; mAb = anticorpo monoclonal; pAb = anticorpo policlonal. Clique aqui para ver uma versão maior desta figura.
Discussão
Este método descreve como extrair rapidamente tubulina endógena de linhagens celulares e, posteriormente, decorar esses microtúbulos em grades crio-EM. Os microtúbulos são sensíveis à temperatura. Despolimerizam em ambiente frio e polimerizam em ambiente quente31. Portanto, é fundamental executar o spin de sonicação e depuração (passos 1.1-1.5) a 4 °C para solubilizar a tubulina. Se algum fator estivesse estabilizando tão bem os microtúbulos que eles não se despolimerizassem nessa etapa, esses microtúbulos e os fatores estabilizadores seriam descartados no pellet após o giro inicial da folga. Após a (re)polimerização dos microtúbulos, é importante manter a solução contendo os microtúbulos polimerizados sempre aquecida. Extraímos os microtúbulos das células HCT116, que são deficientes nas proteínas VASH1, VASH2 e MATCAP. Outras linhagens celulares, assim como tecidos, podem ser usados para extrair microtúbulos29, embora os contaminantes, os isótipos de tubulina e o rendimento possam ser muito diferentes do que é descrito aqui. Plasmídeos superexpressando que contêm enzimas modificadoras também podem ser usados para introduzir modificações específicas na tubulina.
Outros protocolos 18,27,28,29,30 utilizam múltiplos ciclos de polimerização e despolimerização dos microtúbulos para obter microtúbulos livres de outras proteínas interagentes. Aqui, simplificamos esses protocolos e polimerizamos os microtúbulos apenas uma vez. É possível que, devido a essa polimerização única, esses microtúbulos possam co-sedimentar com outras proteínas que interagem com microtúbulos. No entanto, descobrimos que este protocolo fornece microtúbulos suficientemente puros para fins de crio-EM. Se uma amostra mais pura for necessária para ensaios específicos, ciclos adicionais de polimerização e despolimerização poderiam produzir uma amostra mais pura, embora isso possa ser às custas do rendimento de microtúbulos. Neste protocolo, utilizou-se paclitaxel para polimerizar os microtúbulos. No entanto, o paclitaxel poderia enviesar a rede de microtúbulos em direção a uma certa torção e elevação, o que poderia interferir com a afinidade dos microtúbulos da proteína de interesse. Outros reagentes estabilizadores de microtúbulos podem ser usados se o paclitaxel não for adequado; exemplos desses reagentes são moléculas não taxânicas, como o pelorusídeo, ou variantes de GTP não hidrolisáveis, como o GMPCPP17,32.
Para investigar estruturalmente proteínas que se ligam a microtúbulos em grades crio-EM, é necessário ligar uma quantidade suficiente da proteína de interesse aos microtúbulos. Um problema comum é que os complexos de proteínas que são estáveis em solução se desfazem na grade. Para formar o complexo proteico na grade, foi crucial primeiro camuflar os microtúbulos e, em seguida, aplicar a proteína de ligação aos microtúbulos com baixa concentração de sal na grade revestida de microtúbulos, montando assim o complexo proteico diretamente na grade. Outros relataram similarmente um protocolo com baixo teor de sal 33,34 e um protocolo de aplicação em duas etapas34,35,36 para decoração bem sucedida de microtúbulos. É provável que uma menor concentração de sal enviese o complexo proteico em direção a uma interação mais estável devido à diminuição das cargas eletrostáticas. No entanto, devido à baixa concentração de sal, a proteína de interesse está em risco de precipitação. Portanto, é altamente recomendável manter a proteína em ou em torno de concentrações de sal fisiologicamente relevantes até pouco antes de vitrificação das grades. Este protocolo de aplicação em duas etapas provavelmente evita que o complexo proteico se desfaça durante as etapas de blotting ou plunge-freezing. Neste protocolo, utilizamos o Vitrobot. No entanto, métodos de vitrificação mais rápidos (VitroJet) ou o uso de grades livres de manchas (Puffalot) ou dispositivos que têm ambas as propriedades (camaleão) poderiam potencialmente superar a aplicação em duas etapas, mas estes não estão atualmente amplamente disponíveis para teste.
A resolução final da densidade crio-EM reconstruída pode ser afetada por uma série de fatores, incluindo o movimento da proteína ligadora de microtúbulos em relação ao microtúbulo e o nível de decoração que pode ser alcançado. Uma maior decoração de microtúbulos é provavelmente benéfica para a resolução final obtida na reconstrução da densidade 3D. Isso pode ser limitado por alguns fatores, como a maior concentração de proteína que é obtida durante a purificação da proteína de ligação de microtúbulos, a menor concentração de sal que a proteína de interação com microtúbulos pode suportar sem se agregar e o modo de ligação da proteína de interação com microtúbulos (por exemplo, a proteína pode abranger mais de um dímero de tubulina, dificultando assim uma relação de ligação de 1:1). Embora a resolução da reconstrução crio-EM possa estar comprometida por microtúbulos esparsamente decorados, a análise computacional pode contornar muitos problemas, como exemplificado por uma estrutura do complexo microtúbulo-proteína recentemente relatada que foi extremamente escassamente decorada8.
O protocolo que descrevemos aqui apresenta um método rápido e de baixo custo para a obtenção de microtúbulos adequados para fins de crio-EM. Em contraste com a tubulina cerebral suína comercialmente disponível, os microtúbulos derivados de células HCT116 deficientes em MATCAP e vasohibina são totalmente tirosinados (Figura 4). A tubulina HeLa comercial, um reagente caro, em princípio, é relativamente uniformemente tirosinada e contém poucas outras modificações4 , como a glutamilação, mas os lotes podem variar, e a modificação só poderia ser alcançada in vitro. Uma vantagem de extrair microtúbulos de linhagens celulares feitas sob medida é a flexibilidade que se tem para superexpressar ou excluir enzimas modificadoras da tubulina, como a tubulina detirosinases, para criar um pool mais homogêneo de microtúbulos. Isso pode beneficiar a decoração e uniformidade da amostra de crio-EM e, em última análise, beneficiará a facilidade e a qualidade dos mapas de densidade crio-EM e estruturas moleculares derivadas desta amostra.
Divulgações
Os autores não têm conflitos de interesse a declarar.
Agradecimentos
Agradecemos a todos os membros dos grupos Sixma, Brummelkamp e Perrakis por suas frutíferas discussões científicas e por proporcionar um ambiente de trabalho agradável e, especificamente, agradecemos a Jan Sakoltchik ("pessoa 2") por ajudar a determinar a concentração de proteínas retratada na Figura 3C. Também gostaríamos de agradecer à instalação de crio-EM da NKI e ao Centro Holandês de Nanoscopia Eletrônica (NeCEN) da Universidade de Leiden por seu apoio. Este trabalho foi apoiado pela bolsa NWO Vici 016.Vici.170.033 concedida a T.R.B. A.P. e T.R.B. são investigadores Oncode e recebem financiamento da NWO ENW (OCENW. M20.324). L.L. recebeu financiamento do Fundo Austríaco para a Ciência (FWF JB4448-B). Esta pesquisa foi apoiada por uma bolsa institucional da Sociedade Holandesa de Câncer e do Ministério da Saúde, Bem-Estar e Esporte da Holanda.
Materiais
| Name | Company | Catalog Number | Comments |
| Material | |||
| 0.05% trypsin-EDTA | Gibco | 25300-054 | Cell culture |
| 10 cm plate | Falcon | 353003 | Cell culture |
| 15 cm plate | Thermo FisherScientific | 168381 | Cell culture |
| 50 mL tubes | Sarstedt | 62.547255 | Cell culture |
| 300 mesh quantifoil holey carbon copper grid R1.2/1.3 | Quantifoil Micro Tools | N1-C14nCu30-01 | Cryo-EM grid preparation |
| Cell scrapers | Falcon | 353085 | Cell culture |
| DMEM | Gibco | 41966-029 | Cell culture |
| EDTA | Merck | 108418 | Cell culture |
| EGTA | Sigma Aldrich | E3899 | Microtubule extraction |
| Ethane gas | Cryo-EM grid preparation | ||
| FCS | Serana | s-FBS-EU-015 | Cell culture |
| Glycerol | VWR | 24.397.296 | Microtubule extraction |
| GTP | Fisher Scientific | G8877-1G | Microtubule extraction |
| HCT116 VASH1 VASH2 MATCAP KO cells | self made | Wild type HCT116 cells RRID: CVCL_0291 | Cell culture |
| KOH | Merck | 1.05033 | Microtubule extraction |
| MgCl2 | Merck | 105833 | Microtubule extraction |
| Microtubule binding protein | self made | Cryo-EM grid preparation | |
| Needle | BD microlance | 300600 | Microtubule extraction |
| Paclitaxel | Santa Cruz Biotechnology | sc-212517 | caution toxic, microtubule extraction |
| PBS | Fisher Scientific | BP399 | Cell culture |
| Penicillin and streptomycin | Sigma Aldrich | P0781-100mL | Cell culture |
| PIPES | Merck | P8203 | Microtubule extraction |
| PMSF (in EtOH) | Roche | 16837091001 | Microtubule extraction |
| SDS sample buffer | self made | Quality assessment | |
| Syringe | BD plastipak | 309658 | Microtubule extraction |
| Ultra protease tables mini | Fisher Scientific | NC0975224 | Microtubule extraction |
| Whatman blotting paper | Whatman | 47000-100 | Cryo-EM grid preparation |
| Equipment | |||
| Flow hood | cell culture | ||
| GloQube | Quorum | Cryo-EM grid preparation | |
| Grid storage box | SWISSCI | 41018 | Cryo-EM grid storage |
| Heating block, electric or metal | to warm the buffers | ||
| Incubator, cell culture | NUAIR | cell culture | |
| LN2 dewar | Cryo-EM grid storage | ||
| Plunge-tweezers | Electron Microscopy Sciences | 0508-L5-PS | Cryo-EM grid preparation, hole drilled in top to fit the vitrobot |
| Polystyrene box | to keep the buffers warm | ||
| Sonicator | Qsonica | Q700 | Microtubule extraction |
| Standard light microscope | Olympus | CKX 41 | Quality assessment |
| TLA 100.3 rotor | Beckman Coulter | Microtubule extraction | |
| TLA 120.2 rotor | Beckman Coulter | Microtubule extraction | |
| Tubes for TLA 100.3 rotor | Beckman Coulter | 326819 | Microtubule extraction |
| Tubes for TLA 120.2 rotor | Beckman Coulter | 347356 | Microtubule extraction |
| Ultracentrifuge | Beckman Coulter | Optima MAX-XP | Microtubule extraction |
| Vitrobot | FEI, ThermoFischer Scientific | mark IV | Cryo-EM grid preparation |
| Vitrobot polystyrene container assembly with metal ethane cup | ThermoFisher Scientific | 200703 | Cryo-EM grid preparation |
| Water bath | cell culture |
Referências
- Janke, C., Magiera, M. M. The tubulin code and its role in controlling microtubule properties and functions. Nature Reviews Molecular Cell Biology. 21 (6), 307-326 (2020).
- Peris, L., et al. Motor-dependent microtubule disassembly driven by tubulin tyrosination. Journal of Cell Biology. 185 (7), 1159-1166 (2009).
- McKenney, R. J., Huynh, W., Tanenbaum, M. E., Bhabha, G., Vale, R. D. Activation of cytoplasmic dynein motility by dynactin-cargo adapter complexes. Science. 345 (6194), 337-341 (2014).
- Barisic, M., et al. Microtubule detyrosination guides chromosomes during mitosis. Science. 348 (6236), 799-803 (2015).
- Sirajuddin, M., Rice, L. M., Vale, R. D. Regulation of microtubule motors by tubulin isotypes and post-translational modifications. Nature Cell Biology. 16 (4), 335-344 (2014).
- Nogales, E., Kellogg, E. H. Challenges and opportunities in the high-resolution cryo-EM visualization of microtubules and their binding partners. Current Opinion in Structural Biology. 46, 65-70 (2017).
- Manka, S. W., Moores, C. A. Microtubule structure by cryo-EM: Snapshots of dynamic instability. Essays in Biochemistry. 62 (6), 737-751 (2018).
- Chaaban, S., Carter, A. P. Structure of dynein-dynactin on microtubules shows tandem adaptor binding. Nature. 610 (7930), 212-216 (2022).
- Lacey, S. E., He, S., Scheres, S. H., Carter, A. P. Cryo-EM of dynein microtubule-binding domains shows how an axonemal dynein distorts the microtubule. eLife. 8, 47145 (2019).
- Walton, T., Wu, H., Brown, A. Structure of a microtubule-bound axonemal dynein. Nature Communications. 12, 477 (2021).
- Sindelar, C. V., Downing, K. H. An atomic-level mechanism for activation of the kinesin molecular motors. Proceedings of the National Academy of Sciences of the United States of America. 107 (9), 4111-4116 (2010).
- Zhang, R., Alushin, G. M., Brown, A., Nogales, E. Mechanistic origin of microtubule dynamic instability and its modulation by EB proteins. Cell. 162 (4), 849-859 (2015).
- Maurer, S. P., Fourniol, F. J., Bohner, G., Moores, C. A., Surrey, T. EBs Recognize a nucleotide-dependent structural cap at growing microtubule ends. Cell. 149 (2), 371-382 (2012).
- Benoit, M. P. M. H., Asenjo, A. B., Sosa, H. Cryo-EM reveals the structural basis of microtubule depolymerization by kinesin-13s. Nature Communications. 9, 1662 (2018).
- Kellogg, E. H., et al. Near-atomic model of microtubule-tau interactions. Science. 360 (6394), 1242-1246 (2018).
- Brotzakis, Z. F., et al. A structural ensemble of a Tau-microtubule complex reveals regulatory Tau phosphorylation and acetylation mechanisms. ACS Central Science. 7 (12), 1986-1995 (2021).
- Kellogg, E. H., et al. Insights into the distinct mechanisms of action of taxane and non-taxane microtubule stabilizers from cryo-EM structures. Journal of Molecular Biology. 429 (5), 633-646 (2017).
- Vallee, R. B. Reversible assembly purification of microtubules without assembly-promoting agents and further purification of tubulin, microtubule-associated proteins, and MAP fragments. Methods in Enzymology. 134, 89-104 (1986).
- Wloga, D., Joachimiak, E., Louka, P., Gaertig, J. Posttranslational modifications of tubulin and cilia. Cold Spring Harbor Perspectives in Biology. 9 (6), 028159 (2017).
- Nieuwenhuis, J., Brummelkamp, T. R. The tubulin detyrosination cycle: Function and enzymes. Trends in Cell Biology. 29 (1), 80-92 (2019).
- Nieuwenhuis, J., et al. Vasohibins encode tubulin detyrosinating activity. Science. 358 (6369), 1453-1456 (2017).
- Aillaud, C., et al. Vasohibins/SVBP are tubulin carboxypeptidases (TCPs) that regulate neuron differentiation. Science. 358 (6369), 1448-1453 (2017).
- Landskron, L., et al. Posttranslational modification of microtubules by the MATCAP detyrosinase. Science. 376 (6595), (2022).
- Erck, C., et al. A vital role of tubulin-tyrosine-ligase for neuronal organization. Proceedings of the National Academy of Sciences of the United States of America. 102 (22), 7853-7858 (2005).
- Pagnamenta, A. T., et al. Defective tubulin detyrosination causes structural brain abnormalities with cognitive deficiency in humans and mice. Human Molecular Genetics. 28 (20), 3391-3405 (2019).
- Peris, L., et al. Tubulin tyrosination regulates synaptic function and is disrupted in Alzheimer's disease. Brain. 145 (7), 2486-2506 (2022).
- Souphron, J., et al. Purification of tubulin with controlled post-translational modifications by polymerization-depolymerization cycles. Nature Protocols. 14 (5), 1634-1660 (2019).
- Gell, C., et al. Purification of tubulin from porcine brain. Methods in Molecular Biology. 777, 15-28 (2011).
- Bodakuntla, S., Jijumon, A. S., Janke, C., Magiera, M. M. Purification of tubulin with controlled posttranslational modifications and isotypes from limited sources by polymerization-depolymerization cycles. Journal of Visualized Experiments. (165), e61826 (2020).
- Castoldi, M., Popov, A. V. Purification of brain tubulin through two cycles of polymerization-depolymerization in a high-molarity buffer. Protein Expression and Purification. 32 (1), 83-88 (2003).
- Li, G., Moore, J. K. Microtubule dynamics at low temperature: evidence that tubulin recycling limits assembly. Molecular Biology of the Cell. 31 (11), 1154-1166 (2020).
- Hyman, A. A., Salser, S., Drechsel, D. N., Unwin, N., Mitchison, T. J. Role of GTP hydrolysis in microtubule dynamics: information from a slowly hydrolyzable analogue. GMPCPP. Molecular Biology of the Cell. 3 (10), 1155-1167 (1992).
- Sindelar, C. V., Downing, K. H. The beginning of kinesin's force-generating cycle visualized at 9-Å resolution. Journal of Cell Biology. 177 (3), 377-385 (2007).
- Kellogg, E. H., et al. Near-atomic cryo-EM structure of PRC1 bound to the microtubule. Proceedings of the National Academy of Sciences of the United States of America. 113 (34), 9430-9439 (2016).
- Maurer, S. P., Bieling, P., Cope, J., Hoenger, A., Surrey, T. GTPγS microtubules mimic the growing microtubule end structure recognized by end-binding proteins (EBs). Proceedings of the National Academy of Sciences of the United States of America. 108 (10), 3988-3993 (2011).
- Manka, S. W., Moores, C. A. Pseudo-repeats in doublecortin make distinct mechanistic contributions to microtubule regulation. EMBO Reports. 21 (12), 51534 (2020).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoExplore Mais Artigos
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados