Method Article
Системные поставки микроРНК с использованием рекомбинантного аденоассоциированный вирус серотипа 9 для лечения нервно-мышечных заболеваний у грызунов
В этой статье
Резюме
Здесь мы описываем доставки микроРНК с использованием рекомбинантного аденоассоциированный вирус серотипа 9 в мышиной модели нервно-мышечных заболеваний. Один периферийных администрации в мышах привели к устойчивой Мирна гиперэкспрессия в мышцы и двигательных нейронов, обеспечивая возможность для изучения Мирна функции и терапевтический потенциал в vivo.
Аннотация
Система РНК-интерференции по дорожке эндогенного Мирна регулирует экспрессии генов, контролируя синтез белков через post-transcriptional генов. В последние годы Мирна опосредованной гена регулирование показал потенциал для лечения неврологических расстройств, вызванных токсичными усиления функции механизма. Однако эффективные доставке в тканях-мишенях ограничивает его применение. Здесь мы использовали модель трансгенные мыши для позвоночника и бульбарной мышечной атрофии (SBMA), нервно-мышечные заболевания вызваны Хантингтона экспансии в андрогена (AR), чтобы проверить сайленсинга генов недавно выявленных AR-ориентация Мирна, мир-298. Мы оверэкспрессировали мир-298-с помощью рекомбинантной аденоассоциированный вирус (rAAV) вектор серотип 9 для облегчения трансдукция-деления клеток. Одной инъекции хвост вен в SBMA мышей индуцированной постоянной и широко распространенной гиперэкспрессия мир-298 в скелетных мышцах и двигательных нейронов и привели к мелиорации нервно фенотип в мышей.
Введение
Интерферирующим некодирующих РНК, 21-23 нуклеотидов в длину, которые играют важную роль в регуляции экспрессии генов и контроля различных клеточных и метаболических путей. 1 экспрессии генов главным образом регулируется вызывая деградации глушителей или мРНК post-transcriptional ген. 2 адаптивной, обычно дополняют 3' непереведенные региона (утр) кодирование генов, хотя привязка к 5' УТР и Кодирующие области целевого объекта, который также был описан мРНК. 3
Как нынешнее понимание роли микроРНК в патогенезе заболеваний человека расширяется, фармакологические модуляции отдельных адаптивной или Мирна семей становится все более жизнеспособным вариантом терапевтических. По сравнению с другими стратегиями ингибирование РНК, адаптивной имеют много преимуществ: интерферирующим менее токсичны и менее иммуногенность и могут быть легко доставлены в клетки из-за их малого размера. 4 , 5 , 6 интерферирующим обычно имеют много целей в пределах сотовой сети, поэтому потенциальные эффекты пробить и проблемы безопасности, которые необходимо принять во внимание, наряду с эффективной доставки в тканях-мишенях.
Нервно-мышечных заболеваний приобретенных или унаследовали условия, которые влияют на мышцы и двигательных нейронов. Направленные против наркотиков в скелетных мышцах является новой областью исследований, где главной задачей является достижение широкого распространения в пределах терапевтического окна. 7 моторные нейроны являются более трудно ориентированы, главным образом потому, что препарат доступа исключается гематоэнцефалический барьер.
В этом исследовании были использованы клетки культуры и мыши модели спинного мозга и бульбарной мышечной атрофии (SBMA). SBMA является нервно-мышечные заболевания, вызванные токсичных усиления функции механизма, в котором затрагиваются мышечные и двигательных нейронов. 8 , 9 SBMA (Кеннеди болезни; Маккусика #313200) — Х-хромосомой заболевание, характеризующееся мышечная слабость и атрофия, вызванные CAG повторить расширения в AR ген, который кодирует расширенный Хантингтона тракта в AR белка. 10 не болезнь модифицирующие лечение в настоящее время доступна для этого расстройства. Трансгенные мыши модель, используемая в настоящем исследовании резюмирует особенности заболевания, в том числе гендерной специфики, патологии двигательного нейрона и прогрессивная мышечная атрофия. 11
В этом исследовании, наши усилия сосредоточены на выявлении Мирна, непосредственно результате выражение мутант трансген AR и на разработке безопасной и эффективной режим доставки Мирна спинного и скелетных мышцах нашей модели мыши болезни.
Здесь мы определили относительно uncharacterized miRNA, Мирна-298 (присоединение номер MIMAT0004901),12 непосредственно сократить мутант AR выражение в SBMA модели. Для того, чтобы обеспечить доставку мир-298 в тканях-мишенях, мы использовали вирусный стратегию, с рекомбинантным аденоассоциированный вирус серотипа 9 (rAAV9). rAAV9 способен через гематоэнцефалический барьер и посредническая долгосрочный экспрессии генов-деления клеток, включая нейронов. 13 единого системного администрирования AAV9-мир-298 привели к устойчивой выражение Мирна, эффективной трансдукции мышц и двигательных нейронов, вниз регулирование AR выражения и улучшении фенотип болезни в SBMA мышей. 14 эта методология может использоваться для предоставления Мирна или antagomirs гиперэкспрессия в естественных условиях.
протокол
Все процедуры были проведены в соответствии с национальными институтами здравоохранения руководство по уходу и использованию лабораторных животных (8 ред., национальных академий пресс, редакция 2011) и были одобрены Комитетом уход животных NINDS.
1. AAV9-miRNA дизайн выбор стратегии и Мирна
- Использование miRWalk прогнозирования базы данных для выбора кандидата адаптивной, которые взаимодействуют с мРНК 3' УТР регионе целевого гена. 15
Примечание: Ограничить минимальным семян длины последовательности Мирна по крайней мере 7 нуклеотидов. Выберите другие установленные Мирна предсказание программы (Миранда, miRDB, Targetscan) для сравнительного анализа. На основе этих критериев отбора, здесь, мир-185, мир-298, мир-873 и мир-877 были отобраны для дальнейшей оценки. - Извлечение последовательности выбранных Мирна из miRBase (http://www.mirbase.org/).
- Клонировать pri мир (60-70 НТС) и его 250-300 НТС фланговые геномной последовательности с обеих сторон, или макет последовательности, в соответствующие AAV векторных СНГ.
Примечание: Фланкируя последовательности требуется для правильного pri мир выражения и зрелые микроРНК обработки. Выберите двойной промоутер rAAV СНГ вектор с кассетой выражения, например состоящий из человека удлинение промоутер альфа фактор-1 (EIF1α), следуют выбранного Мирна или макет последовательности и промоутер человека цитомегаловирусом (CMV) следуют cDNA кодирования GFP флуоресцентные метки. Промоутер EIFα был выбран потому, что он гарантирует стабильное и однородной выражение, с минимальными рисками подавления. Ткани конкретных или условного промоутеров может использоваться, в зависимости от конкретного приложения. - Подготовить, очистить, и титровать AAV, опубликованных протоколов. 16
Примечание: Здесь, клонирование pri мир в AAV вектор и вирусных производства были исполнены внешней производителя.
2. хвост инъекции Вену AAV-miRNA плазмидной
Примечание: Этот шаг требует перестройки согласно целевого гена и возраст и вес мышей. Используйте институциональные и уход животных и использование Комитет (IACUC) руководящие принципы для определения дозы диапазоне, объем и лучший маршрут администрации, основанный на возраст и вес мышей. Ожидается, что пик начиная 2 недели после инъекции GFP флуоресценции сигнал и Мирна уровни выражения в тканях-мишенях. Следующий протокол относится к мышей-самцов в раннем взрослом возрасте. AAV должны обрабатываться как biohazard руководящими принципами по биобезопасности уровня 1.
- Разделите AAV-miRNA плазмида акций в 100-200 мкл аликвоты, содержащий вирусная нагрузка 1010-1011 вирусных геномов мл (vg/мл) с помощью стерильных фосфатный буфер (PBS). Лаборатории биологически опасных средств индивидуальной защиты должны использоваться для обработки AAV решения.
Примечание: После того, как Алиготе разморожен он может храниться при температуре 4 ° C на срок до двух недель. Вирусная фондовой может храниться в морозильной камере-80 ° C. - Останови мыши в коммерчески доступных взводы, таких как пластиковые или коническую пленку трубку нужного размера.
- Очистите поверхность от хвоста с 70% спирта салфетки.
- Держите теплые площадку (28-30 ° C) под хвост, чтобы увеличение вазодилатации 30 s. Альтернативно, теплые животных, с использованием красного тепла лампы (на расстоянии 2-3 футов) или путем погружения хвост в теплую воду.
-
Начиная от дистальной части хвоста, вставить иглу (27-30 G) загружен с вирусной Алиготе, конические, 15° от хвоста, в Вену. Перед инъекцией убедитесь, что игла вставлена правильно.
- Если почувствуете сопротивление во время инъекции, или припухлость появляется под кожей, остановите процедуру. Извлеките иглу и повторно вставить иглу выше предыдущей инъекции.
Примечание: в качестве альтернативы, это может быть достигнуто, нежно аспирационных иглы и наблюдая за кровь. Жесткий стремление можно свернуть хвост вен. Если Вены бланша во время инъекции, игла вставлена правильно.
- Если почувствуете сопротивление во время инъекции, или припухлость появляется под кожей, остановите процедуру. Извлеките иглу и повторно вставить иглу выше предыдущей инъекции.
- После инъекции, подождите несколько секунд, прежде чем поднять иглы.
- Наблюдать за место инъекции для кровотечение. Придайте умеренного давления, с помощью двух пальцев на сайт до остановки кровотечения.
- Вернуть животное к своей клетке.
3. поведенческие анализов
Примечание: Все эксперименты проводились слепо третьей стороной с сокрытие лечения, однозначно закодированных флаконов. Рандомизированных порядок лечения. При выполнении тестов, описанные ниже, экспериментальных условий (тип номера) и время суток должна контролироваться для снижения вариации. Этот тест должен выполняться на мышах, старше, чем четыре недели для достижения надежных результатов. Мыши были проведены поведенческие оценки один раз перед вирусный инъекций на 5 недель возраста для получения базовых нормальной производительности. После вирусных инъекции мышей были оценены один раз в неделю, начиная 48 ч после инъекции, вплоть до 40 недель возраста.
- Принесите мыши вводится с AAV для тихой, темный номер, свободный от шума или других беспорядков по крайней мере 30 минут до начала испытания. Не беспокоить животных в этот период акклиматизации.
- Акклиматизировать мыши в новую комнату для 30 минут, а затем запустите следующие поведенческие анализов (шаги 3.3 и 3.4). Держите пробел 10 мин между калибровочных поведенческих.
-
Висит провод тест
Примечание: Этот тест контролирует мышечной силы и моторные дисфункции.- Используйте лист обивка выступать в качестве подушки. Поднимите мыши, его хвост и поместите его в центре ГРИД решетку. Поднять стойки 15-20 см над поверхностью и медленно перевернуть экран чтобы животное скорректировать свою хватку на экране.
- После того, как полностью перевернут стойки, запустить таймер и рекордное время падать.
Примечание: Мышь будет висеть с четырьмя конечностями на сетке. Если провод установлено слишком низкое мышей не может повесить на. Если мышь упасть сетке до 60 s, поместите их обратно на сетке, Сброс таймера и повторите эту процедуру до двух больше попыток. Зарегистрируйте лучшую производительность. - Когда время ограничить 60 s достигается, животных возврата к клетке.
-
Ногой печати пробирного
Примечание: Абсорбирующие лист должен быть узких ВПП около 70 см длиной и 5 см шириной с высокими стенами 5 см.- Аккуратно возьмите мышь в одной рукой и применять красными чернилами на передние лапы и синие чернила на задние лапы с помощью кисти.
- Поместите абсорбирующий лист на полу узкие полосы.
- Позволяет мыши, чтобы идти или бежать над абсорбирующий лист по прямой линии в ВПП от одного конца к другой.
- Повторите этот процесс, два раза с помощью мыши с использованием абсорбирующего лист свежий.
- Измерьте расстояние между двух последовательных шагов в движение вперед. Не включают первые и последние несколько следов где животное просто начала и окончания ее выполнения.
4. эвтаназии и ткани урожай
- Используйте камеру эвтаназии или колпаком. При использовании колпаком, выполните процедуру под вытяжного шкафа.
- Замочите хлопок с изофлюрановая и поместите его в колпаке. Используйте разделитель физической чтобы сохранить животных от физического контакта с материалом анестезии. Поместите животное в банке сразу же после этого шага.
Примечание: Колпаке не должно быть предварительно заряженные с изофлюрановая, чтобы избежать возможности гипоксемии у животных. - Продолжить выдержка изофлюрановая до 30 секунд после остановки дыхания.
- Сразу же после удаления мыши из кувшина, усыпить, шейки матки дислокации.
Примечание: Этот шаг должен проходить как можно скорее, чтобы избежать деградации ткани. -
Урожай спинного шнур питания сначала и затем скелетных мышц четырехглавой мышцы.
- Чтобы сжать спинного мозга, подвергать зад мыши и исправить четыре конечности на стороне к доске рассечение.
- Вымойте сайт диссекции с 70% этиловом спирте.
- Выполняйте шейки матки дислокации с помощью острых ножниц.
- Сделайте надрез в коже в срединной линии. Снять шкуру, резки или внимательно разрывает кожи в поперечной плоскости, а затем потянув Пелт вверх и над головой. Удалите головы, резки ножницами под лопатками и в регионе C1-2 столбца (Найдено прилегающих к основанию черепа).
- Сокращение мышц брюшной стенки на вентральной стороне и боков, продолжить в одном направлении, в то время, пока не будет достигнуто позвоночника.
- С помощью острых ножниц удалить позвонков, начиная от шейного отдела спинного. Снимите боковые части позвонков, резки через позвоночной арки с обеих сторон.
- После удаления всего позвонков Освободите спинного мозга.
-
Оснастки заморозить заготовленной тканей в предварительно охлажденный 2-methylbutane, используя следующий метод:
- Половина Заполните чашу из нержавеющей стали с 2-methylbutane и погружать нижней четверти чаши в контейнер с жидким азотом.
- Предварительно охладите 2-methylbutane в жидком азоте для 1-2 мин.
- Место скелетных мышц с щипцами в 2-methylbutane, до тех пор, пока она становится белым. Сразу передача ткани сухим льдом и затем сохранить его в-80 ° C.
- Для спинного иммуноокрашивания внедрите ткани в парафиновых блоков при комнатной температуре до оснастки, замораживания, как описано. 17
- Для биохимического анализа и количественной оценки Мирна1 место заготовленной ткани в cryovial и замораживание в жидком азоте. Хранение образцов-80 ° C.
Результаты
Вирусная нагрузка 1011 vg AAV9-мир-298 было впрыснуто через одной инъекции хвост вен в 5 неделя старый SBMA мышей. Эти мышей нести человека трансген AR с аномально расширенных Хантингтона тракта в АР (AR97Q) и развивать признаки нервно-мышечные заболевания, 10 недель возраста (потеря веса, сгорбленная обратно и атрофии мышц). 11 поясничного отдела спинного мозга и четырехглавой мышцы были собраны на 2, 4, 8 и 12 недель после приема для квантификации Мирна, биохимические пробы и иммуногистохимия (рис. 1). Администрация, лечения и последующего анализа были исполнены ослепленный следователей.
соответственно, qRT ПЦР анализ показал мир-298 выражение в скелетных мышцах и спинного две недели и через четыре недели после лечения с уровнями выражение пик на 8 недель в скелетных мышцах и 12 недель в спинном мозге после инъекции (Рисунок 2 ). С помощью микроскопа (Axiovert 100 М), зеленая Флуоресценция сигнал был обнаружен в мышечной ткани и в мотонейронов спинного мозга путем совместного локализации GFP и мотонейрона маркер холина ацетилтрансфераза (чат) через 10 недель после лечения, когда мышей начинают Показать проявления болезни (рис. 2).
Использование режима же дозы, когорты SBMA мышей был рандомизированных получать либо мир-298 или макет на 7 недель возраста через хвост инъекции Вену для биохимических анализов и функциональных характеристик. Инъекции последовали за вес и поведенческие оценки 40 недель возраста. qRT ПЦР анализ показал, что мир-298 лечение снижает уровень мутант AR в пораженных тканей (рис. 3) и увеличение веса тела и улучшенная производительность мотор (рис. 4), начиная через 10 недель после инъекции.
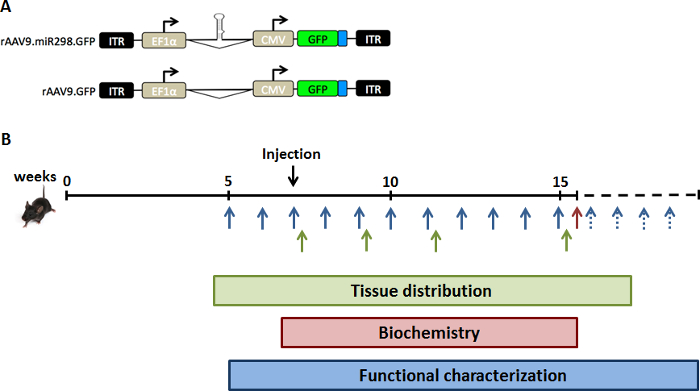
Рисунок 1: схема дизайна исследования. Чтобы увеличить уровни выражения мир-298 в естественных условиях, мы вводили SBMA мышей с (A) вектора AAV двойной промоутер плазмида, выражая GFP и мир-298 или макет. (B) мышах вводили через хвост напрасно одной инъекции в 7 недель возраста (предварительно симптоматической стадии). Спинного мозга и четырехглавой мышцы были собраны из когорты SBMA мышей в разное время точках для анализа распределения ткани (зеленый). Когорта SBMA мышей лечение и жертву на 16 недель возраста для биохимического анализа (красный). Вес и поведенческих анализов были исполнены за неделю до 40 недель возраста для функциональных характеристик (синий). Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.

Рисунок 2: AAV9-мир-298 доставки в мышах. Используя метод, описанный здесь, мышей получил AAV9-мир-298-GFP или AAV9-макет GFP через внутривенные инъекции. Общая микроРНК была собрана из поясничного отдела спинного мозга и четырехглавой мышцы 2,4,8 и 12 недель после инъекции. qRT ПЦР была выполнена для оценки уровня экспрессии мир-298 в (A) четырехглавой мышцы (n = 5) (B) поясничного отдела спинного мозга (n = 5, P < 0.01). Все данные представляются как означает среднее ± стандартная ошибка. Широкое распространение трансдукции вектора AAV в тканях собрано 10 недель после лечения была подтверждена локализации окрашивания для гена GFP в четырехглавой мышцы (C) (Оригинальный масштаб, 10 X. Шкалы бар = 100 мкм) и (D) двигательных нейронов в поясничном отделе спинного мозга (Оригинальный масштаб, 40 X. Шкалы бар = 10 мкм. GFP (зеленый), чат (красный) и DAPI (синий). Рисунок был изменен от doi: 10.1038/mt.2016.13. 14 Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.

Рисунок 3: Мирна-298 гиперэкспрессия результате мутант AR в спинном мозге и четырехглавой мышцы в мышах. qRT ПЦР была проведена оценить уровни выражения AR мРНК в поясничном отделе спинного мозга (A) и (B) четырехглавой мышцы, лечение с AAV9-мир-298-GFP или AAV9-макет GFP. Стенограмма уровни были нормализованы по snoRNA202 (n = 5 на лечение). * P < 0,05, ** P < 0.01. Все данные представляются как средства ± стандартных ошибок. Рисунок был изменен от doi: 10.1038/mt.2016.13. 14

Рисунок 4: мир-298 гиперэкспрессия улучшает моторную функцию и снижает потери веса. Поведенческие оценки была выполнена один раз в неделю (w), между 5 до 40 недели. Тело вес (слева) и висит провод (справа) производительность мышей (n = 15 в группе). Все данные представляются как средства ± стандартных ошибок. Рисунок был изменен от doi: 10.1038/mt.2016.13. 14
Обсуждение
Здесь мы показываем, высоко эффективной и доступной методологии для выбора и доставить через хвост инъекции Мирна с использованием rAAV9 как вирусный вектор целевого скелетных мышц и двигательных нейронов у мышей. 14 по сравнению с другими стратегиями интерференции, адаптивной, менее токсичных и менее иммуногенность. 18 Кроме того, их небольшой размер делает их хорошо подходят для упаковки ограниченного потенциала вирусных векторов. 2 вычислительных алгоритмов и предсказание инструменты позволяют идентифицировать предполагаемый Мирна мРНК-мишеней. После того, как определены, эффекты Мирна на экспрессию генов цели должны быть проверены. Общий подход заключается в overexpress данного микроРНК в пробирке и выявления целевых уровнях выражения протеина с использованием западных анализа. 14 , 19
Различные исследования использовали вирусный и не вирусной стратегии для доставки адаптивной. 13 здесь мы использовали аденоассоциированный вирус (AAV) как средство доставки генов. По сравнению с другими вирусных векторов, Аав вызывает низкой иммуногенностью, позволяет долгосрочного переноса генов, и имеет широкий спектр тропизм в делящихся и -деления клетки. 18 этот метод доставки также можно обойти необходимость химической модификации, которые могут повлиять на функциональность и специфичность молекулы РНК. Есть несколько серотипов AAV, которые главным образом определяются состав капсульных белков. Эти серотипов отличаются в их тропизма и передают различных типов клеток. Необходимо выбрать правильный серотип при рассмотрении ткани-мишени. Мы выбрали rAAV9, благодаря своей высокой электромеханической эффективности в центральной нервной системе и скелетных мышц, после периферийных администрации19,20. Этот подход показал большую эффективность трансдукции новорожденных животных, по сравнению с взрослых животных, скорее всего, из-за различий в составе внеклеточного матрикса, соотношение нейронов и глии и зрелость blood-brain барьер. 21 , 22
Важным шагом в этом протоколе является дизайн вектора выражения. По сравнению с bicistronic векторов, которые сдерживаются ниже выражение гена второй, по сравнению с первый ген рядом с промоутером, двойной промоутер вектор позволяет спина к спине конфигурации, таким образом давая высокое выражение Мирна и EGFP, позволяя локализации микроРНК в ткани мыши, иммунофлюоресценции.
Внутривенные инъекции AAV9 привело к высокой эффективности и однородной трансдукции в тканях-мишенях, скелетных мышц и двигательных нейронов. Этот маршрут инъекции позволяет введенной дозы для достижения кровообращения и пересечь гематоэнцефалический барьер крови, которая имеет важное значение для терапии против центральной нервной системы. Кроме того это неинвазивный метод для доставки в ЦНС. Мир-298 выражение увеличилась в спинной мозг и мышцы после 2-4 недель с одной периферийных инъекции в возрасте 5 недель. Когда с помощью одноцепочечной генома векторы AAV, de novo синтез второй нити ДНК может объясняться задержкой трансдукции. 23
Уровни человеческого мир-298 были обнаружить в обработанных мышей 20 недель после однократного применения, предполагая, что для лечения хронических заболеваний, множественные инъекции могут потребоваться для достижения терапевтический эффект. Однако Мирна деградации с течением времени может иметь ограничения при необходимости непрерывного неоднократные администрации. Кроме того адаптивный иммунитет к векторы AAV могут образовываться еще одним препятствием для успешного гена доставки. 24 таким образом поколение векторы AAV, которые являются иммунологически инертными имеет решающее значение для повторных администрации и достижения долгосрочных эффектов с этой перспективной системы доставки. 25
Ограничение на использование Мирна как терапевтические стратегии является риск-целевого воздействия. Интерферирующим могут взаимодействовать через incomplementary низкопробный спаривать с другими транскрипты гена, который создает угрозу безопасности с этим подходом. Проектирование RNAi последовательностей, включая использование неканонических адаптивной, таких как mirtrons, который обойти комплекс микро процессором и обширную долгосрочную безопасность и переносимость исследования важны прежде чем переводить эту стратегию в безопасное и эффективной терапии. 26 , 27 , 28
Метод, описанный здесь первоначально был разработан для гиперэкспрессия Мирна, но он также может использоваться для Мирна ингибирование терапии с использованием antagomirs.
Раскрытие информации
Авторы не имеют ничего сообщать.
Благодарности
Авторы заявляют никакого конфликта интересов. Мы благодарим SignaGen лаборатории (Rockvile, MD, США) для производства вирус AAV9. Это исследование было поддержано очной программе исследований NINDS, низ. Филипп р. ли был поддержан средств от отдела интрамуральных исследований NICHD. Карло Ринальди был поддержан стипендий от французской ассоциации contre les миопатии (АСМ).
Материалы
| Name | Company | Catalog Number | Comments |
| QIAzol Lysis Reagent | Qiagen | 79306 | Lysis of fatty and standard tissues before RNA isolation |
| miRNeasy Mini Kit | Qiagen | 217004 | Purification of miRNA and total RNA |
| TaqMan MicroRNA Reverse Transcription kit | ThermoFisher Scientific | 4366596 | A highly specific kit that quantitates only mature miRNAs |
| snoRNA202 Primer | ThermoFisher Scientific | 1232 | Taqman miRNA control assay in mouse |
| miR-298 Primer | ThermoFisher Scientific | 2190 | Taqman miRNA-298 assay in mouse |
| Anti-GFP antibody | abcam | ab290 | Rabbit polyclonal to GFP - ChIP Grade |
| Red ink pad | Dovecraft Essentials | ||
| Blue ink pad | Dovecraft Essentials | ||
| AAV9-GFP vector | SignaGen Laboratories | SL100840 | Large scale AAV plasmid construction, packaging and purification |
| mmu-miR-298-5p | ThermoFisher Scientific | MC12525 | mirVana miRNA mimic |
| AAV9-EF1a-has-mir-298-GFP | Vector Biosystems Inc |
Ссылки
- Broderick, J. A., Zamore, P. D. miRNA therapeutics. Gene Therapy. 18, 1104-1110 (2011).
- Esteller, M. Non-coding RNAs in human disease. Nat Rev Genet. 12, 861-874 (2011).
- Pickering, B. M., Willis, A. E. The implications of structured 5' untranslated regions on translation and disease. Semin Cell Dev Biol. 16, 39-47 (2005).
- Bilen, J., Liu, N., Burnett, B. G., Pittman, R. N., Bonini, N. M. MicroRNA pathways modulate polyglutamine-induced neurodegeneration. Mol Cell. 24, 157-163 (2006).
- Lee, Y., Samaco, R. C., Gatchel, J. R., Thaller, C., Orr, H. T., Zoghbi, H. Y. miR-19, miR-101 and miR-130 co-regulate ATXN1 levels to potentially modulate SCA1 pathogenesis. Nat Neurosci. 11, 1137-1139 (2008).
- Liu, N., et al. The microRNA miR-34 modulates ageing and neurodegeneration in Drosophila. Nature. 482, 519-523 (2012).
- Ebner, D. C., et al. Strategies for skeletal muscle targeting in drug discovery. Curr Pharm Des. 10, 1327-1336 (2015).
- Giorgetti, E., Lieberman, A. P. Polyglutamine androgen receptor-mediated neuromuscular disease. Cell Mol Life Sci. 73, 3991-3999 (2016).
- Grunseich, C., Rinaldi, C., Fischbeck, K. H. Spinal and bulbar muscular atrophy: pathogenesis and clinical management. Oral Dis. 20, 6-9 (2014).
- La Spada, A. R., Wilson, E. M., Lubahn, D. B., Harding, A. E., Fischbeck, K. H. Androgen receptor gene mutations in X-linked spinal and bulbar muscular atrophy. Nature. 352, 77-79 (1991).
- Katsuno, M., Adachi, H., Kume, A., Li, M., Nakagomi, Y., Niwa, H., Sang, C., Kobayashi, Y., Doyu, M., Sobue, G. Testosterone reduction prevents phenotypic expression in a transgenic mouse model of spinal and bulbar muscular atrophy. Neuron. 35, 843-854 (2002).
- Boissonneault, V., Plante, I., Rivest, S., Provost, P. MicroRNA-298 and microRNA-328 regulate expression of mouse beta-amyloid precursor protein-converting enzyme 1. J Biol Chem. 284, 1971-1981 (2009).
- Choudhury, S. R., et al. Widespread central nervous system gene transfer and silencing after systemic delivery of novel AAV-AS vector. Mol Ther. 24, 726-735 (2016).
- Pourshafie, N., et al. MiR-298 counteracts mutant androgen receptor toxicity in spinal and bulbar muscular atrophy. Mol Ther. 24, 937-945 (2016).
- Dweep, H., Sticht, C., Pandey, P., Gretz, N. miRWalk--database: prediction of possible miRNA binding sites by "walking" the genes of three genomes. J Biomed Inform. 44, 839-847 (2011).
- McClure, C., Cole, K. L., Wulff, P., Klugmann, M., Murray, A. J. Production and titering of recombinant adeno-associated viral vectors. J Vis Exp. (57), e3348(2011).
- Stuard, D. A., Oorschot, D. E. Embedding, sectioning, immunocytochemical and stereological methods that optimise research on the lesioned adult rat spinal cord. J Neurosci Methods. 61, 5-14 (1995).
- Huang, F., et al. miR-25 alleviates polyQ-mediated cytotoxicity by silencing ATXN3. FEBS Lett. 588, 4791-4798 (2014).
- Kuhn, D. E., Martin, M. M., Feldman, D. S., Terry, A. V., Nuovo, G. J., Elton, T. S. Experimental validation of miRNA targets. Methods. 44, 47-54 (2008).
- Yang, N. An overview of viral and nonviral delivery systems for microRNA. Int J Pharm Investig. 5, 179-181 (2015).
- Bourdenx, M., Dutheil, N., Bezard, E., Dehay, B. Systemic gene delivery to the central nervous system using Adeno-associated virus. Front Mol Neurosci. 7, 50(2014).
- Foust, K. D., Nurre, E., Montgomery, C. L., Hernandez, A., Chan, C. M., Kaspar, B. K. Intravascular AAV9 preferentially targets neonatal neurons and adult astrocytes. Nat Biotechnol. 27, 59-65 (2009).
- Wang, Z., Ma, H. -I., Li, J., Sun, L., Zhang, J., Xiao, X. Rapid and highly efficient transduction by double-stranded adeno-associated virus vectors in vitro and in vivo. Gene Therapy. 10, 2105-2111 (2003).
- Saunders, N. R., Joakim Ek, C., Dziegielewska, K. M. The neonatal blood-brain barrier is functionally effective, and immaturity does not explain differential targeting of AAV9. Nat Biotechnol. 27, 804-805 (2009).
- Boudreau, R. L., Spengler, R. M., Davidson, B. L. Rational design of therapeutic siRNAs: minimizing off-targeting potential to improve the safety of RNAi therapy for Huntington’s disease. Mol Ther. 19, 2169-2177 (2011).
- Duque, S., Joussemet, B., Riviere, C., Marais, T., Dubreil, L., Douar, A. M., et al. Intravenous administration of self-complementary AAV9 enables transgene delivery to adult motor neurons. Mol Ther. 17, 1187-1196 (2009).
- Lowenstein, P. R. Crossing the rubicon. Nat Biotechnol. 27, 42-44 (2009).
- Sibley, C. R., Seow, Y., Curtis, H., Weinberg, M. S., Wood, M. J. Silencing of Parkinson's disease-associated genes with artificial mirtron mimics of miR-1224. Nucleic Acids Res. 40, 9863-9875 (2012).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены