Method Article
Трансплантация неонатальных мышиных сердечных макрофагов взрослым мышам
В этой статье
Резюме
Мы предоставляем протокол для отделения и трансплантации неонатальных сердечных макрофагов во взрослое сердце мыши, что может быть многообещающим способом содействия восстановлению сердца.
Аннотация
В поврежденном миокарде новорожденных макрофаги способствуют пролиферации кардиомиоцитов и ангиогенезу и способствуют регенерации сердца. Настоящее исследование показывает, что трансплантация неонатальных сердечных макрофагов, набранных в результате травмы, способствует регенерации сердца взрослого человека после инфаркта миокарда с улучшением сердечной функции и пролиферации кардиомиоцитов. Результаты показывают, что трансплантация неонатальных сердечных макрофагов может быть многообещающей стратегией лечения сердечной травмы. Здесь мы предоставляем технические детали, в том числе выделение неонатальных сердечных макрофагов из апикальных резекционных сердец неонатальных мышей, трансплантацию макрофагов взрослым мышам, инфарктированным миокардом, и оценку регенерации сердца после макрофагального трансплантата.
Введение
Регенерация сердца является перспективной стратегией восстановления сердечной функции после сердечной травмы и защиты от сердечной недостаточности1,2,3. После повреждения миокарда макрофаги проникают в поврежденное сердце и были исследованы в качестве ключевых факторов во время регенерации сердца новорожденных4,5,6. Помимо очистки некротического клеточного мусора и индуцирования воспаления, макрофаги способствуют ангиогенезу5 и пролиферации кардиомиоцитов7 после инфаркта миокарда у неонатальных мышей.
Наше предыдущее исследование показывает, что трансплантация неонатальных сердечных макрофагов, выделенных из поврежденного сердца новорожденного, усиливает регенерацию сердца у взрослых7,что указывает на то, что трансплантация макрофагов сердца новорожденных может быть многообещающей стратегией лечения сердечной травмы. Здесь мы предоставляем технические детали, в том числе выделение неонатальных сердечных макрофагов из апикальных резекционных сердец неонатальных мышей, трансплантацию макрофагов взрослым мышам, инфарктированным миокардом, и оценку регенерации сердца после трансплантата макрофагов(рисунок 1).
протокол
Все эксперименты проводились в соответствии с Руководством по использованию и уходу за лабораторными животными. Все протоколы для животных были одобрены Институциональным комитетом по уходу за животными и их использованию (IACUC), больницей Фувай, Китайской академией медицинских наук. Асептическая техника требуется на протяжении всей процедуры, чтобы предотвратить загрязнение места операции.
1. Операция апикальной резекции у неонатальной 1-дневной мыши Cx3cr1 GFP/+ (C57BL/6 фон)
- Анестезия
- Выведите всех детенышей мышей из клеток и поместите их в чистую сухую коробку.
- Вставить каждую мышь в лед примерно на 2-3 минуты. Убедитесь, что между льдом и псом мыши есть тонкий барьер, такой как латекс или марля, чтобы предотвратить обморожение.
- Определите достаточную анестезию, наблюдая за следующими признаками: бледная кожа, отсутствие движения конечностей и отсутствие педального рефлекса.
- Торакотомии
- Предварительно охлаждите бронзовую операционную платформу в течение ночи при -20 °C, чтобы помочь сохранить анестезию.
- Вытащенную анестезированную мышь из ящика для льда и положите ее на бронзовую операционную платформу. Закрепите мышь на операционной платформе в положении лежа на спине с помощью медицинской клейкой ленты.
- Поместите операционную платформу с мышью на нее под стереоскоп.
- Продезинфицируйте сундук мышей с помощью подготовительной прокладки, пропитанной бетадином и 70% спиртом, или в соответствии с институциональной политикой.
- Разрезайте кожу с помощью разреза 1 см в четвертой межречной области грудной полости, а затем отделите межребрачные мышцы с помощью микрохирургических ножниц до тех пор, пока к сердцу не будет доступен.
- Поочередно надавливать на грудь и живот с помощью двух щипцов до тех пор, пока сердце не выйдет из грудной клетки без каких-либо механических повреждений.
- Установите ребра ниже и выше небольшого разреза в качестве естественной фиксации для обездвиживания сердца.
- Резекция верхухи желудочков
- Найдите вершину левого желудочка. Вырежьте 1 мм диаметром желудочковой верхушкой ткани с помощью ножниц иридэктомии под стереоскопом.
- Подтвердите, что камера левого желудочка открыта, и начните сочиться.
- Осторожно прижмите сердце обратно к грудной полости с помощью ватного тампона.
- Зашивание мышц, ребер и кожи с помощью 8-0 Проленовые швы.
- Тщательно очистите мышь после операции.
- Послеоперационный уход
- Перенесите мышь с рабочей платформы на нагревательное одеяло с 37 °C, чтобы прогреть тело сразу после операции.
- Подтвердить анабиоз мыши можно, наблюдая за следующими признаками: спонтанное восстановление дыхания, изменение цвета кожи от бледного до розового, движение конечностей.
- Отведите прооперированную мышь обратно к ее матери, как только она выздоровеет.
- При необходимости смешайте управляемую мышь с материалами гнездования матери.
ПРИМЕЧАНИЕ: Важно удалить всех 1-дневных щенков у матери сразу, а затем вернуть их все сразу после того, как все щенки будут восстановлены.
2. Приготовление суспензии макрофагов сердца новорожденных
ПРИМЕЧАНИЕ: Все эти экспериментальные процедуры следует проводить в темном месте и в стерильных условиях.
- Соберите сердце неонатальной мыши Cx3cr1GFP/+ через 1 день после апикальной резекции
- Усыплите мышь Cx3cr1GFP/+ через день после апикальной резекции. Используйте избыток углекислого газа и обезглавливать мышь последовательно, чтобы применить эвтаназию.
- Вытастите сердце из груди и погрузите его в 10-сантиметровую посуду с PBS.
- Отрежьте сосуды и оставшуюся соединительную ткань от желудочков. Отрежьте ушной аппендикс и отток от сердца.
- После того, как сердце перестанет биться, разрезайте сердце на 1-2 мм3 кусочка в буфере PBS с помощью микрохирургических ножниц(рисунок 2A).
- Диссоциация сердца новорожденных мышей
- Переложите собранную сердечную ткань в пробирку, содержащую 2,5 мл предварительно нагретой ферментной смеси(Таблица материалов),и плотно закройте трубку.
- Перевертите трубку и поместите ее колпачком вниз(рисунок 2B).
- Запустите программу диссоциации сердцановорожденных (Таблица материалов).
- Отсоедрите трубку от диссоциатора после завершения программы.
- Добавьте в пробирку 7,5 мл 1x DMEM с 10% FBS.
- Фильтруйте и перенесите суспензию в центрифужную трубку 15 мл(рисунок 2C). Центрифугировать клеточную суспензию при 300 х г в течение 5 минут.
- Повторно суспендируют клеточную гранулу в 1 мл раствора лизиса клеток крови и инкубируют в течение 2 минут при комнатной температуре.
- Добавьте 5-10 мл буфера PBS в суспензию и центрифугу при 300 х г в течение 5 минут.
- Повторно суспендируют ячейку гранулы в 1 мл DMEM с 10% FBS.
- Выделение макрофагов сердца новорожденных
- Сортировать GFP+ неонатальные сердечные макрофаги по FACS. Получают отсортированные макрофаги в стерильной пробирке, содержащей 500 мкл DMEM с 10% FBS.
- Подсчитайте GFP+ макрофаги(рисунок 2D). Повторно суспендировать макрофаг в ДМЭМ с 10% ФБС в концентрации 1 х 106 макрофагов на 200 мкл ДМЭМ для последующей инъекции.
ПРИМЕЧАНИЕ: Количество GFP+ макрофагов невелико у одного новорожденного (приблизительно 1 х 105); поэтому для получения достаточного количества макрофагов для каждой инъекции взрослой мыши следует использовать не менее 10 новорожденных.
3. Трансплантация макрофагов сердца новорожденных
- Провести операцию по инфаркту миокарда взрослой (6-8-недельной) мыши C57BL/6 самца путем перевязки левой передней коронарной артерии8.
- Положите прооперированную мышь на нагретое при 37 °C одеяло до тех пор, пока она не восстановится.
- Внутривенно вводят 200 мкл DMEM с 1 х 106 GFP+ неонатальными сердечными макрофагами в инфарктированную взрослую мышь после операции (примерно через 6 часов) через хвостовую вену.
- Отправьте мышь обратно в чистую клетку.
4. Оценка результатов
- Проверка эффективности впрыска
- Обезболивают прооперированную мышь и собирают урожай сердца через 7 дней после операции по инфаркту миокарда.
- Погрузите сердце в предварительно охлажденный буфер PBS.
- Зафиксируйте сердечную ткань 4% полиформальдегидом в течение 72 часов при комнатной температуре с встряхиванием.
- Обезвоживают сердечную ткань в диметилбензоле и этаноле.
- Встроить сердечную ткань в парафин и разрезать ее на участки толщиной 5 мкм.
- Выполните стандартный протокол иммунофлуоресцентного окрашивания1. Используйте α-актинин для маркировки кардиомиоцитов.
- ОбнаружитьGFP+ макрофаги в сердце, получая трансплантацию.
- Выполните стандартный протокол иммунофлуоресцентного окрашивания1. Используйте α-актинин и рН3 для маркировки кардиомиоцитов и пролиферации клеток соответственно(рисунок 3А).
- Оценка восстановления сердца после трансплантации
- Используйте эхокардиографию на оперируемой мыши через месяц после операции1.
- Анализ сердечной функции путем сравнения фракции выброса левого желудочка и дробного укорочения в разных группах(рисунок 3В).
- Обезболить прооперированную мышь и собрать урожай сердца.
- Повторите шаги 4.1.2-4.1.5.
- Выполните протокол окрашивания Массона.
- Анализ инфарктной области после инъекции макрофага(рисунок 3С).
Результаты
Протокол, описанный здесь, обобщен в блок-схеме(рисунок 1). Мы выполнили операцию апикальной резекции на 1-дневной мыши Cx3cr1GFP/+. Как показано на рисунке 2A,неонатальная мышь Cx3cr1GFP/+ была закреплена на операционной платформе под стереоскопом после анестезии. Мы оказывали поочередное давление на грудную клетку и живот мыши с помощью двух щипцов, которые могут быть настроены как тракт для направления сердца, выскакивающего из грудной клетки. Следует избегать любых дополнительных механических повреждений сердца, которые могут повлиять на регенерацию сердца. Сердце было обездвижено окружающими тканями грудной клетки, что облегчило операцию на миокарде. Мы обнаружили, что отсечение менее 1 мм диаметром резецированной верхушеской ткани ножницами иридэктомии было уместно, когда камера левого желудочка начала сочиться. Успешная индукция модели апикальной резекции необходима для трансплантации макрофагов8,9.
Мы отсортировали макрофаги GFP+ строго по протоколу диссоциации сердца новорожденных1 (рисунок 2).
Неонатальные сердечные макрофаги были введены в инфаркт сердца миокарда взрослой мыши вскоре после изоляции. Чтобы подтвердить эффективность трансплантации макрофагов, мы выполнили иммунофлуоресцентное окрашивание через 7 дней после инъекции. Результаты показали, что GFP+ макрофаги могут быть обнаружены во взрослом сердце инфарктированной мыши с инфарктом, что указывает на успешную трансплантацию неонатального сердечного макрофага. Мы использовали коиммуноразморазведение рН3 с α-актинином. Колокализацией считалась пролиферация кардиомиоцитов. Результаты показали, что количество пролиферативных кардиомиоцитов было повышено в группе, вводимой макрофагами, что указывает на то, что способность к пролиферации кардиомиоцитов у взрослых была повышена после трансплантации(рисунок 3).
Регенерацию сердца взрослой мыши оценивали через 1 месяц после трансплантации. Мы выполнили эхокардиограмму на взрослой мыши и обнаружили, что инъекция макрофагов может улучшить сердечную функцию после инфаркта миокарда. Было выполнено окрашивание Массона, и результаты показали, что инфарктная область была значительно уменьшена после трансплантации неонатального кардиохромага(рисунок 3). Все эти результаты показали, что трансплантация кардиофагов новорожденных способствует регенерации сердца взрослых мышей и пролиферации кардиомиоцитов.
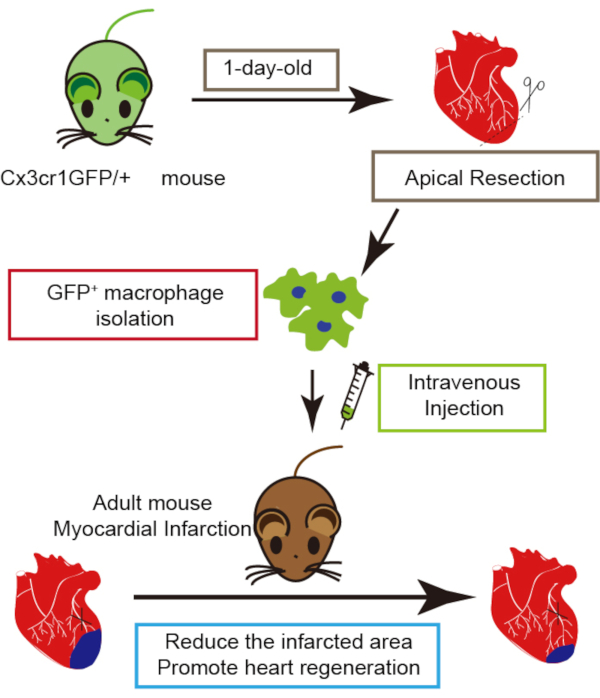
Рисунок 1:Схематическое изображение трансплантации макрофагов сердца новорожденных. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
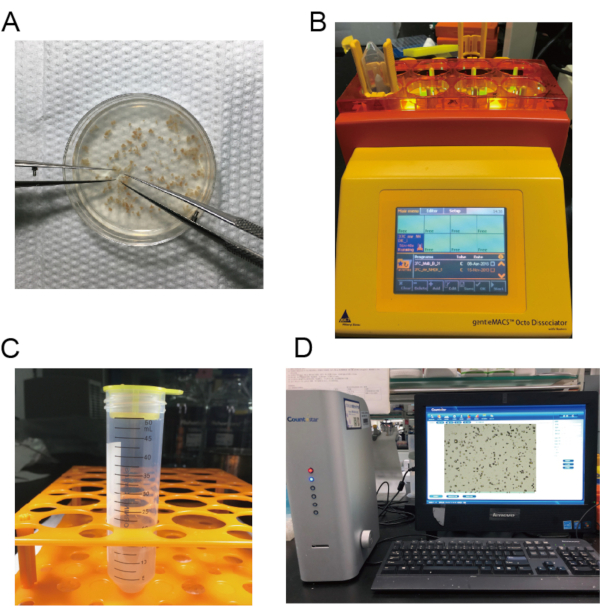
Рисунок 2:Изображения выделения макрофагов. А)Сердца разрезаются на мелкие кусочки. Б)Мышиные сердца диссоциированы. C)Суспензия фильтруется и переносится в центрифужную трубку объемом 15 мл. D)Рассчитано количество неонатальных сердечных макрофагов. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
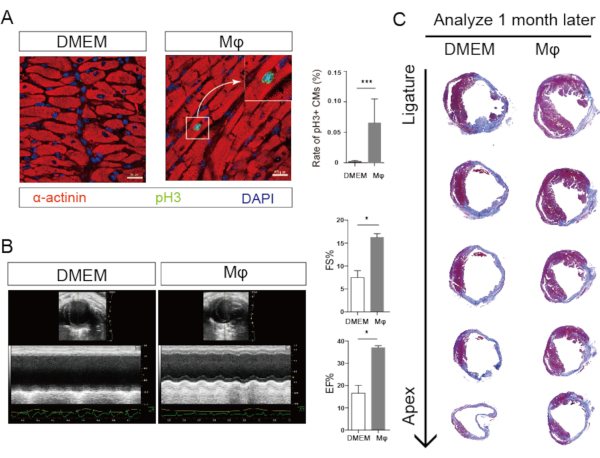
Рисунок 3:Трансплантация макрофагов сердца новорожденных способствует регенерации сердца взрослых. A) (слева) Иммунофлуоресцентные изображения показывают пролиферативные кардиомиоциты (стрелка, pH3 зеленый, α-актинин красный). (Справа) Статистический анализ показывает, что пролиферация кардиомиоцитов увеличивается после трансплантации макрофагов. B) (Слева) Изображения эхокардиограммы показывают сердечную функцию у взрослой мыши через 1 месяц после инфаркта миокарда. (Справа) Статистический анализ показывает, что функция сердца усиливается после трансплантации макрофагов. C)Окрашивание Массона показывает инфарктную область у взрослой мыши через 1 месяц после инфаркта миокарда. (Справа) Статистический анализ показывает, что инфарктная площадь уменьшается после трансплантации Mφ, макрофагов. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
Обсуждение
Здесь мы предлагаем эффективный подход к подготовке, приобретению и трансплантации неонатальных сердечных макрофагов для содействия регенерации сердца взрослых мышей.
Апикальная резекция – это простая и эффективная операция для стимуляции регенерации сердца. Мы оптимизировали детали апикальной резекции, чтобы обеспечить максимальную выживаемость животных, участвующих в операции10. Время анестезии не должно быть больше 3 минут, что приводит к смерти, вызванной гипотермией, или короче 2 минут, что может вызвать чрезмерное кровотечение во время операции. Стандартная апикальная резекция должна была ампутировать около 1,5 мм диаметром верхушечной ткани. Однако целью операции здесь была стимуляция обильной инфильтрации макрофагов в процессе регенерации сердца. Резекция диаметром менее 1,5 мм была приемлемой, поскольку она могла гарантировать максимальную выживаемость и эффективную рекрутмент макрофагов одновременно. Только мастерство оператора влияло на выживаемость, и оперированные мыши не могли пережить длительную продолжительность операции. Оператор должен завершить всю процедуру в течение 5 минут.
В нашем первом исследовании мы обнаружили, что острое воспаление способствует регенерации сердца новорожденных. Интрамиокардиальная микроинъекция иммуногенных частиц зимозана А в сердце неонатальной мыши может способствовать пролиферации кардиомиоцитов6. Недавно Molkentin et al. утверждали, что инфильтрация макрофагов, которая стимулируется внутрисердечной инъекцией зимозана А, клеточного мусора и замораживания / оттаивания убитых клеток, может способствовать восстановлению сердца, подтверждая, что острое воспаление и макрофаги необходимы для восстановления сердца, а не стволовые клетки, дифференцирующиеся в кардиомиоциты11. Sadek et al.5 сообщили, что макрофаги могут способствовать регенерации сердца новорожденных посредством ангиогенеза. Наше недавнее исследование показало, что инъекция неонатальных сердечных макрофагов может способствовать регенерации сердца взрослых и увеличить способность взрослой пролиферации кардиомиоцитов1,7. Трансплантация макрофагов сердца новорожденных может быть многообещающей стратегией для содействия регенерации сердца взрослых мышей. Здесь мы представляем протоколы, чтобы помочь большему количестве исследователей в разработке регенеративных приложений и изучении механизмов регенерации сердца.
Раскрытие информации
Отсутствие конфликта интересов.
Благодарности
Эта работа была поддержана Инновационным фондом медицинских наук Китайской академии медицинских наук (CIFMS, 2016-I2M-1-015), Национальным ключевым проектом исследований и разработок Китая (2019YFA0801500), Национальным фондом естественных наук Китая (NSFC: 81970243, 81770308), Пекинским фондом естественных наук (7172183, 7182140).
Материалы
| Name | Company | Catalog Number | Comments |
| Anti-mouse alpha actinin | Abcam | Ab9465 | |
| Anti-phospho-Histone H3 | Millipore | 06-570 | |
| Anti-rabbit Aurora B | Abcam | Ab239837 | |
| Anti-rabbit Ki67 | Abcam | Ab15580 | |
| gentleMACS Octo Dissociator | Miltenyi Bio Tech, Teterow, Germany | N/A | |
| Goat anti-mouse Alexa Fluor 555 | Invitrogen | A-21137 | |
| Goat anti-rabbit Alexa Fluor 488 | Invitrogen | A-11008 | |
| Neonatal Heart Dissociation Kit | Miltenyi Bio Tech, Teterow, Germany | 130-098-373 |
Ссылки
- Li, Y., et al. gp130 Controls Cardiomyocyte Proliferation and Heart Regeneration. Circulation. 142 (10), 967-982 (2020).
- Pei, J., et al. Hydrogen Sulfide Promotes Cardiomyocyte Proliferation and Heart Regeneration via ROS Scavenging. Oxidative Medicine and Cellular Longevity. , 1412696 (2020).
- Wang, Y., et al. Mydgf promotes Cardiomyocyte proliferation and Neonatal Heart regeneration. Theranostics. 10 (20), 9100-9112 (2020).
- Lavine, K. J., et al. Distinct macrophage lineages contribute to disparate patterns of cardiac recovery and remodeling in the neonatal and adult heart. Proceedings of the National Academy of Sciences of the United States of America. 111 (45), 16029-16034 (2014).
- Aurora, A. B., et al. Macrophages are required for neonatal heart regeneration. Journal of Clinical Investigation. 124 (3), 1382-1392 (2014).
- Han, C., et al. Acute inflammation stimulates a regenerative response in the neonatal mouse heart. Cell Research. 25 (10), 1137-1151 (2015).
- Li, Y., et al. Transplantation of murine neonatal cardiac macrophage improves adult cardiac repair. Cellular & Molecular Immunology. , (2020).
- Yue, Z., et al. PDGFR-β Signaling Regulates Cardiomyocyte Proliferation and Myocardial Regeneration. Cell Reports. 28 (4), 966-978 (2019).
- Wang, J., et al. A long noncoding RNA NR_045363 controls cardiomyocyte proliferation and cardiac repair. Journal of Molecular and Cellular Cardiology. 127, 105-114 (2019).
- Li, Y., et al. Achieving stable myocardial regeneration after apical resection in neonatal mice. Journal of Cellular and Molecular Medicine. 24 (11), 6500-6504 (2020).
- Vagnozzi, R. J., et al. An acute immune response underlies the benefit of cardiac stem cell therapy. Nature. 577 (7790), 405-409 (2020).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены