Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
Berechnung der Herzfrequenzvariabilität aus EKG-Daten von Jugendlichen mit Zerebralparese während aktiver Videospielsitzungen
In diesem Artikel
Zusammenfassung
Dieses Protokoll beschreibt eine Methode zur Berechnung der Herzfrequenzvariabilität (HRV) aus Elektrokardiogramm-Wellenformen (EKG). Wellenformen von kontinuierlichen Herzfrequenzaufnahmen (HR) während aktiver Videospielsitzungen (AVG) wurden verwendet, um die aerobe Leistung von Jugendlichen mit Zerebralparese (CP) zu messen.
Zusammenfassung
Ziel dieser Studie war es, eine Methode zur Berechnung der Herzfrequenzvariabilität (HRV) aus Elektrokardiogramm-Wellenformen (EKG) zu generieren. Die Wellenformen wurden von einem HR-Monitor aufgezeichnet, den Teilnehmer (Jugendliche mit Zerebralparese (CP)) während aktiver Videospielsitzungen (AVG) trugen. Die AVG-Sitzungen wurden entwickelt, um körperliche Aktivität und Fitness (aerobe Leistung) bei den Teilnehmern zu fördern. Ziel war es, die Machbarkeit von AVGs als Interventionsstrategie für physikalische Therapie (PT) zu bewerten. Die maximale HR (mHR) wurde für jeden Teilnehmer ermittelt und die Zielherzfrequenzzone (THRZ) wurde für jede der drei Übungsphasen in der 20 min AVG-Sitzung berechnet: (Aufwärmen bei 40-60% mHR, Konditionierung bei 60-80% mHR und Abkühlung bei 40-60% mHR). Jeder Teilnehmer spielte drei 20-Min-Spiele während der AVG-Session. Alle Spiele wurden auf einer Bank gespielt, weil viele Jugendliche mit CP nicht für längere Zeit stehen können. Jede Spielbedingung unterschied sich mit Teilnehmern, die nur Handsymbole, Hand- und Fußsymbole zusammen oder Fußsymbole nur zum Sammeln von Objekten verwenden. Das Ziel des Spiels (genannt KOLLECT) ist es, Objekte zu sammeln, um Punkte zu sammeln und Gefahren zu vermeiden, um keine Punkte zu verlieren. Gefahren wurden in den Aufwärm- und Abkühlphasen nur verwendet, um eine langsamere, kontrollierte Bewegung zu fördern, um die HR in der Zielherzfrequenzzone (THRZ) aufrechtzuerhalten. Es gab keine Gefahren in der Konditionierungsphase, um höhere Niveaus und intensivere körperliche Aktivität zu fördern. Analytische Methoden wurden verwendet, um HRV (ausgewählte Zeit-Domain- und Frequenz-Domain-Maßnahmen) aus EKG-Daten zu generieren, um aerobe Arbeitsbelastung zu untersuchen. Jüngste Anwendungen von HRV deuten darauf hin, dass kurzfristige Messungen (5 min Bouts) angemessen sind und dass HRV-Biofeedback dazu beitragen kann, die Symptome und die Lebensqualität in einer Vielzahl von gesundheitlichen Bedingungen zu verbessern. Obwohl HR eine gut akzeptierte klinische Maßnahme zur Untersuchung der aeroben Leistung und Intensität von PT-Interventionen ist, kann HRV Während aVG-Sitzungen Informationen über die Funktionen des autonomen Systems, die Erholung und Anpassung liefern.
Einleitung
Zerebralparese (CP) ist die häufigste körperliche Behinderung der Kindheit1. CP wird durch eine neurologische Beleidigung des sich entwickelnden Gehirns verursacht und ist mit motorischen Beeinträchtigungen wie Muskelschwäche, Spastik, Dekonditionierung und verminderter Motorkontrolle und Balanceverbunden 2,3. CP ist eine nicht-progressive Erkrankung, aber mit dem Alter werden Kinder weniger körperlich aktiv und sitzender im Vergleich zu ihren Altersgenossen mit typischer Entwicklung (TD) vor allem wegen der erhöhten Anforderungen an Wachstum an ihre kompromittierte neuromuskuläre und Muskel-Skelett-Systeme4.
Jugendliche mit CP erhalten in der Regel Physiotherapie (PT) Dienstleistungen zur Verbesserung der funktionellen Beweglichkeit und Förderung der körperlichen Aktivität und Fitness (z.B. Aerobe und Muskelausdauer)2. Oftmals gibt es nur begrenzten Zugriff auf PT-Dienste und Community-Ressourcen, um diese PT-Ziele zu erreichen und zu erhalten5,6. Aktive Videospiele (AVGs) können eine praktikable Strategie bei aktivitätsbasierten PT-Interventionen in Klinik-, Heim- oder Gemeinschaftseinstellungen7,8sein. Kommerzielle AVGs haben begrenzte Flexibilität, um das Spiel anzupassen und die spezifischen Bedürfnisse und PT-Ziele für Jugendliche mit CP9zu erfüllen. Allerdings bieten maßgeschneiderte AVGs flexible Spielparameter, um Jugendliche mit CP herauszufordern und gleichzeitig körperliche Aktivität und Fitness zu fördern10.
Unser Team hat ein maßgeschneidertes AVG (kollECT) entwickelt, um die Reaktionen von Jugendlichen auf Bewegung (z. B. körperliche Aktivität und aerobe Fitness) zu untersuchen. Das Spiel verwendet einen Bewegungssensor, um Jugendbewegungen während des Spiels zu verfolgen. Das Ziel des Spiels ist es, so viele Objekte wie möglich für eine hohe Punktzahl zu "sammeln" und die Gefahren zu vermeiden, um Punkte zu verlieren. Objekte können mit Hand- und/oder Fußsymbolen gesammelt werden, wie vom Therapeuten in den flexiblen Spielparametern festgelegt.
Das Entwerfen aktivitätsbasierter PT-Interventionen, die die Intensität der körperlichen Aktivität dosieren, um die aerobe Fitness zu fördern, ist für Jugendliche mit CP11von entscheidender Bedeutung. Benutzerdefinierte AVGs können eine effektive Strategie sein, um Intensität zu dosieren und Jugendliche in körperliche Aktivität zu engagieren, um Fitness zu fördern10. Herzfrequenz-Monitore (HR) werden häufig in der klinischen PT-Praxis verwendet, um aerobe Leistung und Aktivitätsintensität zu bestimmen. Daher werden HR-Monitore helfen, die Durchführbarkeit von AVGs bei der Dosierung der körperlichen Aktivitätsintensität zu bestimmen, um aerobe Fitness zu fördern9. EKG-Daten, die aus einem HR-Monitor generiert werden, können zur Berechnung der Herzfrequenzvariabilität (HRV) verwendet werden. Analytische Methoden wurden verwendet, um HRV aus EKG-Daten zu generieren, um aerobe Arbeitsbelastung zu untersuchen. Jüngste Anwendungen von HRV deuten darauf hin, dass kurzfristige Messungen (5 min Bouts) angemessen sind und dass HRV-Biofeedback dazu beitragen kann, die Symptome und die Lebensqualität in einer Vielzahl von gesundheitlichen Bedingungen zu verbessern32,33,34 . Die Anwendung kurzfristiger HRV-Maßnahmen ist ein geeignetes Mittel zur Beurteilung der Herz-Kreislauf-Funktion während AVG-Sitzungen. Da HRV aus dem R-R-Intervall eines EKG abgeleitet ist, haben wir ausgewählte Zeit-Domain- und Frequenz-Domain-Maßnahmen verwendet. Zeit-Domänen-Messung von HRV quantifiziert die Variablität in den Interbeat-Intervallen, die die Zeit zwischen aufeinanderfolgenden Herzschlägen darstellt. Wir verwendeten AVNN (durchschnittliches NN-Intervall), RMSSD (Wurzelmittelquadrat der aufeinanderfolgenden Unterschiede), SDNN (Standardabweichung des NN-Intervalls), NN50 (Anzahl der NN-Intervalle >50 ms) und PNN50 (Prozentsatz der NN-Intervalle). Frequenzbereichsmessungen schätzen die Verteilung der absoluten oder relativen Leistung in möglicherweise vier Frequenzbänder, die wir speziell auf zwei Frequenzbänder, Niederfrequenz-(LF)-Leistung und Hochfrequenzleistung (HF) zusammen mit dem LF/HF-Verhältnis angesprochen haben. Obwohl HR eine gut akzeptierte klinische Maßnahme ist, kann HRV nützlich sein, da es Informationen über autonome Systemfunktion, Wiederherstellung, Anpassung und eine Schätzung der aeroben Arbeitsbelastung während einer AVG-Sitzung28bereitstellt.
Ziel dieser Studie war es, die Durchführbarkeit der Anwendung von AVG-Strategien zur Förderung von körperlicher Aktivität und Fitness zu untersuchen. Ein zweiter Zweck bestand darin, das AVG-Datenerfassungsprotokoll und die Methodik zur Berechnung der HRV aus EKG-Daten, die über einen HR-Monitor gewonnen wurden, vorzustellen. Diese Maßnahmen und dieses Protokoll können sich für Ärzte als relevant erweisen, um PT-Interventionssitzungen zu überwachen und zu dosieren.
Protokoll
Die Zustimmung des Institutional Review Board wurde eingeholt. Alle Jugendlichen erteilten ihre schriftliche Zustimmung und die Eltern gaben vor der Teilnahme ihre Zustimmung.
1. AVG-Datenerfassungssitzungen
- Die AVG-Spielsitzung
- In dieser Studie, lassen Sie Jugendliche mit CP an einer AVG-Sitzung teilnehmen, die aus drei 20-min-Spielen besteht. Siehe Tabelle 5 für die demografische Jugend. Es wurde erwartet, dass insgesamt 30 Spiele gespielt werden; Allerdings wurden 29 Spiele absolviert, da ein Thema nur 2 Spiele in seiner AVG-Session spielte.
- Lassen Sie die Probanden während der gesamten Sitzung einen HR-Monitor tragen, um HR- und EKG-Antworten aufzuzeichnen.
- In der AVG-Session, lassen Sie Jugend spielen jede AVG, während auf einer Bank mit Füßen flach auf dem Boden und Knie und Hüften gebeugt auf 90 Grad (90/90 sitzen) für Haltungsunterstützung und Stabilität sitzen.
- Verwenden Sie die folgenden drei Spielbedingungen nur für Sammlungsobjekte: 1) Handsymbole; 2) Nur Fußsymbole; und 3) sowohl Hand- als auch Fußsymbole. Verwenden Sie eine ausgeglichene Reihenfolge zwischen Themen. Wählen Sie diese drei Bedingungen zu bestimmen, welche ist effektiver bei der Förderung der körperlichen Aktivität und Fitness und nicht zu anspruchsvoll, um frühe, unangemessene Müdigkeit verursachen.
HINWEIS: Jedes Spiel wurde mit den Phasen der Übung Rezept entwickelt: Aufwärmen, Konditionierung und Abkühlung. [Siehe Tabelle 1]. Darüber hinaus gab es eine Ruhephase, bevor das Spiel begann, die Baseline HR und eine Erholungsphase nach dem Spiel zu dokumentieren, um die Zeit zu dokumentieren, um zur Baseline HR zurückzukehren. - Erlauben Sie Probanden eine Ruhezeit zwischen den Spielen für HR, um auf das Basisniveau zurückzukehren.
- Berechnung von HRV aus EKG-Daten
- Organisieren Sie Daten in 5 min Zeitintervallen, um vergleichbare Daten für jede Phase zu gewährleisten. Daher wurden 6 Phasen für diese Berechnungen definiert: 1) Rest; 2) Aufwärmen; 3) Konditionierung 1 (erste 5 min); 4) Konditionierung 2 (zweite 5 min); 5) Cool-Down (5 min) und 6) Erholung. Die Aufteilung der Konditionierungsphase in zwei 5-Minuten-Phasen ermöglicht die Untersuchung der aeroben Leistung des Faches in kürzeren Intervallen, um Ermüdung aufgrund von Dekonditionierung 12 (Tabelle 4) zu berücksichtigen.
- Um HRV-Messungen für jedes Segment der Sitzung eines Subjekts richtig zu berechnen, führen Sie die R-Peak-Erkennung auf dem Roh-EKG-Signal12,13durch. Verwenden Sie das Rohsignal, um Manipulationen zu vermeiden, die die Daten verzerren könnten.
- Um die Daten zu verarbeiten, rufen Sie die Startzeiten jeder Aufzeichnungssitzung ab und konvertieren Sie aus 'datetime'-Variablen (MM/DD/YYYY HH:MM:SS). SS) auf Sekunden. Keine der Sitzungen trat über zwei Tage auf, sodass der MM/DD/YYYY-Teil während dieser Berechnungen ignoriert werden konnte. Erwerben Sie die Startzeit des Spiels von Interesse aus dem Timing-Tabelle, um jede Spielsitzung in der Elektrokardiogramm -Datei (EKG) zu finden; Diese Zeit wurde in Sekunden konvertiert, nachdem sie aus der Timing-Datei extrahiert wurde. Die Timing-Datei enthielt Startzeiten für jede Phase des Spiels sowie das Ende der Erholungsphase (Tabelle 2).
- Berechnen Sie die Ruhezeit als 5 min vor dem Spielstart und die Erholungsphase als 5 min nach dem Ende der Abklingphase. Sobald diese Zeiten erreicht wurden, erhalten Sie den Speicherort (S) der Spielphase von Interesse innerhalb der EKG-Datei durch die folgende Gleichung:
 (1)
(1)
wobei Phase entweder auf Ruhe, Warmup, Konditionierung 1, Konditionierung 2, Abklingzeit oder Erholung eingestellt ist; die Zeit wurde durch 1/Frequenz geteilt, um die EKG-Abtastrate zu berücksichtigen. Der HR-Monitor hatte eine Abtastrate von 250 Hz und enthielt daher alle 4 ms eine Kennzahl.- Ändern Sie diese Zahl, indem Sie die Abtastrate mit der ersten Eingabeaufforderung aus dem Peak_Detection.m-Programm ändern, um die Verwendung alternativer Aufzeichnungsgeräte zu berücksichtigen. Wählen Sie aus, mit welchem 5-min-Segment sie arbeiten möchten, während Sie das Spitzenerkennungsprogramm ausführen. Dies geschah über eine Aufforderung an den Benutzer. Stellen Sie die Endzeit nach der Startzeit auf 5 min und berücksichtigen Sie die Frequenz des Aufnahmegeräts.
- Nachdem der 5-min-Abschnitt ausgewählt wurde, berechnen Sie einen Schwellenwert für die Peak-Erkennung basierend auf der durchschnittlichen und Standardabweichung der Wellenform.
- Legen Sie
 den Schwellenwert als hoch, kann aber im Programm erhöht werden, wenn die Daten einheitlich sind, um die falsch-positive Erkennung von T-Peaks zu reduzieren, die höher als die entsprechenden R-Peaks sind. Beispiele für diese falsch positiven Ergebnisse sind in Abbildung 1zu sehen.
den Schwellenwert als hoch, kann aber im Programm erhöht werden, wenn die Daten einheitlich sind, um die falsch-positive Erkennung von T-Peaks zu reduzieren, die höher als die entsprechenden R-Peaks sind. Beispiele für diese falsch positiven Ergebnisse sind in Abbildung 1zu sehen. - Weisen Sie zusammen mit einer Mindesthöhe für die R-Spitze einen Mindestabstand zwischen den Spitzen zu, um die Erkennung falscher Spitzen um das gewünschte R zu minimieren. Stellen Sie diesen Wert auf 75, der 0,3 s zwischen Spitzen oder 200 Schlägen pro min (bpm) entspricht (dieser Wert ändert sich mit Frequenz). Der Wert von 200 bpm ist höher als jeder HR, den die Probanden in dieser Studie erreichen, und kann auf der Grundlage der untersuchten Bevölkerung geändert werden.
- Legen Sie
- Sobald der Schwellenwert berechnet wurde, lassen Sie das Programm durch die Wellenform laufen und versuchen, alle R es für RR-Intervall und HRV-Berechnungen zu unterscheiden. Generieren Sie ein vorläufiges Diagramm, damit der Benutzer es auf Unregelmäßigkeiten überprüfen kann, wie in Abbildung 1 oder Abbildung 2dargestellt.
- Korrigieren Sie diese Unregelmäßigkeiten manuell, indem Sie die Erkennungsvariable bearbeiten, die den Mikrovolt-Wert (-V) des Peak in Spalte 1 und die Position in der aktuellen Spielsitzung (s/0.004) in der zweiten Spalte enthält. In den meisten Fällen können die richtigen R-Spitzen leicht gefunden werden, indem Sie in die Problemposition zoomen, wie in Abbildung 1dargestellt. Viele Datensitzungen sind ziemlich einheitlich, wie in Abbildung 3 dargestellt, und erfordern daher nur wenige Korrekturen. Einige Fälle sind jedoch ziemlich chaotisch und erfordern mehr Zeit, um richtige R-Standorte zu überprüfen und zu erhalten.
- Wenn die Schwankungen in der Wellenform es übermäßig schwierig machen, einen Peak richtig zu lokalisieren, ignorieren Sie kleine Segmente von 1-2 s und führen ektopische Beats zu, die in HRV-Berechnungen nicht verwendet werden12.
- Nachdem die R es gefunden wurden, führen Sie das Programm HRV_Measures aus. Berechnen Sie rr-Intervalle zuerst, da sie die Grundlage der in dieser Studie verwendeten HRV-Kennzahlen sind12.
- Erhalten Sie eine Matrix von Intervallen und ignorieren Sie ein Intervall größer als 1,5 s (40 bpm), da die oben genannten ektopischen Beats aus den Berechnungen entfernt wurden. Speichern Sie diese RR-Intervalle für weitere Berechnungen und Überprüfungen von Daten. Verwenden Sie diese Intervalle, um das Wurzelmittelquadrat der aufeinanderfolgenden Unterschiede (RMSSD) mit der folgenden Gleichung zu berechnen:
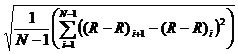 RMSSD = (2)
RMSSD = (2)
Wobei N = Anzahl der RR-Intervalle (R-R)i = Intervall zwischen benachbarten QRS Peaks (R-R)i+1 = Intervall zwischen nachfolgenden Peaks
- Erhalten Sie eine Matrix von Intervallen und ignorieren Sie ein Intervall größer als 1,5 s (40 bpm), da die oben genannten ektopischen Beats aus den Berechnungen entfernt wurden. Speichern Sie diese RR-Intervalle für weitere Berechnungen und Überprüfungen von Daten. Verwenden Sie diese Intervalle, um das Wurzelmittelquadrat der aufeinanderfolgenden Unterschiede (RMSSD) mit der folgenden Gleichung zu berechnen:
- Wählen Sie diese Variable, da sie sich in Intervallen von 1 min bis 24 h in der Länge13,14,15,16,17 als wirksam erwiesen hat und daher zur Beurteilung dieser 5 min verwendet werden kann. Intervalle in den Spielphasen. Zusammen mit RMSSD erhalten Sie die Standardabweichung der NN-Intervalle, um Änderungen der HR während der Phase14,16,18zu messen.
- Verwenden Sie die RR-Intervalle, um NN50 zu berechnen, die Anzahl der Intervalle, die sich vom vorherigen Intervall um mehr als 50 ms12 unterscheiden, die auch in Intervallen von einem min bis 24 h16,17,19verwendet wurde. 20,21.
- Berechnen Sie die Variable NN50 über eine einfache Zählfunktion, die überprüfte, ob die Differenz zwischen aufeinander folgenden RR-Intervalllängen größer als 50 ms war. Sobald NN50 auf diese Weise erhalten wurde, dividieren Sie durch die Gesamtzahl der Intervalle, um pNN50 zu berechnen, was der Prozentsatz der Intervalle, die sich um mehr als 50 ms unterscheiden. Diese Berechnung ermöglichte es, die gemessenen Daten zwischen Themen, Spielen und sogar Sitzungen unterschiedlicher Länge zu vergleichen, da es sich um eine einheitslose Variable13,14 , 16 , 17.
- Berechnen Sie die mittlere RR-Intervalllänge für jede Phase und jeden Gegenstand als separates HRV-Maß16,17,19,22,23,24. Verwenden Sie diese Kennzahl, um die durchschnittliche HR zu berechnen, indem Sie das mittlere RR-Intervall durch 60 s dividieren. Beide Maßnahmen sind leicht vergleichbar über Spielsitzungen, um den Trend der Aktivität des Themas zu beobachten16,17,19,22,23, 24.
- Nach der Berechnung dieser Kennzahlen berechnen Sie die Low Frequency and High Frequency Power Spectral Density (PSD) sowohl für das Roh-EKG des 5-min-Intervalls als auch für die RR-Intervallmatrix, indem Sie PSD von Fast-Fourier-Transformationen13,14 , 17 , 19 , 25. Alle diese Daten wurden dann in einer Tabelle gespeichert, ein Beispiel dafür ist in Tabelle 4dargestellt.
2. Erfassen Sie EKG-Daten vom Patienten
- Bereiten Sie den HR-Monitor Brustgurt und das Bluetooth-Modul für die Anwendung auf das Motiv vor.
- Stellen Sie sicher, dass das Bluetooth-Modul vollständig aufgeladen wurde (3 h) über die Ladestation.
- Schließen Sie das Modul über die Ladestation an den Datencomputer an und öffnen Sie das Konfigurationstool. Geben Sie einen Namen für Protokollierungszwecke ein.
- Wählen Sie das HR-Gerät aus, klicken Sie auf die Registerkarte Zeit und wählen Datum/Uhrzeit festlegen aus, um das Modul mit der richtigen Uhrzeit und dem richtigen Datum zu synchronisieren. Das Gerät kann nun aus der Ladestation entfernt werden.
- Befeuchten Sie die leitfähigen Bereiche (beige) auf dem HR-Monitor Brustgurt, indem Sie eine Hand in Wasser legen und die leitfähigen Bereiche reiben.
- Legen Sie das HR-Monitor-Bluetooth-Modul in den Brustgurt mit den leitfähigen Oberflächen des Moduls aufgereiht mit denen des Brustgurts: Es wird an Ort und Stelle klicken.
- Halten Sie die Taste am Modul gedrückt, bis die Lichter blinken. Das Modul ist jetzt eingeschaltet und nimmt auf.
- Tragen Sie den HR-Monitor-Brustgurt (mit Bluetooth-Modul) auf den Spieler auf, wobei das Modul an der linken Mittelachseilleslinie und dem Gurt knapp unter der Brustmuskulatur ausgerichtet ist. Sobald sie richtig positioniert ist, ziehen Sie das Gerät so an, dass es sich während der Sitzung nicht bewegt, aber für den Spieler nicht unangenehm ist.
- Erfassen Sie ein Signal und sehen Sie sich den Live-Feed an.
- Schließen Sie den Anschluss an den USB-Anschluss des Computers an, der zum Anzeigen der Daten verwendet wird.
- Öffnen Sie das Live View-Programm und geben Sie den Setup-Modus ein, indem Sie auf das Symbol mit Schraubenschlüssel und Schraubendreher klicken.
- Wählen Sie ggf. einen Player aus der Liste aus, oder fügen Sie ein neues Betreff mit der Schaltfläche Neu in der unteren linken Ecke des Bildschirms hinzu.
- Geben Sie für Identifikationszwecke (Name, Alter, Geschlecht, Größe, Gewicht) gewünschte Betreffinformationen ein.
- Klicken Sie auf die Registerkarte Hardware und wählen Sie den aktuellen Betreff aus.
- Klicken Sie unten auf der Registerkarte auf Zuweisen und wählen Sie das aktuelle Gerät aus (als 01 aufgeführt, wenn keine anderen Geräte vorhanden sind). Klicken Sie dann im Popup-Feld auf Zuweisen.
- Klicken Sie auf die Registerkarte Team. Markieren Sie das Motiv und klicken Sie dann auf die rechte Pfeiltaste, um den Spieler in Team Azu platzieren.
- Klicken Sie auf die Registerkarte Bereitstellung, und verschieben Sie dann das neu erstellte Team auf die erste Registerkarte.
- Öffnen Sie die Registerkarte Live-Modus, indem Sie auf das blaue WLAN-Symbol in der oberen linken Ecke klicken.
- Verwenden Sie die Registerkarte Live-Modus, um HR, Atemfrequenz und Körperhaltung des Motivs in Echtzeit zu überwachen.
HINWEIS: Signalstärke, Batterieleistung und Vertrauen der Maßnahmen können ebenfalls angezeigt werden. - Zeichnen Sie das genaue Timing (MM/DD/YYYY HH:MM:SS) des Anfangs und des Endes jeder Sitzung und Phase für die Verarbeitung auf.
- Laden Sie die EKG-Daten vom HR-Monitor herunter.
- Entfernen Sie den Gurt am Ende der Sitzung vom Player und entfernen Sie das Bluetooth-Modul aus dem Brustgurt.
- Legen Sie das Modul in die Ladestation und schließen Sie es an einen Computer an, auf dem das Softwareprogramm installiert ist.
- Öffnen Sie das Protokoll.
- Wählen Sie das Gerät aus dem Dropdown-Menü aus. Alle Sitzungen, die sich derzeit auf dem Gerät befinden, werden mit Datumsangaben und Uhrzeiten angezeigt.
- Deaktivieren Sie das Kontrollkästchen Standardspeicherort verwenden und einen neuen Speicherort auswählen.
- Klicken Sie auf Speichern. Anschließend wird ein Fortschrittsbalken angezeigt. Das Speichern kann je nach Sitzungsdauer bis zu einer Stunde dauern.
- Benennen Sie das Datum um, nachdem es gespeichert wurde.
3. Datenanalyse und Berechnung von Herzfrequenzvariabilitätsmaßnahmen
- Bereiten Sie Dateien für die Verarbeitung vor.
- Benennen Sie EKG-Dateien als 'KOLLECT_Subject_AVG4' (z. B. KOLLECT_01_AVG4.csv').
- Generieren Sie eine Timing-Tabelle im durch Kommas getrennten Variablenformat (.csv), um Timing-Daten während der Datenverarbeitung zu zeichnen. Ein Beispiel für das richtige Format finden Sie in Tabelle 1.
- Importieren Sie die Datums-/Uhrzeitdaten aus der CSV-Datei, und klicken Sie mit der rechten Maustaste auf den Namen der neu erstellten Variablen, und ändern Sie sie in"Timing.mat".
- Vorläufige R-Spitzenerkennung.
- Öffnen und ausführen Peak _ Detection . m.
- Geben Sie die Frequenz des EKG-Aufnahmegeräts ein, wenn das Programm dazu aufgefordert wird.
- Geben Sie die Playernummer für die zu analysierenden Daten ein, wenn Sie dazu aufgefordert werden.
HINWEIS: Einige Spieler haben das aktive Videospiel 4 (AVG4) nicht abgeschlossen und daher werden nur Spieler 1-10 für diese Studie verwendet. Andere Zahlen geben eine Fehlermeldung an. - Geben Sie die Nummer des zu analysierenden Spiels (1, 2 oder 3) ein, wenn Sie dazu aufgefordert werden.
- Geben Sie die zu analysierende Phase ein (Rest, Warmup (WU), Conditioning (Con), Rest oder Recovery).
- Geben Sie bei Bedarf einen Versatz in Minuten oder 0 für keinen Versatz ein.
- Wählen Sie das Vergrößerungswerkzeug aus, und wählen Sie einen Bereich des Diagramms aus, der ausgegeben wird, um ein Fenster mit einer Breite von etwa 2.000 (s/0,004) und einer Höhe zu erstellen, die die vollständige Wellenform anzeigt, wie in Abbildung 3dargestellt. Vergrößern oder herauszoomen, wenn das Fenster nicht einfach visuell überprüft werden kann.
- Überprüfen Sie das Diagramm visuell, um zu bewerten, ob die erkannten Spitzen korrekt beschriftet sind. Siehe Abbildung 1 zum Beispiel von falsch erkannten und verpassten Spitzen, die durch unregelmäßige EKG-Daten verursacht wurden ( Abbildung2).
- Peak-Korrektur
- Korrigieren Sie die falsch erkannten oder fehlenden Peaks, indem Sie die Erkennungsvariable lokalisieren und im Arbeitsbereich doppelklicken.
- Verwenden Sie das Werkzeug Datencursor auf dem Plot der EKG-Wellenform, um die x- und y-Koordinaten der falschen Peak zu erhalten; X (Zeit*Frequenz) ist die erste Spalte in Detection.mat und Y (Spannung) ist die zweite Spalte (Abbildung 3).
- Klicken Sie mit der rechten Maustaste auf das angezeigte Textfeld, und klicken Sie auf Cursoraktualisierungsfunktion auswählen.
- Wählen Sie TooltipUpdate.m aus dem Ordner aus, der die für diese Analyse verwendeten Dateien enthält. Dadurch kann die QuickInfo genauere Werte anzeigen.
- Wenn der Punkt ein falsch positives ist, entfernen Sie ihn aus dem Array, indem Sie auf seine Zeile in der Variable Detection.mat klicken und Control und die Minus-Taste drücken. Ein Beispiel für falsch positive Erkennung ist in Abbildung 3zu sehen.
- Bearbeiten Sie falsch markierte Spitzen, die an nicht markierte Spitzen angrenzen, wie die beiden T-Peaks zeigen, die in Abbildung 1als R markiert sind, indem Sie ihre Werte an die Werte des nicht markierten Peaks anpassen.
- Der Wert des verpassten Peaks kann mit dem Werkzeug Datencursor abgerufen werden.
- Fügen Sie der Erkennungzusätzliche Zeilen hinzu. Steuerung und Plus-Taste für Spitzen, die aufgrund niedriger Spannungsniveaus verpasst werden.
- Geben Sie die Werte in numerischer Reihenfolge ein, um negative Werte während des Berechnungsprozesses zu vermeiden (d. h. fügen Sie den Peak bei 11000 zwischen den Spitzen bei 10908 und 11167 hinzu) (Abbildung 5).
- Stellen Sie sicher, dass die Werte korrekt eingegeben werden, bevor Sie die vollständige Sitzung durchlaufen, da Zahlen gelegentlich abgeschnitten werden, wenn sie eingegeben werden.
- Wiederholen Sie Schritt 2.3, bis alle Spitzen überprüft und/oder korrigiert wurden.
HINWEIS: Einige Dateien weisen eine begrenzte Variabilität der Wellenformamplitude auf und sind schneller zu überprüfen, wie in Abbildung 4 zu sehen ist, während andere variabler sind und möglicherweise einen genaueren Zoom erfordern, um Spitzen während der visuellen Inspektion genau zu lokalisieren.
- Abrufen von HRV-Messberechnungen.
- Speichern Sie das ursprüngliche Plot, das aus Peak_Detection.m generiert wurde, um später darauf zu verweisen.
- Führen Sie HRV_Measures.m aus, um das korrekt beschriftete Diagramm zu generieren. Abbildung 6zeigt eine Stichprobe der korrigierten Daten .
- Ändern des Plottitels mithilfe von Einfügen | Titel im Plotfenster und Ändern in den gewünschten Titel.
- Überprüfen Sie das Fenster für die Ausgabe, die Anwendung benachrichtigt den Benutzer über den Speicherort falsch eingegebene Daten, wenn vorhanden ist.
- Speichern Sie die Variable mit dem Namen Intervall.
- Öffnen Sie die Variable HRV aus dem Arbeitsbereichsfenster, um mittelwertigen RR (ms), Average HR (bpm), RMSSD (ms), SDNN (ms), NN50 (Count), pNN50 (%), low frequency (LF)/ High Frequency (HF) (ECG), LF/HF RR, Low Frequency Power RR und High Frequency Power (RR)) anzuzeigen. Speichern Sie die h-Werte dieser Variablen in einer Tabelle, wie sie in Tabelle 4dargestellt ist.
- Wiederholen Sie die Abschnitte 3.2 - 3.4 für alle anderen Segmente, Sitzungen und Themen, die analysiert werden müssen.
Ergebnisse
Diese Methode liefert Daten zur Analyse der Auswirkungen einer neu entwickelten Methode auf die Herzfrequenzvariabilität (HRV) des Themas. Dazu wird der R-Teil der QRS-Wellenform der EKG-Daten eines Subjekts, wie in Abbildung 6dargestellt, lokalisiert und daraus verschiedene HRV-Werte berechnet. Wenn der PERSONALmonitor ordnungsgemäß mit dem Betreffenden in Kontakt tritt, werden die Daten einheitlich sein, was den Bedarf an Korrekturen erheblich verringert...
Diskussion
Zehn Jugendliche mit CP nahmen an dieser Studie teil (Mittelwert + SD) [ Alter (Jahre) = 15,53 x 3,57 ; Höhe (cm) 154,8 x 12,6; Gewicht (kg) 50,69 x 11,1; Body-Mass-Index (BMI) 50,46 x 29,2; mHR 9 bpm) = 186,8 x 12,4]. Siehe Tabelle 5 für patienten demografie.
Es gibt einige Überlegungen für den Einsatz von HR-Monitoren und die damit verbundenen Maßnahmen von HR und HRV, die sich auf Modifikationen und Fehlerbehebung beziehen. Zwei Fragen, die offensichtlich sind, unabhä...
Offenlegungen
Zu diesem Zeitpunkt haben die Autoren (CL und PAS) nichts zu verraten. Dr. O'Neil ist Mitbegründer von enAbleGames, LLC und Kollect ist eines der Spiele, die von diesem webbasierten Unternehmen angeboten werden. enAbleGames befindet sich in der Phase der Spieleentwicklung und ist derzeit kein öffentliches Unternehmen (www.enAbleGames.com).
Danksagungen
Die Autoren danken den Teilnehmern und ihren Familien für ihre Zeit und Mühe, die sie für die Teilnahme an der Studie aufgewendet haben. Die Autoren würdigen dr. Yichuan Liu und Dr. Hasan Ayaz für ihre Unterstützung bei der Zeitberechnung der PERSONALüberwachung und Dr. Paul Diefenbach bei der Entwicklung der SOFTWARE KOLLECT Active Video Gaming. Die Finanzierung dieser Arbeit wurde von coulter Foundation Grants #00006143 (O'Neil; Diefenbach, PIs) und #00008819 (O'Neil; Diefenbach, PIs).
Materialien
| Name | Company | Catalog Number | Comments |
| BioHarness Bluetooth Module (Electronics sensor) | Zephyr | 9800.0189 | Detects Heart Rate, Resiration Rate, Posture, and Skin Temperature. |
| BioHarness Chest Strap | Zephyr | 9600.0189, 9600.0190 | Sizes Small XS-M, Large M-XL |
| BioHarness Charge Cradle & USB Cable | Zephyr | 9600.0257 | Used to Transfer Data from the Module to a Computer for Analysis. |
| BioHarness Echo Gateway | Zephyr | 9600.0254 | Allows for Realtime Viewing of Subject's Heart Rate. |
| MATLAB R2016a | Mathworks | 1.7.0_.60 | Used for All Programming. |
Referenzen
- Winter, S., Autry, A., Boyle, C., Yeargin-Allsopp, M. Trends in the prevalence of cerebral palsy in a population-based study. Pediatrics. 110 (6), 1220-1225 (2002).
- Fowler, E., et al. Promotion of physical fitness and prevention of secondary conditions for children with cerebral palsy: Section on Pediatrics Research Summit Proceedings. Physical Therapy. 87 (11), 1495-1510 (2007).
- Rosenbaum, P., Paneth, N., Leviton, A., Goldstein, M., Bax, M. A report: The definition and classification of cerebral palsy: April 2006. Developmental Medicine & Child Neurology. 49 (s109), 8-14 (2007).
- Hanna, S., et al. Stability and decline in gross motor function among children and youth with cerebral palsy aged 2 to 21 years. Developmental Medicine & Child Neurology. 51 (4), 295-302 (2009).
- Rimmer, J., Rowland, J. Health promotion for people with disabilities: Implications for empowering the person and promoting disability-friendly environments. American Journal of Lifestyle Medicine. 2 (5), 409-420 (2008).
- Feehan, K., et al. Factors influencing physical activity in children and youth with special health care needs: A pilot study. International Journal of Pediatrics. , (2012).
- Fehlings, D., Switzer, L., Findlay, B., Knights, S. Interactive computer play as motor therapy for individuals with cerebral palsy. Seminars in Pediatric Neurology. 20 (2), 127-138 (2013).
- Sandlund, M., Dock, K., Hager, C., Waterworth, E. Motion interactive video games in home training for children with cerebral palsy: parents’ perceptions. Disability & Rehabilitation. 34 (11), 925-933 (2012).
- Howcroft, J., et al. Active video game play in children with cerebral palsy: Potential for physical activity promotion and rehabilitation therapies. Archives of Physical Medicine and Rehabilitation. 93 (8), 1448-1456 (2012).
- Bilde, P., Kliim-Due, M., Rasmussen, B., Petersen, L., Petersen, T., Nielsen, J. Individualized, home-based interactive training of cerebral palsy children delivered through the Internet. BMC Neurology. 11, 32 (2011).
- Kolobe, T., et al. Research Summitt III proceedings on dosing in children with an injured brain or cerebral palsy. Physical Therapy. 94 (7), 907-920 (2014).
- Schipke, J., Pelzer, M., Arnold, G. Effect of respiration rate on short-term heart rate variability. Journal of Clinical and Basic Cardiology. 2 (1), 92-95 (1999).
- Ernst, G. Heart rate variability. Heart Rate Variability. , 1-336 (2014).
- Francis, J., et al. Association between symptoms of depression and anxiety with heart rate variability in patients with implantable cardioverter defibrillators. Psychosomatic Medicine. 71 (8), 821-827 (2009).
- Mendes, R., et al. Is applying the same exercise-based inpatient program to normal and reduced left ventricular function patients the best strategy after coronary surgery? A focus on autonomic cardiac response. Disability and Rehabilitation: An International Multidisciplinary Journal. 36 (2), 155-162 (2014).
- Muralikrishnan, K., Balakrishnan, B., Balasubramanian, K., Visnegarawla, F. Measurement of the effect of Isha Yoga on cardiac autonomic nervous system using short-term heart rate variability. Journal of Ayurveda and Integrative Medicine. 33 (2), 279-283 (2012).
- Yadav, R. K., Gupta, R., Deepak, K. K. A pilot study on short term heart rate variability & its correlation with disease activity in Indian patients with rheumatoid arthritis. Indian Journal of Medical Research. 136 (4), 593-598 (2012).
- Thuraisingham, R. A. Preprocessing RR interval time series for heart rate variability analysis and estimates of standard deviation of RR intervals. Computer Methods and Programs in Biomedicine. 83 (1), 78-82 (2006).
- Alamili, M., Rosenberg, J., Gögenur, I. Day-night variation in heart rate variability changes induced by endotoxaemia in healthy volunteers. Acta Anaesthesiologica Scandinavica. 59 (4), 457-464 (2015).
- Pal, G., et al. Preference for salt contributes to sympathovagal imbalance in the genesis of prehypertension. European Journal of Clinical Nutrition. 67 (6), 586-591 (2013).
- Telles, S., Raghavendra, B. R., Naveen, K. V., Manjunath, N. K., Kumar, S., Subramanya, P. Changes in autonomic variables following two meditative states described in yoga texts. Journal of Alternative and Complementary Medicine. 19 (1), 35-42 (2013).
- Kičmerová, D. . Methods for Detection and Classification in ECG Analysis. Doctoral thesis. , (2009).
- Murai, K., Hayashi, Y. Evaluation of mental workload for ship handling using physiological indices. , 604-608 (2009).
- Taelman, J., Vandeput, S., Spaepen, A., Van Huffel, S. Influence of mental stress on heart rate and heart rate variability. Heart. 29 (1), 1366-1369 (2009).
- Durantin, G., Gagnon, J. F., Tremblay, S., Dehais, F. Using near infrared spectroscopy and heart rate variability to detect mental overload. Behavioural Brain Research. 259, 16-23 (2014).
- Buchheit, M. Monitoring training status with HR measures: Do all roads lead to Rome?. Frontiers in Physiology. 5, (2014).
- Achten, J., Jeukendrup, A. Heart rate monitoring: Applications and limitations. Sports Medicine. 33 (8), 517-538 (2012).
- Amichai, T., Katz-Leurer, M. Heart rate variability with cerebral palsy: Review of literature and meta-analysis. NeuroRehabilitation. 35, 113-122 (2014).
- Billman, G., Haikuri, H., Sacha, J., Trimmel, K. An introduction to heart rate variability: Methodological considerations and clinical applications. Frontiers in Physiology. 6, (2015).
- Beffara, B., Bret, A., Vermeulen, N., Mermillod, M. Resting high frequency heart rate variability selectively predicts cooperative behavior. Physiology & Behavior. 164, 417-428 (2016).
- Fogt, D., Cooper, P., Freeman, C., Kalns, J., Cooke, W. Heart rate variability to assess combat readiness. Military Medicine. 174, 491-495 (2009).
- Kerppers, I. L., Arisawa, E. A. L., Oliveira, L. V. F., Sarmpaio, L. M. M., Oliverira, C. S. Heart rate variability in individual with cerebral palsy. Archives of Medical Science. 5, 45-50 (2009).
- Giggins, O. M., Persson, U. M., Caulfield, B. Biofeedback in Rehabilitation. Journal of Neuroengineering and Rehabilitation. 10, (2013).
- Shaffer, F., Ginsberg, J. P. An overview of heart rate variability metrics and norms. Frontiers in Public Health. 5, 258 (2017).
- Shaffer, F., McCarty, R., Zeir, C. L. A healthy heart is not a metronome: an integrative review of the heart’s anatomy and heart rate variability. Frontiers in Psychology. 5, 1040 (2014).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten