19.9 : Phase Diagram
The phase of a given substance depends on the pressure and temperature. Thus, plots of pressure versus temperature showing the phase in each region provide considerable insights into the thermal properties of substances. Such plots are known as phase diagrams. For instance, in the phase diagram for water (Figure 1), the solid curve boundaries between the phases indicate phase transitions (i.e., temperatures and pressures at which the phases coexist).
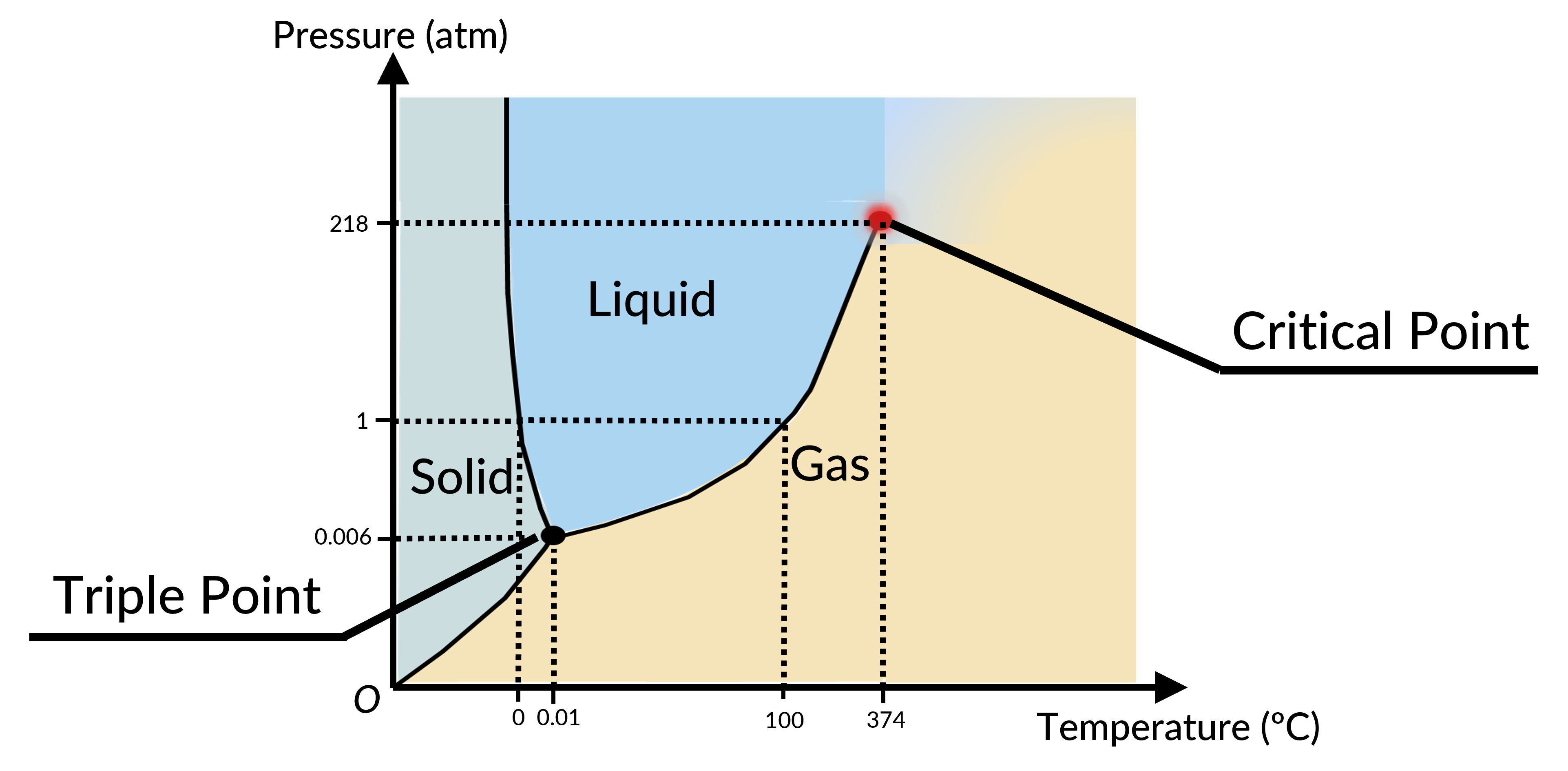
As the pressure increases, the boiling temperature of water rises gradually to 374 °C at a pressure of 218 atm. This can be demonstrated in a pressure cooker, which cooks food faster than an open pot, because the water can exist as a liquid at temperatures greater than 100 °C without all boiling away. The boiling point curve ends at a certain point called the critical point, the temperature above which the liquid and gas phases cannot be distinguished; the substance is called a supercritical fluid. At a sufficiently high pressure above the critical point, a gas has the density of a liquid but does not condense. The pressure at this critical point is known as the critical pressure. Carbon dioxide, for example, is supercritical at all temperatures above 31.0 °C, the point at which all three phases exist in equilibrium. For water, the triple point occurs at 273.16 K (0.01 °C) and 611.2 Pa; this is a more accurate calibration temperature than the melting point of water at 1.00 atm, or 273.15 K (0.0 °C).
Bölümden 19:

Now Playing
19.9 : Phase Diagram
Gazların Kinetik Teorisi
5.7K Görüntüleme Sayısı

19.1 : Durum Denklemi
Gazların Kinetik Teorisi
1.6K Görüntüleme Sayısı

19.2 : İdeal Gaz Denklemi
Gazların Kinetik Teorisi
6.3K Görüntüleme Sayısı

19.3 : Van der Waals Denklemi
Gazların Kinetik Teorisi
3.7K Görüntüleme Sayısı

19.4 : pV Diyagramları
Gazların Kinetik Teorisi
3.9K Görüntüleme Sayısı

19.5 : İdeal Bir Gazın Kinetik Teorisi
Gazların Kinetik Teorisi
3.2K Görüntüleme Sayısı

19.6 : Moleküler Kinetik Enerji
Gazların Kinetik Teorisi
4.8K Görüntüleme Sayısı

19.7 : Moleküler Hızların Dağılımı
Gazların Kinetik Teorisi
3.6K Görüntüleme Sayısı

19.8 : Maxwell-Boltzmann Dağılımı: Problem Çözme
Gazların Kinetik Teorisi
1.3K Görüntüleme Sayısı

19.10 : Ortalama boş yol ve Ortalama boş zaman
Gazların Kinetik Teorisi
3.1K Görüntüleme Sayısı

19.11 : Isı Kapasitesi: Problem Çözme
Gazların Kinetik Teorisi
471 Görüntüleme Sayısı

19.12 : Dalton'un Kısmi Basınç Yasası
Gazların Kinetik Teorisi
1.2K Görüntüleme Sayısı

19.13 : Gazların Kaçış Hızları
Gazların Kinetik Teorisi
868 Görüntüleme Sayısı
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır