Method Article
Mikro-kanallar tarafından Distinctive Kılcal Eylem Bone gibi şablonları Büyük Kemikli Defekt Restorasyon Hücreleri İşe Alım geliştirin edebilirsiniz
Bu Makalede
Özet
A step-by-step generic process to create a bone-like template with engineered micro-channels is presented. High absorption and retention capabilities of the template are demonstrated by capillary action via micro-channels.
Özet
Iyi dağıtılmış ve kalıcı bir şekilde yerleştirilen bir şablonla bağlanmıştır, aktif, gelişen hücre popülasyonu olmadan olağanüstü bir kemik yenilenmesi oluşmaz. Geleneksel şablonlar sayesinde, derin şablonlar içinde hücre infiltrasyonu, dağıtım ve yaşanılan eksikliği iç mikro kanallar sonuçların olmaması. Bu nedenle, mikro kanallı bir çok gözenekli ve düzgün birbirine trabeküler kemik gibi şablon (biyojenik mikroçevresinin şablon; KİT) bu engelleri gidermek için geliştirilmiştir. Roman BMT yenilikçi konseptler (kılcal eylem) tarafından oluşturulan ve bir sünger-şablon kaplama tekniği ile imal edilmiştir. Birbirine bağlı birincil gözenekler (300-400 um) üzerinde trabeküler kemik gözenekleri her trabekülde içinde mikro-kanallar (25-70 um) ve nanopores (100-400 nm) taklit: BMT birçok yapısal bileşenden oluşur Hücreler demirlemek için izin yüzey. Ayrıca, BMT sim olması mekanik test çalışması ile belgelenmiştirİnsan trabeküler kemik (~ 3.8 MPa) 12 kişilerce ilar mekanik dayanım özellikleri.
BMT köprü şekillidir (Π) şablon (3 cm yükseklik ve 4 cm boyunda) boyunca yüksek emilim, tutma, ve hücrelerin yerleşime sergilemiştir. Başlangıçta olan hücreler hemen hücre ortamına BMT nin kılcal hareketi ile diğer ucunda (10 cm mesafe) harekete şablonları bir ucunda içine ekildi. 4 saat sonra, hücreler, homojen bütün kemik iliği işgal normal hücresel davranış sergilemiştir. Kılcal eylem medya ve BMT boyunca dağılımı (aktif göç) içinde süspanse hücrelerin infiltrasyonu oluşturdu. BMT bu yetenekleri gözlenen, biz BMTS fizyolojik koşullar altında çevresinden kemik iliği hücreleri, büyüme faktörleri ve besin absorbe edecek tasarlanır.
BMT hızlı infiltrasyon, homojen dağılımı ve inhabita aracılığıyla güncel sınırlamalar çözebilirBüyük, hacimsel şablonlar hücrelerin nce masif iskelet kusurları onarmak için.
Giriş
The ultimate goal of bone tissue engineering with synthetic constructs is the incorporation of the constructs into the host bone, repopulation of the constructs with host cells, and reconstitution of gas and body fluid exchanges to restore normal bone function. Considerable research has been reported over the last decade in the use of polymeric and ceramic biomaterials for producing scaffolds1,2. However, the ideal material and fabrication technique for optimal bone tissue regeneration has yet to be identified. In addition, there is an overall lack of success in bringing these technologies to the clinic, especially for the reconstruction and restoration of large bone defects. Therefore, restoring critical sized bony defects still remains a clinical challenge1-5.
Ideally, the scaffolds for bone tissue regeneration should exhibit biocompatibility without causing inflammatory responses or foreign body/toxic reactions, have closely matched mechanical properties when compared to those of native bone, and possess a mechanism to allow diffusion and/or transport of ions and nutrients. Strong bonding with the host bone, dynamic bone growth, vascular ingrowth, and biodegradation of the scaffolds are equally desirable. Although the use of biodegradable polymer scaffolds has exhibited progress in terms of tissue ingrowth, there are controversies over their use for bone regeneration.
Notwithstanding these extensive efforts, the highly organized structural synthetic constructs still have limited potential in overcoming the obstacle of passive cell penetration. Most of these approaches have resulted in the in vitro tissue ingrowth with cross-sections of less than a few µm to several mm from the external surface, an incomplete integration with host bone, and only partial bone regeneration in vivo6,7. The pioneering cells do not migrate deeply into the constructs because of the lack of an initial force that pulls them inside before cell colonization begins. Consequently, cell colonization strictly occurs at the scaffold periphery, becoming an obstruction from the periphery to the center of the scaffold. Thus, the diffusion of oxygen and nutrients into the inner parts of the templates becomes limited8. Therefore, it is clear that the architecture of the scaffolds (pore size, porosity, interconnectivity, and permeability) that affect the transport and diffusion of substances throughout the scaffolds is critical for achieving well-distributed cell proliferation and differentiation9,10. Although calcium phosphates have been used in the past for scaffold fabrication, different processes and procedures have often resulted in calcium phosphate scaffolds with varying architectures. Thus, the selection of the manufacturing process becomes important in dictating the scaffold architecture needed for successful bone tissue regeneration.
In conclusion, there are still two major shortcomings of bone tissue engineering that need to be addressed: the initial cell recruitment into the template prior to cell attachment and colonization and the quality of substance flow both into and out of the template.
Protokol
Şablon olarak 1. Poliüretan (PU) Sünger Hazırlanması
- Birbirine gözenekleri içeren hidroksiapatit üretmek için şablonlar PU sünger kullanın. Şablon çubukların oluşumu gibi trabeküller içinde mikro-kanallar oluşumunda temel trabekülleri sağlamak için her sünger kullanın.
- Kes ve uzunluğu genişliği x 1.5 cm x 5 cm yüksekliğinde 3,5 cm boyutlarında 2 köprü şekiller halinde (inç başına gözenekler) süngerler 80 ppi kırpın.
Not: boyutları ve şekilleri seçilebilir istenen birincil gözenek büyüklüğüne göre: 100 ppi, 80 ppi ve 60 ppi. - % 4'lük bir 100 ml olun (ağırlık / hacim), bir 150 ml beher kullanarak NaOH solüsyonu; Daha sonra batırmak ve hazırlanan süngerler tamamen sırılsıklam kadar sıkın.
- Iliklerine sonra ultrasonikatör (42 kHz) olarak sünger ile beher yerleştirin.
- Ultrasonik yüzey özelliklerini değiştirmek için ısı olmadan 15-20 dakika süreyle PU sünger ön davranın.
- Damıtılmış ile durulayın5-10 dakika için su. Durulama ederken, sünger sıkmak ve onlara sünger içinde kalan NaOH kaldırmak için 5 ila 7 kez genişletilmesine izin verir.
- Aşırı su çıkarmak için kağıt havlu ile süngerler sıkıştırın; Daha sonra 60-80 ° C'de bir fırında kurutulur.
Kaplama 2. Hidroksiapatit (HA) Sivi Hazırlık
- HA bulamacın yapmadan önce, bir manyetik karıştırma çubuğu ile bir cam kabın ağırlığı ölçülür. Bu ölçüm, toz / sıvı oranının hesaplanmasında kullanılır.
- Nano boyutlu HA tozu 10 gr ölçün.
- 50 ml'lik cam kaba, damıtılmış su 20 ml ekleyin. 120-140 ° C ve heyecan sıcak plaka manyetik karıştırıcı kullanılarak ısı.
- 300-400 rpm'de karıştırılırken distile suya toz başına polivinil alkol (PVA) (89,000-98,000 MW) 0,3 g (ağırlık / ağırlık% 3) ilave edilir.
- PVA tamamen çözülene kadar karıştırın. Çözelti PVA tam dağılmasından sonra açık olmalıdır.
- O çevirin400-500 rpm'de karıştırılırken ff ısı ve sodyum karboksimetil selüloz (CMC) toz (ultra düşük viskozite) 0.1 g (ağ / ağ% 1) ekleyin. Çözelti PVA tam dağılmasından sonra açık olmalıdır.
- CMC tamamen çözülene kadar karıştırın ve oda sıcaklığına kadar soğumaya.
- 300-400 rpm'de karıştırılırken bir toz başına amonyum poliakrilat dispersant 0.3 g (% 3 w / w) eklenir. Tamamen çözülene kadar karıştırın.
- 300-400 rpm'de karıştırılırken tozun ortalama gliserin, 0.2 g (% 2 w / w) eklenir. Tamamen çözülene kadar karıştırın.
- Yavaş yavaş 600-900 rpm'de karıştırılırken çözelti içine HA, tozu dağıtmak ve 5 dakika boyunca karıştırmaya devam edin.
- HA tozunun herhangi bir topaklanma dağılmasını sağlamak için ultrasonikatör kullanılarak 5 dakika sonikasyon.
- 90-100 ° C sıcaklıkta 600-900 rpm ve sıcaklıkta karıştırılırken karışım içine damıtılmış su ilave bir 5 ml ekleyin.
- Ord 90-100 ° C'de 600-800 rpm'de bir manyetik karıştırıcı kullanılarak karıştırıldıktan tutuner suyun buharlaşması için.
- 1.75-1.8 ait bir toz / sıvı oranı elde edilene kadar zaman zaman cam kaba ve bu karışım dahil olmak üzere bütün ağırlığı ölçülür.
- Toz / sıvı oranının biçimlendirme, toz, reaktifler ve su eksi kapta karıştırıcı (2,1) 'nin ağırlığına, ve eksi HA tozu dahil olmak üzere, karışımı (2,14)' nin toplam ağırlığına göre tozun ağırlığı bölmek (2.2).
Not: Örneğin: (toz, reaktifler, ve su da dahil olmak üzere tüm karışım) 49,05 g ise, B (karıştırıcı ile beher) 33.5 g ve daha sonra C (HA tozu) 10 g'dır.
C / (ABC) = 10 / (49.05-33.5-10) = 1,80 - Bulamaç kaplama için kullanmadan önce oda sıcaklığına kadar soğumasını bekleyin.
3. HA kaplama, Kurutma ve Sinterleme
- Coat bulamaç kadar paslanmaz spatula ile HA kaplama bulamacı ile hazırlanan PU sünger homojen bir cam plaka üzerine PU sünger boyunca dağıtılır.
Not: Fazla leke ayrılmasından sonrary, gözeneklerin bazıları hala yüksek olması nedeniyle bulamaç viskozite bulamaç ile tıkanmış olabilir. - Hafif, birleştiricisi, tekdüzelik ve açık gözenekleri sağlamak bir hava kompresörü kullanarak HA kaplı şablonları darbe için. Bu işlem, homojen bir poliüretan sünger şablonları iç ve dış yüzeyleri üzerinde hem de kaplanmış olmasını sağlar.
Not: a homojen bir kaplama elde değilse, HA kaplanmış şablon sinterleme işlemi sırasında çökecektir ve düşük mekanik gücü nedeniyle işleme sırasında da çatlayabilir. Buna ek olarak, homojen bir kaplama trabeküller içinde mikro-kanallar oluşturmak önemlidir. - Yumuşak bir hava sirkülasyonu ile soğutma koşulları altında 5 saat (20-25 ° C) en az HA kaplanmış şablon kurutun. Bununla birlikte, şablonun boyutuna göre kurutma süresi uzatılabilir.
Not: Kuruduktan sonra, HA kaplı şablonlar genellikle her boyutta yaklaşık% 8 ile% 10 küçülecek. - Kurutma işleminden sonra, HA yerleştirinBir alümina pota üzerine kaplanmış şablonlar. Sonra, bir yüksek sıcaklık fırınında koyun ve aşağıdaki 8 adım sinterleme profili kullanın.
- Isı 2 ° C / dakika kadar 230 ° C.
- Grup 1 ° C / dakika kadar 280 ° C.
- 400 ° C'ye kadar 0,5 ° C / dakika ısıtın.
- Grup 3 ° C / dakika kadar 600 ° C. 1 saat boyunca 600 ° C'de tutun.
- Isı 5 ° C / dakika 1230 ° C'ye kadar. 3 saat boyunca 1230 ° C tutun.
- Oda sıcaklığına kadar soğuması 5 ° C / dak.
Not: Sinterleme daha yaklaşık% 22 HA kaplı sünger şablonları küçüleceğini - Her boyutta% 25.
Şablon içine Hücreleri 4. sızmaları ve inhabitancy
- % 5 CO2 içeren nemli bir atmosferde 37 ° C'de% 10 fetal sığır serumu (FBS) ve% 1 antibiyotik (streptomisin ve penisilin) ile desteklenmiş α-MEM oluşan olmayan bir osteojenik ortam içinde kültür öncesi osteoblastik MC3T3 hücreleri, .
- 10 ml ilave edilirBir 6-çukurlu plaka içinde tek bir kuyuya 2 x 10 6 hücre yoğunluğunda, bir hücre süspansiyonu.
- 6-çukurlu plakaya dikey olarak 3 cm x 4 cm x 1 cm köprüsü şeklinde bir şablon yerleştirin. Bitişik boş kuyuya hücre süspansiyonu içeren plaka içine şablon ve diğer bacağın bir bacak koyun.
- Şablon 10 dakika boyunca hücre süspansiyonu absorbe izin verin.
- Bundan sonra başlangıçta hücre süspansiyonu ile doluydu kuyuya medya 5 ml ekleyin.
- 7 gün geçtikten kadar her 2 veya 3 gün her iki kuyulardan orta yenileyin.
- Hematoksilen ve eozin boyama 11 hücre hareketliliği etkinliğini belirlemek.
- 20-30 dakika% 100 EtOH içinde daldırarak hücreleri ve iskele sabitleyin.
- 1-2 dakika boyunca, Hematoksilin ile leke.
- İki kez 1-2 dakika distile su ile durulayın.
- Daha sonra, 70% içine daldırma ile 95%, 1-2 dakika her biri için, sonra% 100 EtOH kurutmak.
- 20-30 saniye Eosin ile Leke.
- İki kez 12 dakika süreyle distile su ile durulayın.
- 1-2 dakika her biri için,% 70 içine daldırma ile 80%, 90%, 100%, EtOH kurutmak.
- Kesit ve görüntüleme için bir akrilik reçine, skafoldu gömün.
- 3- [4,5-dimetiltiazol-2-il] -2,5-difenil tetrazolyum bromid (MTT) hücre canlılığı deneyi ve Canlı / ölü deneyi (canlı / ölü hücre boyama kiti MPTP) zaman noktaları ile hücre canlılığını belirlemek Gün 3 ve 7 11.
Not: Kemik benzeri şablon fabrikasyon protokollerinin düzeni "Temsilcisi Sonuçlar" oturumunda temsil edilmektedir.
Sonuçlar
BMT genel yapısı trabeküler kemik gibi iç yapıları ile benzersiz bir üç boyutlu bir şablon sergiler. BMT makro gözenekler, mikro kanallar, ve nano-gözenekler içermektedir. Temizle tamamen bağlantılı makro gözeneklerin konfigürasyonları (320 um ortalama boyutlu), mikro kanallar (50 um ortalama çap) ve nano-gözenekler (100 nm ortalama boyutlu) bir tarama elektron mikroskobu ile doğrulanmıştır (EVO-40; ZEISS) yanı sıra, mikro-tomografi vasıtasıyla.
Şekil 1 BMT oluştururken adım adım detaylı protokolleri gösterir. Sinterleme işlemi için poliüretan sünger (P1 - P7 Şekil 1) bileşiğinin hazırlanması ile ilgili protokolleri hassas kontrolü yoluyla, aşağıdaki özellikler elde edilebilir: çok yoğun ve düzgün yüzey HA kaplama ve kurutma işleminden sonra, Bir tam şekilli ve 3-D şablonu boyutlu; trabeküler kemik benzer bir tam olarak birbirine bağlanmış, gözenekli trabeküler ağ; ve mikro kanallar zekâhin gibi harver kanallar ve Volkmann kanallar (Şekil 2 ve 3) olarak içi kemik kanal taklit her trabecula. Bundan başka, nispeten yüksek bir mekanik mukavemet (~ 3,8 MPa), insan trabeküler kemik benzer bir basınç mukavemeti testi ile ölçülmüştür. Trabeküler kemik vertebra insan lomber olanlar ile son derece benzer histomorfometrik parametreler mikro-BT analizi 12 tarafından teyit edildi. Kılcal eylem farklı büyüklükleri hesaplama simülasyon kullanarak Şekil 4 farklı kılcal çapları ile saptandı. Bu simülasyonlar sayesinde, biz BMT birincil gözenekler (300-400 mikron) ve çapları dayalı mikro kanallar (25-70 mikron) içinde değişen emme oranları sergilemek olacağını tahmin. Daha küçük kapillerler güçlü emme kapasiteleri sergiledi. Şekil 5 'de gösterildiği gibi Bu varsayım, bu deneyde doğrulanmıştır.
BMT yüksek bir etki sergilediğinimikro kanal yapılarının kılcal etki ile sıvı emme ve tutma; stevenel mavi leke kolay akışını (Şekil 5) izlemek için sıvı ortam olarak kullanılmıştır. Hesaplamalı simülasyon dayanarak, bu yapılandırmalar ile BMT emer ve 10 saniye içinde toplam mesafe 8.5 cm hücre süspansiyonları kadar korumak için görüldü. Nedeniyle iç yapıları tarafından uyarılan kuvvetli bir kapiler, lekeli ortam, 3 sm (yükseklik) karşı ucuna ulaştığında, 4 cm (uzunluk) 1 dakika ila 40 saniye içinde 1 cm (genişlik) bir köprü şeklinde bir şablon x x. Ayrıca, BMT aktif hücre mobilizasyonu ve birleşme (Şekil 6) gözlenmiştir. Daha sonra, homojen bir hücre mobilizasyonu ve bağlanma düzgün biçimde dağıtılmış bir oluşumunda geliştirilmiş çoğalma ve matriks oluşumu ile sonuçlanmıştır. BMT hücre süspansiyonu ile doymuş sonra Dahası, BMT yoluyla hücrelerin uzun mesafe (~ 10 cm) göç derhal onaylandı. Se eded hücreler havaya maruz ve kültür ortamında daldırılmayan şablonu segmentinde hayatta kaldı. Bu deneyde, kültür ortamı, iskele sadece ayakları dokunmadan kuyularda özel hücrelere sağlandı. Mikrokanallar tarafından sergilenen kılcal eylem daha sonra iskele üst, köprü kısmı ulaşması taze ortam için izin verdi. Kültür, 3 gün sonra, şablon hızlı çoğalan hücrelerle işgal oldu. 7 günlük bir kültürden sonra, her bir hücre dışı matrisler trabecula tarafından sarılmış ve hücreler 13 ile yerleştirilmiştir.
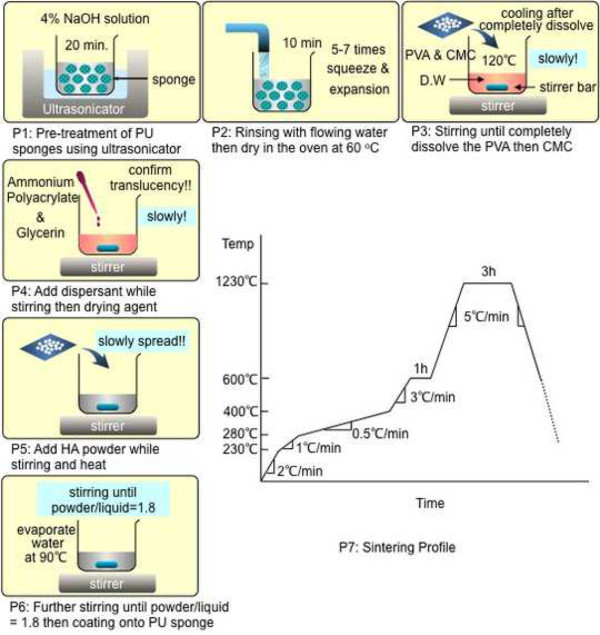
Şekil 1. P7 olumlu mekanik mukavemeti elde edilmesinde çok önemlidir sonra hassas sinterleme profil tutmak son ısı işlemi (P7) PU süngeri (P1) ön muameleden genel kemiği-şablonu imalat protokolü..f = "https://www.jove.com/files/ftp_upload/52947/52947fig1large.jpg" target = "_ blank"> bu rakamın büyük halini görmek için lütfen buraya tıklayınız.

. Şekil 2 Temsilcisi stereo mikroskop, 80 ppi (AmScope SM-2TZ-M) görüntüleri (x4) PU sünger (solda), HA kaplamalı ve BMT (orta) ve sinterlenmiş BMT (sağda) kurutulmuş boyutlu (Boyut: 3. uzunluk x genişlik 1 cm) yükseklik x 4 cm cm. Bu rakamın büyük halini görmek için lütfen buraya tıklayınız.

Bir biyogenik şablon Şekil 3. SEM ve mikro-BT görüntüleri: (A) bir biyogenik şablonun genel bir görüntü, Rong> mikro-kanallar için (B, C, D) ve görüntüler. Trabeküllerinde net mikro kanallar vurgulamak amacıyla, şablon granüle edildi. Bu rakamın büyük halini görmek için lütfen buraya tıklayınız.
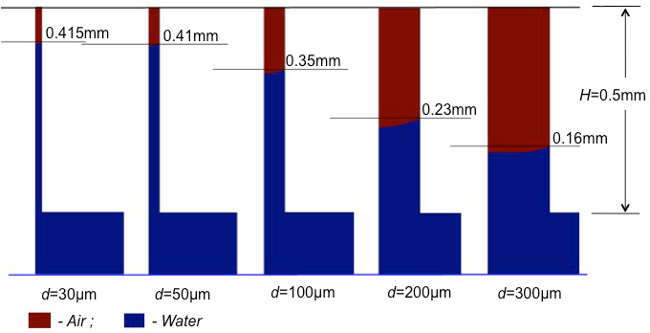
. Şekil farklı kanal çapları ile kılcal eylem 4. Hesaplamalı hesaplama aynı dönemde (0.4 ms), en büyük kılcal sırasında Içinde: 0,16 mm'ye kadar orta (mavi) absorbe (d = 300 mikron birincil gözenek ifade eder) yükseklik, en küçük kılcal: yüksekliği 0.415 mm ye kadar orta absorbe (d = 30 mm mikro-kanal eder). Bu rakamın büyük halini görmek için lütfen buraya tıklayınız.

470 um, 80 ppi ≈ 320 um, 100 ppi ≈ ≈ 60 ppi: Şekil 5. Çıkan primer gözenekler ve mikro kanallar (birincil gözenek boyutlu ortalama çapı ile ilgilidir farklı boyutlarına göre kılcal hareket emme yetenekleri farklılıklar gösterdi ) 200 mikron. sarı çizgiler primer gözenekler ve mikro kanallar kombinasyonu ile oluşturulan kılcal eylemini temsil etmektedir. Kırmızı çizgiler, her trabekülde sergilenen özellikle mikro-kanallar ile uyarılan kılcal eylemi temsil etmektedir. (F) 'de gösterildiği gibi, 100 ppi şablonu 39 saniye içinde şablonun tam bir doyma sonuçlanan kuvvetli kılcal etkiye neden olmuştur. 80 ppi ve 60 ppi şablonları sonra test edildi. (B) 0 sn, (C) 0,5 sn, (D) 1,5 sn, (E) 17.0 sn, (F) 39.0 sn, (G) 50.0 sn, ve (H) 1 dakika daldırma sonra 18 sn. (Şablon boyut: 1cm x 1 cm x yükseklik kübik 4 cm). Bu rakamın büyük halini görmek için lütfen buraya tıklayınız.
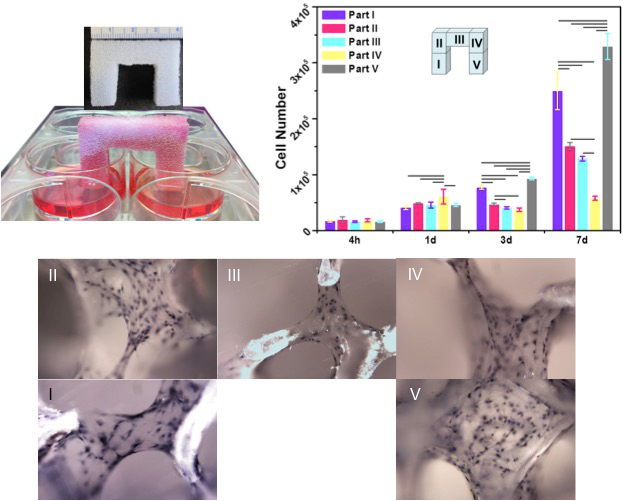
Şekil 6. ilk serpilmiş hücreleri giremeyen ayağın sonuna gelmiş aşılanmış kuyu kılcal hareket ile neden biyojenik şablonları ile giremeyen oyuklara (bölüm V) (Bölüm I). Ile ilgili giriş ve hücre göçü (bölüm V) hemen sonra Tam doygunluk. 3 gün sonra, hücrelerin izdiham tüm şablon açıktı. 7 gün sonra, uzaysal kolajen matriks oluşumu hücre popülasyonlarının (H & E boyama) içinde meydana geldi. (Şablon boyut: yükseklik uzunluk genişlik x 1 cm x 4 cm 3 cm). Cl LütfenBu rakamın büyük halini görmek için buraya ick.
Tartışmalar
Vb hücreleri, büyüme faktörleri, besinler, aşağıdakileri içeren bir çok bileşenli şablonu başarılı kemik rejenerasyonu ve kritik boyutlu, büyük kemik defektlerinin fonksiyonel restorasyonu için gereklidir. Bu faktörlerin içinde, anatomik uyumdur biyolojik özellikler önemlidir. Biyolojik işlevi yerine getirmek için, şablon biyouyumluluk, osteoconductivity mekanik bütünlüğü, yüzey alanı, yeterli bir yüzey dokusu, oksijen ve besin taşınması için araçlar gösterirler. Kolaylaştırılmış penetrasyon şablonuna (aktif istihdam), şablon (tutma) boyunca düzgün dağılım, hızlandırılmış çoğalması ve yüksek canlılığı (yerleşim): Hücresel düzeyde, aşağıdaki özellikleri masif kemik defektleri fonksiyonel restorasyonu için özellikle önemlidir. Son olarak, büyük hücre dışı matrisin bir sonraki oluşumu ve gen ekspresyonunun tetiklenmesi bu hızlı vaskülarizasyon a gibi temel biyolojik süreçlerde önemli olannd osteogenesis.
Sentetik yedek Birçok farklı tipte otomatik / allo kemik greftleri yerine önerilmiştir. Bununla birlikte, mevcut iskelesi organizasyonu mikro-kanal ve nano-gözenekler içeren bir iç mikro-sergilemez, ve bu nedenle etkin bir derin 10 mm'den daha büyük olan sentetik ikame içine hücre infiltrasyonu, dağıtım ve inhabitance kolaylaştırmamaktadır. Onlar verimli, hızlı ve düzgün kemik şablonuna derinlemesine göç hücrelerin öncü fiziksel ipuçları vermeyin. Bunun yerine, hücreler sınırlı pasif alımları iskele dış ve iç alanlar arasında bir eşitsiz dağılımı hücre popülasyonları oluşturur. Bu şablonun iç kısım ulaşan hücrelerinin ilk zorluk artırmaktadır, fakat sentetik yerine diğer ucu ile besin akışı ve hücre iletişimi engelleyen sadece. Hücre d orantısız hücre toplanması ve barınma sonuçlarının Bu tipiskele sonra eath ve eksik kemik büyümesi gövdesine 14,15 implante edilmiştir.
Böylece, bu engelleri gidermek için birincil fiziksel işaret olarak kılcal hareket kavramını tanıttı. Biz iyice aktif BMT derinliklerine hücrelerin işe için sorumlu birincil sürükleme kuvveti hesap verecek kılcal harekete geçirecek BMT mikro kanallar tasarladık.
PU sünger kaplama tekniği birçok benzersiz özellikleri sunar. İlk olarak, kendilerini önceden tanımlanmış şablon yapılarına bağlı iyi kontrollü gözenekli trabeküler yapılar kolay hazırlanması için izin verir (yani, 300-400 mikron için inç başına şablonuna 80 gözenek). Bu osteoblast infiltrasyon 15 gözenek boyutuna optimize etmek için son derece önemlidir. İkincisi, teknik, hücre tehcir 11 başlatılıyor önemli rolü için hesap birbirine mikro kanallar, inşaat olanak. Özel şekiller ve şablonlar boyutları yaratma açısından PU sünger kullanırken Üçüncü olarak, neredeyse herhangi bir sınırlama yoktur. Yapımcısı basit şekiller veya karmaşık geometriler için bile bilgisayarlı lazer kesim için makas kullanabilirsiniz. Bu tam kontrollü teknolojileri kullanarak, BMT yarattı. HA nedeniyle biyolojik uyumluluk ve osteokondüktif kapasitesi 17 arasında başlangıç malzemesi olarak seçilmiştir.
Bu çalışmada, vurgulanan gereken birkaç kritik adımlar vardır. Sıcaklığı çok yüksek ve karıştırma hızı çok düşükse HA çamur hazırlanması sırasında, HA bulamaç beher alt kenarlarında kalmış olur ve kurur. Aşırı HA bulamaç üfleme kaplama işleminden sonra, bir hava basıncı çok yüksek BMT yüzeyinde çatlaklara neden olabilir. Düzgün aşırı HA bulamaç sadece dışarı hava nispeten düşük hava basıncı tutmak için önemlidir. Sinterleme işleminin son olarak, ikinci ve üçüncü etaplarEn önemli (Grup 1 ° C / dakika 280 ° C ısı 0.5 ° C / dakika kadar 400 ° C ye kadar) vardır. HA yoğun olurken, bu sıcaklık aralığında, PU sünger tamamen yanacak. Bu protokol yakından takip değilse, BMT çökmüş veya sinterleme sonrasında ufalanmış olacak.
Bu çalışmada tarif edilen BMT çeşitli avantajlar sunmaktadır. İlk olarak, inter bağlı makro gözenekler (300-400 mikron) insan trabeküler kemik taklit ve pürüzsüz kemik iliği akışı sağlar. İkinci olarak, şablon, kılcal hareket aracılığı kemik hücrelerinin ilk girişini hızlandırmak için, her trabeküler septum içinde mikro-kanallar (25-50 um) oluşur. Şablon sadece 300 mikron gözenekleri (birincil gözenekler) ve hiçbir mikrokanallar olsaydı, hesaplamalı simülasyonu 13 kullanılarak gösterildiği gibi, kılcal eylem kemik iliği şablonun tam doygunluk için yetersiz olacaktır. Bu, özellikle l gerektirecek büyük boy kusurları için de geçerli olurarge boyutu şablonları. Mikrometre büyüklüğünde kanallar sergi son derece etkili sıvı emilimi ve böylece biz mikro kanallar bizim çalışmamızda kılcal eylem için öncelikle sorumlu olması bekleniyor. Üçüncüsü, bizim BMTS stratejik nano-gözenekler yerleştirdik. Literatür verileri hücrelerin nano-desen 18,19 özellikle duyarlı olduğunu gösterir; Bu nedenle, hücre eki artan önemli bir rol oynamak için mikro kanalların duvarlarına nano gözenekleri beklenen. Trabeküler septa yüzeyinde nano boyutta gözenekler (100-400 nm) çapa hücrelerin hareketsiz izin verdi. Genel olarak, bu üç iç yapılarının kombine etkileri şablonun boyunca gelişmiş hücre mobilizasyonu ve yapışma sonuçlandı. Ancak, protokolün bazı sınırlamalar ve mükemmel BMT imal kritik adımlar vardır. Örneğin, kaplama sırasında homojen bir viskoziteye tutma güçlüğü nedeniyle hazırlanan HA bulamacın büyük miktarda, genellikle vardır. Ayrıca yapımında bir sınırlama yokturnedeniyle kaplama sırasında çalışma süresi için hacim olarak 5 cm 3 daha büyük şablonlar. Kaplama kalınlığı üreticisinin teknikleri bağlı olarak değişir hangi kritik öneme sahiptir.
Çalışmamızın bulgular emici ve konvansiyonel alloplastik (veya sentetik) iskeleleri üzerinde potansiyel avantajları sunacak hücreleri tutabilen KİT. Prospektif bir çalışma kemikle ilgili büyüme faktörleri ile birlikte osteogenesis ve / veya anjiyogenez üzerinde BMT faydalarını doğrulamak için kabul ediliyor. Bu nedenle, bizim eşsiz özellikli KİT iskele büyük kusurları sentetik yapıları ve eksik kemik rejenerasyonu içine yetersiz kemik iliği infiltrasyonu önemli engelleri ele iddia.
Bu çalışmanın nihai hedefi zamana / emek-yoğun kemik iliği stroma ihtiyacını ortadan kaldırarak kritik ölçekli kemik defektleri kemik rekonstrüksiyonu ve fonksiyonel restorasyon biyomühendislik mevcut paradigma kolaylaştırmak içinl hücreleri izolasyonu ve genişleme süreçleri. Son olarak, biz kemiğin yeniden inşası için hızlı hücre emilimini, homojen dağılımı ve inhabitance neden mikro kanallar ve nano-gözenekler, 3D-yapıları uygun anatomik kullanmak hedefliyoruz.
Açıklamalar
The authors have nothing to disclose.
Teşekkürler
The authors have no acknowledgements.
Malzemeler
| Name | Company | Catalog Number | Comments |
| polyurethan sponge | Plastifoam | PU-3215 | |
| Sodium Hydroxide | Sigma-Aldrich | 167176 | |
| Hydroxyapatite Powder | Ossgen | ||
| Polyvinyl Alcohol | Sigma-Aldrich | 341584 | |
| Carboxymethyl cellulose sodium salt | Sigma-Aldrich | 360384 | |
| ammonium polyacrylate | Vanderbilt | DARVAN 821A | |
| Glycerin | Sigma-Aldrich | G2289 |
Referanslar
- Petrie Aronin, E. C., et al. Comparative effects of scaffold pore size, pore volume, and total void volume on cranial bone healing patterns using microsphere-based scaffolds. J Biomed Mater Res A. 89 (3), 632-641 (2009).
- Guzmán, R., et al. Chitosan scaffolds containing calcium phosphate salts and rhBMP-2: in vitro and in vivo testing for bone tissue regeneration. PLoS One. 9 (2), e87149 (1371).
- Cha, J. K., et al. Sinus augmentation using BMP-2 in a bovine hydroxyapatite/collagen carrier in dogs. J Clin Periodontol. 41 (1), 86-93 (2014).
- Karageorgiou, V., Kaplan, D. Porosity of 3D biomaterial scaffolds and osteogenesis. Biomaterials. 26 (27), 5474-5491 (2005).
- Fisher, M. B., Mauck, R. L. Tissue engineering and regenerative medicine: recent innovations and the transition to translation. Tissue Eng Part B Rev. 19 (1), 1-13 (2013).
- Manassero, M., et al. Regeneration in Sheep Using Acropora Coral, a Natural Resorbable Scaffold, and Autologous Mesenchymal Stem Cells. Tissue Eng Part A. 19 (13-14), 1554-1563 (2013).
- Reichert, J. C., et al. A tissue engineering solution for segmental defect regeneration in load-bearing long bones. Sci Transl Med. 4 (141), 141ra93 (2012).
- Sachlos, E., Czernuszka, J. T. Making Tissue Engineering Scaffolds Work. Review on The Application of Solid Freeform Fabrication Technology to The Production of Tissue Engineering Scaffolds. Eur Cell Mater. 5, 29-40 (2003).
- Woodard, J. R., et al. The mechanical properties and osteoconductivity of hydroxyapatite bone scaffolds with multi-scale porosity. Biomaterials. 28 (1), 45-54 (2007).
- Correia, C., et al. . Acta Biomater. 8 (7), 2483-2492 (2012).
- Wang, H., Li, Y., Zuo, Y., Li, J., Ma, S., Cheng, L. Biocompatibility and osteogenesis of biomimetic nano-hydroxyapatite/polyamide composite scaffolds for bone tissue engineering. Biomaterials. 28 (22), 3338-3348 (2007).
- Oh, D. S., et al. Bone marrow absorption and retention properties of engineered scaffolds with micro-channels and nano-pores for tissue engineering: a proof of concept. Ceram Int. 39 (7), 8401-8410 (2013).
- Hong, M. H., Kim, Y. H., Ganbat, D., Kim, D. G., Bae, C. S., Oh, D. S. Capillary action: enrichment of retention and habitation of cells via micro-channeled scaffolds for massive bone defect regeneration.J. Mater Sci Mater Med. 25 (8), 1991-2001 (2014).
- Volkmer, E., et al. Hypoxia in static and dynamic 3D culture systems for tissue engineering of bone. Tissue Eng. Part A. 14 (8), 1331-1340 (2008).
- Malda, J., Klein, T. J., Upton, Z. The roles of hypoxia in the in vitro engineering of tissues. Tissue Eng. 13 (9), 2153-2162 (2007).
- Macchetta, A., Turner, I. G., Bowen, C. R. Fabrication of HA/TCP scaffolds with a graded and porous structure using a camphene-based freeze-casting method. Acta Biomater. 5 (4), 1319-1327 (2009).
- Cox, S. C., Thornby, J. A., Gibbons, G. J., Williams, M. A., Mallick, K. K. 3D printing of porous hydroxyapatite scaffolds intended for use in bone tissue engineering applications. Mater Sci Eng C Mater Biol Appl. 47, 237-247 (2015).
- Wan, Y., et al. Adhesion and proliferation of OCT-1 osteoblast-like cells on micro- and nano-scale topography structured poly(l-lactide). Biomaterials. 26 (21), 4453-4459 (2005).
- Zhao, L., Mei, S., Chu, P. K., Zhang, Y., Wu, Z. The influence of hierarchical hybrid micro/nano-textured titanium surface with titania nanotubes on osteoblast functions. Biomaterials. 31 (19), 5072-5082 (2010).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır