Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
Düşük sıcaklık mikrodalga destekli hidrotermal karbonizasyon ile Willow Wood yakıt emisyonu azaltılması
Bu Makalede
Özet
Düşük sıcaklık mikrodalga destekli hidrotermal karbonizasyon tedavisi ile düşük kaliteli biyokütle emisyon öncüsü tükenmesi için bir protokol sunulmuştur. Bu protokol mikrodalga parametrelerini ve biocoal ürün ve proses suyunun analizini içerir.
Özet
Biyokütle, CO2 emisyonları biyokütle büyümesini yeniden entegre olarak sürdürülebilir bir yakıttı. Ancak, biyokütle inorganik öncüleri olumsuz çevresel etki ve süruf oluşumu neden. Seçilen kısa rotasyon baltalık (src) söğüt odun yüksek kül içeriği vardır (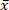 = 1,96%) ve bu nedenle, emisyon ve süruf öncülerinin yüksek bir içerik. Bu nedenle, 150 °C, 170 °C ve 185 °C ' de düşük sıcaklıkta mikrodalga destekli hidrotermal karbonizasyon (MAHC) ile SRC söğüt ağacından minerallerin azaltılması incelenmiştir. Mikrodalgalar tüm reaktör hacminin nüfuz gibi geleneksel reaktörler üzerinden MAHC bir avantajı, reaksiyon ortamında bile sıcaklık iletkenlik olduğunu. Bu, daha iyi bir sıcaklık kontrolü ve daha hızlı bir dolum süresi sağlar. Bu nedenle, bir arkaya depolymerization, dönüşüm ve repolymerization reaksiyonları etkili bir şekilde analiz edilebilir. Bu çalışmada, tedavi edilen ve tedavi edilmeyen SCR söğüt ağacından kütle kaybı, kül içeriği ve bileşimi, Isıtma değerleri ve molar O/C ve H/C oranlarının analizi, MAHC kömür mineral içeriğinin azalmasına ve Isıtma değerinin arttığını göstermiştir. Proses suyu azalma pH gösterdi ve furfural ve 5-metilfurfural içeriyordu. 170 °C ' lik Proses sıcaklığı, enerji giriş ve kül bileşeni azaltmanın en iyi kombinasyonunu göstermiştir. MAHC hidrotermal karbonizasyon sürecinin daha iyi anlaşılması, büyük ölçekli bir endüstriyel uygulama yüksek yatırım maliyetleri nedeniyle olası değildir sağlar.
= 1,96%) ve bu nedenle, emisyon ve süruf öncülerinin yüksek bir içerik. Bu nedenle, 150 °C, 170 °C ve 185 °C ' de düşük sıcaklıkta mikrodalga destekli hidrotermal karbonizasyon (MAHC) ile SRC söğüt ağacından minerallerin azaltılması incelenmiştir. Mikrodalgalar tüm reaktör hacminin nüfuz gibi geleneksel reaktörler üzerinden MAHC bir avantajı, reaksiyon ortamında bile sıcaklık iletkenlik olduğunu. Bu, daha iyi bir sıcaklık kontrolü ve daha hızlı bir dolum süresi sağlar. Bu nedenle, bir arkaya depolymerization, dönüşüm ve repolymerization reaksiyonları etkili bir şekilde analiz edilebilir. Bu çalışmada, tedavi edilen ve tedavi edilmeyen SCR söğüt ağacından kütle kaybı, kül içeriği ve bileşimi, Isıtma değerleri ve molar O/C ve H/C oranlarının analizi, MAHC kömür mineral içeriğinin azalmasına ve Isıtma değerinin arttığını göstermiştir. Proses suyu azalma pH gösterdi ve furfural ve 5-metilfurfural içeriyordu. 170 °C ' lik Proses sıcaklığı, enerji giriş ve kül bileşeni azaltmanın en iyi kombinasyonunu göstermiştir. MAHC hidrotermal karbonizasyon sürecinin daha iyi anlaşılması, büyük ölçekli bir endüstriyel uygulama yüksek yatırım maliyetleri nedeniyle olası değildir sağlar.
Giriş
Hidrotermal karbonizasyon (mahc) için mikrodalgaların uygulanması, fruktoz, glikoz1,2 veya selüloz3gibi biyokütle modeli bileşiklerinin termokimyasal dönüşümü için ve organik substratlar için kullanılmıştır. tercihen atık malzeme4,5,6,7,8,9,10. Mikrodalgaların kullanımı, tedavi edilen biyokütle2,10 ağırlıklı olarak dielektrik solvent11,12, termal kayıplar ile bile ısıtma sağlar gibi avantajlı olduğunu mikrodalgalar yapmak rağmen doğrudan kimyasal bağlar kırmak ve tepkiler teşvik etmek için yeterli enerji transferi değil13. Mikrodalgalar HTC reaktör gemisi tüm reaksiyon hacmine nüfuz ve çelik manto yüksek ısıtma kapasitesi nedeniyle daha yavaş bir Isıtma hızı gösteren konvansiyonel bir reaktör ile mümkün değildir malzeme, doğrudan enerji transferi ve örnek kendisi14. Mikrodalgalar ile numunenin su moleküllerinin bile uyarılması, mikrodalga reaktöründeki sıcaklık eşit şekilde dağıtılmış11,14,15 ve sonra dolum süresi sayesinde geliştirilmiş bir proses kontrolüne olanak sağlar reaksiyon çok daha hızlıdır. Ayrıca, konvansiyonel reaktörler çok daha yavaş ısıtır ve Isıtma sırasında meydana gelen kimyasal reaksiyonlar genellikle son sıcaklığa atanan sonuçlar önyargı olabilir. Bir MAHC reaktöründeki geliştirilmiş proses kontrolü, seçilen HTC reaksiyonları (örn. dehidrasyon veya dearboksilasyon) Sıcaklık bağımlılığı konusunda kesin bir ayrıntı sağlar. HTC-Reactor hacminde bile sıcaklık dağılımının bir diğer avantajı da iç reaktör duvarında2immobilize ve tamamen karbonize partiküllerin alt yapıştıdır. Ancak, su sadece bir ortalama mikrodalga bile elde edilebilir maksimum sıcaklık sınırlar yüksek sıcaklıklarda, azalma mikrodalga absorbans gösterir solvent emici. Bu olumsuz etki, HTC sürecinde asitler üretildiğinde veya tedavi öncesinde Katalizörler (İyonik veya polar türler) eklendiğinde telafi edilir. Mikrodalga indüklenen reaksiyonlar genel11,15 ve özellikle 5-hidrokmetilfurfural (5-HMF) fruktoz gelen kum yatağı katalizör reaksiyonları ile karşılaştırıldığında daha yüksek ürün verimleri göstermek12. Ayrıca daha iyi bir enerji dengesi daha sonra Konvansiyonel Isıtma yöntemleri var15,16.
Hidrotermal karbonizasyon temel kimyasal kavramı bozulma ve biyokütle ardışık polimerizasyon olduğunu. Bu karmaşık etkileşim reaksiyonları sırasında doku oksijen tükenmiş, hangi Isıtma değerini artırır. İlk başta, polimerler hemiselüloz ve selüloz şeker monomerler için hidrolize edilir17, düşük sıcaklıklar ağırlıklı hemiselüloz etkileyen rağmen18,19,20,21. HTC reaksiyonları bu erken aşamada, organik asitler şeker aldehitler ve hemicellulose deasetilasyon dönüşümü oluşur. Bu asitler Asetik olabilir, laktik, levulinik, akrilik veya formik asit20,21,22 ve reaktörde reaksiyon suyu pH azaltmak. Dissosyasyon nedeniyle, proses suyunda iyon ürününü artıran ücretsiz negatif iyonlar oluşturur. Artan iyon ürün biyokütle kül büyük bileşenleri olan cations, çözme sağlar. Bu mekanizma tarafından, doku emisyon öncüleri ve süruf bobinler (örneğin, potasyum, sodyum, kalsiyum, klor ve ağır metaller) tükendi23,24.
Oluşturulan organik asitler Furanlar için şeker monomerlerin dehidratasyonu destekleyebilir. Ortak bir şeker dehidrasyon ürün furfural ve 5-hydroxymethylfurfural, hangi kimyasal sanayi için uygulanabilir ürünler, onlar platform ürünleri olarak hizmet gibi (örneğin, biopolymers sentezi için). 5-metilfurfural selüloz25,26 veya 5-hydroxymethylfurfural27katalizör reaksiyonları ile oluşturulabilir. Biyopolimer sentezi kontrollü koşullarda yapay bir repolimerizasyon olmakla beraber, Furanlar MAHC reaktörünün kompleks kimyasal ortamında yüksek molekül ağırlığı aromatik yapıları da yoğunlaştırabilir, polimerize edebilir ve şekillendirebilir. Değiştirilmiş ahşap hücre matriks ile çözünen organik ve inorganik bileşiklerin etkileşimi reaksiyon sisteminin karmaşıklığı eklemek20. Furan polimerizasyon reaksiyon yolları, Aldol yoğuşması veya/ve moleküler dehidrasyon18,20 ve hidrofobik kabuk ve daha hidrofil çekirdeği28verim hidrochar parçacıkları istihdam. Henüz biyokütle parçacıkları tamamen deforme olup olmadığını ve daha sonra repolymerized ya da biyokütle parçacıkları karbonizasyon için bir şablon olarak hizmet ortaya değil. Ancak, bozulma ve repolimerizasyon reaksiyonları dehidrasyon ve dekarboksilasyon reaksiyonları oluşur, hem de29,30, hangi Van Krevelen diyagramında damla indükler O/c ve siyah karbon H/c oranlarına doğru.
Diğer çalışmalar konvansiyonel reaktör bazlı hidrotermal tedavi31, bir su yıkama kombine mekanik liçi32 veya su/amonyum asetat/hidroklorik asit yıkama33ile soğutma etkisini azaltan mineral kanıtladı iken, bizim çalışmalar ilk kez mikrodalgalar ile düşük sıcaklıkta karbonizasyon sırasında mineral liçi araştırmak. Bu çalışmada yakıt yükseltmesi için emisyon öncüsü liçi üzerinde duruluyor gibi, potasyum, sodyum, magnezyum, kalsiyum, klor, kükürt, azot ve ağır metaller kaderini inceler. İnce toz öncüleri, gaz aşamasında yüksek sıcaklıklarda uçucu tuzları (örn. KCl veya K2so4) oluşturur. Bu tuzlar baca gazı birikdiğinde, çinko gibi ağır metaller çekirdekleme parçacıkları, bir parçacık büyüme zinciri reaksiyonu yol açar olarak onları yıkabilir. Düşük baca gazı sıcaklıklarında, tuz yoğuşması partikül büyümesini daha da tetikler ve bacadan gelen kancerojen ince toz emisyonuyla sonuçlanır. Bu emisyonları mevcut biyokütle yakıtların sürdürülebilirliği ödün ana faktördür. Sürdürülebilir bir enerji kaynağı, pahalı filtreler veya yakıtlarda azaltılması (örneğin, MAHC) ile azaltılmasına dayanır. Bu çalışmada pratik bir yaklaşım takip ederken, kısa rotasyon baltalık (src) söğüt ahşap yüksek büyüme oranları ile potansiyel bir Biyoenerji hammadde olarak seçildi. Bu gazlaştırma tarafından kendi kendine sürdürülebilir bir güç kaynağı için kendi alanlarında çiftçiler tarafından yetiştirilebilir, aynı zamanda doğrudan yanma ile ısı üretimi için. Söğüt SRC bir dezavantajı, düşük bir kök nedeniyle yüksek kabuğu içeriği: Olgun aşamada kabuk oranı. Bark ahşap34,35,36,37 karşılaştırıldığında mineraller bir sürü içerir ve gaz veya parçacık emisyonlarının daha yüksek miktarlarda verir38. Düşük sıcaklık HTC SRC söğüt ahşap yanma özelliklerini artırabilir ve böylece, sürdürülebilir bir ısı ve güç kaynağına katkıda bulunabilir. Bu çalışmada incelenmiştir HTC biocoal bir başka önemli parametre enerji yoğunluğu, daha yüksek ilk yanma sıcaklığı ve yüksek son yanma sıcaklığı39.
Protokol
1. örnek malzemenin hazırlanması
- Beş yaşındaki söğüt hasat, klon tipi "Tordes" ([Salix schwerinii x s. viminalis] x s. vim.), yüksekliği ile 12 − 14 m ve yaklaşık 15 cm Meme çapı.
- 105 °C ' de 24 saat boyunca odun çipi ve cips kurutun.
- Bir kesme fabrikası ile ahşap yongaları kesmek ve 0,12 mm partikül boyutuna bir santrifüj değirmen ile eziyet.
2. mikrodalga destekli hidrotermal karbonizasyon
- 850 W ve 2.455 MHz magnetron frekans ile bir mikrodalga fırın kullanın.
- Bir spatula ile bir 50 mL Politetrafloroetilen (PTFE) reaksiyon damarında 1,3 adımda ham madde 500 mg yer. 10 mL demineralize su ekleyin. Tepsideki basınç valfi, kap kapağı ile aynı seviyede olduğu için reaksiyon kabı kapağını vidalayın.
- Her tedavi sıcaklığı için, mikrodalga fırında hammadde ile oniki reaksiyon gemileri koymak ve fırın kapatın.
- Üç sıcaklık için mikrodalga ile üç ısı programları kurmak: 150 °C (Ramp + 12,5 °C dk-1, tutun 60 dk, pik güç% 50), 170 °c (ramp + 9,6 °c Min-1, tutun 60 min, pik güç% 80%), ve 185 °c (rampa + 5,3 °c Min-1 , 30 dakika tutun, ramp-1,1 °C dk-1 Ila 150 °c, en yüksek güç% 100). Her tek program için mikrodalga fırını başlatın.
- Program tamamlandıktan sonra, reaksiyon kapları çıkarın, onları serin ve yeniden etkinleştirmek için izin. Sonra da içinde basıncı bırakmadan sonra bir duman dolabı altında açın.
- Her reaksiyon gemisine iki kez distile su 35 mL ekleyin. Her gemi için bir Santrifüjü silindir ve santrifüjte çözüm dökün 1.714 x g 10 dakika.
- Proses suyu başka bir tüpün içine boşaltılır ve pH ve gaz kromatografi-kütle spektrometresi (GC-MS) analizi için-5 °C ' de donmuş olarak saklanır.
- Santrifüj silindiri-5 °C ' de kalan biocoal Pelet ile dondurabilirsiniz. Sonra biocoal Pelet çıkarın ve 24 saat için 105 °C ' de kurutun. biocoal Pelet tartın ve MAHC tedavisinin indüklenen kilo kaybını hesaplayın.
- Sonraki analiz için yeterli biocoal (yaklaşık 22 g) üretmek için (sıcaklık başına 48 reaksiyon kapları) sıcaklık başına 2.2 − 2.8 dört kez adımları yineleyin.
3. kül içeriği belirlenmesi
- Bireysel olarak 20 boş seramik yemek tartın. Her 1 g örnekteki (5 x 1 g hammadde ve her sıcaklık tedavisinden 5 x 1 g biocoal) ekleyin.
Not: yemekler etiketlenmediği için, fırınlardaki gemilerin düzenlenmesi için bir plan çizilmelidir. - Açık seramik yemekleri bir kalıp fırını içine yerleştirin ve fırını kapatın.
- Kalıp fırını için bir sıcaklık programı programı (+ 6 °c Min-1 dan 25 °c ila 250 °c, Hold 60 dk, + 10 °c Min-1 ila 550 °c, tutun 120 dk) ve programı başlatın.
- Program tamamlandıktan sonra, mantar fırını 105 °C ' ye kadar soğumasını bırakın. Sonra fırını açın ve seramik yemekleri dışarı çıkarın.
- Seramik yemeklere Silis jeli içeren bir kurutma maddesi ile dolu bir aspiratör (malzeme tablosu) yerleştirin. Bir vakum pompası yardımıyla kurutucu ve vakum kuru kapatın.
- 24 saat soğutma işleminden sonra seramik yemeklerden çıkarın. Kül içeren seramik çanak tartın ve boş seramik çanak ağırlığını çıkararak kül ağırlığı hesaplamak.
- Ham madde veya biocoal kuru kitle tarafından kül ağırlığı bölerek yüzde olarak kül içeriği belirleyin.
4. yüksek ve daha düşük Isıtma değerlerinin belirlenmesi
- Kalorimetre su pompasını etkinleştirin ve kalorimetreye% 99,5 oksijen sağlamak için oksijen valfi açın.
- 1 gr glikoz tartın ve 46.479 J/g tanımlı bir kalorifik değeri ile bir plastik örnek torba içine yerleştirin. bir kalorimetre bombası yanma pota içine örnek çanta koyun.
- Bomba alt iki kez deiyonize su 5 mL ekleyin ve bomba aşağı vida. Bombası Kalorimetre yerleştirin ve Kalorimetre kapatın.
- Örnek ağırlık girin ve örnek çanta yöntemi ayarlarını değiştirin. Kalorimetre başlayın.
- Ölçüm tamamlandıktan sonra, bombayı çıkarın, ters çevirin ve 1 dakika boyunca yavaşça sallayın.
- Bombası sökün, 5 mL iki kez demineralize su çıkarın ve sonraki İyon Kromatografi analizi için bir vida kap kabı içinde saklayın.
- Kalibrasyon standardını elde etmek için 4.2 − 4.6 adımlarını üç kez yineleyin.
- Her MAHC biocoal (150 °C, 170 °C, 185 °C) ve hammadde ile 4.2 − 4.6 beş kez yineleyin.
- Aşağıdaki denklem40kullanarak düşük Isıtma değerini hesaplayın:
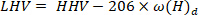
Burada LHV düşük Isıtma değeri, HHV adım 4,4 Kalorimetre elde yüksek ısıtma değeri, ve ω hidrojen içeriği [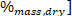 Elemental analiz elde.
Elemental analiz elde.
5. klorun ölçülmesi için İyon Kromatografi
Not: analizden önce iyon kromatografinin kalibrasyonunu kontrol edin.
- Adım 4,8 ' dan 5 mL çözelti çıkarın ve bir 50 mL Volumetrik maskeye iki kez demineralize su 45 mL ekleyin.
- Örnek emme tüpünü örnek bir kabın içine takın ve ön sütuna bir şırınga ile yaklaşık 3 mL örnek çizin. Analiz çalışmasını başlatın.
- Üreticinin talimatlarına göre ölçümleri gerçekleştirin.
- Bölüm 4 ' te hazırlanan her örnek için 5,2 ve 5,3 arasındaki adımları yineleyin.
6. O/C ve H/C oranlarının belirlenmesi için Elemental analiz
- Ölçülecek numuneler için enstrüman kılavuzunda uygun bir yöntem seçin.
- Cihaz kalibre etmek için gerekli tüm 20 mg sülfonamid standartları ve boşluklar olun.
- Bir malzeme örneği hazırlamak için, mikro denge üzerinde kalay folyo örnek 20 mg koyun. Teneke folyo üzerinde örnek tartmak, numune çevresindeki folyo kapatın ve mümkün olduğunca az hava içeren pakete basın. Daha sonra her örnek için bu 5x tekrarlayın.
Not: Biochar örneklerini analiz edebilmek için, örnek miktarı olarak Tungsten trioksit aynı miktarda 1:1 bir oran eklenmesi gerekir. Bu Elemental Çözümleyicisi tam yanma sağlamak için Biochar eksik oksijen telafi etmek için gereklidir. - Hazırlanmış numuneleri Elemental Analizörün otomatik örneklemine takın.
- Elemental Analizörün yanma odası için oksijen ve Helyum valfi açın.
- Cihaz cihaz tarafından belirtilen sıcaklığa ulaştığında analizini başlatın. Bu durumda, sıcaklık 900 °C ' ye ulaşıncaya kadar bekleyin.
- Sulfonamid Standart ağırlığı (adım 6,2) ve ilgili eleman 1 Mol ağırlığı tarafından sülfonamid standardında her öğenin benler hesaplayın.
- Sulfonamid C, H, S ve N, Mol arasındaki ilişkiyi hesaplayın, adım 6,7 elde edilen, ve ilgili zirve alanları.
- Toplam Numune ağırlığının 3,7 adımda elde edilen örnek kül içeriğini çıkarın.
- Sülfonamid standardında ve örnekteki ilgili eleman tepe alanını karşılaştırın ve örnekteki öğenin köstebeği elde etmek için sülfonamid her öğenin köstebek tarafından çarpın.
- Periyodik tablodan öğenin ilgili molar kütlesi ile, adım 6,10 elde edilen öğenin köstebeği çarpılarak örnekteki C, H, S ve N ağırlığını hesaplayın.
- Adım 6,9 elde edilen kül ücretsiz örnek kitle kullanarak örnek oksijen ağırlığı hesaplamak ve C, H, N ve S ağırlığı çıkararak, adım 6,11 elde.
- Ham madde ve MAHC biocoal örneklerinde molar H/C ve O/C oranlarını hesaplayın.
7. indüklenen bağlantılı plazma optik emisyon spektroskopisi
- Tartmak 400 kuru hammadde veya MAHC biocoal mg ve bir spatula ile bir 50 mL PTFE reaksiyon gemisi içine koydu. Ekleyin 3 mL 69% nitrik asit ve 9 mL 35% hidroklorik asit.
- Tepsideki basınç valfi, kap kapağı ile aynı seviyede olduğu için reaksiyon kabı kapağını vidalayın.
- Mikrodalga fırınında analiz edilecek numunelerin reaksiyon damarlarını koyun ve fırını kapatın.
- Organik malzemenin tam bozulması için sıcaklık programı programı: rampa + 15,5 °C Min-1 Ila 200 °c, 30 dk tutun, serin aşağı 180 °c, tutun 5 dakika. mikrodalga fırını başlatın.
- Program tamamlandıktan sonra, reaksiyon kapları çıkarın, onları serin ve yeniden etkinleştirmek için izin. Sonra içinde basıncı bırakmadan sonra bir duman dolabı altında gemiler açın.
- Bir 50 mL ampul silindir içine örnekleri dökün. Sonra iki kez deiyonize su ile iyice reaksiyon gemisi durulayın ve ampul silindir aktarın. Tüm numunelerin bile seyreltme sağlamak için iki kez deiyonize su ile 50 mL işareti için silindir yukarı yukarı.
- 150 μm Mesh filtre kağıdı ile adım 7,6 örnek filtre. 50 mL konik Santrifüjlü tüplerde filtrat doldurun.
- Standart numuneleri ICP-OES ' ı k i Otoenjektör 'a koyun. Standart örnekler bilinen konsantrasyonlardan (0,0001 ppm, 0,001 ppm, 0,1 ppm, 1 ppm 10 ppm, 20 ppm, 50 ppm) unsurların nicelik olarak (CA, as, B, be, Fe, se, Zn, AG, al, ba, bi, CD, Co, CR, cu, GA, K, li , Mg, MN, Mo, na, ni, PB, RB, SR, te, TL, V).
- Örnekleri ICP-OES Otoenjektör koyun ve aynı parametrelerle ICP-OES Analizi çalıştırın.
- ICP-OES analizinden sonra, 7,8 adımda standart örneklerden elde edilen kalibrasyon eğrilerine göre, otomatik olarak mg/kg cinsinden hesaplanan yazılımdan Elemental konsantrasyonu elde edilir.
- Üretilen biocoal içindeki Elemental konsantrasyon azaltma hesaplayın:
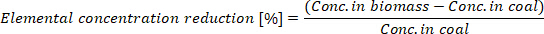
Burada CONC. biyokütle biyokütle ve CONC Elemental konsantrasyon. Kömür içinde biocoal Elemental konsantrasyon.
8. HTC proses suyunun pH değerini ölçme
- Her bir sıvı kesir hammaddenin MAHC tedavi (adım 2,7) ve dört ilgili Beakers üç biocoals doldurun.
- PH sondasını standart çözümlerle kalibre edin.
- Hammadde ve üç MAHC biocoals sıvı fraksiyonu pH ölçmek.
9. gaz kromatografi-kütle spektrometresi
- MAHC tedavisinden (adım 2,7) sıvı fraksiyonları 150 μm Mesh filtre kağıdıyla filtreleyin. Süzülmüş sıvı fraksiyonları 1 mL metanol 20 mL ekleyin.
- Transfer 200 μL bir GC-MS Otomatik Örnekleyici şişe ve GC-MS Otomatik Örnekleyici içinde şişe koymak.
- Methanol ile 10-2, 10-3, 10-4ve 10-5 , furfural ve 5-metilfurfural (analitik Grade) aşağı saf standartları seyreltilen.
- GC-MS Otomatik Örnekleyici standartlarına koyun ve parametreler ile analiz: 230 °c enjektör sıcaklığı ve 1:40 bölünmüş 1 μL enjeksiyon hacmi; 15 m uzunluğunda ve 0,25 mm film kalınlığına sahip 5MS Polar olmayan kolon (malzeme tablosu); sıcaklık programı 30 °C, 2 dakika tutun, rampa + 40 °C/min ila 250 °C, 2 dak tutun; 70 mV ve MS dedektörü ile iyonizasyon 35 − 400 m/z aralığı ile tarama modunda, her 0,3 s tarama.
- Toplam iyon sayımı (TIC) tepe alanı ve bileşik konsantrasyon ile kalibrasyon eğrileri oluşturun.
- Hazırlanan HTC biocoal sıvı faz örneklerini aynı analitik parametrelerle çalıştırın ve standardın saklama süresi ve spektrumlu kütüphanedeki spektrum eşleşerek furfural ve 5 metilfurfural belirleyin.
- Hesaplanan kalibrasyon eğrisini kullanarak furfural ve 5-metilfurfural konsantrasyonlarını belirleyin (adım 9,6) ve furfural ve 5-methylfurfural örnek tepe alanları ekleme.
10. istatistik
- Normal dağılım için Shapiro Wilks testiyle verileri analiz edin.
- Normal olarak dağıtılmış veri kümeleri ve veri kümeleri arasında önemli farklar bulmak için normal olarak dağıtılmış veri kümeleri için t-testi için Mann-Whitney U-test kullanın.
Not: bir veri kümesi normal olarak dağıtılır ve diğeri değilse, Mann-Whitney U testini kullanın.
Sonuçlar
Elemental analizlerin sonuçları söğüt ağacından O/C-H/C oranı ile MAHC biyozarları arasındaki farklılıkları ortaya koymuştur (Şekil 1). Hammadde daha yüksek O/C-H/C oranları ve değerlerin daha yüksek bir varyasyonu gösterir. MAHC tedavisi, mikrodalga reaktöründeki homojenizasyon nedeniyle değer değişimini azalttı. Mikrodalga reaktörü hassasiyetinde bozulma üç aşamaları farklılaşma izin verdi. H/C oranı 150 °C ' de düşür?...
Tartışmalar
MAHC, farklı ısıl işlem yoğunlukları uygulayarak kimyasal bozulmanın adımlarının farklılaşmasını sağlar. Bu nedenle, kütle kaybı, O/C-H/C oranı, Isıtma değeri, kül bileşeni azaltma, proses suyunun pH artışı ve proses suyunda Furanlar birikimi arasındaki etkileşimleri değerlendirmek mümkündür. Geleneksel HTC reaktör yöntemi üzerinden MAHC yönteminin avantajı, tüm reaktör hacmine nüfuz eden mikrodalgalarla termal iletimde dayanır ve reaktör hacmini Isıtma yerine microlevel üzerind...
Açıklamalar
Yazarların ifşa etmesi gereken hiçbir şey yok.
Teşekkürler
Yazarlar, Christoph Warth, Michael Russ, Carola Lepski, Julian Tejada ve Dr. Rainer Kirchhof 'a teknik destek için teşekkür etmek ister. Çalışma, 01DN16036 hibe numarası altında BMBF (proje BiCoLim-Bio-yanıcı limpios) tarafından finanse edilmiştir.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 5MS non-polar cloumn | Thermo Fisher Scientific,Waltham, USA | TraceGOLD SQC | GCMS |
| 9µm polyvinylalcohol particle column | Methrom AG, Filderstadt, Germany | Metrosep A Supp 4 -250/4.0 | Ion chromatography |
| argon | Westfalen AG, Münster, Germany | UN 1006 | ICP-OES |
| calorimeter | IKA-Werke GmbH & Co.KG, Stauffen, Germany | C6000 | higher and lower heating value |
| centrifuge | Andreas Hettich GmbH & Co.KG, Germany | Rotofix 32 A | |
| centrifuge mill | Retsch Technology GmbH, Haan, Germany | ZM 200 | |
| ceramic dishes | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | XX83.1 | Ash content |
| cutting mill | Fritsch GmbH, Markt Einersheim, Germany | pulverisette 19 | |
| D(+) Glucose | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | X997.1 | higher and lower heating value |
| elemental analyzer | elementar Analysesysteme GmbH, Langenselbold, Germany | varioMACRO cube | elemental analysis |
| exicator | DWK Life Sciences GmbH, Wertheim, Germany | DURAN DN300 | Ash content |
| GC-MS system | Thermo Fisher Scientific,Waltham, USA | Trace 1300 | GCMS |
| hydrochloric acid | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | HN53.3 | ICP-OES |
| ICP OES | Spectro Analytical Instruments GmbH, Kleve, Germany | Spectro Blue-EOP- TI | ICP-OES |
| Ion chromatograph | Methrom GmbH&Co.KG, Filderstadt, Germany | 833 Basic IC plus | Ion chromatography |
| kiln dryer | Schellinger KG, Weingarten, Germany | ||
| kiln dryer | Schellinger KG, Weingarten, Germany | Ash content | |
| mesh filter paper | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | L874.1 | ICP-OES |
| microwave oven | Anton Paar GmbH, Graz, Austria | Multiwave Go | |
| muffel furnance | Carbolite Gero GmbH &Co.KG, Neuhausen, Germany | AAF 1100 | Ash content |
| nitric acid | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | 4989.1 | ICP-OES |
| oxygen | Westfalen AG, Münster, Germany | UN 1072 | higher and lower heating value |
| pH-meter | ylem Analytics Germany Sales GmbH & Co. KG, Weilheim,Germany | pH 3310 | pH |
| sample bag | IKA-Werke GmbH & Co.KG, Stauffen, Germany | C12a | higher and lower heating value |
| Standard Laboratory Vessels and Instruments | |||
| standard samples | Bernd Kraft GmbH, Duisburg, Germany | ICP-OES | |
| sulfonamite | elementar Analysesysteme GmbH, Langenselbold, Germany | SLBS4782 | elemental analysis |
| teflon reaction vessels | Anton Paar, Austria | HVT50 | |
| teflon reaction vessels | Anton Paar, Austria | HVT50 | ICP-OES |
| tin foil | elementar Analysesysteme GmbH, Langenselbold, Germany | S12.01-0032 | elemental analysis |
| tungstenVIoxide | elementar Analysesysteme GmbH, Langenselbold, Germany | 11.02-0024 | elemental analysis |
| twice deionized water | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | ||
| twice deionized water | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | higher and lower heating value | |
| twice deionized water | Carl Roth GmbH&Co.KG, Karlsruhe, Germany | ICP-OES |
Referanslar
- Li, C., Zhao, Z. K., Cai, H., Wang, A., Zhang, T. Microwave-promoted conversion of concentrated fructose into 5-hydroxymethylfurfural in ionic liquids in the absence of catalysts. Biomass and Bioenergy. 35 (5), 2013-2017 (2011).
- Möller, M., Harnisch, F., Schröder, U. Microwave-assisted hydrothermal degradation of fructose and glucose in subcritical water. Biomass and Bioenergy. 39, 389-398 (2012).
- Guiotoku, M., Rambo, C. R., Hansel, F. A., Magalhães, W. L. E., Hotza, D. Microwave-assisted hydrothermal carbonization of lignocellulosic materials. Materials Letters. 63 (30), 2707-2709 (2009).
- Guiotoku, M., Rambo, C. R., hansel, F. A., Magalhães, W. L. E., Hotza, D. Microwave-assisted hydrothermal carbonization of lignocellulosic materials. Materials Letters. (63), 2707-2709 (2009).
- Kannan, S., Gariepy, Y., Raghavan, G. S. V. Optimization and characterization of hydrochar produced from microwave hydrothermal cabonization of fish waste. Waste Management. , 159-168 (2017).
- Elaigwu, S. E., Greenway, G. M. Microwave-assisted and conventional hydrothermal carbonization of lignocellulosic waste material: Comparison of the chemical and structural properties of the hydrochars. Journal of Analytical and Applied Pyrolysis. 118, 1-8 (2016).
- Elaigwu, S. E., Greenway, G. M. Microwave-assisted hydrothermal carbonization of rapeseed husk: A strategy for improving its solid fuel properties. Fuel Processing Technology. 149, 305-312 (2016).
- Chen, W. -. H., Ye, S. -. C., Sheen, H. -. K. Hydrothermal carbonization of sugarcane bagasse via wet torrefaction in association with microwave heating. Bioresource technology. 118, 195-203 (2012).
- Nizamuddin, S., et al. Upgradation of chemical, fuel, thermal, and structural properties of rice husk through microwave-assisted hydrothermal carbonization. Environmental science and pollution research international. 25 (18), 17529-17539 (2018).
- Nizamuddin, S., et al. An overview of microwave hydrothermal carbonization and microwave pyrolysis of biomass. Reviews in Environmental Science and Bio/Technology. 17 (4), 813-837 (2018).
- Dallinger, D., Kappe, C. O. Microwave-assisted synthesis in water as solvent. Chemical reviews. 107 (6), 2563-2591 (2007).
- Qi, X., Watanabe, M., Aida, T. M., Smith, J. R. L. Catalytic dehydration of fructose into 5-hydroxymethylfurfural by ion-exchange resin in mixed-aqueous system by microwave heating. Green Chemistry. 10 (7), 799 (2008).
- Nüchter, M., Ondruschka, B., Bonrath, W., Gum, A. Microwave assisted synthesis - a critical technology overview. Green Chem. 6 (3), 128-141 (2004).
- Schanche, J. -. S. Microwave synthesis solutions from personal chemistry. Molecular Diversity. 7 (2-4), 291-298 (2003).
- Kappe, C. O. Controlled microwave heating in modern organic synthesis. Angewandte Chemie (International ed. in English). 43 (46), 6250-6284 (2004).
- Gronnow, M. J., White, R. J., Clark, J. H., Macquarrie, D. J. Energy Efficiency in Chemical Reactions: A Comparative Study of Different Reaction Techniques. Organic Process Research & Development. 9 (4), 516-518 (2005).
- Kruse, A., Dahmen, N. Hydrothermal biomass conversion: Quo vadis?. The Journal of Supercritical Fluids. 134, 114-123 (2018).
- Reza, M. T., et al. Hydrothermal Carbonization of Biomass for Energy and Crop Production. Applied Bioenergy. 1 (1), (2014).
- Libra, J. A., et al. Hydrothermal carbonization of biomass residuals: a comparative review of the chemistry, processes and applications of wet and dry pyrolysis. Biofuels. 2 (1), 71-106 (2011).
- Reza, M. T., Uddin, M. H., Lynam, J. G., Hoekman, S. K., Coronella, C. J. Hydrothermal carbonization of loblolly pine: reaction chemistry and water balance. Biomass Conversion and Biorefinery. 4 (4), 311-321 (2014).
- Funke, A., Ziegler, F. Hydrothermal carbonization of biomass: A summary and discussion of chemical mechanisms for process engineering. Biofuels, Bioproducts and Biorefining. 4 (2), 160-177 (2010).
- Kruse, A., Funke, A., Titirici, M. -. M. Hydrothermal conversion of biomass to fuels and energetic materials. Current opinion in chemical biology. 17 (3), 515-521 (2013).
- Reza, M. T., Lynam, J. G., Uddin, M. H., Coronella, C. J. Hydrothermal carbonization: Fate of inorganics. Biomass and Bioenergy. 49, 86-94 (2013).
- Zhang, D., et al. Comparison study on fuel properties of hydrochars produced from corn stalk and corn stalk digestate. Energy. 165, 527-536 (2018).
- Huang, Y. -. B., Yang, Z., Dai, J. -. J., Guo, Q. -. X., Fu, Y. Production of high quality fuels from lignocellulose-derived chemicals: a convenient C-C bond formation of furfural, 5-methylfurfural and aromatic aldehyde. RSC Advances. 2 (30), 11211 (2012).
- Van de Vyver, S., Geboers, J., Jacobs, P. A., Sels, B. F. Recent Advances in the Catalytic Conversion of Cellulose. ChemCatChem. 3 (1), 82-94 (2011).
- Delidovich, I., Leonhard, K., Palkovits, R. Cellulose and hemicellulose valorisation: an integrated challenge of catalysis and reaction engineering. Energy & Environmental Science. 7 (9), 2803 (2014).
- Sevilla, M., Fuertes, A. B. The production of carbon materials by hydrothermal carbonization of cellulose. Carbon. 47 (9), 2281-2289 (2009).
- Yao, Z., Ma, X. Characteristics of co-hydrothermal carbonization on polyvinyl chloride wastes with bamboo. Bioresource technology. 247, 302-309 (2018).
- Funke, A., Ziegler, F. Hydrothermal carbonization of biomass: A summary and discussion of chemical mechanisms for process engineering. Biofuels, Bioproducts and Biorefining. (4), 160-177 (2010).
- Liu, Z., Balasubramanian, R. Upgrading of waste biomass by hydrothermal carbonization (HTC) and low temperature pyrolysis (LTP): A comparative evaluation. Applied Energy. 114, 857-864 (2014).
- Khalsa, J., Döhling, F., Berger, F. Foliage and Grass as Fuel Pellets-Small Scale Combustion of Washed and Mechanically Leached Biomass. Energies. 9 (5), 361 (2016).
- Saddawi, A., Jones, J. M., Williams, A., Le Coeur, C. Commodity Fuels from Biomass through Pretreatment and Torrefaction: Effects of Mineral Content on Torrefied Fuel Characteristics and Quality. Energy & Fuels. 26 (11), 6466-6474 (2012).
- Kaltschmitt, M., Hartmann, H., Hofbauer, H. . Energie aus Biomasse: Grundlagen, Techniken und Verfahren. , (2016).
- Fengel, D., Wegener, G. . Wood: Chemistry, Ultrastructure, Reactions. , (1989).
- Obernberger, I., Thek, G. Physical characterisation and chemical composition of densified biomass fuels with regard to their combustion behaviour. Biomass and Bioenergy. 27 (6), 653-669 (2004).
- Kenney, W. A., Sennerby-Forsse, L., Layton, P. A review of biomass quality research relevant to the use of poplar and willow for energy conversion. Biomass. 21 (3), 163-188 (1990).
- Tharakan, P. J., Volk, T. A., Abrahamson, L. P., White, E. H. Energy feedstock characteristics of willow and hybrid poplar clones at harvest age. Biomass and Bioenergy. 25 (6), 571-580 (2003).
- Liu, Z., Quek, A., Balasubramanian, R. Preparation and characterization of fuel pellets from woody biomass, agro-residues and their corresponding hydrochars. Applied Energy. , 1315-1322 (2014).
- Technischen Komitee ISO/TC 238. . "Solid biofuels" und Technisches Komitee CEN/TC 335 "Biogene Festbrennstoffe" Solid biofuels - Determination of calorific value (ISO 18125:2017); German version EN ISO 18125:2017. , (2017).
- Kambo, H. S., Dutta, A. A comparative review of biochar and hydrochar in terms of production, physico-chemical properties and applications. Renewable and Sustainable Energy Reviews. 45, 359-378 (2015).
- Knappe, V., et al. Low temperature microwave assisted hydrothermal carbonization (MAHC) reduces combustion emission precursors in short rotation coppice willow wood. Journal of Analytical and Applied Pyrolysis. 134, 162-166 (2018).
- Liu, Z., Quek, A., Kent Hoekman, S., Balasubramanian, R. Production of solid biochar fuel from waste biomass by hydrothermal carbonization. Fuel. 103, 943-949 (2013).
- Hoekman, S. K., Broch, A., Robbins, C., Zielinska, B., Felix, L. Hydrothermal carbonization (HTC) of selected woody and herbaceous biomass feedstocks. Biomass Conversion and Biorefinery. 3 (2), 113-126 (2013).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır