Method Article
Minipiglerde Tek Aşamalı Doku Mühendisliği Ürotelyal Tüpler için Cerrahi Model
Bu Makalede
Özet
Rekonstrüktif cerrahi için doku mühendisliği implantları, karmaşık ve pahalı iskele bileşenleri içeren zahmetli ex vivo kültürleme nedeniyle nadiren klinik öncesi çalışmaların ötesine geçer. Burada, otolog mikrogreftler içeren erişilebilir kollajen bazlı tübüler iskele ile üriner diversiyon için tasarlanmış tek aşamalı bir prosedür sunuyoruz.
Özet
Rekonstrüktif ameliyatlar genellikle greftleme dokusu eksikliği nedeniyle zorlanır. Ürogenital malformasyonların tedavisinde, konvansiyonel çözüm, hastada normal fonksiyonu yeniden sağlamak için bol miktarda olması nedeniyle ortotopik olmayan rekonstrüksiyon için gastrointestinal doku toplamaktadır. Vücuttaki doğal dokuların yeniden düzenlenmesinden sonraki klinik sonuçlar genellikle önemli morbidite ile ilişkilidir; Bu nedenle, doku mühendisliği bu cerrahi alanında özel bir potansiyele sahiptir. Önemli ilerlemelere rağmen, doku mühendisliği iskeleleri, esas olarak malzeme, üretim ve implantasyonun maliyetli ve karmaşık gereksinimleri nedeniyle geçerli bir cerrahi tedavi alternatifi olarak henüz kurulmamıştır. Bu protokolde, üriner diversiyon için bir kanal olarak tasarlanmış, otolog organa özgü doku parçacıkları ile gömülü, basit ve erişilebilir kollajen bazlı tübüler bir iskele sunuyoruz. İskele, birincil cerrahi prosedür sırasında inşa edilir, yaygın olarak bulunan cerrahi malzemeleri içerir ve geleneksel cerrahi beceriler gerektirir. İkinci olarak, protokol, implantasyon sonrası kısa vadeli in vivo sonuçları değerlendirmek için tasarlanmış bir hayvan modelini tanımlar ve prosedürde ek varyasyonlar olasılığı vardır. Bu yayın, otolog doku ve tübüler bir formun kullanımına özel önem vererek, prosedürü adım adım göstermeyi amaçlamaktadır.
Giriş
Ürogenital malformasyonlarda, genellikle hayati bir endikasyon üzerine fonksiyonel anatomiyi eski haline getirmek için rekonstrüktif cerrahi gerekebilir 1,2. Konvansiyonel cerrahi yaklaşımlar, hatalı biçimlendirilmiş veya eksik organları yeniden yapılandırmak için diğer organ sistemlerinden (gastrointestinal sistem gibi) doğal dokuları kullanmıştır; Bununla birlikte, sıklıkla ciddi postoperatif komplikasyon riski ile 3,4. Uzun süreli kateterizasyona ihtiyaç duyan nörojenik mesane disfonksiyonu olan hastalar için üriner diversiyon durumunda, apendiks veya yeniden uyarlanmış ince bağırsak segmentleri genellikle bir idrar kanalı oluşturmak için kullanılır 5,6. Doku mühendisliği, organa özgü özellikleri karşılayacak şekilde uyarlanabilen alternatif bir greftleme dokusu sunar ve böylece hastalar için postoperatif morbiditeyi en aza indirir 7,8. Çeşitli türlerdeki iskeleler kendi başlarına implante edilebilirken, tercihen otolog hücrelerle ek iskele hücreselleşmesinin implantasyon sonrası rejeneratif sonuçları iyileştirdiği gösterilmiştir 9,10,11,12,13,14. Bununla birlikte, doku mühendisliği iskeleleri genellikle karmaşık ve maliyetli bileşenlerden oluşur ve ikincisi, ex vivo hücre kültürü ve iskele tohumlama gereksinimleri zahmetli ve kaynak yoğundur. Bu faktörler, bu alanda onlarca yıl süren araştırmalara rağmen, doku mühendisliği iskelelerinin klinik çevirisini engellemiştir. Karmaşıklığın yanı sıra parasal ve materyalist gereksinimleri azaltarak, doku mühendisliği iskeleleri modern cerrahide hem nadir hem de daha yaygın prosedürleri ele alan geniş bir ölçekte uygulanabilir.
Kollajen daha önce hücre genişlemesi için uygun bir platform olarak kurulmuştur ve ayrıca hücreleri veya dokuyu cerrahi implantasyon için bir iskeleye bağlarken uygun bir biyo-yapıştırıcı görevi görür 15,16,17. Perioperatif otolog mikrogreftleme, birincil prosedür sırasında ilgilenilen dokuyu toplayarak ve doğrudan yeniden implante ederek ex vivo hücre kültürü ihtiyacını ortadan kaldırır. Rezeke edilen dokuyu daha küçük parçacıklar halinde kıyarak, yüzey alanı ve büyüme potansiyeli arttırılır, bu da iskele18 üzerinde daha büyük bir genleşme oranına izin verir. Kollajen bazlı iskele, özellikle ürogenital rekonstrüksiyonlara bağlı kalmaz, ancak teorik olarak içi boş organ rekonstrüksiyonunun birden fazla alanına uygulanabilir.
Bu yazıda, hem kollajeni gömülü otolog ürotelyal mikrogreftlerle birleştiren boru şeklinde bir iskele inşası için bir protokol hem de iskelenin teknik fizibilitesi ve güvenliğinin yanı sıra rejeneratif performansını in vivo olarak değerlendiren bir minipig modeli sunuyoruz. Model, burada sunulan protokol ve yöntem kullanılarak 10 tam yetişkin dişi minipigde değerlendirildi. İskelenin ana avantajı, yapının basitliği ve tek aşamalı implantasyondur, bu da hastayı sonraki birkaç cerrahi prosedürden korur. İşlem, geleneksel cerrahi ortamlarda düzenli cerrahi personel tarafından yapılabilir ve standart ekipman ve malzeme gerektirir. Hayvan modeli, implantasyonu incelemek için kontrollü bir ortama izin verirken, hayvan kolayca normal davranışa dönerken, iskele ve prosedürde değişiklikler uygulama olasılığı da eklenir.
Protokol
Bu deney, hayvan deneklerin laboratuvar kullanımına ilişkin Avrupa mevzuatına uygun olarak ve Danimarka Gıda ve Tarım Bakanlığı tarafından verilen etik izin alındıktan sonra AAALAC tarafından akredite edilmiş bir deney tesisinde gerçekleştirilmiştir (Ref. no. 2022-15-0201-01206).
1. Cerrahi prosedür
- Hayvan hazırlama
- Dişi bir yetişkin Göttingen minipigini ameliyat öncesi en az 12 saat hızlı tutun.
- Ameliyat masasını tüm steril kaplarla birlikte aşağıda anlatıldığı gibi hazırlayın.
- Tam büyümüş standart boyutlu minipigler için, hayvanı 1.25 mL ketamin (100 mg / mL), 6.25 mL ksilazin (20 mg / mL), 1.25 mL metadon (10 mg / mL) ve 2 mL butorphanol (10 mg / mL) (daha sonra sedasyon karışımı olarak anılacaktır) içinde süspanse edilmiş 125 mg zolazepam ve 125 mg tiletamin çözeltisi ile 1.0-1.4 mL / 10 kg ile intramüsküler enjeksiyon ile sedasyon ile sedasyon yapın.
- Görsel kılavuzluğunda endotrakeal entübasyon gerçekleştirin. Anesteziyi yaşamsal belirtiler ve göz ve interdigital refleks testi ile onaylayın. Oftalmik merhemi iki taraflı olarak uygulayın.
- Bilateral kulak damarı kateterleri takın ve propofol (10-15 mg/kg/saat) ve fentanil (5-15 mg/kg/saat) ile anesteziyi sürdürün.
- 8 Fr'lik bir idrar sondası yerleştirin ve uygun boyutta bir luer kilit şırıngası kullanarak mesaneyi 250 mL fizyolojik olarak ılıman izotonik salin ile doldurun.
- Domuzu sırtüstü pozisyona getirin, ardından karnınızı yerle bir edin ve ovalayın. % 70 etanol ile iki tur daha cilt temizliğinden sonra, cerrahi alanı steril örtü ile çerçeveleyin.
- Doku toplama ve cerrahi iskele implantasyonu
- Neşter ve koter ile standart bir alt orta hat laparotomisi yapın, cildi, kası ve peritonu ayırın ve intraperitoneal idrar kesesini yaraya çekin.
- Ön mesane duvarında profilaktik hemostaz yapın ve kalan mesane duvarını hızlı emilebilir örgülü bir koşu ipliği ile kapatırken 1cm2'lik bir proksimal açıklık bırakarak2 cm2'lik bir tam duvar segmentini çıkarın.
- Rezeke edilen örneğin mukozal tabakasını dikkatlice inceleyin ve iskele gömmek için 2cm2'lik bir mukozal örneği 1 mm2 mikrogreftlere kıyın (aşağıda bölüm 2'de açıklanmıştır).
- İskeleyi tamamladıktan sonra, boru şeklindeki yapıyı yavaş emilebilir monofilament çalışan bir sütür ile ön mesane duvarında kalan açıklığa anastomoz edin.
- Boru şeklindeki iskeleyi yamalamak için pubovezikal ligamentten bir peritoneal flep kullanın ve boru şeklindeki iskeleye bir intraluminal 14 Fr antegrad kolon lavmanı (ACE) tıpası yerleştirin.
- İdrarın dışarı sızmasını önlemek için kanalın distal ucunu yavaş emilebilir 4-0 monofilament sütür ile bağlayın ve anastomoz açıklığını doğrulamak için mesane kateteri yoluyla şırıngalarla toplam 250 mL steril salin enjekte edin.
- Transfasyal bir kanalı orta hatta lateral, sağ taraftaki kaudal meme bezine 2-3 cm kaudal olarak künt bir şekilde inceleyin ve kanalı deri altı bir cebe yerleştirin. Konumu cilt seviyesinde işaretlemek için distal kanalı iki transkutan, emilemeyen monofilament sütürle sabitleyin.
- Karın kasının ön kas fasyasını yavaş emilebilir monofilament koşu sütürü ile kapatın, subkutisi hızlı emilebilir örgülü koşu sütürü ile uyarlayın ve cildi emilmeyen monofilament koşu sütürü ile kapatın.
- Anesteziyi bıraktıktan sonra, hayvanı ekstübe edin ve tamamen yürüyene ve güvenli bir şekilde içip yiyebilecek duruma gelene kadar ahırlarda gözlemleyin.
2. İskele yapımı
- Kompozit iskelenin hazırlanması
- Ameliyattan önce (en fazla 2 saat), daha önce tarif edildiği gibi sıvı bir sıçan kuyruğu kollajen tip I çözeltisi hazırlayın17. Kısacası, kollajen çözeltisine 10x minimum esansiyel ortamın (MEM) 4: 1'ini ekleyin ve pH'ı 1 M NaOH ile 7.4'e yaklaştırın ve son olarak 1.64 mg / mL'lik bir nihai kollajen konsantrasyonunu hedefleyerek 1x MEM ekleyin. Solüsyonu daha fazla kullanılana kadar buz üzerinde steril bir şişede saklayın.
- Cerrahi doku rezeksiyonu ve kıyma işleminden sonra, mukozal parçacıkları (yani mikrogreftleri) 1: 6 genişleme oranına sahip 2 cm x 6 cm'lik biyolojik olarak parçalanabilen bir ağa manuel olarak yerleştirin (ör., 2cm2'lik bir mukozal doku 12cm2'lik bir ağa genişletilir) forseps kullanarak.
- Steril bir çelik plakanın üzerine 1 cm x 3 cm x 6 cm (yükseklik x genişlik x uzunluk) ölçülerinde steril bir dikdörtgen çelik kalıp hazırlayın ve ağı, mikrogreftler yukarı bakacak şekilde çelik kalıba yerleştirin. 20 mL kollajen solüsyonunu kalıba nazikçe dökün ve mikrogreftleri ağdan atmamaya dikkat edin. Tüm yapıyı 38 °C steril bir ısıtma odasına aktarın ve beş dakika katılaşmaya bırakın.
- Yeterli katılaşmadan sonra, hidrojeli delikli bir çelik plaka üzerinde duran naylon bir ağ üzerine kaydırın ve kalıbı yavaşça çıkarın.
- Jelenin üzerine bir naylon ağ ve ardından çelik bir plaka yerleştirerek hidrojelden suyu dışarı atın ve ardından çelik plakanın üzerine yerleştirilmiş 120 g ağırlıkla (bu durumda gömme için kullanılan çelik kalıba eşdeğer) 5 dakika boyunca pasif olarak sıkıştırın.
- Kompresyondan sonra, düzleştirilmiş iskeleyi biyolojik olarak parçalanabilen bir stent etrafına, mikrogreftler stentin karşısına bakacak şekilde, 5 cm x 0,6 cm (uzunluk x iç çap) ölçülerinde yuvarlayın ve iskeleyi yavaş emilebilir monofilament çalışan bir sütür ile uzunlamasına yerine dikin. Tamamlanan kanal artık cerrahi implantasyon için hazırdır.
3. Ameliyat sonrası yönetim
- Analjezi ve antibiyotik profilaksisi
- İlk 3 gün buprenorfin (0.05-0.1 mg / kg / 8 saat intravenöz olarak), ilk 4 gün boyunca meloksikam (0.4 mg / kg / gün intramüsküler veya oral olarak) ve trimetoprim (2.7 mg / kg / gün intramüsküler veya 4.2 mg / kg / gün oral) ve sülfadoksin (13.3 mg / kg / gün intramüsküler veya 20.8 mg / kg / gün oral) uygulayın. Kas içi enjeksiyonları, hayvan hala anestezi altındayken ameliyat sonrası uygulayın.
- Dış ven kateterlerinin ve dikiş materyalinin kemirilmesini önlemek için hayvanları tek başına barındırın. Pleksiglas pencerelerden komşu minipiglerle görsel temas ve kalemler arasında burun teması olasılığı sağlayın. Günlük taze saman ve saman ile oyuncaklar ve su temini ad libitum sağlayın ve günde iki kez besleyin.
- Hayvanları doğal davranış, yeme alışkanlıkları, idrar ve dışkı üretimi açısından günlük olarak izleyin ve vücut ağırlığını haftalık olarak değerlendirin.
- Gözlem süresinin sonunda (6 hafta), hayvanları 1-1.4 mL / 10 kg intramüsküler sedasyon karışımı enjeksiyonu ile sedasyon yapın ve hayvanı öldürücü bir pentobarbital enjeksiyon (intravenöz olarak 100 mg / kg) ile sonlandırın.
4. Ölüm sonrası değerlendirmeler
- Kaba anatomi
- Sonlandırmadan sonra, distal kanalı cilt seviyesinde inceleyin ve ACE durdurucusunu çıkarın. Üretrayı plastik bir kelepçe ile kapatın ve bir kateter kullanarak distal kanal açıklığı yoluyla izotonik salin içinde 250 mL 1:20 kontrast iohexol solüsyonu enjekte edin.
- Hayvanı 64 kesitli bilgisayarlı tomografi tarayıcısı ile değerlendirin. Çok düzlemli rekonstrüksiyon kullanarak görüntüleri görselleştirin ve tıbbi görüntü işleme yazılımını kullanarak tüm görüntüleri analiz edin.
- Doğal üretra yoluyla 16.2 Fr esnek sistoskop ile mesane ve kanal lüminesinin endoskopik muayenesini yapın.
- Herhangi bir brüt anatomik bulguyu dikkatlice değerlendirirken kanalı blok halinde inceleyin. Ek olarak, tam duvar mesane biyopsilerini kanal anastomozuna 2 cm mesafeyle rezeke edin ve referans değerler için benzer şekilde işlem yapın.
- Histolojik işleme
- Eksize edilen numuneyi 24 saat boyunca% 10 formalin içinde sabitleyin.
- Kanalı bir neşter ile ortogonal olarak proksimal, medial ve distal kanal segmentlerinin eşit büyüklükte ayrı bölümlerine bölün. Numuneleri artan etanol konsantrasyonları ile kurutun ve mikrotom kesitinden önce parafine gömün.
- Hematoksilen ve eozin (H & E) ve pansitokeratin CK-AE ile 5 μm'lik kesitleri boyayın ve dijital histoloji slayt tarayıcı ile tarayın.
Sonuçlar
Bu çalışmada, kollajen bazlı tübüler bir iskelede in vivo ürotelyal doku genişlemesi sağlanmıştır. İskeleyi perioperatif olarak toplanan ve işlenen otolog doku parçacıkları ile gömerek, prosedür, ameliyat sonrası eşzamanlı immünosupresif tedaviye gerek kalmadan tek aşamalı iskele implantasyonuna izin verir. Cerrahi kullanım, iskelenin biyolojik olarak parçalanabilen bir ağ ve stent ile güçlendirilmesiyle sağlanır (Şekil 1). 6 haftalık gözlemden sonra, makroskopik doku değerlendirmesi konak reddi veya enfeksiyon belirtisi göstermedi ve tübüler iskele açık ve engelsiz olarak ortaya çıktı (Şekil 2). Histolojik değerlendirmelerden, iskelenin tamamını kaplayan ürotelyal kökenli tabakalı bir luminal epitel görülmektedir ve takviye edici biyomateryallerin kalıntıları 6 hafta sonra hala görülebilmektedir (Şekil 3).
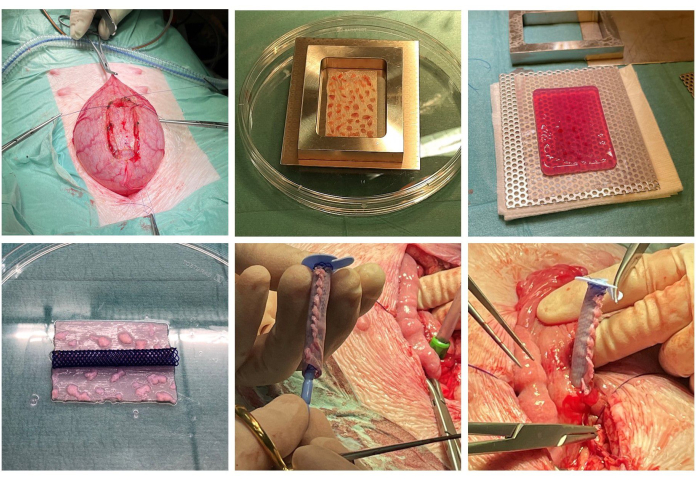
Şekil 1: İskele yapımı ve implantasyonu. Mesane dokusu perioperatif olarak diseke edilir (sol üst). Kıyılmış mukozal mikrogreftler cerrahi bir ağ (üst orta) üzerine genişletilir ve katılaşmış kollajen içine gömülür (sağ üst). Kollajen suyu dışarı atmak için sıkıştırılır ve bir stent hazırlanır (sol altta). İskele stentin etrafına boru şeklinde yerleştirilir ve stentin içine (alt, orta) bir ACE tıpa yerleştirilir. Mesane kısmen kapatılır ve yapı son olarak orijinal doku eksizyonu bölgesinde (sağ altta) mesaneye dahil edilir. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
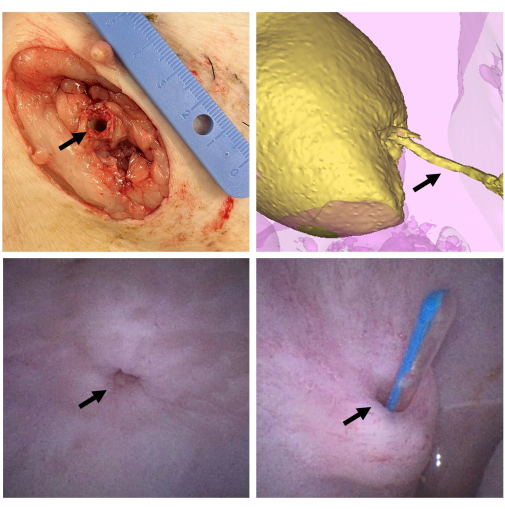
Şekil 2: İskele makroskopik değerlendirmesi. 6 hafta sonra, hayvana ötenazi yapılır ve iskele (ok) cilt seviyesinde (sol üst) disseke edilir. Mesane kontrast (sarı) ile doldurulur ve kanalı (ok) açıklık ve darlık oluşumu belirtileri (sağ üst) açısından değerlendirmek için BT taraması yapılır. 6 hafta sonra mesaneyi ve anastomozu (ok) değerlendirmek için üretra yoluyla sistoskopi yapılır (sol altta). Kanal, dış açıklıktan ve mesaneye (sağ altta) bir kateter (ok) yerleştirilerek açıklık açısından bir kez daha test edilir. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
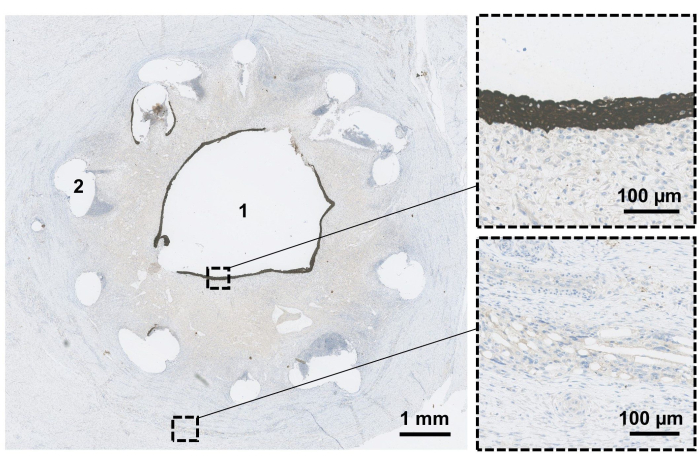
Şekil 3: İskele mikroskobik değerlendirmesi. Rezeke edilen kanal fikse edilir ve kanalı proksimal-distal yönde değerlendirmek için ortogonal enine kesitler yapılır. 6 hafta sonra, epitelizasyonu doğrulamak için kanal lümeni (1) değerlendirilir (büyütülmüş üst). Biyolojik olarak parçalanabilen stent (2) ve ağ malzemelerinin (büyütülmüş alt) kalıntıları bu noktada hala görülebilir. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
Tartışmalar
Bu protokol, gelecekteki rekonstrüktif ameliyatlar için basit ve ulaşılabilir bir teknik sunar. Otolog hücre genişlemesi de dahil olmak üzere doku mühendisliğinde yaygın bir dezavantaj, cerrahi implantasyondan önce gerekli olan pahalı ve önemli hazırlık adımlarıdır. Otolog mikrogreftleme, bu adımların çoğunu basitleştirebilir ve potansiyel olarak tek aşamalı prosedürlere izin verebilir. Kompleks histolojik varlıkların otomatik nakledilmesiyle, pro-rejeneratif parakrin sinyalleme indüklenir18. Daha önceki çalışmalarda, mikrogreftlerin tek başına bir iskeleye uygun şekilde bağlanmadıkça fiziksel ortamlara karşı savunmasız olduğunu deneyimlemiştik 15,19. Kolajen, in vitro doku genişlemesi için uygun bir ortam olarak incelenmiştir ve uygun biyouyumluluğu ve ticari mevcudiyeti nedeniyle amacımız için seçilmiştir. Burada sunulan kompozit iskele daha önce mikrogreft gömme ve kollajen konsantrasyonlarındaki varyasyonları değerlendiren in vitro deneyler sırasında optimize edilmiştir 20,21,22. İn vivo testlerden önce, geçirgenlik, biyomekanik ve bozunma ile ilgili iskele özellikleri in vitro20 olarak değerlendirilmiştir. Ayrıca, in vivo iskele bazlı doku genişlemesi daha önce kemirgen ve tavşan modellerindedoğrulanmıştır 21,22.
Cerrahi model, pediatrik veya ergen hastalarda nörojenik mesane disfonksiyonu için üriner diversiyonun klinik ortamını taklit eden iskelenin tübüler bir versiyonunu değerlendirmek için seçildi. Kritik adımlar, mukozal mikrogreftlerin tam diseksiyonunu ve rezeksiyon zamanından iskele gömülmesine kadar nemli bir ortamın korunmasını içerir. Diğer bir kritik adım, uygun hidrojel katılaşmasını içerir; Kollajenin dikkatli bir şekilde pipetlenmesi, jel içinde hava kabarcıklarının oluşmamasını sağlar ve doğru sıcaklık ayarları ve bileşen çözeltileri, jelin düzgün şekilde katılaşmasını sağlar. Katılaşmış bir jel elde edilmemesi, kollajen delaminasyonu ve mikrogreft dekolmanı riskini artıracaktır. Cerrahi kısım için, mekanik travma veya ayrışma nedeniyle mikrogreftlere zarar vermemek için implantasyon sırasında dikkatli kullanım çok önemlidir. Karın kapatılmadan önce, mesaneyi sıvılarla şişirerek sıvı açıklığı dikkatlice ele alınmalıdır.
Tekniğin sınırlamaları, besin maddelerinin dış ortamdan mikrogreftlere difüzyonu ile ilgili sezgisel olarak üst sınırlara sahip olan iskelenin kalınlığını içerir. Öte yandan, iskele kalınlığındaki bir azalma, uygun olmayan şekilde yüksek geçirgenliğe ve idrar sızıntısına neden olabilir. Mevcut bileşimimiz, değişen kollajen konsantrasyonlarında hücre yenilenmesininkarşılaştırıldığı önceki in vitro değerlendirmelere dayanmaktadır 20. Otolog dokuların mikrogreftlenmesi aynı zamanda sağlıklı greft dokusuna dayanır, bu da mevcut prosedürü kanserli yeniden transplantasyon riskinin uygun şekilde göz ardı edilemediği malign hastalıklar için uygun hale getirmez23; Bununla birlikte, mevcut teknik, bunun bir risk olarak kabul edilmediği fonksiyonel işeme bozukluğu olan vakalar için tasarlanmıştır. Model, klinik ortamdan (yani apandisikovezikostomi prosedürü) birkaç adımı taklit etse de, bu deney, kanal distal olarak bağlandığından, üriner diversiyon için tamamen işlevsel bir stoma kullanmaz. Ayrıca, klinik komplikasyonlar yaşam boyu ortaya çıkabileceğinden, 6 haftalık bir gözlem süresi, darlıklar ve kontinans ile ilgili spesifik sonuçlar hakkında sınırlı bilgi sağlayabilir. Bu nedenle, iyileşmiş kanal cilt seviyesine anastomoz edildikten sonra çalışmaya 6 aylık ek bir takip eklenebilir.
Bu tekniğin perspektifi, mikrogreft doku kökenli ve destekleyici biyomateryalin diğer ilgili alternatiflerle değiştirilmesi durumunda evrensel uygulamalara olanak tanıyan basit tasarımla ilgilidir. Bu bileşenler, iskele mukavemeti, elastikiyet ve biyolojik bozunma ile ilgili organa özgü amaçlara uyacak şekilde değiştirilebilir. Son olarak, erişilebilir ve düşük maliyetli harcamalar, tekniğin tekrarlanabilirliğine ve genişletilmiş bir çevirisine izin verir.
Açıklamalar
Yazarların beyan edebilecekleri herhangi bir çıkar çatışması yoktur.
Teşekkürler
Yazarlar, Kopenhag Üniversitesi Deneysel Tıp Bölümü (AEM) personeline, hayvan ameliyatları ve yetiştiriciliğinin planlanması ve yürütülmesi konusunda yardım için ve ELLA-CS, sro, Hradec Kralove, Çek Cumhuriyeti, çalışmada kullanılan özelleştirilmiş biyobozunur stentler sağladıkları için teşekkür eder. İsveç Tıbbi Araştırma Derneği, Promobilia Vakfı, Rydbeck Vakfı, Samariten Vakfı, Pediatrik Sağlık Hizmetleri Vakfı, Stockholm'deki Frimurare Barnhuset Vakfı ve Novo Nordisk Vakfı (NNFSA170030576) tarafından mali destek sağlandı.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 10x MEM | Gibco, Thermo Fisher Scientific, Waltham, US | 2517592 | Collagen preparation |
| 1x MEM | Gibco, Thermo Fisher Scientific, Waltham, US | 2508924 | Collagen preparation |
| Ambu aScope 4 Cysto | Ambu A/S, Ballerup, DK | 1000682507 | Cystoscope |
| Aquaflush ACE stopper | Abena, Taastrup, DK | ACE12/220501 | ACE stopper |
| Borgal vet inj opl 200 + 40 mg/mL | Ceva Animal Health A/S | 510460 | Sulfonamide/Trimethoprim |
| Bupaq multidose vet 0.3 mg/mL | Salfarm Danmark A/S, DK | 502763 | Buprenorphin |
| Butomidor vet inj 10 mg/mL | Salfarm Danmark A/S, DK | 531943 | Buthorphanol |
| Comfortan vet inj 10 mg/mL | Dechra Veterinary Products A/S, DK | 492312 | Metadone |
| Ethilon suture 3-0 | Ethicon, Johnson & Johnson, New Brunswick, US | SGBCXV | Monofilament non-resorbable |
| Fentanyl inj 50 µg/mL(hamel) | Hameln Pharma ApS, DK | 432520 | Fentanyl |
| Ketador vet inj 100 mg/mL | Salfarm Danmark A/S, DK | 115727 | Ketamine |
| Metacam inj 20 mg/mL t.cattle/pig/horse | Boehringer Ingelheim Animal, DE | 6443 | Meloxcicam |
| Metacam oral suspension 15 mg/mL pigs | Boehringer Ingelheim Animal, DE | 482780 | Meloxcicam |
| Omnipaque | GF Healthcare, Oslo, NO | 16173849 | Contrast for CT |
| Pancytokeratin CK-AE | DAKO Agilent, US | GA053 | Clone AE1/AE3 |
| PDS suture 3-0 | Ethicon, Johnson & Johnson, New Brunswick, US | SEMMTQ | Monofilament slow-resorbable |
| Prolene suture 4-0 | Ethicon, Johnson & Johnson, New Brunswick, US | PGH187 | Monofilament non-resorbable |
| Propolipid t.inj/inf 10 mg/mL | Fresenius Kabi, DK | 21636 | Propofol |
| Rat-tail collagen type I | First Link Ltd, Wolverhampton, UK | 60-30-810 | 2.06 mg/mL protein in 0.6% acetic acid |
| Suprim vet 20 + 100 mg (Solution for use in drinking water) | Dechra Veterinary Products A/S, DK | 33661 | Sulfonamide/Trimethoprim |
| SX-ELLA Degradable Biliary DV stent | ELLA-CS, Trebes, CZ | S23000056-01 | ø 6 mm x 60 mm |
| Vicryl mesh | Ethicon, Johnson & Johnson, New Brunswick, US | VM1208 | Mesh |
| Vicryl suture 4-0 | Ethicon, Johnson & Johnson, New Brunswick, US | SMBDGDR0 | Braided fast-resorbable |
| Xysol vet inj 20 mg/mL | ScanVet Animal Health A/S, DK | 54899 | Xylazine |
| Zoletil 50 vet plv/sol t.inj 25 + 25 mg/mL | Virbac Danmark A/S, DK | 568527 | Tiletamine and Zolazepam |
Referanslar
- Surer, I., Ferrer, F. A., Baker, L. A., Gearhart, J. P. Continent urinary diversion and the exstrophy-epispadias complex. J Urol. 169 (3), 1102-1105 (2003).
- Cranidis, A., Nestoridis, G. Bladder augmentation. Int Urogynecol J Pelvic Floor Dysfunct. 11 (1), 33-40 (2000).
- Atala, A., Bauer, S. B., Hendren, W. H., Retik, A. B. The effect of gastric augmentation on bladder function. J Urol. 149 (5), 1099-1102 (1993).
- Husmann, D. A. Mortality following augmentation cystoplasty: A transitional urologist's viewpoint. J Pediatr Urol. 13 (4), 358-364 (2017).
- Mitrofanoff, P. Trans-appendicular continent cystostomy in the management of the neurogenic bladder. Chir Pediatr. 21 (4), 297-305 (1980).
- Leslie, B., Lorenzo, A. J., Moore, K., Farhat, W. A., Bägli, D. J., Pippi Salle, J. L. Long-term followup and time to event outcome analysis of continent catheterizable channels. J Urol. 185 (6), 2298-2302 (2011).
- Horst, M., Eberli, D., Gobet, R., Salemi, S. Tissue engineering in pediatric bladder reconstruction-The road to success. Front Pediatr. 7, 91(2019).
- Ajalloueian, F., Lemon, G., Hilborn, J., Chronakis, I. S., Fossum, M. Bladder biomechanics and the use of scaffolds for regenerative medicine in the urinary bladder. Nat Rev Uro. 15 (3), 155-174 (2018).
- Dorin, R. P., Pohl, H. G., De Filippo, R. E., Yoo, J. J., Atala, A. Tubularized urethral replacement with unseeded matrices: what is the maximum distance for normal tissue regeneration. World J Uro. 26 (4), 323-326 (2008).
- El Kassaby, A. W., AbouShwareb, T., Atala, A. Randomized comparative study between buccal mucosal and acellular bladder matrix grafts in complex anterior urethral strictures. J Urol. 179 (4), 1432-1436 (2008).
- Casarin, M., et al. Porcine small intestinal submucosa (SIS) as a suitable scaffold for the creation of a tissue-engineered urinary conduit: Decellularization, biomechanical and biocompatibility characterization using new approaches. Int J Mol Sci. 23 (5), 2826(2022).
- Casarin, M., et al. A novel hybrid membrane for urinary conduit substitutes based on small intestinal submucosa coupled with two synthetic polymers. J Funct Biomater. 13 (4), 222(2022).
- Drewa, T. The artificial conduit for urinary diversion in rats: a preliminary study. Transplant Proc. 39 (5), 1647-1651 (2007).
- Liao, W., et al. Tissue-engineered tubular graft for urinary diversion after radical cystectomy in rabbits. J Surg Res. 182 (2), 185-191 (2013).
- Reinfeldt Engberg, G., Lundberg, J., Chamorro, C. I., Nordenskjöld, A., Fossum, M. Transplantation of autologous minced bladder mucosa for a one-step reconstruction of a tissue engineered bladder conduit. Biomed Res Int. 2013, 212734(2013).
- Ajalloueian, F., Nikogeorgos, N., Ajalloueian, A., Fossum, M., Lee, S., Chronakis, I. S. Compressed collagen constructs with optimized mechanical properties and cell interactions for tissue engineering applications. Int J Biol Macromol. 108, 158-166 (2018).
- Chamorro, C. I., Zeiai, S., Engberg, G. R., Fossum, M. Minced tissue in compressed collagen: A cell-containing biotransplant for single-staged reconstructive repair. J Vis Exp. (108), e53061(2016).
- Juul, N., et al. Insights into cellular behavior and micromolecular communication in urothelial micrografts. Sci Rep. 13 (1), 13589(2023).
- Reinfeldt Engberg, G., Chamorro, C. I., Nordenskjöld, A., Fossum, M. Expansion of submucosal bladder wall tissue in vitro and in vivo. Biomed Res Int. 2016, 5415012(2016).
- Juul, N., Ajalloueian, F., Willacy, O., Chamorro, C. I., Fossum, M. Advancing autologous urothelial micrografting and composite tubular grafts for future single-staged urogenital reconstructions. Sci Rep. 13 (1), 15584(2023).
- Willacy, O., Juul, N., Taouzlak, L., Chamorro, C. I., Ajallouiean, F., Fossum, M. A perioperative layered autologous tissue expansion graft for hollow organ repair. Heliyon. 10 (3), e25275(2024).
- Chamorro, C. I., et al. Exploring the concept of in vivo guided tissue engineering by a single-stage surgical procedure in a rodent model. Int J Mol Sci. 23 (20), 12703(2022).
- Casarin, M., Morlacco, A., Dal Moro, F. Bladder substitution: The role of tissue engineering and biomaterials. Process. 9 (9), 1643(2021).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiDaha Fazla Makale Keşfet
This article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır