A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
التوصيف المغناطيسي للمواد الوسيطة في الكيمياء الكهربائية للحالة الصلبة للأطر العضوية الفلزية النشطة للأكسدة والاختزال
In This Article
Summary
يمكن أن توفر المسوحات المغناطيسية خارج الموقع مباشرة معلومات مجمعة ومحلية على قطب مغناطيسي للكشف عن آلية تخزين الشحن خطوة بخطوة. هنا ، يتم إثبات رنين الدوران الإلكتروني (ESR) والقابلية المغناطيسية لمراقبة تقييم الأنواع البارامغناطيسية وتركيزها في إطار عضوي معدني نشط للأكسدة والاختزال (MOF).
Abstract
كان تخزين الطاقة الكهروكيميائية تطبيقا نوقش على نطاق واسع لأطر الأكسدة والاختزال المعدنية العضوية النشطة (MOFs) في السنوات ال 5 الماضية. على الرغم من أن الأطر الفلزية العضوية تظهر أداء متميزا من حيث السعة الوزنية أو المساحية والاستقرار الدوري ، إلا أن آلياتها الكهروكيميائية للأسف ليست مفهومة جيدا في معظم الحالات. ولم تقدم التقنيات الطيفية التقليدية، مثل التحليل الطيفي للأشعة السينية الضوئية الإلكترونية (XPS) والبنية الدقيقة لامتصاص الأشعة السينية (XAFS)، سوى معلومات غامضة ونوعية عن تغيرات التكافؤ في بعض العناصر، وغالبا ما تكون الآليات المقترحة بناء على هذه المعلومات موضع جدل كبير. في هذه المقالة ، نبلغ عن سلسلة من الطرق الموحدة ، بما في ذلك تصنيع الخلايا الكهروكيميائية ذات الحالة الصلبة ، وقياسات الكيمياء الكهروكيميائية ، وتفكيك الخلايا ، وجمع المواد الكهروكيميائية الوسيطة للأطر الفلزية العضوية ، والقياسات الفيزيائية للمواد الوسيطة تحت حماية الغازات الخاملة. باستخدام هذه الطرق للتوضيح الكمي لتطور الحالة الإلكترونية والدوران ضمن خطوة كهروكيميائية واحدة من الأطر الفلزية العضوية النشطة للأكسدة والاختزال ، يمكن للمرء أن يقدم رؤية واضحة لطبيعة آليات تخزين الطاقة الكهروكيميائية ليس فقط للأطر الفلزية العضوية ، ولكن أيضا لجميع المواد الأخرى ذات الهياكل الإلكترونية المرتبطة بشدة.
Introduction
منذ أن تم إدخال مصطلح الإطار المعدني العضوي (MOF) في أواخر تسعينيات القرن العشرين ، وخاصة في أواخر القرن العشرين ، نشأت المفاهيم العلمية الأكثر تمثيلا المتعلقة بالأطر الفلزية العضوية من مساميتها الهيكلية ، بما في ذلك تغليف الضيف ، والفصل ، والخصائص التحفيزية ، واستشعارالجزيئات 1،2،3،4. وفي الوقت نفسه، سرعان ما أدرك العلماء أنه من الضروري أن تمتلك الأطر الفلزية العضوية خصائص إلكترونية مستجيبة للمحفزات من أجل دمجها في الأجهزة الذكية الحديثة. أدت هذه الفكرة إلى تفريخ وازدهار عائلة MOF ثنائية الأبعاد (2D) في السنوات ال 10 الماضية ، مما فتح الباب أمام الأطر الفلزية العضوية للعب أدوار رئيسية في الإلكترونيات5 ، وبشكل أكثر جاذبية ، في أجهزة تخزين الطاقة الكهروكيميائية6. تم دمج هذه الأطر الفلزية العضوية ثنائية الأبعاد كمواد نشطة في البطاريات المعدنية القلوية والبطاريات المائية والمكثفات الزائفة والمكثفات الفائقة7،8،9 ، وأظهرت قدرة هائلة بالإضافة إلى استقرار ممتاز. ومع ذلك ، لتصميم 2D MOFs ذات أداء أفضل ، من الأهمية بمكان فهم آليات تخزين الشحن الخاصة بهم بالتفصيل. لذلك ، تهدف هذه المقالة إلى توفير فهم شامل للآليات الكهروكيميائية للأطر الفلزية العضوية ، والتي يمكن أن تساعد في التصميم الرشيد للأطر الفلزية العضوية الأفضل أداء لتطبيقات تخزين الطاقة.
في عام 2014 ، أبلغنا لأول مرة عن الآليات الكهروكيميائية الصلبة للأطر الفلزية العضوية مع مواقع نشطة للأكسدة والاختزال على كل من الكاتيونات المعدنية والروابط10,11. تم تفسير هذه الآليات بمساعدة تقنيات طيفية مختلفة في الموقع وخارج الموقع ، مثل التحليل الطيفي للأشعة السينية الضوئية (XPS) ، والبنية الدقيقة لامتصاص الأشعة السينية (XAFS) ، وحيود الأشعة السينية (XRD) ، والرنين المغناطيسي النووي في الحالة الصلبة (NMR). منذ ذلك الحين ، أصبح نموذج البحث هذا اتجاها في دراسات الكيمياء الكهربائية للحالة الصلبة للمواد الجزيئية12. تعمل هذه الطرق بشكل جيد لتحديد أحداث الأكسدة والاختزال للأطر الفلزية العضوية التقليدية مع روابط سد الكربوكسيلات ، حيث أن المدارات الجزيئية ومستويات الطاقة لكتل بناء الكتلة المعدنية والروابط العضوية مستقلة تقريبا عن بعضها البعض في هذه الأطر الفلزيةالعضوية 12،13.
ومع ذلك ، عند مواجهة الأطر الفلزية العضوية 2D المرتبطة بقوة مع اقتران π-d كبير ، تم الكشف عن قيود هذه الأساليب الطيفية. أحد هذه القيود هو أن مستويات النطاق لمعظم الأطر الفلزية العضوية ثنائية الأبعاد المذكورة أعلاه لا يمكن اعتبارها مزيجا بسيطا من العناقيد المعدنية والروابط ، بل هي بالأحرى تهجين لها ، في حين أن معظم الطرق الطيفية توفر فقط معلومات نوعية متوسطة حول حالات الأكسدة14. القيد الآخر هو أن تفسير هذه البيانات يعتمد دائما على افتراض المدارات الذرية الموضعية. لذلك ، عادة ما يتم تجاهل الحالات الوسيطة مع تهجين الربيطة المعدنية والحالات الإلكترونية غير المتمركزة ووصفها بشكل غير صحيح باستخدام هذه الطرق الطيفية فقط15. من الضروري تطوير مجسات جديدة للحالات الإلكترونية لهذه المواد الوسيطة الكهروكيميائية ليس فقط للأطر الفلزية العضوية ثنائية الأبعاد ، ولكن أيضا للمواد الأخرى ذات الهياكل الإلكترونية المترافقة أو المرتبطة بقوة ، مثل الأطر العضوية التساهمية16 ، والموصلات الجزيئية ، والبوليمرات المترافقة17.
الأدوات الأكثر شيوعا وقوة لتقييم الهياكل الإلكترونية للمواد هي رنين الدوران الإلكتروني (ESR) وقياسات الحساسية المغناطيسية لجهاز التداخل الكمي فائق التوصيل (SQUID)18,19. نظرا لأن كلاهما يعتمد على الإلكترونات غير المتزاوجة في النظام ، يمكن أن توفر هذه الأدوات معلومات مبدئية حول كثافات الدوران وتوزيعات الدوران وتفاعلات الدوران المغزلي. يوفر ESR كشفا حساسا للإلكترونات غير المتزاوجة ، بينما يعطي قياس الحساسية المغناطيسية المزيد من الإشارات الكمية للخصائص العليا20. لسوء الحظ ، تواجه كلتا التقنيتين تحديات كبيرة لا مفر منها عند استخدامها لتحليل المواد الوسيطة الكهروكيميائية. وذلك لأن العينات المستهدفة ليست نقية ، بل هي خليط من المواد المستهدفة ، والمواد المضافة الموصلة ، والموثق ، والمنتج الثانوي من المنحل بالكهرباء ، وبالتالي فإن البيانات التي تم الحصول عليها21,22 هي مجموع المساهمات من كل من المواد والشوائب. وفي الوقت نفسه ، فإن معظم المواد الوسيطة حساسة للبيئة ، بما في ذلك الهواء أو الماء أو بعض الشوارد أو أي اضطرابات أخرى لا يمكن التنبؤ بها. العناية الإضافية ضرورية أثناء التعامل مع المواد الوسيطة وقياسها. عادة ما تكون التجربة والخطأ ضرورية أثناء التعامل مع مزيج جديد من مادة القطب والكهارل.
هنا ، نقدم نموذجا جديدا ، يسمى القياس المغناطيسي الكهروكيميائي ، لتحليل الحالات الإلكترونية أو حالات الدوران للأطر العضوية العضوية ثنائية الأبعاد والمواد المماثلة باستخدام سلسلة من التقنيات ، باستخدام الكيمياء الكهربائية والتحليل الطيفي ESR خارج الموقع المتغير درجة الحرارة بالإضافة إلى قياسات الحساسية المغناطيسية خارج الموقع 20. لإثبات فعالية هذا النهج ، نستخدم Cu3THQ 2 (THQ = 1،2 ،4،5-رباعي هيدروكسي بنزوكينون ؛ يشار إليه باسم Cu-THQ) ، وهو ممثل 2D MOF ، كمثال. نفسر اختيار المضافات الموصلة والكهارل ، وتصنيع الأقطاب الكهربائية والخلايا الكهروكيميائية ، بالإضافة إلى تفاصيل حول معالجة العينات وقياسها ، بما في ذلك المشكلات المحتملة أثناء القياس. من خلال المقارنة مع الخصائص الكلاسيكية مثل XRD و XAFS ، يمكن أن يوفر قياس المغناطيسية الكهروكيميائية فهما شاملا للآلية الكهروكيميائية لمعظم الأطر الفلزية العضوية. هذا النهج قادر على التقاط حالات وسيطة فريدة وتجنب التعيين غير الصحيح لأحداث الأكسدة والاختزال. يمكن أن يساهم توضيح آليات تخزين الطاقة باستخدام القياس الكهروكيميائي للمغناطيسية أيضا في فهم أفضل للعلاقات بين البنية والوظيفة في الأطر الفلزية العضوية ، مما يؤدي إلى استراتيجيات تركيبية أكثر ذكاء للأطر الفلزية العضوية والمواد الأخرى المترافقة.
Protocol
1. تصنيع القطب
- توليف النحاس THQ MOF
ملاحظة: تم تصنيع مسحوق الكريستالات Cu-THQ MOF عبر طريقة حرارية مائية باتباع الإجراءات المنشورة مسبقا14،20،23.- ضع 60 مجم من رباعي هيدروكسيكينون في أمبولة سعة 20 مل ، ثم أضف 10 مل من الماء المنزوع الغاز. في قنينة زجاجية منفصلة ، قم بإذابة 110 مجم من ثلاثي هيدرات نترات النحاس (II) في 10 مل أخرى من الماء المنزوع الغاز. أضف 46 ميكرولتر من الليجند الإيثيلين ديامين المنافس باستخدام ماصة.
ملاحظة: لإزالة الغازات من الماء منزوع الأيونات ، قم بتدفق غاز النيتروجين لمدة 30 دقيقة قبل الاستخدام. إذا تم تسخين خليط التفاعل لفترة طويلة جدا ، فقد تتشكل شوائب النحاس مع ظهور ذروة حيود حوالي 43 درجة (Cu Kα). - أدخل محلول النحاس في الأمبولة التي تحتوي على رباعي هيدروكسي كينون. يتغير لون المحلول على الفور من الأحمر إلى البحرية. قم بتجميد وضخوإذابة 24 المحلول الناتج ثلاث مرات لإزالة الأكسجين المذاب بشكل أكبر.
- ختم اللهب الأمبولة باستخدام شعلة تحت الفراغ. سخني المحلول إلى 60 درجة مئوية لمدة 4 ساعات.
- بعد التفاعل ، افتح الأمبولة بعناية وأزل المادة الطافية. اغسل الراسب ب 30 مل من الماء منزوع الأيونات بدرجة حرارة الغرفة 3x و 30 مل من الماء الساخن منزوع الأيونات (80 درجة مئوية) عن طريق الطرد المركزي 3x عند 10000 دورة في الدقيقة لمدة 5 دقائق.
- تفريق راسب في الأسيتون عن طريق هز ، ثم تصفية وغسل مع الأسيتون. سخني المنتج تحت فراغ عند 353 كلفن طوال الليل لإزالة المذيب المتبقي في Cu-THQ MOF.
- ضع 60 مجم من رباعي هيدروكسيكينون في أمبولة سعة 20 مل ، ثم أضف 10 مل من الماء المنزوع الغاز. في قنينة زجاجية منفصلة ، قم بإذابة 110 مجم من ثلاثي هيدرات نترات النحاس (II) في 10 مل أخرى من الماء المنزوع الغاز. أضف 46 ميكرولتر من الليجند الإيثيلين ديامين المنافس باستخدام ماصة.
- تحضير أقطاب CuTHQ
ملاحظة: للتمييز بين Cu-THQ MOF والقطب ، يشار إلى الأول باسم Cu-THQ ، بينما يشار إلى خليط Cu-THQ والكربون والموثق ببساطة باسم CuTHQ.- لتحضير قطب Cu-THQ / CB / PVDF ، قم بإذابة 10 مجم من بولي (فلوريد فينيلدين) (PVDF) في 1.4 مل من N-methyl-2-pyrrolidone (NMP). قم بتفريق 50 مجم من Cu-THQ MOF و 40 مجم من أسود الكربون (CB) في المحلول عن طريق التحريك بقوة طوال الليل. قم بتغطية الملاط المتجانس على قرص Al بقطر 15 مم وكتلة ~ 9.7 مجم.
- لتحضير قطب Cu-THQ / Gr / SP / SA ، اتبع نفس الإجراء مثل قطب Cu-THQ / CB / PVDF ، ولكن مع تركيبة ملاط مختلفة: Cu-THQ MOF (80 مجم) ، ألجينات الصوديوم (SA ، 2 مجم) ، والجرافين / Super P (Gr / SP ، 1: 1.8 تخفيف بالوزن ، إجمالي 18 مجم) في الماء / الأيزوبروبانول (تخفيف 1: 1 من حيث الحجم ، إجمالي 1.2 مل).
- تجفيف الأقطاب الكهربائية تحت فراغ في 353 كلفن لمدة 12 ساعة. تنفيس غاز النيتروجين بعد التجفيف وقياس تحميل الكتلة.
2. تجميع البطارية والمعالجة اللاحقة
ملاحظة: نظرا للطبيعة الحساسة للهواء للمواد الوسيطة الكهروكيميائية ، يجب إجراء تجميع البطارية والمعالجة اللاحقة في صندوق قفازات الأرجون بأخلاق صارمة خالية من الهواء.
- تجميع خلايا عملة Li / CuTHQ
- قطع عدة قطع من أقراص الليثيوم بقطر 15.5 مم وفواصل Celgard بقطر 17 مم قبل تجميع البطارية.
- قم بتجميع خلايا عملة Li / CuTHQ (CR2032) من الأسفل إلى الأعلى بالترتيب التالي: الغلاف السالب ، الفاصل (الارتفاع = 0.5 مم) ، الليثيوم ، الفاصل ، قطب CuTHQ (محضر في الخطوة 1.2.1 أو 1.2.2) ، فاصل ، زنبرك ، وقذيفة موجبة (الشكل 1 أ).
- قبل وبعد إضافة الفاصل ، قم بإسقاط ما مجموعه 0.04 مل من المنحل بالكهرباء (1.0 M LiBF4 في كربونات الإيثيلين (EC) / كربونات ثنائي إيثيل (DEC) عند 1: 1 بالوزن٪). لا تستخدم ملاقط معدنية لتثبيت خلية العملة المعدنية بعد تجميعها.
- تحضير المواد الوسيطة الكهروكيميائية
- قم بضغط خلية العملة باستخدام برغي الشد (غير المختوم) بجهاز محلي الصنع (الشكل 1 ب) وقم بتوصيل الجهاز بكابلات القياس في صندوق القفازات. قم بتوصيل الأداة (خارج صندوق القفازات) بالمنافذ المقابلة لخلية العملة. إجراء قياسات الفولتاميتر الدورية وقياسات الشحنة/التفريغ الجلفانوستاتيكي20 لتحقيق المواد الوسيطة عند إمكانات مختلفة (الشكل 2).
- بعد الدورة الكهروكيميائية ، قم بتفكيك خلية العملة بعناية لتجنب أي دوائر قصيرة.
- اشطف قطب CuTHQ المدورة ب 5 مل من كربونات ثنائي ميثيل البطارية (DMC). جفف القطب بشكل طبيعي لمدة 30 دقيقة. اجمع العينة من قرص Al إلى رقائق Al باستخدام ملعقة نظيفة.
- انقل مسحوق العينة إلى أنبوب ESR أو أنبوب الحبار من خلال قمع زجاجي محلي الصنع (الشكل 1C). أغلق أنبوب العينة بإحكام بغطاء وفيلم شفاف. بدلا من ذلك ، قم بتوصيل أنبوب العينة بأنبوب مطاطي وختمه بصمام ، متبوعا بختم اللهب لرأس أنبوب العينة تحت الفراغ.
- بعد القياسات المغناطيسية20 ، افتح أنبوب العينة وأفرغ العينة على رقائق Al . قم بقياس كتلة العينة باستخدام ميزان تحليلي بدقة 0.01 مجم في الهواء. قدر كتلة Cu-THQ من الكتلة الكلية للعينة.
ملاحظة: تقدر كتلة Cu-THQ MOF المدورة بنسبة 50٪ أو 80٪ من الكتلة الكلية ، اعتمادا على نوع الأقطاب الكهربائية المستخدمة ؛ لا يأخذ هذا التقدير في الاعتبار أيونات Li المدرجة والكهارل المتبقية.
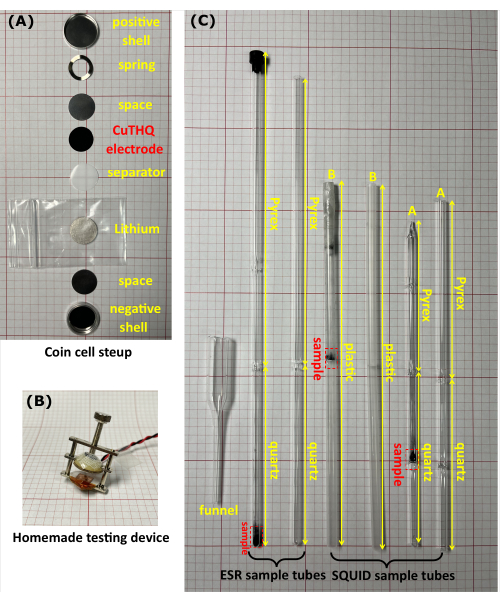
الشكل 1: المعدات المستخدمة في تجارب القياس المغناطيسي خارج الموقع. (أ) صورة فوتوغرافية لخلية عملة معدنية CR2032. (ب) تم استخدام الجهاز محلي الصنع لتقييم خلية العملة غير المختومة في صندوق القفازات. (ج) صور فوتوغرافية لأنابيب عينات ESR و SQUID مع عينات بداخلها أو بدونها. يتكون أنبوب ESR من طرف كوارتز عالي النقاء 10 سم (قسم القياس) ورأس زجاجي من البورسليكات 17 سم. هناك نوعان من أنابيب الحبار. يتكون الأنبوب A من طرف كوارتز 2 سم × 5 سم مع غشاء كوارتز عند نقطة المنتصف ورأس زجاجي من البورسليكات 10 سم ، والأنبوب B عبارة عن أنبوب بلاستيكي (بطول 20 سم) مع غشاء بلاستيكي عند نقطة المنتصف. يبلغ قطر جميع أنابيب العينات الخارجي 5 مم. يرجى النقر هنا لعرض نسخة أكبر من هذا الشكل.
3. تسجيل أطياف ESR في درجات حرارة متغيرة
- تسجيل أطياف ESR في درجة حرارة الغرفة
- بمجرد أن يصبح مطياف ESR جاهزا ، أدخل أنبوب العينة المحضر في تجويف الميكروويف وقم بتوسيط العينة. قم بضبط طور الميكروويف والاقتران والتردد تلقائيا للوصول إلى حالة رنين التجويف. تحقق من Q-dip في وسط الشاشة للحصول على شكل متماثل وعمق أقصى.
ملاحظة: إذا كانت العينة تحتوي على الكثير من الكربون الموصل ، مثل أسود الكربون ، فقد تفشل عملية الضبط التلقائي أو تؤدي إلى عامل جودة صغير (قيمة Q) للتجويف. الكتلة النموذجية للعينة هي 3 ملغ. - اختر المعلمات المثلى ، مثل: الميكروويف: الطاقة ؛ المجال المغناطيسي: وقت الاجتياح. حقل المركز: عرض الاجتياح. التحوير: التردد والعرض ؛ القناة: السعة ، الوقت ثابت. ثم ، اكتسح المجال المغناطيسي وسجل طيف ESR. القيم النموذجية لمعلمات القياس موضحة في الشكل 3 والشكل 4.
- اضبط مقدار إدراج علامة Mn على 800. كرر الخطوتين 3.1.1 و 3.1.2 لتسجيل طيف ESR باستخدام علامة Mn. معايرة المجال المغناطيسي باستخدام ستة خطوط فائقة الدقة لأيونات Mn(II).
- بمجرد أن يصبح مطياف ESR جاهزا ، أدخل أنبوب العينة المحضر في تجويف الميكروويف وقم بتوسيط العينة. قم بضبط طور الميكروويف والاقتران والتردد تلقائيا للوصول إلى حالة رنين التجويف. تحقق من Q-dip في وسط الشاشة للحصول على شكل متماثل وعمق أقصى.
- تحليل شكل الخط من Cu-THQ
- استيراد مجموعة بيانات ESR إلى Python (الإصدار 3.9.7). تطبيع طيف ESR بقسمة الشدة على كتلة العينة ، والجذر التربيعي لطاقة الميكروويف ، وعرض التعديل ، والسعة.
- قم بملاءمة طيف ESR المعاير والطبيعي ل Cu-THQ MOF كما تم إعداده مع دالة Lorentzian المتماثلة محوريا25:
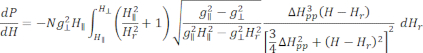
حيث N هو عامل مقياس يتضمن معلمات الأداة g llوثوابت H II، (و) هي المكون الموازي (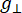 العمودي) لعامل لاندر g والمجال المغناطيسي للرنين المقابل ، Δ Hpp هو عرض الخط من الذروة إلى الذروة ، و
العمودي) لعامل لاندر g والمجال المغناطيسي للرنين المقابل ، Δ Hpp هو عرض الخط من الذروة إلى الذروة ، و 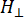 Hrمتغير متكامل.
Hrمتغير متكامل.
ملاحظة: تتوفر رموز Python للدالة Lorentzian في ملف الترميز التكميلي 1 (الذي يسمى AxialLorentz). - احصل على قيمة g متباينة الخواص وعرض الخط من الذروة إلى الذروة لأيونات Cu(II) المتماثلة محوريا.
- قم بملاءمة طيف ESR المعاير والطبيعي مع وظيفة Lorentzian للعينات الجذرية. احصل على قيمة g الخواص وعرض الخط من الذروة إلى الذروة للجذور.
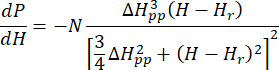
يسمى هذا باسم SymLorentz في ملف الترميز التكميلي 1.
- قياس التركيز الجذري
- طحن 3.45 ملغ من 4-هيدروكسي-2،2،6،6-رباعي ميثيل بيبيريدين-1-أوكسيل (تمبول) و 96.55 ملغ من KBr معا في هاون العقيق حتى يتم تحقيق خليط متجانس. ضع 1 مجم (0.2 ميكرومول) و 2 مجم (0.4 ميكرومول) و 4 مجم (0.8 ميكرومول) من مخاليط TEMPOL / KBr في ثلاثة أنابيب عينة ESR ، على التوالي.
- اتبع الخطوتين 3.1.1 و 3.1.2 لتسجيل أطياف ESR لمعايير TEMPOL / KBr.
- إجراء تركيب خطي لخط الأساس بين التكامل المزدوج لأطياف ESR وعدد الدورات في معايير TEMPOL / KBr. حدد عدد الدورات في Cu-THQ المدورة باستخدام خط الأساس الخطي لمعايير TEMPOL / KBr26.
- تسجيل أطياف ESR في درجات حرارة منخفضة
ملاحظة: استخدم الهيليوم السائل لتحقيق درجة حرارة مبردة. من الضروري ارتداء قفازات مبردة عند العمل مع الهيليوم السائل.- تحقق من طيف ESR في درجة حرارة الغرفة أولا باتباع الخطوة 3.1.
- قم بإخلاء الدرع الحراري إلى مستوى فراغ عالي. قم بتطهير تجويف الميكروويف باستخدام غاز النيتروجين لتجنب التكثيف.
- إدخال الهيليوم السائل من الوعاء إلى cryostat. قم بتبريد العينة تدريجيا إلى أدنى درجة حرارة (حوالي 10 كلفن). انتظر 30 دقيقة لتحقيق التوازن الحراري.
- سجل أطياف ESR المعتمدة على درجة الحرارة أثناء الاحترار. تأكد من أن طيف ESR لا يعاني من تأثير تشبع الطاقة عند درجة حرارة منخفضة ، وأن النسبة بين شدة الإشارة (ارتفاع الذروة إلى الذروة) والجذر التربيعي لطاقة الميكروويف تظل ثابتة في حالة عدم تشبع الطاقة.
ملاحظة: عندما تكون الطاقة مشبعة ، تزداد شدة الإشارة بشكل أبطأ من الجذر التربيعي لطاقة الميكروويف. يمكن أن تنخفض كثافة أخذ العينات تدريجيا مع ارتفاع درجة الحرارة.
4. قياسات الحساسية المغناطيسية
- قم بتوصيل أنبوب العينة بأسفل قضيب العينة. تأكد من أن سطح أنبوب العينة نظيف.
- قم بتطهير حجرة العينة وأدخل أنبوب العينة في الحبار. ضع مجالا مغناطيسيا وقم بتوسيط العينة داخل ملف الكشف. قم بإزالة المجال المغناطيسي الخارجي بعد التوسيط.
ملاحظة: إذا كان تركيز الدوران منخفضا جدا بحيث لا يمكن اكتشافه ، ففكر في زيادة المجال المغناطيسي أو التمركز بعد التبريد إلى 2 كلفن. تبلغ كتلة العينة النموذجية لقياسات الحبار حوالي 6 ملغ. - قم بتبريد النظام إلى 20 K بمعدل 10 K / دقيقة. توقف مؤقتا عن التبريد لمدة 30 دقيقة ، ثم قم بتبريده إلى 2 كلفن لمدة 1 ساعة.
- قياس الحساسية المغناطيسية لقطب CuTHQ المدور تحت مجال مغناطيسي يبلغ 1000 Oe أثناء الاحترار إلى 300 كلفن ؛ يشار إلى هذا باسم عملية تبريد المجال الصفري (ZFC). بعد ذلك ، قم بالتبريد إلى 2 K مرة أخرى وسجل الحساسية المغناطيسية في عملية التبريد الميداني (FC).
- كرر الخطوات من 4.1 إلى 4.4 مع تدوير أقطاب CuTHQ بدرجات اختزال مختلفة.
- قياس الحساسية المغناطيسية للمواد الكربونية (Gr / SP) في ظل نفس الظروف. استخدم هذه النتيجة للتعويض عن الحساسية المغناطيسية لأقطاب CuTHQ.
- تناسب اعتماد درجة حرارة الحساسية المغناطيسية لقانون كوري فايس المعدل:
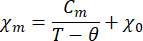
حيث χ m هي القابلية المغناطيسية المولية ، Cmهي ثابت كوري المولي ، θ هي درجة حرارة فايس ، و χ0مصطلح مستقل عن درجة الحرارة.
النتائج
تضمن عملنا السابق مناقشة مفصلة للتحليل الطيفي ESR خارج الموقع وقياسات الحساسية المغناطيسية خارج الموقع ل CuTHQ20 المدورة كهروكيميائيا. هنا ، نقدم النتائج الأكثر تمثيلا وتفصيلا التي يمكن الحصول عليها باتباع البروتوكول الموضح في هذه الورقة.
Discussion
لإنتاج الكاثودات ، من الضروري خلط المادة الفعالة مع الكربون الموصل لتحقيق استقطاب منخفض أثناء العملية الكهروكيميائية. المادة المضافة للكربون هي النقطة الحرجة الأولى لقياس المغنطيسية خارج الموقع . إذا كان الكربون يحتوي على عيوب جذرية ، فلا يمكن ملاحظة ظهور الجذر العضوي المستحث كهرو?...
Disclosures
ليس لدى المؤلفين أي تضارب في المصالح للإعلان عنه.
Acknowledgements
تم دعم هذه الدراسة من قبل الجمعية اليابانية لتعزيز العلوم (JSPS) KAKENHI Grant (JP20H05621). كما يشكر Z. Zhang مؤسسة Tatematsu ومنحة Toyota Riken على الدعم المالي.
Materials
| Name | Company | Catalog Number | Comments |
| 1-Methyl-2-pyrrolidone | FUJIFILM Wako Chemicals | 139-17611 | Super Dehydrated |
| 1mol/L LiBF4 EC:DEC (1:1 v/v%) | Kishida | LBG-96533 | electrolyte |
| 4-Hydroxy-2,2,6,6-tetramethylpiperidine-1-oxyl | FUJIFILM Wako Chemicals | 089-04191 | TEMPOL, for Spin Labeling |
| Ampule tube | Maruemu Corporation | 5-124-05 | 20mL |
| Carbon black, Super P Conductive | Alfa Aesar | H30253 | |
| Conductive Carbon Black | Mitsubishi Chemical | ||
| Copper (II) Nitrate Trihydrate | FUJIFILM Wako Chemicals | 033-12502 | deleterious substances |
| Dimethyl Carbonate | FUJIFILM Wako Chemicals | 046-31935 | battery grade |
| Ethylenediamine | FUJIFILM Wako Chemicals | 053-00936 | deleterious substances |
| Graphene Nanoplatelets | Tokyo Chemical Industry | G0442 | 6-8nm(thick), 15µm(wide) |
| Poly(vinylidene fluoride) | Sigma Aldrich | 182702 | |
| Potassium Bromide | FUJIFILM Wako Chemicals | 165-17111 | for Infrared Spectrophotometry |
| Sodium Alginate | FUJIFILM Wako Chemicals | 199-09961 | 500-600 cP |
| SQUID Magnetometer | Quantum Design | MPMS-XL 5 | |
| Tetrahydroxy-1,4-benzoquinone Hydrate | Tokyo Chemical Industry | T1090 | |
| X-Band ESR | JEOL | JES-F A200 |
References
- Lee, J., et al. Metal-organic framework materials as catalysts. Chemical Society Reviews. 38 (5), 1450-1459 (2009).
- Dolgopolova, E. A., Rice, A. M., Martin, C. R., Shustova, N. B. Photochemistry and photophysics of MOFs: steps towards MOF-based sensing enhancements. Chemical Society Reviews. 47 (13), 4710-4728 (2018).
- Qian, Q., et al. MOF-based membranes for gas separations. Chemical Reviews. 120 (16), 8161-8266 (2020).
- Wang, Q., Astruc, D. State of the art and prospects in metal-organic framework (MOF)-based and MOF-derived nanocatalysis. Chemical Reviews. 120 (2), 1438-1511 (2020).
- Wang, M., Dong, R., Feng, X. Two-dimensional conjugated metal-organic frameworks (2D c-MOFs): chemistry and function for MOFtronics. Chemical Society Reviews. 50 (4), 2764-2793 (2021).
- Baumann, A. E., Burns, D. A., Liu, B., Thoi, V. S. Metal-organic framework functionalization and design strategies for advanced electrochemical energy storage devices. Communications Chemistry. 2 (1), 86 (2019).
- Nam, K. W., et al. Conductive 2D metal-organic framework for high-performance cathodes in aqueous rechargeable zinc batteries. Nature Communications. 10 (1), 4948 (2019).
- Sheberla, D., et al. Conductive MOF electrodes for stable supercapacitors with high areal capacitance. Nature Materials. 16 (2), 220-224 (2017).
- Wang, Z., et al. Ultrathin two-dimensional conjugated metal-organic framework single-crystalline nanosheets enabled by surfactant-assisted synthesis. Chemical Science. 11 (29), 7665-7671 (2020).
- Zhang, Z., Yoshikawa, H., Awaga, K. Monitoring the solid-state electrochemistry of Cu(2,7-AQDC) (AQDC = anthraquinone dicarboxylate) in a lithium battery: Coexistence of metal and ligand redox activities in a metal-organic framework. Journal of the American Chemical Society. 136 (46), 16112-16115 (2014).
- Zhang, Z., Yoshikawa, H., Awaga, K. Discovery of a "bipolar charging" mechanism in the solid-state electrochemical process of a flexible metal-organic framework. Chemistry of Materials. 28 (5), 1298-1303 (2016).
- Li, C., Hu, X., Hu, B. Cobalt(II) dicarboxylate-based metal-organic framework for long-cycling and high-rate potassium-ion battery anode. Electrochimica Acta. 253, 439-444 (2017).
- Liu, J., et al. Reversible formation of coordination bonds in Sn-based metal-organic frameworks for high-performance lithium storage. Nature Communications. 12 (1), 3131 (2021).
- Jiang, Q., et al. A redox-active 2D metal-organic framework for efficient lithium storage with extraordinary high capacity. Angewandte Chemie. 59 (13), 5273-5277 (2020).
- Sakaushi, K., Nishihara, H. Two-dimensional π-conjugated frameworks as a model system to unveil a multielectron-transfer-based energy storage mechanism. Accounts of Chemical Research. 54 (15), 3003-3015 (2021).
- Li, H., et al. 2D organic radical conjugated skeletons with paramagnetic behaviors. Advanced Materials Interfaces. 8 (18), 2100943 (2021).
- Peeks, M. D., et al. Electronic delocalization in the radical cations of porphyrin oligomer molecular wires. Journal of the American Chemical Society. 139 (30), 10461-10471 (2017).
- Krug von Nidda, H. A., et al. Anisotropic exchange in LiCuVO4 probed by ESR. Physical Review B. 65 (13), 134445 (2002).
- Zeng, Z., et al. Pro-aromatic and anti-aromatic π-conjugated molecules: An irresistible wish to be diradicals. Chemical Society Reviews. 44 (18), 6578-6596 (2015).
- Chen, Q., Adeniran, O., Liu, Z. F., Zhang, Z., Awaga, K. Graphite-like charge storage mechanism in a 2D π-d conjugated metal-organic framework revealed by stepwise magnetic monitoring. Journal of the American Chemical Society. 145 (2), 1062-1071 (2023).
- Julien, C. M., Mauger, A., Groult, H., Zhang, X., Gendron, F. LiCo1-yByO2 as cathode materials for rechargeable lithium batteries. Chemistry of Materials. 23 (2), 208-218 (2011).
- Niemöller, A., Jakes, P., Eichel, R. A., Granwehr, J. In operando EPR investigation of redox mechanisms in LiCoO2. Chemical Physics Letters. 716, 231-236 (2019).
- Park, J., et al. Synthetic routes for a 2D semiconductive copper hexahydroxybenzene metal-organic framework. Journal of the American Chemical Society. 140 (44), 14533-14537 (2018).
- Rondeau, R. E. A technique for degassing liquid samples. Journal of Chemical Education. 44 (9), 530 (1967).
- Flores-Llamas, H. Inhomogeneously broadened EPR lineshape of axial powder. Applied Magnetic Resonance. 9 (2), 289-298 (1995).
- Sun, L., et al. Room-temperature quantitative quantum sensing of lithium ions with a radical-embedded metal-organic framework. Journal of the American Chemical Society. 144 (41), 19008-19016 (2022).
- Chen, Y., et al. Successive storage of cations and anions by ligands of π-d-conjugated coordination polymers enabling robust sodium-ion batteries. Angewandte Chemie. 60 (34), 18769-18776 (2021).
- Roessler, M. M., Salvadori, E. Principles and applications of EPR spectroscopy in the chemical sciences. Chemical Society Reviews. 47 (8), 2534-2553 (2018).
- Ji, X., et al. Pauli paramagnetism of stable analogues of pernigraniline salt featuring ladder-type constitution. Journal of the American Chemical Society. 142 (1), 641-648 (2020).
- Noel, M., Santhanam, R. Electrochemistry of graphite intercalation compounds. Journal of Power Sources. 72 (1), 53-65 (1998).
- Wu, K. H., Ting, T. H., Wang, G. P., Ho, W. D., Shih, C. C. Effect of carbon black content on electrical and microwave absorbing properties of polyaniline/carbon black nanocomposites. Polymer Degradation and Stability. 93 (2), 483-488 (2008).
- Yao, M., Taguchi, N., Ando, H., Takeichi, N., Kiyobayashi, T. Improved gravimetric energy density and cycle life in organic lithium-ion batteries with naphthazarin-based electrode materials. Communications Materials. 1 (1), 70 (2020).
- Krzystek, J., et al. EPR spectra from "EPR-silent" species: High-frequency and high-field EPR spectroscopy of pseudotetrahedral complexes of nickel(II). Inorganic Chemistry. 41 (17), 4478-4487 (2002).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved