JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
산화 환원 활성 금속-유기 프레임워크의 고체 전기화학에서 중간체의 자기 측정 특성 분석
요약
현장 자기 조사는 자기 전극에 대한 대량 및 로컬 정보를 직접 제공하여 전하 저장 메커니즘을 단계별로 밝힐 수 있습니다. 여기에서 전자 스핀 공명(ESR) 및 자화율은 산화 환원 활성 금속-유기 프레임워크(MOF)에서 상자성 종 및 그 농도의 평가를 모니터링하기 위해 입증됩니다.
초록
전기화학적 에너지 저장은 지난 5년 동안 산화 환원 활성 금속-유기 프레임워크(MOF)의 응용 분야에서 널리 논의되었습니다. MOF는 중량 측정 또는 면적 커패시턴스 및 순환 안정성 측면에서 뛰어난 성능을 보여 주지만 불행히도 대부분의 경우 전기 화학적 메커니즘이 잘 이해되지 않습니다. X선 광전자 분광법(XPS) 및 X선 흡수 미세 구조(XAFS)와 같은 전통적인 분광 기술은 특정 원소의 원자가 변화에 대한 모호하고 질적인 정보만 제공했으며 이러한 정보를 기반으로 제안된 메커니즘은 종종 매우 논쟁의 여지가 있습니다. 이 기사에서는 고체 상태 전기 화학 전지의 제조, 전기 화학 측정, 전지 분해, MOF 전기 화학 중간체 수집 및 불활성 가스 보호하에 중간체의 물리적 측정을 포함한 일련의 표준화 된 방법을보고합니다. 산화 환원 활성 MOF의 단일 전기 화학 단계 내에서 전자 및 스핀 상태 진화를 정량적으로 명확히하기 위해 이러한 방법을 사용함으로써 MOF뿐만 아니라 강한 상관 관계를 가진 다른 모든 재료에 대한 전기 화학적 에너지 저장 메커니즘의 특성에 대한 명확한 통찰력을 제공 할 수 있습니다.
서문
1990년대 후반, 특히 2010년대에 금속-유기 프레임워크(MOF)라는 용어가 도입된 이후, MOF에 관한 가장 대표적인 과학적 개념은 게스트 캡슐화, 분리, 촉매 특성 및 분자 감지 1,2,3,4를 포함한 구조적 다공성에서 비롯되었습니다 . 한편, 과학자들은 MOF를 최신 스마트 장치에 통합하기 위해 자극 반응형 전자 특성을 보유하는 것이 필수적이라는 것을 빠르게 깨달았습니다. 이 아이디어는 지난 10년 동안 전도성 2차원(2D) MOF 제품군의 탄생과 번성을 촉발하여 MOF가 전자 제품5 및 더 매력적으로 전기화학 에너지 저장 장치6에서 핵심적인 역할을 할 수 있는 문을 열었습니다. 이러한 2D MOF는 알칼리 금속 전지, 수성 전지, 유사 커패시터 및 슈퍼 커패시터 7,8,9에 활물질로 통합되었으며 우수한 안정성과 함께 엄청난 용량을 발휘했습니다. 그러나 더 나은 성능의 2D MOF를 설계하려면 전하 저장 메커니즘을 자세히 이해하는 것이 중요합니다. 따라서 이 기사는 MOF의 전기화학적 메커니즘에 대한 포괄적인 이해를 제공하는 것을 목표로 하며, 이는 에너지 저장 애플리케이션을 위한 더 나은 성능의 MOF를 합리적으로 설계하는 데 도움이 될 수 있습니다.
2014년에 우리는 금속 양이온과 리간드10,11 모두에 산화환원 활성 부위가 있는 MOF의 고체 전기화학적 메커니즘을 처음 보고했습니다. 이러한 메커니즘은 X선 광전자 분광법(XPS), X선 흡수 미세 구조(XAFS), X선 회절(XRD) 및 고체 상태 핵자기 공명(NMR)과 같은 다양한 현장 및 현장 분광 기술의 도움으로 해석되었습니다. 그 이후로, 이 연구 패러다임은 분자 기반 재료의 고체 전기화학 연구의 추세가 되었다12. 이러한 방법은 금속 클러스터 빌딩 블록과 유기 리간드의 분자 궤도 및 에너지 준위가 이러한 MOF에서 거의 독립적이기 때문에 카르복실레이트 가교 리간드를 갖는 기존 MOF의 산화환원 이벤트를 식별하는 데 적합합니다(12,13).
그러나 상당한 π-d 접합과 강한 상관관계가 있는 2D MOF를 만났을 때 이러한 분광 방법의 한계가 노출되었습니다. 이러한 한계 중 하나는 전술한 대부분의 2D MOF의 대역 레벨이 금속 클러스터와 리간드의 단순한 조합으로 간주될 수 없고, 오히려 이들의 혼성화인 반면, 대부분의 분광학적 방법은 산화 상태(14)에 대한 평균적이고 정성적인 정보만을 제공한다는 것이다. 또 다른 한계는 이러한 데이터의 해석이 항상 국부적 인 원자 궤도의 가정을 기반으로한다는 것입니다. 그러므로, 금속-리간드 혼성화 및 비편재화된 전자 상태를 갖는 중간 상태는 일반적으로 이러한 분광학적 방법(15)만으로는 간과되고 잘못 설명된다. 2D MOF뿐만 아니라 공유 유기 프레임워크(16), 분자 전도체 및 공액 폴리머(17)와 같은 유사한 공액 또는 강한 상관 전자 구조를 가진 다른 재료의 이러한 전기화학적 중간체의 전자 상태에 대한 새로운 프로브를 개발할 필요가 있습니다.
재료의 전자 구조를 평가하기 위한 가장 일반적이고 강력한 도구는 전자 스핀 공명(ESR) 및 초전도 양자 간섭 장치(SQUID) 자화율 측정18,19입니다. 둘 다 시스템에서 짝을 이루지 않은 전자에 의존하기 때문에 이러한 도구는 스핀 밀도, 스핀 분포 및 스핀-스핀 상호 작용에 대한 잠정적 정보를 제공할 수 있습니다. ESR은 짝을 이루지 않은 전자의 민감한 검출을 제공하는 반면, 자화율 측정은 상위 특성20에 대해 더 많은 정량적 신호를 제공합니다. 불행하게도, 두 기술 모두 전기 화학 중간체를 분석하는 데 사용될 때 불가피하게 큰 도전에 직면합니다. 이는 대상 샘플이 순수하지 않고 타겟 물질, 전도성 첨가제, 바인더 및 전해질의 부산물의 혼합물이기 때문에 얻은 데이터21,22는 재료와 불순물 모두의 기여도의 합입니다. 한편, 대부분의 중간체는 공기, 물, 특정 전해질 또는 기타 예측할 수 없는 섭동을 포함한 환경에 민감합니다. 중간체의 취급 및 측정 시 각별한 주의가 필요합니다. 시행착오는 일반적으로 전극 재료와 전해질의 새로운 조합을 처리하는 동안 필요합니다.
여기서는 전기화학 및 온도 가변 ex situ ESR 분광법과 ex situ 자화율 측정 20을 활용하여 일련의 기술을 사용하여2D MOF 및 유사 재료의 전자 상태 또는 스핀 상태를 분석하기 위한 전기화학적 자기측정 법이라는 새로운 패러다임을 제시합니다. 이 접근법의 효과를 입증하기 위해 대표적인 2D MOF인 Cu3THQ2(THQ=1,2,4,5-tetrahydroxybenzoquinone; Cu-THQ라고 함)를 예로 사용합니다. 전도성 첨가제 및 전해질의 선택, 전극 및 전기화학 전지의 제조, 측정 중 발생할 수 있는 문제를 포함하여 시료 취급 및 측정에 대한 세부 정보를 설명합니다. XRD 및 XAFS와 같은 고전적인 특성화와 비교함으로써 전기화학적 자기 측정법은 대부분의 MOF의 전기화학적 메커니즘에 대한 포괄적인 이해를 제공할 수 있습니다. 이 접근법은 고유한 중간 상태를 포착하고 산화 환원 이벤트의 잘못된 할당을 방지할 수 있습니다. 전기화학적 자기측정법을 사용한 에너지 저장 메커니즘의 설명은 또한 MOF의 구조-기능 관계를 더 잘 이해하는 데 기여할 수 있으며, 이는 MOF 및 기타 공액 재료에 대한 보다 지능적인 합성 전략으로 이어질 수 있습니다.
프로토콜
1. 전극 제작
- Cu-THQ MOF 합성
참고: Cu-THQ MOF 다결정 분말은 이전에 발표된 절차 14,20,23에 따라 열수법을 통해 합성되었습니다.- 60mg의 테트라 히드 록시 퀴논을 20mL 앰플에 넣은 다음 10mL의 탈기 된 물을 첨가하십시오. 별도의 유리 바이알에 110mg의 구리 (II) 질산염 삼 수화물을 10mL의 탈기 된 물에 용해시킵니다. 피펫을 사용하여 경쟁 리간드 에틸렌디아민 46μL를 추가합니다.
알림: 탈이온수를 탈기하려면 사용하기 전에 30분 동안 질소 가스를 흐르게 하십시오. 반응 혼합물을 너무 오래 가열하면 Cu 불순물이 형성되어 약 43°(Cu Kα)의 회절 피크가 나타날 수 있습니다. - 구리 용액을 테트라하이드록시퀴논을 함유하는 앰플에 도입한다. 용액의 색상이 즉시 빨간색에서 네이비로 바뀝니다. 생성된 용액을24번 동결, 펌핑 및 해동하여 용존 산소를 추가로 제거한다.
- 진공 상태에서 토치를 사용하여 앰플을 화염 밀봉합니다. 용액을 4시간 동안 60°C로 가열합니다.
- 반응 후 앰플을 조심스럽게 열고 상청액을 제거합니다. 침전물을 30 mL의 실온 탈이온수 3x 및 30 mL의 고온 탈이온수(80°C)로 세척하여 10,000rpm에서 5분 동안 3x 원심분리한다.
- 흔들어서 침전물을 아세톤에 분산시킨 다음 여과하고 아세톤으로 세척합니다. 생성물을 353K에서 밤새 진공 상태로 가열하여 Cu-THQ MOF의 잔류 용매를 제거한다.
- 60mg의 테트라 히드 록시 퀴논을 20mL 앰플에 넣은 다음 10mL의 탈기 된 물을 첨가하십시오. 별도의 유리 바이알에 110mg의 구리 (II) 질산염 삼 수화물을 10mL의 탈기 된 물에 용해시킵니다. 피펫을 사용하여 경쟁 리간드 에틸렌디아민 46μL를 추가합니다.
- CuTHQ 전극 준비
참고: Cu-THQ MOF와 전극을 구별하기 위해 전자를 Cu-THQ라고 하고 Cu-THQ, 탄소 및 바인더의 혼합물을 간단히 CuTHQ라고 합니다.- Cu-THQ/CB/PVDF 전극을 준비하기 위해 10mg의 폴리(비닐리덴 플루오라이드)(PVDF)를 1.4mL의 N-메틸-2-피롤리돈(NMP)에 녹입니다. 밤새 격렬하게 교반하여 용액에 Cu-THQ MOF 50mg과 카본 블랙(CB) 40mg을 분산시킵니다. 균일한 슬러리를 직경 15mm, 질량 ~9.7mg의 Al 디스크에 코팅합니다.
- Cu-THQ/Gr/SP/SA 전극을 준비하려면 Cu-THQ/CB/PVDF 전극과 동일한 절차를 따르지만 슬러리 조성이 다릅니다: Cu-THQ MOF(80mg), 알긴산나트륨(SA, 2mg) 및 그래핀/Super P(Gr/SP, 중량 기준 1:1.8 희석, 총 18mg) 중 물/이소프로판올(부피 기준 1:1 희석, 총 1.2mL).
- 전극을 진공 상태에서 353K에서 12시간 동안 건조시킵니다. 건조 후 질소 가스를 배출하고 질량 부하를 측정합니다.
2. 배터리 조립 및 후처리
알림: 전기화학 중간체의 공기에 민감한 특성으로 인해 배터리 조립 및 후처리는 엄격한 에어 프리 방식으로 아르곤 글러브 박스에서 수행해야 합니다.
- Li/CuTHQ 코인 셀 조립
- 배터리를 조립하기 전에 직경 15.5mm의 리튬 디스크와 직경 17mm의 Celgard 분리기를 여러 개 절단합니다.
- Li/CuTHQ 코인 셀(CR2032)을 네거티브 쉘, 스페이서(높이 = 0.5mm), 리튬, 분리막, CuTHQ 전극(1.2.1 또는 1.2.2단계에서 준비), 스페이서, 스프링 및 포지티브 쉘(그림 1A).
- 분리막을 추가하기 전과 후에 총 0.04mL의 전해질(1:1 wt%의 에틸렌 카보네이트(EC)/디에틸 카보네이트(DEC) 중 1.0M LiBF4 )을 떨어뜨립니다. 동전 셀을 조립한 후 금속 핀셋을 사용하여 동전 셀을 잡지 마십시오.
- 전기 화학 중간체 준비
- 집에서 만든 장치(그림 1B)로 조임 나사(밀봉되지 않음)를 사용하여 코인 셀을 압축하고 장치를 글로브 박스의 측정 케이블에 연결합니다. 기기(글로브 박스 외부)를 코인 셀에 해당하는 포트에 연결합니다. 주기적 전압전류법과 정전기 충방전 측정(20 )을 수행하여 서로 다른 전위에서 중간체를 달성한다(그림 2).
- 전기화학적 사이클링 후 단락을 방지하기 위해 코인 셀을 조심스럽게 분해하십시오.
- 순환된 CuTHQ 전극을 5mL의 배터리 등급 디메틸 카보네이트(DMC)로 헹굽니다. 전극을 30분 동안 자연 건조시킵니다. 깨끗한 주걱을 사용하여 Al 디스크에서 Al 호일까지 샘플을 수집합니다.
- 샘플 분말을 수제 유리 깔때기를 통해 ESR 튜브 또는 SQUID 튜브로 옮깁니다(그림 1C). 샘플 튜브를 캡과 투명 필름으로 단단히 밀봉합니다. 또는 샘플 튜브를 고무 튜브에 연결하고 밸브로 밀봉한 다음 진공 상태에서 샘플 튜브의 헤드를 화염 밀봉합니다.
- 자기 측정후 20, 샘플 튜브를 열고 샘플을 알루미늄 호일에 덤프합니다. 공기 중 분해능이 0.01mg인 분석 저울을 사용하여 샘플의 질량을 측정합니다. 샘플의 총 질량에서 Cu-THQ의 질량을 추정합니다.
참고: 순환된 Cu-THQ MOF의 질량은 사용된 전극 유형에 따라 총 질량의 50% 또는 80%로 추정됩니다. 이 추정치는 삽입된 리튬 이온과 잔류 전해질을 고려하지 않습니다.
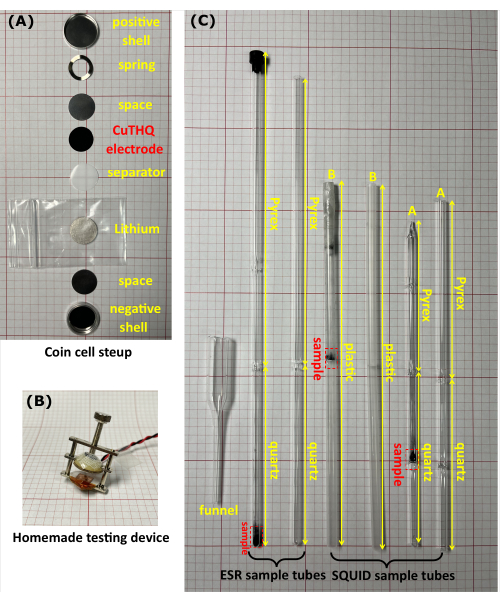
그림 1: 현장 자기 측정 실험에 사용되는 장비 . (A) CR2032 코인 셀의 사진. (B) 집에서 만든 장치를 사용하여 글로브 박스에서 봉인되지 않은 코인 셀을 평가했습니다. (C) 내부에 샘플이 있거나 없는 ESR 및 SQUID 샘플 튜브의 사진. ESR 튜브는 10cm 고순도 석영 팁(측정 섹션)과 17cm 붕규산 유리 헤드로 구성됩니다. 오징어 튜브에는 두 가지 종류가 있습니다. 튜브 A는 중간점에 석영 다이어프램이 있는 2cm x 5cm 석영 팁과 10cm 붕규산 유리 헤드로 구성되며 튜브 B는 중간점에 플라스틱 다이어프램이 있는 플라스틱 튜브(길이 20cm)입니다. 모든 시료 튜브의 외경은 5mm입니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
3. 가변 온도에서 ESR 스펙트럼 등록
- 실온에서 ESR 스펙트럼 기록
- ESR 분광계가 준비되면 준비된 샘플 튜브를 마이크로웨이브 캐비티에 삽입하고 샘플을 중앙에 배치합니다. 마이크로파 위상, 커플링 및 주파수를 자동 조정하여 캐비티의 공진 조건에 도달합니다. 화면 중앙의 Q-dip에서 대칭 모양과 최대 깊이를 확인하십시오.
알림: 샘플에 카본 블랙과 같은 전도성 탄소가 너무 많이 포함되어 있으면 자동 조정 프로세스가 실패하거나 캐비티의 품질 계수(Q-값)가 작아질 수 있습니다. 샘플의 일반적인 질량은 3mg입니다. - 다음과 같은 최적의 매개 변수를 선택하십시오 : 전자 레인지 : 전력; 자기장: 스윕 시간; 중견수: 스윕 폭; 변조 : 주파수, 폭; 채널: 진폭, 시간 상수. 그런 다음 자기장을 스윕하고 ESR 스펙트럼을 기록합니다. 측정 파라미터의 일반적인 값은 그림 3 과 그림 4에 나와 있습니다.
- Mn 마커의 삽입량을 800으로 조정합니다. 3.1.1 및 3.1.2 단계를 반복하여 Mn 마커로 ESR 스펙트럼을 기록합니다. Mn(II) 이온에 대해 6개의 초미세선을 사용하여 자기장을 보정합니다.
- ESR 분광계가 준비되면 준비된 샘플 튜브를 마이크로웨이브 캐비티에 삽입하고 샘플을 중앙에 배치합니다. 마이크로파 위상, 커플링 및 주파수를 자동 조정하여 캐비티의 공진 조건에 도달합니다. 화면 중앙의 Q-dip에서 대칭 모양과 최대 깊이를 확인하십시오.
- Cu-THQ의 라인 형상 분석
- ESR 데이터 세트를 Python(버전 3.9.7)으로 가져옵니다. 강도를 샘플 질량, 마이크로파 전력의 제곱근, 변조 폭 및 진폭으로 나누어 ESR 스펙트럼을 정규화합니다.
- 준비된 Cu-THQ MOF의 보정 및 정규화된 ESR 스펙트럼을 축 대칭 로렌치안 함수25에 맞춥니다.
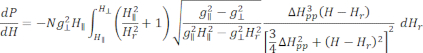
여기서, N은 계기 파라미터 g ll및 HII상수를 포함하는 스케일 팩터이고, ( 및 )는 착륙선 g 계수 및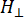 해당 공진 자기장의 평행(
해당 공진 자기장의 평행(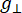 수직) 성분이고,ΔHpp는 피크 대 피크 라인 폭이고, Hr은 적분 변수이다.
수직) 성분이고,ΔHpp는 피크 대 피크 라인 폭이고, Hr은 적분 변수이다.
참고: Lorentzian 함수에 대한 Python 코드는 Supplementary Coding File 1(AxialLorentz로 명명됨)에서 사용할 수 있습니다. - 축 대칭 Cu(II) 이온에 대한 이방성 g-값과 피크 대 피크 선폭을 구합니다.
- 보정 및 정규화된 ESR 스펙트럼을 라디칼 샘플에 대한 Lorentzian 함수에 맞춥니다. 라디칼에 대한 등방성 g-값과 피크 대 피크 선폭을 구합니다.
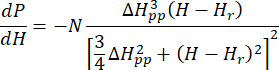
이 파일은 Supplementary Coding File 1에서 SymLorentz로 명명됩니다.
- 라디칼 농도 정량
- 균질한 혼합물이 될 때까지 3.45mg의 4-하이드록시-2,2,6,6-테트라메틸피페리딘-1-옥실(TEMPOL)과 96.55mg의 KBr을 마노 모르타르에서 함께 분쇄합니다. 1mg(0.2μmol), 2mg(0.4μmol) 및 4mg(0.8μmol)의 TEMPOL/KBr 혼합물을 각각 3개의 ESR 샘플 튜브에 넣습니다.
- 3.1.1 및 3.1.2단계에 따라 TEMPOL/KBr 표준에 대한 ESR 스펙트럼을 기록합니다.
- ESR 스펙트럼의 이중 적분과 TEMPOL/KBr 표준의 스핀 수 사이에 선형 기준선 피팅을 수행합니다. TEMPOL/KBr 표준물질26의 선형 기준선을 사용하여 순환된 Cu-THQ의 스핀 수를 결정한다.
- 저온에서 ESR 스펙트럼 기록
알림: 액체 헬륨을 사용하여 극저온을 달성하십시오. 액체 헬륨으로 작업할 때는 극저온 장갑을 착용해야 합니다.- 먼저 3.1단계에 따라 실온에서 ESR 스펙트럼을 확인합니다.
- 열 차폐물을 고진공 수준으로 비우십시오. 응결을 방지하기 위해 질소 가스를 사용하여 마이크로파 캐비티를 퍼지하십시오.
- 액체 헬륨을 용기에서 저온 유지 장치로 주입합니다. 샘플을 최저 온도(약 10K)로 서서히 냉각합니다. 열 평형을 이루기 위해 30분 동안 기다립니다.
- 온난화 동안 온도에 따른 ESR 스펙트럼을 기록합니다. ESR 스펙트럼이 저온에서 전력 포화 효과를 겪지 않고 전력 포화가 없을 때 신호 강도(피크 대 피크 높이)와 마이크로파 전력의 제곱근 사이의 비율이 일정하게 유지되는지 확인합니다.
알림: 전력이 포화되면 신호 강도가 마이크로파 전력의 제곱근보다 느리게 증가합니다. 샘플링 밀도는 온도가 상승함에 따라 점차 감소할 수 있습니다.
4. 자화율 측정
- 샘플 로드의 바닥에 샘플 튜브를 부착합니다. 샘플 튜브의 표면이 깨끗한지 확인하십시오.
- 샘플 챔버를 퍼지하고 샘플 튜브를 SQUID에 삽입합니다. 자기장을 가하고 샘플을 감지 코일 중앙에 배치합니다. 센터링 후 외부 자기장을 제거하십시오.
알림: 스핀 농도가 너무 낮아 감지할 수 없는 경우 2K로 냉각한 후 자기장을 늘리거나 센터링을 늘리는 것이 좋습니다. SQUID 측정을 위한 일반적인 샘플 질량은 약 6mg입니다. - 시스템을 10K/min의 속도로 20K로 냉각합니다. 30분 동안 냉각을 일시 중지한 다음 1시간 동안 2K로 더 냉각합니다.
- 300K로 예열하는 동안 1,000Oe의 자기장 하에서 순환된 CuTHQ 전극의 자화율을 측정합니다. 이를 ZFC(zero-field-cooled) 공정이라고 합니다. 다음으로, 다시 2K로 냉각하고 계자 냉각(FC) 공정에서 자화율을 기록합니다.
- 4.1 단계부터 4.4 단계까지 반복하여 CuTHQ 전극을 서로 다른 환원도로 순환시킵니다.
- 동일한 조건에서 탄소 재료(Gr/SP)의 자화율을 측정합니다. 이 결과를 사용하여 CuTHQ 전극의 자화율을 보정할 수 있습니다.
- 자화율의 온도 의존성을 수정된 Curie-Weiss 법칙에 맞춥니다.
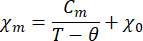
여기서 χm 은 몰 자화율, Cm은 몰 퀴리 상수, θ는 Weiss 온도, χ0는 온도 독립적 항입니다.
결과
우리의 이전 작업에는 전기화학적으로 순환 된 CuTHQ20에 대한 현장 ESR 분광법 및 현장 자기 감수성 측정에 대한 자세한 논의가 포함되었습니다. 여기에서는 이 백서에 설명된 프로토콜에 따라 얻을 수 있는 가장 대표적이고 상세한 결과를 제시합니다.
토론
음극을 생산하기 위해서는 전기화학 공정 동안 낮은 분극을 달성하기 위해 활물질을 전도성 탄소와 혼합해야 합니다. 탄소 첨가제는 현장 자력계의 첫 번째 임계점입니다. 탄소에 라디칼 결함이 있는 경우 ESR 스펙트럼에서 전기화학적으로 유도된 유기 라디칼의 출현을 관찰할 수 없습니다. 이것은 스핀 농도 또는 유기 라디칼 농도를 정확하게 결정하기 어렵게 만드는데, 이는 이들 두 유형...
공개
저자는 선언할 이해 상충이 없습니다.
감사의 말
이 연구는 일본 과학 진흥회 (JSPS) KAKENHI Grant (JP20H05621)의 지원을 받았습니다. Z. Zhang은 또한 재정 지원을 위해 Tatematsu Foundation과 Toyota Riken 장학금에 감사드립니다.
자료
| Name | Company | Catalog Number | Comments |
| 1-Methyl-2-pyrrolidone | FUJIFILM Wako Chemicals | 139-17611 | Super Dehydrated |
| 1mol/L LiBF4 EC:DEC (1:1 v/v%) | Kishida | LBG-96533 | electrolyte |
| 4-Hydroxy-2,2,6,6-tetramethylpiperidine-1-oxyl | FUJIFILM Wako Chemicals | 089-04191 | TEMPOL, for Spin Labeling |
| Ampule tube | Maruemu Corporation | 5-124-05 | 20mL |
| Carbon black, Super P Conductive | Alfa Aesar | H30253 | |
| Conductive Carbon Black | Mitsubishi Chemical | ||
| Copper (II) Nitrate Trihydrate | FUJIFILM Wako Chemicals | 033-12502 | deleterious substances |
| Dimethyl Carbonate | FUJIFILM Wako Chemicals | 046-31935 | battery grade |
| Ethylenediamine | FUJIFILM Wako Chemicals | 053-00936 | deleterious substances |
| Graphene Nanoplatelets | Tokyo Chemical Industry | G0442 | 6-8nm(thick), 15µm(wide) |
| Poly(vinylidene fluoride) | Sigma Aldrich | 182702 | |
| Potassium Bromide | FUJIFILM Wako Chemicals | 165-17111 | for Infrared Spectrophotometry |
| Sodium Alginate | FUJIFILM Wako Chemicals | 199-09961 | 500-600 cP |
| SQUID Magnetometer | Quantum Design | MPMS-XL 5 | |
| Tetrahydroxy-1,4-benzoquinone Hydrate | Tokyo Chemical Industry | T1090 | |
| X-Band ESR | JEOL | JES-F A200 |
참고문헌
- Lee, J., et al. Metal-organic framework materials as catalysts. Chemical Society Reviews. 38 (5), 1450-1459 (2009).
- Dolgopolova, E. A., Rice, A. M., Martin, C. R., Shustova, N. B. Photochemistry and photophysics of MOFs: steps towards MOF-based sensing enhancements. Chemical Society Reviews. 47 (13), 4710-4728 (2018).
- Qian, Q., et al. MOF-based membranes for gas separations. Chemical Reviews. 120 (16), 8161-8266 (2020).
- Wang, Q., Astruc, D. State of the art and prospects in metal-organic framework (MOF)-based and MOF-derived nanocatalysis. Chemical Reviews. 120 (2), 1438-1511 (2020).
- Wang, M., Dong, R., Feng, X. Two-dimensional conjugated metal-organic frameworks (2D c-MOFs): chemistry and function for MOFtronics. Chemical Society Reviews. 50 (4), 2764-2793 (2021).
- Baumann, A. E., Burns, D. A., Liu, B., Thoi, V. S. Metal-organic framework functionalization and design strategies for advanced electrochemical energy storage devices. Communications Chemistry. 2 (1), 86 (2019).
- Nam, K. W., et al. Conductive 2D metal-organic framework for high-performance cathodes in aqueous rechargeable zinc batteries. Nature Communications. 10 (1), 4948 (2019).
- Sheberla, D., et al. Conductive MOF electrodes for stable supercapacitors with high areal capacitance. Nature Materials. 16 (2), 220-224 (2017).
- Wang, Z., et al. Ultrathin two-dimensional conjugated metal-organic framework single-crystalline nanosheets enabled by surfactant-assisted synthesis. Chemical Science. 11 (29), 7665-7671 (2020).
- Zhang, Z., Yoshikawa, H., Awaga, K. Monitoring the solid-state electrochemistry of Cu(2,7-AQDC) (AQDC = anthraquinone dicarboxylate) in a lithium battery: Coexistence of metal and ligand redox activities in a metal-organic framework. Journal of the American Chemical Society. 136 (46), 16112-16115 (2014).
- Zhang, Z., Yoshikawa, H., Awaga, K. Discovery of a "bipolar charging" mechanism in the solid-state electrochemical process of a flexible metal-organic framework. Chemistry of Materials. 28 (5), 1298-1303 (2016).
- Li, C., Hu, X., Hu, B. Cobalt(II) dicarboxylate-based metal-organic framework for long-cycling and high-rate potassium-ion battery anode. Electrochimica Acta. 253, 439-444 (2017).
- Liu, J., et al. Reversible formation of coordination bonds in Sn-based metal-organic frameworks for high-performance lithium storage. Nature Communications. 12 (1), 3131 (2021).
- Jiang, Q., et al. A redox-active 2D metal-organic framework for efficient lithium storage with extraordinary high capacity. Angewandte Chemie. 59 (13), 5273-5277 (2020).
- Sakaushi, K., Nishihara, H. Two-dimensional π-conjugated frameworks as a model system to unveil a multielectron-transfer-based energy storage mechanism. Accounts of Chemical Research. 54 (15), 3003-3015 (2021).
- Li, H., et al. 2D organic radical conjugated skeletons with paramagnetic behaviors. Advanced Materials Interfaces. 8 (18), 2100943 (2021).
- Peeks, M. D., et al. Electronic delocalization in the radical cations of porphyrin oligomer molecular wires. Journal of the American Chemical Society. 139 (30), 10461-10471 (2017).
- Krug von Nidda, H. A., et al. Anisotropic exchange in LiCuVO4 probed by ESR. Physical Review B. 65 (13), 134445 (2002).
- Zeng, Z., et al. Pro-aromatic and anti-aromatic π-conjugated molecules: An irresistible wish to be diradicals. Chemical Society Reviews. 44 (18), 6578-6596 (2015).
- Chen, Q., Adeniran, O., Liu, Z. F., Zhang, Z., Awaga, K. Graphite-like charge storage mechanism in a 2D π-d conjugated metal-organic framework revealed by stepwise magnetic monitoring. Journal of the American Chemical Society. 145 (2), 1062-1071 (2023).
- Julien, C. M., Mauger, A., Groult, H., Zhang, X., Gendron, F. LiCo1-yByO2 as cathode materials for rechargeable lithium batteries. Chemistry of Materials. 23 (2), 208-218 (2011).
- Niemöller, A., Jakes, P., Eichel, R. A., Granwehr, J. In operando EPR investigation of redox mechanisms in LiCoO2. Chemical Physics Letters. 716, 231-236 (2019).
- Park, J., et al. Synthetic routes for a 2D semiconductive copper hexahydroxybenzene metal-organic framework. Journal of the American Chemical Society. 140 (44), 14533-14537 (2018).
- Rondeau, R. E. A technique for degassing liquid samples. Journal of Chemical Education. 44 (9), 530 (1967).
- Flores-Llamas, H. Inhomogeneously broadened EPR lineshape of axial powder. Applied Magnetic Resonance. 9 (2), 289-298 (1995).
- Sun, L., et al. Room-temperature quantitative quantum sensing of lithium ions with a radical-embedded metal-organic framework. Journal of the American Chemical Society. 144 (41), 19008-19016 (2022).
- Chen, Y., et al. Successive storage of cations and anions by ligands of π-d-conjugated coordination polymers enabling robust sodium-ion batteries. Angewandte Chemie. 60 (34), 18769-18776 (2021).
- Roessler, M. M., Salvadori, E. Principles and applications of EPR spectroscopy in the chemical sciences. Chemical Society Reviews. 47 (8), 2534-2553 (2018).
- Ji, X., et al. Pauli paramagnetism of stable analogues of pernigraniline salt featuring ladder-type constitution. Journal of the American Chemical Society. 142 (1), 641-648 (2020).
- Noel, M., Santhanam, R. Electrochemistry of graphite intercalation compounds. Journal of Power Sources. 72 (1), 53-65 (1998).
- Wu, K. H., Ting, T. H., Wang, G. P., Ho, W. D., Shih, C. C. Effect of carbon black content on electrical and microwave absorbing properties of polyaniline/carbon black nanocomposites. Polymer Degradation and Stability. 93 (2), 483-488 (2008).
- Yao, M., Taguchi, N., Ando, H., Takeichi, N., Kiyobayashi, T. Improved gravimetric energy density and cycle life in organic lithium-ion batteries with naphthazarin-based electrode materials. Communications Materials. 1 (1), 70 (2020).
- Krzystek, J., et al. EPR spectra from "EPR-silent" species: High-frequency and high-field EPR spectroscopy of pseudotetrahedral complexes of nickel(II). Inorganic Chemistry. 41 (17), 4478-4487 (2002).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유