Method Article
用运动调节血清治疗韧带结构:转化组织工程模型
摘要
我们提出了一种韧带组织模型,其中三维构建物用人运动调节血清处理,并分析胶原含量,功能和细胞生物化学。
摘要
体外实验对于了解生物学机制至关重要;然而,单层组织培养与人体生理学之间的差距很大,研究结果的翻译往往很差。因此,有更多的替代实验方法的机会。在这里,我们提出一种方法,其中人类细胞从人类前交叉韧带组织残余中分离出来,在培养物中扩增,并用于形成工程化韧带。运动会改变血液中的生化环境,从而改善许多组织,器官和身体过程的功能。在这个实验中,韧带构建培养基补充了通过运动"条件化"的实验人血清。因此,干预是更具生物学意义的,因为实验组织暴露于完整的内源性生化环境,包括结合蛋白和辅助化合物,其可以与未知的感兴趣的代理。治疗后,可以分析工程韧带的机械功能,胶原含量,形态和细胞生物化学。总体而言,传统的单层培养和动物模型,这里介绍的韧带组织的生理模型有四个主要优点。首先,韧带结构是三维的,允许定量的机械性能( 即功能),例如极限拉伸应力,最大拉伸载荷和模量。第二,可以在功能上下文中详细研究这个假设,即boney和sinew元素之间的界面。第三,使用运动后血清制备培养基,可以以不偏不倚的方式调查运动引起的生化环境的影响,该环境负责运动的广泛健康益处。最后,这个实验模型以人性化,道德化的方式推动科学研究取而代之动物,国家卫生研究院,疾病控制中心和食品和药物管理局的核心任务。
引言
肌腱和韧带损伤是常见的,可能对正常的移动性和生活质量造成衰弱的后果。手术干预通常是必要的,但可以有有限和多样的成功4,5 。目前对肌腱和韧带如何发展,成熟和应对伤害的理解是不完全的,因此需要有效的研究模型来提供更有效治疗发展的洞察力5 。为了解决这一知识差距,可以使用动物模型,但是体内研究本身是复杂的,难以控制环境并直接将目标干预到目标组织。相比之下,实验环境可以容易地在体外用传统的单层细胞培养进行控制和监测。然而,这种技术可能会过度简化化学和机械环境,因此可能不会重现晚期细胞的体内行为。组织工程能够结合动物模型中复杂的体内环境的优势与体外环境的控制,并提供了一个额外的学习生理学工具。另外,为了更好地了解韧带的发展,组织工程也可以在需要手术重建时提供移植物组织的来源6 。因此,本文所述的方法验证可用于研究韧带功能和形态的体外 3D工程组织。
已经使用基于纤维蛋白的肌腱或韧带构建体作为体外模型来研究生理过程,包括胶原纤维形成7和肌腱发育8 ,以及其在前列腺的羊模型中评价其作为移植组织的效用的翻译应用ciate ligament(ACL)重建9 。我们的实验室以前已经建立了一个三维工程的韧带模型,跨越两个浮石,磷酸钙骨替代材料,水泥锚。该模型可以容易地经受不同的实验条件,简单地通过用培养基补充生物因子10或施加机械刺激11 。重要的是,这种骨 - 骨韧带模型允许深入分析容易受伤的骨骼和骨骼之间的界面。
在这项研究中,本文提到1提出这种方法,我们感兴趣的是运动诱发变化对生物环境对韧带功能的影响。运动可以改善整个身体各种组织的细胞和器官功能2,3 , 12 ,可能归因于各种已知(例如,IL-6 13 ,IL-15 14 ,流星样15 ,外来体16,17 )的释放以及释放到体循环中的其他未知的生化因子。此外,运动后生化环境富含运动反应性激素,其释放由交感神经系统刺激分泌腺( 例如 ,肾上腺18的皮质醇和儿茶酚胺)以及来自垂体前叶的生长激素19 )。然而,在体内 ,不可能区分运动机械刺激与运动诱导的生物化学变化的影响。虽然一些研究的特点是某些循环激素和细胞因子对运动的预期上升如上所述,有太多的因素,已知和未知,忠实地在体外重述。也就是说,分离体外研究的几个因素不足以解决生化反应的复杂性。在本研究中,我们研究了运动引起的血清生化环境的变化如何影响工程化韧带功能。为了分离生物化学变化的影响,我们在抵抗运动之前和之后获得了人参与者的血清,并使用它治疗了使用人前十字韧带(ACL)成纤维细胞形成的3D工程韧带。使用该模型,我们可以获得功能数据,包括对机械性能和胶原蛋白含量的影响,以及量化对分子信号传导的影响。
研究方案
以下程序遵守经加州大学戴维斯分校机构审查委员会批准的议定书;在开始研究之前,请咨询当地的道德委员会。
1.从人类ACL残留物中分离初级成纤维细胞
注意:保持不育,并在生物安全柜(BSC)中执行所有步骤。
- 获得适当的伦理审查委员会的批准,以收集和使用人体组织,如下所述。
- 通过将100倍抗生素/抗真菌溶液稀释到1倍磷酸盐缓冲盐水(PBS)中来制备5x抗生素/抗真菌(ABAM)溶液。
- 将5X ABAM溶液中的ACL组织碎片收集在50mL锥形管中,在4℃下储存直至消化步骤。如果需要,用剃须刀将组织切成更小的碎片,最大尺寸为1×1×1cm 3 。
小心:符合当地生物危害条例妥善使用生物危害材料,去除和处置生物危害废物。 - 准备足够的胶原酶溶液以淹没组织碎片。在含有1μg青霉素/链霉素和20%胎牛血清(FBS)的高糖Dulbecco改良的Eagle培养基(DMEM)中溶解II型胶原酶(1mg / mL),并在0.22μm下过滤。
- 在PBS中冲洗ACL组织3次。
- 摘要组织。将ACL组织转移到新的50mL锥形管中,并加入足够体积的胶原酶溶液以淹没组织。在37℃下孵育过夜(〜17小时)。
- 在消化持续时间完成之前,通过用10%FBS和100U / mL青霉素补充DMEM高葡萄糖培养基来制备生长培养基(GM)。
- 在消化时间完成前15分钟,每5分钟短暂涡旋含有组织的50mL管3次。
- 使用25 mL血清移液管,大量地消化消化的组织以破坏ti进一步下降并移除细胞。
- 以1,500 xg离心5分钟。吸出上清液并将沉淀重悬于10mL GM中。
- 重复步骤1.8-1.9三次。
- 最后一次离心后,将沉淀重悬于5-10 mL GM。使用小样本的细胞悬液用血细胞计数器进行细胞计数,并使用台盼蓝评估细胞活力。
- 将细胞悬浮液以每平板3-4×10 5个细胞的密度将细胞悬浮液平板化到15cm组织培养板上。
- 在37℃和5%CO 2的无菌培养箱中培养至70%汇合,每三天更换一次GM。使用或储存(见下文)细胞5代。
- 冻结细胞以备将来使用。
- 以70%汇合胰蛋白酶消化细胞如下。吸出培养基并用PBS洗涤细胞。加入足够的预热(37℃)0.05%胰蛋白酶以覆盖组织培养板的底部。将板放在培养基中ator〜5分钟,直到细胞分离(验证细胞使用光学显微镜漂浮)。使用移液器收集细胞并分配到Falcon管中。
- 离心以沉淀细胞,并将细胞重悬于含有20%FBS和10%二甲基亚砜(DMSO)的DMEM高葡萄糖培养基中。将等分细胞悬浮液放入冷冻管中,以-1℃/ min冷却至少24小时。将冷冻冻存于液氮中。
2.准备硅胶涂层
- 准备35毫米组织培养板:移除盖子并在平坦的表面上铺开开放的平板。
- 根据制造商的说明混合硅橡胶套件。
- 使用10 mL注射器,每35 mm板分配2 mL。
- 让硅胶在室温下固化2-3天。
3.准备刷石泥水泥锚
- 提前,准备含有圆柱形的硅胶反模lls用于锚定形成。可以将反模具制成所需锚定形状和尺寸的规格。
- 确定最终锚的所需高度和直径。该方案使用在35mm组织培养皿中由工艺硅氧烷形成的定制模具,其中放置直径约3.25mm的塑料圆筒,使最终模具高度为约6.5mm。最终锚固尺寸约为3-3.5毫米高,直径约3.4毫米,1.5毫米的针从锚的底部伸出。
- 将未固化的硅胶添加到将要制造模具的35毫米的盘子上。相应地放置塑料瓶。
注意:塑料瓶的尺寸将决定最终锚的直径。可以修改塑料圆柱体的位置和使用的硅酮的量,以产生不同高度的锚。模具中孔的底部和模具本身的底部之间的厚度将d引脚可以从锚的底部突出多少,使得锚固件可以稍后被牢固地固定在有机硅涂覆的盘中。 - 使硅树脂固化后,取出塑料圆筒,并将模具从35毫米的培养皿中取出。
- 制备3.5M正磷酸/ 100mM柠檬酸溶液。将0.961g柠檬酸溶解在11.5mL正磷酸中。用MilliQ水将溶液的体积提高至50mL。在室温下储存溶液,防止光照。
- 准备模具:将一个细小针放在模具中每个圆柱形孔的中心。
- 在冰上的塑料称重船中,以1μg/ mL浓度将β-磷酸三钙和正磷酸/柠檬酸溶液合并。
- 用塑料电池刮刀大力混合水泥。
- 研磨水泥以继续混合并将混合物移入模具中
- 以2,250×g离心填充的模具1分钟。
- 使水泥凝固锚固体在室温下放置过夜。
- 从模具中取出锚固件,并在每个有机硅涂层的板上将两个锚定体相隔12毫米。
- 通过喷洒70%乙醇灭菌钉扎板,填充板和盖子,并放入BSC。至少30分钟后,抽吸板并更换盖子,存放在BSC中直至需要。
4.获得人体血清
- 确保本协议获得了适当的伦理审查委员会的批准。
- 确保已从人类受试者获得书面知情同意书,以参与将影响血清预期变化的特定干预( 如运动,食物或药物干预)。在这里,我们描述休息后的收集和抵抗运动后15分钟。
- 使用训练有素的静脉注射器,通过静脉穿刺从参与者获得静息血液样品到适当的抽空容器中。
- 在参与者参与所需的运动方案后15分钟收集运动后血液样本。如前所述1 ,使用本实验中的阻力运动方案来刺激内源性生化反应。
- 有参与者进行五套腿按压,每组之间休息一分钟。接下来,让参与者连续执行一组膝盖伸展和一组绷带卷曲,不用休息,然后重复背靠背练习三次,每组之间休息1分钟。
- 在1500 xg离心10分钟之前让血液凝结。在无菌条件下,将血清转移到无菌管中,以备将来的培养基补充(4℃下储存血清)和生化分析(-20℃下储存的少量血清)。
表示工程韧带
注意:提前扩展主fi并用固定的刷毛锚定剂制备涂有硅油的板。
- 准备试剂:
- 准备凝血酶在DMEM高葡萄糖培养基中溶解牛凝血酶200U / mL。过滤0.22μm,等分,并保存在-20°C。
- 准备纤维蛋白原在DMEM高葡萄糖培养基中溶解20mg / mL的牛纤维蛋白原。在37°C水浴中孵育3-4小时,每30分钟旋转一次以帮助溶解。过滤器为0.22μm(可能需要多个过滤器),等分,并保存在-20°C。
- 准备抑肽酶将抑肽酶溶于10mg / mL的水中。过滤0.22μm,等分,并保存在-20°C。
- 准备氨基己酸。将氨基己酸溶于0.1g / mL的水中。过滤0.22μm,等分,并在4℃下储存。
- 准备抗坏血酸。将抗坏血酸溶解在浓度为50mM的DMEM高葡萄糖培养基中。过滤器为0.22μm,储存于4°C。
- 准备L-脯氨酸。将L-脯氨酸溶于PBS中,浓度为50 mM。过滤器为0.22μm,储存于4°C。
- 准备转化生长因子-β1(TGF-β1)。根据制造商的方向,以10μg/ mL的浓度重建TGF-β1。等分并储存于-20°C。
- 确定实验所需的结构数量,并确保准备足够数量的固定板。推荐生物和技术重复。在这里突出的研究1中 ,使用重复的技术重复和12个生物重复(来自12个人的静息和运动后的血清)。
注意:在BSC的无菌条件下执行以下步骤。 - 通过在15cm板培养至70%汇合来扩增细胞。每个构建体需要2.5×10 5个细胞。
- 胰蛋白酶消化细胞并以3.67×10 3的浓度重悬于GM中5个细胞/ mL。
- 产生所需结构数量的主混合物:对于1次构建,主混合物含有681μL细胞悬浮液(含2.5×10 5个细胞),29μL凝血酶,2μL抑肽酶和2μL氨基己酸。
- 混合好主混合物后,以"图8"模式在每个钉扎板上加入714μL的水泥锚固件。确保主混合物直接接触锚的侧面。
- 轻轻敲击每个平板,将主混合物均匀分布在板上。
- 一次一片,在一个平板上均匀地快速添加286μL纤维蛋白原,并立即将板向前后移动到BSC的表面上,以分布纤维蛋白原,形成细胞嵌入的纤维蛋白凝胶。继续下一盘。
- 将构建体置于保持在37℃和5%CO 2的无菌培养箱中并孵育至少15分钟以允许纤维蛋白原聚合。
- 准备足够的饲料介质(FM),每个构建体2 mL。补充GM与200μM抗坏血酸,50μM脯氨酸和5 ng / mL TGF-β1。
- 加入2毫升FM覆盖每个构造。在保持37℃和5%CO 2的无菌培养箱中培养构建体总共14天或达到所需的终点,每2天用2mL FM刷新培养基
拉伸试验工程胶
注意:使用定制的拉伸试验机在PBS浴中进行拉伸试验;耦合到力传感器的反模压手柄在测试期间将挥发性水泥锚固器保持就位。
- 使用数字卡尺确定韧带结构的长度和宽度;计算组织的横截面面积。
- 从板上取下韧带结构,并将锚固件放在反向模制夹具,确保构造物浸没在PBS中。
- 调整把手之间的距离,将构造的长度设置为其初始长度。
- 开始测试:在0.4 mm / s(或〜3%/ s)的应变速率下将构件变形为失效。
- 测试完成后,处理组织残留物的胶原蛋白含量(见第7节)。
- 从合成的载荷 - 变形数据中,计算应力应变数据并量化感兴趣的机械性能;例如,最大拉伸载荷,极限拉伸强度和模量( 即在应力 - 应变曲线的线性区域上的弹性)。
7.工程胶原胶原含量的定量
- 从黄铁矿水泥锚固件中取出工程韧带,并在120℃下干燥25分钟。
- 确定构建体的干质量并放入单个1.5 mL管中。干构建体可以在室温下储存直到进一步处理。
- 向每个构建体加入200μL6 M HCl。在加热块中在120℃下在通风橱中煮沸2小时。
注意:HCl具有高度腐蚀性和酸性,建议使用防爆/安全锁管或其他固定管道的方法。 - 将管子短暂离心以收集液体,并将其封闭,在通风橱中在加热块中在120℃下蒸发1.5小时。
- 将所得沉淀重悬于200μL羟脯氨酸缓冲液中。储存于-20°C直到需要。
- 准备羟脯氨酸缓冲液。在300 mL水中加入16.6 g柠檬酸,4 mL乙酸,11.4 g NaOH,搅拌至溶解。 pH至6-6.5,体积达500 mL。加入250μL甲苯作为防腐剂,保存在4°C,防止光照。
- 准备试剂。
- 准备反式-4-羟基-L-脯氨酸。溶解于水中以制成4 mg / mL溶液。
- 准备氯胺T。溶解于水中制成14.1 mg / mL溶液。
- 准备醛 - 高氯酸盐。将1.5g 4-二甲基氨基苯甲醛溶于6mL 1-丙醇,2.6mL高氯酸(注意:腐蚀性强,强氧化剂,使用适当的预防措施)和0.5mL水。
- 在一组新的1.5 mL管中,将每个重悬浮的沉淀物的样品稀释到200μL的羟基脯氨酸缓冲液中。
注意:根据样品预期的胶原蛋白含量,稀释度可以为1:4至1:50的样品:缓冲液。因此可能需要进行一些试验和错误测试来确定适用于给定样品组的稀释因子(即将样品置于标准曲线的中间)。 - 准备羟脯氨酸标准品。将羟脯氨酸缓冲液中的羟脯氨酸稀释(见7.5.1)至80μg/ mL。进行系列稀释,使0〜20μg/ mL之间的标准品为6-8 200μL。
- 加入150μL14.1 mg /mL氯胺T溶液,每个标准品和稀释样品。涡旋并在室温下孵育20分钟。
- 向每个样品和稀释样品中加入150μL醛 - 高氯酸盐溶液。涡旋并在60℃加热块中孵育15分钟。根据当地法规(含有高氯酸)处理过量的高氯酸盐溶液作为危险废物。
- 允许标准品和样品冷却,等分200μL每份,一式两份,96孔板。
- 用分光光度计在550 nm读板。根据当地法规(含有高氯酸)处理板和剩余体积在1.5 mL管中作为危险废物。
- 总胶原蛋白和胶原蛋白分数的计算。
- 使用羟脯氨酸标准曲线将每个样品的吸光度值转换为微克的羟脯氨酸。
- 将每个孔乘以2.5,计算羟脯氨酸的含量稀释样品。回想一下,将500μL总混合物(200μL稀释样品+150μL氯胺T+150μLAP溶液)中仅有200μL加入到每个样品孔中。
- 乘以稀释因子(7.7节)计算原始样品中羟脯氨酸的含量。
- 除以0.137计算胶原蛋白(假定胶原含有13.7%羟脯氨酸20 )。
注意:胶原中的哺乳动物羟脯氨酸丰度在组织和哺乳动物物种间略有不同;例如,猪和羊跟腱分别含有13.5和13.7%(羟脯氨酸质量/干组织质量) 21 。在这里,使用13.7%估计胶原蛋白中羟基脯氨酸的百分比,其用于使用以下等式计算组织样品的胶原蛋白含量: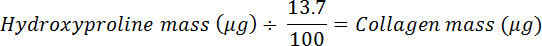
- 除以干质量计算胶原蛋白并转换成百分比。
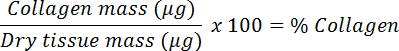
8.分子终点的定量
注意:除了拉伸试验和胶原蛋白含量的主要结果外,可以在2D或3D组织上测量分子终点,以增加机械性的洞察力。生物测定可以用于确定分子终点(参见下文的上下文)运动后血清环境对体外韧带功能的影响)。
- 对于3D组织:
- 按照上述步骤5准备结构。
- 构建治疗/干预后,在液氮中快速冷冻构建体。
- 使用在干冰上冷却的砂浆和研杵,将构造物研磨成粉末。继续步骤8.4 / 5)。
- 对于2D组织:
- 文化人类ACL成纤维细胞在一个mon汇合在含有DMEM的六孔板中。
- 吸入DMEM并根据您的实验策略( 例如时间过程或剂量反应实验)应用治疗培养基。
- 吸出处理介质并用PBS洗涤细胞。
- 使用适当的提取缓冲液/试剂刮洗细胞进行收集(见下文)。
- 蛋白质表达分析:使用胞质提取缓冲液( 例如 ,250mM蔗糖,50mM Tris pH 7.4,5mM MgCl 2和蛋白酶/磷酸酶抑制剂混合物)以获得蛋白质裂解物。进行蛋白质浓度测定,并根据标准的免疫印迹法继续分析。
- 基因表达分析:根据制造商的说明书使用500μLRNA分离试剂分离总RNA,以获得高质量的RNA。按照标准程序进行逆转录和实时定量PCR分析。
- DNA分离:分离和定量g根据制造商的说明使用DNA分离试剂进行染色体DNA测序。通过使用分光光度计来量化DNA浓度以测量260nm处的样品吸光度。
结果
工程韧带形成和实验干预概述
图1显示了工程韧带形成的概况。通过将正磷酸/柠檬酸溶液与磷酸三钙在圆柱孔中组合来制备骨质替代材料22 。或者,如果不是直接测量组织的机械功能,则可以使用3-0丝线缝合作为组织形成的锚。将它们在有机硅涂覆的35mm培养皿中相隔12mm,并通过浸泡在70%乙醇中灭菌。成纤维细胞与ACL重建术前获得的前交叉韧带残留物分离。膨胀后,将2.5×10 5个细胞包封在形成于水泥锚固钉的盘子中的纤维蛋白凝胶中。形成后,韧带约束可以检查机械性能,胶原含量,细胞增殖,基因表达,蛋白质水平和组织形态的变化。
在整个培养过程中,细胞收缩纤维蛋白凝胶并在两个锚点之间形成线性组织( 图2A )。在培养1-2天后,细胞已经附着于纤维蛋白凝胶,延长细胞过程,并开始施加牵引力( 图2B )。由于纤维蛋白凝胶被牵引力收缩并被细胞酶分解,在两个锚点之间产生张力,并且我们的细胞平行于该轴线对齐( 图2B )并开始沉积胶原蛋白。 4-5天后,构建体已经在形成线性圆柱形组织的锚定体周围收缩( 图2A ;在这一点上,外部刺激可以应用于系统此时避免破坏线性组织形成过程)。干预措施可以包括在给定干预后补充培养基与人或动物血清,外源性细胞因子和生长因子,采用机械刺激或改变其他环境因素如氧气压力。使用补充有200μM抗坏血酸,50μML-脯氨酸和5ng / mL TGF-β1的生长培养基(含有10%FBS和100U / mL青霉素的DMEM),我们确定细胞增殖在整个2周培养中持续期间( 图2C ),实际上,光学显微镜显示在培养14天时含有高度排列的细胞的致密组织( 图2B )。
工程韧带评估
在培养期结束时,可以在多个品种中评估工程化韧带的方式。该系统的主要优点是通过机械测试来确定组织的功能变化的能力,这是给予天然韧带的机械作用的重要评估。可以使用单轴拉伸试验来测量机械性能,包括负载损坏,极限拉伸强度和杨氏模量。粘弹性也可以用应力松弛和蠕变试验测量。 图3A描绘了在定制的单轴拉伸试验机中保持在反模压夹具中的工程韧带。右侧把手连接到力传感器,以测量当组织变形失效时穿过韧带的负载。 图3B示出了用于破坏测试的代表性应力 - 应变图。在进行机械测试之后,可以将相同的构建体干燥并加工用于羟脯氨酸测定23以评估总胶原含量以及其它生物学神经测定。每个条件有足够数量的附加样品,可以进行实验干预的彻底检查,包括其对细胞增殖,基因和蛋白质表达的影响以及组织学形态。虽然14天是我们研究的典型终点,但是如图3C所示,工程化韧带通过28天的培养继续改善其机械性能和胶原含量,并且可以在培养物24中存活至少3个月。
供体变异性是实验重复性的重要考虑因素。 图4显示了Lee 等人报道的代表性实验。比较7个不同的ACL供体(n = 3个男性和n = 4个女性),显示了在前面描述的2周培养后典型的拉伸性能和胶原含量补充生长媒体。使用来自类似ACL集合的细胞,供体年龄,损伤后时间,性别等,工程化韧带在雄性和雌性供体之间表现出低的供体变异性和胶原分数差异之间的相似特征。在上述研究中,将工程化韧带用作体外模型,以研究为什么女性与男性相比具有显着更高的ACL损伤风险,并且证明从女性供体分离的ACL成纤维细胞本身不会形成较弱的和较少的胶原工程韧带。
运动后血清环境对体外韧带功能的影响
我们以前已经证明了工程韧带用于探测生理过程的能力1 ,ss ="xref"> 25。在West等人报道的以下代表性实验中1 ,我们确定了运动对韧带功能的生物化学作用,并突出了这里的方法和发现。我们使用人类ACL细胞形成工程化韧带,并在培养的第7天进行干预,由运动前或运动后收集的人血清调理培养基组成。简而言之,我们招募健康的年轻男性参与者,并在急性抗性运动之前和之后收集血液样本,增加循环激素和包括人生长激素(GH)在内的细胞因子。从运动前和运动后血液样品中分离人血清,并在培养基中代替胎牛血清用于工程化韧带培养的第二周( 图5A )。运动前和运动后血清样品使用ELISA分析GH和胰岛素样生长因子1(IGF-1)的变化,其浓度可以通过运动改变( 图5B )。该信息用于将工程化韧带的血清作用与运动中血清的变化相关联。在14天培养期后,使用机械测试和羟脯氨酸测定胶原蛋白含量来评价韧带构建体,并且证明对运动后血清响应的最大拉伸载荷和胶原含量的显着增加。为了评估这种影响是否与运动诱导的GH或IGF-1释放有关,在单独的实验中形成工程化韧带,并用人重组GH或IGF-1的剂量反应进行处理。有趣的是,当血液中血清GH升高时( 图5B- i),培养基中逐渐增加的重组GH浓度不增加胶原蛋白含量( 图5D- i)或机械工程韧带中的属性(数据未显示)。相比之下,血清IGF-1水平在运动后没有增加,但是剂量反应实验显示培养基中增加的水平提高了韧带构建体的胶原蛋白含量( 图4D- ii)。因此,运动确实导致运动后GH的强劲增加,使用rhGH的剂量反应实验提出了GH是否直接对工程化韧带的表型增强负责(至少22kDa同种型单独不是似乎负责)。相反,运动后15分钟血清IGF-1没有改变,在宽范围的浓度范围内测试rhIGF-1显示IGF-1能够改善胶原蛋白含量;然而,应当注意,在估计生理水平的范围内增加rhIGF-1浓度不会显着增加胶原含量。因此,独特的运动后血清环境nment对于改善工程韧带的力学和胶原蛋白是重要的。
在本文突出的研究中,实验血清的量由于伦理考虑而受到限制;因此,使用血清需求较低的短期2D生物测定法进一步探测了所观察到的胶原蛋白增加的分子机制。将ACL成纤维细胞在6孔板中培养至汇合,并在休息或运动后血清处理1小时,并与重组GH,IGF-1,TGF-β1的剂量反应和PI3K / mTORC1中靶标的活化进行比较,ERK1 / 2和Smad信号通路。在运动后血清存在下,PI3K / mTORC1和ERK1 / 2通路显示出更大的活化,分别通过S6K磷酸化( 图5D- i)和ERK1 / 2( 图5D- ii)评估。与激素和细胞因子剂量反应相比,GH对mTOR信号传导具有小的积极作用( 图5D -i),IGF-1在最低剂量下显示出积极的作用,GH,IGF-1和TGF- -β1没有考虑PI3K / mTORC1和ERK1 / 2信号传导的增加。总之,我们的3D工程韧带模型和2D生物测定数据表明,运动后血清环境能够通过激活PI3K / mTORC1和ERK1 / 2途径来改善工程化韧带功能和胶原含量。
总之,使用工程化韧带模型结合运动调节血清,我们能够i)调查运动后血清环境对工程化韧带功能和胶原的影响,ii)将韧带表型的变化与血清激素浓度的变化相关联,目的是确定血清中哪些变化导致变化并且iii)通过使用2D生物测定法探测血清生化环境的分子靶标来确定通过运动后血清激活的导致韧带功能改善的分子机制来进一步扩展其工作范围。
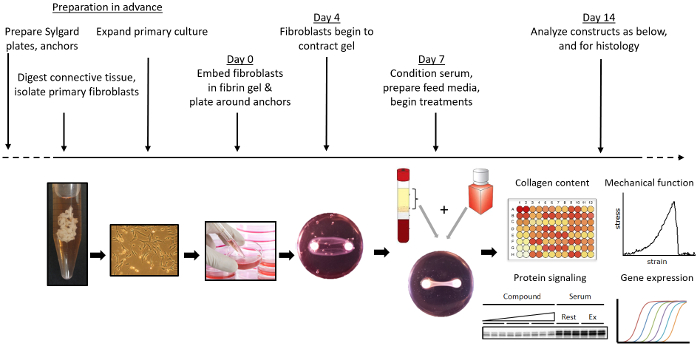
图1:工程韧带的形成和使用概述。制造刷石水泥锚栓并固定在硅胶涂层板中。原代成纤维细胞被分离并从ACL残留物扩增。工程化的韧带通过在纤维蛋白凝胶中围绕两个水泥凝固锚固体包裹成纤维细胞形成。将工程化的韧带培养并用任何特定化学物质或机械( 例如 ,通过生物反应器)所需的刺激进行处理。在所需的终点,可以收集工程化韧带并评估机械性能l性质,基因表达,胶原含量,蛋白质表达和组织学。 请点击此处查看此图的较大版本。
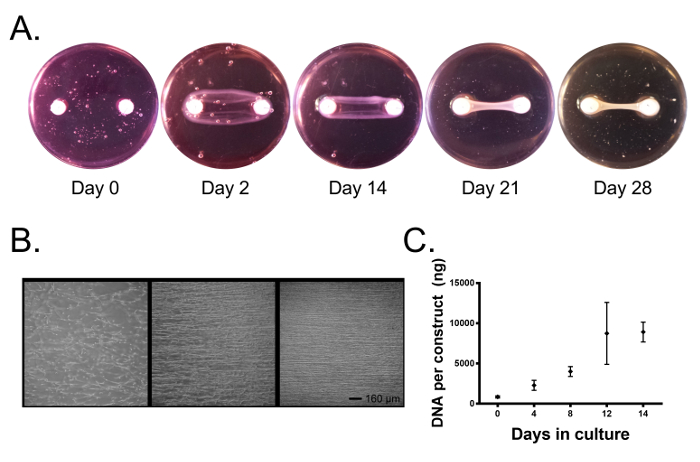
图2.原发性韧带成纤维细胞形成跨越两个水泥凝固锚的纤维蛋白基骨 - 骨工程韧带。 ( A )随着时间的推移,成纤维细胞在纤维蛋白凝胶周围收缩形成线性组织。 ( B )在头三天,细胞附着在纤维蛋白凝胶上并施加牵引力,使细胞与构建体的长轴对齐。超过14天,细胞形成高度排列的组织。刻度尺= 160μm。 ( C )工程韧带的DNA含量继续增加o随着细胞增殖,培养14天。数据以平均值±SD表示,每组n = 3-4组。组。 请点击此处查看此图的较大版本。
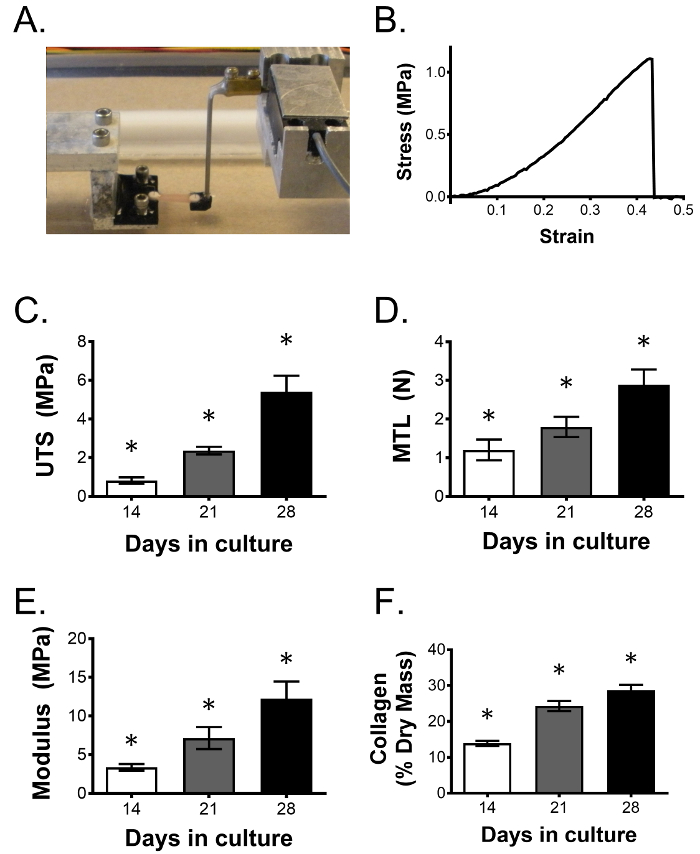
图3:工程韧带机械性能和胶原蛋白含量随时间而改善。 ( A )韧带构建体进行单轴拉伸试验,以确定给定干预对韧带功能的影响。如图所示,两个反模制的3D打印夹具保持由工程化的脊梁桥接的互相形状的锚。锚固件与步进马达和力传感器耦合以产生测试组织的应力/应变曲线,从而可以确定机械性能。 ( B </ strong>)来自工程化韧带的代表性应力 - 应变曲线应变到失效。在28天的过程中,( C )极限拉伸强度(UTS),( D )最大拉伸载荷(MTL),( E )杨氏模量和( F )胶原分数持续改善。数据以平均值±SD表示,每组n = 5个构建体。 *表示与所有其他组有显着差异。 请点击此处查看此图的较大版本。
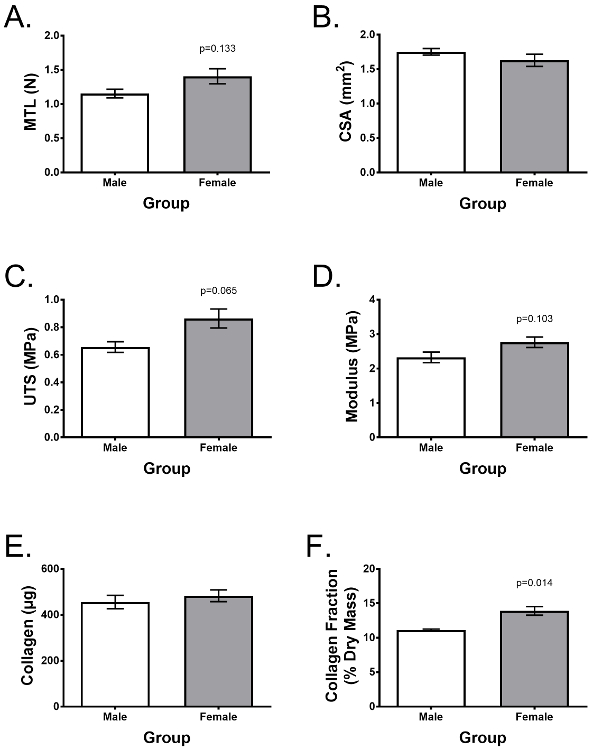
图4:可以评估工程韧带的功能和生物化学含量,显示低供体变异性。工程韧带形成7个不同的供体(n = 3男,n = 4女)。 2周后o评估了( A )最大拉伸载荷,( B )极限拉伸强度(UTS),( C )杨氏模量,( D )横截面积(CSA),( E )每个的总胶原含量的差异构建和( F )胶原蛋白作为干质量的一部分。数据以平均值±标准差表示,统计学显着性为Student's t检验。 *表示与其他组有显着性差异(p <0.05)。 Lee改编自Lee 等人 25 请点击此处查看此图的较大版本。
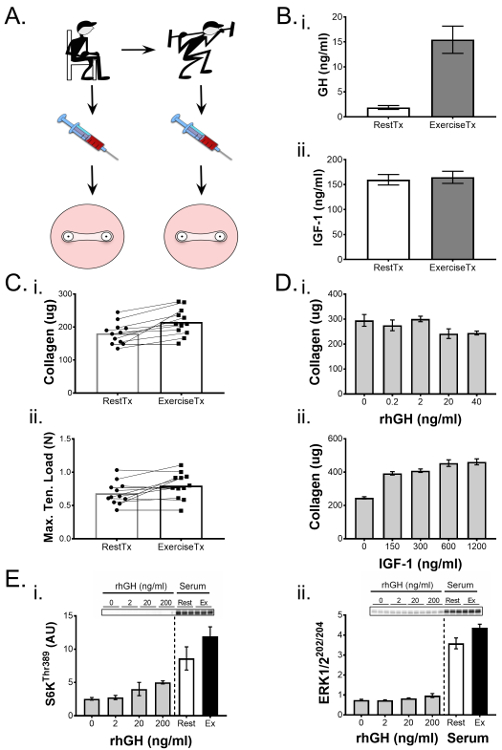
图5.工程韧带表现出对生物反应的机械和生物化学变化gical干预。 ( A )从收集自(RestTx)和运动后(ExTx)的受试者的血液抽吸中分离血清,并用于在培养的第二周治疗工程化韧带。 ( B )(i)通过ELISA定量其余和运动血清中的人生长激素(GH)和(ii)胰岛素样生长因子(IGF)-1水平。 ( C )用ExTx处理的工程韧带表现出改善的(i)胶原含量和(ii)最大拉伸载荷。通过t检验分析成对比较(RestTx和ExTx)的统计学意义,显着性水平设置为p <0.05。 ( D )使用(i)GH和(ii)IGF-1的剂量反应来确定这些因素对由ExTx引起的胶原含量变化的可能贡献。 E)使用2D生物测定来比较增加剂量的GH,RestTx和ExTx对分子信号靶标的影响,例如(i)S6K Thr38的磷酸化9和(ii)ERK1 / 2 Thr202 / Tyr204 。使用ANOVA和Tukey's HSD进行两个以上实验组的统计学比较。数据以平均值±SD表示。 *表示与对照有显着性差异(p <0.05),§表示与150 ng / mL和300 ng / mL IGF-1有显着差异。图改编自West 等 1 请点击此处查看此图的较大版本。
讨论
本手稿描述了韧带组织的模型,这是一个有用的实验平台,用于从组织发育到翻译/临床问题的广泛研究课题的研究者。这里描述的工程韧带模型基于通用协议,可以在整个工作流程中的各个点( 图1和讨论部分 )进行调整。此外,通过用饲养培养基补充条件的人或动物血清,体外环境的固有的还原性质可以更接近于生理领域。
构建体可以使用来自各种来源的成纤维细胞形成
虽然这里显示的方法和代表性结果是基于使用原代ACL成纤维细胞,但可以调整细胞分离方案以收集其他类型的原代成纤维细胞。如上所述在图4中 ,与从年轻人供体分离的原代细胞形成的工程化韧带显示出低的供体变异性。初级细胞受初始隔离和通过限制的限制;细胞系的使用可以提高实验的重现性。使用其他细胞类型可能需要修饰细胞培养基和纤维蛋白凝胶制剂。例如,我们已经观察到,人类间充质干细胞(MSC)不能在2周的时间内在钙质骨水泥锚固体之间形成线性组织,而马超级数字屈肌腱成纤维细胞,马骨髓基质细胞,鸡胚腱成纤维细胞,并且鼠C3H10T1 / 2 MSC快速收缩和消化纤维蛋白凝胶以形成线性组织(未发表的观察)。这种对比可能是细胞收缩力,增殖和纤维蛋白溶解酶生产差异的结果。
化学应用和机械刺激
在本文所述的方法中,基于纤维蛋白的组织形成在水泥凝固锚固件周围,允许通过拉伸生物反应器11施加机械刺激以及用于终点拉伸试验。水泥 - 软组织界面(拟合)的存在也为进一步研究和改进提供了机会22,26(参见下面的临床应用部分)。在这种体外环境中,化学和机械因素的贡献可以更容易地识别;在图5中示出了一个例子,其中运动后血清环境的作用与运动的机械刺激分离。可能需要进行试点研究,以确定实验干预的时间范围,治疗组成以及期望可观察到的变化的适当终点。佛例如,在运动后血清研究1中 ,实验治疗的长度受到用于补充培养基的血清的供应的限制,其中每隔一天喂养构建体。此外,在培养的第二周期间,在除去TGF-β1之前,用抗坏血酸和L-脯氨酸维持培养基补充休息或运动后血清。 TGF-β1是已知的促纤维化生长因子,其在运动后血清中增加27 。因此,为了避免模糊运动后血清的TGF-β1相关作用,该细胞因子在培养基中不能维持。
这种工程化的韧带模型也可用于测试机械拉伸的效果。通过设计反向模型夹具来保持水泥锚固端(类似于图1中所示的单轴拉伸试验机),拉伸生物反应器可以设计成适应绞痛韧带我们的实验室以前已经使用该模型来研究工程化韧带在定制生物反应器11中的单轴拉伸拉伸的分子信号响应,这将为体外拉伸范例的合理设计提供更好的理解,甚至可能在体内拉伸/活动/治疗应用。
工程韧带评估
与传统的单层培养一样,可以测定3D构建体的基因/蛋白质表达;此外,他们的3D形态还提供了评估功能和形态变化的机会,并且构建体可以在文化中保持长期研究( 图3 )。虽然工程化韧带不等同于天然的成熟韧带,但它们与发育中的腱/韧带具有相似性,并且与营养物质的响应与天然组织的表现相似"> 26,生长因子10 ,激素25和运动11,28。因此,在从任何体外模型进行广泛推广之前,谨慎是有必要的,韧带构建体测试的结果可以揭示或通知特定的生理机制,否则可能是不可能在体内进行调查。
补充饲料培养基与调理血清用于具有广泛应用的灵活和动态模型
人血清代谢组是约4500种化合物的环境,包括但不限于糖蛋白,脂蛋白,脂质衍生物,能量底物,代谢物,维生素,酶,激素,神经递质和多种构建块/中间体。 29根据化合物类别29对人血清代谢组进行进一步检查显示另外将实验血清整合到体外实验中的有益效果。也就是说,血清中约4500种化合物中的大多数是疏水性或脂质衍生物,强调结合蛋白质用于转运/溶解的重要性。因此,实验上总结了内源化合物运输动力学,因此生物利用度和化合物 - 靶标相互作用几乎是不可能的。因此,实验性血清对已知依赖辅助分子进行溶解,运输,靶标结合和作用机制的化合物的研究特别有效。
我们的实验室对运动的健康益处有着长期的兴趣。运动会改善整个身体12各种组织中的细胞和器官功能,这可能归因于多种因素(如IL-6 13 ,IL-15 14 ,Meteorin-like 15 ,外来体16,17 ),其被释放到全身循环中。运动后生化环境反映了骨骼肌运动反应激素的释放因素,以及由于分泌腺的交感神经系统刺激释放的因素( 例如 ,肾上腺18的皮质醇和儿茶酚胺以及生长发育激素从垂体前叶19 )。我们最近使用运动前和运动后血清的模型来研究运动诱导的生化环境对工程组织的影响。 1尽管许多重要的运动相关研究问题仍然存在,但是这种模式决不会受到限制。例如,在饮食或药物干预后,或来自不同年龄组或临床人群中,可以从动物或人源获得血清s 30 。以这种方式,感兴趣的外源或内源化合物将以生物可利用量存在于血清和治疗介质中,并且将与内源环境( 即 ,在更生理上下文中)一致地与靶组织相互作用。这种方法是动态的,因为给定的干预将很可能发挥多器官(和多重化合)效应,因此生理环境将被共同修饰。虽然这种方法提出了一些挑战,因为多个系统生物化学变量同时改变,这是一种可以帮助克服纯减少实验方法31,32的缺点的方法。总而言之,实施调理血清与组织工程( 体外仿生 )组织可用作生理学,营养学和临床研究问题的工具。
临床应用很多
这里介绍的组织工程模型可用于研究传统体外模型不能解决的解剖和临床研究问题。 体内的韧带或肌腱包含称为假体的软 - 硬组织过渡区域。容易受到机械应力相关损伤的诱发33可以通过组织化学和电子显微技术22,26在横截面上进行研究。这种独特的界面对于具有低或受限流动性的那些人来说是重要的,因为身体不活动会损害结缔组织将负荷转移到低至高顺应性区域34的能力 ,最终导致组织依从性的总体降低和增加的损伤风险。
我们的实验室最近使用了这种组织工程模型25/ sup>模拟另一个人群,女运动员谁是风险的结缔组织损伤:ACL损伤的发生率比男性同行35的大约五倍。通过以模拟月经周期阶段的浓度处理具有生理浓度的女性性激素(雌激素)的韧带构建体来研究支持这种基于性别的损伤差异的潜在机制。有趣的是,高浓度的雌激素抑制了赖氨酸氧化酶的基因表达和活性,其是负责在韧带和腱的胶原基质中产生赖氨酸 - 赖氨酸交联的主要酶。重要的是,48h的高雌激素(以模拟滤泡期)降低韧带构建刚度,而不改变构建体的胶原密度。从生理角度来看,这表明女性韧带松弛度的增加可能是由于至少部分减少交联形成。从实验的角度来看,这些发现25突显了3D建模模型的实用性,从而允许检查功能交联活动。从临床角度来看,该模型现在可用于快速筛选可以预防韧带功能雌激素负面影响的干预措施。
结束语
在这里,我们提出了一种详细的方法,用于形成工程韧带及其作为3D 体外组织模型的实用性。该模型高度适应广泛的目标,提供细胞类型,干预措施和感兴趣的结果测量的灵活性。用调理血清补充饲料培养基增加了在传统体外环境中无法实现的生理背景,改善了体内生理学的建模。总之,我们认为这是广泛适用的模式l对促进生理和组织工程领域的兴趣有所启发。
披露声明
作者宣称他们没有竞争的经济利益。
致谢
这项工作得到了NSERC博士后研究奖学金(DWDW),ARCS基金奖学金(AL)和加州大学戴维斯分校生物科学学院授权(KB)的支持。
材料
| Name | Company | Catalog Number | Comments |
| Austerlitz Insect pins, minutien stainless steel, size 0.20 | Entomoravia | N/A | For brushite cement anchors |
| β-tricalcium phosphate | Plasma Biotal Ltd (Derbyshire, UK) | N/A | For brushite cement anchors |
| o-phosphoric acid, 85% (w/w) | EMD Millipore | PX0995 | For brushite cement anchors |
| Citric acid | Sigma-Aldrich | 251275-500g | For brushite cement anchors |
| Falcon 35 mm tissue culture dishes | Fisher Scientific | 08-772A | For silicone-coated plates |
| Sylgard 184 silicone elastomer kit | Ellsworth Adhesives | 4019862 | For silicone-coated plates |
| 1x Phosphate-buffered saline (PBS) | Fisher Scientific | SH3002802 | For cell isolation and expansion |
| 100x antibiotic/antimycotic solution | VWR | 45000-616 | For cell isolation |
| Type II collagenase | Thermo Fisher Scientific | 17101015 | For cell isolation |
| 100x penicillin/streptomycin solution | Thermo Fisher Scientific | 15140122 | For cell isolation |
| Steriflip-GP, 0.22 µm pore, polyethersulfone, gamma irradiated | EMD Millipore | SCGP00525 | For reagent sterilization |
| DMEM high glucose with sodium pyruvate and L-glutamine | VWR | 10-013-CV | For cell and tissue culture |
| Fetal bovine serum | BioSera | FBS2000 | Component of tissue digestion media and growth media |
| Penicillin G Potassium Salt | MP Biomedicals | 0219453680 - 100 MU | Component of growth media. Dissolve in water to 100,000 U/mL, filter sterilize, aliquot, and store at -20°C. |
| CELLSTAR polystyrene tissue culture dishes (145 mm x 20 mm) | VWR | 82050-598 | For cell culture |
| Trypan blue | Thermo Fisher Scientific | T10282 | For cell isolation |
| Trypsin-EDTA (0.25%) | Thermo Fisher Scientific | 25200056 | For cell culture. Dilute to 0.05% in PBS |
| Dimethyl sulfoxide | Sigma-Aldrich | 472301 | For cell freezing media |
| Nalgene Mr. Frosty Cryogenic Freezing Container | Thermo Fisher Scientific | 5100-0001 | For cell freezing |
| BD Vacutainer Red Plastic 10 mL | Fisher Scientific | 367820 | For human serum collection |
| Bound Tree Insyte Autoguard IV Catheters, 22 G x 1 inch Needle | Fisher Scientific | 354221 | For human serum collection |
| Thrombin, bovine origin | Sigma-Aldrich | T4648-1KU | For engineered ligament formation. Dissolve at 200 U/mL in DMEM high glucose media. Filter at 0.22 μm, aliquot, and store at -20 °C. |
| Fibrinogen, bovine origin | Sigma-Aldrich | F8630-5G | For engineered ligament formation. Dissolve at 20 mg/mL in DMEM high glucose media. Filter at 0.22 μm, aliquot, and store at -20 °C. |
| Aprotinin from bovine lung | Sigma-Aldrich | A3428 | For engineered ligament formation. Dissolve at 10 mg/mL in water. Filter at 0.22 μm, aliquot, and store at -20 °C. |
| 6-Aminohexanoic acid | Sigma-Aldrich | 07260-100g | For engineered ligament formation. Dissolve at 0.1g/mL in water. Filter at 0.22 μm, aliquot, and store at 4 °C. |
| L-Ascorbic acid 2-phosphate sesquimagnesium salt hydrate | Sigma-Aldrich | A8960-5G | Component of feed media. Dissolve in DMEM high glucose media at a concentration of 50 mM. Filter at 0.22 μm and store at 4 °C. |
| L-proline | Sigma-Aldrich | P5607-25G | Component of feed media. Dissolve in PBS at a concentration of 50 mM. Filter at 0.22 μm and store at 4 °C. |
| Transforming growth factor-β1 | Peprotech | 100-21 | Component of feed media. Reconsistute according to manufacturer's instructions at a concentration of 10 μg/mL. Aliquot and store at -20 °C. |
| Stericup-GP, 0.22 µm, polyethersulfone, 250 mL, radio-sterilized | EMD Millipore | SCGPU02RE | For reagent sterilization |
| Hydrochloric acid | Fisher Scientific | A144-212 | Dilute in water to 6 M |
| 4-Dimethylaminobenzaldehyde | Sigma-Aldrich | 39070-50g | For hydroxyproline assay |
| Chloramine-T trihydrate | Sigma-Aldrich | 402869-100g | For hydroxyproline assay |
| trans-4-Hydroxy-L-proline | Sigma-Aldrich | H54409-100g | For hydroxyproline assay |
| 1-propanol | Sigma-Aldrich | 279544-1L | For hydroxyproline assay |
| Perchloric acid | Sigma-Aldrich | 311421-250ml | For hydroxyproline assay |
| Acetic acid, glacial | EMD Millipore | AX0073-9 | For hydroxyproline assay |
| Sodium hydroxide | Fisher Scientific | S318-500 | For hydroxyproline assay |
| Toluene, anhydrous | Sigma-Aldrich | 244511-1L | For hydroxyproline assay |
| Corning Costar Clear Polystyrene 96-Well Plates | Fisher Scientific | 07-200-656 | For hydroxyproline assay |
参考文献
- West, D. W., et al. The exercise-induced biochemical milieu enhances collagen content and tensile strength of engineered ligaments. J Physiol. 593 (20), 4665-4675 (2015).
- Booth, F. W., Laye, M. J. Lack of adequate appreciation of physical exercise's complexities can pre-empt appropriate design and interpretation in scientific discovery. J Physiol. 587 (Pt 23), 5527-5539 (2009).
- Booth, F. W., Hargreaves, M. Understanding multi-organ pathology from insufficient exercise. J Appl Physiol (1985). 111 (4), 1199-1200 (2011).
- Shearn, J. T., et al. Tendon tissue engineering: progress, challenges, and translation to the clinic. J Musculoskelet Neuronal Interact. 11 (2), 163-173 (2011).
- Liu, C. F., et al. What we should know before using tissue engineering techniques to repair injured tendons: a developmental biology perspective. Tissue Eng Part B Rev. 17 (3), 165-176 (2011).
- Vunjak-Novakovic, G., Altman, G., Horan, R., Kaplan, D. L. Tissue engineering of ligaments. Annu Rev Biomed Eng. 6, 131-156 (2004).
- Bayer, M. L., et al. The initiation of embryonic-like collagen fibrillogenesis by adult human tendon fibroblasts when cultured under tension. Biomaterials. 31 (18), 4889-4897 (2010).
- Guerquin, M. J., et al. Transcription factor EGR1 directs tendon differentiation and promotes tendon repair. J Clin Invest. 123 (8), 3564-3576 (2013).
- Ma, J., et al. Three-dimensional engineered bone-ligament-bone constructs for anterior cruciate ligament replacement. Tissue Eng Part A. 18 (1-2), 103-116 (2012).
- Hagerty, P., et al. The effect of growth factors on both collagen synthesis and tensile strength of engineered human ligaments. Biomaterials. 33 (27), 6355-6361 (2012).
- Paxton, J. Z., Hagerty, P., Andrick, J. J., Baar, K. Optimizing an intermittent stretch paradigm using ERK1/2 phosphorylation results in increased collagen synthesis in engineered ligaments. Tissue Eng Part A. 18 (3-4), 277-284 (2012).
- Safdar, A., et al. Endurance exercise rescues progeroid aging and induces systemic mitochondrial rejuvenation in mtDNA mutator mice. Proc Natl Acad Sci U S A. 108 (10), 4135-4140 (2011).
- Pedersen, B. K., Febbraio, M. A. Muscles, exercise and obesity: skeletal muscle as a secretory organ. Nat Rev Endocrinol. 8 (8), 457-465 (2012).
- Crane, J. D., et al. Exercise-stimulated interleukin-15 is controlled by AMPK and regulates skin metabolism and aging. Aging Cell. 14 (4), 625-634 (2015).
- Rao, R. R., et al. Meteorin-like is a hormone that regulates immune-adipose interactions to increase beige fat thermogenesis. Cell. 157 (6), 1279-1291 (2014).
- Aswad, H., et al. Exosomes participate in the alteration of muscle homeostasis during lipid-induced insulin resistance in mice. Diabetologia. 57 (10), 2155-2164 (2014).
- Safdar, A., Saleem, A., Tarnopolsky, M. A. The potential of endurance exercise-derived exosomes to treat metabolic diseases. Nat Rev Endocrinol. 12 (9), advance online publication 504-517 (2016).
- Maling, H. M., Stern, D. N., Altland, P. D., Highman, B., Brodie, B. B. The physiologic role of the sympathetic nervous system in exercise. J Pharmacol Exp Ther. 154 (1), 35-45 (1966).
- Pritzlaff, C. J., et al. Impact of acute exercise intensity on pulsatile growth hormone release in men. J Appl Physiol (1985). 87 (2), 498-504 (1999).
- Creemers, L. B., Jansen, D. C., van Veen-Reurings, A., van den Bos, T., Everts, V. Microassay for the assessment of low levels of hydroxyproline. Biotechniques. 22 (4), 656-658 (1997).
- Neuman, R. E., Logan, M. A. The determination of hydroxyproline. J Biol Chem. 184 (1), 299-306 (1950).
- Paxton, J. Z., Donnelly, K., Keatch, R. P., Baar, K., Grover, L. M. Factors affecting the longevity and strength in an in vitro model of the bone-ligament interface. Ann Biomed Eng. 38 (6), 2155-2166 (2010).
- Woessner, J. F. Jr The determination of hydroxyproline in tissue and protein samples containing small proportions of this imino acid. Arch Biochem Biophys. 93, 440-447 (1961).
- Paxton, J. Z., Wudebwe, U. N., Wang, A., Woods, D., Grover, L. M. Monitoring sinew contraction during formation of tissue-engineered fibrin-based ligament constructs. Tissue Eng Part A. 18 (15-16), 1596-1607 (2012).
- Lee, C. A., et al. Estrogen inhibits lysyl oxidase and decreases mechanical function in engineered ligaments. J Appl Physiol (1985). 118 (10), 1250-1257 (2015).
- Paxton, J. Z., Grover, L. M., Baar, K. Engineering an in vitro model of a functional ligament from bone to bone. Tissue Eng Part A. 16 (11), 3515-3525 (2010).
- Heinemeier, K., Langberg, H., Kjaer, M. Exercise-induced changes in circulating levels of transforming growth factor-beta-1 in humans: methodological considerations. Eur J Appl Physiol. 90 (1-2), 171-177 (2003).
- Mackey, A. L., Heinemeier, K. M., Koskinen, S. O., Kjaer, M. Dynamic adaptation of tendon and muscle connective tissue to mechanical loading. Connect Tissue Res. 49 (3), 165-168 (2008).
- Psychogios, N., et al. The human serum metabolome. PLoS One. 6 (2), e16957(2011).
- Nguyen, T., et al. The effects of resting and exercise serum from children with cystic fibrosis on C2C12 myoblast proliferation in vitro. Physiol Rep. 2 (6), e12042(2014).
- Joyner, M. J., Pedersen, B. K. Ten questions about systems biology. J Physiol. 589 (Pt 5), 1017-1030 (2011).
- Joyner, M. J. Giant sucking sound: can physiology fill the intellectual void left by the reductionists? J Appl Physiol (1985). 111 (2), 335-342 (2011).
- Benjamin, M., et al. Where tendons and ligaments meet bone: attachment sites ('entheses') in relation to exercise and/or mechanical load. J Anat. 208 (4), 471-490 (2006).
- Arruda, E. M., Calve, S., Dennis, R. G., Mundy, K., Baar, K. Regional variation of tibialis anterior tendon mechanics is lost following denervation. J Appl Physiol (1985). 101 (4), 1113-1117 (1985).
- Arendt, E., Dick, R. Knee injury patterns among men and women in collegiate basketball and soccer. NCAA data and review of literature. Am J Sports Med. 23 (6), 694-701 (1995).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。