Method Article
将新生儿小鼠心脏巨噬细胞移植到成年小鼠体内
摘要
我们为新生儿心脏大噬体分离和移植到成年小鼠心脏提供了一个协议,这可能是促进心脏修复的有希望的方法。
摘要
在受伤的新生儿心肌中,巨噬细胞促进心肌细胞增殖和血管生成,促进心脏再生。本研究表明,损伤引起的新生儿心脏巨噬细胞移植可促进心肌梗塞后成人心脏再生,改善心脏功能和心肌细胞增殖。结果表明,新生儿心脏大噬体移植可能是心脏损伤治疗的一个有希望的策略。在这里,我们提供了技术细节,包括新生儿心脏巨噬细胞与剖腹产受伤的新生儿小鼠心脏分离,将巨噬细胞移植到心肌梗塞的成年小鼠体内,以及宏噬移植后心脏再生的估计。
引言
心脏再生是一个有希望的策略,恢复心脏功能后,心脏损伤,并防止心力衰竭1,2,3。心肌损伤后,巨噬细胞渗入受伤心脏,被探索为新生儿心脏再生4、5、6的关键因素。除了清除坏死细胞碎片和诱导炎症外,巨噬细胞在新生儿小鼠心肌梗塞后促进血管生成5和心肌细胞增殖7。
我们先前的研究表明,从受伤的新生儿心脏中分离出的新生儿心脏巨噬细胞移植可以增强成人心脏再生7,表明新生儿心脏巨噬细胞移植可能是治疗心脏损伤的有希望的策略。在这里,我们提供了技术细节,包括新生儿心脏巨噬细胞从剖腹产受伤的新生儿小鼠心脏分离,将巨噬细胞移植到心肌梗塞的成年小鼠体内,以及估计大噬细胞移植后心脏再生(图1)。
研究方案
所有实验都是根据《实验室动物使用和护理指南》进行的。所有动物协议均获中国医学科学院福威医院动物护理与使用委员会(IACUC)批准。在整个手术过程中需要无菌技术,以防止手术部位的污染。
1. 新生儿1天大 Cx3cr1 GFP/+ 鼠标(C57BL/6 背景)的剖腹产切除手术
- 麻醉
- 把所有的老鼠幼崽从笼子里拿出来,放在一个干净的干箱里。
- 将每只老鼠嵌入冰中约2-3分钟。确保冰和老鼠幼崽之间有一个薄的屏障,如乳胶或纱布,以防止冻伤。
- 通过观察以下迹象来识别足够的麻醉:皮肤苍白、肢体运动不足和缺乏踏板反射。
- 开 胸 术
- 在 -20 °C 下将青铜操作平台预热过夜,以帮助保持麻醉。
- 将麻醉鼠标从冰盒中取出,放在青铜操作平台上。使用医用胶带将鼠标固定在操作平台上的支撑位置。
- 将操作平台与鼠标放在立体镜下。
- 使用浸泡在βdine和70%酒精中的预制垫对鼠标胸部进行消毒,或符合机构政策。
- 在胸腔的第四个间骨区域切开1厘米的皮肤,然后用显微手术剪刀分离腹腔间肌肉,直到心脏被访问。
- 交替按胸部和腹部与两个钳子的帮助下,直到心脏外化出胸部没有任何机械损伤。
- 将小切口下方和上方的肋骨设置为自然固定,以固定心脏。
- 心室顶点截断
- 找到左心室的顶点。使用立体镜下的虹膜剪刀切割直径为 1 mm 的心室顶点组织。
- 确认左心室暴露,并开始渗出。
- 使用棉签轻轻将心脏压回胸腔。
- 用 8-0 缝合肌肉、肋骨和皮肤普罗琳缝合线。
- 操作后彻底清洁鼠标。
- 手术后护理
- 操作后,将鼠标从操作平台转移到 37 °C 加热毯上,立即为身体加热。
- 通过观察以下迹象来确认小鼠的厌食:自发呼吸恢复、肤色从苍白变为粉红色以及四肢运动。
- 一旦它恢复,把手术鼠标带回它的母亲身边。
- 如有必要,将操作鼠标与母亲的筑巢材料混合。
注意:重要的是立即将所有1天大的幼崽从母亲身上移走,然后在所有的幼崽被找回后立即全部归还。
2. 新生儿心脏巨噬体悬浮的准备工作
注:所有这些实验程序应在黑暗的地方和无菌条件下进行。
- 在剖腹产后1天收获新生儿 Cx3cr1GFP/+ 小鼠的心脏
- 在剖析一天后,对 Cx3cr1GFP/+ 鼠标实施安乐死。使用过量的二氧化碳,并按顺序斩首小鼠以实施安乐死。
- 将心脏从胸口取出,浸入带 PBS 的 10 厘米盘子中。
- 切断血管和剩余的结缔组织远离心室。切开尿道附录,使出道远离心脏。
- 心脏停止跳动后,使用显微手术剪刀将心脏切成1-2毫米3片PBS缓冲器(图2A)。
- 新生儿鼠心脏分离
- 将收获的心脏组织转移到含有2.5mL预热酶混合物(材料表)的管子中,并紧紧关闭管子。
- 倒置管子,并将其与盖下来(图2B)。
- 运行新生儿心脏分离程序(材料表)。
- 程序完成后,将管子从分离器中分离。
- 在管子中加入 7.5 mL 的 1x DMEM,并加入 10% 的 FBS。
- 过滤并将悬架转移到 15 mL 离心机管(图 2C)。将电池悬架离心 300 x g,5 分钟。
- 将细胞颗粒重新吸回1兆升的血细胞裂解溶液中,并在室温下孵育2分钟。
- 在悬架和离心机中加入 5-10 mL 的 PBS 缓冲器,在 300 x g 下 5 分钟。
- 以 1 mL 的 DMEM 中重新使用 10% FBS 的细胞颗粒。
- 新生儿心脏巨噬体隔离
- 排序 Gfp= 由 FACS 的新生儿心脏巨噬细胞。在含有 500 μL DMEM 的无菌管中接收分类巨噬细胞,并配有 10% FBS。
- 计算 GFP+ 巨噬细胞 (图 2D)。以每 200 μL DMEM 1 x 106 巨噬细胞的浓度,以 10% FBS 重用 DMEM 中的宏噬菌体,以便以后注射。
注:GFP+ 巨噬细胞的数量在一个新生儿中很小(大约 1 x 105):因此,至少应使用10个新生儿来获得足够的巨噬细胞,每次成年小鼠注射。
3. 新生儿心脏大噬体移植
- 通过将左前冠状动脉8连合,对成人(6-8周大)雄性C57BL/6小鼠进行心肌梗塞手术。
- 将操作鼠标放在 37 °C 加热毯子上,直到恢复。
- 手术后(大约6小时后),通过尾静脉向梗塞的成年小鼠静脉注射200微升DMEM,配以1×106 GFP+新生儿心脏巨噬细胞。
- 把老鼠送回干净的笼子里
4. 结果评估
- 注塑效率验证
- 麻醉手术鼠标,在心肌梗塞手术后7天收获心脏。
- 将心脏浸入预冷却的 PBS 缓冲器中。
- 在室温下用4%多甲醛修复心脏组织72小时,并发抖。
- 二甲苯和乙醇中的心脏组织脱水。
- 将心脏组织嵌入石蜡中,切成厚度为 5 μm 的部分。
- 执行标准免疫荧光染色协议1。使用α作用素标记心肌细胞。
- 检测接受移植的心脏中的 GFP+ 巨噬细胞。
- 执行标准免疫荧光染色协议1。分别使用α-actinin和pH3标记心肌细胞和细胞增殖(图3A)。
- 移植后心脏修复评估
- 操作后一个月在操作鼠标上使用声心动图1。
- 通过比较不同组的左心室弹出分数和分数缩短(图3B),分析心脏功能。
- 麻醉手术鼠标和收获心脏。
- 重复步骤 4.1.2-4.1.5。
- 执行马森的染色协议。
- 分析巨噬体注射后的梗塞区域(图3C)。
结果
此处描述的协议在流程图(图 1)中汇总。我们在1天大的Cx3cr1GFP/+鼠标上进行了剖析手术。如图2A所示,新生儿Cx3cr1GFP/+鼠标在麻醉后被固定在立体镜下的操作平台上。在两个钳子的帮助下,我们交替地对老鼠的胸部和腹部施加压力,这两个钳子可以设置为引导心脏从胸部弹出的通道。应避免对心脏造成任何额外的机械损伤,以免影响心脏再生。心脏被周围的胸组织固定,这有利于心肌手术。我们发现,当左心室开始渗出时,用虹膜剪刀切断直径小于1毫米的切除顶点组织是合适的。成功引入乳腺剖面模型是巨噬体移植8、9的必要条件。
我们严格按照新生儿心脏分离协议1(图2)对GFP+巨噬细胞进行排序。
新生儿心脏巨噬细胞在分离后不久被注射到心肌梗塞的成年小鼠心脏中。为了确认大噬体移植的效率,我们在注射后7天进行了免疫荧光染色。结果表明,在成人心肌梗塞小鼠心脏中可以发现GFP-巨噬细胞,表明新生儿心脏巨噬细胞移植成功。我们采用了pH3与α-actinin共同免疫染色。共同定位被认为是心肌细胞增殖。结果表明,大噬细胞注射组的增殖性心肌细胞数量增加,表明移植后成人心肌细胞增殖能力增强(图3)。
移植1个月后,对成年小鼠心脏再生进行了评估。我们在成年小鼠身上进行了心电图检查,发现大额注射可以增强心肌梗塞后的心脏功能。马森的染色进行了,结果表明,新生儿心脏巨噬体移植后,梗塞面积显著减少(图3)。所有这些结果表明,新生儿心脏巨噬细胞移植促进成年小鼠心脏再生和心肌细胞增殖。
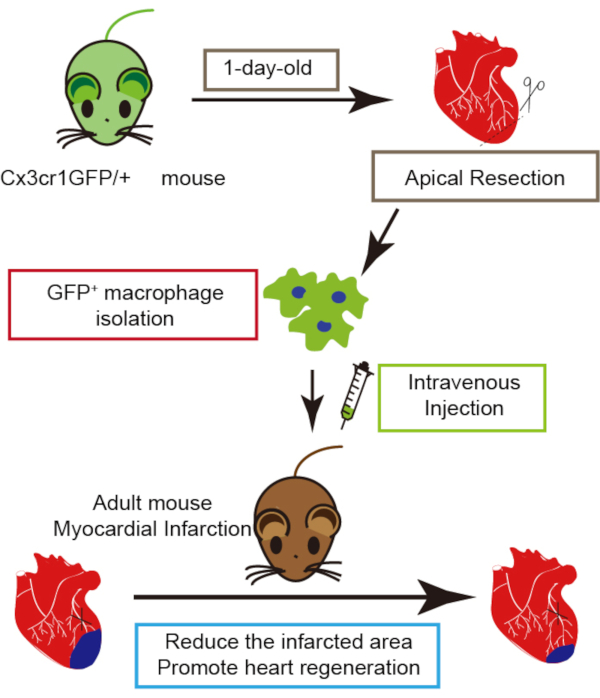
图1:新生儿心脏大噬细胞移植的示意图,请点击这里查看此图的较大版本。
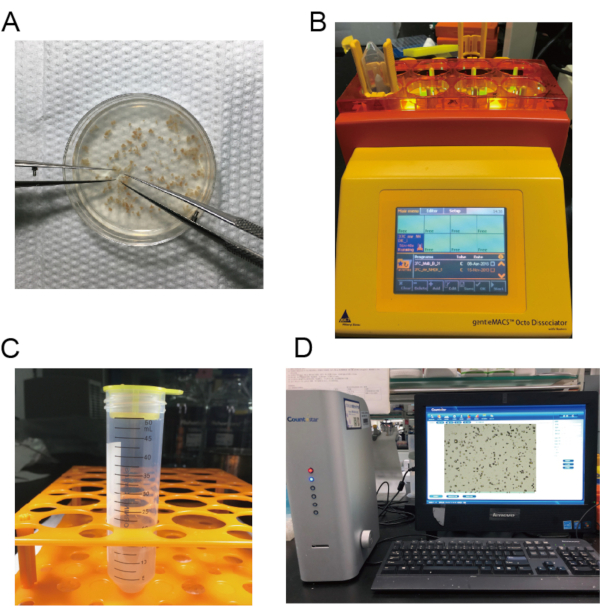
图2:巨噬体隔离图像。A) 心被切成小块。 B) 老鼠的心是分离的。 C) 悬架被过滤并转移到15mL离心机管。 D) 计算新生儿心脏巨噬细胞的数量。 请单击此处查看此图的较大版本。
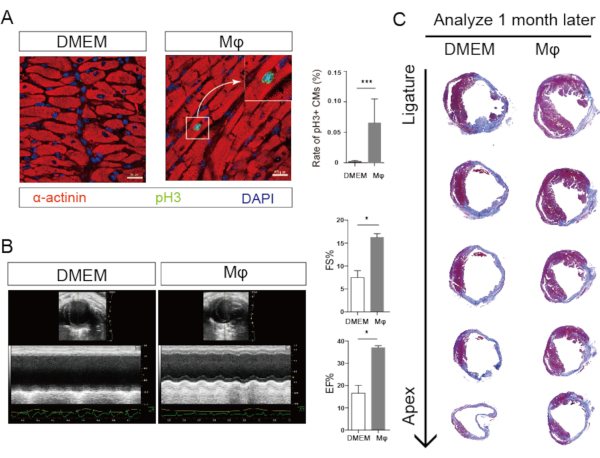
图3:新生儿心脏大噬体移植促进成人心脏再生。A) (左) 免疫荧光图像显示增殖性心肌细胞(箭头,pH3 绿色,α-行动素红色)。(右)统计分析表明,大噬细胞移植后心肌细胞增殖增加。 B) (左) 心电图图像显示心肌梗塞后1个月成年小鼠的心脏功能。(右)统计分析表明,大噬体移植后心脏功能增强。 C) 马森的染色显示成年小鼠心肌梗塞1个月后的梗塞区域。(右)统计分析表明,大噬体移植后,梗塞面积减少。 请单击此处查看此图的较大版本。
讨论
在这里,我们提供了一个有效的方法来准备,获得和移植新生儿心脏巨噬细胞,以促进成年小鼠心脏再生。
Apical剖析是刺激心脏再生的简单而有效的手术。我们优化了剖析的细节,以确保参与手术的动物的最大存活率。麻醉时间不应超过3分钟,这会导致体温过低导致的死亡,或短于2分钟,这将导致手术过程中出血过多。标准顶点剖析应截肢约1.5毫米直径的顶点组织。然而,这里的手术的目的是刺激心脏再生过程中丰富的巨噬体渗透。直径小于1.5毫米的截流是可以接受的,因为它可以保证最大的存活率和有效的巨噬体招募在同一时间。只有操作员的熟练程度影响了存活率,手术鼠在长时间的手术中无法存活。操作员应在 5 分钟内完成整个程序。
在我们以前的研究中,我们发现急性炎症促进新生儿心脏再生。免疫原性酶A颗粒进入新生儿小鼠心脏的心肌内微注射可促进心肌细胞增殖6。最近,Molkentin等人声称,由注射酶A、细胞碎片和冷冻/解冻杀死的细胞刺激的巨噬细胞渗透可以促进心脏修复,证实急性炎症和巨噬细胞在心脏修复中至关重要,而不是干细胞分化成心肌细胞11。萨德克等人5日报告说,巨噬细胞可以通过血管生成促进新生儿心脏再生。我们最近的研究表明,新生儿心脏巨噬细胞注射可以促进成人心脏再生,提高成人心肌细胞增殖1,7的能力。新生儿心脏大噬体移植可能是促进成年小鼠心脏再生的一项很有前途的策略。在这里,我们介绍协议,以帮助更多的研究人员的再生应用开发和探索心脏再生机制。
披露声明
没有利益冲突。
致谢
这项工作得到了中国医学科学院医学创新基金(CIFMS,2016-I2M-1-015)、中国国家重点研究发展项目(2019YFA0801500)、中国国家自然科学基金(NSFC:81970243、81770308)、北京自然科学基金会(7172183、7182140)的支持。
材料
| Name | Company | Catalog Number | Comments |
| Anti-mouse alpha actinin | Abcam | Ab9465 | |
| Anti-phospho-Histone H3 | Millipore | 06-570 | |
| Anti-rabbit Aurora B | Abcam | Ab239837 | |
| Anti-rabbit Ki67 | Abcam | Ab15580 | |
| gentleMACS Octo Dissociator | Miltenyi Bio Tech, Teterow, Germany | N/A | |
| Goat anti-mouse Alexa Fluor 555 | Invitrogen | A-21137 | |
| Goat anti-rabbit Alexa Fluor 488 | Invitrogen | A-11008 | |
| Neonatal Heart Dissociation Kit | Miltenyi Bio Tech, Teterow, Germany | 130-098-373 |
参考文献
- Li, Y., et al. gp130 Controls Cardiomyocyte Proliferation and Heart Regeneration. Circulation. 142 (10), 967-982 (2020).
- Pei, J., et al. Hydrogen Sulfide Promotes Cardiomyocyte Proliferation and Heart Regeneration via ROS Scavenging. Oxidative Medicine and Cellular Longevity. , 1412696 (2020).
- Wang, Y., et al. Mydgf promotes Cardiomyocyte proliferation and Neonatal Heart regeneration. Theranostics. 10 (20), 9100-9112 (2020).
- Lavine, K. J., et al. Distinct macrophage lineages contribute to disparate patterns of cardiac recovery and remodeling in the neonatal and adult heart. Proceedings of the National Academy of Sciences of the United States of America. 111 (45), 16029-16034 (2014).
- Aurora, A. B., et al. Macrophages are required for neonatal heart regeneration. Journal of Clinical Investigation. 124 (3), 1382-1392 (2014).
- Han, C., et al. Acute inflammation stimulates a regenerative response in the neonatal mouse heart. Cell Research. 25 (10), 1137-1151 (2015).
- Li, Y., et al. Transplantation of murine neonatal cardiac macrophage improves adult cardiac repair. Cellular & Molecular Immunology. , (2020).
- Yue, Z., et al. PDGFR-β Signaling Regulates Cardiomyocyte Proliferation and Myocardial Regeneration. Cell Reports. 28 (4), 966-978 (2019).
- Wang, J., et al. A long noncoding RNA NR_045363 controls cardiomyocyte proliferation and cardiac repair. Journal of Molecular and Cellular Cardiology. 127, 105-114 (2019).
- Li, Y., et al. Achieving stable myocardial regeneration after apical resection in neonatal mice. Journal of Cellular and Molecular Medicine. 24 (11), 6500-6504 (2020).
- Vagnozzi, R. J., et al. An acute immune response underlies the benefit of cardiac stem cell therapy. Nature. 577 (7790), 405-409 (2020).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。