Method Article
Adsorptionsvorrichtung Basierend auf einem Langatate Crystal Micro für Hochtemperatur-Hochdruck-Gas Adsorption in Zeolith H-ZSM-5
In diesem Artikel
Zusammenfassung
A protocol for high-temperature and high-pressure gas adsorption measurements on zeolite H-ZSM-5 using an adsorption measurement device based on a langatate crystal microbalance is presented. Prior to the adsorption measurements, the synthesis of zeolite H-ZSM-5 on the langatate crystal microbalance sensor by the steam-assisted crystallization (SAC) method is demonstrated.
Zusammenfassung
Wir stellen eine Hochtemperatur- und Hochdruck-Gasabsorptionsmessvorrichtung basierend auf einer Hochfrequenz-Oszillatormikrowaage (5 MHz langatate Kristall-Mikrowaage, LCM) und seine Verwendung zur Gasadsorptionsmessungen in Zeolith H-ZSM-5. Vor den Adsorptionsmessungen, Zeolith H-ZSM-5-Kristallen auf der Goldelektrode in der Mitte des LCM synthetisiert wurden, ohne durch die Dampfunterstützung Kristallisation (SAC) Verfahren zum Oszillator die Verbindungspunkte der Goldelektroden bedeckt, so daß die Zeolithkristalle bleiben mit dem oszillierenden Mikrowaage angebracht, während während der Adsorptionsmessungen gute elektrische Leitfähigkeit der LCM zu halten. Im Vergleich zu einem herkömmlichen Quarzkristall - Mikrowaage (QCM) , die auf Temperaturen unter 80 ° C begrenzt ist, das LCM kann die Adsorptionsmessungen prinzipiell bei Temperaturen so hoch wie 200-300 ° C realisieren (dh bei oder nahe der Reaktionstemperatur von die Zielanwendung von einem einstufigenDME-Synthese aus Synthesegas), aufgrund der Abwesenheit von kristallinen Phasenübergängen bis zu seinem Schmelzpunkt (1.470 ° C). Das System wurde angewendet , um die Adsorption von CO 2, H 2 O, Methanol und Dimethylether (DME), die jeweils in der Gasphase auf Zeolith H-ZSM-5 in dem Temperatur- und Druckbereich von 50-150 ° C zu untersuchen und 0-18 bar sind. Die Ergebnisse zeigten, dass die Adsorptionsisothermen dieser Gase in H-ZSM-5 kann auch durch Langmuir-Typ-Adsorptionsisothermen ausgestattet werden. Darüber hinaus sind die ermittelten Parameter Adsorption, dh Adsorptionskapazitäten, Adsorptionsenthalpien und Adsorption Entropien, zu vergleichen und zu Literaturdaten. In dieser Arbeit werden die Ergebnisse für die CO 2 als ein Beispiel gezeigt.
Einleitung
Adsorption Eigenschaften beeinflussen stark die Leistung von katalytischen Materialien, damit eine genaue Kenntnis dieser Eigenschaften können bei der Charakterisierung, Design und Optimierung solcher Materialien unterstützen. Jedoch werden die Adsorptionseigenschaften von einkomponentigen Adsorptionsmessungen oft bei Raumtemperatur oder auch unter flüssigem Stickstoff Bedingungen im allgemeinen beurteilt, und somit eine Erweiterung der praktischen Situationen können zu einer starken Abweichung von der realen Verhalten führen. In situ Adsorptions - Messungen an katalytischen Materialien , insbesondere bei hoher Temperatur und hohem Druck, nach wie vor eine große Herausforderung.
Eine Adsorptions - Messvorrichtung auf einem Quarzkristall - Mikrowaage basiert (QCM) ist vorteilhaft gegenüber den kommerzialisierten volumetrische und gravimetrische Methoden in einer Weise , dass sie eine hochgenaue für die Massen Sorption Anwendungen zufriedenstellend stabil in einer kontrollierten Umgebung, und günstiger 1-2. However ist die herkömmliche QCM - Analyse auf Temperaturen unter 80 ° C 1-2 beschränkt. Um diese Einschränkung zu überwinden, entwickelten wir eine Adsorptions - Messvorrichtung basierend auf einer Hochtemperatur - Hochfrequenz - Oszillatormikrowaage (langatate Kristall - Mikrowaage, LCM) 3, die Adsorptionsmessungen prinzipiell bei Temperaturen so hoch wie 200-300 ° realisieren C aufgrund der Abwesenheit von kristallinen Phasenübergängen bis zu seinem Schmelzpunkt (1470 ° C) 4. Das LCMS in dieser Arbeit verwendet werden , haben eine AT-Schnitt ( das heißt, die Platte des Kristallmikrowaage enthält die x - Achse des Kristalls und wird von 35 ° 15 'von der z - Achse geneigt) und eine Resonanzfrequenz von 5 MHz. Dieses Gerät wurde den Adsorptions - Messungen von CO 2 aufgebracht, H 2 O, Methanol und Dimethylether (DME), die jeweils in gasförmigen Zustand auf Zeolith H-ZSM-5 in dem Temperaturbereich von 50-150 ° C und Druckbereich von 0-18 bar 3, am validati Zielauf der Simulationsmodelle für die Optimierung von bifunktionellen Kern-Schale - Katalysatoren zur einstufigen Herstellung von DME aus dem Synthesegas 5-6. Wie dieses Gerät für Gasadsorptionsmessungen zu betreiben ist im Protokollabschnitt dargestellt.
Vor den Adsorptionsmessungen, Zeolith H-ZSM-5 - Kristallite (0,502 mg) wurden durch die Dampfunterstützung Kristallisation (SAC) Verfahren nach de la Iglesia et al in der Mitte des LCM auf der Goldelektrode synthetisiert. 7, derart, dass die Zeolith-Kristallite auf dem oszillierenden Mikro befestigt bleiben. Wie in 1 gezeigt ist , verwendet das LCM in der Adsorptions - Messvorrichtung hat auf beiden Seiten polierte Goldelektroden, die das LCM mit einem Oszillator zu verbinden helfen. Da die Zeolithkristalle an den Verbindungspunkten der Goldelektroden an den Oszillator würde signifikant die elektrische Leitfähigkeit zu verringern (wie in Figur 1 angedeutet) und damit dieMeßempfindlichkeit des LCM wurden die Zeolith H-ZSM-5 - Kristallen auf dem LCM über das Verfahren SAC abgelagerten nicht abdeckt , diese Verbindungsstellen 3. Die Einzelheiten über die Synthese von Zeolith H-ZSM-5 auf LCM sind im Folgenden kurz zusammengefasst Protokollabschnitt und in dem Video-Protokoll im Detail gezeigt.
Protokoll
Achtung: Bitte konsultieren Sie alle relevanten Sicherheitsdatenblätter (MSDS) vor dem Gebrauch. Einige der Chemikalien, die in der Synthese von Zeolith H-ZSM-5 verwendet werden, sind akut giftig und krebserregend. Nanomaterialien können zusätzliche Risiken im Vergleich zu ihrer Masse Pendant. Bitte alle geeigneten Sicherheitspraktiken verwenden, wenn eine Reaktion Nanokristall einschließlich der Verwendung von technischen Kontrollen (Dunstabzug, Glovebox) und persönliche Schutzausrüstung durchführen (Schutzbrille, Handschuhe, Kittel, in voller Länge Hosen, geschlossene Schuhe). Außerdem achten Sie besonders, wenn die Adsorption Messungen mit Methanol und DME durchgeführt wird, da beide brennbare und explosive Gefahrstoffe.
1. Synthese von Zeolith H-ZSM-5 auf dem LCM
- Herstellung einer Zeolithsynthesemischung
Hinweis: Das endgültige Synthesemischung die folgende molare Zusammensetzung hatte wie adaptiert von de la Iglesia et al . 7: 1 SiO 2: 50 H 2 O: 0,07 Na 2 O: 0,024 TPA 2 O: 0,005 Al 2 O 3. Somit ist der theoretische Si / Al-Molverhältnis des synthetisierten Zeolith H-ZSM-5 100.- Man löst 0,14 g Natriumhydroxid in 20,30 g entionisiertem Wasser mittels Rühren. Alternativ mit 16,8 g deionisiertem Wasser 3,64 g 1 M NaOH gemischt.
- In 1,16 g Tetrapropylammoniumhydroxid (TPAOH) Lösung, und rühren Sie die Lösung, bis es klar erscheint.
- In 5,0 g Tetraethylorthosilikat (TEOS) Lösung tropft und rühren Sie die Lösung, bis es klar erscheint.
- Halten Rühren unter Zugabe von 0,09 g Aluminiumnitrat - Nonahydrat (Al (NO 3) 3 · 9H 2 O, fest) in die Lösung.
- Halten Sie das Rühren, bis der feste Aluminiumnitratnonahydrat gelöst ist. Beachten Sie, dass das hergestellte Zeolithsynthesemischung sollte aufgrund seiner Alterung innerhalb von 5 Stunden verwendet werden.
- Synthese von Zeolith ZSM-5 auf dem LCM über SAC 3
- Reinigen Sie das LCM vor der Zeolith - Synthese
- Waschen Sie die LCM gründlich mit dem de-ionisiertes Wasser.
- Setzen Sie das LCM in einem Becher mit dem de-ionisiertes Wasser, und reinigen Sie es in einem Ultraschallbad.
- Trocknen Sie die LCM bei 80 ° C in einem Ofen.
- Zeolith - Synthese
- Vorsichtig mehrere Tropfen des hergestellten Zeolithsynthesemischung auf der Elektrode in der Mitte des LCM wie in Figur 1 mit einer Pipette dargestellt, da nur der Zeolith auf der Goldelektrode abgeschieden kann die Resonanzfrequenzverschiebung des LCM 8 führen. Außerdem vermeiden an den Verbindungsstellen der Goldelektroden mit dem Oszillator der Synthesemischung ausbreitet, da der Zeolith auf den Verbindungspunkten signifikant die elektrische Leitfähigkeit verringern würde und damit die Meßempfindlichkeit des LCM. Zusätzlich Entfernen der Zeolithkristalle auf den Verbindungsstellen nach dem Deposition werden die Elektroden zerstören.
- Trocknen der LCM mit der Synthesemischung bei 80 ° C für 2 Stunden eine hochviskose gelartige Phase darauf zu erhalten.
- Eine kleine Menge von entionisiertem Wasser (ca. 10 ml) in einem mit Teflon ausgekleideten Autoklav (80 ml), um den Dampf während der Zeolithsynthese zu erzeugen.
- Setzen Sie den Teflon Halter in dem Autoklaven, die sich am Boden des Autoklaven während der Zeolithsynthese das LCM horizontal über dem flüssigen Wasser unterstützt.
- Halten des Autoklaven in einem Ofen bei 150 ° C für 48 Stunden den Zeolithen auf dem LCM über den SAC-Verfahren zu synthetisieren.
- Gleich nach dem SAC, waschen Sie die beschichteten LCM mit dem de-ionisiertes Wasser und trocknen bei 80 ° C für 2 Stunden.
- Entfernen des organischen Templats in den Zeolithkristallen durch Kalzinierung in einem Hochtemperaturofen unter einer oxidativen Atmosphäre. Programm der Ofen wie folgt: a) Erhöhen der Temperatur von Umgebungstemperatur bis 450 ° C mit einer Geschwindigkeit von 3 ° C min -1; b) Halten Sie diebei 450 ° C Temperatur für 4 h; c) Verringern der Temperatur von 450 ° C auf Raumtemperatur mit einer Geschwindigkeit von 3 ° C min -1.
- Man löst 26,75 g Ammoniumchlorid (NH 4 Cl, fest) in 0,4 l entionisiertem Wasser. Noch ein de-ionisiertem Wasser in der Lösung , so dass die endgültige NH 4 Cl - Lösung 0,5 L ist und die Konzentration von 1 mol dm -3 aufweist .
- Setzen Sie den beschichteten LCM in die NH 4 Cl - Lösung (0,2 L) in einem Becherglas und Ionenaustausch der Na-ZSM-5 - Kristallen auf dem LCM beschichtet bei 20 ° C für 2 Stunden. Wiederholen Sie den Ionenaustausch unter Verwendung von 0,2 L frisches NH 4 Cl - Lösung , die NH 4 -ZSM-5 - Kristalle zu erhalten.
- Besorgen Sie sich die H-ZSM-5 durch Endcalcinierung den gleichen Parametern wie in Schritt 1.2.2.7 erwähnt.
- Reinigen Sie das LCM vor der Zeolith - Synthese
2. Adsorption Messungen mit dem LCM-basierten Adsorptionsmessung Gerät 3
Hinweis: In dieser Arbeit wird die LCMohne Beschichtung und dem einen beschichtet mit H-ZSM-5 (im letzten Abschnitt) hergestellte "Referenz LCM" bezeichnet und "Probe LCM" bezeichnet. Außerdem wird die Probe vor LCM Zeolith deposition "LCM entladen Probe" bezeichnet. In einer früheren Veröffentlichung in Journal of Physical Chemistry C 3, eine detaillierte Beschreibung des LCM-basierten Absorptionsmessvorrichtung gefunden werden. In dieser Arbeit wird der Betrieb der Vorrichtung zur Gasadsorptionsmessungen in dieser kurzen Protokoll vorgestellt und in dem Video-Protokoll im Detail.
- Vorbereitung vor der Adsorption Messungen
- Tests über die Auswirkungen von Temperatur und Druck auf die Differenz in Resonanzfrequenzen des Referenz und entladen Probe LCMs
- Reinigen Sie den O-Ring, der LCM-Halter, und die Probenkammer mit Aceton und Druckluft.
- Setzen Sie die Referenz- und entladen Probe LCMs in einem Becher mit entionisiertem Wasser und reinigen Sie sie in einem ultrasound Bad.
- Legen Sie das saubere Referenz und entladen Probe LCMs auf dem LCM Halter, der mit dem Oszillator über hochtemperaturbeständige elektrische Leitungen verbunden ist.
- Vortest die installierten LCMs mit dem Oszillator, um sicherzustellen, dass die Resonanzfrequenzen erfolgreich erkannt werden können.
- Schließen der Probenkammer und Evakuieren es durch eine Vakuumpumpe.
- Ändern Sie den Druck in der Probenkammer über die Dosierung reines N 2.
- Kontrolle der Temperatur innerhalb der Probenkammer durch eine Temperatursteuerung.
- Messung der Resonanzfrequenzen des Referenz und entladen Probe LCMs in den untersuchten Temperatur- und Druckbereichen, dh 50-150 ° C und 0-16 bar, um die Wirkung von Temperatur und Druck auf die Differenz in Resonanzfrequenzen der zu wissen Referenz- und entladen Probe LCMs (
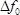 in Schritt 2.2.4). Die Tests zeigen, dass
in Schritt 2.2.4). Die Tests zeigen, dass  deutlich von der Temperatur (1200 bis 3000 Hz bei 50 bis 150 ° C) beeinflusst wird, während der Gasdruck hat keinen signifikanten Einfluss ( Änderung von
deutlich von der Temperatur (1200 bis 3000 Hz bei 50 bis 150 ° C) beeinflusst wird, während der Gasdruck hat keinen signifikanten Einfluss ( Änderung von 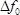 kleiner als 300 Hz im Druckbereich von 0 bis 16 bar). Verwenden Sie die ermittelten Werte von
kleiner als 300 Hz im Druckbereich von 0 bis 16 bar). Verwenden Sie die ermittelten Werte von 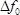 in der Gleichung Sauerbrey in Schritt 2.2.4 die adsorbierte Gasmenge auf dem Zeolith zu berechnen.
in der Gleichung Sauerbrey in Schritt 2.2.4 die adsorbierte Gasmenge auf dem Zeolith zu berechnen.
- Die Aktivierung der Probe LCM
- Reinigen Sie den O-Ring, der LCM-Halter, und die Probenkammer mit Aceton und Druckluft.
- Setzen Sie die Referenz LCM in einem Becher mit entionisiertem Wasser, und reinigen Sie es in einem Ultraschallbad.
- Legen Sie das saubere Referenz LCM und Proben LCM auf dem LCM Halter, der mit dem Oszillator über hochtemperaturbeständige elektrische Leitungen verbunden ist.
- Pretest die plaCED LCMs den Oszillator, dass die Resonanzfrequenzen, um sicherzustellen, indem erfolgreich erkannt werden können.
- Schließen der Probenkammer und Evakuieren es durch eine Vakuumpumpe.
- Aktivieren der Probe LCM bei hohen Temperaturen (mindestens 50 ° C höher als die Temperaturen der Adsorptions-Messungen, 200 ° C in dieser Arbeit) in Vakuumbedingungen über Nacht, um sicherzustellen, dass nur eine vernachlässigbare Gasmenge auf dem H-ZSM-5 adsorbiert .
- Tests über die Auswirkungen von Temperatur und Druck auf die Differenz in Resonanzfrequenzen des Referenz und entladen Probe LCMs
- Adsorptionsmessungen
Hinweis: In dieser Arbeit wurde die Adsorption Messung von CO 2 bei 50 ° C vorgelegt wird , ein Beispiel zu geben. Die erhaltenen Daten aus der Messung (beispielsweise Resonanzfrequenzen) und den berechneten Massen von adsorbierten CO 2 auf dem H-ZSM-5 kann 3 in Tabelle S1 des Grundinformationen unserer früheren Veröffentlichung.- Die Temperatur innerhalb der Probenkammer bei der gewünschten Temperatur des adsorpti auf Messungen (dh 50 ± 0,1 ° C) durch einen Temperaturregler, unter Vakuumbedingungen, das heißt, nur mit einer vernachlässigbaren Menge an adsorbiertem Gas.
- Schließen Sie den Oszillator auf die Probe LCM und messen seine Resonanzfrequenz durch die unterstützende Software des Oszillators über die Montage der experimentellen Daten mit einem Butterworth-Van Dyke Ersatzschaltungsmodell.
- Schaltet die Verbindung des Oszillators mit dem Referenz LCM und Messung seiner Resonanzfrequenz.
- Verwenden der gemessenen Resonanzfrequenzen der Proben- und Referenz LCMs unter Vakuumbedingungen , die Masse von H-ZSM-5 auf der Probe abgeschieden LCM zu bestimmen (ohne adsorbiertes Gas) entsprechend der Gleichung Sauerbrey 2, 8:
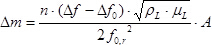
woher 413 / 54413eq4.jpg "/> ist der Unterschied in der Masse in g, bei dem die Anzahl der Harmonischen der Kristall (in dieser Studie angetrieben wird,
bei dem die Anzahl der Harmonischen der Kristall (in dieser Studie angetrieben wird, 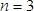 ),
), 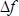 ist die Differenz der Resonanzfrequenzen des Referenz- und Proben LCMs in Hz,
ist die Differenz der Resonanzfrequenzen des Referenz- und Proben LCMs in Hz, 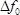 ist die Differenz der Resonanzfrequenzen zwischen der Referenz und entladen Probe LCM in Hz,
ist die Differenz der Resonanzfrequenzen zwischen der Referenz und entladen Probe LCM in Hz, 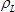 ist die Dichte des langatate Kristall (6,13 g cm -3) 4,
ist die Dichte des langatate Kristall (6,13 g cm -3) 4, 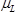 ist die effektive piezoelektrisch Schubmodul des langatate Kristall (1,9 × 10 12 g cm -1 sec -2) 4 versteift,/files/ftp_upload/54413/54413eq10.jpg "/> der Resonanzfrequenz des Referenz - LCM, das heißt der unbelasteten LCM,
ist die effektive piezoelektrisch Schubmodul des langatate Kristall (1,9 × 10 12 g cm -1 sec -2) 4 versteift,/files/ftp_upload/54413/54413eq10.jpg "/> der Resonanzfrequenz des Referenz - LCM, das heißt der unbelasteten LCM, 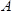 Der Bereich des LCM (1,539 cm 2) 3.
Der Bereich des LCM (1,539 cm 2) 3.
Hinweis: In dieser Arbeit wurde die Masse von H-ZSM-5 auf der Goldelektrode in der Mitte des LCM abgeschieden ist 0,502 mg, die bei 50 ° C eine Resonanzfrequenzverschiebung von 14.100 Hz verursacht. - Steuern den Gasdruck von CO 2 in der Probenkammer durch Dosierung Reingas aus dem Gaszylinder über einen Massendurchflussregler (für Methanol und DME, vom Verdampfer manuell über ein Dosierventil in die Kammer) oder durch Evakuierung durch eine Vakuumpumpe . Hier verwenden Sie einen Druckbereich von CO 2 Adsorption Messungen von 0-16 bar , wie in Abbildung 2 dargestellt.
- Warten , bis Gleichgewichtsbedingungen und eine stabile Temperatur erreicht, beispielsweise die Temperatur innerhalb von 50 ± 0.1 ° C variiert.
- Connect den Oszillator an die Probe LCM und Messung seiner Resonanzfrequenz nach Kontakt mit dem Gas bei einem gegebenen Druck.
- Schaltet die Verbindung des Oszillators mit dem Referenz LCM und Messung seiner Resonanzfrequenz unter den gleichen Bedingungen.
- Gemäß der Sauerbrey obigen Gleichung gezeigt ist, berechnen die Gesamtmasse an H-ZSM-5 auf der Probe LCM und Gas auf dem H-ZSM-5 unter diesem Gasdruck adsorbiert aufgebracht. Durch Subtraktion in Schritt bestimmt die Masse von H-ZSM-5 (ohne adsorbierte Gas) 2.2.4, die Masse an CO 2 adsorbiert auf dem H-ZSM-5 unter diesem Gasdruck erhalten wird .
- Wiederholen Sie die Resonanzfrequenzmessungen für Probe und Referenz LCMs für variierenden Drücken, um alle Massen von CO 2 zu erhalten , adsorbiert auf dem H-ZSM-5 - Probe unter verschiedenen Gasdrücken.
- Schließlich erhalten bei 50 ° C in der untersuchten Druckbereich von 0-16 bar über die Berechnung alle Massen von CO 2 adsorbiert das Gas Adsorptionsisothermeauf dem H-ZSM-5-Probe unter verschiedenen Gasdrücken nach 2.2.9 zu Schritt.
- Für Adsorptionsisothermen bei anderen Temperaturen, ändern Sie die stabile Temperatur den Temperaturregler verwenden, und wiederholen Sie die Schritte 2.2.1 bis 2.2.11.
- Montieren Sie die Adsorptionsisothermen mit Adsorptions - Modelle wie Langmuir - Modelle über die Methode der kleinsten Quadrate die Adsorption Parameter wie Adsorptionskapazitäten, Adsorptionsenthalpien zu bestimmen und Adsorption Entropien (siehe vorherige Veröffentlichung 3 und dessen Hintergrundinformationen).
Ergebnisse
Abbildung 1 zeigt die Fotografien, Lichtmikroskopie und Rasterelektronenmikroskopie (SEM) -Bilder des beschichteten und unbeschichteten LCM Sensor (links), sowie deren Röntgenbeugung (XRD) -Muster (rechts). Von beiden, Licht- und Rasterelektronenmikroskopie (1b und c), wobei die Verbindungspunkte der Goldelektroden an den Oszillator weniger mit Zeolithkristallen als der Mittelbereich des LCM bedeckt. Die meisten der Zeolithkristalle auf dem LCM-Sensor isoliert und zeigen charakteristische abgerundete Boot Morphologie, mit der (010) -Ebene nach oben überwiegend. Außerdem zeigen einige Kristalle zusätzlich das typische Verwachsung Verhalten ( "Zwillingskristalle"). Darüber hinaus hat die geladene H-ZSM-5 (Si / Al - Molverhältnis von 100 gemß der Zusammensetzung der Synthesemischung) auf dem langatate Kristall durch XRD und wellenlängendispersive Röntgen (WDX) -Spektroskopie 3 sucht.
In Figur 2, CO 2 Adsorptionsisothermen für die H-ZSM-5 - Zeolith mit dem LCM - Gerät in einem Temperaturbereich von 50-150 ° C und Druckbereich von 0-16 bar erhalten wurde , sowie der Sitz der einzelnen Standort Langmuir Isotherme Modell der experimentellen Daten sind ein repräsentatives Beispiel zu geben, gezeigt. Wie in Figur 2 gezeigt, wurden die ermittelten Adsorptionsisothermen von CO 2 auch mit einem einzigen Standort Langmuir - Isotherme ausgestattet. 3 zeigt das Diagramm von ln (K 'i) vs. 1,000 / T für CO 2 von der Adsorptionsisothermen abgeleitet, dh die Temperaturabhängigkeit der Absorptionskonstanten von der Passung der Adsorptionsisotherme bestimmt wird . Die Adsorptionsenthalpien und Entropien von CO 2 wurden durch Anpassung der van't Hoff - Gleichung bestimmt (die Hintergrundinformationen der früheren Veröffentlichung sehen3). Die Ergebnisse der Modellanpassung zeigen , daß die Adsorptionskapazität, Adsorption Enthalpie und Entropie Adsorption für CO 2 in H-ZSM-5 sind 4,0 ± 0,2 mmol g -1, 15,3 ± 0,5 kJ mol -1 und 56,3 ± 1,5 J mol -1 K -1, jeweils 3.
Die hohe Qualität der Anpassung der einzelnen Standort Langmuir - Isotherme und van't Hoff - Gleichung , wie in den 2 und 3 unterstützt die Annahme einer konstanten Adsorptionskapazität (dh Sättigungsbeladung) und der Enthalpie (dh Adsorptionswärme) an gültig verwendet zumindest für den Bereich von Bedingungen. Außerdem vergleicht die Adsorption Parameter CO 2 durch das LCM-basierten bestimmt Adsorption Meßvorrichtung in dieser Arbeit auch auf Werte in der Literatur berichtet , 9-12, das heißt die Adsorptionsfähigkeit, Adsorption Enthalpie und Entropie Adsorption reportet für CO 2 in MFI-Zeolithe variieren im Bereich von 2,1 bis 3,8 mmol g -1, 19 bis 28,7 kJ mol -1, und 43,7 bis 82,7 J mol -1 K -1, bzw. in dem Temperaturbereich von 30 -200 ° C und Druckbereich von 0 bis 5 bar.

Figure 1. Beschichtete langatate Kristall - Mikrosensor (links). (A) Die Fotos des beschichteten und unbeschichteten Sensor (rechts), (b) der Lichtmikroskopie und (c) rasterelektronenmikroskopische Aufnahmen. Die Röntgenbeugungsmuster von beschichteten und unbeschichteten LCM Sensor (rechts). Diese Zahl wurde bereits 3 aus einer früheren Veröffentlichung geändert. Nachdruck mit freundlicher Genehmigung der American Chemical Society ( Foto 2015). Bitte klicken Sie hier um ein , um zu vergrößern version von dieser Figur.
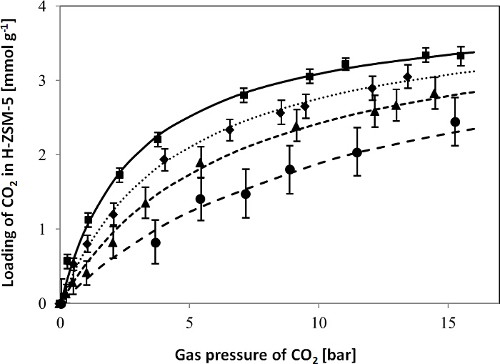
Abbildung 2. Adsorptionsisothermen für CO 2 in H-ZSM-5 bei 50 (  ), 75 (
), 75 (  ), 100 (
), 100 (  ) Und 150 ° C (
) Und 150 ° C (  ). Die Symbole stellen die experimentellen Daten zeigen die Fehlerbalken die Messunsicherheit der Resonanzfrequenzen verursacht werden , beispielsweise durch die Temperatur Instabilität und berechnet nach der Gleichung Sauerbrey wie in Schritt 2.2.4 beschrieben, und die Linien die fit der Single-Site Langmuir-Isotherme Modell an die experimentellen Daten. Diese Zahl has wurde von einer früheren Veröffentlichung 3 geändert. Nachdruck mit freundlicher Genehmigung der American Chemical Society ( Foto 2015). Bitte hier klicken , um eine größere Version dieser Figur zu sehen.
). Die Symbole stellen die experimentellen Daten zeigen die Fehlerbalken die Messunsicherheit der Resonanzfrequenzen verursacht werden , beispielsweise durch die Temperatur Instabilität und berechnet nach der Gleichung Sauerbrey wie in Schritt 2.2.4 beschrieben, und die Linien die fit der Single-Site Langmuir-Isotherme Modell an die experimentellen Daten. Diese Zahl has wurde von einer früheren Veröffentlichung 3 geändert. Nachdruck mit freundlicher Genehmigung der American Chemical Society ( Foto 2015). Bitte hier klicken , um eine größere Version dieser Figur zu sehen.
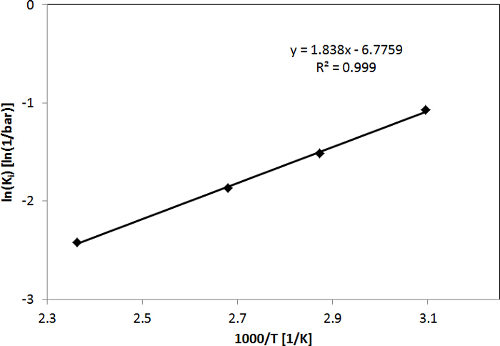
Abbildung 3. ln (K i) gegenüber 1000 / T Adsorptionsenthalpien und Entropien für CO 2 zu bestimmen. Diese Zahl wurde bereits 3 aus einer früheren Veröffentlichung geändert. Nachdruck mit freundlicher Genehmigung der American Chemical Society ( Foto 2015). Bitte hier klicken , um eine größere Version dieser Figur zu sehen.
Diskussion
In dieser Arbeit wird die erfolgreiche Synthese der Zeolith H-ZSM-5 - Kristallen auf der Goldelektrode in der Mitte des LCM Sensors durch SAC gezeigt, dh wird der Zeolith erfolgreich auf dem LCM - Sensor geladen , ohne dabei die Verbindungspunkte der Goldelektroden an den Oszillator. Somit kann der Zeolith oszilliert zusammen mit dem LCM-Sensor, während das LCM Sensor seine gute elektrische Leitfähigkeit und Meßempfindlichkeit hält. Im Vergleich zu den herkömmlichen QCM Vorrichtungen , die unter 80 ° C begrenzt werden, wird das LCM - Gerät in dieser Arbeit vorgestellten erfolgreich für die Adsorption Messungen so hoch wie 150 ° C, dh bei oder nahe der Temperatur von Reaktionen in der Industrie bei Temperaturen. Jedoch ist die vorliegende LCM Gerät unter 200 ° C begrenzt. Bei Temperaturen höher als 200 ° C kann die Messunsicherheit der Masse des adsorbierten Gases überschreiten, da mit zunehmender Temperatur oberhalb 150 ° C, um die Masse des AdsorBett Gas hat eine signifikante Abnahme, während die Messunsicherheit deutlich aufgrund der abnehmenden Temperaturregelgenauigkeit erhöht. So wird in zukünftigen Experimenten sollte ein neues Verfahren entwickelt werden, um mehr Zeolith auf dem LCM abzuscheiden, die mehr Gas zu adsorbieren verursacht, und kompensiert zudem die Wirkung der Temperatur und der Druck auf 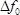 . Dies könnte dazu beitragen, das Anwendungsspektrum der LCM-Gerät auf höhere Temperaturen zu verlängern.
. Dies könnte dazu beitragen, das Anwendungsspektrum der LCM-Gerät auf höhere Temperaturen zu verlängern.
Während des Versuches sind die kritischsten Schritte in der Zeolithsynthese Schritte 1.2.2.1, 1.2.2.4, 1.2.2.5 und 1.2.2.7, während die in der Adsorptions-Messungen sind Schritte, 2.1.1.3, 2.1.1.4, 2.2.1, 2.2 0,5 und 2.2.6. In Schritt 1.2.2.1, nicht zu viel von der Synthesemischung auf dem LCM platzieren, die an den Verbindungsstellen der Goldelektroden ausbreiten würde. In Schritt 1.2.2.4, setzen Sie vorsichtig die Teflon-Halter mit dem LCM im Autoklaven, um sicherzustellen, dass die LCM ist horizontal und nicht in Kontakt mit der Flüssigkeit Wasser am Boden. In den Schritten 1.2.2.5 und 1.2.2.7, nicht über eine höhere Temperatur in der Zeolith-Synthese und der Kalzinierung verwendet werden, da unsere bisherigen Versuche zeigen, dass es zu einem Abbau des LCM führt. In der Adsorptions-Messungen hat die Position der LCM Sensoren eine erhebliche Auswirkung auf die Konnektivität der LCM-Sensoren mit dem Oszillator, und damit auf die Qualität der Resonanzfrequenzsignale. Daher besonderes Augenmerk auf die Schritte 2.1.1.3 und 2.1.1.4, in dem die LCMs auf dem Halter geladen werden und vorab getestet. Die LCM in der Lage sein sollte , dass sie mit dem Oszillator über den Anschlussstellen der Elektroden verbunden sind (dargestellt in Abbildung 1). Dies ist zwingend hohe Qualität Resonanzfrequenzsignale ermöglicht eine hohe Messgenauigkeit zu erzielen. Zusätzlich wird in den Schritten 2.2.1 und 2.2.6, sicherzustellen, dass eine stabile Temperatur vor den Messungen erreicht wird, da dies auch die Messung accu erhöhtrassig. Darüber hinaus wird in Schritt 2.2.5, führen Sie das Gas langsam, um im Inneren eine kleine Änderung der Temperatur zu haben. Dies hilft, die Temperatur stabil wird wieder nach einer kurzen Zeit.
Da die SAC-Syntheseverfahren für Zeolith H-ZSM-5 auf dem LCM Sensor könnte leicht auf andere Zeolithe erweitert werden, das LCM-basierte Adsorption Meßvorrichtung soll auch für sie verwendet werden sollen. Darüber hinaus aufgrund ihrer hohen Genauigkeit und niedrigen Kosten, ist dieses Gerät auf jedes Material anwendbar sein erwartet, die auf dem LCM überzogen werden könnte, um dessen Adsorptionseigenschaften bei hohen Temperaturen zu untersuchen.
Offenlegungen
The authors have nothing to disclose.
Danksagungen
This research has been funded by Deutsche Forschungsgemeinschaft (DFG) within the framework of the priority program 1570: porous media with defined pore system in process engineering - modeling, application, synthesis, under grant numbers DI 696/9-1 to -3 and SCHW 478/23-1 to -3.
Materialien
| Name | Company | Catalog Number | Comments |
| tetraethyl orthosilicate (TEOS), other name: tetraethoxysilane | Alfa Aesar | A14965 | purity > 98%, acutely toxic, inflammable and explosive |
| aluminum nitrate nonahydrate: Al(NO3)3•9H2O | Chempur | 000176 | purity > 98.5% |
| tetrapropylammonium hydroxide: (TPAOH) | Sigma-Aldrich | 254533 | 1 mol dm-3 aqueous solution, skin corrosive |
| sodium hydroxide: NaOH | Merck | 106498 | purity > 99%, skin corrosive |
| Ammonium chloride: NH4Cl | Merck | 101145 | purity > 99.8%, harmful |
| Carbon dioxide (CO2) | Air Liquide | --- | purity > 99.7% |
| high-pressure stainless steel chamber | Büchi AG, Uster, Switzerland | Midiclave | Volume = 300 ml, up to 200 bar, 300 °C |
| langatate crystal microbalance sensors | C3 Prozess- and Analysentechnik GmbH, Munich, Germany | --- | Diameter: 14 mm, resonant frequency: 5 MHz |
| high-frequency oscillating microbalance | Gamry Instruments, Warminster, USA | eQCM 10M | Frequency range: 1 MHz - 10 MHz (15 MHz), resolution: 20 mHz |
Referenzen
- Tsionsky, V., Gileadi, E. Use of the Quartz Crystal Microbalance for the Study of Adsorption from the Gas Phase. Langmuir. 10, 2830-2835 (1994).
- Venkatasubramanian, A., et al. Gas Adsorption Characteristics of Metal-Organic Frameworks via Quartz Crystal Microbalance Techniques. J. Phys. Chem. C. 116, 15313-15321 (2012).
- Ding, W., et al. Investigation of High-Temperature and High-Pressure Gas Adsorption in Zeolite H-ZSM-5 via Langatate Crystal Microbalance: CO2, H2O, Methanol and Dimethyl Ether. J. Phys. Chem. C. 119, 23478-23485 (2015).
- Davulis, P. M., Pereira da Cunha, M. High-Temperature Langatate Elastic Constants and Experimental Validation up to 900 °C. IEEE Trans Ultrason Ferroelectr Freq Control. 57, 59-65 (2010).
- Ding, W., Li, H., Pfeifer, P., Dittmeyer, R. Crystallite-Pore Network Model of Transport and Reaction of Multicomponent Gas Mixtures in Polycrystalline Microporous Media. Chem. Eng. J. 254, 545-558 (2014).
- Ding, W., et al. Simulation of One-Stage Dimethyl Ether Synthesis over Core/Shell Catalyst in Tube Reactor. Chem Ing Tech. 87, 702-712 (2015).
- de la Iglesia, O., et al. Preparation of Pt/ZSM-5 Films on Stainless Steel Microreactors. Catal. Today. 125, 2-10 (2007).
- Sauerbrey, G. Verwendung von Schwingquartzen zur Wägung dünner Schichten und zur Mikrowägung. Zeitschrift für Physik. 155, 206-222 (1959).
- Wirawan, S. K., Creaser, D. CO2 Adsorption on Silicalite-1 and Cation Exchanged ZSM-5 Zeolites Using a Step Change Response Method. Microporous Mesoporous Mater. 91, 196-205 (2006).
- Choudhary, V. R., Mayadevi, S. Adsorption of Methane, Ethane, Ethylene, and Carbon Dioxide on High Silica Pentasil Zeolites and Zeolite-like Materials Using Gas Chromatography Pulse Technique. Sep. Sci. Technol. 28, 2197-2209 (1993).
- Choudhary, V. R., Mayadevi, S. Adsorption of Methane, Ethane, Ethylene, and Carbon Dioxide on Silicalite-I. Zeolites. 17, 501-507 (1996).
- Zhu, W. D., Hrabanek, P., Gora, L., Kapteijn, F., Moulijn, J. A. Role of Adsorption in the Permeation of CH4 and CO2 through a Silicalite-1 Membrane. Ind. Eng. Chem. Res. 45, 767-776 (2006).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten