Method Article
Адсорбция устройство, основанное на лангатата Кристалл микровесов для высоких температур газа высокого давления адсорбции в цеолите H-ZSM-5
В этой статье
Резюме
A protocol for high-temperature and high-pressure gas adsorption measurements on zeolite H-ZSM-5 using an adsorption measurement device based on a langatate crystal microbalance is presented. Prior to the adsorption measurements, the synthesis of zeolite H-ZSM-5 on the langatate crystal microbalance sensor by the steam-assisted crystallization (SAC) method is demonstrated.
Аннотация
Мы представляем устройство высокого измерения температуры и адсорбции газа высокого давления на основе высокочастотного колеблющегося микровесов (5 МГц лангатата кристалл микровесов, LCM) и его использование для измерения адсорбции газа в цеолита H-ZSM-5. До начала измерения адсорбции, цеолит H-ZSM-5 кристаллы были синтезированы на золотом электроде в центре МДК, без покрытия точки соединения золотых электродов с генератором, с помощью способа паровой помощь кристаллизации (НКК), так что кристаллы цеолита остаются прикрепленными к колеблющимся микровесов, сохраняя при этом хорошую электропроводимость МДК во время измерения адсорбции. По сравнению с обычным кристалла кварца (QCM) , которое ограничено до температур ниже 80 ° C, МДК можно реализовать измерения адсорбции в принципе при температурах до 200-300 ° С (то есть, на уровне или близко к температуре реакции целевое применение одноступенчатыхСинтеза ДМЭ из синтез-газа), в связи с отсутствием кристаллического фазовых переходов вплоть до точки плавления (1470 ° C). Система была применена к исследованию адсорбции СО 2, H 2 O, метанол и диметиловый эфир (ДМЭ), каждый в газовой фазе, на цеолит H-ZSM-5 в температуре и давлении диапазоне 50-150 ° С и 0-18 бар, соответственно. Результаты показали, что изотермы адсорбции этих газов в H-ZSM-5 может быть хорошо обтянуты изотерм адсорбции Ленгмюра типа. Кроме того, определены параметры адсорбции, т.е. адсорбции мощности, адсорбции энтальпий и адсорбции энтропиями, сравните хорошо литературным данным. В этой работе, результаты для СО 2 приведены в качестве примера.
Введение
Адсорбционные свойства сильно влияют на эффективность каталитических материалов, следовательно, точное знание этих свойств может помочь в характеристике, проектирования и оптимизации таких материалов. Тем не менее, адсорбционные свойства , как правило , судить по однокомпонентных адсорбционных измерений часто при комнатной температуре или даже при температуре жидкого условиях азота, и , следовательно , расширение к практическим ситуациям может привести к серьезному отклонению от реального поведения. В натурные измерения адсорбции на каталитических материалов , особенно при высокой температуре и в условиях высокого давления, по-прежнему остаются большой проблемой.
Устройство измерения адсорбции на основании кристалла кварца (QCM) является более предпочтительным по сравнению коммерциализованной объемных и гравиметрических методов таким образом , что он является очень точным для применения в массовых сорбционными, удовлетворительно стабильными в контролируемой среде, и более доступным 1-2. HoweveR, обычный анализ QCM ограничен до температур ниже 80 ° C 1-2. Для того , чтобы преодолеть это ограничение, мы разработали устройство измерения адсорбции , основанный на высокотемпературном высокочастотной колебательный микровесов (лангатата кристалла микровесов, LCM) 3, которая может осуществить измерения адсорбции в принципе при температурах до 200-300 ° с, в связи с отсутствием кристаллического фазовых переходов вплоть до точки плавления (1470 ° C) 4. В МДК , используемые в этой работе имеют АТ-разрез (т.е., пластина из кристалла микровесов содержит ось х кристалла и наклонена на 35 ° 15 'от оси г) и резонансной частотой 5 МГц. Это устройство было применено для измерения адсорбции СО 2, H 2 O, метанол и диметиловый эфир (ДМЭ), каждый в газообразном состоянии, на цеолит H-ZSM-5 в интервале температур 50-150 ° С и давлений 0-18 бар 3, направленный на validatiна имитационных моделей для оптимизации бифункциональных катализаторов ядро-оболочка для производства одностадийного ДМЭ из синтез - газа 5-6. Как работать с этим устройством для измерения адсорбции газа представлен в разделе протокола.
До начала измерения адсорбции, цеолит Н-ZSM-5 кристаллиты (0,502 мг) синтезировали на золотом электроде в центре LCM паром при содействии кристаллизации методом (НКК) в соответствии с де ла Iglesia и др. , 7, в таким образом, что кристаллитов цеолита остаются прикрепленными к колеблющимся микровесов. Как показано на рисунке 1, LCM , используемый в устройстве для измерения адсорбции имеет полированные золотые электроды с обеих сторон, которые помогают соединить LCM к генератору. Так как кристаллы цеолита на точках соединения золотых электродов к генератору бы значительно уменьшить электропроводностью (как показано на рисунке 1) и , таким образом,измерение чувствительности LCM, цеолит H-ZSM-5 кристаллы осаждаются на LCM с помощью метода НКК , не покрывающая эти точки соединения 3. Подробности о синтезе цеолита H-ZSM-5 на LCM кратко изложены в разделе в соответствии с протоколом и показано в видео протоколе подробно.
протокол
Внимание: Пожалуйста, обратитесь все соответствующие паспорта безопасности материала (MSDS) перед использованием. Некоторые из химических веществ, используемых при синтезе цеолита H-ZSM-5 являются остро токсичными и канцерогенными. Наноматериалы могут иметь дополнительные риски по сравнению с их насыпной коллегой. Пожалуйста, используйте все надлежащие практики в области безопасности при проведении реакции нанокристаллической в том числе использование технических средств контроля (вытяжкой, GLOVEBOX) и средств индивидуальной защиты (защитные очки, перчатки, лабораторный халат, полная длина брюк, закрытые носок обуви). Кроме того, обратите особое внимание, когда, выполняя измерения адсорбции с метанолом и DME, поскольку оба являются легковоспламеняющиеся и взрывоопасные опасных материалов.
1. Синтез Цеолит H-ZSM-5 на LCM
- Приготовление синтеза цеолитов смеси
Примечание: Окончательный синтез смесь имела следующий молярный состав , как адаптировано из де ла Iglesia и др . 7: 1 SiO 2: 50 H 2 O: 0,07 Na 2 O: 0,024 TPA 2 O: 0,005 Al 2 O 3. Таким образом, теоретический Si / Al мольное отношение синтезированного цеолита H-ZSM-5 составляет 100.- Растворить 0,14 г гидроксида натрия в 20,30 г деионизированной воды с помощью перемешивания. В качестве альтернативы, смесь 3,64 г 1 М NaOH с 16,8 г деионизированной воды.
- Добавить 1,16 г гидроксида тетрапропиламмони раствора (ТПА), и перемешайте раствор до тех пор, пока не появится ясно.
- Добавить г раствора по каплям 5,0 тетраэтилортосиликат (ТУС) и перемешайте раствор до тех пор, пока не появится ясно.
- Продолжайте перемешивание, при добавлении 0,09 г нитрата алюминия нонагидрата (Al (NO 3) 3 · 9H 2 O, твердое тело) в раствор.
- Продолжайте размешивать, пока твердый нитрат алюминия нонагидрата не растворится. Обратите внимание, что приготовленный цеолит синтеза смесь следует использовать в течение 5 часов из-за его старения.
- Синтез цеолита ZSM-5 на LCM с помощью САК - 3
- Очистите LCM до синтеза цеолита
- Вымойте тщательно LCM с деионизованной водой.
- Поместите LCM в химический стакан с деионизованной водой, и очистить его в ультразвуковой ванне.
- Сушат LCM при 80 ° С в печи.
- синтез Цеолит
- Осторожно поместите несколько капель приготовленного синтеза цеолитов смеси на электроде в центре МДК , как показано на фиг.1 , с помощью пипетки, так как только цеолит , осажденный на золотом электроде может привести к резонансной частоте сдвиг LCM 8. Кроме того, во избежание распространения синтетической смеси на точках соединения золотых электродов к генератору, так как цеолит по точкам соединения значительно уменьшило бы электропроводностью и, таким образом, измерения чувствительности LCM. Кроме того, удаление кристаллов цеолита по точкам соединения после Depositioп разрушит электроды.
- Сушат МДК с синтетической смеси при 80 ° С в течение 2 часов для получения высоковязкого гелеобразную фазу на нем.
- Добавьте небольшое количество деионизированной воды (около 10 мл) в тефлоном автоклаве (80 мл) для получения водяного пара во время синтеза цеолита.
- Поместите держатель фторопластов в автоклаве, которое поддерживает LCM горизонтально над жидкой воды в нижней части автоклава в процессе синтеза цеолита.
- Хранить в автоклаве в печи при температуре 150 ° С в течение 48 ч, чтобы синтезировать цеолит на LCM с помощью метода САК.
- Сразу же после САК, промойте LCM, покрытую деионизованной водой и высушить при температуре 80 ° С в течение 2 ч.
- Удалить органическую матрицу, в кристаллы цеолита прокаливанием в высокотемпературной печи при окислительной атмосфере. Программа печи следующим образом : а) увеличение температуры от комнатной до 450 ° С со скоростью 3 ° С мин -1; б) ДержитеТемпература при 450 ° С в течение 4 ч; в) Уменьшение температуры от 450 ° C до комнатной температуры со скоростью 3 ° С мин -1.
- Растворить 26,75 г хлорида аммония (NH 4 Cl, в твердом состоянии ) в 0,4 л деионизированной воды. Добавить еще деионизованной водой в растворе , так что конечная раствора NH4Cl составляет 0,5 л и имеет концентрацию 1 моль дм -3.
- Поместите LCM покрытую в раствором NH4Cl (0,2 л) в химическом стакане, и ионообменная кристаллы Na-ZSM-5 с покрытием на LCM при 20 ° С в течение 2 часов. Повторите ионообменной с использованием 0,2 л свежего раствора NH 4 Cl , чтобы получить NH 4 -ZSM-5 кристаллов.
- Получение H-ZSM-5 с помощью окончательной кальцинации с использованием тех же самых параметров, как указано в шаге 1.2.2.7.
- Очистите LCM до синтеза цеолита
2. Измерения адсорбции Использование LCM на основе устройства Адсорбция измерения 3
Примечание: В данной работе МДКбез покрытия и с покрытием одной H-ZSM-5 (полученного в предыдущем разделе), называется "ссылочный LCM" и "образец LCM", соответственно. Кроме того, образец LCM перед нанесением цеолита, называется "разгружен образец LCM". В предыдущей публикации в журнале физической химии C 3, подробное описание LCM на основе устройства для измерения адсорбции можно найти. В этой работе, работа устройства для измерения адсорбции газа представлен в этом коротком протоколе и в видео-протоколе подробно.
- Подготовка к измерениям адсорбции
- Испытания по воздействию температуры и давления на разность резонансных частот опорного и выгружается образец МДК
- Очистите уплотнительное кольцо, держатель LCM, и камеру образца с ацетоном и сжатым воздухом.
- Поместите опорные и выгружается образцы LCMS в стакане с деионизированной водой и очистить их в улtrasound ванна.
- Аккуратно положите чистую ссылку и выгружается образца ЖХ на держателе LCM, который соединен с генератором через термостойкие электрических кабелей.
- Претест установленные LCMS, используя генератор, чтобы гарантировать, что резонансные частоты могут быть обнаружены успешно.
- Закройте камеру для образца, и эвакуировать его с помощью вакуумного насоса.
- Изменение давления в камере для образца с помощью дозирующего чистого N 2.
- Контроль температуры внутри камеры для образца при помощи регулятора температуры.
- Измерьте резонансные частоты обращения и выгружается образца LCMS в исследуемом диапазоне температур и давлений, т.е. 50-150 ° С и 0-16 бар, чтобы знать , влияние температуры и давления на разнице резонансных частот справка и разгруженные образец МДК (
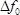 на этапе 2.2.4). Испытания показали, что
на этапе 2.2.4). Испытания показали, что  в значительной степени зависит от температуры (от 1200 до 3000 Гц при 50-150 ° С), в то время как давление газа не оказывает существенного влияния ( изменение
в значительной степени зависит от температуры (от 1200 до 3000 Гц при 50-150 ° С), в то время как давление газа не оказывает существенного влияния ( изменение 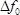 меньше, чем 300 Гц в диапазоне давлений 0-16 бар). Используйте определенные значения
меньше, чем 300 Гц в диапазоне давлений 0-16 бар). Используйте определенные значения 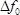 в уравнении Sauerbrey на шаге 2.2.4 для расчета адсорбированного количества газов на цеолите.
в уравнении Sauerbrey на шаге 2.2.4 для расчета адсорбированного количества газов на цеолите.
- Активация образца LCM
- Очистите уплотнительное кольцо, держатель LCM, и камеру образца с ацетоном и сжатым воздухом.
- Поместите эталонный LCM в химическом стакане деионизированной водой, и очистить его в ультразвуковой ванне.
- Аккуратно положите чистую эталонный образец и LCM LCM на держателе LCM, который соединен с генератором через термостойкие электрических кабелей.
- Претест НОАКCED МДК с использованием генератора, чтобы убедиться, что резонансные частоты могут быть обнаружены успешно.
- Закройте камеру для образца, и эвакуировать его с помощью вакуумного насоса.
- Активация образца LCM при высоких температурах (по меньшей мере, 50 ° С выше, чем температура измерений адсорбции, 200 ° C в этой работе) в условиях вакуума в течение ночи, чтобы гарантировать, что только незначительное количество газа, адсорбированного на H-ZSM-5 ,
- Испытания по воздействию температуры и давления на разность резонансных частот опорного и выгружается образец МДК
- Адсорбционные измерения
Примечание: В данной работе, измерение адсорбции СО 2 при 50 ° С представлена привести пример. Полученные данные измерения (например, резонансные частоты) и вычисленных масс адсорбированного СО 2 на H-ZSM-5 можно найти в таблице S1 несущего информацию о нашей предыдущей публикации 3.- Доведите температуру внутри камеры для образца при требуемой температуре adsorpti на измерениях (т.е. 50 ± 0,1 ° С) при помощи регулятора температуры, в условиях вакуума, то есть, только с незначительным количеством адсорбированного газа.
- Подключите генератор к образцу LCM, и измерить его резонансной частоты с помощью программного обеспечения, поддерживающего осциллятора с помощью подгонки экспериментальных данных с моделью эквивалентной схеме Баттерворта-Van Dyke.
- Включите подключение генератора к опорному LCM, и измерить его резонансную частоту.
- С помощью измерения резонансной частоты образца и эталонных LCMS в условиях вакуума для определения массы H-ZSM-5 , осажденный на образце LCM (без адсорбированного газа) в соответствии с уравнением Sauerbrey 2, 8:
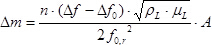
где 413 / 54413eq4.jpg "/> разница в массе в граммах, это номер гармоники, на которой приводится кристалл (в данном исследовании,
это номер гармоники, на которой приводится кристалл (в данном исследовании, 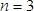 ),
), 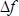 разница в резонансных частот эталонных образцов и LCMS в Гц,
разница в резонансных частот эталонных образцов и LCMS в Гц, 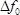 есть разность резонансных частот между опорным и выгружается образца LCM в Гц,
есть разность резонансных частот между опорным и выгружается образца LCM в Гц, 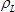 плотность кристалла лангатата (6,13 г см -3) 4,
плотность кристалла лангатата (6,13 г см -3) 4, 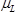 является эффективным пьезоэлектрическим напрягся модуль сдвига лангатата кристалла (1,9 × 10 12 г см -1 сек -2) 4,/files/ftp_upload/54413/54413eq10.jpg "/> является резонансная частота опорного LCM, т.е. выгружается LCM,
является эффективным пьезоэлектрическим напрягся модуль сдвига лангатата кристалла (1,9 × 10 12 г см -1 сек -2) 4,/files/ftp_upload/54413/54413eq10.jpg "/> является резонансная частота опорного LCM, т.е. выгружается LCM, 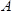 , Площадь LCM (1,539 см 2) 3.
, Площадь LCM (1,539 см 2) 3.
Примечание: В данной работе, масса H-ZSM-5, осажденный на золотом электроде в центре LCM является 0,502 мг, что вызывает резонансный сдвиг частоты 14100 Гц при 50 ° C. - Контроль давления газа СО 2 внутри камеры для образца с помощью дозирующего чистого газа из газового баллона через регулятор массового расхода (для метанола и простого диметилового эфира, от испарителя вручную через дозирующий клапан в камеру), или путем откачки через вакуумный насос , Здесь используется диапазон давления СО 2 адсорбционных измерений 0-16 бар , как показано на рисунке 2.
- Подождите , пока условия равновесия и стабильная температура не была достигнута, например, температура колеблется в пределах 50 ± 0,1 ° С.
- Колорадоnnect осциллятора к образцу LCM, и измерения его резонансной частоты после воздействия газа при заданном давлении.
- Включите подключение генератора к опорному LCM, и измерить его резонансной частоты при тех же условиях.
- В соответствии с уравнением Sauerbrey, показанной выше, рассчитать общую массу H-ZSM-5, осажденный на LCM образца и газа, адсорбированного на H-ZSM-5, при этом давление газа. Путем вычитания массы Н-ZSM-5 (без адсорбированного газа) , определенный на этапе 2.2.4, масса СО 2 , адсорбированного на H-ZSM-5 , при этом давление газа получается.
- Повторите резонансные измерения частоты для образца и эталонных LCMS для различного давления, для того , чтобы получить все массы СО 2 , адсорбированных на образце Н-ZSM-5 при различных давлениях газа.
- И, наконец, получить изотерму адсорбции газа при 50 ° С в исследуемом диапазоне давлений 0-16 бар с помощью вычисления всех массы СО 2 , адсорбированногона образце Н-ZSM-5 при различных давлениях газа в соответствии со стадией 2.2.9.
- Для получения изотерм адсорбции при других температурах, изменить стабильную температуру с помощью регулятора температуры, и повторите шаги 2.2.1 2.2.11.
- Установить изотермы адсорбции при адсорбции моделей , таких как модели Ленгмюра с помощью метода наименьших квадратов для определения параметров адсорбции , как адсорбции мощностей, адсорбции энтальпий и энтропий адсорбции (см предыдущую публикацию 3 и подтверждающей его информации).
Результаты
На рисунке 1 показаны фотографии, световой микроскопии и сканирующей электронной микроскопии (SEM) изображения на мелованной и немелованной датчика LCM (слева), а также их дифракции рентгеновских лучей (ДРЛ) модели (справа). Из обоих, световой и сканирующей электронной микроскопии (рис 1b и С), соединительные точки золотыми электродами на генератор менее покрыты кристаллов цеолита по сравнению с центром области LCM. Большинство кристаллов цеолита на вершине LCM-датчика изолированы и показывают характерную морфологию округло-лодка, с (010) -плоскость преимущественно лицевой стороной вверх. Кроме того, некоторые кристаллы дополнительно показывают типичное поведение сросшуюся ( "двойниковых кристаллов"). Кроме того, загруженная H-ZSM-5 (молярное отношение Si / Al от 100 в зависимости от состава смеси для синтеза) на кристалле лангатата было исследовано методом РСА и по длине волны рентгеновской (WDX) спектроскопии 3,
На рисунке 2, CO 2 Изотермы адсорбции цеолита H-ZSM-5 , полученный с LCM устройством в интервале температур 50-150 ° С и диапазоне давлений 0-16 бар, а также подгонке одного сайта Ленгмюра изотермы модели к экспериментальным данным, приведены, чтобы дать типичный пример. Как показано на рисунке 2, определены изотермы адсорбции СО 2 были оснащены одной площадке Ленгмюра изотермы скважины. На рисунке 3 показана схема LN (I K ') по сравнению с 1000 / T для CO 2, полученные из изотерм адсорбции, т.е. температурная зависимость констант адсорбции определяется из подгонки изотерм адсорбции. Адсорбционные энтальпиями и энтропиями CO 2 определяли путем подгонки с уравнением Вант - Гоффа (см Вспомогательная информация о предыдущей публикации3). Результаты подгонки модели показывают , что поглощающая способность, адсорбции энтальпии и энтропии адсорбции для СО 2 в H-ZSM-5 4,0 ± 0,2 ммоль г -1, 15,3 ± 0,5 кДж моль -1 и 56,3 ± 1,5 Дж моль -1 K -1, соответственно 3.
Высокое качество подгонки одного сайта Ленгмюра изотермы и уравнение Вант - Гоффа , как показано на рисунках 2 и 3 поддерживает предположение о способности постоянной адсорбции (т.е. насыщения нагрузки) и энтальпия (т.е. теплота адсорбции) , чтобы быть действительным по крайней мере в диапазоне условий, используемых. Кроме того, параметры адсорбции СО 2 , определенные LCM на основе устройства для измерения адсорбции в этой работе хорошо сопоставимы со значениями , описанными в литературе 9-12, то есть, адсорбционная способность, адсорбция энтальпия и энтропия адсорбции репоrted для CO 2 в цеолитах MFI-типа варьируются в диапазоне 2.1-3.8 ммоль г -1, 19-28.7 кДж моль - 1, и 43.7-82.7 Дж моль -1 К -1 соответственно, в интервале температур от 30 -200 ° C и диапазон давлений 0-5 бар.

Рисунок 1. Покрытый лангатата датчик микровесов кристалла (слева). (А) фотографии с покрытием и без датчика (справа), (б) световой микроскопии и (с) с помощью сканирующей электронной микроскопии изображений. Рентгеновские дифрактограммы мелованной и немелованной датчика LCM (справа). Эта цифра была изменена с предыдущей публикации 3. Печатается с разрешения Американского химического общества (Авторское право 2015). Пожалуйста , нажмите здесь , чтобы увидеть увеличенную верSion этой фигуры.
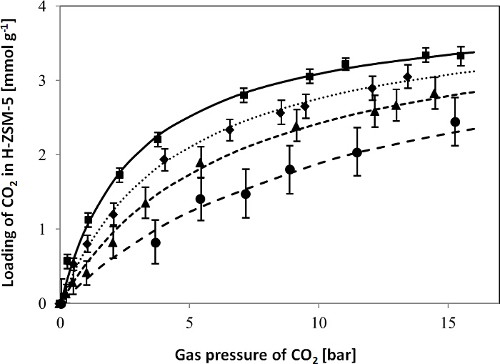
Рисунок 2. Изотермы адсорбции CO 2 в H-ZSM-5 при 50 (  ), 75 (
), 75 (  ), 100 (
), 100 (  ), И 150 ° С (
), И 150 ° С (  ). Символы представляют экспериментальные данные, планки погрешностей указывают на погрешность измерения резонансных частот , вызванные, например, нестабильность температуры, и рассчитывается в соответствии с уравнением Sauerbrey , как описано в шаге 2.2.4, а линии представляют подгонку из одного сайта Ленгмюра изотермы модели с экспериментальными данными. Эта цифра гаы были изменены из предыдущей публикации 3. Печатается с разрешения Американского химического общества (Авторское право 2015). Пожалуйста , нажмите здесь , чтобы посмотреть увеличенную версию этой фигуры.
). Символы представляют экспериментальные данные, планки погрешностей указывают на погрешность измерения резонансных частот , вызванные, например, нестабильность температуры, и рассчитывается в соответствии с уравнением Sauerbrey , как описано в шаге 2.2.4, а линии представляют подгонку из одного сайта Ленгмюра изотермы модели с экспериментальными данными. Эта цифра гаы были изменены из предыдущей публикации 3. Печатается с разрешения Американского химического общества (Авторское право 2015). Пожалуйста , нажмите здесь , чтобы посмотреть увеличенную версию этой фигуры.
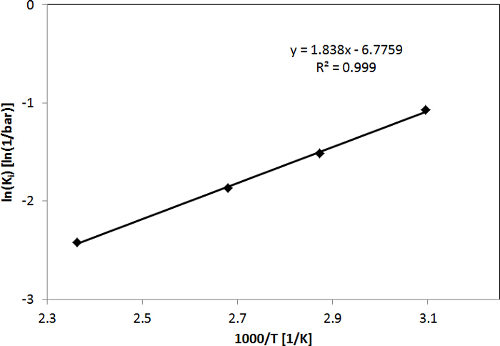
Рисунок 3. п (K I) по сравнению с 1000 / T для определения адсорбции энтальпии и энтропии для CO 2. Эта цифра была изменена с предыдущей публикации 3. Печатается с разрешения Американского химического общества (Авторское право 2015). Пожалуйста , нажмите здесь , чтобы посмотреть увеличенную версию этой фигуры.
Обсуждение
В этой работе, успешный синтез цеолита H-ZSM-5 кристаллов на золотом электроде в центре датчика LCM ККД демонстрируется, т.е. цеолит успешно загружен на датчике LCM без покрытия точек подключения золотые электроды к генератору. Таким образом, цеолит может колебаться вместе с датчиком LCM, в то время как датчик LCM сохраняет хорошую электропроводность и чувствительность измерения. По сравнению с обычными устройствами QCM , которые ограничены ниже 80 ° C, МДК устройство представлено в этой работе успешно применяется для измерения адсорбции при температурах до 150 ° С, то есть на уровне или близко к температуре реакции в промышленности. Тем не менее, настоящее LCM устройство ограничено ниже 200 ° C. При температурах выше 200 ° C, погрешность измерения может превышать массу адсорбированного газа, так как при повышении температуры выше 150 ° С, массу adsorкровать газ имеет значительное снижение, в то время как погрешность измерения значительно увеличивается за счет уменьшения точности контроля температуры. Таким образом, в будущих экспериментах, новый метод должен быть разработан, чтобы внести больше цеолита в расчете на МДК, что вызывает больше газа адсорбировать, и к тому же компенсирует влияние температуры и давления на 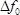 , Это могло бы помочь расширить диапазон применения LCM устройства до более высоких температур.
, Это могло бы помочь расширить диапазон применения LCM устройства до более высоких температур.
В ходе эксперимента, критические стадии синтеза цеолита Ступени 1.2.2.1, 1.2.2.4, 1.2.2.5 и 1.2.2.7, а те, в адсорбционных измерений являются шагами 2.1.1.3, 2.1.1.4, 2.2.1, 2.2 0,5 и 2.2.6. На шаге 1.2.2.1, избегать размещения слишком много смеси для синтеза на LCM, которая будет распространяться на точках соединения золотых электродов. На шаге 1.2.2.4, осторожно установите держатель тефлоновую с LCM в автоклаве, чтобы гарантировать, что МДК является чorizontal и не контактирует с жидкой водой на дне. На этапах 1.2.2.5 и 1.2.2.7, не следует использовать более высокую температуру в синтезе цеолита и прокаливания, так как наши предыдущие эксперименты показывают, что это приводит к деградации LCM. В измерения адсорбции, положение датчиков LCM оказывает существенное влияние на возможности подключения датчиков LCM к генератору, и, следовательно, на качество резонансных частотных сигналов. Поэтому, обратить особое внимание на шаги 2.1.1.3 и 2.1.1.4, в котором будут загружены МДК на держателе и апробировать. В МДК должны находиться в положении , что они связаны с генератором через точки подключения электродов (показано на рисунке 1). Это обязательное условие для получения высокого качества сигналов резонансной частоты обеспечивает высокую точность измерений. Кроме того, на этапах 2.2.1 и 2.2.6, убедитесь, что стабильная температура достигается перед измерениями, так как это также увеличивает Акку измеренияколоритный. Кроме того, на шаге 2.2.5, подавать газ медленно, чтобы иметь небольшое изменение температуры внутри. Это помогает температура стать стабильным снова через короткий промежуток времени.
Поскольку метод синтеза САК для цеолита H-ZSM-5 на датчике LCM может быть распространен на другие цеолиты легко, устройство измерения адсорбции LCM на основе, как ожидается, будет использоваться для них. К тому же, из-за своей высокой точностью и низкой стоимостью, это устройство, как ожидается, будет применимо к любому материалу, который может быть нанесен на LCM, для того, чтобы исследовать его адсорбционные свойства при высоких температурах.
Раскрытие информации
The authors have nothing to disclose.
Благодарности
This research has been funded by Deutsche Forschungsgemeinschaft (DFG) within the framework of the priority program 1570: porous media with defined pore system in process engineering - modeling, application, synthesis, under grant numbers DI 696/9-1 to -3 and SCHW 478/23-1 to -3.
Материалы
| Name | Company | Catalog Number | Comments |
| tetraethyl orthosilicate (TEOS), other name: tetraethoxysilane | Alfa Aesar | A14965 | purity > 98%, acutely toxic, inflammable and explosive |
| aluminum nitrate nonahydrate: Al(NO3)3•9H2O | Chempur | 000176 | purity > 98.5% |
| tetrapropylammonium hydroxide: (TPAOH) | Sigma-Aldrich | 254533 | 1 mol dm-3 aqueous solution, skin corrosive |
| sodium hydroxide: NaOH | Merck | 106498 | purity > 99%, skin corrosive |
| Ammonium chloride: NH4Cl | Merck | 101145 | purity > 99.8%, harmful |
| Carbon dioxide (CO2) | Air Liquide | --- | purity > 99.7% |
| high-pressure stainless steel chamber | Büchi AG, Uster, Switzerland | Midiclave | Volume = 300 ml, up to 200 bar, 300 °C |
| langatate crystal microbalance sensors | C3 Prozess- and Analysentechnik GmbH, Munich, Germany | --- | Diameter: 14 mm, resonant frequency: 5 MHz |
| high-frequency oscillating microbalance | Gamry Instruments, Warminster, USA | eQCM 10M | Frequency range: 1 MHz - 10 MHz (15 MHz), resolution: 20 mHz |
Ссылки
- Tsionsky, V., Gileadi, E. Use of the Quartz Crystal Microbalance for the Study of Adsorption from the Gas Phase. Langmuir. 10, 2830-2835 (1994).
- Venkatasubramanian, A., et al. Gas Adsorption Characteristics of Metal-Organic Frameworks via Quartz Crystal Microbalance Techniques. J. Phys. Chem. C. 116, 15313-15321 (2012).
- Ding, W., et al. Investigation of High-Temperature and High-Pressure Gas Adsorption in Zeolite H-ZSM-5 via Langatate Crystal Microbalance: CO2, H2O, Methanol and Dimethyl Ether. J. Phys. Chem. C. 119, 23478-23485 (2015).
- Davulis, P. M., Pereira da Cunha, M. High-Temperature Langatate Elastic Constants and Experimental Validation up to 900 °C. IEEE Trans Ultrason Ferroelectr Freq Control. 57, 59-65 (2010).
- Ding, W., Li, H., Pfeifer, P., Dittmeyer, R. Crystallite-Pore Network Model of Transport and Reaction of Multicomponent Gas Mixtures in Polycrystalline Microporous Media. Chem. Eng. J. 254, 545-558 (2014).
- Ding, W., et al. Simulation of One-Stage Dimethyl Ether Synthesis over Core/Shell Catalyst in Tube Reactor. Chem Ing Tech. 87, 702-712 (2015).
- de la Iglesia, O., et al. Preparation of Pt/ZSM-5 Films on Stainless Steel Microreactors. Catal. Today. 125, 2-10 (2007).
- Sauerbrey, G. Verwendung von Schwingquartzen zur Wägung dünner Schichten und zur Mikrowägung. Zeitschrift für Physik. 155, 206-222 (1959).
- Wirawan, S. K., Creaser, D. CO2 Adsorption on Silicalite-1 and Cation Exchanged ZSM-5 Zeolites Using a Step Change Response Method. Microporous Mesoporous Mater. 91, 196-205 (2006).
- Choudhary, V. R., Mayadevi, S. Adsorption of Methane, Ethane, Ethylene, and Carbon Dioxide on High Silica Pentasil Zeolites and Zeolite-like Materials Using Gas Chromatography Pulse Technique. Sep. Sci. Technol. 28, 2197-2209 (1993).
- Choudhary, V. R., Mayadevi, S. Adsorption of Methane, Ethane, Ethylene, and Carbon Dioxide on Silicalite-I. Zeolites. 17, 501-507 (1996).
- Zhu, W. D., Hrabanek, P., Gora, L., Kapteijn, F., Moulijn, J. A. Role of Adsorption in the Permeation of CH4 and CO2 through a Silicalite-1 Membrane. Ind. Eng. Chem. Res. 45, 767-776 (2006).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены