Method Article
Untersuchung der elektrophysiologischen und thermographischen Sicherheitsparameter von chirurgischen Energiegeräten während der Schilddrüsen- und Nebenschilddrüsenchirurgie im Schweinemodell
In diesem Artikel
Zusammenfassung
Die sichere Anwendung neu entwickelter chirurgischer Energiegeräte in der Schilddrüsen-/Nebenschilddrüsenchirurgie zieht die Aufmerksamkeit der Chirurgen auf sich. Tierexperimentelle Modelle können unnötige Versuche und Irrtümer in der Humanchirurgie vermeiden. Ziel dieses Berichts ist es, elektrophysiologische und thermographische Methoden zur Bewertung der Sicherheitsparameter von SEDs in der Schilddrüsen-/Nebenschilddrüsenchirurgie zu demonstrieren.
Zusammenfassung
In der Schilddrüsen- und Nebenschilddrüsenchirurgie bieten chirurgische Energiegeräte (SEDs) eine effizientere Hämostase als die herkömmliche Clamp-and-Tie-Hämostase in Bereichen mit reicher Blutversorgung. Wenn jedoch ein SED in der Nähe des Nervus laryngeus recurrens (RLN) aktiviert wird, kann die vom SED erzeugte Hitze den Nerv irreversibel verletzen. Um SEDs sicher in der Schilddrüsen-/Nebenschilddrüsenchirurgie anzuwenden, werden in diesem Artikel experimentelle Schweinemodellstudien vorgestellt, um die Aktivierungs- und Kühlsicherheitsparameter von SEDs in standardisierten elektrophysiologischen (EP) bzw. thermografischen (TG) Verfahren zu untersuchen. In den EP-Sicherheitsparameter-Experimenten wird kontinuierliches intraoperatives Neuromonitoring (C-IONM) angewendet, um die RRN-Funktion in Echtzeit zu demonstrieren. Die EP-Aktivierungsstudie bewertet den sicheren Aktivierungsabstand von SEDs; Die EP-Kühlstudie bewertet die sichere Abkühlzeit von SEDs. Im TG-Sicherheitsparameter-Experiment wird eine Wärmebildkamera verwendet, um die Temperaturänderung nach Aktivierung des SED aufzuzeichnen. Die TG-Aktivierungsstudie bewertet die laterale thermische Ausbreitungsdistanz nach SED-Aktivierung in einer trockenen oder feuchten Umgebung und ob Rauch und Spritzer erzeugt werden. Die TG-Kühlstudie bewertet die Abkühlzeit. Dies wird dazu beitragen, die Sicherheitsparameter neu entwickelter SEDs zu ermitteln, die in der Schilddrüsen-/Nebenschilddrüsenchirurgie eingesetzt werden, und Sicherheitsrichtlinien zur Vermeidung von RRN-Verletzungen und damit verbundenen Komplikationen bereitzustellen.
Einleitung
Eine effiziente Blutstillung ist ein sehr wichtiges Thema in der Schilddrüsen- und Nebenschilddrüsenchirurgie. In den letzten Jahrzehnten war einer der größten Fortschritte in der Schilddrüsen- und Nebenschilddrüsenchirurgie die Entwicklung von chirurgischen Energiegeräten (SEDs)1. SEDs bieten eine effizientere Hämostase als die herkömmliche Clamp-and-Tie-Technik in Bereichen mit reicher Blutversorgung, was den intraoperativen Blutverlust und die Operationszeit2, die postoperative Hypokalzämie3 und das lebensbedrohliche postoperative Hämatom4 reduziert. In neueren Studien wird berichtet, dass SEDs bei 65,7 % der Thyreoidektomie-Patienten eingesetzt werden5, und die jährliche Anwendung von SED nimmt jedes Jahr zu.
SEDs haben sich jedoch nicht als überlegen gegenüber konventionellen Techniken in Bezug auf rezidivierende Larynxnervverletzungen (RLN) bei Schilddrüsen- und Nebenschilddrüsenoperationen erwiesen 4,6,7. Thermische Verletzungen und laterale thermische Ausbreitung auf das RLN treten oft unerwartet auf, wenn ein SED in der Nähe des Nervs aktiviert wird, und diese Art von Verletzung ist in der Regel schwerwiegend und irreversibel. Im Vergleich zu einer mechanischen Zug- oder Kompressionsnervenverletzung weist die thermische Nervenverletzung eine geringere Verzerrung der äußeren Struktur auf, aber eine stärkere Schädigung des inneren Endoneuriums, einschließlich der Myelinscheide und des Axons 8,9,10,11. Diese Art von Verletzung hat nicht nur Schwierigkeiten bei der Wiedererlangung der normalen Funktion, sondern ist auch in der klinischen Sequenz weniger reversibel als eine Traktionsverletzung10,12. Darüber hinaus sind thermische Verletzungen für den Chirurgen oft unsichtbar und können im Verlauf der Operation nicht erkannt werden13,14. Daher sollten Chirurgen die thermischen Auswirkungen von SED berücksichtigen, um eine thermische Schädigung der RLN während einer Schilddrüsen- und Nebenschilddrüsenoperation zu vermeiden.
Schweinemodelle werden am häufigsten für die RRN-Forschung verwendet, da die Anatomie und Physiologie von Schweinen denen des Menschen sehr ähnlich sind 15,16,17,18,19,20. Das experimentelle Schweinemodell ermöglicht eine einfache Handhabung, ist weit verbreitet und kostengünstig9. Für elektrophysiologische (EP) Informationen ist das intraoperative Neuromonitoring (IONM) hilfreich, um Mechanismen der Nervenverletzung zu erkennen und die postoperative Stimmbandfunktion vorherzusagen 21,22,23,24,25,26,27. Darüber hinaus ermöglicht die kontinuierliche IONM (CIONM) die Früherkennung von Nervenverletzungen nach risikoreichen Eingriffen, da sie durch wiederholte vagale Stimulation eine sofortige Rückmeldung für die Nervenfunktion geben kann28,29,30. Untersuchungen zur EP-Aktivierung und -Kühlung können den sicheren SED-Aktivierungsabstand vom RLN und die sichere Abkühlzeit nach SED-Aktivierung bestimmen, bevor das RLN kontaktiert wird. Für thermografische Informationen ist eine Wärmebildkamera hilfreich, um die Temperaturänderung (Aktivierung und Abkühlung) auszuwerten, und der hyperthermische Bereich kann nach SED-Aktivierungen visualisiert werden 31,32,33,34,35. In einer früheren Studie trat eine thermische Schädigung des RLN auf, wenn die Gewebetemperatur die kritische Temperatur von 60 °C im porcinen CIONM-Modell36 erreichte. Untersuchungen zur TG-Aktivierung und -Kühlung können die laterale thermische Ausbreitungsstrecke, das Auftreten von Rauch und Spritzern sowie die Temperaturänderung während der Kühlung mit oder ohne Muskelberührungsmanöver (MTM) bestimmen. Um SED sicher in der Schilddrüsen-/Nebenschilddrüsenchirurgie anzuwenden, wird in diesem Artikel eine experimentelle Schweinemodellstudie vorgestellt, um die EP- und TG-Sicherheitsparameter von SEDs unter standardisierten Verfahren zu untersuchen.
Protokoll
Die Tierversuche wurden vom Institutional Animal Care and Use Committee (IACUC) der Kaohsiung Medical University, Taiwan, genehmigt (Protokoll-Nr.: IACUC-110082).
1. Tiervorbereitung und Anästhesie
- Bedingungen für die Selektion der Schweine: Ausgewählte Duroc-Landrace-Schweine im Alter von 3 bis 4 Monaten und einem Gewicht von 18 bis 30 kg.
- Vorbereitung vor dem Versuch: Die Schweine 8 h ohne Futter und 2 h ohne Wasser vor der Narkose fasten.
- Anästhesieeinleitung: 30 Minuten vor der Operation 2 mg/kg Tiletamin/Zolazepam intramuskulär verabreichen
HINWEIS: Neuromuskuläre Blocker wurden während der Anästhesieeinleitung nicht verwendet. - Auswahl des Endotrachealtubus: Verwenden Sie einen handelsüblichen 6,0-mm-Elektromyographie-Endotrachealtubus (EMG) (die Aufzeichnungselektroden) in der routinemäßig klinisch verwendeten Weise.
- Intubation: Lassen Sie den Anästhesisten die Ableitungselektroden mit Hilfe der direkten Laryngoskopie in Bauchlage intubieren. In dieser Studie wurde der Endotrachealtubus durch endtidales Kohlendioxid (etCO2)-Monitoring und Thoraxauskultation auf 24 cm fixiert, um die geeignete Tubusposition zu gewährleisten.
- Anästhesieerhaltung: Legen Sie das Schwein auf den Rücken, strecken Sie den Hals und fixieren Sie den Endotrachealtubus. Stellen Sie das Atemzugvolumen auf 8 bis 12 ml/kg und eine Atemfrequenz von 15 bis 20 Atemzügen pro Minute ein. Verwenden Sie 1 % bis 2 % Sevofluran zur Aufrechterhaltung der Vollnarkose.
HINWEIS: Neuromuskuläre Blocker wurden während der Anästhesieerhaltung nicht verwendet. - Während des Versuchs ist neben der kontinuierlichen Überwachung der Körperkerntemperatur des Tieres darauf zu achten, dass die Versuchstemperatur in einem angemessenen Bereich liegt. Wenn das Tier einen Abfall der Körpertemperatur erfährt, sollte sofortige thermische Unterstützung wie eine warme Decke bereitgestellt werden.
2. Tierhaltung (Abbildung 1 und Abbildung 2)
- Überprüfen Sie eine chirurgische Anästhesieebene.
- Hautschnitt: Machen Sie einen 15 cm langen queren Halsschnitt auf der Haut 1 cm über dem Brustbein (Abbildung 1A).
- Heben Sie den subplastysmatischen Lappen auf das Zungenbeinniveau an.
- Trennen Sie die Gurtmuskeln über den Mittellinienansatz und ziehen Sie sich seitlich zurück, um den Schilddrüsenknorpel, den Krikoidknorpel, die Trachealringe und die Schilddrüse sichtbar zu machen.
HINWEIS: Die Ränder der Gurtmuskeln müssen für TG-Studien sorgfältig und ordentlich präpariert werden. - Nach der Exposition werden die Muskeln sternocleidomastoideus (SCMs) beidseitig präpariert (Abbildung 1B).
HINWEIS: Die Ränder der SCMs müssen für EP-Studien sorgfältig und sauber präpariert werden. - Identifikation, Freilegung und Präparation entlang der rekurrenten Kehlkopfnerven (RLNs) und Vagusnerven (VNs) bilateral (Abbildung 2).
HINWEIS: IONM kann bei diesem Schritt behilflich sein. - Führen Sie die Experimente der EP- und TG-Studien nach Schritt 4 und Schritt 5 durch.
- Halten Sie die Ferkel nach Abschluss des gesamten Experiments unter 4%-6% Sevofluran und euthanasieren Sie sie auf humane Weise durch eine Überdosis Tiletamin/Zolazepam (6 mg/kg).
3. Informationen und Einstellungen zu chirurgischen Energiegeräten (SEDs)
- Einzelheiten zu SEDs finden Sie in der Materialtabelle.
HINWEIS: In dieser Studie werden fortgeschrittene bipolare SEDs (als Gerät A bezeichnet) verwendet, um die EP- und TG-Studien zu demonstrieren.
4. Elektrophysiologische (EP) Studie
- Kontinuierliche IONM-Einstellung (Abbildung 3)
Anmerkungen: Stellen Sie sicher, dass die Aufzeichnungselektroden wie in Schritt 1.5 beschrieben intubiert sind.- Installieren Sie die Masseelektroden außerhalb der chirurgischen Schnittwunde.
- Installieren Sie die Stimulationselektroden: Installieren Sie eine 2,0-mm-APS-Elektrode (Automatic Periodic Stimulation) auf einer Seite des VN.
- Schließen Sie alle Elektroden an der Verbindungsbox an und überprüfen Sie, ob die Verbindungsbox mit dem Überwachungssystem verbunden ist (Nerve Integrity Monitoring System) und ob das Überwachungssystem eingeschaltet ist (Abbildung 3A).
- Vergewissern Sie sich, dass das Überwachungssystem anzeigt, dass die Elektroden korrekt angeschlossen sind.
- Wählen Sie die Seite Überwachung und klicken Sie auf Erweiterte Einstellungen.
- Klicken Sie auf APS, um die APS-Stimulation auf 1/min für langsame Rate, 1/s für schnelle Geschwindigkeit und Alarmgrenzen auf 50 % und 2000 μV für Amplituden und 10 % für Latenz einzustellen. Klicken Sie dann auf OK, um die Einstellungen abzuschließen.
HINWEIS: Die Einstellung anderer Spalten hängt vom Experimentator ab. - Klicken Sie in der Spalte Ereignisse auf Ereigniserfassung und legen Sie den Ereignisschwellenwert auf 100 μV fest.
HINWEIS: Abbildung 3B zeigt die Protokollschritte 4.1.5-4.1.7. - Suchen Sie die Vagus APS Stim-Spalte und stellen Sie den Stimulationsstrom auf 1,0 mA ein. Klicken Sie auf Baseline; Auf der rechten Seite des Bildschirms wird ein neues Fenster mit dem Titel "Einrichten der APS-Baseline" angezeigt.
- Geben Sie den Sitzungstitel und die Sitzungskommentare ein. Wählen Sie den zu testenden Kanal aus, und das System beginnt automatisch mit der 20-maligen Messung. Die Basisamplitude und die Latenz werden automatisch berechnet und angezeigt. Klicken Sie auf Akzeptieren , wenn die Baseline korrekt ist.
HINWEIS: Abbildung 3C zeigt die Protokollschritte 4.1.8-4.1.9. - Klicken Sie auf das Schnellvorlauf-Symbol in der Spalte Vagus APS Stim , um einen Test zu starten. Klicken Sie nach jedem EP-Experiment auf das Pulse-Symbol , um die Aufnahme zu stoppen.
- Wählen Sie die Seite Berichte aus, und legen Sie das Berichtsausgabeformat fest, um die Datei auf USB zu speichern.
HINWEIS: Das Beispiel für einen C-IONM-Bericht ist in Abbildung 3D dargestellt.
- EP-Aktivierungsstudie (Abbildung 4)
- Entwickeln Sie experimentelle Richtlinien, bevor Sie mit einem Experiment beginnen.
ANMERKUNG: Abbildung 4A zeigt ein gängiges Beispiel für ein EP-Aktivierungsstudienprotokoll, das entsprechend den SED-Merkmalen angepasst werden kann. Bei einigen Geräten mit Aktivierungszyklen ist die einzelne Aktivierungszeit ein einzelner Aktivierungszyklus, der meist zwischen 2 und 4 s liegt. Die meisten SEDs haben keinen Aktivierungszyklus, und die einzelne Aktivierungszeit beträgt 3 s. - Aktivierungsabstandstests bei 5 mm:
- Tragen Sie die SED in einem Abstand von 5 mm zum RLN auf das Weichgewebe auf und aktivieren Sie die SED (Einzelaktivierung).
- Beobachten Sie die EMG-Veränderung. Dreimal mit dem gleichen Aktivierungsabstand arbeiten, es sei denn, es tritt eine wesentliche Änderung der EMG-Amplitude auf.
Anmerkungen: Abbildung 4B zeigt den Aktivierungsabstandstest bei 5 mm.
- Aktivierungsabstandstests bei 2 mm:
- Tragen Sie die SED in 1 mm Abstand auf das Weichgewebe in der Nähe der RLN auf und aktivieren Sie die SED (Einzelaktivierung).
- Beobachten Sie die EMG-Veränderung. Dreimal mit dem gleichen Aktivierungsabstand arbeiten, es sei denn, es tritt eine wesentliche Änderung der EMG-Amplitude auf.
- Aktivierungsabstandstests bei 1 mm:
- Tragen Sie die SED in einem Abstand von 1 mm zum RLN auf das Weichgewebe auf und aktivieren Sie die SED (einmalige Aktivierung).
- Beobachten Sie die EMG-Veränderung. Dreimal mit dem gleichen Aktivierungsabstand arbeiten, es sei denn, es tritt eine erhebliche Änderung der EMG-Amplitude auf
- Wenn während der Schritte 4.2.2-4.2.4 eine erhebliche Abnahme der EMG-Amplitude beobachtet wird, ist das RRN-Experiment zu stoppen. Zeichnen Sie das Echtzeit-EMG 20-60 Minuten lang kontinuierlich auf, um festzustellen, ob die Verletzung reversibel ist. (Abbildung 4C)
- Erfassen Sie die Versuchsergebnisse manuell als Tabelle (Tabelle 1).
- Entwickeln Sie experimentelle Richtlinien, bevor Sie mit einem Experiment beginnen.
- Studie zur EP-Kühlung (Abbildung 5)
- Entwickeln Sie experimentelle Richtlinien, bevor Sie mit einem Experiment beginnen.
HINWEIS: Abbildung 5A zeigt ein gängiges Beispiel für ein EP-Kühlungsstudienprotokoll, das entsprechend den SED-Eigenschaften angepasst werden kann. - Abkühlzeittests von 5 s:
- Wenden Sie die SED-Einzelaktivierung auf den SCM-Muskel an. Berühren Sie den RLN nach 5 s des Wartens und Abkühlens mit der Spitze des SED.
- Beobachten Sie die EMG-Veränderung. Dreimal zur gleichen Abkühlzeit betreiben, es sei denn, es tritt eine wesentliche Änderung der EMG-Amplitude auf.
- Abkühlzeittests von 2 s:
- Wenden Sie die SED-Einzelaktivierung auf den SCM-Muskel an. Berühren Sie den RLN nach 2 s des Wartens und Abkühlens mit der Spitze des SED.
- Beobachten Sie die EMG-Veränderung. Dreimal zur gleichen Abkühlzeit betreiben, es sei denn, es tritt eine wesentliche Änderung der EMG-Amplitude auf.
HINWEIS: Abbildung 5B zeigt den Abkühlzeittest von 2 s.
- Fahren Sie sofort mit Muskelberührungsmanövern (MTM) fort:
- Wenden Sie die SED-Einzelaktivierung auf den SCM-Muskel an. Berühren Sie schnell (ca. 1 s) die aktivierte Oberfläche des SED mit einer anderen Position des SCM (MTM, Abbildung 5C).
- Berühren Sie die RLN mit der Spitze des SED unmittelbar nach dem MTM und beobachten Sie die EMG-Veränderung. Dreimal zur gleichen Abkühlzeit betreiben, es sei denn, es tritt eine wesentliche Änderung der EMG-Amplitude auf.
- Fahren Sie sofort ohne Muscle Touch Maneuver (MTM)-Tests fort:
- Wenden Sie die SED-Einzelaktivierung auf den SCM-Muskel an. Berühren Sie den RLN sofort mit der Spitze des SED ohne MTM.
- Beobachten Sie die EMG-Veränderung. Betreiben Sie die gleiche Abkühlzeit dreimal, es sei denn, es tritt eine wesentliche Änderung der EMG-Amplitude auf. Wenn eine erhebliche Abnahme der EMG-Amplitude beobachtet wird, befolgen Sie Schritt 4.3.6.
- Wenn eine erhebliche Abnahme der EMG-Amplitude beobachtet wird, ist das RRN-Experiment zu stoppen. Überwachen Sie dann die Echtzeit-EMG-Reaktion mindestens 20 Minuten lang, um festzustellen, ob die RRN-Verletzung reversibel ist oder nicht (Abbildung 5D).
- Erfassen Sie die Versuchsergebnisse manuell als Tabelle (Tabelle 2).
- Entwickeln Sie experimentelle Richtlinien, bevor Sie mit einem Experiment beginnen.
5. Thermographische (TG) Studie
- Richten Sie das Wärmebildsystem ein (Abbildung 6).
HINWEIS: Wärmebildkamera mit Temperaturempfindlichkeit bis zu einem Temperaturbereich von -20 °C bis 650 °C. Das Bild wird jede Sekunde aktualisiert.- Platzieren Sie die Kamera 50 cm vom Zielgewebe entfernt in einem Winkel von 60° zum Versuchstisch (Abbildung 6A).
HINWEIS: Im Operationsfeld, gemessen mit einer Wärmebildkamera, wird die Temperatur entsprechend der Farbskala angezeigt. Der Ort mit der höchsten Temperatur auf dem Bildschirm wird mit einem "+"-Zeichen markiert und die entsprechende Temperatur angezeigt (Abbildung 6B) - Wählen Sie den Videomodus und drücken Sie die Aufnahmetaste.
HINWEIS: Die von der Wärmebildkamera überwachten Vorgänge werden kontinuierlich in Videoform aufgezeichnet.
- Platzieren Sie die Kamera 50 cm vom Zielgewebe entfernt in einem Winkel von 60° zum Versuchstisch (Abbildung 6A).
- Führen Sie die Tiervorbereitung für die TG-Studie durch:
- Erfassen Sie die Hintergrundtemperatur des Experimentierfeldes mit der Wärmebildkamera. Die Hintergrundtemperatur sollte im Bereich von 25 ± 2 °C liegen (Abbildung 6C). Wenn die Hintergrundtemperatur diesen Bereich überschreitet, stellen Sie die Temperatur der Laborklimaanlage ein und testen Sie erneut.
- Standard-Gurtmuskeldicke für die SED-Aktivierung: Bereiten Sie die Gurtmuskulatur für die TG-Studie vor, wie in Schritt 2.3 beschrieben. Die Standard-Gurtmuskeldicke für die SED-Aktivierung beträgt 5 mm (Abbildung 6D).
- TG-Aktivierungsstudie (Abbildung 6 und Abbildung 7)
- Tests in trockener Umgebung: Wischen Sie die Oberfläche der Muskeln des Schweineriemens mit trockener Gaze ab.
- Tests der gesamten Klinge in einer trockenen Umgebung (Abbildung 7A):
- Fassen Sie den Gurtmuskel über die gesamte Länge der Klinge mit SED (Abbildung 6E).
- Maximale Aktivierungstemperatur auswerten: Nach einmaliger Aktivierung wird während der Messung die maximale Temperatur auf dem Bildschirm angezeigt (Abbildung 7B).
- Seitliche Wärmeausbreitung auswerten: Messen Sie den Durchmesser der 60 °C Isothermenlinie nach einmaliger Aktivierung.
- Rauch und Spritzer auswerten: Nach einer einmaligen Aktivierung, wenn die höchste Temperatur auf dem Bildschirm 60 °C überschreitet, zeichnen Sie Rauch und Spritzer auf dem Bildschirm auf. Wiederholen Sie fünf Messungen in verschiedenen Bereichen.
Anmerkungen: Die maximale Aktivierungstemperatur wurde nur mit Tests der gesamten Klinge in einer trockenen Umgebung bewertet.
- Ein Drittel (1/3) der Schaufeltests in einer trockenen Umgebung (Abbildung 7C):
- Fassen Sie den Gurtmuskel mit einer vorderen 1/3-langen Klinge unter Verwendung von SED (Abbildung 6F). Bewerten Sie die seitliche Wärmeausbreitung, den Rauch und die Spritzbildung (Abbildung 7D) wie in Schritt 5.3.1.1 beschrieben. Wiederholen Sie fünf Messungen in verschiedenen Bereichen.
- Tests der gesamten Klinge in einer trockenen Umgebung (Abbildung 7A):
- Tests in nasser Umgebung: Die Muskeln des Schweineriemens kurz vor der SED-Aktivierung 3 s lang in sterilem Wasser einweichen.
- Tests der gesamten Klinge in einer feuchten Umgebung (Abbildung 7E): Fassen Sie den Gurtmuskel über die gesamte Länge der Klinge mit SED und bewerten Sie die seitliche Wärmeausbreitung (Abbildung 7F), Rauch und Spritzer wie in Schritt 5.3.1.1 beschrieben. Wiederholen Sie fünf Messungen in verschiedenen Bereichen.
- Ein Drittel (1/3) der Tests in einer feuchten Umgebung (Abbildung 7G): Fassen Sie den Gurtmuskel mit einer vorderen 1/3-langen Klinge unter Verwendung von SED und bewerten Sie die seitliche Wärmeausbreitung, den Rauch (Abbildung 7H) und das Spritzen, wie in Schritt 5.3.1.1 beschrieben. Wiederholen Sie fünf Messungen an verschiedenen Stellen.
- Zeichnen Sie die Versuchsergebnisse manuell als Tabelle auf (Tabelle 3).
- Tests in trockener Umgebung: Wischen Sie die Oberfläche der Muskeln des Schweineriemens mit trockener Gaze ab.
- TG-Kühlstudie (Abbildung 8)
- Trockene Umgebung: Wischen Sie die Oberfläche der Schweinebandmuskeln mit trockener Gaze ab, wie in Schritt 5.3.1 beschrieben.
HINWEIS: In der TG-Kühlstudie wurden alle Aktivierungen in einer trockenen Umgebung mit Aktivierung der gesamten Schaufel durchgeführt. - Minimale Abkühlzeit ohne MTM auswerten: Beginnen Sie nach einmaliger SED-Aktivierung mit der gesamten Klinge auf dem Gurtmuskel mit der Aufzeichnung der Abkühlzeit, bis die höchste Temperatur auf dem Bildschirm weniger als 60 °C betrug. Wiederholen Sie fünf Messungen in verschiedenen Bereichen.
HINWEIS: Wenn Sie die Abkühlzeit und -temperatur der SED-Klinge nach einmaliger Aktivierung und MTM messen, bedecken Sie den SED-aktivierten Muskelbereich und den MTM-berührenden Muskelbereich mit Gaze, da die hohe Temperatur in diesen Bereichen oben auf dem TG-Bildschirm erkannt wird und die tatsächlich zu messende Temperatur stört. - Bewerten Sie die Klingentemperatur nach MTM: Nach einer einmaligen Aktivierung des SED mit der gesamten Klinge auf dem Gurtmuskel berühren Sie schnell (~1 s) die aktivierte Oberfläche des SED mit einer anderen Position des Gurtmuskels (Abbildung 8A). Notieren Sie dann die Temperatur unmittelbar nach dem Verlassen des SED aus dem Gurtmuskel bei geöffneter Klinge (Abbildung 8B).
- Bewerten Sie die minimale Abkühlzeit mit MTM: Wenn die Temperatur nach Schritt 5.4.3 mehr als 60 °C beträgt, beginnen Sie mit der Aufzeichnung der Abkühlzeit, bis die höchste Temperatur auf dem Bildschirm weniger als 60 °C beträgt. Wiederholen Sie fünf Messungen in verschiedenen Bereichen.
- Erfassen Sie die Versuchsergebnisse manuell als Tabelle (Tabelle 4).
- Trockene Umgebung: Wischen Sie die Oberfläche der Schweinebandmuskeln mit trockener Gaze ab, wie in Schritt 5.3.1 beschrieben.
6. Interpretationen von Daten
- Präsentieren Sie die Sicherheitsparameter EP und TG in tabellarischer Form mit Rauch- und Spritzmarkierung.
HINWEIS: Hier werden die EP- und TG-Sicherheitsparameter von SED in tabellarischer Form dargestellt und Rauch und Spritzwasser sind mit den Symbolen * bzw. # gekennzeichnet. In EP- und TG-Studien sind im Endergebnis die maximalen Daten aufgeführt (siehe Tabelle 5).
Ergebnisse
Die Tieroperation wurde an jedem Ferkel durchgeführt und die anatomischen Strukturen wurden identifiziert, wie in Abbildung 1 und Abbildung 2 dargestellt. Mehrere Strukturen wurden fein säuberlich präpariert (SCM-Muskeln und Gurtmuskeln) und sorgfältig präpariert (RLNs und VNs) nach dem in Abbildung 1 und Abbildung 2 gezeigten standardisierten Verfahren. Die in dieser Studie getesteten SEDs sind in ergänzenden Tabellen dargestellt. Unter Anwendung der im Abschnitt Protokoll beschriebenen Standardverfahren können die Sicherheitsparameter von SEDs im Tierversuch ermittelt werden.
Elektrophysiologische (EP) Studie
CIONM besteht aus drei Hauptteilen: der Stimulationselektrode, der Aufzeichnungselektrode und dem Überwachungssystem (Abbildung 3A). Nachdem sichergestellt ist, dass das CIONM-System verfügbar ist, kann die Signaländerung während der EP-Studie gut dokumentiert werden. (Abbildung 3D).
EP-Aktivierungsstudie: Die Protokolle der EP-Aktivierungsstudie sind in Abbildung 4A dargestellt. Der sichere Aktivierungsabstand ist definiert als einmalige Aktivierung des SED an einer Position, die größer als dieser Abstand ist, ohne dass es zu einer wesentlichen Änderung der EMG-Amplitude kommt. Die APS-EMG-Signalaufzeichnungen der EP-Aktivierungsstudie sind in Abbildung 4C dargestellt. Ein Beispiel für die Demonstration der experimentellen Ergebnisse der EP-Aktivierungsstudie ist in Tabelle 1 dargestellt. Die endgültigen Interpretationen sind in Tabelle 5 dargestellt.
EP-Kühlungsstudie: Die Studienprotokolle zur EP-Kühlung sind in Abbildung 5A dargestellt. Die sichere Abkühlzeit ist definiert als eine Abkühlung von mehr als dieser Zeit nach einer einmaligen Aktivierung des SED, die keine wesentliche Änderung der EMG-Amplitude verursacht. Unmittelbar nach einmaliger Aktivierung des SED wurde eine MTM von 1 s durchgeführt, die je nach Auftreten einer erheblichen EMG-Amplitudenänderung bestimmte, ob die SED sicher oder unsicher war. Die APS-EMG-Signalaufzeichnungen der EP-Aktivierungsstudie sind in Abbildung 5D dargestellt. Ein Beispiel für die Demonstration der experimentellen Ergebnisse der EP-Kühlstudie ist in Tabelle 2 dargestellt. Die endgültigen Interpretationen sind in Tabelle 5 dargestellt.
Thermographische (TG) Studie
Die standardisierte Einstellung des Wärmebildsystems ist in Abbildung 6A dargestellt. Die Temperaturanzeigen, die höchste Temperaturmarkierung ("+"-Zeichen) und die Farbskala sind in Abbildung 6B dargestellt. Die Hintergrundtemperatur des Versuchsbereichs wird wie in Abbildung 6C dargestellt aufgezeichnet. Die Gurtmuskeln wurden mit einer Standarddicke von 5 mm präpariert, die in Abbildung 6D dargestellt ist. Die Definition der gesamten Klinge und der dritten Klinge wurde in Abbildung 6E,F demonstriert.
TG-Aktivierungsstudie: Die maximale Temperatur wurde mit der gesamten Klinge in einer trockenen Umgebung getestet; Die Ergebnisse sind in Tabelle 3 dargestellt. Die TG-Aktivierungsstudie umfasst vier Kombinationen: Tests mit ganzer Schaufel in einer trockenen Umgebung (Abbildung 7A, B), Tests mit einem Drittel der Schaufel in einer trockenen Umgebung (Abbildung 7C, D), Tests mit ganzer Schaufel in einer feuchten Umgebung (Abbildung 7E, F) und Tests mit einem Drittel der Schaufel in einer feuchten Umgebung (Abbildung 7G, H). Im Vergleich zur trockenen Umgebung treten auf dem TG-Bildbildschirm in der feuchten Umgebung tendenziell Wärmespritzer und seitliche Wärmeausbreitung auf. Verschiedene SEDs haben unterschiedliche laterale Wärmeausbreitungs- und Rauch-/Spritzbildungsmuster, wenn sie mit einer ganzen Klinge oder einem Drittel einer Klinge aktiviert werden, entsprechend ihren unterschiedlichen Hämostasemechanismen. Die thermische Spreizdistanz ist definiert als der weiteste Abstand zwischen der 60 °C Isothermenlinie und der SED-Schaufel nach einer einmaligen Aktivierung. Die experimentellen Ergebnisse sind in Tabelle 3 dargestellt. Die endgültigen Interpretationen sind in Tabelle 5 dargestellt.
TG-Kühlstudie: Die sichere Abkühlzeit ist definiert als eine Abkühlung von mehr als dieser Zeit nach einmaliger Aktivierung des SED und liegt auf dem TG-Schirm deutlich unter 60 °C. Die MTM (Abbildung 8A) ist eine gute Kühlmethode, bei der die Temperatur unter dem TG-Bildgebungsbildschirm schnell abgesenkt wird. Unmittelbar nach einer einmaligen Aktivierung des SED wurde eine MTM von 1 s durchgeführt, und die Temperatur an der Schaufel, die 60 °C überschreitet oder nicht, bestimmt, ob die SED sicher bzw. unsicher ist (Abbildung 8B). Die experimentellen Ergebnisse, einschließlich der minimalen Abkühlzeit ohne MTM, der Schaufeltemperatur nach MTM und der minimalen Abkühlzeit mit MTM, sind in Tabelle 4 dargestellt. Die endgültigen Interpretationen sind in Tabelle 5 dargestellt.
Interpretationen von Daten
Entsprechend den in den Experimenten gewonnenen Daten werden die Sicherheitsparameter von SED in eine Tabelle integriert (Tabelle 5 zeigt die Daten, die mit Advanced bipolar SEDs (in der Materialtabelle als Device A bezeichnet) gesammelt wurden). Gerät A ist eines der Geräte, die in dieser Studie zur Untersuchung verwendet werden. Diese Daten deuten darauf hin, dass Chirurgen bei der Verwendung dieses SED einen ausreichenden Sicherheitsabstand und eine ausreichende Abkühlzeit einhalten, sich an unterschiedliche Operationsumgebungen und unterschiedliche Greiflängen anpassen, beobachten sollten, ob ein unregelmäßiges thermisches Ausbreitungsmuster (Rauch und Spritzer) auftritt, und die Temperatur des SED nach einer einmaligen Aktivierung und unmittelbar nach der Durchführung der MTM bewerten sollten.
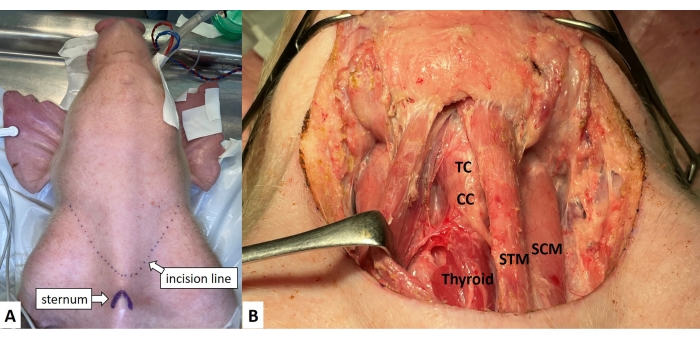
Abbildung 1: Hautschnitt und Dissektion der Muskeln sternocleidomastoideus. (A) 15 cm über dem Brustbein wird eine 15 cm lange transversale zervikale Hautschnittlinie angelegt. (B) Die Gurtmuskeln werden seitlich zurückgezogen, um den Schilddrüsenknorpel, den Krikoidknorpel, die Trachealringe und die Schilddrüse sichtbar zu machen. Abkürzungen: SCM = M. sternocleidomastoideus, STM = Gurtmuskeln, TC = Schildknorpel, CC = Krikoidknorpel, Schilddrüse = Schilddrüse. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
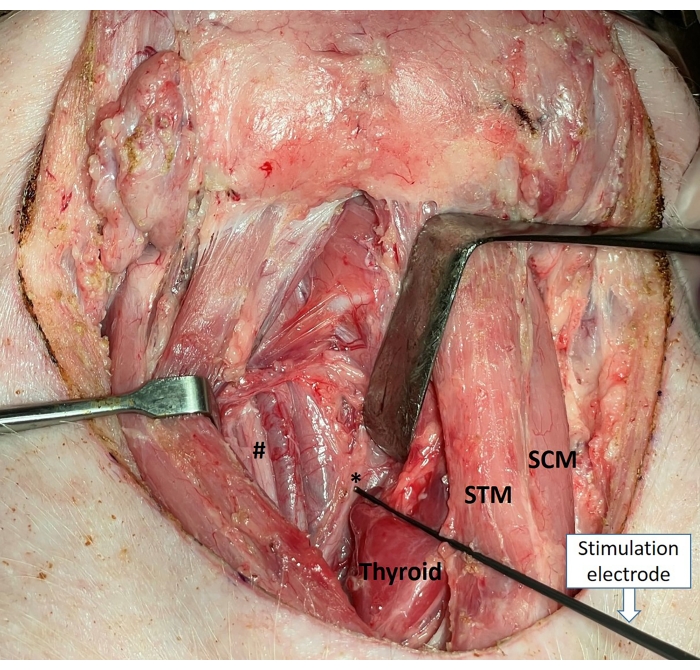
Abbildung 2: Identifizieren und Verfügbar machen der RLNs (*) und VNs (#) verfügbar. Abkürzungen: SCM = M. sternocleidomastoideus, S = Gurtmuskeln, TG = Schilddrüse, RLN = Nervus laryngeus recurrens, VN = Vagusnerven. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.

Abbildung 3: C-IONM-Einstellungen und Aufzeichnungen. (A) Elektroden des C-IONM einrichten: Aufzeichnungselektroden - EMG Endotrachealtubus 6# wurde intubiert; Stimulationselektroden wurden auf dem VN installiert (*); Masseelektroden-Elektroden wurden außerhalb der chirurgischen Schnittwunde installiert. Alle Elektroden waren mit dem Überwachungssystem verbunden. (B) Die erweiterten Einstellungen von APS-Stimuli. (C) Stellen Sie den Stimulationsstrom ein und beginnen Sie, die Baseline in der Spalte Vagus APS Stim zu erhalten, und die Baseline-Latenz und -Amplitude werden im neuen Fenster automatisch getestet und berechnet (APS-Baseline wird festgelegt). (D) Das Beispiel eines C-IONM-Berichts. Abkürzungen: APS = automatische periodische Stimulation, EMG = Elektromyographie, ETT = Endotrachealtubus, C-IONM = kontinuierliches intraoperatives neuronales Monitoring, RLN = Nervus laryngeus recurrens, VN = Vagusnerven. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
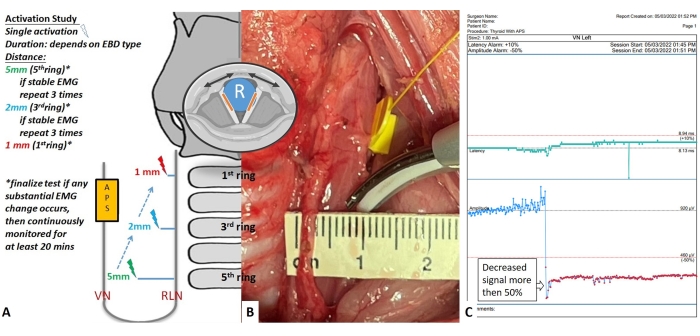
Abbildung 4: Flussdiagramm der Studienprotokolle zur EP-Aktivierung . (A) Einzelne Aktivierungstests werden am RLN von den proximalen (kaudalen) Segmenten zu den distalen (kranialen) Segmenten in unterschiedlichen Abständen durchgeführt. Wenn die EMG-Antwort nach den drei Aktivierungstests im Abstand von 5 mm am proximalen Segment unverändert blieb, wurde ein weiterer Test im Abstand von 2 mm durchgeführt. Wenn die EMG-Antwort nach wiederholten Tests im Abstand von 2 mm stabil geblieben ist, werden die abschließenden Sicherheitstests im Abstand von 1 mm oder durch direktes Berühren der SED-Spitze mit dem RLN durchgeführt. Wenn nach einem Test eine erhebliche Abnahme der EMG-Amplitude beobachtet wird, ist die Seite des RLN-Experiments abgeschlossen, und die EMG-Reaktion wird mindestens 20 Minuten lang kontinuierlich überwacht. (B) Die SED wird in einem Abstand von 5 mm in der Nähe des linken RLN getestet. (C) APS-EMG-Signal bei der Durchführung der Aktivierungsstudie. Abkürzungen: SED = surgical energy device, RLN = recurrender Kehlkopfnerv, EMG = elektromyographisch, APS = automatische periodische Stimulation. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.

Abbildung 5: Flussdiagramm des Studienprotokolls zur EP-Kühlung . (A) Die Tests werden am RLN von den proximalen (kaudalen) Segmenten bis zu den distalen (kranialen) Segmenten durchgeführt. Nach der SED-Aktivierung am ipsilateralen SCM-Muskel (weißer Pfeil) und nach unterschiedlichen Abkühlzeiten berühren Sie die Spitze des RLN (gelber Stern) für einen Zeitraum von 5 s. Wenn die EMG-Reaktion nach drei Tests von 5 s Abkühlzeit unverändert geblieben ist, werden 2 s Abkühlzeittests durchgeführt. Wenn die EMG-Antwort nach wiederholten Tests unverändert geblieben ist, werden die abschließenden Sicherheitstests durch Berühren der SED-Spitze mit dem RLN unmittelbar nach einer einfachen oder doppelten Aktivierung mit oder ohne Berührungsmanöver (Sternchen) durchgeführt. (B) Die Spitze des SED wird geöffnet, um den inneren nicht beschichteten Teil des RLN zu berühren. (C) Das Berührungsmanöver (Sternchen) ist nach der Aktivierung ein schnelles Berühren/Abkühlen mit SCM. (D) Das APS-EMG-Signal bei der Durchführung der Kühlungsstudie. Abkürzungen: RLN = Nervus laryngeus recurrens, SCM = sternocleidomastoid, EMG = electromyographic. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
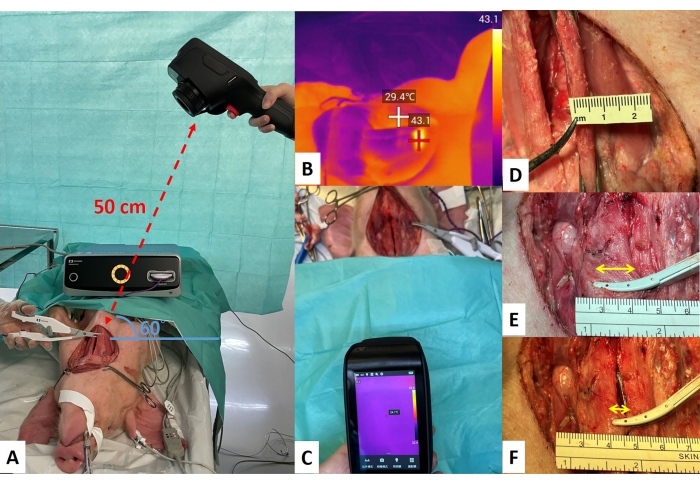
Abbildung 6: Einstellung des Wärmebildsystems . (A) Die Kamera wurde 50 cm vom Zielgewebe entfernt und in einem Winkel von 60° vom Versuchstisch platziert. (B) Das Operationsfeld wird mit einer Wärmebildkamera gemessen. Die Temperatur wird entsprechend der Farbskala angezeigt und die höchste Temperatur auf dem Bildschirm ist mit einem "+"-Zeichen gekennzeichnet. (C) Zeichnen Sie die Hintergrundtemperatur des Versuchsbereichs auf. (D) Die Standard-Gurtmuskeldicke für die SED-Aktivierung beträgt 5 mm. (E) Test der gesamten Klinge in einer trockenen Umgebung. (F) Ein Drittel (1/3) Klingentests in einer trockenen Umgebung. Abkürzung: SED = surgical energy devices. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
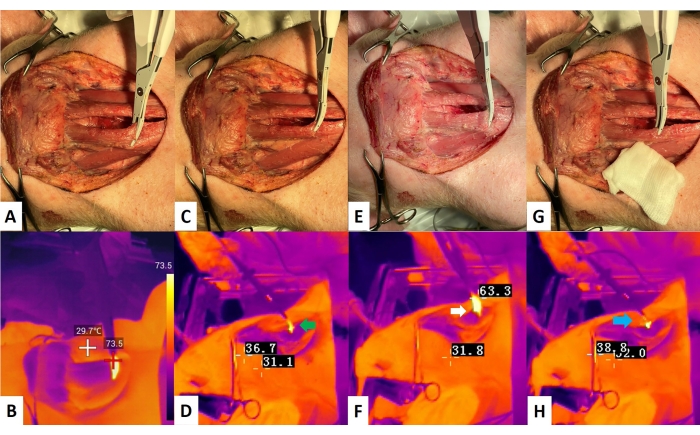
Abbildung 7: TG-Aktivierungsstudie. (A,B) A: Tests der ganzen Klinge in einer trockenen Umgebung; B: TG-Bild, die maximale Aktivierungstemperatur beträgt während der Aktivierung mehr als 60 °C. (C,D) C: Ein Drittel (1/3) Klingentests in einer trockenen Umgebung; D: TG-Bild, Spritzen (grüner Pfeil) wird nach der Aktivierung beobachtet. (E) Prüfungen ganzer Klingen in nasser Umgebung; (F) TG-Bild, deutlichere laterale Wärmeausbreitung (weißer Pfeil) im Vergleich zur trockenen Umgebung. (G) Ein Drittel (1/3) Klingentests in einer nassen Umgebung. (H) TG-Bild, Rauch (blauer Pfeil) ist im Vergleich zu trockener Umgebung deutlicher. Abkürzung: TG = Thermografie. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
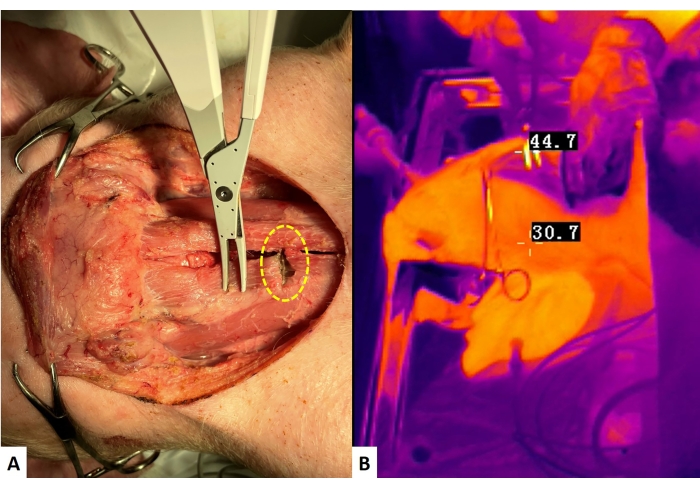
Abbildung 8: TG-Kühlstudie mit MTM . (A) Nach einmaliger Aktivierung des SED mit der gesamten Klinge auf dem Gurtmuskel (gelb gestrichelter Linienkreis) wird die aktivierte Oberfläche des SED schnell (ca. 1 s) mit einer anderen Position des Gurtmuskels berührt. (B) Das TG-Bild zeigt die SED-Temperatur unmittelbar nach dem Verlassen des SED aus dem Gurtmuskel bei geöffneter Klinge. Wenn die Temperatur mehr als 60 °C beträgt, beginnen Sie mit der Aufzeichnung der Abkühlzeit, bis die höchste Temperatur auf dem Bildschirm weniger als 60 °C beträgt. Abkürzungen: TG = thermographic, MTM = muscle tough maneuver, SED = surgical energy devices. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
| Nerv Nein. | 5 mm, | 2 mm, |
| Amplitudenstatus | Amplitudenstatus | |
| Nerv 1 | stabil (3) | stabil (3) |
| Nerv 2 | stabil (3) | stabil (3) |
| Nerv 3 | stabil (3) | stabil (3) |
| LOS, Signalverlust; Die Zahl in Klammern gibt die Anzahl der Tests an | ||
Tabelle 1: Elektrophysiologische (EP) Aktivierungsstudie. Dies ist eines der Ergebnisse der EP-Aktivierungsstudie. Jede Distanz wird dreimal untersucht, bis das EMG-Signal verringert wird oder verloren geht. Jede SED wird mit drei Nerven überprüft. Diese Daten werden mit Gerät A (Materialtabelle) ermittelt.
| Nein. Nerv | 5 Sek., | 2 s, | Sofort ohne MTM, |
| Amplitudenstatus | Amplitudenstatus | Amplitudenstatus | |
| Nerv 1 | stabil (3) | stabil (3) | LOS (1) |
| Nerv 2 | stabil (3) | stabil (3) | 47% Verlust (2) |
| Nerv 3 | stabil (3) | stabil (3) | LOS (2) |
| MTM, Muskelberührungsmanöver; LOS, Signalverlust; Die Zahl in Klammern gibt die Anzahl der Tests an | |||
Tabelle 2: Elektrophysiologische (EP) Kühlungsstudie. Dies ist eines der Ergebnisse der EP-Kühlungsstudie. Jede Distanz wird dreimal untersucht, bis das EMG-Signal verringert wird oder verloren geht. In diesem Experiment werden auch die MTM untersucht. Jede SED wird mit drei Nerven überprüft. Diese Daten werden mit Gerät A (Materialtabelle) ermittelt.
| Maximale Aktivierungstemperatur (°C) | |||||
| Klinge | Prüfung 1 | Prüfung 2 | Prüfung 4 | Prüfung 5 | Maximum |
| Ganze Klinge | 74.7 | 73.5 | 72.3 | 74.1 | 77.4 |
| Seitlicher thermischer Spreizabstand (in trockener Umgebung) (mm) | |||||
| Klinge | Prüfung 1 | Prüfung 2 | Prüfung 4 | Prüfung 5 | Maximum |
| Ganze Klinge | 3.7 | 5.2 | 4.9 | 4.2 | 5.3 |
| Ein Drittel der Klinge | 4.2 | 4.7 | 4.5 | 5.0# | 5.2# |
| Seitlicher thermischer Streuabstand (in nasser Umgebung) (mm) | |||||
| Klinge | Prüfung 1 | Prüfung 2 | Prüfung 4 | Prüfung 5 | Maximum |
| Ganze Klinge | 5.2*# | 4.3# | 6.7 | 4.6# | 6,7*# |
| Ein Drittel der Klinge | 3,9*# | 4.5# | 5.1# | 5,7*# | 5,7*# |
| * mit Rauch; # mit Spritzern | |||||
Tabelle 3: Thermografische (TG) Aktivierungsstudie. Dies ist eines der Ergebnisse der TG-Aktivierungsstudie. Jede Aktivierung wird fünfmal unter der Kamera überprüft. Diese Daten werden mit Gerät A (Materialtabelle) ermittelt.
| Minimale Abkühlzeit (bis 60 °C) ohne MTM(s) | ||||
| Prüfung 1 | Prüfung 2 | Prüfung 3 | Prüfung 4 | Prüfung 5 |
| 6 | 5 | 5 | 6 | 6 |
| Schaufeltemperatur nach MTM (°C) | ||||
| Prüfung 1 | Prüfung 2 | Prüfung 3 | Prüfung 4 | Prüfung 5 |
| 66.4 | 44.7 | 65.3 | 61.5 | 51.8 |
| Minimale Abkühlzeit (bis 60 °C) mit MTM(s) | ||||
| Prüfung 1 | Prüfung 2 | Prüfung 3 | Prüfung 4 | Prüfung 5 |
| 2 | - | 2 | 1 | - |
Tabelle 4: Thermografische (TG) Kühlungsstudie. Dies ist eines der Ergebnisse der TG-Kühlungsstudie. Jede Aktivierung wird fünfmal unter der Kamera untersucht und die Abkühlzeit aufgezeichnet. Diese Daten werden mit Gerät A (Materialtabelle) ermittelt.
| EP-Sicherheitsparameter | Gerät A |
| Aktivierungs-Distanz | 2 mm |
| Abkühlzeit | 2 $ s |
| TG-Sicherheitsparameter | Gerät A |
| Aktivierungstemperatur @ | 77.4 °C |
| Seitlicher thermischer Spreizungsabstand | |
| Trockenzustand: ganze Klinge (ein Drittel der Klinge) | 5,3 mm (5,2# mm) |
| Nasszustand: ganze Klinge (ein Drittel der Klinge) | 6,7 mm*# (5,7*# mm) |
| Abkühlzeit | |
| ohne MTM | 6 s |
| mit MTM (Schaufeltemperatur nach MTM) | 2 s (66,4 °C) |
| $ Kein EMG-Signalverlust nach Verwendung von MTM zur Kühlung der SEDs; @ mit ganzer Klinge in trockener Umgebung; | |
| * mit Rauch; # mit Spritzern; MTM, Muskelberührungsmanöver | |
Tabelle 5: Elektrophysiologische (EP) und thermografische (TG) Sicherheitsparameter. Die Tabelle enthält die in dieser Studie bewerteten EP- und TG-Sicherheitsparameter. Diese Daten werden mit Gerät A (Materialtabelle) ermittelt.
Diskussion
Die Entwicklung von SEDs basiert auf der Erwartung von Schilddrüsenchirurgen, eine effektive Hämostase während einer Schilddrüsenoperation zu erreichen. Die hohe Temperatur, die durch SED erzeugt wird, ist jedoch ein Risikofaktor, der nicht ignoriert werden kann. Mit der zunehmenden Verbreitung von SED werden auch thermische Verletzungen der Nerven häufiger auftreten. Daher liegt es in der Verantwortung der Schilddrüsenchirurgen, die SED verwenden, zu verstehen, wie das Gerät sicher zu bedienen ist. Es ist jedoch nicht ratsam, Sicherheitsparameter wiederholt durch Versuch und Irrtum beim Menschen zu überprüfen. Damit ist der Wert von Tierversuchen aufgezeigt. Darüber hinaus ist ein standardisierter Prozess notwendig, um die möglichen thermischen Auswirkungen der SEDs15,17 zu qualifizieren und zu quantifizieren, um Schilddrüsenchirurgen maximal Richtlinien für die sichere Durchführung von Operationen an die Hand zu geben.
In dieser Studie erfordern mehrere Schritte mehr Aufmerksamkeit. In den EP-Studien konnten neuromuskuläre Blockadewirkstoffe die EMG-Signale während des neuronalen Monitorings stören und wurden während der Anästhesieeinleitung und -erhaltung nicht eingesetzt. In den TG-Studien sollten andere Wärmequellen als die SED-Tests entfernt werden. Wenn die Wärmequellen nicht entfernt werden können (z. B. der Aktivierungsbereich für die Kühlstudie oder die Muskelstrapazierfähigkeit nach MTM), ist es notwendig, die nicht getesteten Wärmequellen mit Gaze zu blockieren. In den TG-Studien sollte bestätigt werden, dass die Temperatur der SEDs vor der Aktivierung innerhalb der Hintergrundreferenztemperatur (25 ± 2 °C) liegt, andernfalls sollte eine Kühlmaßnahme ergriffen werden, und die Schaufel sollte vor Beginn des Experiments als trocken eingestuft werden.
Mehrere frühere Studien haben zur Definition der Sicherheitsparameter EP 15,37,38,39,40,41,42,43 und TG31,32 für verschiedene SEDs in Aktivierungs- und Kühlungsstudien in verschiedenen schweineschilddrüsenchirurgischen Modellen beigetragen. Das aktuelle Protokoll integriert nicht nur die Erfahrungen der Vergangenheit, sondern optimiert und standardisiert den Prozess weiter. In der EP-Studie kam es nach der Aktivierung von SED ohne sicheren kritischen Abstand oder sichere Abkühlzeit zu einer irreversiblen und schnellen Verletzung. In der TG-Studie beobachteten wir das 60 °C isotherme Feld und die Entstehung von Rauch/Spritzern. Chirurgen können die thermischen Ausbreitungsmuster in verschiedenen Aktivierungsumgebungen und unterschiedlichen Greifbereichen besser verstehen.
Diese Studie weist noch einige Einschränkungen auf. Erstens ist die Temperatur in der Umgebung nicht die gleiche wie im Operationssaal, und die Temperatur des Ferkels ist nicht die gleiche wie die Körpertemperatur eines Menschen. Zweitens sind die Ergebnisse des Schweinemodells möglicherweise nicht auf alle klinischen Praktiken am Menschen anwendbar. Die tierexperimentelle Studie liefert Chirurgen nicht nur SED-Informationen, die vom Menschen nicht gewonnen werden können, sondern dient auch als wertvolle Forschungsplattform, um in Zukunft Informationen über thermische Verletzungen für neu entwickelte SEDs zu ermitteln. Diese Informationen können Chirurgen bei der Auswahl von Instrumenten und chirurgischen Strategien helfen, die thermische Schäden während der Schilddrüsen- und Nebenschilddrüsenchirurgie reduzieren können.
Dieser Artikel demonstriert das Standardverfahren für die Verwendung von Tierversuchen, damit Schilddrüsenchirurgen ein umfassenderes Verständnis von (1) dem sicheren Aktivierungsabstand und der Abkühlzeit für SEDs, (2) der maximalen Temperatur, die durch die Aktivierung von SEDs erzeugt wird, und (3) unregelmäßiger lateraler thermischer Ausbreitung und Rauch/Spritzen, die möglicherweise den Nerv verletzen können, erlangen können.
Offenlegungen
Die Autoren erklären, dass die Untersuchung ohne kommerzielle oder finanzielle Beziehungen durchgeführt wurde, die als potenzieller Interessenkonflikt ausgelegt werden könnten.
Danksagungen
Diese Studie wurde durch Zuschüsse des Kaohsiung Medical University Hospital, der Kaohsiung Medical University (KMUH109-9M44), des Kaohsiung Municipal Siaogang Hospital/Kaohsiung Medical University Research Center (KMHK-DK(C)110009, I-109-04, H-109-05, I-108-02) und des Ministeriums für Wissenschaft und Technologie (MOST 109-2628-B-037-014, MOST 110-2314-B-037-104-MY2, MOST 110-2314-B-037-120), Taiwan, unterstützt.
Materialien
| Name | Company | Catalog Number | Comments |
| Automatic periodic stimulation (APS) | Medtronic, Jacksonville, FL | 2.0 mm | |
| Advanced bipolar surgical energy devices(SEDs) | Medtronic, Minneapolis, MN | LigaSure Exact Dissector (Device A) | Generator: Valleylab LS10 energy platform Power setting: Default |
| Bipolar electrocautery | Generator: ForceTriad energy platform Power setting: 30 watts | ||
| Duroc-Landrace pigs | 3–4 months old; weighing 18–30 kg | ||
| Electromyography (EMG) Endotracheal tube (ETT) | Medtronic, Jacksonville, FL | #6 NIM Standard Tube | Recording electrodes |
| Ferromagnetic SEDs | Domain Surgical, Salt Lake City, Utah | FMwand, and Fmsealer | Generator: FMX G1 Generator Power setting: FMwand (Max 45); FMsealer (Max 3) |
| Hybrid SEDs (Ultrasonic and Advance bipolar SEDs) | Olympus Co Inc, Tokyo, Japan | Thunderbeat | Generator: Thunderbeat generator ESG USG 400 Power setting: SEAL&CUT mode (Level 1); SEAL mode (Level 3) |
| Monopolar electrocautery | Generator: ForceTriad energy platform Power setting: 15 watts | ||
| Nerve Integrity Monitoring (NIM) system | Medtronic, Jacksonville, FL | NIM 3.0 | Intraoperative neuromonitoring (IONM) equipment |
| Sevoflurane | 1% to 2% for anesthesia maintenance | ||
| Tiletamine/Zolazepam | 2 mg/kg for anesthesia induction | ||
| Thermal imaging camera | Ezo Corp., Taiwan | Thermal camera D4A (384x288 pixels) | Thermal image recording equioments |
| Ultrasonic SEDs | Ethicon, Johnson and Johnson, Cincinnati, OH | Harmonic Focus+ | Generator: Ethicon Endo-Surgery Generator G11 Power setting: Level 5 |
| Ultrasonic SEDs | Medtronic, Minneapolis, MN | Sonicision | Generator: Sonicision Reusable Generator Power setting: maximum power mode (55 kHz) |
Referenzen
- Wang, J. J., et al. Improving voice outcomes after thyroid surgery - review of safety parameters for using energy-based devices near the recurrent laryngeal nerve. Front Endocrinol. 12, 793431 (2021).
- Cakabay, B., et al. LigaSure versus clamp-and-tie in thyroidectomy: a single-center experience. Advances in Therapy. 26 (11), 1035-1041 (2009).
- Chiang, F. Y., et al. Comparison of hypocalcemia rates between LigaSure and clamp-and-tie hemostatic technique in total thyroidectomies. Head & Neck. 41 (10), 3677-3683 (2019).
- Liu, C. -. H., et al. Comparison of surgical complications rates between LigaSure small jaw and clamp-and-tie hemostatic technique in 1,000 neuro-monitored thyroidectomies. Frontiers in Endocrinology. 12, 313 (2021).
- Moran, K., et al. Energy vessel sealant devices are associated with decreased risk of neck hematoma after thyroid surgery. Updates in Surgery. 72 (4), 1135-1141 (2020).
- Pacilli, M., et al. Energy based vessel sealing devices in thyroid surgery: a systematic review to clarify the relationship with recurrent laryngeal nerve injuries. Medicina. 56 (12), 651 (2020).
- Garas, G., et al. Which hemostatic device in thyroid surgery? A network meta-analysis of surgical technologies. Thyroid. 23 (9), 1138-1150 (2013).
- Wu, C. W., et al. Intraoperative neuromonitoring for the early detection and prevention of RLN traction injury in thyroid surgery: A porcine model. Surgery. 155 (2), 329-339 (2014).
- Wu, C. -. W., et al. Intraoperative neural monitoring in thyroid surgery: lessons learned from animal studies. Gland Surgery. 5 (5), 473-480 (2016).
- Dionigi, G., et al. Severity of recurrent laryngeal nerve injuries in thyroid surgery. World Journal of Surgery. 40 (6), 1373-1381 (2016).
- Wu, C. W., et al. Recurrent laryngeal nerve (RLN) injury in thyroid surgery: lessons learned from the intraoperative neural monitoring (IONM). International Journal of Head and Neck Science. 1 (1), 19-26 (2017).
- Dionigi, G., et al. Recurrent laryngeal nerve injury in video-assisted thyroidectomy: lessons learned from neuromonitoring. Surg Endosc. 26 (9), 2601-2608 (2012).
- Dionigi, G. Energy based devices and recurrent laryngeal nerve injury: the need for safer instruments. Langenbeck's Archives of Surgery. 394 (3), 579-580 (2009).
- Kern, K. A. Medicolegal analysis of errors in diagnosis and treatment of surgical endocrine disease. Surgery. 114 (6), 1167-1174 (1993).
- Wu, C. W., et al. Intra-operative neural monitoring of thyroid surgery in a porcine model. Journal of Visualized Experiments. (144), e57919 (2019).
- Wu, C. W., et al. Investigation of optimal intensity and safety of electrical nerve stimulation during intraoperative neuromonitoring of the recurrent laryngeal nerve: a prospective porcine model. Head & Neck. 32 (10), 1295-1301 (2010).
- Dionigi, G., et al. Safety of energy based devices for hemostasis in thyroid surgery. Gland Surgery. 5 (5), 490 (2016).
- Björck, G., et al. New animal model for assessment of functional laryngeal motor innervation. Ann Otol Rhinol Laryngol. 121 (10), 695-699 (2012).
- Wu, C. W., et al. Feasibility of intraoperative neuromonitoring during thyroid surgery using transcartilage surface recording electrodes. Thyroid. 28 (11), 1508-1516 (2018).
- Wu, C. W., et al. Transcutaneous recording during intraoperative neuromonitoring in thyroid surgery. Thyroid. 28 (11), 1500-1507 (2018).
- Chiang, F. Y., et al. The mechanism of recurrent laryngeal nerve injury during thyroid surgery--the application of intraoperative neuromonitoring. Surgery. 143 (6), 743-749 (2008).
- Randolph, G. W., et al. Electrophysiologic recurrent laryngeal nerve monitoring during thyroid and parathyroid surgery: international standards guideline statement. Laryngoscope. 121, 1-16 (2011).
- Wu, C. -. W., et al. Informed consent for intraoperative neural monitoring in thyroid and parathyroid surgery - consensus statement of the International Neural Monitoring Study Group. Frontiers in Endocrinology. 12 (1598), (2021).
- Chiang, F. Y., et al. Standardization of intraoperative neuromonitoring of recurrent laryngeal nerve in thyroid operation. World Journal of Surgery. 34 (2), 223-229 (2010).
- Wu, C. W., et al. International neuromonitoring study group guidelines 2018: Part II: Optimal recurrent laryngeal nerve management for invasive thyroid cancer-incorporation of surgical, laryngeal, and neural electrophysiologic data. Laryngoscope. 128, 18-27 (2018).
- Schneider, R., et al. International neural monitoring study group guideline 2018 part I: Staging bilateral thyroid surgery with monitoring loss of signal. Laryngoscope. 128, 1-17 (2018).
- Wu, C. W., et al. Training courses in laryngeal nerve monitoring in thyroid and parathyroid surgery-The INMSG Consensus Statement. Frontiers in Endocrinology. 12, 705346 (2021).
- Dionigi, G., et al. Continuous monitoring of the recurrent laryngeal nerve in thyroid surgery: a critical appraisal. International Journal of Surgery. 11, 44-46 (2013).
- Schneider, R., et al. A new anchor electrode design for continuous neuromonitoring of the recurrent laryngeal nerve by vagal nerve stimulations. Langenbecks Archives of Surgery. 394 (5), 903-910 (2009).
- Sinclair, C. F., et al. Clarifying optimal outcome measures in intermittent and continuous laryngeal neuromonitoring. Head & Neck. 44 (2), 460-471 (2021).
- Hayami, M., et al. Steam induced by the activation of energy devices under a wet condition may cause thermal injury. Surgical Endoscopy. 34 (5), 2295-2302 (2020).
- Hayami, M., et al. Lateral thermal spread induced by energy devices: a porcine model to evaluate the influence on the recurrent laryngeal nerve. Sure Endosc. 33 (12), 4153-4163 (2019).
- Smith, C. T., Zarebczan, B., Alhefdhi, A., Chen, H. Infrared thermographic profiles of vessel sealing devices on thyroid parenchyma. Journal of Surgical Research. 170 (1), 64-68 (2011).
- Seehofer, D., et al. Safety and efficacy of new integrated bipolar and ultrasonic scissors compared to conventional laparoscopic 5-mm sealing and cutting instruments. Surgical Endoscopy. 26 (9), 2541-2549 (2012).
- Kim, F. J., et al. Temperature safety profile of laparoscopic devices: Harmonic ACE (ACE), Ligasure V (LV), and plasma trisector (PT). Surgical Endoscopy. 22 (6), 1464-1469 (2008).
- Lin, Y. C., et al. Electrophysiologic monitoring correlates of recurrent laryngeal nerve heat thermal injury in a porcine model. Laryngoscope. 125 (8), 283-290 (2015).
- Chávez, K. V., et al. Safety assessment of the use of ultrasonic energy in the proximity of the recurrent laryngeal nerve in a porcine model. The American Journal of Surgery. 215 (1), 186-190 (2018).
- Wu, C. W., et al. Recurrent laryngeal nerve safety parameters of the H armonic F ocus during thyroid surgery: Porcine model using continuous monitoring. The Laryngoscope. 125 (12), 2838-2845 (2015).
- Huang, T. Y., et al. Safety parameters of ferromagnetic device during thyroid surgery: Porcine model using continuous neuromonitoring. Head Neck. 42 (10), 2931-2940 (2020).
- Dionigi, G., et al. Safety of LigaSure in recurrent laryngeal nerve dissection-porcine model using continuous monitoring. The Laryngoscope. 127 (7), 1724-1729 (2017).
- Huang, T. -. Y., et al. Safety of Ligasure exact dissector in thyroidectomy with continuous neuromonitoring: a porcine model. Gland Surgery. 9 (3), 702 (2020).
- Kim, H. K., Chai, Y. J., Lee, H. Y., Kim, H. Y., Dionigi, G. Comparing the safety of harmonic ACE and ACE+ around the recurrent laryngeal nerve in swine models. Annals of Surgical Treatment Research. 94 (6), 285-290 (2018).
- Kwak, H. Y., et al. Thermal injury of the recurrent laryngeal nerve by THUNDERBEAT during thyroid surgery: findings from continuous intraoperative neuromonitoring in a porcine model. Journal of Surgical Research. 200 (1), 177-182 (2016).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten