Festphasen-Synthese
Überblick
Quelle: Vy M. Dong und Diane Le, Department of Chemistry, University of California, Irvine, CA
Merrifield Festphasen-Synthese ist ein Nobelpreis gewinnen Erfindung wo ein Edukt-Molekül ist auf einer festen Unterlage gebunden und erfährt aufeinander folgende chemische Reaktionen, um eine gewünschte Verbindung zu bilden. Wenn die Moleküle an einem festen Träger gebunden sind, können durch Waschen entfernt Verunreinigungen, während die Ziel-Verbindung an das Harz gebunden bleibt überschüssige Reagenzien und Nebenprodukte entfernt werden. Speziell, präsentieren wir ein Beispiel der Festphasen-Peptidsynthese (SPPS) um dieses Konzept zu demonstrieren.
Grundsätze
Festphasen-Synthese ist eine Methode verwendet, um die Synthese von Molekülen zu optimieren. Es wird oft in der kombinatorischen Chemie (eine Technik verwendet, um eine große Anzahl von Molekülen in kurzer Zeit vorbereiten) verwendet, um Bibliotheken zu erzeugen Verbindungen wegen der einfachen Reinigung und insgesamt chemische Synthese. Festphasen-Synthese beinhaltet in der Regel die Verwendung eines Harzes; ein nicht löslich, Polymer-basierten Material, welches pre-functionalized ist, so dass der Start Gebäude Blockcan leicht binden. Die Bausteine sind in der Regel geschützt, sobald sie auf das Harz hinzugefügt werden, und sie können leicht deprotected und behandelt mit dem nächsten gewünschten Baustein in Lösung (Abbildung 1). Sobald das gewünschte Molekül synthetisiert wurde, kann es leicht aus dem Harz gespalten.
Denn es robust ist, wurde Festphasen-Synthese zur Synthese von Nukleinsäuren, Oligosaccharide und am häufigsten Peptide. Entdeckt und im Jahre 1963 von Merrifield berichtet, ist SPPS die am häufigsten verwendete Methode zur Erzeugung Bibliotheken Peptide geworden. Merrifield gewann den Nobelpreis 1984 für die Erfindung der SPPS. SPPS profitieren einfach von Fmoc (Basis Sensitive) oder Boc (Säure empfindlich)N-Gruppen auf die Aminosäuren zum Aufbau von Bibliotheken von Peptiden in kürzester Zeit zu schützen. HBTU (Haftvermittler) und ich-Pr2EtN (Base) Aktivieren der C-Terminus der Aminosäure für die Kopplung mit einer anderen Aminosäure. Fmoc Gruppen schützen kann durch 4-Methylpiperidine, entfernt werden, während Boc Gruppen zu schützen durch starke Säuren wie Trifluoroacetic Säure entfernt werden kann. In diesem Experiment demonstrieren wir durch die Synthese von einem Dipeptid SPPS. Den Kaiser-Test, eine qualitative Methode, um auf das Vorhandensein von primären Aminen testen dient uns dazu, um den Fortschritt der Reaktion zu überwachen.
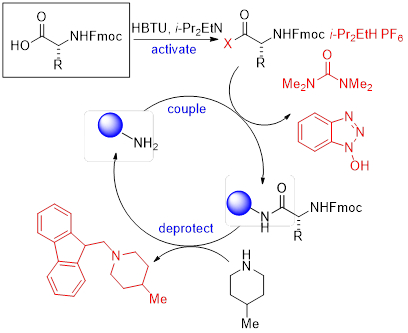
Abbildung 1. Konzept der Festphasen-Peptidsynthese (SPPS).
Verfahren
1. laden das Harz
- Ein 100mL Peptid-Synthese Schiff fügen Sie 2-Chlorotrityl-Chlorid (CTC) Harz (1,1 Mmol/g, 0,360 g, 0.400 Mmol hinzu). Geben Sie 20 mL DMF und es ihnen ermöglichen, für 30 min unter N Schwellen2.
- Abtropfen lassen Sie die Perlen unter Vakuum und 10 mL DMF.
- Fügen Sie 500 mg Fmoc-Ala-OH (1,60 Mmol) und 2,5 mL i -Pr2EtN und Mischung unter N2 für 15 Minuten.
- Das Lösungsmittel im Vakuum abgießen und die Beladung mit Fmoc-Ala-OH für 15 min wiederholen.
- Abtropfen lassen das Lösungsmittel im Vakuum und die Perlen mit 10 mL DMFunder N2waschen und abtropfen lassen unter Vakuum 3 X.
2. Deprotection der Fmoc-Gruppe
- 10 mL 20 % 4-Methylpiperidine in DMF und rühren Sie die Perlen unter N2 für 15 Minuten.
- Abtropfen Sie das Lösungsmittel im Vakuum und wiederholen Sie den Deprotection.
- Waschen Sie die Perlen mit 10 mL DMF unter N2 und Abfluss unter Vakuum 3 X.
(3) durchführen der Kaiser-Test
- Der Kaiser-Test durchgeführt werden durch Zugabe von 1 bis 2 Tropfen der Lösung A (0,5 mL 0,01 M KCN, 24,5 mL Pyridin), Lösung B (1 g Ninhydrin-, 20 mL n-Butanol), und C-Lösung (20 g Phenol, 10 mL n-Butanol) jeweils in zwei Reagenzgläser. Ein Reagenzglas wird das Steuerelement sein, während andererseits die Reaktion zu überwachen.
- Hinzu kommen ein paar Perlen des Harzes aus dem Reaktionsgefäß Reaktion Reagenzglas und erwärmen die zwei Reagenzgläser bis 110 ° C.
- Wenn die Deprotection abgeschlossen ist, schaltet sich der Inhalt des Reagenzglases eine dunkle blau/lila Farbe. Wenn die Deprotection unvollständig oder fehlerhaft ist, bleibt die Lösung gelb. Vergleichen Sie das Reaktionsgefäß Test mit Reagenzglas Kontrolle.
4. Kupplung die nächsten Bausteine
- Entleeren Sie das Lösungsmittel im Vakuum.
- Waschen Sie die Perlen mit 10 mL N-Methyl-2-pyrrolidon unter N2 und Abfluss das Lösungsmittel im Vakuum.
- Fügen Sie zunächst die nächsten Kupplung auf 10 mL NMP, 620 MgFmoc-Phe-OH (1,6 Mmol), 610 mg HBTU (1,6 Mmol) und 2,5 mLi -Pr2EtN, und lassen Sie das Harz unter N2 für 30 min Blasen wirft.
- Entleeren Sie das Lösungsmittel im Vakuum.
- Waschen Sie die Perlen mit 10 mL DMF unter N2 und Abfluss unter Vakuum 3 X.
- Führen Sie den Kaiser testen (siehe Schritte 3.1-3.3), um die Fertigstellung der Kupplung zu suchen. Die Perlen und die Lösung im Reagenzglas sollte gelb sein.
(5) Spalten das Peptid aus dem Harz
- Die restlichen Fmoc-Gruppe mit Schritte 2.1-2.3 zu Spalten.
- Nachdem das Lösungsmittel im Vakuum abgelassen wird, fügen Sie 40 mL-Dekolleté-Lösung (95 % TFA, 2,5 % H2O, 2,5 % Tipps hinzu), Harz und Blase unter N2 für 3 h.
- Legen Sie eine neue Auffangkolben auf der Peptid-Synthesizer und drain TheTFA Lösung, die das gewünschte Peptid unter Vakuum in die neue Flasche enthält.
(6) Niederschlag und ich spendet des Peptids
- Trennen Sie die TFA-Lösung in 4 konische Fläschchen und jedes Fläschchen, das Peptid auszufällen fügen Sie 25 mL kalten Äther (−20 ° C hinzu).
- Zentrifugieren Sie die Fläschchen (3.000 u/min, 0-4 ° C) für 20 min. Dekantieren die restliche TFA und Äther-Lösung aus der konischen Vials und konzentrieren den Peptid-Niederschlag um die gewünschte Dipeptid als weißer Feststoff zu leisten.
Ergebnisse
Repräsentative Ergebnisse für Festphasen-Peptid-Synthesisfor Verfahren 3.
| Prozedurschritt | Farbe der Lösung |
| 3.1 | Steuern - klar, hellgelb Reaktion – klar, hellgelb |
| 3.2 | Steuern - klar, hellgelb Reaktion – dunkelblau |
| 3.3 | Dunkel blaue Lösung, Perlen blau – komplette Deprotection oder Kupplung gescheitert Farblos, Perlen gelb – Deprotection ist fehlgeschlagen oder vollständig ausfüllen Farblose Lösung Perlen rot – unvollständig Kupplung oder unvollständige Deprotection |
Tabelle 1. Vertreter ergibt sich für Procedu 3.
Anwendung und Zusammenfassung
In diesem Experiment haben wir ein Beispiel der Festphasen-Synthese über SPPS durch die Synthese von einem Dipeptid gezeigt.
Festphasen-Synthese ist in der kombinatorischen Chemie verbreitet, Bibliotheken von Verbindungen für schnelle Screening aufzubauen. Es ist allgemein verwendet, Peptide, Oligosaccharide und Nukleinsäuren zu synthetisieren. Darüber hinaus wurde dieses Konzept in der chemischen Synthese umgesetzt. Weil es heterogen ist, können in nachfolgenden Reaktionen diesen Volumenkörper unterstützt Reagenzien oft recycelt und wiederverwendet werden.
pringen zu...
Videos aus dieser Sammlung:

Now Playing
Festphasen-Synthese
Organic Chemistry II
41.3K Ansichten

Reinigung der Glaswaren
Organic Chemistry II
123.9K Ansichten

Nucelophile Substitution
Organic Chemistry II
99.6K Ansichten

Reduktionsmittel
Organic Chemistry II
43.2K Ansichten

Grignard-Reaktion
Organic Chemistry II
149.3K Ansichten

n- Butyllithium Titration
Organic Chemistry II
48.1K Ansichten

Dean-Stark-Falle
Organic Chemistry II
100.7K Ansichten

Ozonolyse von Alkenen
Organic Chemistry II
67.2K Ansichten

Organokatalyse
Organic Chemistry II
17.0K Ansichten

Palladiumkatalysierte Kreuzkupplungsreaktionen
Organic Chemistry II
34.7K Ansichten

Hydrierung
Organic Chemistry II
49.7K Ansichten

Polymerisation
Organic Chemistry II
94.9K Ansichten

Schmelzpunkt
Organic Chemistry II
150.1K Ansichten

Infrarot-Spektroskopie
Organic Chemistry II
216.2K Ansichten

Polarimeter
Organic Chemistry II
100.3K Ansichten
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten