Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Aislamiento y cultivo de células troncales de la cresta neural de los folículos del cabello humano
En este artículo
Resumen
En este artículo se presenta un robusto protocolo para el aislamiento y cultivo de células de la cresta neural madre de folículos pilosos humanos.
Resumen
Los folículos pilosos experimentan un crecimiento durante toda la vida y el ciclo del cabello es un proceso bien controlado que implica proliferación de células madre y la quiescencia. Bulto del pelo es un nicho bien caracterizado para las células madre adultas 1. Este segmento de la vaina radicular externa contiene un número de tipos diferentes de células madre, incluyendo células madre epiteliales, células melanocitos 2 madre 3 y de la cresta neural como las células madre 4-7. Los folículos pilosos son una fuente rica y accesible para los diferentes tipos de células madre humanas. Nosotros y otros han aislado células madre de la cresta neural (CTCN) de folículos pilosos humanos fetales y adultos 4,5. Estas células madre humanas son la etiqueta de retención de células y son capaces de auto-renovación a través de la división celular asimétrica in vitro. Ellos expresan marcadores neuronales inmaduras de células de la cresta, pero no marcadores de diferenciación. Nuestro estudio demostró que la expresión de perfiles que comparten un patrón de expresión génica similar con murino piel inmadura CRE neuralcélulas ST. Exhiben multipotencia clonal que puede dar lugar a linajes de células miogénicas, melanocíticos, y después neuronal en clonal in vitro de cultivo celular solo. Las células diferenciadas no sólo adquirir linaje marcadores específicos, sino también demostrar las funciones adecuadas en condiciones ex vivo. Además, estos CTCN mostrar potencial de diferenciación hacia linajes mesenquimales. Células neuronales diferenciadas pueden persistir en cerebro de ratón y retener marcadores neuronales de diferenciación. Se ha demostrado que el pelo del folículo derivado CTCN puede ayudar a la regeneración del nervio, y mejorar la función motora en los ratones trasplantados con estas células madre después de una lesión transección de la médula espinal 8. Además, los nervios periféricos han sido reparados con injertos de células madre 9, y la implantación de las células precursoras derivadas de la piel adyacentes a aplastadas nervios ciáticos se ha traducido en la remielinización 10. Por lo tanto, los folículos pilosos / piel CTCN derivados ya han mostrado resultados prometedores para regenerative terapia en modelos preclínicos.
Reprogramación de células somáticas a madre pluripotentes inducidas (iPS) de células ha demostrado un enorme potencial para la medicina regenerativa. Sin embargo, existen todavía muchos problemas con las células iPS, en particular el efecto a largo plazo de la integración oncogén / virus y tumorigenicidad potencial de las células madre pluripotentes no han sido adecuadamente tratadas. Todavía hay muchos obstáculos que superar antes de que las células iPS pueden utilizarse para la medicina regenerativa. Mientras que las células madre adultas se sabe que son seguros y que se han usado clínicamente durante muchos años, tales como trasplante de médula ósea. Muchos pacientes se han beneficiado ya del tratamiento. Autólogo de células madre adultas son todavía células preferidas para el trasplante. Por lo tanto, las células adultas y de fácil acceso expandible madre en la piel humana / folículos pilosos son una valiosa fuente para la medicina regenerativa.
Protocolo
1. Preparación de placas de cultivo tisular
- Escudo cada pocillo con suficiente poli-D-lisina (PDL) para cubrir el fondo del pozo. Dejar que las placas secar en la campana.
- Después de que los pozos están secos, enjuague con agua estéril y aspirar. Dejar que las placas secar en la campana.
- Cuando capa seca, con fibronectina (que se disolvió en agua BioWhittaker noche a 37 º C a una concentración de 1 mg en 6 ml).
- Añadir medio NCSC [95 ml de DMEM/F12, 1 ml Penn / Strep (P / S), 1 ml N2, 2 ml B27, 100 l mercaptoetanol (2ME; 50 mM de existencias), bFGF (20 ng / ml de medio), IGF -1 (20 ng / ml de medio) y EGF (20 ng / ml de medio)] antes de fibronectina seco en las placas,
2. Extraer células del folículo piloso del cuero cabelludo humano
- Antes de iniciar el procedimiento de CTCN aislamiento, es necesario preparar las medias respectivas y reactivos (véase la Tabla 1).
- Fresh piel de un adulto humano cuero cabelludo de los procedimientos de cirugía estética o FeTal tejido del cuero cabelludo se recogió, se lavó con PBS que contenía penicilina-estreptomicina.
- La piel entonces se transfiere en tubos de 50 ml y se incubaron en DMEM con Dispasa (10 mg / ml) durante la noche a 4 ° C. La incubación durante 2-4 horas a 37 ° C es también eficaz. Trozos de piel debe ser de una anchura máxima de 1 cm para permitir la enzima de penetrar.
- Transferencia de la piel en una placa de Petri esterilizada; salga de cada pelo de la piel, sujetando el eje del cabello cerca de la superficie de la piel y tirando firmemente y sin problemas. Los folículos pilosos muestran la morfología de cualquiera anágena (Figura 1A) o telógena (Figura 1B).
- Incubar los fragmentos folículo aislado en 0,05% de tripsina-EDTA (Invitrogen) durante 15-20 minutos a temperatura ambiente con agitación periódica, añadir 4 ml de DMEM con FBS al 10% para detener la reacción. El epitelio folicular se tripsinizaron y se filtró a través de filtro de 40 micras para obtener una suspensión de una sola célula que contiene células de diferente tamaño y forma.
- Girara 200 xg durante 5 min, eliminar el sobrenadante cuidadosamente, volver a suspender en 1 ml de PBS que contenía 2% de suero (FBS).
- Alternativamente, desplumados folículos pilosos pueden ser colocados en cultivo sin digestión con tripsina para crecer esferas de pelo in situ.
3. Aislamiento de CTCN folículo piloso Uso de Ordenación Celda de flujo citométrico
- Único folículo piloso suspensión de células se obtuvieron por digestión con tripsina y se marcaron con anticuerpos contra CD271 (APC conjugado) / HNK1 (conjugado a FITC) o CD271 / integrina alfa4 (conjugado con PE) durante 40 min en hielo en la oscuridad.
- Centrifugar durante 5 min a 200 xg, a temperatura ambiente y aspirar el sobrenadante.
- Resuspender las células en PBS que contenía 2% de suero (FBS), y antes de la clasificación, PI se añade a la puerta de las células muertas.
- Realizar la clasificación de células por citometría de flujo (FACS). Recoger CD271 +, + HNK1 células doble positivas o CD271 +, integrina alfa 4 + células doble positivas (Figura 2).
- Después de claseción, CD271 +, + HNK1 células doble positivas o CD271 +, la integrina alfa 4 + células positivas dobles se cultivaron en placas de fijación ultra-bajos en el medio NCSC
4. Cultura de CTCN Primaria
- Cultivar las células foliculares disociadas o FACS ordenados células en placas de fijación ultra-bajos en el medio NCSC, cambie medio todos los días.
- Compruebe cultivo celular todos los días bajo el microscopio. CTCN se empieza a formar pequeños agregados flotantes después de varios días y bien formadas esferas en 2-5 semanas en el cultivo dependiendo de la edad de los donantes (Figura 3A). Crecimiento Externo aparecerá en unos días en la región del bulbo y bien formados esferas in situ en varias semanas (Figura 3B) cuando los folículos pilosos se enteras cultivadas en el medio NCSC.
5. La expansión de CTCN
- Lavar las células una vez con PBS.
- Añadir precalentado (a 37 ° C, crítico) Accutase e incubar a 37 ° C durante 5-10min con agitación periódica para asegurarse de esferas de células madre neuronales disocia en células individuales (por NCSC fijación cultivadas, las células se incuban con Accutase a 37 ° C durante 5 min para asegurarse de que células madre del folículo del pelo desprendido).
- Lavar y centrifugar las células dos veces durante 5 min a 200 xg, a temperatura ambiente en medio DMEM/F12 para eliminar cualquier solución Accutase restante.
- Vuelva a suspender las células con medio de cultivo NCSC.
- Para el cultivo flotante, poner las células en placas de fijación ultra-bajas. Para el cultivo de apego, puesto que las células pretratadas en placas de cultivo de tejidos.
6. Los resultados representativos
Medio NCSC cultivo es suficiente para mantener hNCSCs en un estado indiferenciado sin la necesidad de células alimentadoras. Los queratinocitos no proliferan y gradualmente murió en el medio. Ciertas células redondas pequeñas se proliferan y forman agregados pequeños en suspensión después de 3 a 5 días. Estos agregados flotantes aumentó lentamente itamaño n, generados en tres dimensiones como estructuras de esfera, que denominamos esferas de cabello (Figura 3A). Si cultivaron en placas recubiertas, las CTCN se adhieren a la superficie y no forma ningún esferas. Los CTCN conectados crecen más rápido que en suspensión. Las células madre que forman la esfera-o adjunto expresan marcadores CTCN. Cuando los folículos pilosos son enteros culturas, las esferas se forman en el área correspondiente a la región protuberancia (Figura 3B).
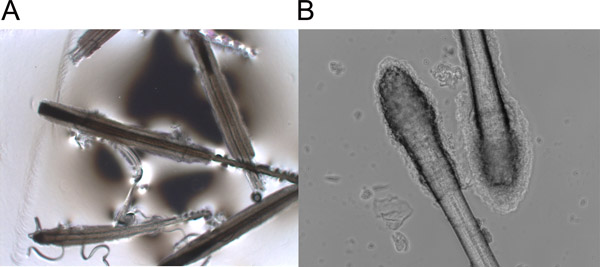
Figura 1. Desplumados anágena (A) y telógena (B) folículos pilosos.
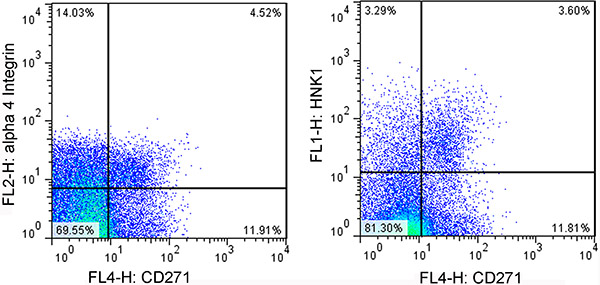
Figura 2. Imágenes representativas de análisis FACS de CTCN panel izquierdo:. Células son gated usando anticuerpos anti-CD271 y anti alphe-4 integrina anticuerpos. Panel derecho: las células están cerradas utilizando anticuerpos anti-CD271 y anti-HNK1.

Figura 3. Morfología de las esferas de pelo (A) Morfología de esferas flotantes de pelo, panel izquierdo:. Baja energía, panel de la derecha:. Alta potencia (B) Morfología de la esfera de pelo in situ en la región protuberancia, panel izquierdo: una esfera de pelo en bulto telógeno, panel de la derecha: una esfera pelo en la región bulto de un folículo de cabello anágeno.
Discusión
Los métodos de aislamiento de células y cultivo descritos son reproducible y robusto. Hemos generado CTCN de docenas de individuos a través de un amplio rango de edades. Aunque es mejor para procesar el tejido justo después de la cosecha de tejidos, se encontró que los tejidos del cuero cabelludo puede ser almacenado de forma segura en los medios de comunicación sobre hielo para el transporte durante la noche con un impacto mínimo sobre la viabilidad celular.
Es importante tratar el t...
Divulgaciones
No tenemos nada que revelar.
Agradecimientos
Este trabajo es apoyado por el NIH subvención R01AR054593 y R01AR054593-S1 a Xu.
Materiales
| Name | Company | Catalog Number | Comments |
| DMEM | Invitrogen | 11965-092 | |
| DMEM/F12 | Invitrogen | 11330-32 | |
| Heat-inactivated FBS | Hyclone | SH30071.03 | |
| B27 supplement | Invitrogen | 17504044 | |
| N2 supplement | Invitrogen | 17502048 | |
| bFGF | Invitrogen | PHG0026 | |
| EGF | R&D system | 236-EG-01M | |
| IGF-I | R&D system | 291-G1-050 | |
| 0.05% Trypsin/EDTA | Invitrogen | 25300-054 | |
| Dispase | Invitrogen | 17105041 | |
| Penicillin-Streptomycin | Invitrogen | 15070063 | |
Table 1. | |||
Referencias
- Cotsarelis, G., Cheng, S. Z., Dong, G., Sun, T. T., Lavker, R. M. Existence of slow-cycling limbal epithelial basal cells that can be preferentially stimulated to proliferate: implications on epithelial stem cells. Cell. 57, 201-209 (1989).
- Cotsarelis, G., Sun, T. T., Lavker, R. M. Label-retaining cells reside in the bulge area of pilosebaceous unit: implications for follicular stem cells, hair cycle, and skin carcinogenesis. Cell. 61, 1329-1337 (1990).
- Tanimura, S., et al. Hair follicle stem cells provide a functional niche for melanocyte stem cells. Cell Stem Cell. 8, 177-187 (2011).
- Yu, H., et al. Isolation of a novel population of multipotent adult stem cells from human hair follicles. Am. J. Pathol. 168, 1879-1888 (2006).
- Yu, H., Kumar, S. M., Kossenkov, A. V., Showe, L., Xu, X. Stem cells with neural crest characteristics derived from the bulge region of cultured human hair follicles. J. Invest. Dermatol. 130, 1227-1236 (2010).
- Wong, C. E., et al. Neural crest-derived cells with stem cell features can be traced back to multiple lineages in the adult skin. J. Cell Biol. 175, 1005-1015 (2006).
- Sieber-Blum, M., Grim, M., Hu, Y. F., Szeder, V. Pluripotent neural crest stem cells in the adult hair follicle. Dev. Dyn. 231, 258-269 (2004).
- Amoh, Y., et al. Implanted hair follicle stem cells form Schwann cells that support repair of severed peripheral nerves. Proc. Natl. Acad. Sci. U.S.A. 102, 17734-17738 (2005).
- Koliatsos, V. E., Xu, L., Yan, J. Human stem cell grafts as therapies for motor neuron disease. Expert Opin. Biol. Ther. 8, 137-141 (2008).
- McKenzie, I. A., Biernaskie, J., Toma, J. G., Midha, R., Miller, F. D. Skin-derived precursors generate myelinating Schwann cells for the injured and dysmyelinated nervous system. J. Neurosci. 26, 6651-6660 (2006).
- LeDouarin, N. M., Kalcheim, C. . The Neural Crest. , (1999).
- Tumbar, T., et al. Defining the epithelial stem cell niche in skin. Science. 303, 359-363 (2004).
- Roh, C., et al. Multi-potentiality of a new immortalized epithelial stem cell line derived from human hair follicles. In Vitro Cell Dev. Biol. Anim. 44, 236-244 (2008).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados