È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
L'isolamento e la coltura di cellule staminali neurali Crest di follicoli dei capelli umani
In questo articolo
Riepilogo
Questo articolo presenta un protocollo robusto per l'isolamento e la coltura di cellule staminali neurali cresta di follicoli dei capelli umani.
Abstract
Follicoli dei capelli sottoposti a crescita continua e ciclo del capello è un ben controllato processo che coinvolge la proliferazione delle cellule staminali e della quiete. Rigonfiamento dei capelli è una nicchia ben caratterizzato per le cellule staminali adulte 1. Questo segmento della guaina esterna della radice contiene un certo numero di diversi tipi di cellule staminali, comprese le cellule staminali epiteliali 2, cellule staminali melanociti 3 e cresta neurale come cellule staminali 4-7. Follicoli dei capelli rappresentano una fonte accessibile e ricco per i diversi tipi di cellule staminali umane. Noi e gli altri hanno isolato le cellule staminali neurali cresta (NCSCs) di follicoli piliferi umani fetali e adulti 4,5. Queste cellule staminali umane sono etichette-cellule di sostegno e sono in grado di auto-rinnovamento attraverso la divisione cellulare asimmetrica in vitro. Esprimono immaturi marcatori di cellule neurali della cresta, ma non marcatori di differenziazione. Il nostro studio dei profili di espressione hanno dimostrato di condividere un simile pattern di espressione genica con la pelle di topo immaturo neurale crest cellule. Essi mostrano multipotenza clonale che possono dare origine a linee cellulari miogeniche, melanocitari e neuronale dopo coltura in vitro clonale singola cella. Le cellule differenziate non solo acquisire lineage-specifici marcatori, ma anche dimostrare funzioni appropriate in condizioni ex vivo. Inoltre, questi NCSCs mostrano il potenziale di differenziazione verso linee mesenchimali. Differenziati cellule neuronali possono persistere nel cervello di topo e mantenere marcatori del differenziamento neuronale. E 'stato dimostrato che follicolo pilifero derivato NCSCs può aiutare la ricrescita dei nervi, e migliorare la funzione motoria nei topi trapiantati con queste cellule staminali seguendo sezionare lesione spinale 8. Inoltre, i nervi periferici sono state riparate con innesti di cellule staminali 9, e l'impianto di pelle cellule derivate da precursori adiacenti schiacciato nervo sciatico ha portato a rimielinizzazione 10. Pertanto, i follicolo / pelle NCSCs capelli derivati hanno già mostrato risultati promettenti per rLa terapia egenerative in modelli preclinici.
Riprogrammazione di cellule somatiche di staminali pluripotenti indotte (iPS), le cellule hanno mostrato un enorme potenziale per la medicina rigenerativa. Tuttavia, ci sono ancora molti problemi con le cellule iPS, in particolare l'effetto a lungo termine di oncogene / virus integrazione e tumorigenicità potenziale delle cellule staminali pluripotenti non sono stati adeguatamente affrontati. Ci sono ancora molti ostacoli da superare prima che le cellule iPS possono essere utilizzati per la medicina rigenerativa. Considerando che le cellule staminali sono noti per essere sicuri e sono stati utilizzati clinicamente per molti anni, come trapianto di midollo osseo. Molti pazienti hanno già beneficiato del trattamento. Autologhe cellule staminali adulte sono cellule ancora preferite per il trapianto. Pertanto, le facilmente accessibili ed espandibile cellule staminali adulte in pelle umana / follicoli piliferi sono una fonte preziosa per la medicina rigenerativa.
Protocollo
1. Preparazione delle piastre di coltura dei tessuti
- Coat ogni pozzetto con sufficiente poli-D-lisina (PDL) per coprire il fondo del pozzo. Lasciare le piastre ad asciugare nella cappa.
- Dopo che i pozzi sono asciutti, risciacquare con acqua sterile, e aspirare. Lasciare le piastre ad asciugare nella cappa.
- Quando asciutto, cappotto con fibronectina (che è stato disciolto in acqua BioWhittaker notte a 37 ° C ad una concentrazione di 1 mg in 6 ml).
- Aggiungere mezzo NCSC [95 ml DMEM/F12, 1 ml Penn / Strep (P / S), 1 ml N2, 2 ml B27, 100 microlitri mercaptoetanolo (2ME, 50 magazzino mM), bFGF (20 ng / ml di media), IGF -1 (20 ng / ml di mezzo) e EGF (20 ng / ml di mezzo)] prima fibronectina secco nelle piastre,
2. Estrarre cellule del follicolo dei capelli dal cuoio capelluto umano
- Prima di iniziare la procedura di NCSCs isolanti, bisogna preparare i rispettivi medias e reagenti (vedi Tabella 1).
- Fresco di un adulto cuoio capelluto umano dalle procedure di ringiovanimento del viso o feTal tessuto cuoio capelluto viene raccolto, lavato con PBS contenente penicillina-streptomicina.
- La pelle viene quindi trasferito in provette da 50 ml e incubate in DMEM con dispasi (10 mg / ml) per una notte a 4 ° C. Incubazione per 2-4 ore a 37 ° C è anche efficace. Pezzi della pelle dovrebbe essere una larghezza massima di 1 cm per consentire l'enzima di penetrare.
- Trasferire la pelle in una piastra Petri sterile; togliere ogni capelli dalla pelle afferrando l'albero dei capelli vicino alla superficie della pelle e tirando con forza e senza intoppi. I follicoli piliferi mostrano morfologia sia anagen (Figura 1A) o telogen (Figura 1B).
- Incubare i frammenti isolati nel follicolo 0,05% tripsina-EDTA (Invitrogen) per 15-20 minuti a temperatura ambiente con agitazione periodicamente, aggiungere 4 ml di DMEM con 10% FBS per arrestare la reazione. L'epitelio follicolare è tripsinizzate e filtrata attraverso filtro 40 micron per ottenere una cella singola sospensione contenente cellule di varie dimensioni e forma.
- Girarea 200 xg per 5 minuti, il surnatante con cura, risospendere in 1 ml di PBS contenente 2% di siero (FBS).
- In alternativa, follicoli piliferi pizzicate possono essere posti in coltura senza digestione con tripsina per crescere sfere capelli in situ.
3. Isolamento di NCSCs follicolo pilifero mediante cell sorting citometria a flusso
- Follicolo cella singola sospensione sono stati ottenuti dalla digestione con tripsina e marcate con anticorpi anti CD271 (APC-coniugato) / HNK1 (FITC-coniugato) o CD271 / integrina alfa4 (PE-coniugato) per 40 min in ghiaccio, al buio.
- Centrifugare per 5 minuti a 200 xg a temperatura ambiente e aspirare il surnatante.
- Risospendere le cellule in PBS contenente 2% di siero (FBS), e prima della cernita, PI viene aggiunto per escludere le cellule morte.
- Effettuare selezione cellulare mediante citometria a flusso (FACS). Raccogliere CD271 +, HNK1 + cellule doppie positive o CD271 +, alfa4 integrina + cellule doppio positive (Figura 2).
- Dopo sortavoce, CD271 +, HNK1 + cellule doppie positive o CD271 +, alfa4 integrina + cellule doppie positive sono coltivate in ultra-basso piastre di fissaggio nel medio NCSC
4. Cultura della NCSCs primarie
- Cultura delle cellule follicolari dissociate o FACS ordinati cellule in ultra-low piastre di fissaggio nel mezzo NCSC, cambiare mezzo ogni giorno.
- Controllare coltura cellulare ogni giorno al microscopio. NCSCs inizierà a formare piccoli aggregati galleggianti dopo diversi giorni e ben formate sfere in 2-5 settimane in coltura in funzione dell'età dei donatori (Figura 3A). Conseguenza apparirà in un paio di giorni in corrispondenza della zona rigonfiamento e ben formati sfere in situ in diverse settimane (Figura 3B) quando i follicoli piliferi intere sono coltivate in mezzo NCSC.
5. Ampliamento della NCSCs
- Lavare le cellule una volta con PBS.
- Aggiungere pre-riscaldata (a 37 ° C, critica) accutase e incubare a 37 ° C per 5-10min con agitazione periodicamente per assicurarsi che le sfere di cellule staminali neurali dissociato in singola cella (per NCSC allegato colto, incubare le cellule con accutase a 37 ° C per 5 minuti per assicurarsi che le cellule staminali dei follicoli piliferi a schiera).
- Lavare le cellule due volte e centrifugare per 5 min a 200 xg a temperatura ambiente in mezzo DMEM/F12 per rimuovere qualsiasi residuo della soluzione accutase.
- Risospendere le cellule con terreno di coltura NCSC.
- Per la cultura galleggiante, mettere le cellule in ultra-low piastre di fissaggio. Per la cultura attaccamento, mettere le cellule in piastre pretrattate coltura di tessuti.
6. Risultati rappresentativi
Mezzo di coltura NCSC è sufficiente a mantenere hNCSCs in uno stato indifferenziato senza la necessità di cellule feeder. Cheratinociti non proliferano e gradualmente morì nel mezzo. Alcune piccole cellule rotonde proliferare e formare piccoli aggregati in sospensione dopo 3 a 5 giorni. Tali aggregati galleggianti lentamente aumentato in dimensioni, generati sfera tridimensionale strutture simili, che abbiamo chiamato sfere capelli (Figura 3A). Se coltivate in piastre rivestite, le NCSCs si attaccano alla superficie e non costituiscono alcun sfere. Le NCSCs allegati crescere più velocemente in sospensione. Le cellule staminali di formazione di sfere o fissati esprimono marcatori NCSCs. Quando i follicoli piliferi sono intere culture, sfere si formano alla superficie corrispondente alla regione di rigonfiamento (Figura 3B).
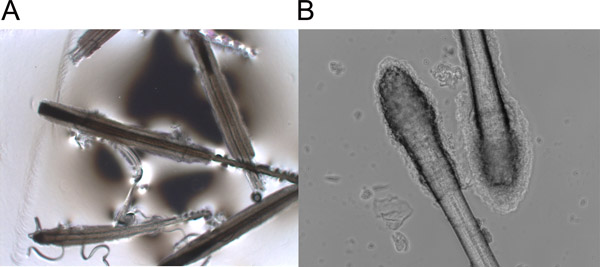
Figura 1. Pizzicate anagen (A) e telogen (B) follicoli piliferi.
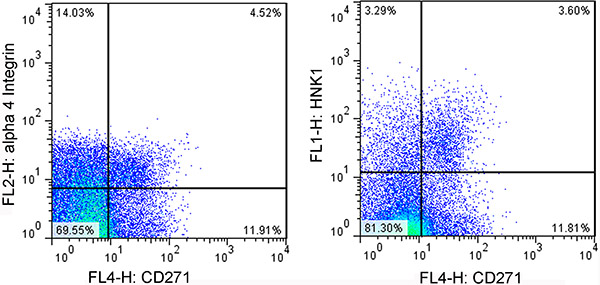
Figura 2. Immagini rappresentative della analisi FACS di NCSCs pannello sinistro.: Le cellule sono gated utilizzando anticorpi anti-CD271 e anti-alphe quattro anticorpi integrine. Pannello di destra: le cellule sono gated utilizzando anticorpi anti-CD271 e anti-HNK1.

Figura 3. Morfologia di sfere capelli (A) Morfologia di sfere galleggianti capelli, pannello di sinistra:. Bassa potenza, pannello di destra:. Alta potenza (B) Morfologia della sfera capelli in situ in corrispondenza della zona rigonfiamento, pannello di sinistra: una sfera di capelli a rigonfiamento telogen, pannello di destra: una sfera di capelli nella regione rigonfiamento di un follicolo pilifero anagen.
Discussione
I metodi di isolamento e la coltura di cellule di cui sono riproducibili e robusti. Abbiamo generato NCSCs da decine di persone in una vasta gamma di età. Anche se è meglio per elaborare il tessuto subito dopo la raccolta del tessuto, abbiamo scoperto che i tessuti del cuoio capelluto può essere immagazzinato in modo sicuro nei media sul ghiaccio per il trasporto durante la notte con un impatto minimo sulla vitalità cellulare.
È importante per trattare il tessuto cuoio capelluto con ant...
Divulgazioni
Non abbiamo nulla da rivelare.
Riconoscimenti
Questo lavoro è sostenuto da NIH sovvenzione R01AR054593 e R01AR054593-S1 a Xu.
Materiali
| Name | Company | Catalog Number | Comments |
| DMEM | Invitrogen | 11965-092 | |
| DMEM/F12 | Invitrogen | 11330-32 | |
| Heat-inactivated FBS | Hyclone | SH30071.03 | |
| B27 supplement | Invitrogen | 17504044 | |
| N2 supplement | Invitrogen | 17502048 | |
| bFGF | Invitrogen | PHG0026 | |
| EGF | R&D system | 236-EG-01M | |
| IGF-I | R&D system | 291-G1-050 | |
| 0.05% Trypsin/EDTA | Invitrogen | 25300-054 | |
| Dispase | Invitrogen | 17105041 | |
| Penicillin-Streptomycin | Invitrogen | 15070063 | |
Table 1. | |||
Riferimenti
- Cotsarelis, G., Cheng, S. Z., Dong, G., Sun, T. T., Lavker, R. M. Existence of slow-cycling limbal epithelial basal cells that can be preferentially stimulated to proliferate: implications on epithelial stem cells. Cell. 57, 201-209 (1989).
- Cotsarelis, G., Sun, T. T., Lavker, R. M. Label-retaining cells reside in the bulge area of pilosebaceous unit: implications for follicular stem cells, hair cycle, and skin carcinogenesis. Cell. 61, 1329-1337 (1990).
- Tanimura, S., et al. Hair follicle stem cells provide a functional niche for melanocyte stem cells. Cell Stem Cell. 8, 177-187 (2011).
- Yu, H., et al. Isolation of a novel population of multipotent adult stem cells from human hair follicles. Am. J. Pathol. 168, 1879-1888 (2006).
- Yu, H., Kumar, S. M., Kossenkov, A. V., Showe, L., Xu, X. Stem cells with neural crest characteristics derived from the bulge region of cultured human hair follicles. J. Invest. Dermatol. 130, 1227-1236 (2010).
- Wong, C. E., et al. Neural crest-derived cells with stem cell features can be traced back to multiple lineages in the adult skin. J. Cell Biol. 175, 1005-1015 (2006).
- Sieber-Blum, M., Grim, M., Hu, Y. F., Szeder, V. Pluripotent neural crest stem cells in the adult hair follicle. Dev. Dyn. 231, 258-269 (2004).
- Amoh, Y., et al. Implanted hair follicle stem cells form Schwann cells that support repair of severed peripheral nerves. Proc. Natl. Acad. Sci. U.S.A. 102, 17734-17738 (2005).
- Koliatsos, V. E., Xu, L., Yan, J. Human stem cell grafts as therapies for motor neuron disease. Expert Opin. Biol. Ther. 8, 137-141 (2008).
- McKenzie, I. A., Biernaskie, J., Toma, J. G., Midha, R., Miller, F. D. Skin-derived precursors generate myelinating Schwann cells for the injured and dysmyelinated nervous system. J. Neurosci. 26, 6651-6660 (2006).
- LeDouarin, N. M., Kalcheim, C. . The Neural Crest. , (1999).
- Tumbar, T., et al. Defining the epithelial stem cell niche in skin. Science. 303, 359-363 (2004).
- Roh, C., et al. Multi-potentiality of a new immortalized epithelial stem cell line derived from human hair follicles. In Vitro Cell Dev. Biol. Anim. 44, 236-244 (2008).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon