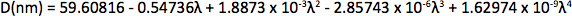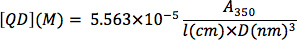Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Compact Puntos Cuánticos for Imaging sola molécula
En este artículo
Resumen
Se describe la preparación de puntos cuánticos coloidales con un tamaño minimizado hidrodinámico para imágenes de fluorescencia de una sola molécula. En comparación con los puntos cuánticos, estas nanopartículas son similares en tamaño a las proteínas globulares y están optimizados para el brillo de una sola molécula, la estabilidad contra la fotodegradación, y la resistencia a la unión no específica a proteínas y células.
Resumen
Una sola molécula de imágenes es una herramienta importante para la comprensión de los mecanismos de la función biomolecular y para la visualización de la heterogeneidad espacial y temporal de los comportamientos moleculares que subyacen a la biología celular 1-4. Para la imagen de una molécula individual de interés, que se conjuga típicamente a una etiqueta fluorescente (tinte, proteína, perla o punto cuántico) y se observaron con epifluorescencia o de reflexión interna total de fluorescencia (TIRF) microscopía. Aunque los tintes y las proteínas fluorescentes han sido el pilar de imágenes de fluorescencia durante décadas, su fluorescencia es inestable bajo altos flujos de fotones necesarios para observar las moléculas individuales, produciendo sólo unos pocos segundos de observación antes de la pérdida completa de la señal. Perlas de látex y perlas marcada con colorante de proporcionar una mayor estabilidad de la señal, pero a expensas de tamaño hidrodinámico drásticamente más grande, que puede alterar perjudicialmente a la difusión y el comportamiento de la molécula en estudio. ntent "> Los puntos cuánticos (QDs) ofrecen un equilibrio entre estos dos regímenes problemáticos. Estas nanopartículas están compuestas de materiales semiconductores y pueden ser diseñados con un tamaño compacto hidrodinámicamente con una excepcional resistencia a la fotodegradación 5. Por tanto, en años recientes los puntos cuánticos han sido instrumentales en que permite observación a largo plazo del comportamiento complejo macromolecular en el nivel de moléculas individuales. Sin embargo estas partículas han todavía ha encontrado que exhiben deterioro de la difusión en ambientes de hacinamiento molecular, tales como el citoplasma celular y la hendidura sináptica neuronal, donde sus tamaños son todavía demasiado grandes 4,6 , 7.
Recientemente hemos diseñado los núcleos y revestimientos de superficies de puntos cuánticos para el tamaño minimizado hidrodinámico, mientras que equilibrar las compensaciones a la estabilidad coloidal, fotoestabilidad, el brillo, y de unión no específicos que han obstaculizado la utilidad de QDs compactos en el pasado 8,9. El objetivo de este artículo es demostrarla síntesis, la modificación, y la caracterización de estos nanocristales optimizados, compuesto de una aleación Cd Hg x 1-x núcleo Se recubierta con un aislante Zn Cd y 1-y shell S, recubierto adicionalmente con un ligando multidentado polímero modificado con polietilenglicol corto ( cadenas PEG) (Figura 1). En comparación con los nanocristales de CdSe convencionales, Hg x CD 1-x aleaciones de Se ofrecen mayores rendimientos cuánticos de fluorescencia, fluorescencia a longitudes de onda roja e infrarroja cercana para una mejor relación señal-ruido en las células, y la excitación a no citotóxicas longitudes de onda visibles. Multidentados revestimientos de polímero se unen a la superficie de nanocristales en una conformación cerrada y plana para minimizar el tamaño hidrodinámico, y PEG neutraliza la carga de la superficie para minimizar la unión no específica a las células y biomoléculas. El resultado final es un brillante fluorescente nanocristales con emisión entre 550-800 nm y un tamaño hidrodinámico total de cerca de 12 nm. Esto es en el sAME intervalo de tamaño como muchas proteínas solubles globulares en células, y sustancialmente más pequeños que los convencionales de puntos cuánticos PEGilados (25-35 nm).
Protocolo
Los procedimientos de síntesis siguientes implican estándar sin aire técnicas y el uso de un vacío / colector de gas inerte; metodología detallada se puede encontrar en las referencias 10 y 11. MSDS para todas las sustancias potencialmente tóxicas e inflamables deben ser consultados antes de su uso y compuestos inflamables todo y / o aire-lábil debe alícuotas en viales sellados septo en una caja de guantes o bolsa de guantes.
1. Síntesis de seleniuro de cadmio mercurio (Hg Cd x 1-x Se) Quantum Dot Cores
- Preparar una solución 0,4 M de selenio en trioctilfosfina (TOP). Añadir selenio (0,316 g, 4 mmol) a una 50 ml de 3 bocas, a continuación, evacuar y llenar con argón mediante una línea de Schlenk. Bajo condiciones libres de aire (nitrógeno seco o argón), añadir 10 ml de TOP y calor a 100 ° C mientras se agita durante 1 h para dar una solución clara, incolora. Enfriar la solución a temperatura ambiente y ajustar el matraz a un lado.
- Para una 250 ml de 3 bocas, añadir óxido de cadmio (CdO 0,0770 g, 0,6 mmol), ácido tetradecylphosphonic (TDPA, 0,3674 g, 1,32 mmol), y octadeceno (ODE, 27,6 ml), y evacuar la solución utilizando una línea Schlenk mientras se agita. Aumentar la temperatura a 100 ° C y evacuar por un adicional de 15 minutos para eliminar impurezas de bajo punto de ebullición de punto.
- En atmósfera de argón o nitrógeno gas, se calienta la mezcla a 300 ° C durante 1 hora para disolver completamente la CdO. La solución cambia de un color rojizo a transparente e incoloro. Enfriar la solución a temperatura ambiente.
- Añadir hexadecilamina (HDA, 7,0 g) a la solución de cadmio, calentar a 70 ° C, y evacuar. Una vez que una presión constante se alcanza, aumentar la temperatura a 100-110 ° C y la de reflujo de la solución durante 30 min. Cambie la válvula de línea de Schlenk de gas inerte e insertar el termopar directamente en la solución.
- Bajo condiciones libres de aire, añadir difenilfosfina (DPP, 100 l) a la solución y aumentar la temperatura a 310 ° C. Retirar 7,5 ml de 0,4 M TOP-Se solución(3 selenio mmol) en una jeringa desechable de plástico unido a una aguja de calibre 16.
- Una vez que la temperatura se equilibra a 310 ° C, ajustar el controlador de temperatura a 0 ° C y rápidamente inyectar la solución de TOP-Se directamente en la solución de cadmio. La solución cambia de incoloro a amarillo-naranja y rápidamente la temperatura se reducirá y aumentará de nuevo a ~ 280 ° C. Después de 1 min de reacción, retirar el matraz de la camisa de calentamiento y enfriar rápidamente con una corriente de aire hasta que la temperatura es inferior a 200 ° C.
- Cuando la temperatura alcanza 40 ° C, se diluye con 30 ml de hexano; más del precursor de cadmio restante se asentará de solución. Eliminar este precipitado por centrifugación (5.000 xg, 10 min).
- En cada uno de seis tubo de polipropileno de 50 ml de centrífuga cónico, diluir 12 ml de la solución de nanocristales crudo con acetona 40 ml, de centrifugación (5.000 xg durante 10 min), y se decanta cuidadosamente y descartar el sobrenadante.
- Disolver el nanocrgránulos ystal en hexano (25 ml volumen total). Extraer esta solución 3 veces con un volumen igual de metanol, manteniendo la fase superior. Para la tercera extracción, el volumen de metanol puede ajustarse a ~ 15 ml para obtener una solución de hexano concentrada de puntos cuánticos CdSe puros a aproximadamente 200 mM. El rendimiento típico de esta reacción es 3 mol de nanocristales de CdSe con un diámetro de 2,3 nm (50-60% rendimiento de la reacción).
- Determine el diámetro de nanocristales y concentración midiendo el espectro de absorción UV-Vis y la consulta de la tabla de tallas de ajuste de Mulvaney y compañeros de trabajo 12 y las correlaciones de extinción de Bawendi y compañeros de trabajo 13. Consulte el Apéndice para obtener más información.
- Intercambio de cationes mercurio: los nanocristales pueden ser parcialmente intercambiado con mercurio para desplazamiento al rojo de la absorción y emisión de fluorescencia. Mezclar la siguiente juntos en el orden en un vial de vidrio de 20 ml con barra de agitación (esta reacción puede ser escalado según se desee): 3 ml de hexano, 2 ml de cloroformo, 1 ml de 200 mM CdSe QD solución (200 nmol), 15 oleilamina l (OLA), y 500 l de una solución 0,1 M de Hg (OT) 2 en cloroformo. Mercury octanethioate (HgOT 2) se pueden preparar haciendo reaccionar acetato de mercurio y octanotiol en metanol (véase el apéndice). Medida que la reacción de intercambio de cationes, en la medida de desplazamiento al rojo puede ser vigilado con espectrofotometría de absorción UV-Vis. Después de que la banda de absorción deseada ha sido alcanzada, medir la absorción de la solución de nanocristales en 350 nm y determinar el coeficiente de extinción nuevo, suponiendo que la concentración de nanocristales no ha cambiado (30,7 mu M en este ejemplo). Se detiene la reacción mediante la eliminación del mercurio sin reaccionar: añadir 5 ml de decano, 10 ml de hexano, y 7 ml de metanol y se extrae la solución, manteniendo la fase superior que contiene los nanocristales. Se extrae dos veces más con hexano y metanol, y ajustar el volumen de metanol de modo que la fase superior es de ~ 7 ml. Si las fases son lentos para separar, la solución se puede centrifugar (5000 xg,10 min). Añadir 100 TOP l, 100 l OLA, y 100 l de ácido oleico a los nanocristales seguidas por 40 ml de acetona para inducir la precipitación. Recoge los nanocristales mediante centrifugación y se dispersan en 3 ml de hexano. Se centrifuga de nuevo para eliminar los componentes insolubles y determinar la concentración de nanocristales de nuevo, usando el coeficiente de extinción nuevo a 350 nm. Dejar que la solución de nanocristales de edad durante al menos 24 horas a temperatura ambiente antes de proceder a la siguiente etapa.
2. El crecimiento de sulfuro de cadmio Zinc (Zn Cd y 1-y S) Shell
- Preparar 0,1 M soluciones precursoras shell en 50 ml de 3 bocas matraces. Cadmio precursor: hidrato de acetato de cadmio (230,5 mg, 1 mmol) y 10 ml oleilamina (OLA). Precursor de zinc: acetato de zinc (183,5 mg, 1 mmol) y 10 ml OLA. Precursor de azufre: azufre (32,1 mg, 1 mmol) y 10 ml ODE. Bajo vacío, calentar cada solución a reflujo durante 1 h para dar soluciones claras, y luego cargar con argón. La solución de azufre puedese enfrió a temperatura ambiente, pero los precursores de cadmio y de zinc se mantiene a aproximadamente 50 ° C. Los cálculos de las cantidades de precursores de concha se puede encontrar en la referencia 14.
- Añadir a un matraz de 3 bocas: Hg x Cd 1-X SE puntos cuánticos (120 nmol, 2,3 nm de diámetro), ODE (2 ml), y óxido de trioctilfosfina (TOPO, 250 mg). Evacuar fuera del hexano a temperatura ambiente usando la línea de Schlenk. Aumentar la temperatura a 100 ° C y reflujo durante 15 min. Cambie la válvula de la línea de Schlenk de argón o nitrógeno gaseoso y introducir el termopar en la solución de nanocristales.
- Aumentar la temperatura a 120 ° C, añadir 0,5 monocapas de solución de precursor de azufre (140 l), y permitir que la reacción procediera durante 15 min. Pequeñas alícuotas (<50 l) se puede eliminar usando una jeringa de vidrio para controlar el progreso de la reacción usando fluorescencia y / o UV-Vis espectrofotometría de absorción. Aumentar la temperatura a 140 ° C, añadir 0,5 monocapas de solución cadmio precursor (140 l), y permitir que la reacción procediera durante 15 min. Añadir 500 anhidro mu l OLA a la solución de reacción.
- A 160 ° C agregar 0,5 monocapas de solución de precursor de azufre (220 l), seguido por una cantidad igual de solución de zinc precursor a 170 ° C con 15 min entre cada adición. Luego, a 180 ° C agregar 0,25 monocapas de solución de precursor de azufre (150 l) y solución de zinc precursor en intervalos de 15 min.
- Enfriar la solución a temperatura ambiente de nuevo y calcular un coeficiente de extinción nuevo para estas partículas utilizando un espectro de UV-Vis, suponiendo que el número de nanocristales no ha cambiado (120 nmol en 3,8 ml de solución de reacción). Almacenar la solución de reacción como una mezcla en bruto en un congelador; los nanocristales pueden ser descongelados y se purifica según sea necesario usando el mismo método descrito en las secciones 1.8 y 1.9.
- Los nanocristales pueden ser caracterizados utilizando microscopia electrónica, UV-Vis espectroscopia de absorción, y espectroscopia de fluorescencia. Rendimiento cuántico puede sercalculado absolutamente usando una esfera de integración o relativamente en comparación con un estándar conocido utilizando los métodos de referencia 15.
3. Fase de transferencia
- Añadir purificó núcleo / corteza Hg x Cd 1-x Se / Cd y Zn 1-y S puntos cuánticos (5 ml, 20 mM) a una ml 50 3-bocas, y eliminar el hexano bajo un alto vacío para producir una película seca. Llenar el matraz con argón, se añade piridina anhidra (3 ml) a la película de nanopartículas y calentar la suspensión a 80 ° C. En el transcurso de 1-2 horas las nanopartículas se disolverá completamente.
- Añadir 1-tioglicerol (1 ml) a la solución y se agita a 80 º C durante 2 h. Luego enfriar la solución a temperatura ambiente y se añade trietilamina (0,5 ml) para desprotonar tioglicerol. Se agita durante 30 min. La solución puede enturbiarse después de la adición de trietilamina debido a la pobre solubilidad de los nanocristales polares en esta mezcla de disolventes.
- Transferir la solución a un QD cont cónico de 50 ml tubo de centrífugaaining una mezcla de 20 ml de hexano y 20 ml de acetona, y mezclar bien. Aislar los nanocristales precipitados mediante centrifugación (5.000 xg, 10 min), y se lava el precipitado con acetona.
- Disolver el precipitado QD en DMSO (5 ml) con baño de ultrasonidos y, a continuación centrifugar (7.000 xg, 10 min) para eliminar los agregados posibles. Determinar la concentración de nanopartículas a partir de un espectro de absorción UV-Vis. Esta solución de puntos cuánticos puros se debe utilizar dentro de 3 horas, como los tioles de superficie puede oxidar lentamente en condiciones ambientales en el aire.
- Diluir la solución de QD a 10 micras o menor, con DMSO y transferir a un matraz de 50 ml. Preparar un 5 mg / ml de solución de ácido poliacrílico tiolado (síntesis descrita en el Apéndice) en DMSO. Añadir la solución de polímero (0,15 mg de polímero por nmol QDs) gota a gota a la solución QD mientras se agitaba y desgasificar la solución a temperatura ambiente durante 5 min.
- Se purga la solución QD / polímero con argón y se calienta a 80 ° C durante 90 min. Luego enfriar la solución a temperatura ambiente unad gota a gota añadir un volumen igual de borato de sodio 50 mM, pH 8. Se agita durante 10 min.
- Purificar los puntos cuánticos a través de diálisis (20 kDa de corte) en borato de sodio 50 mM, pH 8, y luego se concentran las partículas utilizando un filtro centrífugo (10 kDa de corte). Determinar la concentración de un espectro de absorción UV-Vis.
4. PEG Coating
- En un vial de vidrio de 4 ml con barra de agitación, mezcla 1 nmol de puntos cuánticos en tampón de borato con un exceso molar de 40.000 x 750 Da monoamino-polietilenglicol (30 mg, 40 mmol). Si una funcionalidad química específica es que se añaden a los nanocristales (por ejemplo, hidrazida o maleimida), puede ser introducido mediante la sustitución de una fracción de la amino-PEG heterobifuncional con un amino-PEG (30% fracción molar normalmente funciona bien). Diluir la solución de nanocristales a 1 mM con tampón de borato. Esta reacción puede hacerse a escala según se desee.
- Preparar una solución fresca de DMTMM (20 mg, 72 mmol) en DMSO (144 l). Esta solución puede calentarse brevemente unDer una corriente de agua de grifo caliente o sumergidos en un baño de ultrasonidos para disolver completamente el DMTMM. Añadir rápidamente un exceso de 25.000 x molar de esta solución 0,5 M DMTMM (50 l) a la solución QD y se agita a temperatura ambiente durante 30 min.
- Repita el paso cuatro veces más 4,2 para saturar la superficie de nanocristales con PEG. Por último, añadir 200 l 1 M Tris buffer para inactivar la reacción y purificar los nanocristales usando la diálisis, filtros centrífugos, o ultracentrifugación.
- Los nanocristales pueden ser analizados para monodispersidad, el tamaño hidrodinámico, y la carga superficial, usando la cromatografía líquida, la electroforesis en gel de agarosa, y microscopía de fluorescencia. Para determinar el tamaño hidrodinámico y la distribución de tamaño utilizando un sistema automatizado de cromatografía líquida (GE AKTAprime Plus), usar una columna de Superose 6, una velocidad de flujo de 0,5 ml / min con PBS eluyente tampón, y la detección de la absorción a 260 o 280 nm. Comparar los tiempos de elución de nanopartículas con los de patrones de peso molecular. Para gel de agarosa de electroforesisresistencia, preparar un gel de agarosa al 0,5% en 50 mM de tampón de borato de sodio (pH 8,5) o 50 mM de tampón de fosfato de sodio (pH 7,4), mezclar muestras de 1 m con 10% de glicerol y de carga a los pozos, y funcionar a 100 V durante 30 min . Imagen de los nanocristales en el gel usando una varilla de UV o transiluminador UV y para la excitación de fluorescencia. Para la imagen de los nanocristales en el nivel de una sola molécula usando microscopía de fluorescencia, diluir las partículas a 0,2 nM en tampón fosfato 10 mM, gota 2,5 ml de la solución sobre un cubreobjetos de vidrio, y se coloca cuidadosamente un cubreobjetos segundos en la parte superior del líquido talón para difundir una película entre los cubreobjetos. Imagen de la superficie con destino partículas usando un objetivo de alta apertura numérica (lo ideal es por lo menos 1,40) en cualquiera de los modos de epifluorescencia o TIRF con excitación a longitudes de onda entre 400-580 nm y una cámara CCD multiplicador de electrones. Parámetros exactos de imagen variará entre configuración microscopía.
Resultados
La figura 2 muestra la absorción y fluorescencia representante de nanocristales CdSe Hg, Cd x 1-x nanocristales SE después de intercambio catiónico, y Hg Cd x 1-x Se / Cd y Zn 1-y S después de nanocristales crecimiento de la concha. Los nanocristales de CdSe núcleo tienen un rendimiento cuántico de fluorescencia cerca de 15% (incluida la longitud de onda larga profundo-trampa de emisión), pero esta eficiencia cae a menos del 1% después de mercurio de c...
Discusión
En comparación con los convencionales CdSe puntos cuánticos, aleación ternaria Hg Cd x 1-x nanocristales de Se puede ajustar en tamaño y longitud de onda de fluorescencia de forma independiente. El tamaño se selecciona por primera vez durante la síntesis de nanocristales de CdSe núcleos, y la longitud de onda de fluorescencia se elige en una etapa de intercambio de cationes secundaria de mercurio, que no altera sustancialmente el tamaño de nanocristales 9. Es importante permitir que el Hg p...
Divulgaciones
No hay conflictos de interés declarado.
Agradecimientos
Los autores desean agradecer al Dr. Hong Yi en el Núcleo de la Universidad Emory Microscopía Integrado de imágenes de microscopía electrónica. Este trabajo ha sido patrocinado por el NIH subvenciones (PN2EY018244, R01 CA108468, U54CA119338 y 1K99CA154006-01).
Materiales
| Name | Company | Catalog Number | Comments |
| Nombre del reactivo | Empresa | Número de catálogo | Comentarios (opcional) |
| Selenio | Sigma-Aldrich | 229865 | |
| Tri-n-octilfosfina | Strem | 15-6655 | 97% de pureza, inestable en aire |
| Óxido de cadmio | Sigma-Aldrich | 202894 | Altamente tóxico: el uso precaución |
| Tetradecylphosphonic ácido | PCI Síntesis | 4671-75-4 | |
| Octadeceno | Alfa Aesar | L11004 | El grado técnico |
| Hexadecilamina | Sigma-Aldrich | H7408 | |
| Difenilfosfina | Sigma-Aldrich | 252964 | Pirofórico |
| Mercury acetato | Sigma-Aldrich | 456012 | Altamente tóxico: el uso precaución |
| 1-octanotiol | Sigma-Aldrich | 471836 | Olor fuerte |
| El ácido oleico | Sigma-Aldrich | W281506 | |
| Acetato de zinc | Alfa Aesar | 35792 | |
| Cadmio acetato hidrato | Sigma-Aldrich | 229490 | Altamente tóxico: el uso precaución |
| Oleilamina | Fisher Scientific | AC12954 | Inestable en el aire |
| Azufre | Sigma-Aldrich | 344621 | |
| Óxido de trioctilfosfina | Strem | 15-6661 | 99% |
| Piridina | VWR | EM-PX2012-6 | Anhidro |
| Tioglicerol | Sigma-Aldrich | M1753 | Olor fuerte |
| Se añadió trietilamina | Sigma-Aldrich | 471283 | Anhidro |
| Diálisis tubería | Spectrum Labs | 131342 | 20 kDa de corte |
| Filtro centrífugo | Millipore | UFC801024 | 10 kDa de corte |
| Monoamino-PEG | Rapp Polymere | 12 750-2 | 750 Da |
| DMTMM, 4 - (4,6-dimetoxi-1 ,3,5-triazin-2-il)-4-metilmorfolinio hidrato de cloruro | Alfa Aesar | H26333 | |
| AKTAprime Plus sistema de cromatografía | GE Healthcare | ||
| Superose 6 10/300 GL cromatografía en columna | GE Healthcare | 17-5172-01 | |
| Agarosa, OmniPur | VWR | EM-2120 | |
Apéndice Síntesis de mercurio octanethiolate: Se añade lentamente una solución de metanol de acetato de mercurio (1 eq.) A una solución en agitación de 1-octanotiol (3 eq.) E hidróxido de potasio (3 eq.) En metanol a temperatura ambiente. Aislar el mercurio (II) octanethiolate precipitado por filtración, lavar dos veces con metanol y una vez con éter, y luego se seca a vacío. Síntesis de polímero multidentado: Disolver ácido poliacrílico (1 g, 1.773 Da) en 25 ml de dimetilformamida (DMF) en un 150 ml de tres bocas y de la burbuja con argón durante 30 min. Añadir una solución anhidra de cisteamina (374 mg, 4,87 mmol) en 10 ml de DMF. A temperatura ambiente con agitación vigorosa, se añade lentamente diisopropilcarbodiimida anhidro (DIC, 736 mg, 5,83 mmol) durante 30 min, seguido de trietilamina (170 l, 1,22 mmol), y permitir que la reacción continúe durante 72 horas a 60 ° C. Añadir mercaptoetanol (501 mg, 6,41 mmol) para inactivar la reacción, y se agita durante 2 horas a temperatura ambiente. Eliminar la DMF por evaporación rotatoria y aislar el polímero con la adición de una mezcla 2:1 de acetona enfriada con hielo: cloroformo, seguido de centrifugación. Se disuelve el polímero en ~ 5 ml de DMF anhidro, se filtro, precipitado de nuevo con éter dietílico, y repetir. Se seca el producto al vacío y en atmósfera de argón tienda. Determinación del diámetro del núcleo de CdSe: A partir del espectro de absorción UV-Vis determinar la longitud de onda de la primera pico excitón (λ, en nm), que es el pico más larga longitud de onda (por ejemplo, aproximadamente 498 nm para CdSe en la Figura 2a), y utilizar el dimensionamiento curva de Mulvaney y compañeros de trabajo 12:
Determinación de la concentración de nanocristales CdSe: Desde un fondo sustraído de UV-Vis espectro de una solución ópticamente transparente de nanocristales de CdSe, determinar la longitud de onda de absorción a 350 nm. Las diluciones en serie se puede utilizar para determinar si la absorción óptica está dentro del rango lineal de la ley de Beer. La concentración de nanocristales (QD, en M) puede determinarse enchufando el diámetro de nanocristales (D, en nm), el valor de absorción óptica (A 3sa), y la longitud del camino cubeta (l, en cm) en la siguiente ecuación a partir la correlación empírica de Bawendi y compañeros de trabajo 13:
|
Referencias
- Toprak, E., Selvin, P. R. New fluorescent tools for watching nanometer-scale conformational changes of single molecules. Annu. Rev. Biophys. Biomol. Struct. 36, 349-369 (2007).
- Joo, C., Balci, H., Ishitsuka, Y., Buranachai, C., Ha, T. J. Advances in single molecule fluorescence methods for molecular biology. Annu. Rev. Biochem. 77, 51-76 (2008).
- Pinaud, F., Clarke, S., Sittner, A., Dahan, M. Probing cellular events, one quantum dot at a time. Nat. Method. 7, 275-285 (2010).
- Smith, A. M., Wen, M. M., Nie, S. M. Imaging dynamic cellular events with quantum dots. Biochemist. 32, 12-17 (2010).
- Smith, A. M., Duan, H. W., Mohs, A. M., Nie, S. M. Bioconjugated quantum dots for in vivo molecular and cellular imaging. Adv. Drug Deliv. Rev. 60, 1226-1240 (2008).
- Smith, A. M., Nie, S. M. Next-generation quantum dots. Nature Biotech. 27, 732-733 (2009).
- Groc, L., Lafourcade, M., Heine, M., Renner, M., Racine, V., Sibarita, J. -. B., Lounis, B., Choquet, D., Cognet, L. Single trafficking of neurotransmitter receptor: comparison between single-molecule/quantum dot strategies. J. Neurosci. 27, 12433-12437 (2007).
- Smith, A. M., Nie, S. M. Minimizing the hydrodynamic size of quantum dots with multifunctional multidentate polymer ligands. J. Am. Chem. Soc. 130, 11278-11279 (2008).
- Smith, A. M., Nie, S. M. Bright and compact alloyed quantum dots with broadly tunable near-infrared absorption and fluorescence spectra through mercury cation exchange. J. Am. Chem. Soc. 133, 24-26 (2011).
- Shriver, D. F., Drezdzon, M. A. . The Manipulation of Air-Sensitive Compounds. , (1986).
- Errington, R. J. . Advanced Practical Inorganic and Metalorganic Chemistry. , (1997).
- Jasieniak, J., Smith, L., van Embden, J., Mulvaney, P., Califano, M. Re-examination of the size-dependent absorption properties of CdSe quantum dots. J. Phys. Chem. C. 113, 19468-19474 (2009).
- Leatherdale, C. A., Woo, W. K., Mikulec, F. V., Bawendi, M. G. On the absorption cross section of CdSe nanocrystal quantum dots. J. Phys. Chem. B. 106, 7619-7622 (2002).
- Smith, A. M., Mohs, A. M., Nie, S. M. Tuning the optical and electronic properties of colloidal nanocrystals by lattice strain. Nature Nanotech. 4, 56-63 (2009).
- Demas, J. N., Crosby, G. A. The measurement of photoluminescence quantum yields. A review. J. Phys. Chem. 75, 991-1024 (1971).
- Van Embden, J., Jasieniak, J., Mulvaney, P. Mapping the optical properties of CdSe/CdS heterostructure nanocrystals: the effects of core size and shell thickness. J. Am. Chem. Soc. 131, 14299-14309 (2009).
- Smith, A. M., Duan, H. W., Rhyner, M. N., Ruan, G., Nie, S. M. A systematic examination of surface coatings on the optical and chemical properties of semiconductor quantum dots. Phys. Chem. Chem. Phys. 8, 3895-3903 (2006).
- Zhang, X., Mohandessi, S., Miller, L. W., Snee, P. T. Efficient functionalization of aqueous CdSe/ZnS nanocrystals using small-molecule chemical activators. Chem. Comm. 47, 3532-3534 (2011).
- Bucio, L., Souza, V., Albores, A., Sierra, A., Chavez, E., Carabez, A., Guiterrez-Ruiz, M. C. Cadmium and mercury toxicity in a human fetal hepatic cell line (WRL-68 cells). Toxicol. 102, 285-299 (1995).
- Han, S. G., Castranova, V., Vallyathan, V. J. Comparative cytotoxicity of cadmium and mercury in a human bronchial epithelial cell line (BEAS-2B) and its role in oxidative stress and induction of heat shock protein 70. J. Toxicol. Environ. Health Part A. 70, 852-860 (2007).
- Strubelt, O., Kremer, J., Tilse, A., Keogh, J., Pentz, R. J. Comparative studies on the toxicity of mercury, cadmium, and copper toward the isolated perfused rat liver. J. Toxicol. Environ. Health Part A. 47, 267-283 (1996).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados