Method Article
La optimización y utilización de
En este artículo
Resumen
La producción de proteína transitoria en plantas de Nicotiana sobre la base de infiltración al vacío con agrobacterias llevando vectores de lanzamiento (virus del mosaico del tabaco a base) es un enfoque rápido y económico para producir antígenos de vacunas y proteínas terapéuticas. Hemos simplificado el procedimiento mejorado y la acumulación de destino mediante la optimización de las condiciones de cultivo de bacterias, la selección de especies huéspedes, y co-introducción de supresores de silenciamiento de ARN.
Resumen
La producción de proteína transitoria mediada por Agrobacterium en plantas es un enfoque prometedor para producir antígenos de vacunas y proteínas terapéuticas en un corto período de tiempo. Sin embargo, esta tecnología sólo está empezando a aplicar a la producción a gran escala, muchos obstáculos tecnológicos para aumentar la escala de ahora están siendo superados. Este sentido, demuestran un método simple y reproducible para la producción de proteína transitoria a escala industrial basado en la infiltración de vacío de plantas de Nicotiana con Agrobacteria llevar vectores de lanzamiento. Optimización del cultivo de Agrobacterium en medio AB permite la dilución directa del cultivo bacteriano en agua Milli-Q, lo que simplifica el proceso de infiltración. Entre tres especies estudiadas de Nicotiana, N. excelsiana (N. benthamiana × N. excelsior) fue seleccionado como el anfitrión más prometedor debido a la facilidad de la infiltración, el alto nivel de producción de la proteína reportera, y alrededor de dos fedad mayor producción de biomasa en condiciones ambientales controladas. La inducción de de Agrobacterium que alberga pBID4-GFP (virus del mosaico del tabaco a base) usando productos químicos tales como acetosiringona y monosacárido no tuvo efecto sobre el nivel de producción de proteínas. La infiltración de planta bajo de 50 a 100 mbar durante 30 o 60 segundos dio como resultado aproximadamente 95% de la infiltración de tejidos de las hojas de plantas. La infiltración con GV3101 de Agrobacterium cepa de laboratorio mostró la mayor producción de proteínas en comparación con cepas de laboratorio de Agrobacteria LBA4404 y C58C1 y de tipo salvaje cepas Agrobacteria at6, AT10, at77 y A4. Co-expresión de un ARN viral de silenciamiento supresor, p23 o p19, en N. benthamiana resultado en la acumulación antes y aumento de la producción (15-25%) de proteína diana (hemaglutinina del virus de la gripe).
Introducción
Las plantas son ahora reconocidos como una plataforma segura, fiable, escalable y de bajo costo para la producción de productos biofarmacéuticos recombinantes heterólogas y proteínas industriales 1-3 y tienen importantes ventajas sobre los sistemas de expresión de células microbianas y animales 4. Las plantas son capaces de expresar proteínas correctamente plegadas con modificaciones post-traduccionales, incluyendo anticuerpos multiméricos reunidos 5-7. Varias proteínas farmacéuticas recombinantes derivados de las plantas están sufriendo evaluación clínica 8. Estos incluyen las vacunas específicas para cada paciente recombinantes idiotipo (scFv) para el tratamiento del linfoma no Hodgkin 9, pandemia basada en la hemaglutinina y candidatos para vacunas antigripales estacionales 10,11 (Cummings et al., Presentado a la Vacuna), anti-Streptococcus antígeno de superficie que / anticuerpo II para el tratamiento de la caries dental 12, y la insulina humana para el tratamiento de la diabetes 13. Además, Reco humanaglucocerebrosidasa mbinant para la terapia de reemplazo enzimático en pacientes con enfermedad de Gaucher ha sido aprobado en Israel y en los EE.UU. y está previsto en el Programa de Acceso Ampliado fuera de los EE.UU. 14,15.
Proteínas heterólogas se pueden producir en transformada de manera estable (transgénica o transplastómica) o plantas transformadas transitoriamente. La producción de proteína transitoria ofrece varias ventajas sobre la producción en plantas transgénicas, incluyendo marco de tiempo corto para conseguir la expresión y acumulación 16, y se puede lograr mediante la introducción de vectores binarios bacterianas o vectores virales de plantas recombinante en tejidos de las plantas 4. El sistema de expresión transitoria más avanzado se basa en el uso de «vectores de lanzamiento 'que combinan los componentes de virus de plantas y plásmidos binarios, y se entregan por agroinfiltración 17,18. Agroinfiltration de un vector de lanzamiento basado en mosaico del tabaco (TMV) se ha aplicado con éxito en el laboratorioescala para producir antígenos de vacunas contra patógenos como el virus del papiloma humano 19, Yersinia pestis 20, los virus gripales A 21,22, Bacillus anthracis 23, y el virus de la viruela en 24 N. benthamiana hojas. expresión transitoria mediada por Agrobacterium es también un método prometedor para la producción simultánea de múltiples proteínas 2,25-27. Por ejemplo, los sistemas de expresión transitoria de plantas han sido utilizadas para producir anticuerpos recombinantes específicos de tumor 28,29, un anticuerpo recombinante glicosilada contra el receptor del factor de crecimiento epidérmico 30, y un anticuerpo monoclonal específico para el ántrax antígeno protector 31,32. Co-infiltración de plantas de Nicotiana benthamiana con un gen diana y un supresor de resultados de silenciamiento de genes en una mayor expresión de la proteína diana 33,34.
Agroinfiltration es un método común para introdu uniformementebacterias Cing que albergan un gen de interés en los tejidos vegetales 35-37. Infiltración al vacío de Agrobacterium para la expresión génica transitoria en planta intacta hojas es un método rápido, escalable, y útil para la producción de proteínas extrañas sin la necesidad de generar plantas transgénicas 38-41. Durante agroinfiltration vacío, las plantas se da la vuelta al revés y partes aéreas sumergidas en una suspensión de Agrobacterium. A continuación se aplica el vacío que causa los gases para la evacuación de los espacios intercelulares de la hoja a través de los estomas. Rápida re-presurización siguiente publicación de los resultados de vacío en la infusión de la suspensión de Agrobacterium en la hoja. A raíz de la infiltración de vacío de Agrobacteria, las plantas se cultivan más y expresión objetivo es monitoreado. Los niveles más altos de expresión diana se observan típicamente 2-3 días después de la infiltración (ppp) con un vector binario y 4-7 ppp con un vector de lanzamiento, después de lo cual el nivel de expresión típicamente dismiSES 17,18,42-45. Agrobacterium tumefaciens es el vehículo más ampliamente utilizado para la entrega de un gen de interés en una planta para la producción de proteínas. Agroinfiltration funciona excepcionalmente bien en N. benthamiana pero relativamente poco en la mayoría de otras plantas, incluyendo Arabidopsis thaliana 46.
En este estudio, hemos desarrollado un método simple, eficiente y económico para la producción de proteína transitoria en 5-6 semanas de edad N. benthamiana utilizando A. tumefaciens infiltración. El principal inconveniente de escalado industrial de la técnica de la agroinfiltración es la centrifugación de las bacterias cosechadas y la resuspensión del sedimento bacteriano en medio que contenía 4'-hidroxi-3 ', 5'-dimetoxiacetofenona (acetosiringona), monosacáridos, y 2 - (N-morfolino) -etanosulfónico (MES) tampón para la inducción de los genes vir. Hemos sido capaces de superar estos problemas mediante la optimización de la Agrobacterium el crecimiento en medio AB (medio mínimo) seguido por la dilución directamente en agua Milli-Q y mediante el control de la duración y las condiciones de infiltración. También hemos comparado la producción de proteínas diana en el N. de tipo silvestre las especies de acogida tabaco benthamiana y N. Excelsior, así como en N. híbrido excelsiana.
Protocolo
1. Planta que crece
Para la posterior agroinfiltration evaluamos dos especies de Nicotiana de tipo salvaje (N. benthamiana y N. excelsior) y un híbrido (N. excelsiana) cultivadas hidropónicos en lana de roca en las instalaciones interiores.
- Remojar la lana de roca en una solución de abono para las plantas.
- Siembre las semillas de tipo salvaje de N. benthamiana, N. excelsior y N. excelsiana (híbrido de N. benthamiana × N. excelsior) en los nutrientes empapada superficie de lana de roca.
- Cultiva plantas de las semillas bajo condiciones controladas (24 ° C y humedad relativa de 40-65%) y un fotoperiodo de día largo (14 horas de luz y 10 horas de oscuridad, con iluminación de 130 a 150 E · m -2 s -1) para 4-5 semanas para N. benthamiana y N. excelsiana, y 5-6 semanas para N. excelsior.
2. Construcción de vectores para Agroinfiltration
- Inserte un gen indicador sintético (proteína verde fluorescente [GFP]), de larga duración de la hemaglutinina (HA) de la cepa del virus de la influenza A/California/04/2009 (HAC1), y re-ingeniería de la enzima liquenasa (LicKM) 18 por separado en el vector de lanzamiento pBID4 18 (vector basado en TMV) para obtener pBID4-GFP, pBID4-HAC1 y pBID4-LicKM, respectivamente 18,32,41,47.
- Introducir 10-50 ng de pBID4 llevar las buenas prácticas agrarias o HAC1 en células electrocompetentes de A. tumefaciens cepa GV3101 y LicKM en células electrocompetentes de A. Agrobacterium cepas GV3101, C58C1, GLA4404, AT06, At10, At77 y A4 con el electroporador MicroPulser gen.
- Utilice la agrobacterias transformadas para los experimentos de infiltración a menos que se indique lo contrario.
3. Aspire infiltración de Agrobacterium en plantas de Nicotiana
- Crecer A. tumefaciens cepas durante la noche (O / N) en medio LB, med YEBio o medio AB suplementado con 50 mg / l de kanamicina a 28 ° C con agitación a 200-250 rpm.
- Diluir agrobacterias en agua Milli-Q para una densidad óptica a 600 nm (600) de células 0.5 o Agrobacterium centrífuga crecido en LB o YEB o AB en 4000 × g durante 10 min a 4 ° C, volver a suspender en medio de inducción (sal 1x MS, MES 10 mM, acetosiringona 200 mM, 2% de sacarosa [MMA]) a A 600 de 0,5, y se agita a temperatura ambiente durante 1-3 hr, salvo que se indique lo contrario.
- Infiltrarse en las plantas en una cámara de vacío sumergiendo tejidos aéreos de la planta Nicotiana en suspensión de Agrobacterium y la aplicación de un vacío 50-400 mbar durante 30 o 60 segundos. La infiltración óptima se aplica rutinariamente en 50-100 mbar durante 60 segundos.
- Una vez que se rompe el vacío, retire las plantas de la cámara de vacío, enjuague en agua, y crecer durante 5-7 días en las mismas condiciones de crecimiento utilizadas para el crecimiento pre-infiltración.
- Para probar la eficaciade productos químicos que inducen gen vir de Agrobacterium, diferentes concentraciones de acetosiringona (0, 100, 200 o 400 micras) se añadieron a la agrobacterias se suspendieron en tampón de infiltración (1x MS, MES 10 mM, 2% de glucosa). Para el efecto de monosacárido en la inducción del gen vir, diferentes porcentajes de glucosa (0, 1, 2 o 4%) se añadieron a agrobacterias en suspensión en el tampón de infiltración (1x MS, MES 10 mM, 200 mM de acetosiringona). N. benthamiana plantas se infiltraron como se ha mencionado anteriormente en las etapas 3.3 y 3.4).
- Laboratorio de cepas de Agrobacterium GV3101, C58C1 y LBA4404 y las cepas de tipo salvaje A4, AT06, AT10 y At77 alberga el vector pBID4-LicKM se diluyeron en agua Milli-Q a A 600 de 0,5. N. benthamiana plantas se infiltraron con cada cepa en particular como se mencionó anteriormente en los pasos 3.3 y 3.4.
4. Procedimiento Co-agroinfiltration para el supresor de silenciamiento viral
- Mix las culturas Milli-Q agua-diluido Agrobacterium GV3101 que portan el gen GFP y el silenciamiento viral p19 supresor de tomate enanismo arbustivo del virus (TBSV) en 1:01, 2:01, 3:01 y 4:01 ratios. Infíltrate N. benthamiana plantas como se describió anteriormente.
- Infíltrate N. benthamiana plantas con una mezcla de dos culturas Agrobacterium GV3101 diluidas en agua Milli-Q: el primero lleva el plásmido pBID4-HAC1 y el segundo que lleva uno de los supresores de silenciamiento - p19 de TBSV o p23 del virus de la tristeza de los cítricos, en el plásmido pCassp ( pCassp19) y en el plásmido binario pGR bajo el promotor 35S (PGR-P23), respectivamente, en la relación 04:01.
5. Análisis Western Blot
- Recoger muestras de hojas al azar de N. benthamiana, N. excelsior o N. plantas excelsiana en 4-7 ppp y pulverizar en nitrógeno líquido a un polvo fino.
- Añadir tres volúmenes de tampón PBS 1x que contienen 0,5% de TritonX-100 a cada muestra.
- Agite suavemente las muestras extraídas durante 15 min a 4 ° C.
- Haga girar el extracto durante 5 min y recoger la proteína soluble total en un tubo Eppendorf limpio.
- Diluir los extractos a una dilución apropiada (1:50 1:100) en tampón de extracción 1x PBS, y añadir 5 × tampón de muestra (Tris-HCl 250 [pH 6,8], 10% de SDS, 0,5% azul de bromofenol, 50% de glicerol v / v, y DTT 500 mM) a una final concentración de 1 ×.
- Muestras hervir durante 5 min.
- Proteínas separadas en un 10% SDS-PAGE, transferencia a una membrana de transferencia Immobilon-P, y bloquean con un 0,5% I-bloque.
- Detectar GFP usando anticuerpo policlonal de conejo anti-GFP antisuero a 1:5.000 y HAC1 usando anticuerpo monoclonal de ratón anti-poli-histidina en 1:1.000 en solución de bloqueo durante 1 hora.
- Después de etiquetado anticuerpo primario, lavar las membranas tres veces durante 10 minutos cada uno con 1 × PBST-20 e incubar con una peroxidasa de rábano picante (HRP) conjugado con anticuerpo anti-conejo a 1:5.000 o un conjugado de HRPd anticuerpo anti-ratón en 1:10.000 durante 1 hora, por las buenas prácticas agrarias y la detección HAC1, respectivamente.
- Procesar las transferencias de Western utilizando el sustrato SuperSignal West Pico quimioluminiscente.
- Utilice la GeneTools Software para analizar la intensidad de banda de la proteína y obtener la cantidad calibrada banda.
La producción de proteínas: (Calibrado cantidad x de dilución de la muestra) / cantidad de muestra cargada) x 4 = mg / kg.
Ecuación: La producción de proteínas (P), la cantidad calibrada (C), la dilución de la muestra (D) y la cantidad de Muestra cargada (S).
6. Ensayo Zimograma
- N.-LicKM infiltrado-pBID4 Recoger benthamiana muestras de tejido al azar.
- Extracto de proteínas usando los mismos métodos descritos anteriormente para el análisis de transferencia de Western y luego analizar por 10% de SDS-PAGE con 0,1% liquenano incluidos en los geles.
- Después de la electroforesis, los geles de lavar dos veces durante 10 minutos cada uno en tampón de lavado (Tris-HCl 100 [pH 8,0] y 0,1% de Triton X-100) Y luego incubar en tampón de lavado a 65 ° C durante 1 hora.
- Después de la incubación, desechar el tampón de lavado y manchar los geles con 0,5% de Rojo Congo durante 5 min a temperatura ambiente.
- Enjuague los geles en agua Milli-Q tres veces durante 10 minutos cada uno, y añadir 1 M NaCl para visualizar la actividad liquenasa. La proteína liquenasa bacteriana purificada se utilizó como control positivo para la actividad de la enzima.
7. Imaging GFP
- Realizar la detección visual de la fluorescencia de GFP en plantas enteras transformadas transitoriamente utilizando una lámpara UV de longitud de onda larga de mano.
- Fotografía transitoriamente transformado plantas con una cámara digital a través de un Amarillo 8, ES 52 filtro (tiempo de exposición, 15 seg).
- Obtener imágenes de Western blot análisis utilizando el software GeneSnap en un GeneGnome y cuantificar los resultados utilizando el software GeneTools, con una curva de calibración basada en el estándar GFP purificada.
- Cuantificar proteína HAC1 utilizando una curva de calibración basada en purified HAC estándar de la proteína de la cepa del virus de la influenza A/Indonesia/05/05.
- Calcule los valores medios 3-4 repeticiones para todos los experimentos.
Resultados
Los requerimientos de nutrientes para el crecimiento vegetal. El uso de medio de crecimiento de plantas hidropónico (lana de roca) y solución de nutrientes asegura la uniformidad de N. crecimiento benthamiana y elimina complejidades (mecánica, regulación y eficiencia) asociado con el uso del suelo para el cultivo de plantas. Crecimos N. benthamiana en losas de lana de roca empapadas en fertilizantes disponibles comercialmente para determinar las condiciones óptimas para el crecimiento de la planta y la acumulación de biomasa. Hemos observado 95-100% germinación de la semilla. Hay que señalar que la inclusión de fósforo es fundamental para lograr la germinación, porque nos dimos cuenta de que la solución de nutrientes que carecen de fósforo no apoyó la germinación y el crecimiento de N. semillas benthamiana (Figura 1A).
Efectos de crecimiento de Agrobacterium y los medios de comunicación de infiltración en la salud y la producción de proteínas de la planta. Hemos probado varias condiciones de medios para optimizar la eficiencia de tél agroinfiltration técnica para la producción a gran escala. Las bacterias (A. tumefaciens cepa GV3101) que albergan el constructo pBID4-GFP se cultivaron O / N en diferentes condiciones de los medios de comunicación (YEB, LB o AB), y, o bien se centrifugaron y se resuspendieron en medio de inducción (MMA) (que contiene 1 × Murashige y Skoog [MS] Mezcla de sal basal, 10 mM de MES pH 5.6, 20 g / L de sacarosa y 200 mM de acetosiringona) o diluido en agua Milli-Q a 600 de 0,5 antes de usar para la infiltración de la planta. Hemos observado que la infiltración al vacío de las plantas con bacterias diluidas en agua resultó en la producción de proteínas comparables a los logrados con cualquier medio de infiltración en los informes anteriores 42,48. En contraste, la infiltración con agrobacterias sin diluir crecido en YEB o medio LB que resultó en marchitamiento completo de N. benthamiana deja en menos de 24 h después de la infiltración, mientras Agrobacteria sin diluir cultivadas en medio AB no tuvieron efecto sobre la salud de las plantas infiltradas (datuna que no se muestra). Como se ilustra en la Figura 1B, las plantas infiltradas con cultivos de Agrobacterium se cultivan en YEB, LB o AB medios de comunicación y se diluyó con agua Milli-Q (01:05, A 600 de 0,6-0,8 o 1:10, A 600 de 0.3-0.4) mostraron no hay síntomas y exhibieron una producción media de GFP de 1645, 1520 y 1839, respectivamente. agrobacterias centrifugó y se resuspendió en medio de inducción (MMA) no mostró síntomas y ninguna diferencia significativa en la producción de proteínas en comparación con agrobacterias directamente diluido en agua Milli-Q ( 1671 ± 102 y 1667 ± 131 mg / kg, respectivamente). Por lo tanto, se recomienda utilizar agua Milli-Q para la dilución de cultivos de Agrobacterium para la infiltración de la planta y se utiliza de forma rutinaria en nuestros experimentos posteriores para alcanzar una A600 de 0,5.
Efectos de la densidad celular suspensión de Agrobacterium y curso temporal de la expresión de destino. A continuación examinó si la densidad celular bacterianaafecta a la eficiencia de la infiltración y los niveles de expresión diana. Para este fin, se evaluó cuatro densidades de suspensión de células diferentes de Agrobacterium que llevan pBID4-GFP, un 600 de 1,0, 0,5, 0,1 y 0,05. Después de la infiltración, N. benthamiana plantas fueron controlados por el desarrollo de síntomas visibles y curso temporal de la expresión de destino mediante la recopilación de muestras a las 4, 7 y 10 dpi. A las 4 ppp, se observaron diferencias notables en la fluorescencia de GFP entre plantas infiltradas con diferentes densidades de células en suspensión de Agrobacterium (sin expresión de GFP se observó en A 600 de 0,05). A los 7 dpi, GFP fluorescencia fue similar en las plantas se infiltró en las densidades de células en suspensión de un 600 1.0, 0.5 y 0.1, pero fue menor en las plantas se infiltró en un A 600 de 0.05. Como se muestra en la Figura 1C, estos datos fueron confirmados por análisis de Western blot de las muestras recogidas en 4 dpi, que muestran la producción muy baja de proteína en A 600 de 0,05 (5 mg / kg) y más alto en A 600 de 1,0 (1,739 mg / kg). En 7 dpi, las plantas no mostraron diferencias significativas en la producción estimado de GFP en A 600 de 1,0, 0,5 y 0,1 (1662, 1870 y 1890, respectivamente), mientras que A 600 de 0.05 mostraron que la producción de GFP inferior (1.199 mg / kg). En contraste, en 10 dpi no se observaron diferencias en la producción de GFP entre las plantas infiltradas con cualquiera de las cuatro densidades de suspensión celular (1218, 1181, 1197 y 1304).
La infiltración con cepas alternativas de Agrobacterium. Para aumentar la diversidad de cepas de Agrobacterium disponible para la producción de proteína transitoria, hemos probado de tipo salvaje cepas. Estas cepas, aisladas de la corona-hiel de huéspedes naturales, fueron amablemente proporcionados por el doctor Gelvin (Universidad de Purdue, West Lafayette, Indiana). Para examinar su utilidad en la producción de proteínas transitoria, hemos infiltrado en N. benthamiana con las siguientes cepas de Carrying pBID4-LicKM 18: A. rhizogenes (A4) y A. tumefaciens de tipo salvaje Nester cepas A348, A208, A281 y (llamado At6, At10, At77 y, respectivamente), así como cepas de laboratorio de ingeniería de A. Agrobacterium GV3101, C58C1, y LBA4404. Las hojas infiltradas se recogieron a 7 dpi y el nivel de expresión LicKM se estimó por el ensayo de Western blot. Como se muestra en la Figura 2A, el más alto nivel de la producción LicKM se puede lograr con las cepas GV3101, A4 y LBA4404 (~ 1750 ± 163, 1650 ± 26 y 1450 ± 117 mg / kg, respectivamente), con ligeras diferencias; el nivel más bajo de expresión (~ 900 ± 102 mg / kg) con C58C1; y la producción intermedia con At6, At10 y At77 (~ 1250 ± 19, 1100 ± 42 y 1200 ± 111 mg / kg, respectivamente). La actividad enzimática liquenasa se demostró usando el ensayo de Zimograma. Figura 2B muestra que liquenasa producen en tejidos de las plantas infiltradas usando cualquiera de losCepas de Agrobacterium era enzimáticamente activa. También hay que señalar que las plantas de N. benthamiana infiltrados con cepas A4 y At77 mostró síntomas patológicos (retraso del crecimiento, elongación pecíolo y se encrespan, y la hoja de curling), mientras que con la cepa At10 los síntomas fueron leves. No se observaron síntomas en plantas de N. benthamiana infiltrados con la cepa GV3101 de laboratorio (Figura 2C).
La infiltración de especies alternativas de Nicotiana. Comparamos las tasas de generación de biomasa y la producción de proteínas en dos especies de tipo salvaje del género Nicotiana (N. benthamiana y N. excelsior) y en una especie híbrida, N. excelsiana (N. benthamiana × N. excelsior). De las especies ensayadas, N. benthamiana, una gran cantidad ampliamente utilizado para la producción de proteína transitoria mediante sistemas de expresión basados en Agrobacterium o basados en virus 2,34,49, llega a la preparación la infiltración dentro de 4-5 semanas de germinación. El período de crecimiento necesario para generar el nivel óptimo de biomasa también es de 4-5 semanas para N. excelsiana pero es más prolongado (6-7 semanas) para N. excelsior. Además, los entrenudos de plantas son relativamente cortos para N. Excelsior en comparación con otras especies de Nicotiana.
Asimismo, se observó que la infiltración de vacío de N. benthamiana y N. excelsiana a 50-250 mbar durante 60 segundos es muy eficiente para agroinfiltration de hojas enteras, mientras que N. Excelsior es difícil de infiltrar debido a sus dosel y correosas hojas inferiores, incluso cuando se aplicó un vacío tres veces durante 1 minuto cada uno en la presencia de tensioactivos no iónicos tales como Sillwet-77 o S240. Además, la tasa de germinación de N. excelsiana y N. semillas excelsior fue ~ 40-50%; con el fin de aumentar la tasa de germinación de 90-100%, semillas deben ser tratados con 10% Bleach durante 1 hora antes de la siembra. Bajo las mismas condiciones de crecimiento, la biomasa de hojas más alta que puede ser generada de N. excelsiana es aproximadamente dos veces mayor en comparación con N. benthamiana (Tabla 1).
La producción de proteínas fue examinado en N. benthamiana, N. excelsior y N. excelsiana infiltra con la cepa GV3101 de Agrobacterium que alberga pBID4-GFP. La acumulación de GFP se evaluó a los 7 dpi en las hojas infiltradas enteros usando luz UV seguido por análisis de transferencia Western. Figura 3A muestra una distribución uniforme de GFP en N. benthamiana y N. excelsiana y distribución desigual en N. excelsior (debido a la dificultad de la infiltración de un área de la hoja entera de N. excelsior). Figura 3B muestra el nivel de la producción de GFP estimado por iluminación con luz UV en las hojas infiltradas recogidos de las tres especies de Nicotiana en 7 dpi. La acumulación de GFPnivel mento fue mayor en N. benthamiana (~ 2,23 g / kg) que en N. excelsiana y N. Excelsior (~ 1,89 y 1,54 g / kg, respectivamente). El bajo nivel de la producción de proteínas en N. excelsior se debe a la infiltración y distribución de GFP acumulado en la hoja de recogida desigual.
Hemos observado que las hojas superiores expuestas directamente a la luz a menudo presentan los niveles más tempranos y más altos de acumulación de GFP transitorio (2-4 dpi) que las hojas bajo el dosel. Sin embargo, en nuestros estudios, la acumulación de GFP fue la más alta a los 7 dpi y se distribuye uniformemente a través de la mayoría de las hojas, excepto en hojas no infiltrados recién crecientes que no muestran la acumulación de GFP.
Efectos de la presión de vacío y la duración de la producción de proteína transitoria. Vacío infiltración aumenta significativamente los niveles de expresión transitoria que comparan a la presión aplicada por inyección mano con una jeringa sin aguja 42. La aplicación de unde vacío hace que los gases a evacuar de planta sumergida sale a través de los estomas. Cuando se rompe el vacío y la presión aumenta rápidamente, la suspensión de Agrobacterium se conduce en hojas para reemplazar los gases evacuados 50.
Para probar el efecto de la presión de vacío en las hojas de N. benthamiana, que se infiltró en las plantas con la cepa GV3101 de Agrobacterium que alberga pBID4-GFP bajo varias presiones de vacío (50-400 mbar) durante 30 o 60 segundos. Se demostró que el vacío más fuerte (por debajo de 50 mbar) aplicada durante 30 o 60 segundos en los resultados de los daños mecánicos de las hojas infiltradas, que conduce a marchitamiento tejido y muerte de la planta poco después de la infiltración (24-48 h). Por otro lado, la aplicación del vacío más suave (400 mbar) da como resultado la infiltración de sólo el 50% de la superficie de la hoja y un nivel disminuido de producción de GFP (303 ± 90 mg / kg) (Figura 4A). Es importante destacar que se observó ninguna diferencia en la producción de GFP bajo 50, 100 y 200 mbar (1.651 ± 107, 1688 ± 40, 1594 ± 26 mg / kg, respectivamente) (Figura 4A) y leve o no, efectos perjudiciales sobre la salud de la planta cuando se aplicaron presiones de vacío 50 a 200 mbar durante 30 o 60 seg. Por lo tanto, se recomienda 50 a 100 mbar de presión de vacío para los experimentos de infiltración.
El efecto de la duración del vacío sobre la expresión diana se evaluó mediante la infiltración de una plana de N. benthamiana plantas cada hora con una A 600 de 0,5 de GV3101 que albergan pBID4 -. GFP durante 8 h en el mismo cultivo de Agrobacterium Figura 4B muestra que el nivel de la producción de GFP fue similar en todos los puntos de tiempo de hasta 8 horas, lo que sugiere que en este período de tiempo que el de Agrobacterium mantiene su capacidad de lanzar un ADN de una sola hebra.
Efecto de la inducción química en la producción de proteínas. Algunos metabolitos fenólicos vegetales y azúcares pueden indgenes de virulencia de UCE A. tumefaciens 1,52. Como consecuencia, se ha informado de muchos productos químicos y monosaccharaides para mejorar la producción de proteína transitoria en varias especies de plantas. Acetosiringona se añade más comúnmente a cultivos de A. tumefaciens para inducir el operón vir antes agroinfiltration 40,53-57.
Hemos evaluado el efecto de diferentes concentraciones de acetosiringona (0, 100, 200 y 400 micras) y de glucosa (0-4%) en la producción de proteína GFP transitoria en N. benthamiana infiltra con la cepa GV3101 de Agrobacterium que alberga pBID4 - GFP. Para este propósito, células de Agrobacterium en medio de inducción de MMA que contienen diferentes concentraciones de acetosiringona y glucosa durante 1-3 horas antes de la infiltración que una re-suspensión. De acuerdo con los resultados tanto de observación visual (datos no mostrados) y análisis de transferencia Western (Figura 4C), ninguna de las concentraciones probadasde estos compuestos inducida por un aumento significativo de la fluorescencia de GFP o la producción de proteínas en comparación con el control donde los medios de inducción no contenían acetosiringona o glucosa.
Efecto de la co-infiltración de un supresor de silenciamiento en la producción transitoria de los genes GFP y HAC1 en N. benthamiana deja. Se ha demostrado previamente que la co-expresión de un supresor de silenciamiento (p19 del virus del enanismo arbustivo del tomate [TBSV]) interfiere con el post-transcripcional silenciamiento génico (PTGS), lo que resulta en una mayor producción de proteínas informadoras 34.
Hemos evaluado el efecto de la co-infiltración de N. benthamiana con el vector de lanzamiento que lleva el gen GFP reportero (pBID4-GFP) y p19. Antes de la infiltración, una A600 de 0,5 diluciones de A. culturas tumefaciens GV3101 que albergan pBID4-GFP y p19, respectivamente, se mezclaron en proporciones de 01:01, 02:01, 03:01 y 04:01. expresoiones del supresor de silenciamiento fue controlada por el promotor del virus del mosaico de la coliflor 35S. Como se indica por los resultados de análisis de transferencia Western a los 7 dpi (Figura 5A), la presencia de p19 no aumentar o disminuir la producción de GFP en N. benthamiana, en cualquier proporción de las dos suspensiones de Agrobacterium.
También hemos comparado los efectos de dos genes supresores de silenciamiento viral - p19 p23and - sobre la prevención de PTGS para HAC1. Los cultivos de Agrobacterium que llevan el vector de lanzamiento pBID4-HAC1 (H1N1 A/California/04/2009) y uno de los dos plásmidos supresores de silenciamiento virales se diluyeron a una A 600 de 0,5, mezclado en una proporción de 4:01, respectivamente, y co-infiltrado en 4-5-semanas de edad N. benthamiana. Una suspensión de A. tumefaciens que llevan pBID4 - HAC1 solo se infiltró como control. Las muestras de hojas infiltradas se recogieron de 3 a 8 dpi. El experimento fue repeATED tres veces y los niveles medios de la expresión HAC1 determinaron por análisis de transferencia de Western.
Como se demuestra en la Figura 5B, co-infiltración de N. benthamiana con p23 o p19 dio lugar a (642 ± 157 y 764 ± 108 mg / kg, respectivamente) un aumento en la producción de HAC1 en comparación con el uso de ningún supresor de silenciamiento (aproximadamente 15-25%, respectivamente) a las 6 dpi. Esto sugiere que p23 y p19 son eficientes en nuestro sistema. Sin embargo, hay que señalar que la acumulación de HAC1 se produjo un día antes, cuando pBID4-HAC1 fue co-infiltrada con p19. Por lo tanto, nuestros resultados demuestran que los efectos de la p19 supresor de silenciamiento en HAC1 y la acumulación de GFP son diferentes, lo que sugiere la mejora selectiva de la expresión y / o la estabilidad de algunas proteínas en N. transitoria benthamiana.
También se observó que tanto en la presencia y en la ausencia de un supresor de silenciamiento el nivel de la proteína PROD HAC1ucción comenzó a declinar a los 7 dpi. Esto indica que el momento de la caída de la producción de proteína transitoria en N. benthamiana infiltrado con el vector de lanzamiento es específica de la diana.
El banco de células de Agrobacterium que alberga el vector de lanzamiento se evaluó cada año para la estabilidad del gen diana, la viabilidad de Agrobacterium y el nivel de acumulación de la proteína. El glicerol balance del banco de células de la cepa GV3101 transformado con pBID4-HAC1 que se almacenó a -80 ° C se ha demostrado para ser muy estable durante más de tres años sin cambios en el nivel de producción de proteína transitoria en N. infiltrada benthamiana plantas. Figura 5C muestra que la producción de proteínas HAC1 estimado por Western Blot en los años de 2010, 2011, 2012 y 2013 fue de 670, 685, 566 y 683 mg / kg, respectivamente. La producción media HAC1 en N. benthamiana plantas fue de 651 ± 49,4 mg / kg.
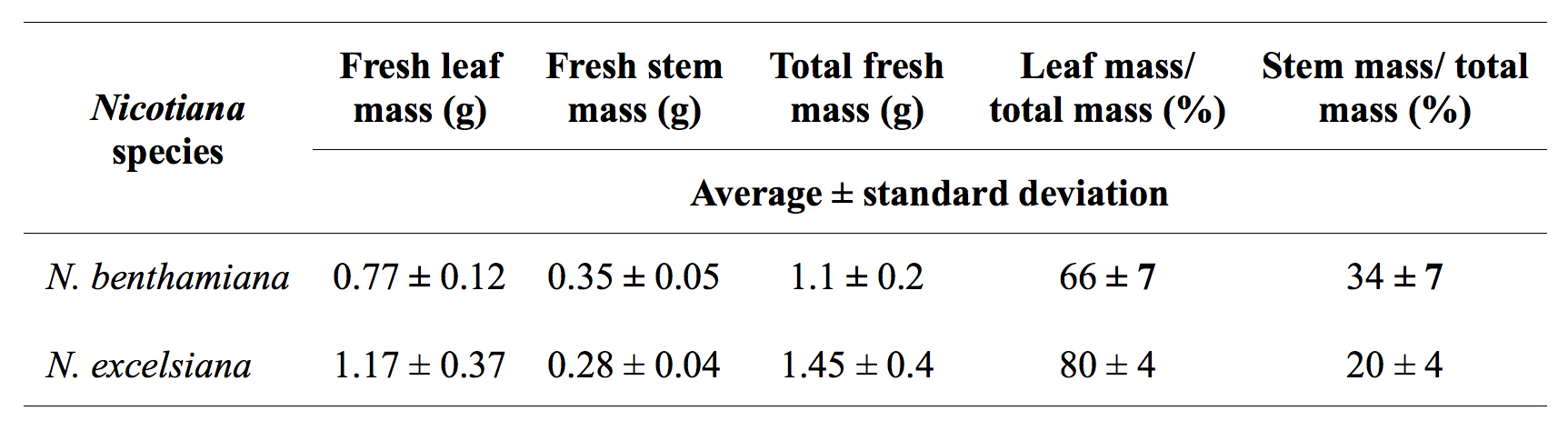
Tabla 1. Comparación de N. benthamiana y N. producción de biomasa vegetal excelsiana.
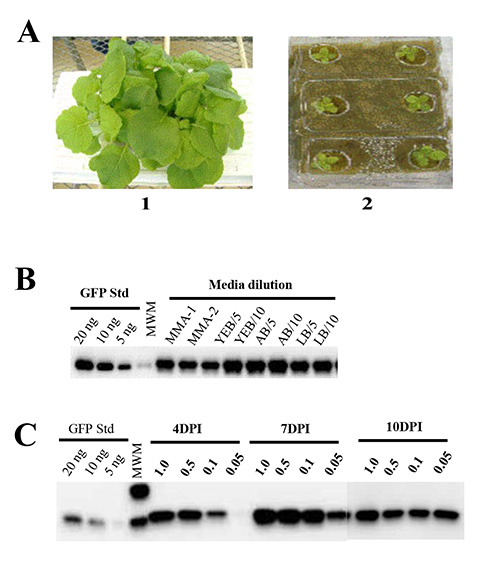
Figura 1. Análisis de transferencia de Western de la expresión génica transitoria en N. benthamiana. (A) N. de seis semanas de edad, benthamiana 1) las plantas que crecen en una solución de fertilizante que contiene 4,8% de fósforo y 2) las plantas que crecen en una solución de fertilizante que contiene 0% de fósforo. Veinticinco por g de peso fresco de hoja equivalente fue cargado por carril. (B) Comparación de la producción de GFP en las plantas de vacío infiltrada con PBID4-GFP albergar culturas Agrobacterium GV3101 cultivadas en tres medios diferentes: YEB, AB y LB. Culturas GV3101 cultivan O / N en YEB o medio LB se centrifugaron a baja velocidad y se resuspendieron en medio de inducción (MMA) (carriles: MMA-1 y MMA-2, respectivamente), o se cultivan de O / N en YEB, LB o Media AB y directamente diluido a 1:05 o 1:10 con agua Milli-Q (carriles: YEB / 5 y YEB/10; AB / 5 y AB/10; LB / 5 y lb/10) (C) de comparación. de la expresión de GFP a las 4, 7 y 10 dpi siguientes infiltración al vacío con diferentes concentraciones de (A 600 de 1,0, 0,5, 0,1 y 0,05) de A. tumefaciens cepa GV3101 llevar pBID4-GFP.
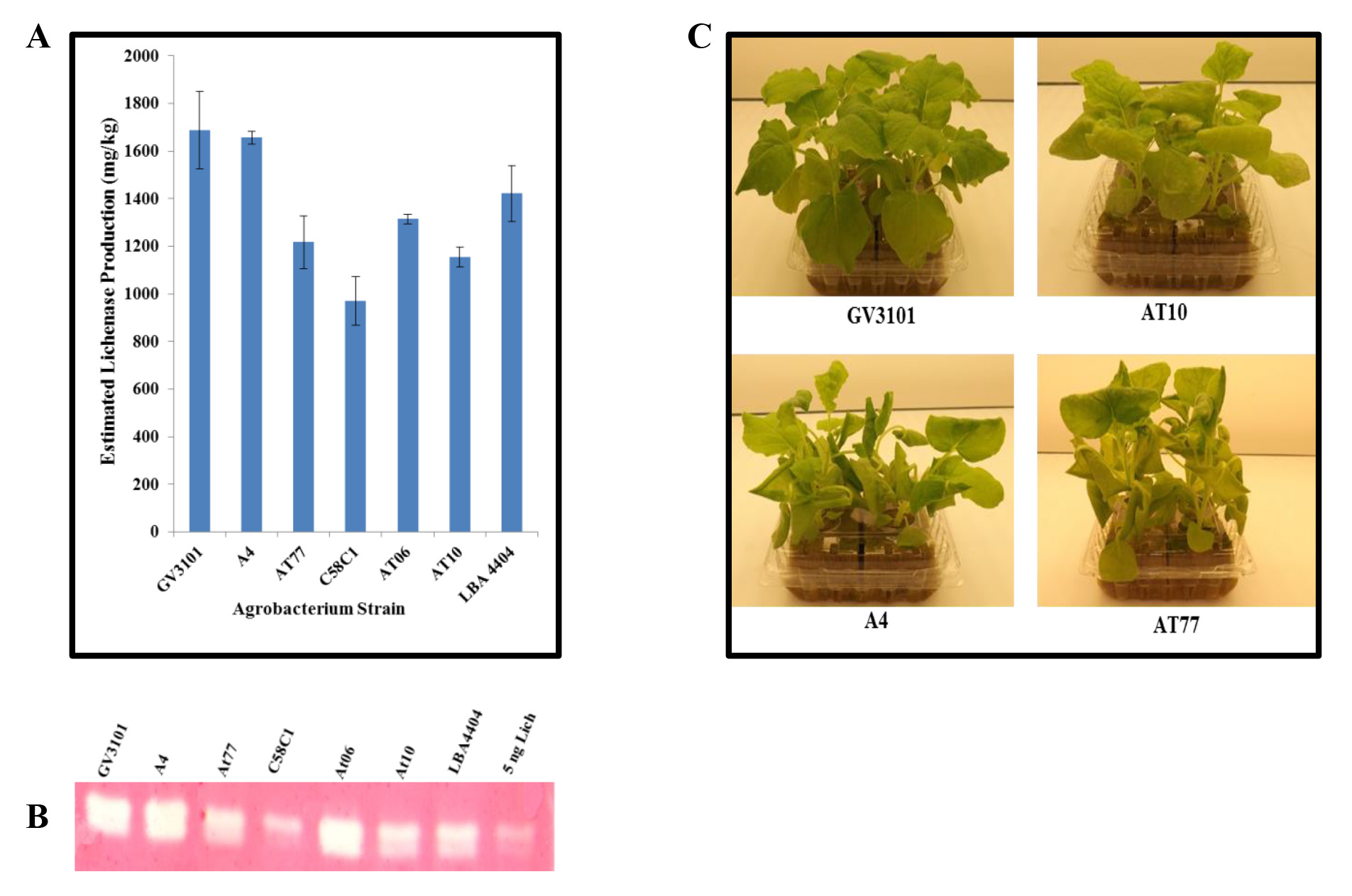
Figura 2. Comparación de la producción liquenasa transitoria y la actividad después de la infiltración de vacío de N. benthamiana plantas con difealquilar cepas de Agrobacteria. Las cepas de Agrobacteria (GV3101, A4, At77, C58C1, AT6, AT10 y LBA4404) que albergan el vector de lanzamiento pBID4-LicKM fueron infiltrados individualmente en hojas de N. benthamiana. Hojas infiltradas se recogieron a los 7 dpi. (A) liquenasa producción cuantificado por transferencia de Western. (B) ensayo de Zimograma demostrando la producción liquenasa través de la actividad enzimática. (C) Efecto de Agrobacterium (de tipo salvaje A4, At10, At77 y cepa de laboratorio GV3101) infiltración en N. benthamiana salud de las plantas a los 7 dpi. Veinticinco g de peso fresco de hoja equivalente fue cargado por carril.
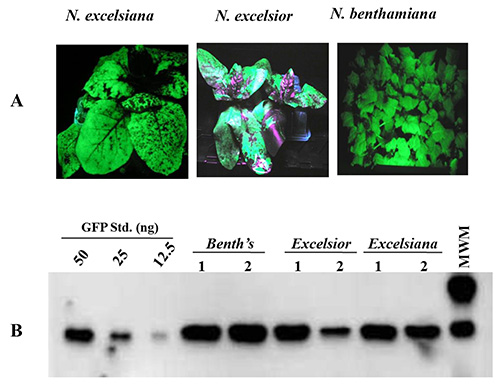
Figura 3. Transitoria la expresión de GFP en hojas de N. benthamiana, N. y N. excelsiana excelsior a los 7 dpi después de la infiltración de vacío con A. tumefaciens que alberga el lanzamiento vector pBID4 - GFP. (A) El examen visual de la expresión de GFP bajo luz UV. (B) Western blot de la acumulación de las buenas prácticas agrarias.
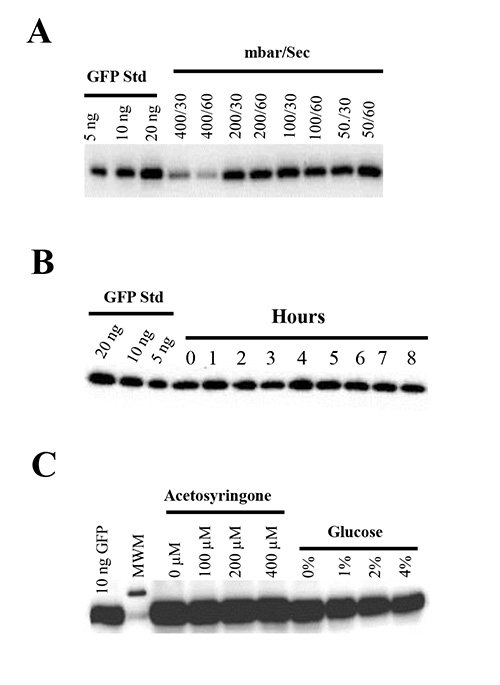
Figura 4. (A) Efectos de la presión de vacío en la expresión de GFP transitoria y la sanidad vegetal. N. benthamiana plantas se infiltraron con pBID4 -. GFP bajo presiones de vacío de 400, 200, 100 o 50 mbar, al tiempo de mantenimiento del vacío de 30 o 60 segundos (B) Estabilidad y la infectividad de A. Agrobacterium en N. benthamiana se infiltró con Agrobacterium GV3101 que albergan pBID4-GFP cultivó en medio AB y se diluyó a una A 600 de 0,5. Agroinfiltration se realizó mediante la infiltración de una plana de N. benthamiana plantas cada hora en el mismo cultivo diluido de Agrobacterium (carriles 0-8). (C) Efecto de diferentes concentraciones de acetosiringona y la glucosa en la expresión transitoria de GFP. La cepa GV3101 de Agrobacterium que alberga pBID4 - GFP se cultiva O / N en medios YEB, se centrifugó y se resuspendió a una A 600 de 0,5, ya sea en MMA que contiene 2% de glucosa con acetosiringona a 0, 100, 200 o 400 mM, o en MMA que contiene 200 acetosiringona M con glucosa a 0, 1, 2 o 4%. Las suspensiones de Agrobacterium se mantuvieron durante 3 horas a temperatura ambiente antes de la infiltración.
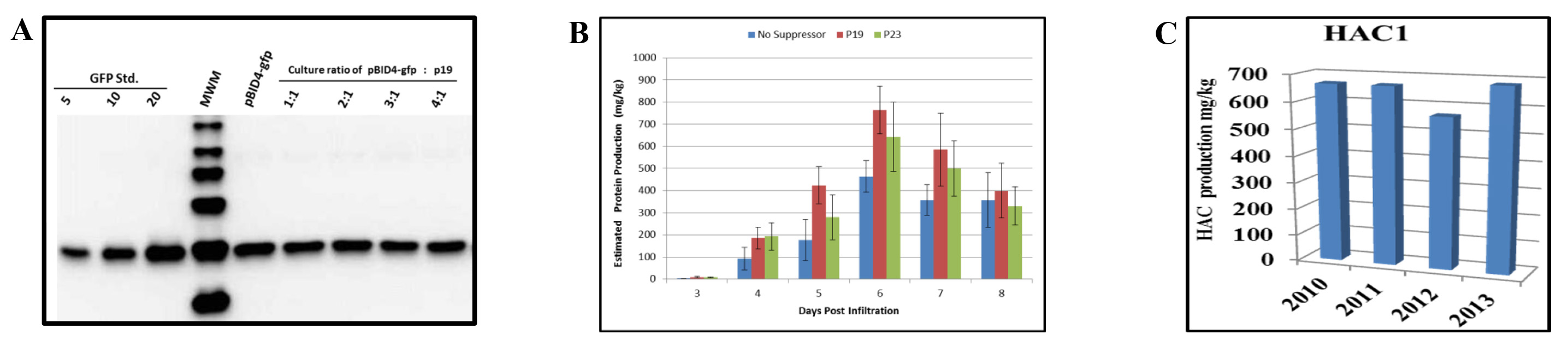
Figura 5. Efectos de silenciamiento de los supresores de la producción de proteína transitoria en N. benthamiana deja. (Un) Análisis de transferencia Western de la proteína GFP después de la co-infiltración de pBID4-GFP y p19 en diferentes proporciones. Las muestras recogidas a los 7 dpi (25 g de peso fresco de hoja equivalente fue cargado por carril). (B) Un cultivo de Agrobacterium llevando pBID4-HAC1 se mezcló de forma individual en una proporción de 4:01 con una cultura que lleva el p19 o p23 supresor de silenciamiento plásmidos. Las combinaciones resultantes de cultivos de Agrobacterium fueron de vacío se infiltraron en las plantas. Tejidos infiltrados de HAC1 se recolectaron diariamente hasta 8 ppp para la cuantificación de proteínas recombinantes. (C) Estabilidad del banco de células de Agrobacterium. Las plantas se infiltraron con el mismo lote de la banco de células de Agrobacterium cada año para evaluar la acumulación de proteínas. Cincuenta g de peso fresco de hoja equivalente fue cargado por carril. Haga clic aquí para ver una versión más grande de thes figura.
Discusión
En este estudio, hemos desarrollado un protocolo agroinfiltration simple para la producción de proteína transitoria de rutina en las especies de Nicotiana seleccionados utilizando cepas de Agrobacterium que llevan el vector de lanzamiento. Además, hemos identificado las condiciones óptimas para lograr el nivel más alto de producción de proteína recombinante en nuestro sistema de expresión de la planta transitoria.
Infiltración de vacío de la A. tumefaciens GV3101 diluida cepa que alberga los pBID4 vector de lanzamiento en N. benthamiana, N. excelsiana y N. Excelsior resultaron en niveles más altos de producción de proteína diana dentro de 7 dpi en comparación con otras especies de plantas, tales como Pisum sativum infiltrado con GV3101 que albergan el virus del mosaico de la alfalfa - o del mosaico del pepino vectores basados en virus que expresan el gen reportero GFP bajo el promotor 35S 41, o Lactuca sativa, Solanum lycopersicumpersicum y Arabidopsis thaliana infiltrado con la cepa de A. C58C1 tumefaciens que portan el gen reportero de beta-glucuronidasa 57. N. benthamiana y N. excelsiana fuera fácil para aspirar infiltrarse a 50 mbar durante 30-60 segundos, con 90-95% de eficiencia de la infiltración. El 5-10% restante del área de la hoja no se infiltró a causa de algún flotante de hojas en la superficie de la suspensión de Agrobacterium durante la aplicación del vacío. Dado que el vector de lanzamiento tiene capacidad para el movimiento de célula a célula 18, la acumulación de proteína transitoria se produce en hojas enteras, así como los pecíolos a 7 dpi. A 10 dpi, la producción estimada de GFP fue ligeramente inferior debido a que el vector de expresión pBID4 es capaz de pasar de célula a célula, pero no para mover sistémicamente 18; por lo tanto, las hojas recién crecido no contienen el vector y no contribuyen a la producción de la meta. Además, la degradación de la proteína recombinante con el tiempo mAy contribuir a reducir el nivel de proteína en 10 dpi. Nuestros resultados mostraron que la infiltración de la A. altos niveles tumefaciens cepa GV3101 mediadas de la producción de proteína transitoria en N. benthamiana. Por otra parte, la proteína objetivo puede ser diseñado como fusiones N-terminales, C-terminales o internos a liquenasa (LicKM), β-1 ,3-1 ,4-glucanasa, que es una enzima termoestable a partir de Clostridium thermocellum y confiere termoestabilidad a muchos objetivo la proteína de fusión 18. Infiltración de N. benthamiana con A. tumefaciens cepas de tipo salvaje (AT6, AT10 y at77) que albergan el gen de interés provocado síntomas leves o graves encresparse hoja, pecíolo de elongación, y se encrespan. No se observaron síntomas patológicos en N. benthamiana infiltra con la cepa GV3101 de laboratorio que alberga el vector vacío pBID4, mientras que algunos genes insertados en pBID4 y se transforma en laboratorio cepas GV3101, C58C1 o LBA4404 suscitó reacciones necróticas suaves y hojasclorosis / síntomas de amarillamiento en las regiones infiltrados de hojas. Síntomas necróticos causados por Agrobacterium de tipo salvaje o cepas desarmadas en las plantas solanáceas se ha informado anteriormente 56,57. La respuesta necrótica puede resultar de factores de virulencia del sistema de secreción de tipo III, proteínas bacterianas transferidos a la célula vegetal por el sistema de secreción de tipo IV, y / o sensibilidad a la flagelina 58-60. Hemos encontrado que la producción transitoria de proteínas heterólogas también puede provocar la patogenicidad y una respuesta hipersensible en planta infiltrado hojas. Muchos investigadores informaron que agroinfiltración de diferentes especies de plantas con vectores binarios de plantas producidas hasta 5-20 veces los niveles más altos de producción de proteína transitoria en comparación con plantas transformadas de forma estable 28,57. Nuestros datos muestran que N. benthamiana se infiltró con GV3101 que albergan pBID4-GFP altos niveles expresados transitoriamente de GFP, que es similar a la reportada para el rendimiento de GFPN. benthamiana se infiltró con Agrobacterium que lleva el vector viral Pich-GFPSYS (hasta 80% de proteína soluble total) 44. Agroinfiltration utilizando nuestro vector de lanzamiento resultó en alta producción de la proteína LicKM termoestable, 50 veces mayor que la observada usando un plásmido binario estándar de 18.
Para probar la infectividad de A. tumefaciens y la estabilidad del vector de lanzamiento, que se infiltraron en un plano de N. benthamiana cada hora durante un máximo de 8 horas con el mismo cultivo diluido en agua Milli-Q de GV3101 que alberga el plásmido pBID4-GFP. Nuestros datos muestran que la cepa GV3101 es infeccioso eficaz durante al menos 8 horas y pBID4 (el vector de lanzamiento) es muy estable durante el tiempo de 8 horas la infiltración.
Glicerol de la cepa GV3101 que alberga el vector de lanzamiento pBID4-HAC1 (banco de células) se almacenan a -80 ° C se ha demostrado para ser muy estable durante tres años sin cambios en prote transitoriaen la producción en plantas infiltradas.
Plantas de N. benthamiana cultivadas en condiciones óptimas y entre 35 y 42 días después de la siembra fueron óptimas para vacío infiltración mediada por la expresión génica transitoria 40. Plantas más jóvenes (3-4 semanas de edad) no pueden ser infiltrados por completo a causa de las hojas que flotan en la superficie de la suspensión celular y daño en los tejidos de los efectos mecánicos de la aplicación de vacío. En las plantas de más de 45 días, N. benthamiana atornillar etapa, en las condiciones óptimas de luz utilizados, el nivel de expresión transitoria es baja.
Los compuestos de bajo peso molecular fenólicos (acetosiringona) y monosaccharaides (glucosa) se sabe que inducen genes vir en A. tumefaciens 55,61. Por otra parte, la infiltración de N. benthamiana con el vector pCAMBIA binario (GFP) en la presencia de acetosiringona en las concentraciones de 50-600 mM, se mostró a aumentar ligeramente transitoriala expresión del gen 40. Se estudió el efecto de diferentes concentraciones de acetosiringona y la glucosa en nuestro sistema mediante la adición de estos compuestos a las culturas GV3101 que albergan pBID4-GFP en las MMA durante 3 horas, y se encontraron diferencias en la expresión de GFP. Curiosamente, culturas GV3101 que albergan pBID4-GFP y diluidas en agua Milli-Q para una A 600 de 0,5 y se infiltraron sin la inducción de genes vir expresaron las mismas cantidades de GFP como aquellos infiltrado con los cultivos inducidos. El A. gen vir tumefaciens (s) potencialmente podría ser inducida por los compuestos fenólicos vegetales (acetosiringona y el ácido sinapínico) y monosaccharaides de plantas (glucosa y fructosa) presentes en el tejido de la hoja. Por lo tanto, se especula que niveles similares de expresión de GFP en presencia o ausencia de inductores exógenos de genes vir pueden ser el resultado del efecto de citoplásmicos inductores de genes vir presentes durante la replicación de la puesta en marcha del vector que expresa GFP en las células vegetales.
Wild-tipo N. benthamiana se ha utilizado como un modelo de acogida para la producción de proteína transitoria 49. Sin embargo, relativamente bajo rendimiento de biomasa de N. benthamiana 's dificulta su aplicación para la producción a gran escala de proteínas recombinantes. El anfitrión óptima debe combinar un alto nivel de expresión transitoria, fácil crecimiento en un invernadero, y ser susceptible a la infiltración de Agrobacterium 2. Para seleccionar un huésped alternativo, hemos infiltrado en dos especies de tipo salvaje diferentes de Nicotiana (N. benthamiana y N. excelsior) y un híbrido N. excelsiana (N. benthamiana × N. excelsior) con la A. tumefaciens GV3101 cepa que alberga el plásmido pBID4-GFP. Entre estas tres especies, el nivel de expresión de GFP fue ligeramente superior en N. . N. benthamiana plantas excelsior mostraron dificultad para agroinfiltration vacío debido a sus hojas coriáceas y N. excelsianaproducido aproximadamente dos veces más biomasa en las mismas condiciones de crecimiento. La producción transitoria de GFP a los 7 dpi es relativamente similar en N. benthamiana y N. excelsiana. Por lo tanto, N. excelsiana puede ser un anfitrión más adecuado para la producción de proteína recombinante.
La producción de proteína transitoria mediada por Agrobacterium está limitada por PTGS 26, que puede ser superado por la co-expresión de silenciamiento de genes supresores de origen virus de la planta 62. La producción de proteína transitoria ha sido previamente demostrado ser mejorado 50 veces en la presencia de la proteína p19 de TBSV, que inhibe PTGS en tejidos infiltrados 34. En nuestro estudio, se evaluó el efecto de dos supresores de silenciamiento virales (p19 y p23) por separado co-infiltrado con el vector de lanzamiento pBID4-HAC1. La co-infiltración de estos supresores de silenciamiento parecía tener poca influencia sobre la expresión transitoria de HAC1, con sólo un ligero aumento en HAC1la acumulación de proteínas (15-25%) en la presencia de p23 co-infiltrada o p19. Para influir positivamente en la producción de proteínas, pueden necesitar ser seleccionado específicamente para ser eficaz para las especies de plantas específicas y vector vírico 63 supresores de silenciamiento. TMV helicasa tiene un supresor de la actividad de silenciamiento de ARN 64,65. Nuestros datos confirman esta observación como co-infiltración de p23 o p19 con pBID4-HAC1 dio lugar a ningún aumento de GFP o un ligero aumento en la producción de proteínas HAC1 transitoria.
En conclusión, se ha modificado y optimizado las condiciones de crecimiento de Agrobacterium y las plantas y la mejora de la eficiencia de infiltración al vacío. Esta tecnología nos permitió crecer y de infiltrarse en cientos de kilogramos de material vegetal en unas pocas horas. Éxito automatizamos la técnica de la expresión transitoria planta para la producción de vacunas de alto rendimiento a escalas industriales bajo las actuales prácticas correctas de fabricación (cGMP) condiciones. Para obtener más información aboautomatización ut y utilización del sistema de la planta transitoria de la producción de proteínas para la producción de proteínas recombinantes, incluyendo candidatos a vacuna subunidad, en condiciones de cGMP, se recomienda acudir a la página web www.fhcmb.org/ .
Divulgaciones
No tenemos nada que revelar.
Agradecimientos
Este trabajo fue apoyado por Fraunhofer EE.UU. Centro para la Biotecnología Molecular, Ibio, Inc. y la Agencia de Proyectos de Investigación Avanzada de Defensa (subvención # HDTRA1-07-C-0054). Los autores agradecen los regalos generosos por los Dres. Stanton Gelvin de Ciencias Biológicas Departamento de la Universidad de Purdue (Agrobacterium tumefaciens cepas) y Wayne Fitzmaurice de Gran Escala Biología Corp. (semillas excelsiana N.), así como Jennifer Nicholson Colección de Nicotiana EE.UU., la Universidad Estatal de Carolina del Norte (semillas excelsior N. ). Los autores agradecen a Margaret Shillingford y Christopher casco para proporcionar plantas y su excelente asistencia técnica. Los autores también agradecen a los Dres. Stephen Streatfield y Natasha Kushnir por su asistencia editorial.
Materiales
| Name | Company | Catalog Number | Comments |
| Nicotiana benthamiana | Tobacco Germplasm Collection, Crop Science Dept., North Carolina State University | PI 555478 TW16 | Infiltration |
| Nicotiana excelsior | Tobacco Germplasm Collection, Crop Science Dept., North Carolina State University | PI 555685 TW47 | Infiltration |
| Nicotiana excelsiana | Dr. Wayne Fitzmaurice, Large Scale Biology Corporation, Vacaville, CA | LSBC EBA 042304.02 | Infiltration |
| Vacuum skid | Abbas, Ashland, MA | Custom made | Plant infiltration |
| Rockwool | Grodan Inc., Ontario, Canada | AO 50/40 | Hydroponic media for growing plant |
| 2-(N-Morpholino) ethanesulfonic acid | Acros Organics, Thermo Fisher Scientific, NJ | 172595000 | Buffer |
| Murashige & Skoog salt (MS salt) | Phyto Technology Lab | M524 | Tissue culture media |
| Acetosyringone | Sigma-Aldrich, St. Louis, MO | D134406-5G | Agrobacterium induction |
| Immobilon-P transfer membrane | Millipore, Billerica, MA | IPVH00010 | Western blotting |
| I-block | Applied Biosystems, Foster City, CA | T2015 | Western blotting |
| Rabbit polyclonal anti-GFP antiserum | Washington Biotechnology, Baltimore, MD | Western blotting | |
| Mouse anti–poly-histidine monoclonal antibody | Qiagen GmbH, Hilden | 34670 | Western blotting |
| Horseradish peroxidase-conjugated anti-rabbit antibody | Jackson ImmunoResearch, West Grove, PA | 111-035-003 | Western blotting |
| Horseradish peroxidase-conjugated anti-mouse antibody | Jackson ImmunoResearch, West Grove, PA | 115-035-003 | Western blotting |
| SuperSignal® West Pico chemiluminescent substrate | Thermo Scientific Pierce, Rockford, IL | 34078 | Western blotting |
| Lichenan (1-3: 1-4-beta-D-glucan) | Megazyme, Bray, Co. Wicklow, Ireland | P-LICHN | Lichenase Activity |
| Congo Red | Sigma-Aldrich, St. Louis, MO | C6277 | Gel staining |
| Digital camera | Olympus, Center Valley, PA | C-8080 | Chemiluminescence imaging |
| GeneGnome | Syngene, Frederick, MD | Chemiluminescence imaging | |
| GFP standard | Made in house | Chemiluminescence imaging | |
| Plant fertilizer solution | Griffin Greenhouse Nursery Supplies, Newark, DE | 67-23-20 | Plant growing |
| Lichenase Standard | Purified in house | Western blotting | |
| MicroPulser Electroporator | BioRad, Hercules, CA | 165-2100 | Agrobacterium transformation |
Referencias
- Ma, J. K., Drake, P. M., Christou, P. The production of recombinant pharmaceutical proteins in plants. Nature Reviews Genetics. 4, 794-805 (2003).
- Sheludko, Y. V., Sindarovska, Y. R., et al. Comparison of several Nicotiana species as hosts for high-scale agrobacterium-mediated transient expression. Biotechnology and Bioengineering. 96, 608-614 (2007).
- Mett, V., Farrance, C. E., Green, B. J., Yusibov, V. Plants as biofactories. Biologicals. 36, 354-358 (2008).
- Yusibov, V., Rabindran, S. Recent progress in the development of plant derived vaccines. Expert Review of Vaccines. 7, 1173-1183 (2008).
- Stoger, E., Sack, M., Fischer, R., Christou, P. Plantibodies: Applications, advantages and bottlenecks. Current Opinion in Biotechnology. 13, 161-166 (2002).
- Mahmoud, K. Recombinant Protein Production: Strategic Technology and a Vital Research Tool. Research Journal of Cell and Molecular Biology. 1, 9-22 (2007).
- Rai, M. P. H. Expression systems for production of heterologous proteins. Current Science. 80, 1121-1128 (2001).
- Yusibov, V., Streatfield, S. J., Kushnir, N. Clinical development of plant-produced recombinant pharmaceuticals: vaccines, antibodies and beyond. Human Vaccines. 7, 313-321 (2011).
- McCormick, A. A., Reddy, S., et al. Plant-produced idiotype vaccines for the treatment of non-Hodgkin's lymphoma: Safety and immunogenicity in a phase I clinical study. Proceedings of the National Academy of Sciences of the United States of America. 105, 10131-10136 (2008).
- Medicago Inc, . . , (2013).
- Medicago Inc, . . , (2013).
- Planet Biotechnology Inc, . . , (2013).
- Sys Genetics, S. e. m. B. i. o. . , (2013).
- Protalix, . , (2013).
- Protalix, . , (2013).
- Plesha, M. A., Huang, T. -. K., et al. Optimization of the bioprocessing conditions for scale-up of transient production of a heterologous protein in plants using a chemically inducible viral amplicon expression system). Biotechnology Progress. 25, 722-734 (2009).
- Gleba, Y., Klimyuk, V., Marillonnet, S. Magnification - A new platform for expressing recombinant vaccines in plants. Vaccine. 23, 2042-2048 (2005).
- Musiychuk, K., Stephenson, N., et al. A launch vector for the production of vaccine antigens in plants. Influenza and Other Respiratory Viruses. 1, 19-25 (2007).
- Massa, S., Franconi, R., et al. Anticancer activity of plant-produced HPV16 E7 vaccine. Vaccine. 25, 3018-3021 (2007).
- Mett, V., Lyons, J., et al. A plant-produced plague vaccine candidate confers protection to monkeys. Vaccine. 25, 3014-3017 (2007).
- Mett, V., Musiychuck, K., et al. A plant-produced influenza subunit vaccine protects ferrets against virus challenge. Influenza and Other Respiratory Viruses. 2, 33-40 (2008).
- Shoji, Y., Chichester, J. A., et al. Plant expressed HA as a seasonal influenza vaccine candidate. Vaccine. 26, 2930-2934 (2008).
- Chichester, J. A., Musiychuk, K., et al. Immunogenicity of a subunit vaccine against Bacillus anthracis. Vaccine. 25, 3111-3114 (2007).
- Golovkin, M., Spitsin, S., et al. Smallpox subunit vaccine produced in Planta confers protection in mice. Proceedings of the National Academy of Sciences of the United States of America. 104, 6864-6869 (2007).
- Porta, C., Lomonossoff, G. Use of viral replicons for the expression of genes in plants. Molecular Biotechnology. 5, 209-221 (1996).
- Johansen, L. K., Carrington, J. C. Silencing on the spot: induction and suppression of RNA silencing in the Agrobacterium-mediated transient expression system. Plant Physiology. 126, 930-938 (2001).
- Vézina, L. P., Faye, L., et al. Transient co-expression for fast and high-yield production of antibodies with human-like N-glycans in plants. Plant Biotechnology Journal. 7, 442-455 (2009).
- Vaquero, C., Sack, M., et al. Transient expression of a tumor-specific single-chain fragment and a chimeric antibody in tobacco leaves. Proceedings of the National Academy of Sciences of the United States of America. 96, 11128-11133 (1999).
- Galeffi, P., Lombardi, A., et al. Expression of single-chain antibodies in transgenic plants. Vaccine. 23, 1823-1827 (2005).
- Rodríguez, M., Ramírez, N. I., et al. Transient expression in tobacco leaves of an aglycosylated recombinant antibody against the epidermal growth factor receptor. Biotechnology and Bioengineering. 89, 188-194 (2004).
- Hull, A., Criscuolo, C. J., et al. plant-produced monoclonal antibody for the treatment of anthrax. Vaccine. 23, 2082-2086 (2005).
- Roy, G., Weisburg, S., Rabindran, S., Yusibov, V. A novel two-component Tobacco mosaic virus-based vector system for high-level expression of multiple therapeutic proteins including a human monoclonal antibody in plants. Virology. 405, 93-99 (2010).
- Silhavy, D., Molnar, A., et al. A viral protein suppresses RNA silencing and binds silencing-generated, 21-to 25-nucleotide double-stranded RNAs. EMBO Journal. 21, 3070-3080 (2002).
- Voinnet, O., Rivas, S., Mestre, P., Baulcombe, D. An enhanced transient expression system in plants based on suppression of gene silencing by the p19 protein of tomato bushy stunt virus. Plant Journal. 33, 949-956 (2003).
- Bechtold, N., Pelletier, G. In planta Agrobacterium-mediated transformation of adult Arabidopsis thaliana plants by vacuum infiltration. Methods in Molecular Biology. 82, 259-266 (1998).
- Bechtold, N., Ellis, J., Pelletier, G. In planta Agrobacterium mediated gene transfer by infiltration of adult Arabidopsis thaliana plants. C. R. Academy of Science Paris, Life Sciences. 316, 1194-1199 (1993).
- Tague, B., Mantis, J. In planta Agrobacterium-mediated transformation by vacuum infiltration. Methods in Molecular Biology. 323, 223-215 (2006).
- Fischer, R., Vaquero-Martin, C., et al. Towards molecular farming in the future: transient protein expression in plants. Biotechnology and Applied Biochemistry. 30, 113-116 (1999).
- Horn, M. E., Woodard, S. L., Howard, J. A. Plant molecular farming: systems and products. Plant Cell Reports. 22, 711-720 (2004).
- Wydro, M., Kozubek, E., Lehmann, P. Optimization of transient Agrobacterium-mediated gene expression system in leaves of Nicotiana benthamiana. Acta Biochimica Polonica. 35, 289-298 (2006).
- Green, B. J., Fujiki, M., et al. Transient protein expression in three Pisum sativum (green pea) varieties. Biotechnology Journal. 4, 1-8 (2009).
- Kapila, J., DeRycke, R., Van Montagu, M., Angenon, G. An Agrobacterium-mediated transient gene expression system for intact leaves. Plant Science. 122, 108-101 (1997).
- Yang, Y., Li, R., Qi, M. In vivo analysis of plant promoters and transcription factors by agroinfiltration of tobacco leaves. Plant Journal. 22, 543-551 (2000).
- Marillonnet, S., Thoeringer, C., Kandzia, R., Klimyuk, V., Gleba, Y. Systemic Agrobacterium tumefaciens-mediated transfection of viral replicons for efficient transient expression in plants. Nature Biotechnology. 23, 718-723 (2005).
- Gleba, Y., Klimyuk, V., Marillonnet, S. Viral vectors for the expression of proteins in plants. Current Opinion in Biotechnology. 18, 134-141 (2007).
- Goodin, M. M., Zaitlin, D., Naidu, R. A., Lommel, S. A. Nicotiana benthamiana: Its history and future as a model for plant-pathogen interactions. Molecular Plant-Microbe Interactions. 21, 1015-1026 (2008).
- Shoji, Y., Bi, H., et al. Plant-derived hemagglutinin protects ferrets against challenge infection with the A/Indonesia/05/05 strain of avian influenza. Vaccine. 27, 1087-1092 (2009).
- Llave, C., Kasshau, K. D., Carrington, J. C. Virus-encoded suppressor of posttranscriptional gene silencing targets a maintenance step in the silencing pathway. Proceedings of the National Academy of Sciences of the United States of America. 97, 13401-13406 (2000).
- McCormick, A. A., Kumagai, M. H., et al. Rapid production of specific vaccines for lymphoma by expression of the tumor-derived single-chain Fv epitopes in tobacco plants. Proceedings of the National Academy of Sciences of the United States of America. 96, 703-708 (1999).
- Simmons, C. W., VanderGheynst, J. S., Upadhyaya, S. K. A model of agrobacterium tumefaciens vacuum infiltration into harvested leaf tissue and subsequent in planta transgene transient expression. Biotechnology and Bioengineering. 102, 965-970 (2009).
- Ankenbauer, R. G., Nester, E. W. Sugar-mediated induction of Agrobacterium tumefaciens virulence genes: structural specificity and activities of monosaccharides. Journal of Bacteriology. 172, 6442-6446 (1990).
- Cangelosi, G. A., Ankenbauer, R. G., Nester, E. W. Sugars induce the Agrobacterium virulence genes through a periplasmic binding protein and a transmembrane signal protein. Proceedings of the National Academy of Sciences of the United States of America. 87, 6708-6712 (1990).
- Stachel, S. E., Nester, E. W., Zambryski, P. C. A plant cell factor induces Agrobacterium tumefaciens vir gene expression. Proceedings of the National Academy of Sciences of the United States of America. 83, 379-383 (1986).
- Rogowsky, P. M., Close, T. J., Chimera, J. A., Shaw, J. J., Kado, C. I. Regulation of the vir genes of Agrobacterium tumefaciens plasmid pTiC58. Journal of Bacteriology. 169, 5101-5112 (1987).
- Hiei, Y., Ohta, S., Komari, T., Kumashiro, T. Efficient transformation of rice (Oryza sativa L.) mediated by Agrobacterium and sequence analysis of the boundaries of the T-DNA. Plant Journal. 6, 271-282 (1994).
- Vander Hoorn, J. A. L., Laurent, F., Roth, R., De Wit, P. J. G. M. Agroinfiltration is a versatile tool that facilitates comparative analyses of Avr9/cf-9-induced and Avr4/Cf-4-induced necrosis. Molecular Plant-Microbe Interactions. 13, 439-446 (2000).
- Wroblewski, T., Tomczak, A., Michelmore, R. Optimization of Agrobacterium-mediated transient assay of gene expression in lettuce, tomato and Arabidopsis. Plant Biotechnology Journal. 3, 259-273 (2005).
- Salmond, G. P. C. Secretion of extracellular virulence factors by plant pathogenic bacteria. Annual Review of Phytopathology. 32, 181-200 (1994).
- Felix, G., Duran, J. D., Volko, S., Boller, T. Plants have a sensitive perception system for the most conserved domain of bacterial flagellin. Plant Journal. 18, 265-276 (1999).
- Goodner, B., Hinkle, G., et al. Genome sequence of the plant pathogen and biotechnology agent Agrobacterium tumefaciens C58. Science. 294, 2323-2328 (2001).
- Lee, Y. -. W., Jin, S., Sims, W. -. S., Nester, E. W. Genetic evidence for direct sensing of phenolic compounds by the vir A protein of Agrobacterium tumefaciens. Proceedings of the National Academy of Sciences of the United States of America. 92, 12245-12249 (1995).
- Voinnet, O., Pinto, Y. M., Baulcombe, D. C. Suppression of gene silencing: a general strategy used by diverse DNA and RNA viruses. Proceedings of the National Academy of Sciences of the United States of America. 96, 14147-14152 (1999).
- Voinnet, O. RNA silencing as a plant immune system against viruses. Trends in Genetics. 17, 449-459 (2001).
- Ding, X. S., Liu, J., et al. The Tobacco mosaic virus 126-kDa protein associated with virus replication and movement suppresses RNA silencing. Molecular Plant-Microbe Interactions. 17, 583-592 (2004).
- Harries, P. A., Palanichelvam, K., Bhat, S., Nelson, R. S. Tobacco mosaic virus 126-kDa protein increases the susceptibility of Nicotiana tabacum to other viruses and its dosage affects virus-induced gene silencing. Molecular Plant-Microbe Interactions. 21, 1539-1548 (2008).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados