Method Article
Detección rápida de la transcriptasa inversa del VIH y inhibidores de la integrasa
En este artículo
Resumen
Aquí se describe la citotoxicidad celular y ensayos de infectividad redondas individuales que permiten la detección rápida y precisa de los compuestos para determinar su citotoxicidad celular (CC 50) y los valores de IC50 contra WT y VIH-1 resistente drogas.
Resumen
Aunque un número de medicamentos contra el VIH se han aprobado, todavía hay problemas con la toxicidad y la resistencia a los medicamentos. Esto demuestra la necesidad de identificar nuevos compuestos que pueden inhibir la infección por los resistentes a los medicamentos del VIH-1 cepas comunes con una toxicidad mínima. Aquí se describe un ensayo eficiente que se puede utilizar para determinar rápidamente la citotoxicidad celular y la eficacia de un compuesto frente a las cepas virales WT y mutantes.
La línea celular diana deseada se sembró en una placa de 96 pocillos, y después de una incubación de 24 horas, se añaden seriada diluciones de los compuestos a ensayar. No hay manipulaciones adicionales son necesarios para los ensayos de citotoxicidad celular; para anti VIH Ensayos de una cantidad predeterminada de cualquiera de un WT o VIH-1 resistente vector de medicamento que expresa luciferasa se añade a las células. La citotoxicidad se midió utilizando un ensayo de luminiscencia dependiente de ATP y el impacto de los compuestos sobre la infectividad se mide mediante la determinación de la cantidad de luciferase en la presencia o la ausencia de los inhibidores putativos.
Este ensayo de exploración tarda 4 días en completarse y varios compuestos pueden ser examinados en paralelo. Los compuestos se criban por triplicado y los datos se normalizan a los niveles de infectividad / ATP en ausencia de compuestos diana. Esta técnica proporciona una medición rápida y precisa de la eficacia y la toxicidad de los compuestos potenciales anti-VIH.
Introducción
La disponibilidad de las drogas dirigidas a varios pasos esenciales en el ciclo vital del virus VIH-1 ha llevado a la terapia de combinación de drogas (llamada terapia altamente activa antirretroviral, o HAART) que ha mejorado en gran medida el tratamiento de las infecciones por el VIH-1, y la supervivencia a largo plazo de los pacientes. TARGA, que típicamente utiliza combinaciones de dos nucleósidos de la transcriptasa inversa (RT) y los inhibidores ya sea un inhibidor de proteasa o un inhibidor no nucleósido de la RT, ahora se ha convertido una enfermedad mortal en una condición de vida larga 1-5. Sin embargo, a pesar de los muchos éxitos de la terapia HAART en una supresión sostenida de la replicación viral, tiene limitaciones. TARGA no erradica el VIH, por lo que los pacientes no se curan y el tratamiento es de por vida. Hay problemas con la toxicidad del fármaco y con la aparición de cepas resistentes a los medicamentos. La resistencia puede surgir de todos los medicamentos contra el VIH aprobados contra, incluidos los medicamentos recientemente aprobados que se dirigen a la integrasa del VIH (IN). Resistencia a los medicamentos probablemente surge becauso de mutaciones espontáneas que se producen durante la replicación viral (tasa de error de 3 x 10 -5 ciclo de mutaciones / base / reproducción) 6. Cuando surgen mutaciones en los genes que codifican para los objetivos de los fármacos anti retrovirales, un pequeño subconjunto de estas mutaciones dará lugar a una reducción en la susceptibilidad de la cepa viral a los medicamentos. Para evitar el desarrollo de resistencia a los medicamentos, las concentraciones de fármacos deben mantenerse en niveles que suprimen totalmente la replicación del VIH. La mala adherencia al régimen terapéutico agrava el problema y puede conducir a la rápida evolución de la resistencia a 7-9. Aunque las concentraciones de fármaco pueden variar en los pacientes debido a la diferente absorción, metabolismo, distribución, y los niveles de excreción, altas concentraciones de drogas pueden conducir a la toxicidad 10. Puesto que la terapia continua para la vida del paciente, hay serias preocupaciones de seguridad acerca de la toxicidad a largo plazo de los antirretrovirales. Los antirretrovirales utilizados en la terapia HAART puede tener efectos adversos and ha habido incidencias donde los efectos secundarios han sido peligrosa para la vida 11-15. Los problemas de los pacientes se encuentran con el desarrollo de la resistencia y toxicidad subyacen a la necesidad de desarrollar nuevos fármacos que bloquean eficazmente la replicación de las cepas resistentes a los medicamentos comunes del virus con una toxicidad escasa o nula a largo plazo.
Por lo tanto, hay una necesidad de un ensayo que puede seleccionar compuestos que bloquean los pasos esenciales en el ciclo de vida viral rápidamente. Aquí se describe un ensayo eficiente que se puede utilizar para evaluar la citotoxicidad de un compuestos y su capacidad para bloquear la replicación de ambos WT y cepas de VIH resistentes a los fármacos rápidamente y de manera eficiente. El ensayo se utiliza es similar a un ensayo que fue desarrollado para la detección de resistencia a los medicamentos en el virus aislado de pacientes 16-18.
Aunque el ensayo se puede utilizar sin modificación para la detección de compuestos que pueden bloquear la transcripción inversa del VIH, vamos a describe usando el ensayo para evaluar EN inhibidores. EN es una enzima viral esencial que inserta el ADN viral en el genoma celular 19. Aunque se están desarrollando una serie de prometedores en inhibidores, algunos de los cuales están actualmente en fase de ensayos clínicos, sólo Isentress 20, 21 (también conocido como raltegravir o RAL) y, más recientemente, elvitegravir (EVG) 22 y Dolutegravir (DTG) 23 han sido aprobado por la FDA. Estos compuestos son activos contra el VIH tanto B y subtipos no B en cultivo celular y en los pacientes 24, 25. Sin embargo, el tratamiento con RAL selecciona para resistente a los medicamentos del VIH-1 en los mutantes, incluyendo Y143R, N155H y G140S/Q148H 24, 26-31. N155H y G140S/Q148H también reducen la eficacia de EVG, que hace hincapié en la necesidad de diseñar y desarrollar la segunda generación de los inhibidores de transferencia de cadena (INSTIs) que son eficaces contra estas mutaciones de resistencia.
Protocolo
1. Preparación de cepas madres
- Hacer reservas de maestros de los compuestos a ensayar en DMSO. Preparar las poblaciones a una concentración estándar de 20 mm.
Nota: cualquier concentración superior a 10 mM se puede utilizar. Los compuestos que pueden utilizarse como controles positivos para validar este ensayo incluyen RAL, EVG, y DTG. - Asegurar los compuestos se disolvieron en DMSO por agitación las soluciones múltiples veces durante 15 segundos e incubar a temperatura ambiente durante 1 hora. Guarde las soluciones madre 20 mM en la oscuridad a -20 ° C hasta su uso.
2. Preparación de las placas de 96 pocillos durante la investigación de compuestos
- Elija la línea de células para ser probado (por ejemplo, HOS o TZM-bl) y sembrar 100 l de esas células a una densidad de 4 x 10 4 células / ml (4.000 células / pocillo) en medios de comunicación (por ejemplo, modificado Eagle o DMEM medio Dulbecco suplementado con 5% (v / v) de suero fetal bovino, 5% de suero de ternero recién nacido, y penicilina (50 unidades / ml) más estreptomycin).
3. Generación de Virus Stocks
Producir VSV-G-pseudotyped VIH mediante la transfección de células 293 (como se muestra en la Figura 1, paso 1) 32-34.
- El día antes de la transfección, placa 293 células en placas de 100 mm de diámetro a una densidad de 1,5 x 10 6 células.
- En el día de la transfección, transfectar las células 293 con 16 g de tipo salvaje o mutante del VIH (pNLNgoMIVR - ΔLUC) y 4 g de VEV (pHCMV-g) usando el método de fosfato de calcio 35.
- Aproximadamente 6 horas después de la precipitado de fosfato de calcio se añade, lavar las células 293 dos veces con tampón fosfato salino (PBS) y se incuban con medio fresco durante 48 horas. [DMEM suplementado con 5% (v / v) de suero fetal bovino, 5% de suero de ternero recién nacido, y penicilina (50 unidades / ml) más estreptomicina (50 mg / ml)].
- Se recoge el virus que contiene sobrenadantes mediante la eliminación de los medios de comunicación desde el diámetro 100 mmplatos, aclarar los sobrenadantes por centrifugación a baja velocidad a 3.000 rpm durante 10 min, filtrar los sobrenadantes a través de un filtro de 45 micras de tamaño de poro de la jeringa, el tratamiento de los sobrenadantes con Turbo DNasa durante 30 min a TA y se diluye en los sobrenadantes de los medios de comunicación para la preparación en ensayos de infección . Almacene los sobrenadantes virales congelados, en alícuotas, a -80 ° C.
Nota: la cantidad de p24 en el sobrenadante se determina mediante el uso de un kit de ensayo de inmunoabsorción p24 de VIH-1 ligado a enzimas. La concentración de p24 se utiliza para controlar la cantidad de virus en la muestra. Aproximadamente 500 ng de virus se añadió a las células HOS sembradas en placas sobre platos de 60 mm de diámetro a una densidad de 1,5 x 10 5 células / placa en el día antes de la infección. Después de un 48 horas de incubación, las células se cosecharon, recogieron por centrifugación, se lavaron, y se resuspendieron en 100 l de PBS. Añadir una cantidad igual de reportero luminiscencia reactivo de ensayo de genes y medir la actividad luciferasa como se describe en las secciones 5.4.1 y5.4.2. A partir de este, una dilución apropiada de virus se puede hacer como se describe en el paso 4.6.
4. Compuesto Proyección en placas de 96 pocillos
Screen cada compuesto por triplicado y promediar los resultados.
Nota: el efecto de cada compuesto sobre la replicación viral se corrige mediante la normalización al nivel de la replicación obtenida en ausencia de cualquier compuesto.
- Determinar el rango de concentración empírica que se proyectarán.
Nota: por lo general, las pantallas con 11 diluciones seriadas se realizan añadiendo el compuesto de la columna de platos por columna y pantallas con 7 diluciones seriadas se hacen añadiendo el compuesto por fila. Uno triplicado conjunto de pozos debe ser reservado para el control sin compuesto. Además, una columna o una fila deben permanecer en blanco para actuar como control negativo / fondo. Por último, si se trata de una citotoxicidad celular o ensayo de infectividad dictará si se añade el virus. - Preparardiluciones en serie a partir de la solución madre 20 mM. Las concentraciones se eligen en función de la gama de concentraciones determinado empíricamente para ser sometidas a ensayo (como se muestra en la Tabla 1). Preparar las diluciones en medios de comunicación en 10 veces la concentración final deseada, es decir, si la concentración final va a ser 100 M, hacer una reserva de trabajo 1 mM.
Nota: Los compuestos con IC 50 s por encima de 5-10 M no suelen ser buenos candidatos para el desarrollo de fármacos. En los ensayos iniciales ponemos a prueba los compuestos sólo contra el vector PESO. Compuestos prometedores que inhiben eficazmente el vector PESO entonces se miden frente a un panel de mutantes resistentes a los medicamentos. - Retire las placas de 96 pocillos de la incubadora y añadir las diluciones en serie de los compuestos a ensayar a los pocillos en triplicado (como se muestra en la Figura 1, paso 2).
Nota: el volumen añadido al pozo debe ser 1/10 de volumen de la concentración final. Por lo tanto, añadir 22 l / pocillo (volumen final pAdemás virus ost es de 220 l) para los ensayos de infectividad. Para los ensayos de citotoxicidad, añadir 11 l / pocillo (volumen final es de 110 l / pocillo). - Devolver las placas de 96 pocillos a la incubadora. Para una pantalla de citotoxicidad celular, incubar las placas de 96 pocillos 48 horas a 37 ° C y no se necesitan más manipulaciones en el Protocolo 4: continuar con el Protocolo 5 Para los ensayos de infectividad, continúe siguiendo las instrucciones que figuran en el Protocolo 4..
- Ensayos de infectividad solamente. Retirar las placas de la incubadora después de un mínimo de 3 horas de incubación a 37 ° C con los compuestos a ser analizados.
Nota: esto permite que el compuesto para ser absorbido por las células antes de la infección con el vector de VIH. - Preparar una dilución de stock del virus 33, 34 (por lo general aproximadamente 01:03) que producirá una señal de luciferasa entre 0,2-1,5 unidades relativas de luciferasa (RLU) en células no tratadas. Una placa entera tomará aproximadamente 10 ml de diluciónvirus ted. Añadir 100 l de virus a cada uno de los pozos, utilizando ya sea un 8 o 12 Pipeta multicanal. No agregue virus a los pocillos de control negativo / fondo. Vuelva a poner las placas a la 37 ° C incubadora durante 48 horas.
Nota: una acción de dilución del virus 1:03 dilución es típico que producirá una señal de luciferasa entre 0,2 -1,5 RLU basado en un ensayo de p24 demostrando que la concentración viral en el sobrenadante es de aproximadamente 500 ng en 1,0 ml.
5. Preparación y evaluación de la citotoxicidad y la infectividad en placas de 96 pocillos
- Aspirar los medios de comunicación de los pozos (rojo fenol en los medios de comunicación puede interferir con la señal de luciferasa). Usar una pipeta de vidrio con una punta de pipeta 200 l unida al extremo. Comience en la parte superior de los medios de comunicación y trabajar poco a poco hacia abajo, hacia la parte inferior del pozo. No gaste demasiado tiempo en el fondo del pozo, o las células pueden ser removidos del pozo.
- Añadir 100 l de PBS suplementado con 0,5 mM de MgCl 2 a cada pocillo. Esto tiene que ser hecho inmediatamente después de que se retiró el medio de manera que las células no se sequen.
- Sólo para los ensayos de citotoxicidad, añadir 5 ml de tampón de sustrato a partir del ensayo de detección de luminiscencia de ATP a cada vial de reactivo liofilizado suministrado. Un vial es suficiente para una placa de 96 pocillos.
- Añadir 50 l de tampón de lisis celular del ensayo de detección de luminiscencia de ATP a cada pocillo. Agitar la placa de 96 pocillos a 700 rpm a temperatura ambiente durante 5 min utilizando un termomezclador compacto.
- Añadir 50 l de reactivo de ensayo de detección de luminiscencia ATP reconstituido a cada pocillo con excepción de los pozos de control / fondo negativos. Agitar a 700 rpm a temperatura ambiente durante 5 min utilizando un termomezclador compacto. Incubar las placas a temperatura ambiente durante 20 minutos para permitir tiempo para el desarrollo de la señal.
- Lea la placa de 96 pocillos usando el luminómetro de microplacas.
Nota: abrir el programa luminómetro de microplacas SoftMax Pro. Asegúrese de que el luminómetro está configurado para medir luminescence con una sensibilidad de 5 lecturas / pocillo.
- Sólo para los ensayos de infectividad, añadir 10 ml de tampón de sustrato a partir del ensayo de gen informador de luminiscencia a cada vial de reactivo liofilizado suministrado. Un vial es suficiente para cada placa de 96 pocillos.
- Añadir 100 l de reactivo de ensayo reconstituida reportero gen de luminiscencia para cada pocillo. Incubar a temperatura ambiente durante 20 minutos para permitir tiempo para el desarrollo de la señal.
- Lea la placa de 96 pocillos usando un luminómetro de microplaca como se realizó en la sección 5.3.3.
6. Determinación de la CC 50 e IC 50 valores para los Compuestos
- La transferencia de los datos de la luciferasa del luminómetro de microplacas en una hoja de cálculo Excel.
- Promedio tanto los datos de la luciferasa, por triplicado, y los datos de la señal de fondo / de control. Restar la señal de fondo media / de control de la señal media por triplicado para todo el intervalo de concentración.
- normalizar la corrección de fondo a la señal promedio de los intervalos de concentración en contra de la actividad, si se trata de la citotoxicidad o la infectividad, en ausencia de cualquier compuesto para determinar el porcentaje de inhibición.
Nota: el porcentaje de inhibición se define como la actividad de la luciferasa en presencia de fármaco dividido por la actividad de la luciferasa en ausencia de fármaco multiplicado por 100.
- Utilice el programa de software para obtener Kaleidagraf CC 50 e IC 50 valores
- Traslado tanto el intervalo de concentraciones determinado empíricamente y la inhibición de la actividad de la luciferasa por ciento en Kaleidagraf.
- Representar gráficamente los datos con el rango de concentración en el eje x y la inhibición de la actividad de la luciferasa por ciento en el eje y.
Resultados
Si el ensayo (Figura 1, los pasos 1 y 2) se realizó con éxito, entonces los valores de luciferasa deberían ser similares a los datos presentados en la Tabla 2 explorar a través de la gama de concentración.; un compuesto potencialmente potente revelará aumento de la actividad de la luciferasa de izquierda a derecha, y el control debe tener la mayor actividad de la luciferasa. Si la actividad de la luciferasa no supere 0,1 unidades relativas de luciferasa (RLU) en toda la gama de concentración, esto normalmente indica que el compuesto mató a las células. Si los datos de la luciferasa es mayor que o igual a 2,0 RLU a través de todas las diluciones en serie, a continuación, los compuestos no fueron capaces de inhibir el VIH-1 infecciones a las concentraciones ensayadas.
Trazado de la concentración de los compuestos frente a la inhibición de la actividad de la luciferasa por ciento en Kaleidagraf (Tabla 3, parte A), después de realizar el análisis de regresión lineal, se producen resultados similares para t manguera se muestra en la Tabla 3, parte B.

Figura 1. Preparación de VIH-1 reservas de virus y de la configuración de la citotoxicidad celular y Single-ronda Infectividad Los ensayos. En el paso 1, las células 293T se transfectan con pNL4.3ΔEnv.LUC y VSV-G y se incubaron durante 48 h para producir el virus 34 . El virus se recoge y se almacena (congelado a -80 ° C en alícuotas) hasta que se utiliza en los ensayos de infectividad. Para el paso 2, células HOS se siembran en una placa de 96 pocillos y se incubaron durante 24 h. Las células se incubaron previamente con diluciones seriadas de los compuestos a ensayar durante 3 horas y después se infectaron con el virus (ya sea WT o resistente a las drogas). Después de una incubación de 48 horas, se midió la actividad de luciferasa.
le1.jpg "width =" 300 "/>
Tabla 1. Selección de Medicamentos de serie de prototipos de dilución. Un examen más riguroso consiste en 11 diluciones en serie que normalmente se inician a los 10 M y desembocan en 0.0005 M. Las diluciones en serie se preparan 10x; hay 100 l de células y 100 l de virus en cada pocillo). En este volumen y siguiendo estos cálculos, las diluciones en serie serán suficientes para 3 filas de una placa entera de 96 pocillos. Los ensayos de citotoxicidad se preparan de manera similar; sin embargo, las 11 diluciones en serie comienzan en 250 M y terminan a las 0.05 mM. Sólo 11 l de las diluciones se añaden a los pocillos en la placa que contiene 100 l de células. Por favor, haga clic aquí para ver una versión más grande de esta figura.
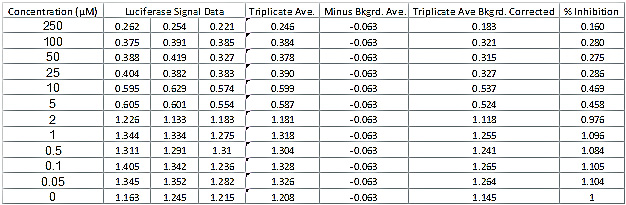
Tabla 2. Lectura de datos de la señal de luciferasa y Determinación del porcentaje de inhibición de la actividad luciferasa. La tabla de datos muestra un conjunto típico de datos de la luciferasa para un compuesto éxito. La tabla también muestra los cálculos adicionales necesarios para determinar el porcentaje de inhibición de la actividad de la luciferasa y la CC 50 e IC 50 valores. Haga clic aquí para ver una versión más grande de esta figura.
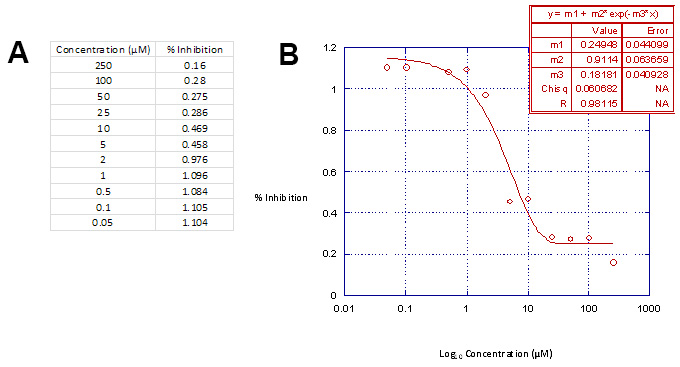
Tabla 3. Análisis de Regresión Lineal tabla de datos. Parte A. Representación gráfica de la gama de concentración utilizada en comparación con el porcentaje de inhibición de la actividad de luciferasa en Kaleidagraf producirá las curvas de inhibición apropiadas. Parte B, Las curvas de inhibición se define por la 3 paramétricofunción sigmoidal y ajuste a los datos mediante análisis de regresión lineal 18. Esta tabla de datos se utiliza en conjunción con Microsoft Excel para calcular las concentraciones de fármaco necesaria para inhibir el virus de la integración y la citotoxicidad celular en un 50%, por ejemplo, IC 50 y CC 50. Haga clic aquí para ver una versión más grande de esta figura.
Discusión
Se describe un ensayo rápido, eficiente y reproducible que se puede utilizar para seleccionar compuestos para la citotoxicidad y por su capacidad para inhibir la replicación de ambos WT y resistente VIH-1 de drogas. La capacidad de identificar rápidamente compuestos y probar su eficacia y la citotoxicidad es crucial en el desarrollo de nuevos y mejores medicamentos contra el VIH-1. Una vez que se identifican los compuestos de plomo, análogos del compuesto de plomo pueden ser producidos y probados utilizando el mismo ensayo. El ensayo es relativamente simple. Hay dos controles positivos y negativos que permiten al usuario a diagnosticar los problemas más comunes (compuestos tóxicos, problemas con el vector stock). El uso de un conjunto por triplicado de pocillos sin compuesto añadido muestra que se ha producido la infección viral. El hecho de que la citotoxicidad se mide en un ensayo independiente Evita mala interpretación de una reducción de la luciferasa causada por la citotoxicidad como un efecto específico sobre la replicación viral.
Los pasos críticosen el protocolo se preparan las placas de manera que las células se distribuyen uniformemente en los pocillos, los pocillos que tienen las concentraciones apropiadas de los compuestos a ensayar, la adición de la misma cantidad de virus a cada uno de los pocillos, y midiendo la actividad de luciferasa a determinar la CC 50 e IC 50 valores.
El ensayo es seguro, cuantitativa y reproducible. El ensayo es seguro porque el vector es de replicación defectuosa. El ensayo es cuantitativa y reproducible, ya que se basa en un único vector redondo que expresa luciferasa, que puede ser ensayada con precisión y convenientemente. En un ensayo de replicación del virus ronda múltiples, el CI medido 50 depende del número de ciclos de vida virales; este es un problema particular cuando los ensayos implican ambos WT y los virus resistentes a los fármacos que pueden tener capacidades significativamente diferentes de replicación.
Se han realizado varios ensayos enzimáticos informado anteriormente de que puedaser utilizado para la detección de inhibidores de la IN. Los ensayos que implican la tecnología de PCR en tiempo real para medir ADN integrado requieren proteínas recombinantes purificadas (s), y son, en general, tanto más mano de obra intensiva y costosa 36, 37. Aunque es posible utilizar ensayos enzimáticos para medir el impacto de los compuestos sobre las otras enzimas virales (RT y proteasa), cada enzima requiere su propio sistema de ensayo. El ensayo de vector de ronda, como se describe, puede ser utilizado, sin modificación, para la detección de inhibidores de la RT. Un ensayo similar se puede utilizar para la detección de inhibidores de la proteasa; Sin embargo, en un ensayo de inhibidor de la proteasa, los compuestos deben ser añadidos a las células utilizadas para producir los vectores. Un ensayo relacionados, utilizando diferentes células y vectores, también se puede utilizar para la detección de envoltura (env) y los inhibidores de la fusión de entrada del VIH. Por último, el ensayo se puede usar, en una escala más grande, con dispensadores de automatización robótica. Por lo tanto, el ensayo se puede usar para cribar grandes bibliotecas de compuestos contra WT y mutant VIH. Sin embargo, el hecho de el ensayo puede detectar un inhibidor de la replicación del VIH que actúa en diferentes etapas de los puntos ciclo de vida viral a una limitación en la interpretación de los datos. Por sí mismo el ensayo no define lo que paso en el ciclo de vida está bloqueado por un compuesto. Si surge esta pregunta, se puede resolver mediante el uso de tiempo de los ensayos de adición 38, y probando el compuesto contra las proteínas virales recombinantes purificadas.
Lamentablemente, a pesar del éxito de los medicamentos contra el VIH, todavía hay problemas con la resistencia y la toxicidad. En ausencia de una vacuna eficaz contra el VIH, hay una necesidad no sólo para desarrollar nuevos fármacos terapéuticos que serán eficaces contra los mutantes resistentes a los fármacos existentes, sino también para desarrollar fármacos profilácticos que pueden reducir la propagación del virus. Si el uso profiláctico de medicamentos contra el VIH comprende el ámbito del tratamiento de las personas infectadas, este enfoque colocará una carga especial en el desarrollo de fármacos que se tienen loco o nada de toxicidad a largo plazo.
Divulgaciones
Los autores no tienen nada que revelar.
Agradecimientos
Esta investigación fue apoyada por el Programa de Investigación Intramural del Instituto Nacional del Cáncer.
Materiales
| Name | Company | Catalog Number | Comments |
| DMSO | Sigma | D2650 | |
| DMEM | Corning Cellgro | 10-017 | |
| ATPlite Luminescence ATP Detection Assay System | Perkin Elmer | 6016941 | |
| Steady Lite Plus High Sensitivity Luminescence Reporter Gene Assay System | Perkin Elmer | 6016751 | |
| Dulbecco's PBS | Gibco-Life Technologies-Invitrogen | 14190-136 | |
| SpectraMax Gemini EM | Molecular Devices | ||
| KaleidaGraph | Synergy Software | ||
| Nunc F96 Microwell White Polystyrene Plate | Thomas Scientific | 12-566-26 | |
| Eppendorf Thermomixer Compact | Sigma Aldrich | T1442-1EA | |
| Turbo DNase | Ambion-Life Technologies-Invitrogen | AM2238 | |
| Millex HA Filter Unit, 0.45 µM | Millipore | SLAHA033SS | |
| Alliance HIV-1 p24 Elisa Kit | Perkin Elmer | NEK050B001KT | |
| HOS cells | ATCC | CRL-1543 | |
| TZM-bl cells | NIH AIDS Reagent Program | 8129 | |
| pNL4.3ΔEnv.LUC | NIH-NCI HIV Drug Resistance Program- Hughes Lab | ||
| VSV-G | NIH-NCI HIV Drug Resistance Program- Hughes Lab | ||
| SoftMax Pro | Molecular Devices | 0200-310 |
Referencias
- Mouton, Y., et al. Impact of protease inhibitors on AIDS-defining events and hospitalizations in 10 French AIDS reference centres. Federation National des Centres de Lutte contre le SIDA. AIDS. , 101-105 (1997).
- Hammer, S. M., et al. A controlled trial of two nucleoside analogues plus indinavir in persons with human immunodeficiency virus infection and CD4 cell counts of 200 per cubic millimeter or less AIDS Clinical Trials Group 320 Study Team. New Eng. J. Med. 337, 725-733 (1997).
- Hogg, R. S., et al. Improved survival among HIV-infected patients after initiation of triple-drug antiretroviral regimens. Can. Med. Assoc. 160, 659-665 (1999).
- Egger, M., et al. Impact of new antiretroviral combination therapies in HIV infected patients in Switzerland: prospective multicentre study. Swiss HIV Cohort Study. BMJ. 315, 1194-1199 (1997).
- Gulick, R. M., et al. Treatment with indinavir, zidovudine, and lamivudine in adults with human immunodeficiency virus infection and prior antiretroviral therapy. New Eng. J. Med. 337, 734-739 (1997).
- Perelson, A. S., Neumann, A. U., Markowitz, M., Leonard, J. M., Ho, D. D. HIV-1 dynamics in vivo: virion clearance rate, infected cell life-span, and viral generation time. Science. 271, 1582-1586 (1996).
- Simoni, J. M., Amico, K. R., Pearson, C. R., Malow, R. Strategies for promoting adherence to antiretroviral therapy: a review of the literature. Curr. Infect. Dis. Rep. 10, 515-521 (2008).
- Simoni, J. M., Amico, K. R., Smith, L., Nelson, K. Antiretroviral adherence interventions: translating research findings to the real world clinic. Curr. HIV/AIDS Rep. 7, 44-51 (2010).
- Volberding, P. A., Deeks, S. G. Antiretroviral therapy and management of HIV infection. Lancet. 376, 49-62 (2010).
- Acosta, E. P., et al. Novel method to assess antiretroviral target trough concentrations using in vitro susceptibility data. Antimicr. 56, 5938-5945 (2012).
- Rockstroh, J. K., et al. Long-term treatment with raltegravir or efavirenz combined with tenofovir/emtricitabine for treatment-naive human immunodeficiency virus-1-infected patients: 156-week results from STARTMRK. Clin. Infect. Dis. 53, 807-816 (2011).
- Fernandez-Montero, J. V., Eugenia, E., Barreiro, P., Labarga, P., Soriano, V. Antiretroviral drug-related toxicities - clinical spectrum, prevention, and management. Exp. Opin. Drug Safety. , (2013).
- Lunzen, J., et al. Once daily dolutegravir (S/GSK1349572) in combination therapy in antiretroviral-naive adults with HIV: planned interim 48 week results from SPRING-1, a dose-ranging, randomised, phase 2b trial. Lancet Infect Dis. 12, 111-118 (2012).
- Sax, P. E., et al. Co-formulated elvitegravir, cobicistat, emtricitabine, and tenofovir versus co-formulated efavirenz, emtricitabine, and tenofovir for initial treatment of HIV-1 infection: a randomised, double-blind, phase 3 trial, analysis of results after 48 weeks. Lancet. 379, 2439-2448 (2012).
- Sax, P. E., et al. Abacavir/lamivudine versus tenofovir DF/emtricitabine as part of combination regimens for initial treatment of HIV: final results. Infect. Dis. 204, 1191-1201 (2011).
- Kellam, P., Larder, B. A. Recombinant virus assay: a rapid, phenotypic assay for assessment of drug susceptibility of human immunodeficiency virus type 1 isolates. Antimicr. Agents Chemother. 38, 23-30 (1994).
- Hertogs, K., et al. A rapid method for simultaneous detection of phenotypic resistance to inhibitors of protease and reverse transcriptase in recombinant human immunodeficiency virus type 1 isolates from patients treated with antiretroviral drugs. Antimicr. Agents Chemother. 42, 269-276 (1998).
- Petropoulos, C. J., et al. A novel phenotypic drug susceptibility assay for human immunodeficiency virus type 1. Antimicr. Agents Chemother. 44, 920-928 (2000).
- Engelman, A., Mizuuchi, K., Craigie, R. HIV-1 DNA integration: mechanism of viral DNA cleavage and DNA strand transfer. Cell. 67, 1211-1221 (1991).
- Hazuda, D. J., et al. Inhibitors of strand transfer that prevent integration and inhibit HIV-1 replication in cells. Science. 287, 646-650 (2000).
- Nguyen, B. Y., et al. Raltegravir: the first HIV-1 integrase strand transfer inhibitor in the HIV armamentarium. Ann. N.Y. Acad. Sci. 1222, 83-89 (2011).
- Wills, T., Vega, V. Elvitegravir: a once-daily inhibitor of HIV-1 integrase. Exp. Opin. Invest. Drugs. 21, 395-401 (2012).
- Kobayashi, M., et al. In Vitro antiretroviral properties of S/GSK1349572, a next-generation HIV integrase inhibitor. Antimicr. Agents Chemother. 55, 813-821 (2011).
- Cooper, D. A., et al. Subgroup and resistance analyses of raltegravir for resistant HIV-1 infection. Eng. J. Med. 359, 355-365 (2008).
- Briz, V., et al. Raltegravir and etravirine are active against HIV type 1 group O. AIDS Res.Human Retroviruses. 25, 225-227 (2009).
- Fransen, S., et al. Loss of raltegravir susceptibility by human immunodeficiency virus type 1 is conferred via multiple nonoverlapping genetic pathways. J. Virol. 83, 11440-11446 (2009).
- Goethals, O., et al. Primary mutations selected in vitro with raltegravir confer large fold changes in susceptibility to first-generation integrase inhibitors, but minor fold changes to inhibitors with second-generation resistance profiles. Virology. 402, 338-346 (2010).
- Goethals, O., et al. Resistance mutations in human immunodeficiency virus type 1 integrase selected with elvitegravir confer reduced susceptibility to a wide range of integrase inhibitors. J. Virol. 82, 10366-10374 (2008).
- Canducci, F., et al. Dynamic patterns of human immunodeficiency virus type 1 integrase gene evolution in patients failing raltegravir-based salvage therapies. AIDS. 23, 455-460 (2009).
- Ceccherini-Silberstein, F., et al. Characterization and structural analysis of HIV-1 integrase conservation. AIDS Rev. 11, 17-29 (2009).
- Charpentier, C., et al. Drug resistance profiles for the HIV integrase gene in patients failing raltegravir salvage therapy. HIV Med. 9, 765-770 (2008).
- Julias, J. G., et al. Effects of mutations in the G tract of the human immunodeficiency virus type 1 polypurine tract on virus replication and RNase H cleavage. J. Virol. 78, 13315-13324 (2004).
- Hare, S., et al. Structural and functional analyses of the second-generation integrase strand transfer inhibitor dolutegravir (S/GSK1349572). Mol. Pharmacol. 80, 565-572 (2011).
- Adachi, A., et al. Production of acquired immunodeficiency syndrome-associated retrovirus in human and nonhuman cells transfected with an infectious molecular clone. J. Virol. 59, 284-291 (1986).
- Kemp, S. D., et al. A novel polymorphism at codon 333 of human immunodeficiency virus type 1 reverse transcriptase can facilitate dual resistance to zidovudine and L-2',3'-dideoxy-3'-thiacytidine. J. Virol. 72, 5093-5098 (1998).
- Butler, S. L., Hansen, M. S., Bushman, F. D. A quantitative assay for HIV DNA integration in vivo. Nat. Med. 7, 631-634 (2001).
- Brussel, A., et al. Longitudinal monitoring of 2-long terminal repeat circles in peripheral blood mononuclear cells from patients with chronic HIV-1 infection. AIDS. 17, 645-652 (2003).
- Daelemans, D., Pauwels, R., De Clercq, E., Pannecouque, C. A time-of-drug addition approach to target identification of antiviral compounds. Nat. Protoc. 6, 925-933 (2011).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados