Method Article
Análisis Phosphopeptide de roedores epidídimo Espermatozoides
En este artículo
Resumen
Proteomic analysis of any cell type is highly dependent on both purity and pre-fractionation of the starting material in order to de-complexify the sample prior to liquid chromatography mass spectrometry (MS). By using back-flushing techniques, pure spermatozoa can be obtained from rodents. Following digestion, phosphopeptides can be enriched using TiO2.
Resumen
Los espermatozoides son bastante único entre los tipos de células. Aunque producida en el testículo, tanto la transcripción de genes nucleares y la traducción se desconectan una vez que el de células redondas pre-cursor empieza a alargarse y se diferencian en lo que se morfológicamente reconocido como un espermatozoide. Sin embargo, el espermatozoide es muy inmaduro, al no tener la capacidad para la motilidad o reconocimiento huevo. Ambos de estos eventos se producen una vez que el tránsito espermatozoides un órgano secundario conocido como el epidídimo. Durante el paso ~ 12 días que tarda una célula de esperma pase a través del epidídimo, modificaciones post-traduccionales de las proteínas existentes desempeñan un papel crucial en la maduración de la célula. Una faceta importante de este tipo es la fosforilación de proteínas. Con el fin de caracterizar eventos de fosforilación que tienen lugar durante la maduración del esperma, ambas poblaciones de células de esperma puros y pre-fraccionamiento de fosfopéptidos deben establecerse. Usando técnicas de lavado de nuevo, un método para el aislamiento de pura espermatozoides oalta calidad y el rendimiento f de los epidídimos distal o caudal se esboza. Se explican los pasos para la solubilización, digestión, y pre-fraccionamiento de fosfopéptidos de esperma a través de cromatografía de afinidad TiO2. Una vez aislado, fosfopéptidos pueden ser inyectados en MS para identificar los dos eventos de fosforilación de proteínas sobre residuos de aminoácidos específicos y cuantificar los niveles de fosforilación que tienen lugar durante los procesos de maduración de esperma.
Introducción
Después de haber salido de los testículos, los espermatozoides presentan una gran diferencia aún notablemente, estas células son inmaduras 1,2. Como tales, carecen de funcionalidad completa, incluyendo la capacidad de nadar y se unen a un ovocito 3. Aunque se necesita más la maduración de la célula espermática, esto no puede tener lugar a través de rutas canónicas, ya que en esta fase de su proceso de diferenciación celular, que son incapaces de transcripción de genes y más biosíntesis de proteínas 4. Competencia Biológica se confiere a los espermatozoides a medida que salen del testículo y entran en una parte del sistema reproductor masculino conocida como el epidídimo 5. El epidídimo es un tubo bien enrollada, altamente diferenciada que conecta los conductos eferentes (de los testículos) a los conductos deferentes y está presente en todos los mamíferos machos 6. Los espermatozoides adquieren progresivamente su potencial fertilizante durante el descenso del epidídimo, basándose en el medio ambiente luminal siempre cambiante que es created por las células epiteliales del epidídimo locales 7. Las diversas actividades secretoras y re-absorción presentes en el acto medio del epidídimo para modificar la propia esperma, cambiando su proteína, carbohidratos y lípidos composición 6. La importancia del epidídimo, en particular la región inicial "caput" de esta estructura se ha ejemplificado mediante técnicas de ligadura quirúrgica 8. Los espermatozoides retenidos dentro del testículo por eferente ligadura del conducto se carece por completo de cualquier capacidad de fertilizar el ovocito 9-11.
Además del entorno del epidídimo, las vías de transducción de señales en el trabajo a los espermatozoides después de la traducción modificar el complemento espermatozoide existente. Por ejemplo, los espermatozoides desde los primeros regiones del epidídimo mostrar diferentes patrones de fosforilación de proteínas en comparación con aquellas últimas regiones 5,12. Esto no es sorprendente, ya que hay grandes diferencias en la capability del esperma de estas regiones. Por ejemplo, los espermatozoides de principios, caput epidídimo son immotilite. Por el contrario, las células de esperma de la región de caballo se someterán adelante motilidad progresiva una vez colocado en medio isotónico. Dado que las células de espermatozoides del epidídimo son incapaces de biosíntesis de proteínas de novo, todas las vías intrínsecas que regulan la función espermática deben ser a través de modificaciones post-traduccionales (PTM). Por lo tanto, es lógico pensar que la proteómica, y en particular la investigación de los PTM como la fosforilación debe ser un impulso importante si queremos entender la maduración de células de esperma.
Un método alternativo para obtener los espermatozoides de los epididymidies utilizar retro-lavado a contracorriente 13-16. Aunque esta técnica es ciertamente más tiempo y tiene un mayor grado de habilidad por parte del operador, los espermatozoides obtenidos demuestran consistentemente pureza superior a 99,99%. Además, a diferencia de todas las otras técnicas, los espermatozoides can aislarse en un estado de reposo, por lo que es posible estudiar cómo se inicia la motilidad de los espermatozoides. Como preparación de la muestra es el aspecto más importante para el análisis proteómico, el aislamiento de los espermatozoides se ha convertido en uno de los aspectos más importantes de los estudios de proteómica de esperma. Este protocolo proporciona una explicación de cómo los espermatozoides son aislados de la cola del epidídimo. Después de esto, el 2 fosfopéptido procedimiento de enriquecimiento de TiO se describe, con referencia específica sobre cómo extraer los péptidos de las células de esperma altamente diferenciados. El enfoque de la EM puede ser utilizado para distinguir cambiantes fosfopéptidos si uno tuviera que comparar los espermatozoides del epidídimo caudal en un estado (inmóviles o no capacitado) a otra (móviles, capacitado, acrosoma reaccionado, etc.) haciendo de este un poderoso enfoque para estudiar los espermatozoides función.
Protocolo
1. Preparación de medios de cultivo y Platos
- Hacer 200 ml de Biggers Whitten y Whitten (BWW) 17 Solución de trabajo mediante la adición de 5,54 g de NaCl, 0,356 g de KCl, 0,25 g de CaCl2, 0,162 g H 2 KO 4 P, y 0,294 g MgSO4 a 1 l de agua Milli-Q . Esta es la solución madre y puede mantenerse a 4 ° C durante un máximo de un mes.
- De la solución madre, añadir 420 mg de NaHCO 3 -, 200 mg de glucosa, 6 mg de piruvato de sodio, 600 mg albúmina de suero bovino, 0,74 ml de lactato de sodio y 4,0 ml de tampón HEPES a 193 ml de la Bolsa de BWW. Esta es la solución de trabajo y siempre es fresco en el día y se equilibró a 37 ° C antes de usar.
- Para hacer la cánula, tomar polietileno tubo (PE) con un diámetro interno de 0,4 mm y un diámetro externo de 1,1 mm y mantenga a fuego lento (típicamente llama de metanol) de tal manera que el tubo comienza a derretirse. Inmediatamente tirar el tubo outward para estirar y crea el diámetro exterior más estrecho.
- Cut para producir un estrechamiento de un extremo que permite la fácil canulación de los conductos deferentes.
- Cortar el otro extremo de la cánula a aproximadamente 15 cm. Inserte una aguja de 30 G en el extremo romo, y adjuntar una jeringa de 3 ml a ella (completamente retraído).
- Hacer una boquilla de succión por el corte de una longitud de 20 cm de tubo de PE (4,2 mm de diámetro interno, 6,4 mm de diámetro exterior). Inserte una boquilla en un extremo.
- Inserte el soporte del tubo de vidrio micro capilar y el cristal micro-capilar en sí (por lo general 3 l de un ratón, 40 l durante una rata).
2. La eliminación de epidídimo de ratón
- La eutanasia a los ratones de acuerdo con los procedimientos aprobados por la IACUC específicos de cada institución.
- Tome el animal y hacer una pequeña incisión en el escroto para exponer el epidídimo. Tire el testículo y el epidídimo fuera de la cavidad con un par de # 5 pinzas de relojero.
- Cortar los conductos deferentes tal que al menos 1-2 cm de permanecer unidos a la cola del epidídimo. Además, cortar los conductos eferentes proximales y los tejidos que conectan el epidídimo a los testículos y quitar toda la pista reproductor masculino.
- Coloque toda la pista reproductor masculino con un microscopio de disección con un rango de aumentos del orden de 5-40X.
3. cannulating el Epidídimo
- Tape abajo de la cánula al microscopio, de tal manera que 1-2 cm del extremo (en forma de cono) estrechado es libre y visible a través de la lente.
- Tome un par de relojería # 5 pinzas y estrechar suavemente cada lado del conducto deferente y tire de los conductos deferentes en la cánula, de manera que la cánula entra en los conductos deferentes.
- Tome un trozo de seda no absorbible trenzada negro tratado (tamaño 5-0) y haga un nudo alrededor de los conductos deferentes canulados. Asegúrese de que el nudo se tira con fuerza para mantener la cánula en el interior de los conductos deferentes, cuando la presión del aire from se aplica la jeringa.
4. retrógrada o retrolavado del caudal del epidídimo Espermatozoides
- Utilizando relojeros # 5 pinzas, agarra el extremo distal de los epidídimos cauda y quitar la túnica albugínea con el fin de exponer una sola túbulo epididimario.
- Usando las pinzas, tire suavemente del túbulo para exponer y luego desmenuzar con el fin de crear una abertura para que el esperma sea liberado.
- Presione suavemente sobre las 3 ml (ratón) o 20 ml (rata) de la jeringa con el fin de expulsar el aire de la jeringa en el conducto deferente. A la presión apropiada, los espermatozoides comenzará a salir lentamente del túbulo rota en el extremo distal de la cola del epidídimo. En este momento, aplicar succión a la boquilla para dibujar los espermatozoides en el capilar de vidrio. Nota: Normalmente, en un ratón, 2-3 l de espermatozoides se puede obtener en función de la edad del animal. Un testamento de rata, en el rendimiento promedio de 30-40 l.
5. Lavadoy lisis los espermatozoides en Preparación de Proteómica
- Expulsar los espermatozoides desde el capilar de vidrio en 1 ml de solución de solución BWW (37 ° C) soplando suavemente en la boquilla o adjuntar una jeringa y expeler el aire para empujar los espermatozoides de nuevo fuera de los capilares.
- Una vez que las células de esperma se difunden, lavar 3x (300 xg, 5 min) con 1 ml BWW para eliminar las proteínas contaminantes. Después del lavado final, eliminar el sobrenadante. Nota: En este punto, los espermatozoides pueden ser congelados para su uso posterior.
- Solubilizar proteínas utilizando 4% CHAPS, 2 M tiourea y 50 mM Tris, pH 7,4 durante 1 hora con vórtice intermitente.
- Después de la lisis de las células, se centrifuga (10.000 xg, 20 min), tome sobrenadante y transferir a un tubo nuevo. Nota: En este punto, la cuantificación de proteínas se puede realizar.
6. enlace disulfuro reducción y alquilación
- Añadir DTT 10 mM como concentración final de proteínas lisadas, vortex e incubar a temperatura ambiente durante 30 min.
- Añadir 50 mM idodoacetamide como una concentración final de lisado, vórtice y se incuba a temperatura ambiente durante 30 min en la oscuridad.
7. Precipitación
- Cloroformo metanol precipitar la muestra mediante la adición de 1 volumen de lisado (400 l como un ejemplo), añadir un volumen (400 l) de metanol y 0,5 volúmenes (200 l) cloroformo.
- Vortex la muestra y centrifugado (10.000 xg, 2 min).
- Observe que aparecerán dos fases después de la centrifugación. Deseche todos pero 2 mm de la capa superior (teniendo cuidado de no molestar a la interfaz).
- Añadir 1 volumen (400 l) de metanol, el tubo invertido 1-2x suavemente para mezclar y girar de nuevo (10.000 xg, 15 min). Desechar el sobrenadante que perder y pellet secar al aire durante 3-4 min.
8. digestión con tripsina
- Reconstituir tripsina en bicarbonato de amonio 25 mM que contenía 1 M de urea a una relación de 50: 1 (W / W; proteínas: tripsina) y se incubaron ovedejarían de a 37 ° C preferiblemente a 700 rpm en un termomezclador.
- Girar (10.000 xg, 15 min) para agregar material no digerido. Transferir el sobrenadante a un nuevo tubo.
9. Phosphopeptide Enriquecimiento
- Realizar la purificación y enriquecimiento de fosfopéptidos de la digestión tríptica como se describió anteriormente 18. Diluir péptidos trípticos 10 veces en tampón de DHB [tampón de DHB consta de: 350 mg / ml de ácido 2,5 dihydrobenzesulfonic (DHB), 80% (v / v) ACN (acetonitrilo), 2% (v / v) TFA (trifluoroacético ácido)] y se aplican a secar TiO2 perlas (200 mg).
- Deja en un rotador a temperatura ambiente durante 1 hora.
- Lavar la muestra con tampón DHB, girar y retirar el sobrenadante. A continuación, lavar la muestra tres veces con tampón de lavado [80% ACN (v / v), 2% de TFA (v / v)] para eliminar el DHB.
- Después de la centrifugación final, eluir directamente los fosfopéptidos utilizando tampón de elución mediante la adición de 25 l de un hidróxido de amonio 2,5%, pH ≥ solución de 10,5. Sfijar y eliminar el sobrenadante. Neutralizar inmediatamente con ~ 0,3 l de ácido fórmico.
Resultados
La calidad de los resultados de cualquier análisis proteómico es dependiente en gran medida del material de partida. Con MS modernas, ligeras contaminaciones en preparaciones de muestras son fácilmente recogidos. Por lo tanto, es fundamental, en el caso de la proteómica de células de esperma, para elegir un método que da espermatozoides altamente puro. Como se ilustra en la Figura 1, la toma retroactiva retrógrado se utiliza para recuperar espermatozoides del epidídimo cauda. Esto implica la canulación del conducto deferente con tubo de PE que permita aplicar un poco de presión de aire de la jeringa conectada. Figura 1A muestra la cola del epidídimo, junto con los conductos deferentes. Figura 1B es un plano corto de cómo el conducto deferente se ata en el que el se inserta la cánula. Al hacerlo, por lo que, los espermatozoides son liberados al final extirpado de un túbulo de caudal del epidídimo. Como se muestra en la Figura 2A, los espermatozoides se extraen de las regiones de vértice de la caudun epidídimo y se aspiró en un capilar de vidrio en un estado de reposo (Figura 2B). Esto tiene varias ventajas sobre los tradicionales métodos de "swim-up", no menos importante de los cuales es la capacidad de realizar un análisis phoshoproteomic de espermatozoides antes y después de la activación de la motilidad. Los espermatozoides puede ser expulsado en los medios de comunicación de su elección. Figura 2C (izquierda) muestra cómo buscar el esperma inmediatamente después de la expulsión en medios BWW. Muchas de las células están agrupados. Sin embargo, después de 10 min de la competencia de las células se demuestra porque nadan a la homogeneidad en la solución (Figura 2C, células del lado derecho). Dado que la técnica de lavado a contracorriente tiene muy poco impacto en las células de esperma, que obtener cerca de 100% de motilidad y las células dispersar rápidamente en los medios de comunicación sin provocación externa. En un experimento típico de lavado a contracorriente, el esperma se recuperó de la Swiss-ratón contieneentre 5.1 x 10 6 células. Esto es altamente dependiente de la edad del animal y puede variar de diferentes cepas de ratones. En una rata noruega, típicamente obtenemos 200 x 10 6 espermatozoides, ± 20%. La figura 2D representa la pureza de espermatozoides obtenidos de la cola del epidídimo de rata.
Además de la propia muestra, una de las principales cuestiones relativas a la preparación de la muestra es el rendimiento de la digestión con tripsina. La precipitación de proteínas juega un papel importante, no sólo en la eliminación de los detergentes y sales no deseadas, ambos de los cuales son incompatibles con MS, sino también en la desnaturalización de las proteínas. Hemos encontrado la precipitación de metanol-cloroformo para trabajar mejor. No sólo se ha informado de este procedimiento para precipitar las proteínas de baja abundancia mejor que otros, incluyendo precipitación con TCA 19, pero tiene ventajas adicionales. Después de la precipitación TCA, a menudo es necesario volver a ajustar el pH después de la suspensión de la pastilla TCA que puede permanecer bastanteácido. Aunque el sedimento precipitado de TCA se puede lavar en soluciones orgánicas altas para eliminar el ácido, esto se suma a la muestra manipulación y irreproducibilidad de los resultados. El fracaso para neutralizar el ácido que puede reducirse el rendimiento de péptidos trípticos. Precipitación metanol-cloroformo no es sólo rápido, pero no acidificar la muestra. La figura 3 ilustra el sedimento de proteína típicamente visto desde 100 g de muestra entre la interfase inferior y superior.
El aislamiento de fosfopéptidos puede ocurrir en un número de maneras; Sin embargo reproducibilidad depende de cómo la muestra se ha manejado hasta e incluyendo esta etapa. Uno de los métodos de desarrollo más comunes es TiO2, desarrollado originalmente por el grupo de Martin Larsen 18,20,21. Aunque se describe como un proceso para utilizar en microcolumnas, podemos obtener datos reproducibles usando cromatografía por lotes. El éxito del proceso depende en gran medida del tampón de elución, que debe estar loco e con la composición correcta; de lo contrario fosfopéptidos no se eluyen en absoluto.
La reproducibilidad de los datos de protocolo y representativos de TiO2 enriquecido fosfopéptidos de espermatozoides del epidídimo cauda en un no móviles (Figura 4 arriba) y móviles (Figura 4 abajo) estado de m / z 650-670 puede ser visto. Hemos demostrado que esta es una técnica extremadamente reproducible incluso cuando se utiliza repeticiones biológica 17. Las rayas azules que aparecen con el tiempo son péptidos que eluyen de una columna de nano-C18 como aumenta la concentración de acetonitrilo. Claramente, en la población móviles (n = 3 se muestra, n = 8 típicamente de ejecución), hay un grupo de péptido, con una masa monoisotopic alrededor de la gama Da 651.5 que está completamente ausente en el rango no móviles. Espectrometría de masas en tándem se utiliza entonces para identificar este péptido.
546 / 51546fig1highres.jpg "/>
Figura 1:. La canulación de la cola del epidídimo (A) Imagen de la cola del epidídimo. La cánula es grabado para exponer aproximadamente 1-2 cm del extremo pre-tirado. Esto se inserta en el conducto deferente mediante finas # 5watchmakers fórceps. (B) La cánula se mantiene en su lugar mediante la vinculación de seda fina alrededor de un segmento que contiene tanto los conductos deferentes y la cánula. Desde el ratón, aproximadamente 2-3 l de células epidídimo caudal y el líquido se recogen a una concentración de 1 x 10 6 / l. Desde la rata (que se muestra), aproximadamente 30-40 l de fluido se obtienen a concentraciones similares.
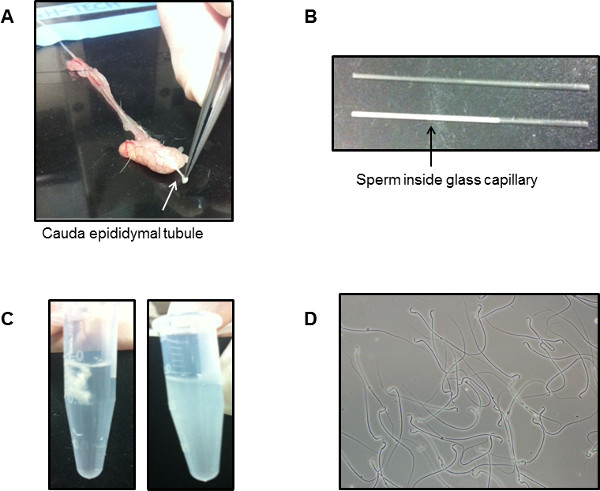
Figura 2: capilar de vidrio utilizado para recoger los espermatozoides del epidídimo competente. (A) Un túbulo desde el vértice de la cauda e pididymis es aislado y roto. La posición aproximada de la que esto ocurre se muestra. (B) La parte superior de la imagen muestra un tubo capilar de vidrio vacía y el fondo muestra una de una rata previamente toma retroactiva. No hay contaminación de la sangre y la mínima contaminación de células epiteliales. (C) Como los espermatozoides están todavía sin diluir en el fluido del epidídimo, que no han comenzado a activar. Cuando los espermatozoides son expulsados inicialmente en una solución BWW, salen como una "cadena" compacto (lado izquierdo). La competencia de la célula es fácilmente establecido, ya que después de 10 minutos la mayoría de los espermatozoides nadan en una solución sin ninguna perturbación externa (lado derecho). (D) Una foto de una alícuota de células epidídimo caudal inmediatamente después de que se han dejado de nadar demostrará la pureza de las células.
g3highres.jpg "/>
Figura 3:. Precipitación de metanol-cloroformo Una vez que los espermatozoides han sido solubilizado, la fracción soluble es metanol-cloroformo precipitado para asegurar la desnaturalización de las proteínas y la eliminación de sustancias contaminantes. El sedimento de proteína aparece en la interfase entre las fases de metanol / agua y cloroformo. La capa superior se retira cuidadosamente a fin de no perturbar este pellet. Es común dejar alrededor de 2-3 mm de la fase superior de modo que se pierde ninguna proteína.
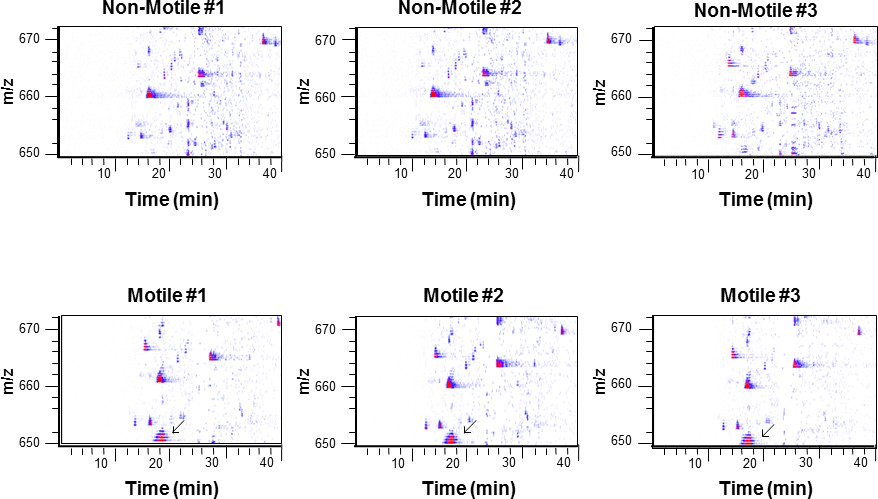
Figura 4:. Típica TiO2 perfil de fosfopéptidos enriquecido utilizando el protocolo descrito, los espermatozoides del epidídimo caudal se aislaron en cualquiera immotile (arriba, N = 3) o estados móviles (parte inferior, N = 3). Un grupo de péptidos con una masa mono-isotópica del ~ 651.5 DA se muestra a estar presentes en las poblaciones móviles pero completamente ausente en los immotile (flecha). Las comparaciones de este tipo se conocen como "libre de etiquetas (basado en MS)". La masa de péptido y el tiempo de retención se utilizan entonces para dirigir el compuesto para-espectrometría de masas en tándem e identificar la proteína de la que se deriva el péptido.
Discusión
Los pasos críticos para un análisis proteómico exitosa y reproducible de los espermatozoides son: 1) la pureza del material de partida; 2) eliminación de sales y detergentes no deseados; 3) la desnaturalización de las proteínas en toda su extensión para permitir que la tripsina para digerir un alto rendimiento de proteínas y 4) reducir al mínimo la manipulación de la muestra para reducir la pérdida de péptido.
Con el fin de retrolavar éxito la cola del epidídimo, es esencial para localizar el área de la cual los espermatozoides se cerrará. En el caso de rata y ratones, esto es en el vértice de la superficie cóncava, en el medio de la región caudal del epidídimo (véase la figura 2A). Si uno viene más hacia el conducto deferente, retrolavado es más fácil y la tasa de éxito es generalmente más alta. Sin embargo, esto viene por la pérdida de número de espermatozoides. Alternativamente, si se intenta moverse más proximal a la corpus, a continuación, la cantidad de presión requerida para empujar los espermatozoides a través de la epididymcol conductos es a menudo tan alto, que los daños en el epidídimo se produce inevitablemente.
El retrolavado del epidídimo se realiza tradicionalmente usando agua saturada aceite mineral y una solución salina equilibrada en la propia jeringa como un medio para eliminar los espermatozoides 22-25. Ambos procedimientos son potencialmente problemática de LC-MS. En primer lugar, es probable que bloquear los nano-columnas nano-C18 que se utilizan básicamente en todo el mundo para el análisis y la atención proteómicos deben tomarse para que ninguno se lleva adelante en el procedimiento de mineral. Si esto ocurre, es imposible continuar y la muestra se pierde esencialmente. Esto se puede superar mediante el uso de BWW u otras soluciones salinas equilibradas en la jeringa, sin embargo, aunque esto tiene éxito, pronto reconoció que muchos de los espermatozoides móviles se vuelven tan pronto como la solución BWW entró en contacto y se mezcla con el caudal del epidídimo las células. Para evitar este problema, simplemente BackFlush los espermatozoides con el aire. No sólo es el qualdad de los espermatozoides comparable a la de los métodos basados en líquidos, pero la cantidad es idéntico.
Phosphoproteomics es quizás una de las pocas formas de establecer vías de señalización que se están produciendo en los espermatozoides después de la eyaculación. Una de las principales vías que estamos investigando es el proceso de capacitación. Los espermatozoides debe someterse a "capacitación" antes de que sea capaz de unirse a un huevo. En la práctica, esto se consigue básicamente mediante la incubación de los espermatozoides durante un período de tiempo (40 min ratón; rata 1,5 hr; humana 3-24 hr) en solución BWW con albúmina de suero. Previamente, nosotros y otros han demostrado un papel para varias quinasas implicadas en la capacitación. De interés, la supresión de la PKA μ II producen ratones cuyos espermatozoides nadar espontáneamente in vitro, pero no puede someterse a la hiperactivación 26. Este último es un sello distintivo de capacitación, por lo que cambiar su patrón de natación espermatozoides a partir de una velocidad alta, baja amplitud, a una bajavelocidad, alta amplitud de frecuencia de batido. Hemos demostrado quinasas de base que intervienen en este proceso incluyen PP60-CSRC (SRC) 13,27 c-sí 28 y c-ABL 14. Curiosamente, la inhibición de SRC detiene capacitación dependiente de la fosforilación de tirosina 13. Sin embargo, esto se puede superar con ácido ocadaico, lo que sugiere que SRC no está directamente implicada en la aparición general de fosforilación de la tirosina 29, pero puede regular una fosfatasa 29. El problema de usar BWW como medio para forzar espermatozoides de epidídimo es que una vez activado, los espermatozoides de ratón sólo toma unos 40 minutos para capacitar. Dado que el aislamiento de los espermatozoides puede tomar 5 min / ratón y, a menudo varios ratones se utilizan en un experimento, a continuación, será espermatozoides en diferentes etapas de madurez en el inicio del experimento. Para superar esto, la presión de aire puede ser utilizado para empujar los espermatozoides del epidídimo caudal dentro de una cánula de vidrio. No sólo son todos los inact espermaive y esencialmente tal como se les encontraron en el medio caudal, hace posible la comparación fosfoproteómica no móviles y móviles.
Manipulación para fosfoproteómica muestra debe mantenerse a un mínimo cuando se comparan los espermatozoides en dos estados funcionales diferentes. El uso de cloroformo metanol sobre otros métodos tradicionales de proteína precipitación 1) disminuye la necesidad de etapas de lavado adicionales, 2) quita casi todos los rastros de sales y grasas y 3) tiene una capacidad probada para precipitar las proteínas de baja abundancia sobre TCA 19. Se recomienda la precipitación de proteínas antes de la digestión con tripsina ya que no sólo hace esto ayuda para desnaturalizar la proteína (que ayuda a la digestión de tripsina), pero elimina muchos de los metabolitos MS-incompatibles presentes en la célula.
La comparación de fosfopéptidos de esperma se puede hacer en un número de maneras. En el nivel básico, una simple comparación de la fosfopéptido identificado en una muestra, para que en otromuestra en el proceso conocido como "conteo espectral" se puede hacer. Sin embargo la crítica ha sido en este enfoque básicamente porque los estudios proteómicos primeros estaban usando réplicas de baja (para una discusión más completa ver Lundren et al. 30). Un enfoque más sofisticado es mirar a la intensidad de la masa progenitora péptido y comparar esto con las otras muestras (comparación libre de etiquetas). En el ejemplo mostrado en la Figura 4, un péptido ausente de la de no móviles (Figura 4 arriba), pero presente en la motilidad (Figura 4 abajo) los espermatozoides de m / z 650-670 puede ser visto. Este proceso, denominado etiqueta basada en MS cuantificación libre es una estrategia sin etiquetas.
Una estrategia alternativa comúnmente utilizado para reducir la cantidad de carreras necesarias para la cuantificación proteómica es el uso de isótopos. Como la masa de un isótopo es diferente, el espectrómetro de masas puede ser utilizado para comparar las intensidades de la eluting péptidos. Sin embargo, a diferencia de la mayoría de los otros tipos de células, algunos marcaje isotópico no se puede aplicar a los espermatozoides. Por ejemplo, la adición de isótopos estables (un isótopo pesado se agrega a una muestra, mientras que una versión más ligera se agrega a otro) se puede utilizar en cultivo de tejidos. Cuando los isótopos se incorporen en la proteína, un análisis de proteómica se puede realizar mediante la combinación de las dos muestras (Multiplexing). Sin embargo, en el caso de los espermatozoides, esto no puede hacerse, simplemente en virtud del hecho de que 1) el etiquetado de isótopos requiere varios pasajes (hasta 8) en cultivo de tejidos y 2) las células de esperma no tiene la transcripción del gen nuclear y la traducción y por lo tanto, no pueden incorporar los isótopos en toda su proteína de todos modos. Una forma de evitar esto es ordenar ratones radiomarcados, sin embargo, estos son muy caros. Un enfoque alternativo es utilizar una etiqueta química. Esto se ha hecho cuando los ratones no capacitados se compararon con los ratones capacitados. En este caso, un D 0 D y una 3 -label se utiliza para distinguir entre una muestra y otra en el espectrómetro de masas 31. Otros enfoques pueden incluir el uso de iTRAQ (etiquetas isobáricas para cuantificación relativa y absoluta), con lo lisinas están etiquetados químicamente con diferentes isótopos de masas; iCAT (isótopo codificado marcador de afinidad) con lo cual cisteínas se etiquetan con diferentes isótopos de masas y etiquetado de agua pesada y ligera.
En cada caso, sin embargo, una cosa hay que tener en cuenta. El MS sólo informa lo que está presente en una muestra, y esto es un reflejo de todo lo que ha sucedido a la muestra hasta que punto. Reducción al mínimo de manipulación de la muestra mientras que maximiza el rendimiento en cada etapa es necesaria para un análisis proteómico éxito.
Divulgaciones
The authors declare that they have no competing financial interests.
Agradecimientos
The authors would like to acknowledge the NHMRC for career development award and grant support APP1066336 which supported this work.
Materiales
| Name | Company | Catalog Number | Comments |
| 2,5-Dihydroxy-1,4-benzoquinone | Aldrich | 195464 | |
| 2-D Quantitation Kit | VWR (GE Healthcare) | 80-6483-56 | |
| Albumin from bovine serum | Sigma | A7030 | |
| Ammonia solution 25% | Merck | 1.05432 | |
| Ammonium bicarbonate | Sigma | A6141 | |
| Calcium chloride | Sigma | C5080 | |
| CHAPS 3-[3-(cholamidopropyl)dimethylammonio]-1-propanesulfonate | Research Organics | 1300C | |
| Chloroform | BDH | 10077.6B | |
| Disodium hydrogen phosphate | Merck | 1.06580 | |
| Dithiothreitol (DTT) | Sigma | D9779 | |
| Formic acid | Sigma | O6440 | |
| Glucose | Sigma | G6152 | |
| Glutamine-L | Sigma | G7513 | |
| Hepes (free acid) | Sigma | H3375 | |
| Iodoacetic acid free acid | Sigma | I4386 | |
| Lactic acid | Sigma | L1750 | |
| Magnesium chloride | Res. Org. | 0090M | |
| Methanol | Merck | 10158.6B | |
| Percoll (sterile) | VWR (GE Healthcare) | GEHE17-0891-01 | |
| Phosphatase Inhibitor Cocktail Halt | ThermoFisher Scientific (Pierce) | PIE78420 | |
| Potassium chloride | Sigma | P9333 | |
| Potassium hydrogen carbonate | Medical Store | CH 600 | |
| Sodium bicarbonate | Sigma | S3817 | |
| Sodium chloride | Sigma | S7653 | |
| Sodium dihydrogen phosphate | Merck | 1.06346 | |
| Sodium hydrogen carbonate | BDH | 10247.4V | |
| Sodium pyruvate | Sigma | S8636 | |
| Tris, ultra pure grade | Amresco (Astral) | AM0497 | |
| Trypsin Gold, mass spec grade | Promega | V5280 | |
| Urea | Sigma | U5128 | |
| Zinc chloride | Sigma | Z0173 | |
| 0.4 mm Polyethylene tubing | Goodfellow | ET317100 | |
| 30 G needle | Terumo | NN2038R | |
| 3 ml Syringe | Terumo | SS035 | |
| 4.2 mm Polyethylene tubing | Goodfellow | ET317640 | |
| Braided silk (5-0) | Dynek | CSS0100 | |
| Trichloroacetic acid | Sigma | 299537 | |
| TiO2 beads (from disassembled column) | Titansphere | 6HT68003 | |
| Eppendorf Tube | Eppendorf | 22431081 | |
| C7B30 | Sigma | C0856 |
Referencias
- Blandau, R., Rumery, R. E. The relationship of swimming movements of epididymal spermatozoa to their fertilizing capacity. Fertil. Steril. 15, 571-579 (1964).
- Tournade, A. Différence de motilité des spermatozoïdes prélevés dans les divers segments de l’épididyme. C. R. Soc. Biol. 74, 738-739 (1913).
- Wyker, R., Howards, S. S. Micropuncture studies of the motility of rete testis and epididymal spermatozoa. Fertil. Steril. 28, 108-112 (1977).
- Eddy, E. M. Male germ cell gene expression. Recent progress in hormone research. 57, 103-128 (2002).
- Lin, M., Lee, Y. H., Xu, W., Baker, M. A., Aitken, R. J. . Ontogeny of Tyrosine Phosphorylation-Signaling Pathways During Spermatogenesis and Epididymal Maturation in the Mouse. 75 (4), 588-597 (2006).
- Jones, R. Plasma membrane structure and remodelling during sperm maturation in the epididymis. J. Reprod. Fertil. Suppl. 53, 73-84 (1998).
- Robaire, B., Hinton, B. T., Orgebin-Crist, M. C., Neill, J. D. . The Epididymis. 3, 1072-1120 (2006).
- Lacham, O., Trounson, A. Fertilizing capacity of epididymal and testicular spermatozoa microinjected under the zona pellucida of the mouse oocyte. Mol. Reprod. Dev. 29, 85-93 (1991).
- Bedford, J. M. Effects of duct ligation on the fertilizing ability of spermatozoa from different regions of the rabbit epididymis. J. Exp. Zool. 166, 271-281 (1967).
- Orgebin-Crist, M. C. Studies on the function of the epididymis. Biol, Reprod. 1, 155-175 (1969).
- Orgebin-Crist, M. C. Maturation of spermatozoa in the rabbit epididymis: effect of castration and testosterone replacement. J. Exp. Zool. 185, 301-310 (1973).
- Lin, M., Hess, R., Aitken, R. J. Induction of sperm maturation in vitro in epididymal cell cultures of the tammar wallaby (Macropus eugenii): disruption of motility initiation and sperm morphogenesis by inhibition of actin polymerization. Reproduction. 124, 107-117 (2002).
- Baker, M. A., Hetherington, L., Aitken, R. J. Identification of SRC as a key PKA-stimulated tyrosine kinase involved in the capacitation-associated hyperactivation of murine spermatozoa. J. Cell. Sci. 119, 3182-3192 (2006).
- Baker, M. A., Hetherington, L., Curry, B., Aitken, R. J. Phosphorylation and consequent stimulation of the tyrosine kinase c-Abl by PKA in mouse spermatozoa; its implications during capacitation. Dev. Biol. 333, 57-66 (2009).
- Baker, M. A., et al. Use of Titanium Dioxide To Find Phosphopeptide and Total Protein Changes During Epididymal Sperm Maturation. J. Proteome. Res. 10 (3), 1004-1017 (2010).
- Baker, M. A., Weinberg, A., Hetherington, L., Velkov, T., Aitken, J. Post-Ejaculatory Changes in the Metabolic Status of Rat Spermatozoa as Measured by GC-MS. Metabolomics. 11, 1-14 (2012).
- Biggers, J. D., Whitten, W. K., Whittingham, D. G. . The culture of mouse embryos in vitro. , (1971).
- Larsen, M. R., Thingholm, T. E., Jensen, O. N., Roepstorff, P., Jorgensen, T. J. Highly selective enrichment of phosphorylated peptides from peptide mixtures using titanium dioxide microcolumns. Mol. Cell. Proteomics. 4, 873-886 (2005).
- Wessel, D., Flugge, U. I. A method for the quantitative recovery of protein in dilute solution in the presence of detergents and lipids. Anal. Biochem. 138, 141-143 (1984).
- Thingholm, T. E., Jorgensen, T. J., Jensen, O. N., Larsen, M. R. Highly selective enrichment of phosphorylated peptides using titanium dioxide. Nat. Protoc. 1, 1929-1935 (2006).
- Thingholm, T. E., Larsen, M. R. The use of titanium dioxide micro-columns to selectively isolate phosphopeptides from proteolytic digests. Methods. Mol. Biol. 527, 57-66 (2009).
- Ecroyd, H., Asquith, K. L., Jones, R. C., Aitken, R. J. The development of signal transduction pathways during epididymal maturation is calcium dependent. Dev. Biol. 268, 53-63 (2004).
- Ecroyd, H., Jones, R. C., Aitken, R. J. Tyrosine Phosphorylation of HSP-90 During Mammalian Sperm Capacitation. Biol. Reprod. 69 (6), 1801-1807 (2003).
- Jones, R., Mann, T., Sherins, R. Peroxidative breakdown of phospholipids in human spermatozoa, spermicidal properties of fatty acid peroxides, and protective action of seminal plasma. Fertil. Steril. 31, 531-537 (1979).
- Wade, M. A., Jones, R. C., Murdoch, R. N., Aitken, R. J. Motility activation and second messenger signalling in spermatozoa from rat cauda epididymidis. Reproduction. 125, 175-183 (2003).
- Nolan, M. A., et al. Sperm-specific protein kinase A catalytic subunit C{alpha}2 orchestrates cAMP signaling for male fertility. Proc. Natl. Acad. Sci. U.S.A. 101, 13483-13488 (2004).
- Mitchell, L. A., Nixon, B., Baker, M. A., Aitken, R. J. Investigation of the role of SRC in capacitation-associated tyrosine phosphorylation of human spermatozoa. Mol. Hum. Reprod. 14, 235-243 (2008).
- Leclerc, P., Goupil, S. Regulation of the human sperm tyrosine kinase c-yes. Activation by cyclic adenosine 3',5'-monophosphate and inhibition by Ca(2). Biol. Reprod. 67, 301-307 (2002).
- Krapf, D., et al. Inhibition of Ser/Thr phosphatases induces capacitation-associated signaling in the presence of Src kinase inhibitors. J. Biol. Chem. 285, 7977-7985 (2010).
- Lundgren, D. H., Hwang, S. I., Wu, L., Han, D. K. Role of spectral counting in quantitative proteomics. Expert. Rev. Proteomics. 7, 39-53 (2010).
- Platt, M. D., Salicioni, A. M., Hunt, D. F., Visconti, P. E. Use of differential isotopic labeling and mass spectrometry to analyze capacitation-associated changes in the phosphorylation status of mouse sperm proteins. J. Proteome. Res. 8, 1431-1440 (2009).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados