Method Article
Evaluación de una anastomosis coronaria Conector asistida por láser Novela - el videoclip Trinidad - en un modelo porcino de bypass sin circulación extracorpórea
En este artículo
Resumen
This paper describes a novel nonocclusive coronary anastomotic connector in a porcine off-pump coronary artery bypass (OPCAB) model. This easy-to-use coronary connector has intrinsic potential to facilitate minimally invasive OPCAB surgery.
Resumen
Para simplificar y facilitar el corazón palpitante (es decir, fuera de la bomba), cirugía de revascularización coronaria mínimamente invasiva, un nuevo conector de la anastomosis coronaria, el videoclip Trinidad, se desarrolla sobre la base de la técnica de anastomosis no oclusiva asistida por láser excimer. El conector Clip Trinidad permite simplificada, sin suturas, y la conexión no oclusiva del injerto a la arteria coronaria, y un excimer láser catéter láser-golpes la apertura de la anastomosis. En consecuencia, debido a la construcción anastomosis completa no oclusiva, acondicionado coronaria (es decir, ocluyendo o maniobras) no es necesario, en contraste con la técnica anastomótica convencional, por lo tanto, simplificar el procedimiento de bypass fuera de la bomba. Antes de la aplicación clínica en la cirugía de revascularización coronaria, la seguridad y la calidad de este nuevo conector serán evaluados en un estudio a largo plazo porcino experimental sin bomba de revascularización coronaria (OPCAB). En este trabajo se describe la forma de evaluar tque anastomosis coronaria en el modelo porcino OPCAB utilizando diversas técnicas para evaluar su calidad. Los resultados representativos se resumen y demostraron visualmente.
Introducción
Sin bomba de bypass de arteria coronaria (OPCAB) cirugía potencialmente puede reducir la morbilidad asociada con el uso de circulación extracorpórea en la cirugía de revascularización coronaria (por ejemplo, las complicaciones tromboembólicas, excesivo retener de líquidos, transfusiones de sangre, y la activación del sistema inmune) y puede ser de beneficio para los pacientes con alto riesgo de complicaciones asociadas con la circulación extracorpórea y la manipulación de la aorta 1. La cirugía de revascularización coronaria mínimamente invasiva (por ejemplo, cirugía, o toracoscópica asistida por robot), reduce el tamaño de las incisiones, y por lo tanto, reduce el tiempo de recuperación del paciente, la estancia hospitalaria y las tasas de morbilidad 2. A pesar de los beneficios potenciales para (un subconjunto de) pacientes en necesidad de revascularización coronaria, la adopción de estas técnicas no se ha generalizado. Una de las razones es que una bomba fuera mínimamente invasiva enfoque para la cirugía de bypass coronario es técnicamente muy difícil.
ontenido "> Para simplificar y facilitar el corazón palpitante (es decir, fuera de la bomba), cirugía de revascularización coronaria mínimamente invasiva, un nuevo conector de la anastomosis coronaria se desarrolla: el videoclip Trinidad 3,4, basado en el excimer anastomosis no oclusiva asistida por láser (ELANA ) técnica de 5-9. El conector permite simplificada, sin suturas, y la conexión no oclusiva del injerto a la arteria coronaria, y un catéter de láser perfora la apertura de la anastomosis. En consecuencia, debido a la construcción completa anastomosis no oclusiva, acondicionado coronaria láser excimer (es decir, ocluyendo o atrapar y maniobras) no es necesario, en contraste con la técnica anastomótica convencional, por lo tanto, simplificar el procedimiento de bypass.Precediendo a los estudios con respecto a un conector coronaria ELANA prototipo predecesor, demostrado su viabilidad en relativamente grandes arterias (diámetro interior [ID] 2.4 milímetros [mm]) en un modelo de conejo aguda 5. Másencima, en un modelo de OPCAB esternotomía abierta porcina, la curación adecuada con hiperplasia intimal mínimo fue encontrado en el largo plazo 6,7.
Recientemente, la técnica de la anastomosis coronaria se ha mejorado aún más hacia la aplicación clínica. Las modificaciones de diseño del conector y el catéter de láser excimer permiten una construcción simplificado y acelerado (es decir, el montaje sin sutura del injerto) a clínicamente relevante, las arterias coronarias de pequeño calibre (ID 1.4 a 1.6 mm). Antes de la aplicación clínica en la cirugía de revascularización coronaria, la seguridad y la calidad de este nuevo conector serán evaluados en un modelo DCSCEC esternotomía abierta porcina en el largo plazo (6 meses de seguimiento), de acuerdo con el protocolo descrito en este documento.
Este protocolo describe nuestro modelo experimental porcino OPCAB y proporciona una descripción detallada del procedimiento de anastomosis coronaria. Además, las opciones se describen por intraoperatorias, postoperative, y la evaluación post-mortem de la anastomosis, que son de vital importancia en la evaluación de la calidad de la anastomosis. En este trabajo, la sección de Resultados Representante resume los resultados de un estudio piloto en el modelo DCSCEC porcino (n = 3 cerdos, con un seguimiento de 5 horas), que se realizó antes del estudio preclínico.
Protocolo
NOTA: Los animales recibieron atención humanitaria en el cumplimiento de la "Guía para el Cuidado y Uso de Animales de Laboratorio", elaborado por el Instituto de Recursos Animales de Laboratorio, Consejo Superior de Investigaciones Científicas. El comité de la experimentación animal de la Universidad de Utrecht aprobó el protocolo.
1. El procedimiento de anastomosis coronaria
NOTA: Siempre use gafas de protección láser cuando el láser está activo.
- Montaje del videoclip Trinidad
- Abra el tenedor superior del conector 3 (Figura 1) con la pinza de aneurisma aplicador (Figura 4A) e insertar en el lumen del injerto perfundido, dirigida distalmente (Figura 5A). Asegúrese de que la longitud total del tenedor se coloca intraluminal. Posteriormente, suelte el aplicador.
- Ocluir la arteria mamaria proximal con un clip de bulldog no traumática y carefully enjuague lumen los injertos 'con una solución de heparina salina. Posteriormente, introducir el catéter láser 4 (figura 2) por vía intravascular, a través del extremo distal libre del injerto, en el conector, y fijar por el clip de fijación externa (Figura 3).
- Iniciar succión de vacío a través del catéter en el injerto (para aplicar vacío a través del catéter, conectar un tubo de vacío para el catéter y a una bomba de vacío), activar el láser y láser de perforar el injerto una vue, resultando en un orificio de la anastomosis de 0,8 por 2,0 mm. Suelte la succión al vacío directamente después del tratamiento con láser. Compruebe visualmente si la pared arterial está totalmente extirpado.
- Retire el fragmento de láser perforada del injerto (es decir, "aleta"), que se adjunta al canal de vacío del catéter, y dejar el catéter fijado en el injerto y el conector (Figura 5B).
- Conexión no oclusiva del injerto a la Recipient
- Abra el tenedor inferior del conector con el aplicador Vasco (Figura 4B) e insertar en el lumen de la arteria coronaria perfundido, dirigida distalmente (Figura 5C). Asegúrese de que la longitud total del tenedor se coloca intraluminal. Posteriormente, suelte el aplicador.
- Arteriotomıa láser perforado
- Iniciar succión de vacío sobre la pared coronaria y posteriormente láser-Punch la pared coronaria bajo flujo coronario nativa completa, resultando en un orificio de 0,8 por 2,0 mm. No aplique fuerza sobre el catéter durante la construcción.
- Retire el clip de fijación con el aplicador de clips de aneurisma y posteriormente retirar el catéter. Compruebe si el colgajo láser perforado está unido al canal de vacío del catéter y cesar la succión de vacío (Figura 5D).
- Después de la recuperación de la aleta, ocluir el extremo distal del injerto por un clip temporal (por ejemplo, clip bulldog). Si una diversiónde derivación ficticia se confirma (es decir, la recuperación de la aleta éxito y flujo de derivación adecuada), ligar permanentemente el extremo distal del injerto usando un hemoclip (Figura 5E).
- En caso de un fallo de recuperación de aleta (es decir, una solapa de forma incompleta tratada con láser todavía está parcialmente unido a la pared coronaria), retraer el conector, cerrar la arteria coronaria parcialmente tratada con láser con suturas de prolene (8-0), y crear una nueva anastomosis, a partir de en el paso 1.1.2.
2. Los animales, anestesia y eutanasia
- Animales y Anestesia
- Utilice femenina (por ejemplo, Landrace holandés) cerdos (70-90 kg [kg]) y alimentar a una dieta normal.
- Administrar 320 miligramos (mg) de ácido acetilsalicílico y 75 mg de clopidogrel por vía oral al día, empezando 3 días antes de la cirugía. Continúe con este protocolo de anticoagulación hasta la terminación.
- Administrar fentanilo 25 microgramos (mg) por vía transdérmica para 3día: 25 mg 24 horas antes de la intervención y 25 mg en el día 1 después de la operación para la analgesia postoperatoria.
- Para la inducción de la anestesia administrar ketamina (10 mg / kg), midazolam (0,5 mg / kg), y atropina (0,04 mg / kg) por vía intramuscular.
- Posteriormente, administrar tiopental sódico (4 mg / kg), midazolam (0,5 mg / kg), citrato de sufentanilo (6 mg / kg), y 1000/100 mg de amoxicilina-ácido clavulánico (profilaxis antibiótica) a través de una línea intravenosa.
- Intubar y ventilar con una mezcla de oxígeno y aire (1: 1 volumen / volumen).
- Utilice un colirio y posteriormente cerrar los ojos para prevenir la deshidratación de los ojos.
- Entonces administrar como una infusión intravenosa continua de midazolam (0,7 mg / kg / hr), citrato de sufentanilo (6 mg / kg / hr), bromuro de pancuronio (0,1 mg / kg / hr), y solución salina (300 ml / hr). Comience con 300 mg amiodaron en solución de almidón hidroxietil 500 ml a través de la línea intravenosa.
- Inserte una línea arterial en la arteria femoral fo control de la presión sanguínea intra-arterial y muestras de sangre arterial.
NOTA: Ninguna cirugía se iniciará antes de que esta línea de presión es funcional. Uno puede detectar el dolor, en caso de que el animal no está suficientemente anestesiado, por un aumento de la frecuencia cardíaca y la presión arterial. Si se detecta un aumento de la frecuencia cardíaca y la presión arterial, aumentar la administración de midazolam y el citrato de sufentanilo. - Administrar metoprolol por vía intravenosa (intervalo de 5-20 mg) para reducir la irritabilidad mecánica del corazón hasta una frecuencia cardíaca de aproximadamente 50-70 se obtiene latidos / min.
- Cateterizar la vejiga a través de la uretra durante el procedimiento.
- Recuperación
- Detener la anestesia si se eliminan los drenajes (vea los pasos 03.09 a 03.11).
- Si el animal está alerta y recobró el conocimiento suficiente para respirar adecuadamente después de la extubación, devolver el animal a la jaula (es decir, el área de alojamiento de los animales). No deje que el animal sea desatendidofore este punto.
- Coloque una máscara de oxígeno 0,5 litros (L) delante del hocico mediante una instalación segura y protegida.
- No devuelva un animal que ha sido objeto de un tratamiento quirúrgico para la compañía de otros animales hasta que se recupere completamente.
- Después de la operación, administrar synolux (amoxicilina-ácido clavulánico; 250 mg / 20 kg) por vía oral dos veces al día en el día 1 como una profilaxis antibiótica, y meloxicam (0,4 mg / kg) por vía intramuscular diaria en el día 1 y 2 para la analgesia postoperatoria.
- Eutanasia
- Totalmente heparinizar por 25.000 UI de heparina (obtener un tiempo de coagulación activado [ACT] de por lo menos 4 veces el valor de control) para evitar la coagulación post-mortem.
- La eutanasia a los animales con pentobarbital sódico (200 mg / kg) por vía intravenosa y confirmar la muerte antes de comenzar con los exámenes post-mortem - parte 6 de este protocolo.
3. Cirugía
NOTA: Una sala de operaciones estándar es requirojo para el procedimiento, que contiene todo el material estándar y equipo (al menos un monitor de presión arterial, un dispositivo de electrocardiografía y un oxímetro de pulso). Un conjunto estándar toracotomía, una arteria torácica (ITA) retractor interna, un conjunto de microcirugía y los instrumentos-experimento específico deben ser preparados y esterilizados. Se recomienda el uso de un bucle quirúrgico y un faro quirúrgico.
- Abrir el tórax mediante esternotomía. Sin rodeos diseccionar (con el dedo) el pericardio del esternón. Entonces vio o división (con un martillo y buril) el esternón del proceso xifoides hasta el manubrio. Utilice bonewax para evitar la fuga de la médula esternal.
- Cosecha de la izquierda (o derecha) ITA de la segunda costilla hasta el diafragma, parcialmente heparinizar (ACT al menos 2,5 veces el valor de control), y el clip y diseccionar el ITA en el sitio distal.
- Inmovilizar y presentar la arteria coronaria diana por un estabilizador de tejido en el lugar previsto(Diámetro exterior [OD] 1.6 a 1.9 mm, medida con un calibrador, o, ID 1.4 a 1.6 mm, medido con ultrasonido epicárdico [ECUS]). Diseccionar el objetivo coronaria, eliminar el tejido peri-adventicia suelto, y cubrir el objetivo coronaria con una gasa empapada en la papaverina.
- Preparar la ligadura permanente de la arteria coronaria nativa ± 2,0 a 3,0 cm proximal a la anastomosis (ver sección 3.7) por una amplia disección lateral de la arteria coronaria, de tal manera que un hemoclip puede ligar completamente la arteria coronaria.
- Diseccionar el área objetivo del ITA, ± 2,0 a 3,0 cm proximal al extremo libre distal, retire el tejido peri-adventicia, y medir el calibre (OD 2,0 a 4,0 mm).
- Construir la anastomosis con el Clip Trinidad como se ha descrito anteriormente, o alternativamente, la construcción de una anastomosis suturada a mano y utilizar un shunt para minimizar la isquemia miocárdica.
- Ligar la arteria coronaria proximal con 3 hemoclips medianas. Asegúrese de que no hay ramas laterales son ocluido y laligadura es 100% oclusiva, impidiendo el flujo competitivo.
NOTA: Ajuste y establecer el flujo de injerto mediante la colocación de clips de ligadura atraumáticas temporales en la arteria coronaria, mientras que se mantiene una presión representante arterial media y la posición fisiológica del corazón; para construir un puente de bajo flujo, ligar la coronaria suficientemente distal, y para permitir un mayor flujo de injerto, ligar la coronaria relativamente más proximal 10. - Cubra la anastomosis con pericardio para evitar la tracción incontrolada en la anastomosis, después de cerrar el tórax.
- Colocar un mediastinal y / o un drenaje pleural y conectarse a un sistema de aspiración.
- Cierre el pecho.
- Una vez que los desagües dejan de producir, extraer los drenajes.
4. Examen intraoperatoria
- General intraoperatoria de datos
- Registre las dimensiones de los objetivos de la ITA y la arteria coronaria con un calibrador (OD) o ECUS (ID; véase la sección 3.3), el tiempo de construcción de la anastomosis (minutos o segundos), cualquier fuga de la anastomosis (categorizar: por ejemplo, la hemostasia directa, exudación, o fuga a paso ligero 5,6), y tenga en cuenta si se necesitan puntos extra para obtener la hemostasia.
- Tiempo de tránsito medición de flujo (TTFM)
- Registre el flujo medio, curvas de flujo, el porcentaje de llenado diastólico, y el índice de pulsatilidad (PI), combinada con la presión arterial media.
NOTA: Modern consolas TTFM calculan estas variables de forma automática. - Coloque la sonda de flujo del tiempo de tránsito en un segmento de esqueleto del injerto distal con gel acuoso para mejorar el contacto de la sonda. Utilizar diferentes tamaños de sonda para evitar la distorsión o compresión del injerto.
- Mida por una presión arterial sistémica adecuada, antes y después de soltar el estabilizador de tejidos, con el corazón en su posición fisiológica, y de nuevo antes del cierre pecho.
- Calcular la PI para (max-min flujo flujo) Caudal / media. El PI es un indio de la calidad de la anastomosis 11,12.
- Registre el flujo medio, curvas de flujo, el porcentaje de llenado diastólico, y el índice de pulsatilidad (PI), combinada con la presión arterial media.
- Opcional: Pico hiperémicas Respuesta Flow
- A una presión arterial media de 90 mm Hg, sujetar el injerto durante 30 segundos y, posteriormente, medir la respuesta hiperémica del flujo pico, ± 30 min después de la liberación del estabilizador tejido 6.
- Calcular la respuesta coronaria pico de flujo en hiperemia (es decir, el flujo de reserva de la anastomosis) por el flujo del injerto pico medio dividido por el flujo basal media de 90 mmHg.
- Duplicar la medición después de 10 min.
- Opcional: epicárdica Ultrasonido
- Coloque la sonda ECUS en la anastomosis con gel acuoso para mejorar el contacto de la sonda. Adquirir una transversal y longitudinal imagen de la anastomosis ITA-LAD con el corazón estabilizado por el estabilizador de tejidos.
- Registre la anchura, la longitud, y la altura de la anastomosis con el sistema de ecus y evaluar la calidad de la geometría de la anastomosis y la salida coronaria tract 13. Si reducido (por ejemplo, por Back o captura pared lateral), revisar la anastomosis.
NOTA: Metal (por ejemplo, un hemoclip o un conector anastomótica) influye en la calidad de imagen.
- Angiografía Coronaria intraoperatoria: Opcional
- Visualice el bypass por un angiografía coronaria estándar. Introducir un catéter a través de la arteria ilíaca. Grado de la permeabilidad de acuerdo con los criterios Fitzgibbon.
5. Seguimiento de Examen
- Angiografía coronaria
- Visualizar el bypass por una angiografía coronaria estándar y la permeabilidad de acuerdo con los criterios Fitzgibbon grado.
- Opcional: Medición de tránsito de flujo Tiempo
- Haga una incisión subaxilar en la línea dorsal-ventral, siguiendo la curvatura torácica. Si es necesario, retire parcialmente la segunda o tercera costilla, y diseccionar el ITA proximal.
- Medir y registrar el injertofluir por la medición de flujo del tiempo de tránsito (ver sección 4.2).
- Opcional: reserva fraccional de flujo y la reserva de flujo coronario
- Administrar nitroglicerina intracoronaria (200 mg) para prevenir los espasmos.
- Medir simultáneamente la presión intracoronaria y la velocidad de flujo. Registre la presión y el caudal, en combinación con las señales de presión y ECG aórticos.
- Calcular la reserva fraccional de flujo (RFF) de (3) consecutivos mediciones directamente distales (coronarias) y proximal (LITA) a la anastomosis, y en la arteria coronaria circunfleja (Cx; controlar las arterias coronarias). Realizar las mediciones al inicio y durante la hiperemia máxima, inducida por un bolo de adenosina intracoronaria (60 mg).
- Calcular la reserva de flujo coronario (CFR) como la relación de la velocidad del flujo hiperémica máxima por la velocidad de flujo en la línea de base 14.
- Opcional: Tomografía de Coherencia Óptica
- Utilice una coherencia óptica de dominio de frecuencia paratomografía sistema (OCT) para obtener imágenes de la derivación con un retroceso automático de velocidad de 20 mm / seg y un color continuo de contraste por inyección manual.
- Record hiperplasia de la íntima y la dimensión de la derivación (es decir, el área de la luz de referencia de la coronaria e ITA 1,0 cm abajo y aguas arriba de la anastomosis, respectivamente, y el orificio de la anastomosis) 7,15.
6. postmortem Exámenes
- Explantación, Fijación, e inspección macroscópica
- Para minimizar el riesgo de dañar el bypass, explantar el corazón en bloque, incluyendo el esternón y las costillas, y marcar la parte muy proximal de la ITA para la infusión de formalina.
NOTA: Algunos días después de un procedimiento de tórax abierto, el corazón está completamente unida al esternón por adherencias del tejido conectivo. Realización de una esternotomía puede dañar el bypass y, por lo tanto, no se recomienda. - Realice una FIJACIÓN perfundidopara arreglar la carretera de circunvalación en su forma fisiológica, lo que permite su posterior interpretación histológica adecuada. Infundir el ITA con formol (4%) en una cabina de flujo a ± 90 mm Hg:
- Coloque una botella con formalina (1 L) ± 1 metro más alto que el corazón.
- Conectar un tubo (por ejemplo, un tubo de silicona de un sistema de infusión estándar o similar) entre la botella y el ITA proximal.
- Infundir la formalina en el corazón, a través de la ITA y la anastomosis, durante aproximadamente 60 min o hasta que todo formalina está completamente infundido.
- Entonces, extirpar cuidadosamente el bypass con una cuchilla, tijeras y fórceps. Deje algo de fibrina / tejido de la cicatriz, miocardio, ITA proximal y coronaria, y distal coronaria, que se adjunta a la anastomosis.
- Fijar la anastomosis, una parte de referencia de la ITA (± 1 cm aguas arriba de la anastomosis), y una parte de referencia de la LAD (± 1 cm aguas abajo de la anastomosis), durante la noche en formalina al 4%.
- Abra la longit arteria coronariaudinally en la pared inferior e inspeccione la anastomosis utilizando 10 o 20 aumentos. Registre el ancho y largo de la boca anastomótica por perpendicularmente fotografiar el orificio con una regla al lado de él. Posteriormente, medir la anchura y longitud de la anastomosis digitalmente.
- Para minimizar el riesgo de dañar el bypass, explantar el corazón en bloque, incluyendo el esternón y las costillas, y marcar la parte muy proximal de la ITA para la infusión de formalina.
- Análisis histológico
- Incrustar la anastomosis y las piezas de referencia en plástico (metacrilato de metilo).
- Sección en transversales (o longitudinales) planos con una sierra de diamante, a partir de 5 mm aguas abajo, continuando hasta 5 mm aguas arriba de la anastomosis, y la mancha con hematoxilina y eosina.
- Grabar y evaluar la aposición de la pared del vaso, zona anastomótica, la formación de trombos, hiperplasia de la íntima, la superficie expuesta nonintimal sangre-16 (BENIS; intraluminal la exposición de la superficie del conector y el borde de láser [es decir, la superficie medial y adventicia de ambos el injerto y la coronaria arteria]), aguda y la reacción celular inflamatoria crónica (células polimorfonucleares, macrófagos y células gigantes de cuerpo extraño), y el daño tisular 6.
- Realizar mediciones utilizando un paquete de software.
- Opcional: Microscopía Electrónica de Barrido
- Fijar la anastomosis, después de la fijación perfundido descrito anteriormente (véase la sección 6.1.2), en una solución de glutaraldehído al 2% tamponado en tampón fosfato 0,1 M purificada.
- Ponga la anastomosis 1 hora en 1% de tetróxido de osmio tamponado para completar la fijación.
- Después de la fijación, deshidratar la anastomosis en una serie graduada (50, 70, 90, y 100%) de etanol y CO en líquido 2 mediante el método de punto crítico.
- Posteriormente, abrir la pared posterior de la coronaria y la pared superior de la ITA en el sitio anastomótico con una cuchilla quirúrgica agudo.
- Fijar la muestra en tinas de exploración y cubrir con una fina capa de platino por el procesamiento por pulverización catódica para mejorar la calidad de la imagen.
- Luego de evaluar la surfa anastomótica intravascularce (es decir, la evaluación de endotelial y / o la cobertura de trombocitos) utilizando un microscopio electrónico de barrido 6.
Resultados
Se realizó un estudio piloto previo a la evaluación de la nueva trinidad videoclip en un gran estudio preclínico de seguridad a largo plazo para evaluar la viabilidad. En este estudio piloto, 3 anastomosis LITA-a LAD (n = 1 por animal) se construyeron con el conector en el modelo porcino DCSCEC por 1 investigador (DS). A 5 horas de seguimiento se programó.
El conector de la anastomosis coronaria activar completamente no oclusiva, sin suturas, y la construcción de la anastomosis rápida (media 3,4 ± 0,4 min). En todas las anastomosis hemostasia completa se demostró con una tasa de recuperación de aleta 100%. Los datos operativos, que se enumeran en la Tabla 1, demuestran la viabilidad del conector de la anastomosis coronaria en el modelo DCSCEC porcino. Curvas de flujo atractivos normales con picos mínimos sistólica, un PI por debajo de 5, y un relleno predominante diastólica injerto (llenado diastólico [DF] 80%) se mide constantemente durante el seguimiento, como se ve en la Figura 6, que es sugcongestiva para un injerto de coronaria patente. La respuesta del flujo hiperémico pico medio, tras 30 seg oclusión del injerto, fue de 5,6 ± 0,5, lo que indica una reserva de flujo coronario adecuado. A las 5 horas de seguimiento, la inspección macroscópica demostró anastomosis de patente sin formación de trombo intraluminal como puede verse en la Figura 8A. Figura 7 muestra un ejemplo de un angiograma a las 5 semanas de seguimiento, y un ejemplo de la post-mortem macroscópico e histológico inspección se mostró en las figuras 8B y C, tanto que demuestra claramente una anastomosis remodelado y totalmente patente a las 5 semanas de seguimiento (resultados iniciales del estudio preclínico). Por otra parte, los ejemplos de octubre y SEM imágenes de un estudio previo con una ELANA conector anastomosis coronaria predecesor 6,7 demuestran una anastomosis patente sin reducir la formación de hiperplasia de la íntima, y una cobertura completa con el endotelio, respectivamente, a los 6 meses de seguimiento (Figura 9 ).
| Anastomosis (n) | 3 |
| LITA (mm, OD) | 3,2 ± 0,2 |
| LAD (mm, OD) | 1,8 ± 0,0 |
| El tiempo de construcción (min) | 3,4 ± 0,4 * |
| Tasa de recuperación de la aleta (%) | 100 (3/3) |
| Hemostasia completa (%) | 100 (3/3) |
| Puntada extra | 0 |
| Flujo de línea de base de injerto (ml / min) | 20 ± 3 |
| Flujo de injerto en t = 5 hr (ml / min) | 18 ± 5 |
| Respuesta del flujo en hiperemia máxima (pico / flujo basal) | 5.6 ± 0.5 |
Tabla 1: Datos Operativos del pimucho estudio. Los datos presentados como media ± desviación estándar o% (n).
* Incluye: montaje del conector, la conexión del injerto coronario, la arteriotomía láser perforado, y la ligadura del injerto distal.
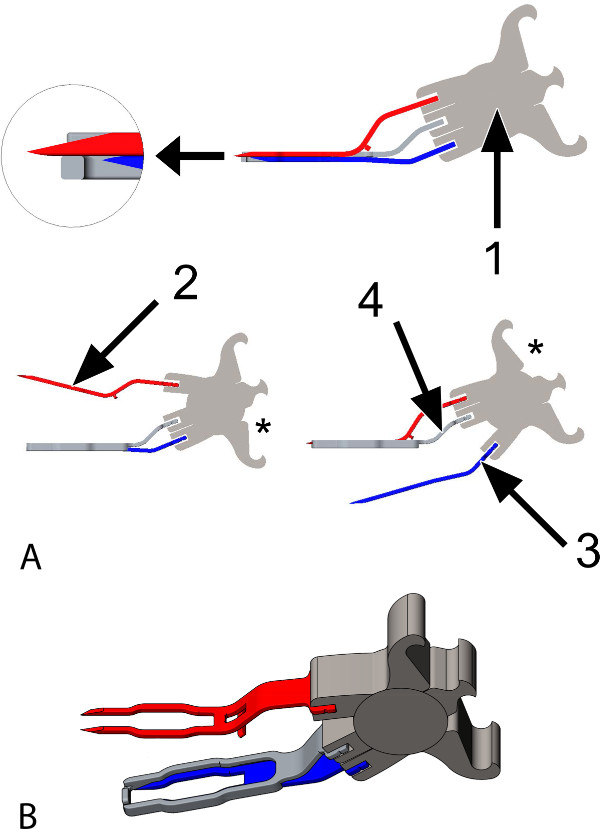
Figura 1:. La Trinidad de clip (A) Animado imágenes del conector de la anastomosis coronaria, una vista lateral. El conector está construido de titanio y es adecuado para las arterias coronarias diana con un diámetro interior (ID) entre 1,4 y 1,6 mm. El conector consta de: 1: Un muelle, que permite a los 2 horquillas para abrir y cerrar, individualmente uno por uno (inferior izquierda y el panel de la derecha), mediante la colocación de un aplicador en 1 de los ejes de la primavera (ver asteriscos, no aplicador se muestra). Además, proporciona una compresión activa de los 2 tenedores. 2 y 3: Dos horquillas con cada 2 patillas afiladas, que se adjunta a la primavera (1); el tenedor superior (2, rojo) se insertará en el injerto, el tenedor inferior (3, azul) se insertará en la arteria coronaria 4: Una banda extravascular (2 veces el espesor de los pasadores; ilustra de forma transparente en la parte superior. panel), adyacente a las horquillas más de su longitud, por la presente la obtención de compresión lateral extra. Se inserta en la primavera, en medio de los puntos de anclaje de las horquillas. Al abrir el tenedor inferior (3, azul; inferior derecha), el tenedor superior (2, rojo) mantiene compresión (del injerto) sobre la banda (4). La subsección ampliada (parte superior izquierda) demuestra la posición de la punta del tenedor superior más larga (2, rojo) en una muesca en la parte frontal de la banda extravascular (4). (B) Imagen animada del conector, un VI superior diagonalew. El tenedor superior se abre (aplicador no se muestra).
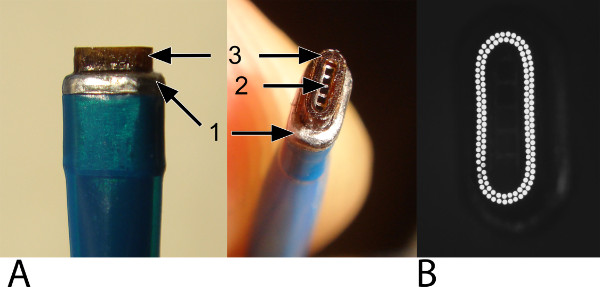
Figura 2:. El catéter de láser ovalada El catéter láser ovalada se utiliza para la arteriotomía láser perforado en el injerto y la arteria coronaria. Tenga en cuenta que el catéter láser no soldar o sellar la anastomosis (A) La banda exterior (1; parte más ancha). Facilita el posicionamiento y la estabilización en el conector de la anastomosis y proporciona seguridad (es decir, se evita que el catéter láser de deslizarse a través del conector y dañar la pared inferior de la arteria coronaria). El canal de vacío (2) tiene una ubicación céntrica y está rodeado de fibras de láser (3). (B) una vista desde arriba en la punta del catéter láser. Una fila de 2 fibras de láser se visualiza.

Figura 3:.. El clip de fijación An, clip de fijación temporal externa se utiliza para fijar y estabilizar el catéter de láser en el conector montado de la anastomosis, asegurando el posicionamiento perpendicular adecuada del catéter durante la construcción anastomosis (A) A la vista lateral (izquierda) y una vista inferior (derecha). El muelle (1) proporciona una fuerza en tanto la carcasa (2), que mantiene el catéter, y las barras (3), que capturan el conector. (B) Las flechas apuntan en el catéter, que es perpendicular obsesionado por el clip de fijación y forma un complejo estabilizado con el conector y el injerto (no mostrado).
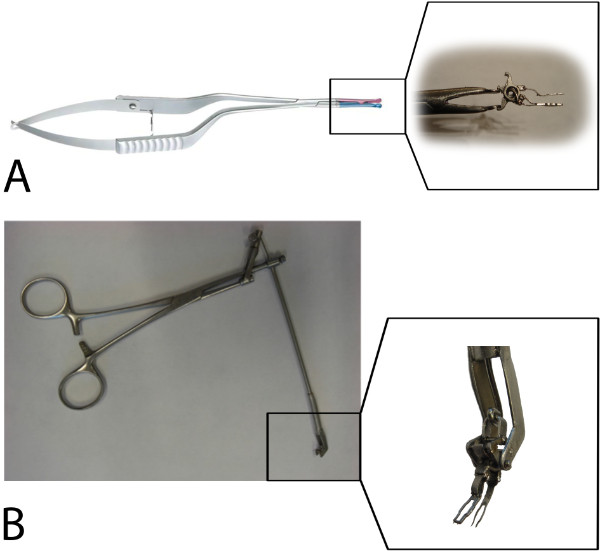
Figura 4: Los aplicadores (A).Un aplicador de clips de aneurisma estándar controla el tenedor superior a través de la eje de aplicación inferior del resorte (ver la subsección) y, además, el clip de fijación. (B) Un prototipo Vasco aplicador controla el tenedor inferior a través de la eje de aplicación superior del muelle (véase la subsección).
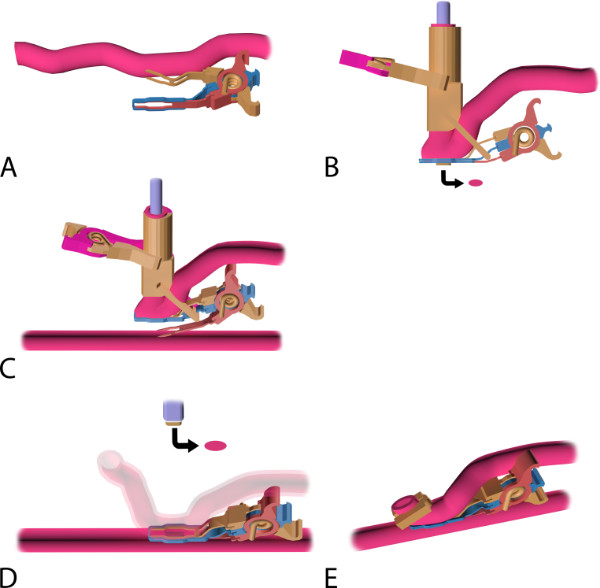
Figura 5: El procedimiento de anastomosis coronaria con el Sistema de Clip Trinidad (A) de montaje del conector de la anastomosis coronaria:. Un aplicador (no mostrado) se utiliza para insertar el tenedor superior del conector en el lumen del injerto perfundido, dirigida distalmente. Nota: al liberar el aplicador, el conector se cierra y activa comprime el injerto entre los 2 tenedores y la banda extravascular (B) El injerto montado y láser con perforaciones.. El catéter se introduce por vía intravascular de láser, a través de la distal extremo libre del injerto, en el conector, y está fijada perpendicularmente por el clip de fijación externa. El injerto es láser con perforaciones. Los puntos de flecha en el fragmento de láser perforada del injerto (es decir, "aleta") (C) de conexión no oclusiva del injerto a la coronaria: un aplicador. (No se muestra) se utiliza para insertar el tenedor inferior. El tenedor perfora la pared coronaria y está completamente insertado en el lumen de la coronaria perfundido, dirigida distalmente. Durante la inserción, el tenedor superior mantiene la compresión del injerto sobre la banda extravascular, asegurando la fijación adecuada del injerto durante esta maniobra, mientras que el clip de fijación asegura un posicionamiento perpendicular adecuada del catéter láser. (D) arteriotomía Laser-perforada de la coronaria arteria: el conector está cerrado y comprime ambas paredes de los vasos (es decir, de injerto y la arteria coronaria) entre los 2 horquillas intraluminales y la banda extravascular. La pared coronaria es láser perforado by el catéter obsesionado, perpendicularmente posicionado en la pared de la arteria coronaria. Posteriormente, se retira el clip de fijación y el catéter retraído, incluyendo la solapa recuperado (véase la flecha). (E) anastomosis Final. A hemoclip de ligadura se coloca en el extremo distal del injerto. Nota: El conector completa permanece in situ y no se quita después de la construcción anastomosis.
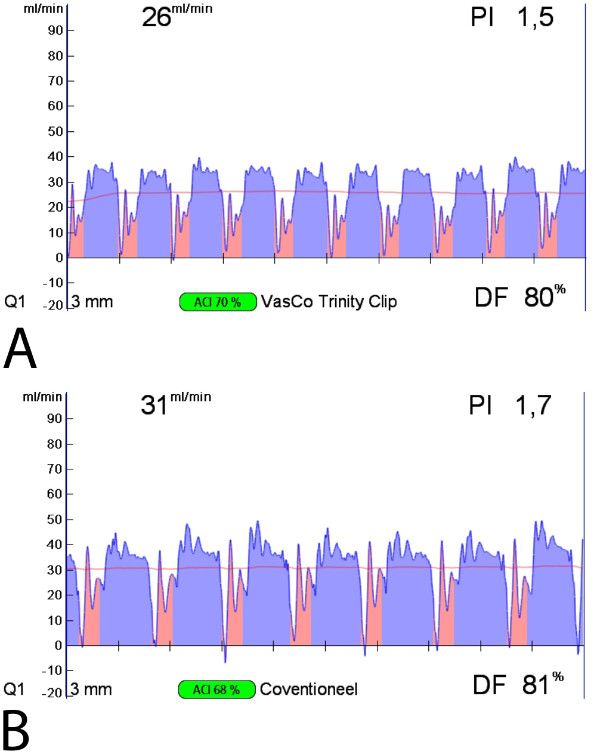
Figura 6: mediciones de flujo de tiempo de tránsito intraoperatorias del videoclip Trinidad facilitó dejó arteria torácica interna (LITA) -para-izquierda descendente anterior (LAD) anastomosis y una anastomosis convencional suturada a mano-LITA-a LAD Tanto el facilitado (A). y (B) de derivación-LITA-a LAD suturada a mano muestran una curva normal atractivo flujo, un PI por debajo de 5, y un Predomina nt llenado diastólico del injerto (llenado diastólico [DF] 80%) con picos sistólicos mínimos, sugerentes para un injerto coronario patente.
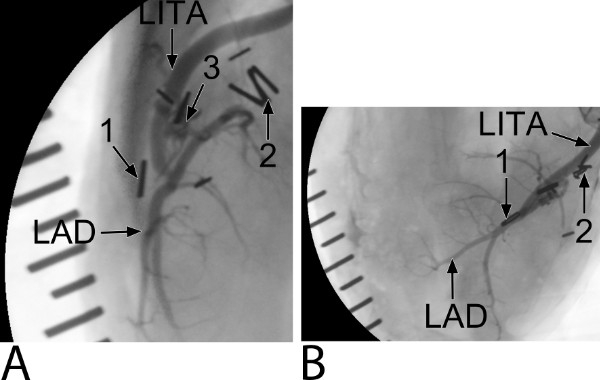
Figura 7: Cinco semanas angiograma coronario del videoclip Trinidad facilitó la arteria torácica interna izquierda (LITA) arteria (LAD) anastomosis -para izquierda descendente anterior (un ejemplo del estudio preclínico) (A) Una vista del lado lateral.. Hemoclips de ligadura se colocan en el extremo distal de la LITA (1) y LAD nativa proximal (2). El conector (3) sólo se puede ver en la vista lateral. Nota, la cobertura de las horquillas y la banda extravascular del conector por la materia no radiopaco se ve. El extremo distal de la ATII no está llena de contraste, lo que sugiere la remodelación mediante la racionalización de la neoíntima. (B) Una vista superior.
ghres.jpg "/>
Figura 8: La curación y remodelación del videoclip Trinidad facilitó dejó arteria torácica interna (LITA) arteria descendente anterior (LAD) anastomosis -para izquierda:. Vista macroscópico e histológico (A) Aspecto macroscópico del interior de la LAD a las 5 horas de seguimiento . Una anastomosis patente sin ninguna formación de trombo intraluminal se demuestra. El tenedor inferior del conector está posicionado intraluminal, sin capturar o dañar la pared coronaria lateral o inferior. Un borde cortado con láser pequeño y afilado (0,1 mm), tanto de la LITA y la DA, es visible entre los tenedores, y las dos paredes del vaso se coloca exactamente en la parte superior de uno al otro, sin superposición de tejido de la adventicia. (B) macroscópica vista desde el interior de la LAD a las 5 semanas de seguimiento (un ejemplo del estudio preclínico). Una anastomosis patente se muestra y las horquillas intraluminal y el borde láser están completamente cubierta por un pañuelo de papel. capa, sin estrechamiento del orificio de la anastomosis (C) sección transversal histológico, a mediados de la anastomosis, a las 5 semanas de seguimiento (12.5X magnificado; un ejemplo del estudio preclínico). Simplificación de la cobertura de las horquillas (inicialmente intraluminal expuestas) (1) del conector por el neo-íntima (NI) es visible. La subsección ampliada (ampliación 40X) demuestra el borde láser retraída y remodelado. Entre las horquillas y la banda extravascular, la compresión de la pared arterial se ve sin remodelado adverso (por ejemplo, la erosión, la luxación, o la formación de pseudoaneurisma). Por otra parte, la pared inferior no se ve afectada, sin ninguna reacción de hiperplasia de la íntima (que podrían ser indicativos de [láser] daño), y no hay reacciones de células inflamatorias excesivas se encuentran (que podría ser provocada por el implante de cuerpo extraño). El extremo distal del LITA, el 'callejón sin salida', está lleno de trombo organizado, cubierto por tejido neointimal, la racionalización de la anastomosis (no mostrado). Por último, el resorte del conector está totalmente integrado, extravascularmente, entre el LITA y LAD, sin efectos de la erosión o daño a las paredes arteriales adyacentes (no se muestra). Nota: la interrupción de la pared inferior coronaria es causada por longitudinalmente apertura de la arteria coronaria antes de la inspección. Una barra de escala (1 mm) se proporciona en la esquina inferior izquierda.
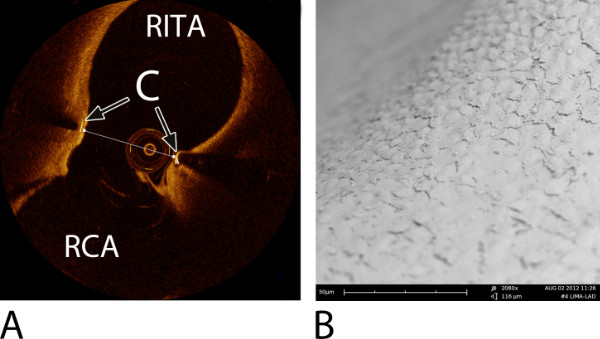
Figura 9: Ejemplo de una imagen intracoronaria tomografía de coherencia óptica (OCT) de una arteria mamaria interna derecha (RITA) -para-arteria coronaria derecha (RCA) anastomosis y un microscopio electrónico de barrido (SEM) de una arteria mamaria interna izquierda (LITA ) -a-arteria descendente anterior izquierda (LAD) anastomosis. Ambos fueron construidos con un predecesor conector coronaria ELANA 6,7. (A) Una imagen octubre a los 6 meses de seguimiento, la sección transversal, a mediados de anastomosis 7. Nota: el cable OCT es visible en el lumen. La línea transversal representa la anchura mínima de la anastomosis (= 2,2 mm). C = conector; RITA = derecha de la arteria torácica interna; RCA = arteria coronaria derecha. (B) Una imagen detallada SEM a nivel del tenedor del conector demostrando una cobertura completa con endotelio (ampliación 2,080X), a los 6 meses de seguimiento 6,7.
Discusión
En este trabajo se describe un nuevo conector coronaria anastomosis, el videoclip Trinidad, y la manera de evaluar un nuevo dispositivo de este tipo en un modelo porcino de bypass sin circulación extracorpórea. Se proponen diferentes técnicas para evaluar la calidad de una anastomosis, facilitado por el nuevo conector o convencionalmente construida: intraoperatorios, postoperatorios, y técnicas de post-mortem. Evaluación de la calidad y la seguridad de la anastomosis facilitado -, así como el proceso de curación y remodelación - en el corto y largo plazo, es de suma importancia antes de la aplicación clínica futura del conector de la anastomosis coronaria.
Actualmente, sólo el 1 conector de la anastomosis coronaria se utiliza clínicamente 17,18, varios otros dispositivos demostraron resultados experimentales o clínicos desfavorables, o desarrolladores no lograron comercializar el producto 19-21. En comparación con otros métodos para facilitar la anastomosis coronaria, el clip de Trinidad incluye varios interecaracterísticas Sting. En primer lugar, debido a la conexión no oclusiva de las paredes de los vasos, acondicionado coronaria (es decir, atrapar o derivación) es redundante, lo que permite la construcción de la anastomosis en un campo sin sangre y sin una restricción de tiempo, y por lo tanto, la reducción de la manipulación de la arteria coronaria. En segundo lugar, la construcción es relativamente sencilla y directa, ni de una incisión separada en la arteria coronaria ni la colocación de puntos de sutura adicionales para obtener la hemostasia son necesarios. En tercer lugar, el conector es un dispositivo de bajo perfil, sin un sistema de dispositivo de despliegue voluminosos; por lo tanto, no va a obstaculizar la construcción de bypass de difícil acceso o áreas remotas del corazón, y, así, potencialmente ampliará las posibilidades de revascularización a través de abordajes mínimamente invasivos.
Preguntas importantes sobre el comportamiento biológico de la anastomosis facilitado todavía sin respuesta. ¿Cuáles son los efectos de láser perforando la arteriotomía en tanto el ITA y la DA?Podría la superficie no expuesta de la íntima de sangre (es decir, el material de las horquillas y la medial y el borde de la adventicia láser), en relación con el objetivo de dimensión pequeña coronaria, ser una limitación potencial de la formación de hiperplasia de la íntima excesiva en el largo plazo? Para responder a estas preguntas, un estudio preclínico, utilizando el modelo porcino como se describe en este documento, se evaluará la permeabilidad a largo plazo y, además, la sanidad y los efectos de remodelación en cuanto la formación de hiperplasia de la íntima, con la consiguiente reducción potencial de la anastomosis. Además, en este estudio preclínico, la permeabilidad, la curación y la remodelación de la anastomosis facilitado serán comparados con el control, la mano-suturado convencionalmente, anastomosis. El modelo porcino es adecuado para estas preguntas de investigación debido a su parecido a la fisiología humana y la anatomía de las arterias coronarias del corazón y, y su expedita respuesta de curación (por ejemplo, la formación de hiperplasia de la íntima), en la que A 6 meses de seguimiento duración en el modelo porcino es comparable a 1,5-3 años de seguimiento de la arteria coronaria humana stent 22. Sin embargo, las arterias del cerdo joven y saludable no están enfermos y compatible, y por lo tanto diferentes a los vasos enfermos humanos encontrados en la práctica quirúrgica cardio-torácica. Por lo tanto, antes de la introducción clínica, la viabilidad y la seguridad del conector se evaluaron también en un modelo de cadáver aterosclerótica humana. Por otra parte, una tendencia a la hipercoagulabilidad se encuentra en cerdos 23. Por lo tanto, para evaluar la anastomosis facilitadas en las pequeñas arterias coronarias calibre, el modelo porcino es todo un reto. Para este momento, el protocolo descrito en este tratamiento antiplaquetario (75 mg de clopidogrel y 320 mg de ácido acetilsalicílico) está justificada. Además, el régimen antiplaquetario es en previsión de la superficie expuesta nonintimal sangre de la anastomosis (BENIS). En nuestro estudio anterior, hemos demostrado que la superficie nonintimal anastomosis de un coron predecesorconector ary completamente endotelizado después de 10 días 6,7. El papel de la terapia antiplaquetaria en clínicas, utilizando este conector, debe basarse en la tasa de endotelialización. Una vez que la superficie nonintimal se endotelizado, el régimen antiplaquetario puede ser bajado.
El láser excimer es un láser de contacto y sólo éxito láser-punch la pared del vaso en el caso de que haya contacto con láser-tejido circunferencial directa completa. El paso más crítico en la construcción anastomosis, por lo tanto, es la posición correcta del catéter de láser sobre la pared del vaso del injerto y la arteria coronaria. Este paso tiene que ser entrenado en la ex vivo modelos de cadáver (por ejemplo, corazón de cerdo) para minimizar la curva de aprendizaje. Escenarios posibles que se traducirá en un fracaso recuperación solapa del láser, y que deben tenerse en cuenta, se describe a continuación: 1) El conector de la anastomosis coronaria está diseñado para conectar el injerto a la arteria coronaria, y secondly, para servir como una plataforma láser. El conector presenta las paredes de los vasos (es decir, una superficie de tejido recta, sin protuberancias) y permite una posición perpendicular del catéter en la pared del vaso. Si el conector está-mal posicionado (por ejemplo, la inserción incompleta, Back o pared lateral de captura, el posicionamiento intramural o -adventitial), la presentación pared del vaso es subóptima (es decir, no hay superficie recta). Por lo tanto, en el caso de una posición mal, uno debe siempre colocar el conector antes hasta el punto de no retorno (es decir, la arteriotomía). 2) El clip de fijación está diseñado para mantener el catéter láser perpendicular en el conector durante la construcción. Sin embargo, el clip de fijación no está diseñada para resistir un montón de fuerza contra, por lo que el cirujano tiene que soportar el catéter láser durante la construcción. Si no se admiten suficientemente, el catéter puede dislocar. 3) Para garantizar un contacto óptimo con láser de tejido, la pared coronaria tiene que ser diseccionado libre operi-adventicia f sueltos tejido, hacia la pared lateral. Asegúrese de que la superficie con láser consiste sólo en la pared coronaria, de su íntima hasta su adventicia, y no el tejido peri-adventicia es capturado en el conector.
Si por desgracia, la construcción de la anastomosis falla, se debe retraer el clip (por apertura del tenedor inferior solamente) y luego cierre la lesión coronaria (± 2 mm de longitud) con suturas de reparación (8-0 prolene). Los cerdos son generalmente muy sensibles al estrés isquémico. Por lo tanto, se recomienda el precondicionamiento isquémico antes de la oclusión de la coronaria para reparar el defecto. Posteriormente, una nueva anastomosis puede construirse distal a la primera puerta. El injerto todavía está montado por el tenedor superior del conector. Así que después de catéter re-posicionamiento y fijación, el conector puede ser insertado directamente en la arteria coronaria.
Las técnicas de evaluación más importantes anastomosis son la angiografía coronaria (s oro clínicatandard) e histología (estándar de oro experimental, combinado con la angiografía coronaria). Sin embargo, la evaluación intraoperatoria de la calidad de la anastomosis por mediciones de flujo de tiempo de tránsito (TTFM) es muy informativo. TTFM es rápido, y en tiempo real no invasiva y fácil, y por otra parte, la interpretación correcta puede reducir el número de errores técnicos, no visible, 11,12,24-26. Las modernas consolas TTFM calculan automáticamente y se muestran en tiempo real el flujo medio, la curva de flujo, y el índice de pulsatilidad (IP), y muchos otros parámetros. El PI se calcula por (max-min de flujo de flujo) de flujo / media y es un indicador de la calidad de la anastomosis, mientras que el flujo medio por sí sola no es un indicador fiable. Un flujo de baja media (<15 ml / min) con una buena PI (<5) y una buena curva de flujo diastólico se puede encontrar una anastomosis perfecta en un pequeño objetivo coronaria con una segunda vuelta moderado, mientras que un buen flujo medio ( > 15 ml / min) con un patrón de llenado diastólico anormal y un altoPI (> 5) es sugestiva de una imperfección de la anastomosis o un fracaso del injerto (es decir, torsión, compresión o retorcimiento del injerto). En este caso, se debe considerar la revisión de la anastomosis. Por lo tanto, una buena evaluación de la calidad de la anastomosis debe incluir la interpretación de la curva de flujo, el índice de pulsatilidad, y el flujo media, combinada con el estado clínico. Sin embargo, la especificidad y la sensibilidad informado de TTFM no son uniformes, y, por lo tanto, la precisión diagnóstica es objeto de debate. Además, el valor de corte de la PI es empíricamente determinado sobre la base de la experiencia clínica en lugar de los estudios clínicos. La consola TTFM utilizamos actualmente en el estudio preclínico con animales dispone de imágenes de ultrasonido epicárdico. Si todavía hay incertidumbre en cuanto a la calidad de la anastomosis después de las mediciones de flujo, una imagen en tiempo real de ultrasonido epicárdico puede ser de gran ayuda en la evaluación adicional de la anastomosis, por la presente el aumento de la una de diagnósticoP recisi ó 27-31.
Una alternativa experimental para las mediciones TTF es la respuesta hiperémica del flujo pico 32, es decir, la reserva de flujo coronario, que es la relación del flujo hiperémica pico, después de 30 segundos-oclusión del injerto, y el flujo base. La respuesta del flujo hiperémico pico debe ser> 4 para una anastomosis distal. Si la anastomosis está dirigido proximal en la arteria coronaria, la respuesta del flujo hiperémico máximo puede ser ligeramente inferior y debe ser> 3 6. Una respuesta hiperémica flujo ausente es sugerente para un error de anastomosis técnico o un fallo del injerto. En ese caso, consulte a las mediciones TTF y el estado clínico, y considerar la revisión de la anastomosis. Tenga en cuenta que el flujo de reserva absoluta varía con la presión arterial (por lo tanto, siempre hay que medir a la misma presión arterial media, por duplicado) y que el precondicionamiento isquémico puede influir negativamente en la respuesta del flujo en hiperemia máxima. Por otra parte, el hypere picorespuesta del flujo de micrófono no es un método validado y un valor de corte absoluta no se ha definido. Hemos seleccionado empíricamente la corte sobre la base de nuestra experiencia experimental.
Finalmente, la técnica de anastomosis descrito en este protocolo es una técnica anastomótica experimental con el objetivo y el potencial para ser aplicado en el ajuste mínimamente invasiva clínica. En la actualidad, los materiales para la aplicación de la técnica se muestra en este documento no son productos finalizados o listos para el mercado, sino más bien instrumentos de prototipo. Todavía hay una ventana de mejora (por ejemplo, aplicador versátil y el catéter de láser flexible), que se llena en pronto. Esta nueva tecnología tiene un potencial interesante, y será evaluado a fondo en un estudio preclínico mediante el uso de este protocolo.
Divulgaciones
The authors declare that they have no competing financial interests. C.A.F. Tulleken holds shares in AMJ b.v., Utrecht, The Netherlands. D. Stecher, G. Bronkers, J.O.T. Noest, C.A.F. Tulleken, and M.P. Buijsrogge are registered as co-inventors of patents regarding the ELANA technique, without financial benefits.
Agradecimientos
Este estudio fue apoyado por el Centro Médico Universitario de Utrecht, Vascular Conectar bv, y EuroTransBio, proyecto ELANA Keyhole (ETB110014). Medistim siempre que la consola VeriQ C, y los precios reducidos para las sondas de ultrasonido y de flujo fueron facturados. Reconocemos las contribuciones constructivas de Evelyn Velema, Marlijn Jansen, Joyce Visser, Grace Croft, Martijn van Nieuwburg, Cees Verlaan, Rik Mansvelt Beck, Sander van Thoor, André van Dieren, y sus colegas de la Universidad de Utrecht Centrales Animalario.
Materiales
| Name | Company | Catalog Number | Comments |
| Trinity Clip | Vascular Connect b.v., Utrecht, The Netherlands | Initial Prototype and Proprietary Design | |
| Excimer Laser System CVX-300 | Spectranetics Corp., Colorado Springs, CO | ||
| Oval laser catheter | Vascular Connect b.v., Utrecht, The Netherlands | Initial Prototype and Proprietary Design | |
| Silicon Extension Tube (vacuum tube) | Medela, Baar, Switzerland | ||
| Medela Dominant 50 Pump (vacuum pump) | Medela, Baar, Switzerland | ||
| Fixation clip | Vascular Connect b.v., Utrecht, The Netherlands | Initial Prototype and Proprietary Design | |
| Standard Aneurysm clip applier | Peter Lazic, GmbH, Tuttlingen, Germany | ||
| VasCo applicator | Vascular Connect b.v., Utrecht, The Netherlands | Initial Prototype and Proprietary Design | |
| Microvascular Acland clamp B-3V | S&T Marketing Ltd, Neuhausen,Switzerland | ||
| Aneurysm clip Yasargil-type, curved, 9 mm | Scanlan International, Inc, Saint Paul, Minn | ||
| Weck Hemoclip | Teleflex Medical, Research Triangle Park, NC | ||
| Hemochron Signature Elite | International Technidyne Corporation (ITC), Edison, NJ, USA | ||
| Hemochron Jr. Activated Clotting Time Plus (ACT+) (cartridge) | International Technidyne Corporation (ITC), Edison, NJ, USA | ||
| Arteriotomy shunt | Medtronic, Inc, Minneapolis, Minn | ||
| Octopus Evolution AS (cardiac tissue stabilizer) | Medtronic, Inc, Minneapolis, Minn | ||
| [header] | |||
| VeriQ C (TTFM and epicardial ultrasound) | Medi-Stim ASA, Oslo, Norway | ||
| Allura Xper FD20 | Philips, Eindhoven, the Netherlands | ||
| Combowire | Volcano Corporation, San Diego, CA, USA | ||
| ComboMap system | Volcano Corporation, San Diego, CA, USA | ||
| C7 Dragonfly (frequency domain optical coherence tomography (OCT) system) | LightLab Imaging, Inc., Westford, MA | ||
| AnalySiS (software package) | Soft-Imaging Software GmbH, Münster, Germany | ||
| Philips XL30LAB (scanning electron microscope) | FEI Europe, Eindhoven, The Netherlands | ||
Referencias
- Halkos, M. E., Puskas, J. D. Off-pump coronary surgery: where do we stand in 2010. Curr Opin Cardiol. 25, 583-588 (2010).
- Lapierre, H., Chan, V., Sohmer, B., Mesana, T. G., Ruel, M. Minimally invasive coronary artery bypass grafting via a small thoracotomy versus off-pump: a case-matched study. Eur J Cardiothorac Surg. 40, 804-810 (2011).
- Blood vessel connectors and methods for blood vessel connection. US patent. , WO2012NL50747 20121026 (2013).
- Van Thoor, A. C. E., Stecher, D., Keizer, D. M. Catheter apparatus and method. US patent. , WO2013NL50142 20130305 (1995).
- Stecher, D., et al. A new nonocclusive laser-assisted coronary anastomotic connector in a rabbit model. J Thorac Cardiovasc Surg. 145, 1124-1129 (2013).
- Stecher, D., et al. The nonocclusive laser-assisted coronary anastomotic connector in an off-pump porcine bypass model. J Thorac Cardiovasc Surg. 147, 1390-1397 (2014).
- Stecher, D., et al. Six-Month Healing of the Nonocclusive Coronary Anastomotic Connector in an Off-Pump Porcine Bypass Model. Innovations (Phila). 9, 130-136 (2014).
- Tulleken, C. A., Verdaasdonk, R. M., Berendsen, W., Mali, W. P. Use of the excimer laser in high-flow bypass surgery of the brain). J Neurosurg. 78, 477-480 (1993).
- Doormaal, T. P., et al. Patency, flow, endothelialization of the sutureless Excimer Laser Assisted Non-occlusive Anastomosis (ELANA) technique in a pig model. J Neurosurg. 115, 1221-1230 (2011).
- Buijsrogge, M. P., Grundeman, P. F., Verlaan, C. W., Borst, C. Unconventional vessel wall apposition in off-pump porcine coronary artery bypass grafting: low versus high graft flow. J Thorac Cardiovasc Surg. 123, 341-347 (2002).
- Walpoth, B. H., et al. Transit-time flow measurement for detection of early graft failure during myocardial revascularization. Ann Thrac Surg. 66, 1097-1100 (1998).
- Ancona, G., Karamanoukian, H. L., Salerno, T. A., Schmid, S., Bergsland, J. Flow measurement in coronary surgery. Heart Surg Forum. 2, 121-124 (1999).
- Lovstakken, L., et al. Blood flow imaging: a new two-dimensional ultrasound modality for enhanced intraoperative visualization of blood flow patterns in coronary anastomoses. J Am Soc Echocardiogr. 21, 969-975 (2008).
- Koudstaal, S., et al. Assessment of coronary microvascular resistance in the chronic infarcted pig heart. J Cell Mol Med. 17, 1128-1135 (2013).
- Agostoni, P., Stella, P. R. Optical coherence tomography: new (near-infrared) light on stent implantation. Heart. 95, 1895-1896 (2009).
- Scheltes, J. S., van Andel, C. J., Pistecky, P. V., Borst, C. Coronary anastomotic devices: blood-exposed non-intimal surface and coronary wall stress. J Thorac Cardiovasc Surg. 126, 191-199 (2003).
- Balkhy, H. H., Wann, L. S., Arnsdorf, S. Early patency evaluation of new distal anastomotic device in internal mammary artery grafts using computed tomography angiography. Innovations. 5, 109-113 (2010).
- Matschke, K. E., et al. The Cardica C-Port System: clinical and angiographic evaluation of a new device for automated, compliant distal anastomoses in coronary artery bypass grafting surgery--a multicenter prospective clinical trial. J Thorac Cardiovasc Surg. 130, 1645-1652 (2005).
- Suyker, W. J., et al. Stapled coronary anastomosis with minimal intraluminal artifact: The S2 Anastomotic System in the off-pump porcine model. J Thorac Cardiovasc Surg. 127, 498-503 (2004).
- Carrel, T., et al. Clinical and angiographic results after mechanical connection for distal anastomosis in coronary surgery. J Thorac Cardiovasc Surg. 127, 1632-1640 (2004).
- Filsoufi, F., et al. Automated distal coronary bypass with a novel magnetic coupler (MVP system). J Thorac Cardiovasc Surg. 127, 185-192 (2004).
- Fischell, T. A., Virmani, R. Intracoronary brachytherapy in the porcine model: a different animal. Circulation. 104, 2388-2390 (2001).
- Kostering, H., Mast, W. P., Kaethner, T., Nebendahl, K., Holtz, W. H. Blood coagulation studies in domestic pigs (Hanover breed) and minipigs (Goettingen breed). Lab Anim. 17, 346-349 (1983).
- Ancona, G., et al. Graft revision after transit time flow measurement in off-pump coronary artery bypass grafting. Eur J Cardiothorac Surg. 17, 287-293 (2000).
- Di Giammarco, G., et al. Predictive value of intraoperative transit-time flow measurement for short-term graft patency in coronary surgery. J Thorac Cardiovasc Surg. 132, 468-474 (2006).
- Kieser, T. M., Rose, S., Kowalewski, R., Belenkie, I. Transit-time flow predicts outcomes in coronary artery bypass graft patients: a series of 1000 consecutive arterial grafts. Eur J Cardiothorac Surg. 38, 155-162 (2010).
- Haaverstad, R., et al. Intraoperative color Doppler ultrasound assessment of LIMA-to-LAD anastomoses in off-pump coronary artery bypass grafting. Ann Thorac Surg. 74, 1390-1394 (2002).
- Klein, P., Meijer, R., Eikelaar, J. H., Grundeman, P. F., Borst, C. Epicardial ultrasound in off-pump coronary artery bypass grafting: potential aid in intraoperative coronary diagnostics. Ann Thorac Surg. 73, 809-812 (2002).
- Dessing, T. C., et al. Geometry assessment of coronary artery anastomoses with construction errors by epicardial ultrasound. Eur J Cardiothorac Surg. 26, 257-261 (2004).
- Budde, R. P., Meijer, R., Dessing, T. C., Borst, C., Grundeman, P. F. Detection of construction errors in ex vivo coronary artery anastomoses by 13-MHz epicardial ultrasonography. J Thorac Cardiovasc Surg. 129, 1078-1083 (2005).
- Di Giammarco, G., et al. Intraoperative graft verification in coronary surgery: increased diagnostic accuracy adding high-resolution epicardial ultrasonography to transit-time flow measurement. Eur J Cardiothorac Surg. , (2013).
- Pijls, N. H. J., et al. Coronaire fysiologie en myocardischemie. Cardiologie. 2, 169-170 (2008).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados