Method Article
Chips de microfluídica para dispersión ligera dinámica In Situ mediante difracción de rayos x de cristal y In Situ para la cristalografía Serial
* Estos autores han contribuido por igual
En este artículo
Resumen
Este protocolo describe en detalle cómo fabricar y operar dispositivos de microfluidos para la recogida de datos de difracción de rayos x a temperatura ambiente. Además, describe cómo supervisar la cristalización de proteínas por la dispersión ligera dinámica y obtenidos de cómo procesar y analizar datos de difracción.
Resumen
Este protocolo describe fabricación dispositivos microfluídicos con bajo fondo de rayos x optimizada para goniómetro base de Cristalografía serial blanco fijo. Los dispositivos son con motivos de pegamento epoxy usando litografía blanda y son adecuados para en situ el experimentos de difracción de rayos x a temperatura ambiente. Los pocillos de la muestra son con tapa en ambos lados con ventanas de hoja polimérica polyimide que permiten la recopilación de datos de difracción con bajo fondo de rayos x. Este método de fabricación es poco exigente y de bajo costo. Después de la contratación de una oblea maestro SU-8, todos de fabricación puede completarse fuera de una sala limpia en un entorno de laboratorio de investigación típicos. El protocolo de diseño y fabricación de chip utilizan válvulas capilares a microfluidically dividir una reacción acuosa en nanoliter definido tamaño de gotitas. Este mecanismo de carga evita la pérdida de la muestra de canal muerto-volumen y puede fácilmente realizarse manualmente sin uso de bombas u otros equipos para accionamiento líquido. Describimos cómo aislado nanoliter tamaño de gotas de solución de proteína puede ser monitoreada en situ por luz dinámica dispersión control proteína cristal nucleación y crecimiento. Después de cristales adecuados se cultivan, conjuntos de datos de difracción de rayos x completa pueden recogerse mediante goniómetro base de la cristalografía de rayos x serie en situ fijadas objetivo a temperatura ambiente. El protocolo proporciona secuencias de comandos personalizadas para procesar conjuntos de datos de difracción usando un conjunto de herramientas de software para resolver y refinar la estructura cristalina de la proteína. Este enfoque evita los artefactos posiblemente inducidos durante la criopreservación o cristal manual de experimentos de Cristalografía convencional. Presentar y comparar tres estructuras de la proteína que se resolvieron con pequeños cristales con dimensiones de aproximadamente 10-20 μm en chip. Por cristalización y diffracting en situ, manejo y por lo tanto mecánico se reduce al mínimo los disturbios de frágiles cristales. El protocolo detalla cómo fabricar un chip de microfluidos transparente radiografía personalizado adecuado para en situ serial Cristalografía. Como casi cada cristal puede ser utilizado para la recolección de datos de difracción, estos chips microfluídicos son un método muy eficiente de cristal.
Introducción
Conocer la estructura 3D de una proteína es esencial para entender su funcionalidad. Las estructuras de resolución atómica cerca hasta ahora se obtienen comúnmente por cristalografía de rayos x. Esta técnica expone cristales proteicos a la radiación de rayos x y luego se analizan los patrones de difracción resultante para el refinamiento y la determinación de la estructura. En Cristalografía de rayos x tradicionales, un conjunto de datos de difracción completa se registra de un cristal solo, ideal grande a temperaturas criogénicas. Tales cristales, sin embargo, en su mayoría no son triviales para crecer, e identificar condiciones de criopreservación adecuados puede convertirse en un desafío en sí mismo y a veces también puede provocar desviaciones de la estructura nativa de la proteína del5.
Recientes avances en láser de electrones libres de rayos x (FEL) y beamlines del sincrotrón han permitido resolver estructuras de cristales más pequeños, como nuevas líneas de enfoque micro, haz de rayos x mayor brillantez, y detectores de rayos x mejorados se convirtió hay disponibles6,7. Por lo general, pequeños cristales son fáciles de crecer que grande y defecto cristales gratis8,9. Sin embargo, pequeños cristales sufren de daño de la radiación de rayos x mucho más rápido que grandes cristales. Esto es porque en comparación con un cristal grande, una mayor dosis de rayos x debe ser proyectada en un menor volumen de cristal que difractan de resolución comparable. Por lo tanto, incluso criogénico protección a menudo no es suficiente para grabar un conjunto de datos de difracción completa desde una sola microcrystal.
Para superar este obstáculo, Cristalografía de la serie se ha convertido en el método de elección para recoger y combinar patrones de difracción de muchos microcristales aleatoriamente orientados a obtener un conjunto completo de datos. Radiación se reduce al mínimo daño inducido cristal repartiendo la dosis total de rayos x utilizado para resolver una estructura de las proteínas sobre un gran número de cristales5,10. En un ' difractar antes de destruir ' vil experimento, cada cristal es utilizado para una exposición usando pulsos de rayos x de femto-segundos. Líneas de micro focus en fuentes de sincrotrón de tercera generación a su vez pueden llevar a cabo serial Cristalografía con pocos milisegundos corta rayos x exposiciones11,12,13,14. Sin oscilación de cristal o rotación durante la recolección de datos, sin embargo, las reflexiones de Bragg sólo parciales se pueden grabar y por lo tanto decenas de miles o más patrones de difracción son típicamente necesarios para la determinación de estructura15. Hasta la fecha, un conjunto diverso de métodos de entrega de la muestra se ha desarrollado para la cristalografía serial, como recientemente ha comentado14,16,17,18,19. Entre aquellos, varios objetivo fijo basado en la entrega de la muestra estrategias con éxito fueron combinadas con la rotación del cristal durante exposiciones de rayos x que significativamente menos patrones de difracción pueden proporcionar igualmente conjuntos de datos completos y también consume menos muestra comparada clásica Cristalografía serie experimentos donde son imágenes fijas grabadas7,16,20,21,22,23 , 24.
Presentamos un protocolo para fabricar dispositivos microfluídicos con bajo fondo de rayos x. Los dispositivos son con motivos de pegamento epoxy de 5 minutos utilizando litografía blanda y son convenientes para los experimentos de difracción de rayos x in situ en la temperatura que se benefician de la integración de la preparación de la muestra directamente en la instalación de rayos x, como el caso de estudios de tiempo resuelto que siguen cinética inducida por mezcla18,19. Canales de microfluidos son con tapa en ambos lados con papel de polyimide poliméricos, dando por resultado x-Ray windows con un espesor combinado de cerca de 16 μm que permiten la proyección de imagen de fondo rayos x baja. Todos los materiales utilizados ofrecen buena resistencia solvente. Este método de fabricación es comparable simple y barato. Después de la contratación de una oblea maestro SU-8, todos de fabricación puede completarse fuera de una sala limpia en un entorno de laboratorio de investigación típicos.
En un ejemplo, describimos chips para goniómetro base de Cristalografía serial blanco fijo. En primer lugar, se discuten las consideraciones diseño y fabricación para el uso de válvulas capilares a microfluidically dividir una reacción acuosa en un número seleccionado de nanoliter tamaño de gotitas. Este mecanismo de carga evita la pérdida de la muestra de canal muerto-volumen y dividir fácilmente se puede realizar manualmente sin uso de bombas u otros equipos para accionamiento líquido. Tales nanoliter aislada tamaño de gotas de solución de proteína son monitoreados en situ con dispersión ligera dinámica (DLS) para control proteína cristal nucleación y crecimiento. Previamente se ha demostrado que se pueden realizar mediciones de DLS en dispositivos microfluídicos que consiste en una estructura de polidimetilsiloxano (PDMS) enlazada a un cristal diapositiva25,26. Porque la capa de poliamida tiene una alta transmisión para longitudes de onda más de 550 nm, el enfoque puede ampliarse a las mediciones en las virutas transparentes de rayos x, cuando se utiliza una longitud de onda de láser adecuado27,28. Basándose en los resultados DLS, nucleación inicial puede ser observado y posterior evaporación de la gota puede interrumpirse para obtener cristales de proteínas menos pero más grande.
Después de suficientes cristales se cultivan, conjuntos de datos de difracción de rayos x completa luego se pueden recoger mediante goniómetro base de la cristalografía de rayos x serie en situ fijadas objetivo a temperatura ambiente. Conjuntos de datos de difracción son procesados usando un conjunto de herramientas de software y scripts personalizados para resolver la estructura cristalina de la proteína. Esta técnica evita artefactos inducidas a menudo durante la criopreservación utilizada en experimentos de Cristalografía convencional.
Comparamos tres estructuras objetivo de proteína que se resolvieron con 10-20 μm pequeños cristales cultivados en chip a una resolución mejor y 2 Å. Por cristalización y diffracting en situ, manejo y por lo tanto mecánico se reduce al mínimo los disturbios de frágiles cristales. Este protocolo puede aplicarse para cristales proteicos que difractan a alta resolución y baja resolución (1.7 Å a 3.0 Å). Como casi cada cristal puede ser utilizado para la difracción, se desperdicia poca muestra, haciendo de este un método muy eficiente de cristal.
Este protocolo proporciona a una guía detallada sobre cómo preparar chips de microfluídica transparente radiografía en situ proteína cristalización y difracción recogida de datos. El procedimiento fue cuidadosamente diseñado para beneficiarse de microfluidos precisión sin necesidad de equipos sofisticados en el laboratorio. Además, recopilación de datos en la línea de sincrotrón puede realizarse sin necesidad de un goniómetro especializado o un humidificador para facilitar la reproducción de los resultados por no expertos. La técnica presentada puede aplicarse para serie milisegundo Cristalografía recolección a temperatura ambiente manteniendo el daño de la radiación mínima y sin la introducción de estrés a los cristales después de crecimiento por manipulación cryo-protección o cristal. Por lo tanto, el método descrito es adecuado para cualquier proyecto de cristalización de proteínas.
Protocolo
1. diseño y fabricación de amo de la viruta
- Diseño de máscara
- Esquema canal deseado geometrías utilizando un adecuado programa de dibujo de CAD. Para cada capa de photoresist, preparar una máscara individual. Todos los diseños utilizados en el presente Protocolo se discuten en detalle en la sección de resultados y están disponibles como AutoCad '. DWG' formato en el archivo adicional 1.
Nota: Para la construcción de dispositivos todo-PDMS, la proporción de aspecto de altura a anchura de canal no debe exceder 1:10 para evitar colapso de canal. Láminas de poliamida y epoxi curado son más robustos y en principio deberían permitir también mayores proporciones. Sin embargo, nosotros deliberadamente no excedía el 1:10 ratio, por lo que inicial diseños podría ser el prototipo dispositivos tradicionales de PDMS. - Archivos CAD se traducen en patrones de la película de emulsión. Utilice una resolución nominal de k PPP 64 para permitir características exactas hasta aproximadamente 5 μm tamaño.
Nota: Esto puede hacerse a través de un servicio comercial. Servicios de imágenes pueden preferir diferentes convenios dibujos para optimizar la conversión de archivos para la proyección de imagen de la máscara. Infórmese acerca de las convenciones de dibujos preferidas por adelantado para evitar el laborioso de problemas durante la conversión. Máscaras con características transparentes sobre fondo negro serán patrón de SU8 fotoresistencia características sobre la oblea para producir microcanales PDMS funcional durante el moldeado de la réplica. A su vez, rasgos negros en máscaras de fondo transparente se necesitan para preparar moldes PDMS conveniente para la fabricación de la viruta de la radiografía. Se recomienda ordenar ambas polaridades de máscara para permitir la validación de prototipos y el diseño temprana fabricar dispositivos PDMS antes de traducir el diseño en chips de rayos x.
- Esquema canal deseado geometrías utilizando un adecuado programa de dibujo de CAD. Para cada capa de photoresist, preparar una máscara individual. Todos los diseños utilizados en el presente Protocolo se discuten en detalle en la sección de resultados y están disponibles como AutoCad '. DWG' formato en el archivo adicional 1.
- Fabricación principal SU8
Nota: Este es el único proceso que debe realizarse en una sala limpia. Si no hay equipo de cleanroom crítica, el paso completo puede subcontrata a empresas de servicios de fundición de MEMS que entregan a listo modelados masters de SU8. SU8 de proceso según la instrucción de la hoja de datos. Pasos 1.2.1 a 1.2.4 Resumen general SU8 fabricación principal flujo de trabajo, con los parámetros completados para el diseño de chip de rayos x de tres capas enumeradas en la tabla 1. Una introducción a SU8 de múltiples capas, alineación ha sido publicado previamente29.- Vierta aproximadamente 1 mL de SU8 resistir en la capa de oblea y spin de 3 pulgadas SU8 hasta el espesor deseado utilizando la velocidad adecuada y tiempo tal como se especifica en la tabla 1 (figura 1, paso 1). Pre-cocer la fotoprotección según el grosor de la capa a 65 ° C y 95 ° C durante unos minutos. Realizar el pre-cocer al horno para solidificar SU8 para evitar que se pegue el photomask y para mejorar la adherencia de resistir al sustrato (figura 1, paso 2).
- Exponga la fotoprotección a la luz UV como se especifica en la tabla 1 seguido de un post-exposición-cueza al horno a 95 ° C para completar catalítico la fotoreducción que se inicia durante la exposición (figura 1, paso 3).
- Repita estos pasos para cada capa subsecuente. A continuación, alinee los patrones de la capa subsiguiente con el maestro mediante un alineador de la máscara y el calibrador a Vernier alineación marcas29.
- Lavar todas SU8 resisten mediante el desarrollo de la oblea en acetato de éter metílico de propilenglicol (PGMEA), hasta que el isopropanol enjuague ya no muestra precipitación lechosa (figura 1, paso 4). Seco la oblea con nitrógeno a presión.
Nota: El Isopropanol es un disolvente pobre de SU8 y su precipitación indica residual permanece sin curar.
- Fabricación de molde PDMS
- Colocar un trozo de papel de aluminio (15 × 15 cm) en una placa Petri (10 cm) y el maestro de SU8 sobre el papel de aluminio en la caja Petri para el retiro fácil del maestro después de curar la PDMS.
- Mezcla base de silicona con curado agente (10:1), resultando en un total de 25 g, vigorosamente con una espátula en un tarro o un mezclador mecánico. Una oblea de 3 pulgadas en caja Petri (10 cm) consume unos 25 g de PDMS en una losa de 5 mm de espesor.
- Vierta PDMS premezclado en SU8-master (figura 1, paso 5) a una altura de 4 mm. desecar el PDMS por 5 min para eliminar burbujas de aire hasta que no, o sólo algunas burbujas permanecen en la superficie PDMS.
- Curar el PDMS en una estufa a 70 ° C durante 1 h. Luego corte el PDMS curado con un bisturí y pelar con cuidado el molde PDMS del maestro SU8 (figura 1, paso 6). Corte hasta el maestro para prevenir grietas PDMS durante la peladura.
- Opcional: Preparar rodajas transversales de los moldes PDMS para confirmar que todos SU8-capas en el maestro tengan el espesor deseado (figura 1). Primeras pruebas diseño microfluídico canal pueden realizarse en todos los chips PDMS.
Nota: Una réplica moldeada de PDMS puede ser enlazado directamente a un sustrato de vidrio después de perforar los puertos de acceso (paso 3.3) en el PDMS por activación de plasma2 O utilizando 20 s, 0,4 mbar O2, 50 W, 13.56 MHz. Como se señaló en el punto 1.2., esto requiere enfrente de polaridad de la máscara y la oblea por lo tanto esquema de fabricación de la viruta de la radiografía.
2. fabricación de chips in Situ rayos x
- Diluir ambos precursores de la resina de epoxy en etanol a una concentración final de etanol de 40% en peso. Una masa total de 0,25 g de cada precursor de resina epoxy en etanol es suficiente para un chip de 1 cm2 .
Nota: Esto reduce la viscosidad de la resultante epoxy de 5 minutos para facilitar la mezcla de burbujas de aire y bastidor réplica del molde y para minimizar el espesor de la capa de epoxy curado final. El etanol se evapora a través de los PDMS durante la etapa de curado. - Desgasificar el molde PDMS en un desecador de vacío durante 30 minutos, por lo que puede absorber pequeñas burbujas de aire de la resina de epoxy en la etapa de moldeo.
- Corte la lámina de polyimide a unos 70 × 70 mm y alrededor de un 75 × 50 mm cristal portaobjetos con cinta para obtener una superficie plana y rígida con la cinta en la parte trasera. Plasma Active la hoja con 50 W, 13.56 MHz, 0,4 mbar O2 plasma de 20 s, luego incubar la hoja-corredera completa en una solución acuosa de 1 vol % (3-aminopropil) Isobutiltrimetoxisilano (APTS) o (3-glycidyloxypropyl) Isobutiltrimetoxisilano (GPTS) durante 5 minutos a 20 ° C.
- Mezclar bien ambas soluciones de precursor de epoxy de etanol diluido para asegurar el óptimo comportamiento de curado. Recuperar moldes de PDMS de la cámara de vacío y colocarlos sobre una superficie plana. Entonces rápidamente dispensar una gota de resina mezclada en cada microestructura sobre el molde utilizando una micropipeta (aproximadamente 10 μL 1 cm2 de microestructuras) (figura 1, paso 7a).
- Recuperar el sándwich de papel-slide de polyimide de la solución acuosa de silano (APTS o GTPS). Secar la lámina con aire comprimido o nitrógeno.
- Coloque el sándwich de láminas portaobjeto de polyimide preparado en la resina de epoxy depositado (figura 1, paso 7b). Presione firmemente el portaobjetos de cristal unido a la lámina de polyimide contra el molde PDMS. Coloque una hoja de metal sobre el portaobjetos de vidrio y luego pesos de depósito presionando hasta 1,4 N/cm2 para 1 h, mientras que las curaciones de resina de epoxy a temperatura ambiente.
Nota: Idealmente, no la resina permanece en la hoja en las áreas donde las estructuras en el molde tienen la altura máxima. Corresponden a los pozos de cristalización donde la cristalización ocurre luego.- Opcional: Si precisa moldeado de pequeñas características es crítico, el molde PDMS puede ser reforzado con un marco de aluminio durante el moldeado paso31.
- Retire el portaobjetos de vidrio con la lámina de poliamida y epoxi estampado de peeling del molde de PDMS (paso 8 de lafigura 1 ). Plasma Active el lado estampado epoxy con 50 W, 13.56 MHz, 0,4 mbar O2 plasma de 20 s.
- Después del retiro de la hoja del polyimide de la cámara del plasma, incubar la lámina patrón de epoxy en una solución de % acuosa APTS (GPTS) vol 1 durante 5 minutos a 20 ° C. Asimismo, preparar una segunda hoja de polyimide sin patrón con la complementaria 1 vol % GPTS (o pisos) silano activación. Después de la incubación, seco hoja estructurado y no estructurado con aire a presión.
- Coloque el epoxy lado boca arriba sobre una superficie plana, utilizando la tensión superficial de una gota de agua por debajo como mediador para evitar que se encrespa de la hoja y para asegurar la llanura máxima. Luego colocar la segunda hoja del polyimide activado y ligeramente rayado con el dedo de una esquina al contrario que en enlace y para evitar la formación de burbujas.
3. acceso a puertos para la entrega de fluido
- Preparar 4 mm espesor losas PDMS en una placa de Petri según pasos 1.3.1 a 1.3.3 sin utilizar al maestro SU8. Cortar la losa en bloques PDMS de tamaño adecuado para cubrir todos los puertos de entrada en el chip, sin cubrir los compartimientos individuales de la cristalización de la viruta.
- Plasma Active tanto, bloquear el chip y el PDMS de 50 W, 13.56 MHz, 0,4 mbar O2 plasma de 20 s. Para la vinculación química, luego incubar cada parte en un 1 vol % APTS o GPTS solución acuosa durante 5 minutos a 20 ° C. Secar cada parte con aire presurizado y presiona la losa PDMS en la viruta de hoja.
- Para mejorar la vinculación, coloque el chip en una losa plana de PDMS y cubrirlo con una hoja plástica, seguida de un portaobjetos de vidrio limpio y un bloque de metal. Por último, depositar pesos para presionar hasta 1,4 N/cm2 de sobre 1 h.
- Perfore los orificios de acceso con un punzón de biopsia de 0,75 mm en cada posición donde puertos de entrada y salida están marcados en el diseño de chip y sellar la parte de atrás con cinta. El chip es ahora accesible para cualquier tubería con un diámetro exterior que empareja el diámetro del agujero (como se describe en el paso 4.2).
4. tratamiento superficial
- Preparar un 1:20 dilución de 9 wt % fluoropolímero de acciones en fluoro-solvente para una concentración final de 0,45% en peso. Almacenar las soluciones y diluciones en una nevera en la oscuridad a 4 ° C.
- Carga a la 1:20 dilución de fluoropolímero en una jeringa de 1 mL Luer-lock. Coloque un 27 × 5/8" la aguja a la jeringa y luego un tubo de PTFE a la aguja.
- Conectar la tubería a la salida de la viruta de rayos x e inyecte la solución de trabajo de fluoropolímero preparada en el paso 4.1 hasta que todos los canales están llenos.
- Coloque el chip con el lado plano hacia abajo sobre una placa caliente de 190 º C durante 5 minutos evaporar el solvente todos para depositar el fluoropolímero en una capa de película delgada.
Nota: Al utilizar una nueva geometría, comprobar si los canales se obturado con fluoropolímero durante este proceso de recubrimiento. Si es así, diluir más la solución.
5. proteína preparación
- Pesan la taumatina liofilizadora y disolver en solución amortiguadora listada en la tabla 2 para el volumen adecuado para obtener una concentración final de proteína de 40 mg mL-1.
- Dializan glucosa isomerasa contra el buffer enumerado en la tabla 2 según el protocolo del fabricante.
- Preparar la proteína tiorredoxina como se describió anteriormente por Schubert et. al. 30.
- Verificar las concentraciones de proteína final fotométricamente usando los coeficientes de extinción resumidos en el cuadro 2, calculadas por el programa ProtParam32.
- Preparar todas las soluciones con agua ultrapura y filtrar con un filtro de 0.2 μm.
- Las soluciones de proteínas a 20 ° C durante 15 min a x 16100 g de centrífuga y tomar el sobrenadante para experimentos de cristalización.
6. proteína cristalización en viruta de la radiografía
- Para cristalizar las proteínas en chips de microfluídica, mezclar cantidades iguales de solución de proteína y precipitante. Concentración de proteínas, composición del tampón y composición precipitante se resumen en la tabla 2. Preparar un volumen total de alrededor de 20 μl para llenar un chip de microfluidos.
- Inmediatamente después de mezclar, inyectar la solución en el puerto de entrada de la viruta a través de una jeringa, junto a un 27 × 5/8" aguja y tubo de PTFE con 0,75 mm de diámetro externo (detallado en el paso 4.2).
Nota: El procedimiento de llenado para el diseño de la serie requiere de un cebado previo de la viruta con aceite fluorado, que más fácil se hace el aceite fluorado de carga desde el puerto de salida antes de inyectar la solución de cristalización a través del puerto de entrada. Todos los pasos de carga deben controlarse utilizando un microscopio para controlar la presión de la jeringa aplicada y el caudal correspondiente." - Después de rellena el chip, separar los compartimientos individuales cristalización inyectando aceite fluorado en el puerto de entrada de la viruta. Sellar el chip bloqueando todos los puertos de entrada y salida de la viruta. Esto puede hacerse insertando un clip.
Nota: Debido a los compartimientos de cristalización están llenos por la solución de proteína/precipitado, el aceite fluorado sólo llena el canal de la entrada de la viruta, sin afectar la solución en los compartimientos de la cristalización. - Para imitar la cinética de cristalización de la difusión de vapor, coloque el chip sellado a temperatura ambiente y normal de la atmósfera para permitir que la gota en el compartimiento de cristalización a encogerse por la evaporación del agua a través de la hoja del polyimide.
- Después de cristal formación se observa mediante un microscopio o medidas DLS (paso 7), trasvasar el chip microfluídico completa de la solución precipitante adecuada, para detener la evaporación de los pozos de cristalización hasta la difracción de rayos x se realiza el experimento.
7. dinámica luz dispersión de mediciones en pozos de cristalización en el Chip
Nota: DLS las mediciones se realizaron con una láser de potencia de salida de 100 mW, una longitud de onda de 660 nm y la luz dispersada se detectó en un ángulo de dispersión de 142°. Porque todas las soluciones de muestra investigados eran acuosas el índice de refracción del agua (n = 1.33) fue utilizado en todos los cálculos.
- Lugar la microfluídica de la viruta en el en el soporte de placa de formato SBS del instrumento utilizando el adaptador descrito en el paso 8.1 DLS. Inserte el adaptador en el dispositivo.
- Cuidadosamente ajuste el enfoque de láser dentro de un compartimiento en el chip de microfluidos utilizando el motor x, y, z-etapa. Porque el chip de microfluidos es muy fino, ajustar el nivel de z, aplicando los pasos del pequeño incremento.
Nota: Un ajuste correcto es confirmado por una alta intercepción y una cola lisa de la función de autocorrelación resultante de la medición de DLS. Puede crearse un archivo de calibración para que coincida con la posición de cada cristalización individual en el chip de microfluidos, permitiendo mediciones automatizadas de DLS en varios compartimientos con el tiempo. - Realizar cada medición DLS en 293 K para 30 s y repetir la medición cada 5 min hasta el final del experimento de cristalización.
Nota: Nucleación inicial puede ser seguido por la distribución de radio de las mediciones de DLS en el tiempo y formación cristalina acertado puede en paralelo seguirán el microscopio incorporado del lector de placa DLS.
8. difracción recogida de datos
- Adaptadores para línea Goniómetros
- Imprimir los adaptadores para el goniómetro de la placa para posicionar y rotar las fichas de rayos x durante la recogida de Datos cristalográficos.
- Fabricar los adaptadores para el base goniómetro en una impresora 3D manía-grado usando la configuración por defecto de los parámetros según lo recomendado por el fabricante.
Nota: Los adaptadores fueron diseñados utilizando un sistema CAD 3D y los archivos de coordenadas de los adaptadores se unen en '. STL'-formato de archivo en el suplemento. - Corregir las fichas de rayos x para el adaptador usando cinta de doble cara.
-
Cristalografía de rayos x en situ
- Recopilar datos de difracción con un tamaño de haz de 10 × 5 μm (FWHM de perfil gaussiano) a 296 K. uso de rayos x con una energía de 12.8 keV y un flujo de 2.2 · 1011 fotones · s-1 en el haz atenuado y patrones de difracción de registro utilizando un detector de píxeles Pilatus de 6 M híbrido.
Nota: Los dispositivos microfluídicos que contiene extractos de plantas, cristales de glucosa isomerasa o tiorredoxina se utilizan para en situ radiografía cristalográficos experimentos en línea EMBL P14 de sincrotrón PETRA III. Flujo y tamaño de foco de haz disponible pueden diferir en otras fuentes de rayos x. El número de cristales de proteína expuesta, el número de patrones de difracción de cada cristal, el rango del ángulo de oscilación por la exposición y el tiempo de exposición se resume en la tabla 3. - Proceso de conjuntos de dos patrones de difracción consecutivas individualmente usando el programa XDS33. Utilizar el script de bash "xds.sh" en el suplemento.
- Crear archivos de HKL para cada conjunto de datos de todos los cristales y la escala usando el software XSCALE33. Utilizar el script de bash "xscale.sh" en el suplemento para crear un archivo de entrada para XSCALE.
Nota: Sólo conjuntos de cristales que tienen coeficientes de correlación superior a 90%, lo que indica un alto grado de isomorfismo, deberían ampliarse. El criterio conservador ‹I/σ (I) › (> 2) pueden usarse para determinar la cáscara de resolución más alta. Reemplazo molecular usando el programa MOLREP34 de la suite de CCP435 puede utilizarse para obtener las fases para otro modelo del edificio mediante el uso de las coordenadas 3D de banco de datos de la proteína (PDB), se muestra en la tabla 3. - Perfeccionar todas las estructuras isotópicamente con Refmac535,36 y FOCHA37 para inspección visual del modelo final.
Nota: Las moléculas de solvente deben añadirse automáticamente durante el proceso de refinamiento y necesitan ser verificadas para confirmar posiciones químicamente razonables. Todos los modelos deben ser inspeccionados para identificar a afloramientos de Ramachandran.
- Recopilar datos de difracción con un tamaño de haz de 10 × 5 μm (FWHM de perfil gaussiano) a 296 K. uso de rayos x con una energía de 12.8 keV y un flujo de 2.2 · 1011 fotones · s-1 en el haz atenuado y patrones de difracción de registro utilizando un detector de píxeles Pilatus de 6 M híbrido.
9. datos evaluación
- Daño de la radiación
- Analizar la decadencia del poder de difracción en el tiempo usando un método descrito por Owen et al38. Para ello, calcular la suma total de I/σ(I) (proporcionado por XDS33) de todas las reflexiones indexadas de cada conjunto de datos evaluados de la difracción (patrón de difracción consecutivas 2), para utilizar como valor de referencia. Use el script bash "ISigma.sh" del suplemento.
- Normalizar el poder de difracción de cada conjunto de datos a la potencia media de difracción del primer conjunto de datos.
- Analizar el cambio de los valores de Rmeas en el tiempo tomando los valores de Rmeas de los archivos de Correct.LP de XDS33 (bash script "Rmeas.sh" del suplemento).
- Orientación cristalina
- Determinar los ángulos de Euler para obtener información sobre la distribución de las orientaciones de enrejado cristalino en respeto al sistema de coordenadas de laboratorio. Calcular los ángulos de Euler de la matriz de orientación del XDS en el archivo de salida XPARM39 utilizando el software Matlab. Utilizar el script de bash "rotation_matrix.sh" para extraer la matriz de rotación de cada cristal del archivo XPARM. Utilizar el archivo de salida como entrada en Matlab para calcular los ángulos de Euler utilizando el rotro2eu.m de función de Matlab (fichero complementario).
Nota: Una descripción detallada del cálculo ha sido publicada por Zarrine-Afsar et al40. - Convertir los ángulos de Euler obtenidos de radianes a grados. Grupo los ángulos de Euler obtenidos para todos los planos de rotación tres (xy, xz y zy) en clases de 10° y trazar utilizando el software origen9.
- Determinar los ángulos de Euler para obtener información sobre la distribución de las orientaciones de enrejado cristalino en respeto al sistema de coordenadas de laboratorio. Calcular los ángulos de Euler de la matriz de orientación del XDS en el archivo de salida XPARM39 utilizando el software Matlab. Utilizar el script de bash "rotation_matrix.sh" para extraer la matriz de rotación de cada cristal del archivo XPARM. Utilizar el archivo de salida como entrada en Matlab para calcular los ángulos de Euler utilizando el rotro2eu.m de función de Matlab (fichero complementario).
Resultados
Epoxy es un material de relleno excelente para la fabricación de la viruta de la radiografía. Es barata, sencilla y robusta al proceso sin necesidad de herramientas especializadas (figura 1). Reducción de viscosidad de epoxy diluyendo con 40 wt % de etanol facilita la eliminación del exceso de resina sobre el pozo de la cristalización, dando por resultado definido x-Ray windows. Diluciones de etanol superiores dio lugar a defectos en la resina curada. Mediante el análisis de cortes transversales de viruta de la radiografía, se determinó el espesor total de la ventana de ambos lados que unos 19 μm de espesor, que está muy cerca el espesor nominal de las láminas de poliimida usado de 2 × 7.5 μm (figura 2)
Ensayos de cristalización fueron aislados en varios nanoliter tamaño reacción compartimentos cada uno, utilizando un mecanismo capilar válvula como se describe anteriormente41. Esta técnica de 'store-entonces-crear' carga evita la pérdida de la muestra de canal muerto-volumen y fácilmente se puede realizar manualmente, eliminando la necesidad de utilizar bombas u otro equipo de impulsión de fluidos42. El chip es imprimar con aceite fluorado antes de cargar la muestra acuosa. La tensión superficial en la interfase aceite-agua entre aceite de cebado y los resultados de la muestra acuosa en una diferencia de presión a través de la interfaz. Esta presión de Laplace depende del radio de curvatura y la tensión superficial de la interfaz. Para reducir al mínimo su energía, la interfaz debe minimizar su superficie, que es equivalente a maximizar sus radios principales de curvatura en el volumen constante. Una interfaz de baja curvatura en un canal de ancho tiene una menor presión de Laplace entonces una interfaz de alta curvatura en un segmento de canal estrecho. Por lo tanto, la toma de muestra preferencial entra y atraviesa el ancho Puente canal en lugar de fluir a través de las restricciones de válvula capilar estrecho. Por último, la toma de muestra es seguida por aceite fluorado para separar los pocillos de la muestra en gotas independientes.
Carga robusta y fiable se logró con caudales de hasta 1 mL/h en una serie y un arreglo bien paralelo (figura 3). En el diseño 'serial', bien entrada y capilares constricción de la válvula está conectados secuencialmente a través de un puente canal31. En contraste, en el diseño 'paralelo', dos canales principales separados conectan todas las entradas bien o capilar válvulas sólo43. Anteriormente ya se habían combinados ambos conceptos de acuerdo con el control de la formulación a la composición de la pantalla, que es un aspecto útil en la cristalización de la proteína43,44. El diseño de la serie tiene sólo dos puertos fluidos, una entrada y una salida. Tiene menos puertos líquidos y debido a esto, es más sencillo de construir y operar. El diseño paralelo tiene 4 puertos de fluido, 2 para el canal principal que conecta los pozos y 2 para ligarse encima de las válvulas capilares para dejar aire o escape de exceso de aceite. Carga por lo tanto puede proceder de ambos lados del canal principal. Este diseño en general tiene menor resistencia al flujo para igual número de pozos debido a su puente más corto. Por lo tanto es más adecuado para dispositivos a escala con un alto número de pozos. Además, los pozos de muestra son orientados más cerca juntos, que ofrece ventajas para el automatizado de la proyección de imagen.
Muestra completa carga bien se observó para ambos diseños, si bien construido como una altura de dos o un diseño de tres altura. En un diseño de dos alturas, la muestra bien y los canales de derivación son de igual altura. El diseño de tres altura requiere una tercera máscara, canales de derivación de una capa adicional de SU8 y un paso de alineación para asegurar que los pozos de muestra ser mayores que la anterior. Esta diferencia de altura promueve la entrada de líquido de la muestra en el pozo a través del mismo tubo capilar válvula principio que detiene el flujo en las limitaciones. Aquí, el techo más bien corresponde a una baja presión de Laplace del menisco y flujo a lo largo de la dirección de puente avance sólo es favorecida después de pozos han llenado completamente las limitaciones de la válvula bloquean flujo y desviación por la carretera de circunvalación. Sin embargo, carga exitoso no requiere estrictamente los pozos a ser mayor que el by-pass válvula capilar adecuado puede lograrse también mediante el ajuste de anchos de canal por consiguiente. Sin embargo, en nuestra experiencia, los pozos más altos realizaron significativamente más robusto y carga libre de defecto se observó en hasta diez veces mayores tasas de flujo en todos los diseños de tres altura en comparación con sus equivalentes de dos alturas. Este efecto fue más pronunciado en el diseño paralelo.
Para imitar la cinética de cristalización de la difusión de vapor, la permeabilidad finita de la hoja del polyimide fue explotada para controlar la evaporación del agua con el tiempo. Tasas de evaporación experimental fueron cuantificadas mediante el control del cambio de volumen de gota con el tiempo al equiparar el área superficial de la gota y bien de altura (figura 4). La evaporación de los pozos de la cristalización en la viruta de la radiografía no procede de manera lineal, como una superficie que encoge de la gota coincidiendo con el aumento de resultados de la concentración de solutos en una tasa de evaporación reducida en tiempo45. La evaporación inicial siguió un ritmo aproximadamente lineal de alrededor de 0,5 nL h-1 en los pozos de la geometría de la composición serial.
Para entender mejor la cinética de cristalización, DLS fueron mediciones en los pozos de la cristalización del chip microfluídico. Para la medición inicial de DLS, un chip PDMS en una diapositiva de cristal se utilizó para proporcionar mejores propiedades ópticas para el experimento de dispersión de la luz. Este chip tenía las mismas dimensiones así como la viruta de la radiografía. PDMS tiene una mayor permeabilidad de vapor de agua que la poliamida de las ventanas de polyimide en los rayos x chip45. Puesto que las escalas de flujo linealmente con la distancia, la trayectoria de evaporación de un polyimide ventana bien puede combinarse con una ventana correspondiente de PDMS de espesor apropiado.
DLS los resultados muestran que la distribución de la radio cambia con el tiempo (Figura 4A-B), demostrando que las medidas DLS permiten para detectar la nucleación inicial antes de que se observan partículas cristalinas primera. Esta información puede utilizarse para nuclear y crecer monocristales por pozo externamente ajustando la tasa de evaporación y por lo tanto niveles de sobresaturación en una etapa temprana de la nucleación46.
La viruta de la radiografía se fijó en un adaptador 3D impreso para el goniómetro de placa compatible de SBS en la línea de EMBL de sincrotrón P14 en PETRA III (figura 5A). Alternativamente, un marco impreso 3D más pequeños puede utilizarse para chips de montaje radiografía estándar línea Goniómetros21. La taumatina cristales tienen un tamaño de 10-20 μm (figura 5B) y difractan hasta una resolución de 2.0 Å (figura 5). Como era de esperar, la contribución del fondo de rayos x de las dos ventanas de láminas de poliimida fino de la viruta de la radiografía se limita a anillos de dispersión de polímero de poliamida 11 Å (2θ = ~ 5°) y 33 Å (2θ = ~ 1,7 °) para la longitud de onda rayos x 0.97 Å. Estos dos anillos no molestan procesamiento de datos. Se recolectó un conjunto de datos total 83 cristales de extractos de plantas y 10 patrones de difracción fueron registrados de cada cristal con una rotación de 1° en cada fotograma. Procesamiento de datos y parámetros de refinamiento, así como las estadísticas de la base de datos de extractos de plantas son listadas y comparadas con los dos otros conjuntos de datos de isomerasa de glucosa y tiorredoxina que también fueron recogidos en situ se enumeran en la tabla 3 y Tabla 4.
El decaimiento de la intensidad de la potencia normalizada de la difracción en el tiempo fue investigado por la división del conjunto de datos de extractos de plantas en cinco sub conjuntos de datos (dos patrones de difracción fueron utilizados por subconjunto para mantener conjuntos de datos completos). Como se muestra en la Figura 6B, el poder de difracción comenzó a disminuir después de la primera base de datos de sub y fue inferior al 50% en el cuarto conjunto de sub. Como resultado, los valores Rmeas de los sub conjuntos de datos también están aumentando con el tiempo, lo que indica daño de la radiación de rayos x durante la recolección de datos. Presumimos que los radicales libres generados durante la exposición de la radiografía rápidamente degradan cristales vecinos en el mismo compartimiento de la reacción. Por ejemplo, tales daños de rayos x secundarios fueron que menos pronunciado en un enfoque experimental relacionado, donde los cristales se han distribuido sobre un área significativamente mayor en un sandwich de poliamida21. Para minimizar los daños de rayos x general, sólo un pequeño número de patrones de difracción de un cristal particular debe ser recogido a temperatura ambiente. También, se debe exponer solamente un cristal de proteína solo por compartimiento del chip microfluídico. Sin embargo, todos los modelos de estructura refinados utilizando los conjuntos de datos procesados muestran muy buena estereoquímica y estadística adecuado (tabla 4). Además, todos los mapas de densidad electrónica final fueron de muy buena calidad.
En anteriores enfoques de Cristalografía en chips transparentes de rayos x, la orientación y arreglo de los cristales tenía que ser manipulado deliberadamente para obtener una distribución al azar de cristal orientaciones40 o fue obtenido por movimientos de cristal dentro de la capa de líquido21. Para evaluar la orientación del cristal en los chips de microfluídica transparente radiografía descrito en el presente Protocolo, se determinó la orientación de la célula de unidad de todos los cristales expuestos con respecto al sistema de coordenadas de laboratorio. Para los cristales bipiramidales de taumatina, una ligera preferencia se observó (Figura 7A), mientras que se obtuvo una distribución amplia de cristales de glucosa isomerasa (figura 7B). Razonamos que en la escala de nanómetros, mayoría de los materiales exhibe significativa rugosidad. Por lo tanto, cristales podían espontáneamente nuclear sobre la superficie en significativamente menos orientaciones sesgadas espontáneamente. Un núcleo de cristal puede estar bloqueado en una orientación, sin dejar de crecer al tamaño adecuado sin reorientar con respecto a la normal de la superficie. De hecho, nucleation superficie cristal mediada ha sido una molestia para cristalógrafos tratando de lazo un cristal conectado fuera de la superficie sin dañar el cristal en el proceso. Aquí, podemos utilizar directamente tales cristales para recopilación de datos de difracción. Sin embargo, existen limitaciones específicas del sistema, como la tiorredoxina reveló una fuerte preferencia por ciertas orientaciones en el xy, xz y yz-planos (figura 7). Demuestran los ejemplos demostrados que la distribución de la orientación no solo depende en el ambiente de crecimiento sino también en la forma de cristal. Los cristales de la tiorredoxina han alargado formas que tienden a crecer en la orientación preferida, mientras que los cristales de la taumatina bipiramidal tetragonal o los cristales de isomerasa de glucosa ortorrómbica no muestran este comportamiento. Sin embargo, en todos los casos, incluso con orientaciones recomendado: la gama accesible de rotaciones de cristal resultó en suficientemente buena cobertura del espacio recíproco y datos completos por lo tanto para todos investigado las proteínas. Así, medidas adicionales no tuvieron que ser tomado al seleccionar cristales para la exposición de rayos.

Figura 1 : Esquema de microfluidos fabricación de chips de rayos x. (1) SU-8 se dispensa en un sustrato de silicio y centrifugado recubiertos para obtener el espesor de la capa deseada. (2) fotoprotección está expuesta a la radiación UV a través de una mascarilla. (3) sin exponer photoresist entonces es desarrollado lavando consecutivamente con PGMEA y isopropanol, resultando en (4) un maestro SU-8 para el bastidor más pasos. (5) PDMS está empapada, y (6) después de curado el molde del PDMS, se pela el amo de SU-8. pegamento de epoxi (7a) se dispensa en el molde de PDMS y (7b) una lámina de polyimide activado químicamente a la resina de epoxy. (8) después de curar, se pela la hoja de poliimida con la película de epoxy fina con motivos del molde de PDMS. (9) en un último paso, el dispositivo es con tapa con una segunda hoja de polyimide para rendir una cerrado bajo rayos x fondo microfluídicos la viruta. Haga clic aquí para ver una versión más grande de esta figura.

Figura 2 : Fotografía (izquierda) e imágenes de microscopia de cortes transversales de las fichas del finales. Se muestran un segmento representativo canal (medio) y un pozo de cristalización (derecha) de dos chips separados. Las flechas indican distancias medidas. Todas las dimensiones están en μm. haga clic aquí para ver una versión más grande de esta figura.

Figura 3 : Diseños de esquemas de cristalización bien con [un] paralelo o disposición serial [B], visto desde arriba y de lado, con dimensiones que se indican en μm. Alturas típicas del canal fueron: bypass de 50 μm, 50-60 μm cristalización bien, 5-10 μm capilar válvula, correspondiente bien volúmenes de unos 2,5 nL (diseño en paralelo) y 8 nL (disposición serial). Representante de carga bien del comportamiento se muestra utilizando colorantes alimentarios. El chip fue preparado con 12% en peso de 1H, 1 H, 2H, 2H-perfluoro-1-octanol en FC-43, antes de colorante alimentario fue inyectado en los pozos de almacenamiento. Las flechas blancas indican la dirección del flujo. Imágenes Resumen de mostrar dispositivos cargados todos los pozos cargados defecto carga libre, ilustrando muestra robusta. El diseño paralelo se ilustra como un diseño de tres alturas, con pozos de cristalización más altos que el puente, mientras que la disposición serial es representado como un diseño de dos alturas con pozos y derivación de igual altura. Caudales típicos fueron alrededor de 150 μL/h durante la carga, pero se observó defecto carga libre para caudales de hasta 1 mL/h en un diseño de altura tres. Haga clic aquí para ver una versión más grande de esta figura.

Figura 4 : In situ dispersión de luz dinámica de una cristalización bien con el tiempo. [A] microscópica imagen serie de la cristalización bien. La gota almacenada continua se contrae como vapor de agua se evapora con el tiempo. Primera microcristales de taumatina pueden observarse después de la distribución de radio hidrodinámico de correspondiente de 4 h. [B] de las partículas de la taumatina medido por DLS durante el mismo proceso de cristalización en [A]. La formación de una segunda fracción radio, indicando eventos de nucleación inicial pueden verse después de aproximadamente 1-2 h. [C] volume representativos disminución de dos volúmenes de gota de referencia debido a la pérdida de agua por evaporación con el tiempo. Haga clic aquí para ver una versión más grande de esta figura.

Figura 5 : recopilación de datos en situ difracción. [A] chips de microfluídica individuales están montados por un adaptador 3D impreso (azul) en un goniómetro de placa. [B] taumatina cristales en la microfluídica chip durante la exposición de la radiografía como imagen por el microscopio en línea en línea P14. [C] difracción de cristales de extractos de plantas se registró a una resolución de 2.0 Å, con un insignificante bajo fondo. Haga clic aquí para ver una versión más grande de esta figura.

Figura 6 : Evaluación de los datos de los datos de difracción de cristales de extractos de plantas en el chip de microfluidos, registrado en la temperatura ambiente. [A] densidad electrónica del modelo refinado taumatina usando el marco 1-2 conjunto de datos solamente (contorno azul en 1.5 σ). [B] decaimiento de intensidad de cristales de extractos de plantas en función de la dosis de rayos x. [C] evolución del valor Rmeas en dosis de rayos x. El cuadro de parcelas en [B] y [C] con cuartiles (valores superior 75%, mediana 50%, valores 25% inferior y medio) y bigotes con un 95% intervalos de confianza representan el decaimiento de la intensidad de difracción y Rmeas de todos los cristales expuestos (n = 83). Haga clic aquí para ver una versión más grande de esta figura.
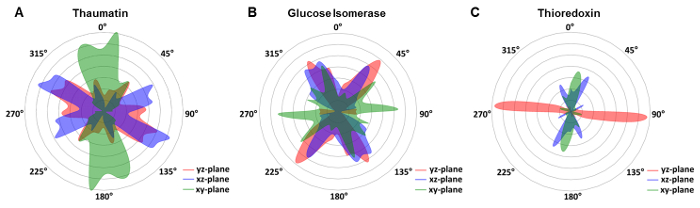
Figura 7 : Distribución de orientaciones de la célula de unidad en el papel de chip de microfluidos con respecto al sistema de coordenadas de laboratorio. [A] los cristales de la taumatina bipiramidal demostraron una amplia distribución de orientaciones que abarca casi 180° en el xy-(azul), con el plano xz (verde) y plano de yz-(red). [B] isomerase de la glucosa también muestra una amplia distribución, mientras que [C] tiorredoxina mostraron una fuerte preferencia para ciertas orientaciones. Haga clic aquí para ver una versión más grande de esta figura.
| Capa de SU8 | Capa de vuelta | Pre-cocer al horno | Exponer | Después de cocer al horno |
| [65 / 95 ° C] | [65 / 95 ° C] | |||
| 1 capa dest : pozos | 1000 RPM | 0 / 10 min | 200 mJ/cm2 | 1 / 4 min |
| 15 μm SU8-3010 | ||||
| capa dend 2: derivación | 2000 RPM | 0 / 16 min | 220 mJ / cm2 | 1 / 5 min |
| 35 μm SU8-3025 | ||||
| 3 capa derd : válvulas | 3000 RPM | 0 / 3 min | 150 mJ / cm2 | 1 / 2 min. |
| 5 μm SU8-3005 |
Tabla 1: ejemplo de proceso de SU8 para diseño de chip de tres capas paralelo rayos x. Este orden capa permitirá un molde PDMS de fundición para la fabricación de la viruta de la radiografía. Para molde directamente un PDMS en prototipos, invertir la capa pedidos durante la fabricación principal a partir de la 3rd terminar con la 1 capa dest en lugar de otro.
| Proteína | Concentración de la proteína | Tampón de proteínas | precipitante | Grupo espacio, entrada PDB | Coeficiente de extinción M-1 cm-1 |
| Taumatina (Thaumatococcus daniellii) | 40 mg mL-1 | mM 50 Bis-Tris, pH 6,5 | 1.1 tartrato de sodio de M, 50 mM Tris, pH 6.8 | I4222, 1LR2 | 29420 |
| Isomerase de la glucosa (Streptomyces rubiginosus) | 25 mg mL-1 | 10 mM HEPES, 1 mM MgCl2, pH 7.0 | 100 mM Bis-Tris, 2.7 M sulfato de amonio, pH 5.7 | I222, 4ZB2 | 46410 |
| Tiorredoxina (Wuchereria bancrofti) | 34 mg mL-1 | 20 mM Tris-HCl, 5 mM EDTA, 150 mM NaCl, pH 8.0 | 27.5% PEG1500, 100 mM de tampón con SPG, pH 6.3 | P41212, 4FYU | 24075 |
Tabla 2: Condiciones de cristalización y grupos del espacio de cristales proteicos dispuestos, incluyendo el código de coeficiente y pdb de extinción.
| Proteína | Número de cristales expuestos | Número del patrón de difracción por cristal | Rango de oscilación por exposición [°] | Tiempo de exposición [ms] | Entrada PDB para Señor |
| Taumatina (Thaumatococcus daniellii) | 103 | 10 | 1 | 40 | 1LR2 |
| Isomerase de la glucosa (Streptomyces rubiginosus) | 69 | 100 | 0.1 | 80 | 4ZB2 |
| Tiorredoxina (Wuchereria bancrofti) | 68 | 10 | 1 | 40 | 4FYU |
Tabla 3: parámetro de colección datos de difracción de rayos x.
| Datos colección estadísticauna | taumatina (Cuadro 1-20) | isomerase de la glucosa (marco de 1-100) | tiorredoxina (Marco de 1-10) |
| Línea de | P14 | ||
| Longitud de onda [Å] | 0.96863 | ||
| Grupo del espacio | P41212 | I222 | P42212 |
| Parámetros de celda unidad: a = b, c [Å] | 58.62, 151.48 | 93.91, 99.60, 103.04 | 58.45, 151.59 |
| Número de cristales | 101 | 41 | 34 |
| Oscilación total [°] | 10 | 10 | 10 |
| Resolución [Å] | 30.1.1989 (1.95 – 1,89) | 30.1.1975 (1.80, 1.75) | 30.3.2000 (3.20-3.00) |
| Temperatura [K] | 296 | 296 | 296 |
| P.i.m.Rb | 7.5 (25.5) | 8.8 (28.0) | 9.1 (33.2) |
| Medida reflexiones | 1553200 | 690000 | 1111196 |
| Reflexiones únicas | 21850 | 48942 | 44449 |
| I/σ(I) promedio | 6.07 (1,78) | 5.85 (1.66) | 4.08 (1.47) |
| MN(I) medio juego correlación CC(1/2) | 96.2 (72.2) | 95.8 (68,2) | 97.9 (75.3) |
| Integridad [%] | 99.8 (100.0) | 100.0 (99.9) | 99.9 (100.0) |
| Redundancia de | 71.1 | 14.1 | 25 |
| Estadísticas de refinamiento | |||
| Rango de resolución [Å] | 30/01/1989 | 30/01/1975 | 30/03/2000 |
| R / Rgratis [%] | 18.8/23.9 | 18.1/20.5 | 18.9/23.1 |
| Átomos de la proteína | 1550 | 3045 | 1129 |
| Moléculas de agua | 51 | 111 | 56° |
| Moléculas de ligando | 20 | 0 | 0 |
| Desviación de RMS | |||
| Longitud de enlace [Å] | 0.02 | 0.026 | 0.01 |
| Ángulo de enlace [°] | 2.04 | 2.22 | 1.43 |
| Factor B [Å2] | |||
| Proteína | 22.6 | 20 | 50 |
| Agua | 25.1 | 27.1 | 29.7 |
| Ligand | 20.4 | ||
| Análisis del diagrama de Ramachandran | |||
| Regiones más favorecidas [%] | 97.67 | 95,32 | 96.13 |
| Regiones permitidas [%] | 2.44 | 4.16 | 3.64 |
| Permitió generosamente regiones [%] | 0.49 | 0,52 | 0.23 |
| a: los valores entre paréntesis son para el shell de resolución más alta. | |||
b: ( ), donde I (hkl) es la intensidad media de la reflexiones hkl, Σhkl es la suma sobre todas las reflexiones y Σi es la suma sobre medidas de reflexión hkl. ), donde I (hkl) es la intensidad media de la reflexiones hkl, Σhkl es la suma sobre todas las reflexiones y Σi es la suma sobre medidas de reflexión hkl. | |||
Tabla 4: Estadísticas de colección de datos de conjuntos de datos de extractos de plantas, isomerase de la glucosa y tiorredoxina.
Archivo adicional 1: chip_geometry.dwg. Archivo CAD de las geometrías del chip utilizado. Haga clic aquí para descargar este archivo.
Archivo adicional 2: goniometer_adapter.stl. Especifica el adaptador de goniómetro de rayos x chip de fichero STL. Haga clic aquí para descargar este archivo.
Archivo adicional 3: xds.sh. Bash script para la creación de archivos de entrada para procesar cuñas de datos de difracción por XDS. Haga clic aquí para descargar este archivo.
Archivo adicional 4: xscale.sh. Bash script para fusionar datos de difracción de subconjuntos y crear un archivo HKL. Haga clic aquí para descargar este archivo.
Adicional-archivo 5: ISigma.sh. Bash script para extraer los valores de ISigma de todos los subconjuntos individuales. Haga clic aquí para descargar este archivo.
Adicional-archivo 6: Rmeas.sh. Bash script para extraer valores de Rmeas de todos los subconjuntos individuales. Haga clic aquí para descargar este archivo.
7 de archivo adicional: rotation_matrix.sh. Bash script para preparar el archivo de entrada de Matlab calcular los ángulos de Euler de la matriz de rotación. Haga clic aquí para descargar este archivo.
Discusión
Fabricamos dispositivos microfluídicos para difracción de rayos x en situ por resina epoxi como llenar la hoja de material y poliimida como material de la ventana de dibujo. Nuestro procedimiento había optimizado distintos pasos del proceso de fabricación por anterior radiografía chip diseños16,21. Hemos reducido el espesor de la ventana y así el fondo dispersión y también facilitando la fabricación menos pasos de proceso se requiere. en situ cristalización utilizando el protocolo descrito tiene importantes beneficios. Permite la recopilación de datos de difracción a temperatura ambiente y excluye de tal modo la necesidad de protección del crio, que en algunos casos contiene el riesgo de introducir artefactos en la estructura de la proteína. Además, los cristales no están sujetos a estrés físico, porque puede evitar la transferencia de los cristales de su medio ambiente nativo. A través de este procedimiento, los cristales mantienen su alta calidad y no sufren de ningún tratamiento.
En nuestra experiencia, los pasos más críticos dentro del protocolo giran en torno a controlar el proceso de cristalización. Los parámetros para obtener cristales adecuados rayos x con dimensiones adecuadas necesitan ser identificadas empíricamente y no pueden ser tomados directamente de experimentos de difusión de vapor. Utilizando concentraciones idénticas de la proteína y precipitado no siempre produjo cristales en fichas diferentes, o a veces en diferentes pozos en el mismo chip. Esto indica que deben considerarse cuidadosamente, todos los factores que influyen en el crecimiento y la nucleación del cristal como cinética de composición o cristalización de licor madre (a través de la trayectoria de evaporación). Como grandes cristales difractan a mayor resolución, idealmente se cultivan adecuadamente grandes cristales. El proceso de nucleación del cristal y el crecimiento se puede seguir con las mediciones de DLS. Ajuste el enfoque de láser dentro de la ~ 50 μm compartimientos de cristalización fina del chip pueden ser difíciles y requieran cuidadosa alineación manual. Mediante el uso de pozos de más de 100 μm, auto-alineación láser era factible y confiable, tal que varios pozos podrían controlarse a través de planes de adquisición automatizada.
Las fichas de polyimide basado en rayos x producen sólo un bajo fondo y demostrar la idoneidad de estos dispositivos para rutina de recolección de datos de difracción de rayos x mediante la resolución de estructuras de tres proteínas de modelo. La mejor resolución obtenida en chip diferenció, en comparación con las resoluciones previamente alcanzadas, de cristales de proteína significativamente mayores y recogida de datos de rayos x convencional. Esto podría ser debido a varios factores y mayor optimización de condiciones de cristalización puede mejorar aún más la difracción. Fue posible recolectar datos en situ de difracción hasta 1,8 resolución Å aplicar cristal con dimensiones menores a 30 μm. El análisis detallado de datos de difracción de la taumatina proporciona conocimientos sobre el daño de la radiación. Para limitar la extensión del daño de la radiación, se debe exponer solamente un solo cristal por compartimento en el dispositivo de microfluidos, como puede ocurrir la difusión de los radicales y en cristales vecinos. Para mejorar la velocidad de recogida de datos, esto debe ser automatizado en el futuro.
Debido a la morfología del cristal, en algunos casos puede ocurrir una orientación preferida. Esto ocurrió por ejemplo con el dataset de la tiorredoxina, donde los cristales tenían una orientación fuertemente preferida con respecto a las ventanas de la viruta. Hasta aquí, podríamos recoger un conjunto de datos de difracción completa. Si cristales exhiben una orientación preferida en el chip y en particular si el grupo correspondiente del espacio tiene también una simetría bajo, entonces la integridad del conjunto de datos debe ser vigilada durante la colección tal que suficiente caña de patrones de difracción recogidos.
Estudios tiempo-resolved usando estos chips son directamente posibles usando la luz inducida por reacciones con un enfoque de prueba de bomba. La transmisión ligera de aluminio del polyimide para el laser de la bomba necesita ser aclarado y también ópticamente claro polyimide o COC podría ser utilizado. Las geometrías de microfluidos actuales no permiten para substrato mezcla de experimentos después de que los cristales crecen. Sin embargo, esperamos que el descrito rayos x chip fabricación protocolo también sea conveniente para tal mezcla diseños para ambos difracción de rayos x de tiempo resuelto así como dispersión de enfoques19.
Divulgaciones
Los autores no tienen nada que revelar.
Agradecimientos
Este trabajo fue financiado por el fondo de la semilla de muelle PIF-2015-46, el BMBF concede 05K16GUA y 05K12GU3 y el cluster de excelencia "El centro de Hamburgo para ultrarrápida de imágenes, estructura, dinámica y Control de la materia a escala atómica" de la Deutsche Forschungsgemeinschaft (DFG). La obra de autores afiliados con el centro para Free-Electron Laser Science fue financiada por la Asociación de Helmholtz a través de fondos de programa orientado. Los datos de MX del sincrotrón fue recogidos en línea P14 operado por EMBL Hamburgo en el anillo del almacenaje PETRA III (DESY, Hamburgo, Alemania).
Materiales
| Name | Company | Catalog Number | Comments |
| SU-8 3000 Series | MicroChem Corp. | SU-8 3000 | Photoresist |
| PGMEA | Sigma-Aldrich | 484431 | Developer |
| Isopropyl alcohol | Solvent | ||
| Ethanol | Solvent | ||
| Epoxy glue | UHU | Plus Schnellfest 5 min | Epoxy glue |
| PDMS | Dow Corning | Sylgard 184 | Silicone |
| Kapton foil | Dupont/ American Durafilm | HN grade, gauge 30 (7.5 μm) | polyimide foil |
| APTS | Sigma-Aldrich | 440140 | Chemical |
| GPTS | Sigma-Aldrich | 440167 | Chemical |
| Cytop CTX-109AE | Asahi Glass Co. Ltd | Cytop CTX-109AE | Cytop fluoropolymer coating |
| CT-Solv 100E | Asahi Glass Co. Ltd | CT-Solv 100E | Cytop fluoro-solvent |
| HFE-7500 | 3M | Novec 7500 | Fluorinated oil |
| AutoCAD | AutoDesk Inc. | AutoCAD | CAD Software |
| Biopsy Punch | Harris | Uni-core 0.75 mm | |
| Photo mask | JD Photo Data | ||
| 3 inch wafer | University Wafer | Silicon wafer | |
| Mask aligner | SÜSS MicroTec | MJB4 | Mask aligner |
| PDMS mixer | Thinky | ARE-250 | |
| Plasma machine | Diener electronic | Zepto | |
| Thaumatin | Sigma Aldrich | T7638 | Protein |
| Glucose Isomerase | Hamton Research | HR7-102 | Protein |
| Bis-Tris | Sigma Aldrich | B9754 | Chemical |
| Sodium Tartrate | Merck | 106664 | Chemical |
| Tris-HCl | Sigma Aldrich | 10812846001 | Chemical |
| HEPES | Carl Roth | 6763.2 | Chemical |
| Magnesium Chloride | Sigma Aldrich | 208337 | Chemical |
| Ammonium Sulfate | Sigma Aldrich | A4418 | Chemical |
| EDTA | Sigma Aldrich | E6758 | Chemical |
| Sodium Chloride | Sigma Aldrich | 1064060250 | Chemical |
| PEG1500 | Molecular Dimensions | MD2-100-6 | Chemical |
| SPG buffer | Jena Bioscience | CSS-389 | Chemical |
| SpectroLight600 | XtalConcepts | DLS Instrument | |
| Nanodrop | Thermo Scientific | Spectrophotometer | |
| Zentrifuge | Eppendorf | ||
| Ultimaker2 | Ultimaker | 3D printer | |
| Form2 | Formlabs | 3D printer | |
| Amicon Filter | Sartorius Stedim | 0.2 µm filter | |
| Tubing | Adtech Polymer Engineering Ltd | Bioblock/05 | PTFE tubing 0.3 mm Inner Diameter x 0.76 mm Outer Diameter |
| Syringes | BD | 309628 | 1ml Luer-Lock Tip |
| Needle | Terumo Agani Needle | AN*2716R1 | 27Gx5/8" |
Referencias
- Rasmussen, B. F., Stock, A. M., Ringe, D., Petsko, G. A. Crystalline ribonuclease A loses function below the dynamical transition at 220 K. Nature. 357 (6377), 423-424 (1992).
- Tilton, R. F. J. R., Dewan, J. C., Petsko, G. A. Effects of temperature on protein structure and dynamics: X-ray crystallographic studies of the protein ribonuclease-A at nine different temperatures from 98 to 320 K. Biochemistry. 31 (9), 2469-2481 (1992).
- Fraser, J. S., Clarkson, M. W., Degnan, S. C., Erion, R., Kern, D., Alber, T. Hidden alternative structures of proline isomerase essential for catalysis. Nature. 462 (7273), 669-673 (2009).
- Juers, D. H., Matthews, B. W. The role of solvent transport in cryo-annealing of macromolecular crystals. Acta Crystallogr. D. 60 (Pt 3), 412-421 (2004).
- Huang, C. Y., et al. In meso in situ serial X-ray crystallography of soluble and membrane proteins. Acta Crystallogr. D. 71 (Pt 6), 1238-1256 (2015).
- Gati, C., et al. Atomic structure of granulin determined from native nanocrystalline granulovirus using an X-ray free-electron laser. P. Natl. Acad. Sci. USA. 114 (9), 2247-2252 (2017).
- Gati, C., et al. Serial crystallography on in vivo grown microcrystals using synchrotron radiation. IUCrJ. 1 (Pt 2), 87-94 (2014).
- von Dreele, R. B. Multipattern Rietveld refinement of protein powder data. J. Appl. Crystallogr. 40 (1), 133-143 (2007).
- Cherezov, V. Lipidic cubic phase technologies for membrane protein structural studies. Curr. Opin. Struct. Biol. 21 (4), 559-566 (2011).
- Gati, C. Data processing and analysis in serial crystallography at advanced X-ray sources. , Dissertation, Hamburg (2015).
- Stellato, F., et al. Room-temperature macromolecular serial crystallography using synchrotron radiation. IUCrJ. 1 (Pt 4), 204-212 (2014).
- Botha, S., et al. Room-temperature serial crystallography at synchrotron X-ray sources using slowly flowing free-standing high-viscosity microstreams. Acta Crystallogr. D. 71 (Pt 2), 387-397 (2015).
- Nogly, P., et al. Lipidic cubic phase serial millisecond crystallography using synchrotron radiation. IUCrJ. 2 (Pt 2), 168-176 (2015).
- Martin-Garcia, J. M., Conrad, C. E., Coe, J., Roy-Chowdhury, S., Fromme, P. Review: Serial femtosecond crystallography: A revolution in structural biology. Arch. Biochem. Biophys. 602, 32-47 (2016).
- White, T. A., et al. CrystFEL: A software suite for snapshot serial crystallography. J Appl Crystallogr. 45 (2), 335-341 (2012).
- Perry, S. L., et al. A microfluidic approach for protein structure determination at room temperature via on-chip anomalous diffraction. Lab Chip. 13 (16), 3183-3187 (2013).
- Schlichting, I. Serial femtosecond crystallography: the first five years. IUCrJ. 2 (Pt 2), 246-255 (2015).
- Sui, S., Perry, S. L. Microfluidics: From crystallization to serial time-resolved crystallography. Struct. Dynam.-US. 4 (3), (2017).
- Ghazal, A., Lafleur, J. P., Mortensen, K., Kutter, J. P., Arleth, L., Jensen, G. V. Recent advances in X-ray compatible microfluidics for applications in soft materials and life sciences. Lab Chip. 16 (22), 4263-4295 (2016).
- Heymann, M., et al. Room-temperature serial crystallography using a kinetically optimized microfluidic device for protein crystallization and on-chip X-ray diffraction. IUCrJ. 1 (Pt 5), 349-360 (2014).
- Schubert, R., et al. A multicrystal diffraction data-collection approach for studying structural dynamics with millisecond temporal resolution. IUCrJ. 3 (Pt 6), 393-401 (2016).
- Weierstall, U., et al. Lipidic cubic phase injector facilitates membrane protein serial femtosecond crystallography. Nat. Commun. 5, 3309(2014).
- Conrad, C. E., et al. A novel inert crystal delivery medium for serial femtosecond crystallography. IUCrJ. 2 (Pt 4), 421-430 (2015).
- Cohen, A. E., et al. Goniometer-based femtosecond crystallography with X-ray free electron lasers. P. Natl. Acad. Sci. USA. 111 (48), 17122-17127 (2014).
- Erskine, D., YU, P. Y., Freilich, S. C. High-Pressure Visible Spectroscopy of Polyimide Film. J. Polym. Sci. Pol. Lett. 26 (11), 465-468 (1988).
- Tsai, C. -L., Yen, H. -J., Chen, W. -C., Liou, G. -S. Novel solution-processable optically isotropic colorless polyimidothioethers-TiO2 hybrids with tunable refractive index. J. Mater. Chem. 22 (33), 17236-17244 (2012).
- Destremaut, F., Salmon, J. -B., Qi, L., Chapel, J. -P. Microfluidics with on-line dynamic light scattering for size measurements. Lab Chip. 9 (22), 3289-3296 (2009).
- Chastek, T. Q., Iida, K., Amis, E. J., Fasolka, M. J., Beers, K. L. A microfluidic platform for integrated synthesis and dynamic light scattering measurement of block copolymer micelles. Lab Chip. 8 (6), 950-957 (2008).
- Heymann, M., Fraden, S., Kim, D. Multi-Height Precision Alignment With Selectively Developed Alignment Marks. J. Microelectromech. S. 23 (2), 424-427 (2014).
- Schubert, R., et al. Reliably distinguishing protein nanocrystals from amorphous precipitate by means of depolarized dynamic light scattering. J Appl Crystallogr. 48 (5), 1476-1484 (2015).
- Aghvami, S. A., et al. Rapid prototyping of cyclic olefin copolymer (COC) microfluidic devices. Sensor Actuat. B-Chem. 247, 940-949 (2017).
- Walker, J. M. The Proteomics Protocols Handbook. , Humana Press Inc. Totowa, NJ. (2005).
- Kabsch, W. XDS. Acta Crystallogr D. 66 (Pt 2), 125-132 (2010).
- Vagin, A., Teplyakov, A. Molecular replacement with MOLREP. Acta Crystallogr. D. 66 (Pt 1), 22-25 (2010).
- Winn, M. D., et al. Overview of the CCP4 suite and current developments. Acta Crystallogr. D. 67, 235-242 (2011).
- Murshudov, G. N., et al. REFMAC5 for the refinement of macromolecular crystal structures. Acta Crystallogr. D. 67 (Pt 4), 355-367 (2011).
- Emsley, P., Lohkamp, B., Scott, W. G., Cowtan, K. Features and development of Coot. Acta Crystallogr. D. 66 (Pt 4), 486-501 (2010).
- Owen, R. L., et al. Exploiting fast detectors to enter a new dimension in room-temperature crystallography. Acta Crystallogr. D. 70 (Pt 5), 1248-1256 (2014).
- Kabsch, W. Automatic-Indexing of Rotation Diffraction Patterns. J. Appl. Crystallogr. 21, 67-71 (1988).
- Zarrine-Afsar, A., et al. Crystallography on a chip. Acta Crystallogr. D. 68 (Pt 3), 321-323 (2012).
- Boukellal, H., Selimović, S., Jia, Y., Cristobal, G., Fraden, S. Simple, robust storage of drops and fluids in a microfluidic device. Lab Chip. 9 (2), 331-338 (2009).
- Aghvami, S. A., et al. Rapid prototyping of cyclic olefin copolymer (COC) microfluidic devices. Sens. Actuator B Chem. 247, 940-949 (2017).
- Shemesh, J., et al. Stationary nanoliter droplet array with a substrate of choice for single adherent/nonadherent cell incubation and analysis. Proc. Natl. Acad. Sci. USA. 111 (31), 11293-11298 (2014).
- Sun, M., Bithi, S. S., Vanapalli, S. A. Microfluidic static droplet arrays with tuneable gradients in material composition. Lab Chip. 11 (23), 3949-3952 (2011).
- Shim, J. -U., et al. Control and measurement of the phase behavior of aqueous solutions using microfluidics. J. Am. Chem. Soc. 129 (28), 8825-8835 (2007).
- Schubert, R., Meyer, A., Baitan, D., Dierks, K., Perbandt, M., Betzel, C. Real-Time Observation of Protein Dense Liquid Cluster Evolution during Nucleation in Protein Crystallization. Cryst. Growth Des. 17 (6), 3579(2017).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados