Method Article
Funcionalización de compuestos de plata/dióxido de titanio en recubrimientos a base de quitosano y sus rendimientos de conservación de óvulos
* Estos autores han contribuido por igual
En este artículo
Resumen
Para mejorar la estabilidad y la esterilizabilidad de los recubrimientos a base de quitosano y ampliar la aplicación de nanopartículas específicas en la conservación de alimentos, los compuestos de Ag/TiO2 se sintetizan para funcionalizar los recubrimientos de quitosano para la conservación de huevos. La morfología de la cáscara de huevo, la pérdida de peso, la unidad de Haugh y el pH de la albúmina se utilizan para caracterizar el rendimiento de conservación de los recubrimientos.
Resumen
Los huevos son una excelente fuente de proteínas, minerales y vitaminas, que se han consumido popularmente en la dieta diaria en todo el mundo. Sin embargo, los microporos y las microgrietas de las cáscaras de huevo provocan la pérdida de humedad y la fuga deCO2, lo que acelera el deterioro del huevo y la pérdida económica. Para mejorar la estabilidad y la capacidad de esterilización de los materiales de recubrimiento existentes a base de quitosano y para desarrollar nuevos nanocompuestos multifuncionales para la conservación antibacteriana y de huevos, se sintetizan y aplican compuestos de plata/dióxido de titanio (Ag/TiO2) para modificar el quitosano y prolongar la vida útil de los huevos. Las imágenes de microscopio electrónico (SEM) se utilizan para analizar la estructura y morfología de las partículas compuestas y la morfología de las cáscaras de huevo recubiertas. Los rendimientos de conservación de los recubrimientos compuestos se evalúan mediante varios parámetros: pérdida de peso, unidad de Haugh, pH de la albúmina y morfologías de la cáscara de huevo de las muestras. La adopción de compuestos de Ag/TiO2 contribuye a un efecto sinérgico con el quitosano, lo que podría prolongar aún más el período de conservación. Sin embargo, los rendimientos del recubrimiento de quitosano están limitados actualmente por las especies y concentraciones de partículas existentes, lo que requiere optimización en estudios futuros. Los métodos de este estudio examinan nuevos materiales de recubrimiento, que podrían crearse mediante la adición de nanopartículas específicas en el precursor del recubrimiento, para lograr los efectos combinativos de la nanopartícula y el precursor, así como para preparar nuevos recubrimientos multifuncionales en el campo de la conservación de alimentos.
Introducción
Como excelentes y populares fuentes de proteínas, sal inorgánica y vitaminas, los huevos son proveedores populares para la nutrición humana, que se producen y consumen en todo el mundo a gran escala 1,2. Aunque las cáscaras de huevo son barreras protectoras naturales, son demasiado frágiles para mantener su integridad durante el transporte y el almacenamiento de los huevos. El intercambio gaseoso y la penetración microbiana entre la albúmina del huevo y el medio ambiente, que puede ocurrir fácilmente a través de pequeños poros en las cáscaras de huevo, conducirían a la pérdida deCO2, así como al deterioro de la calidad del huevo 3,4. Además, las pequeñas grietas en las cáscaras de huevo aumentarían el riesgo de contaminación microbiana. Por lo tanto, se deben desarrollar urgentemente métodos efectivos de conservación de óvulos para el beneficio económico y la salud humana.
En la actualidad, existen dos tipos de vías para la conservación de óvulos. La primera forma es desactivar los microorganismos de las cáscaras de huevo 5,6,7,8. El proceso de desactivación extiende el período de conservación del huevo al limpiar la superficie de la cáscara del huevo lejos de la erosión de los microorganismos ambientales y la humedad. Por otro lado, recubrir los pequeños poros y grietas de la cáscara del huevo con materiales funcionales específicos también podría servir como un excelente método para evitar la pérdida de vapor de agua y CO2 de la albúmina del huevo, así como para proteger la cáscara del huevo de la destrucción de microorganismos. Al ser sencillos, eficaces y ahorradores de energía, los recubrimientos atraen cada vez más la atención para la conservación de los huevos. Los principios básicos que deben cumplir los materiales de recubrimiento adecuados son la estabilidad química, la permeabilidad efectiva, la amplia disponibilidad y la seguridad confiable. Los materiales de recubrimiento más estudiados son el aceite 9,10, las proteínas11, los biopolímeros3 y el quitosano12.
El quitosano ha sido considerado como un material de recubrimiento popular debido a sus excelentes propiedades de formación de película, actividad antibacterianay seguridad. Se ha demostrado que los cambios fisicoquímicos del huevo y la contaminación microbiana están protegidos por un recubrimiento de quitosano, que ha servido como una forma eficiente para la conservación del huevo. Sin embargo, como polímero hidrófilo con poca barrera al vapor de agua y adsorción de humedad, el quitosano es inestable en un ambiente de alta humedad, lo que limita los efectos de conservación y reduce la vida útil de los huevos hasta cierto punto.
Para superar este problema y promover el rendimiento de conservación del quitosano, se han utilizado nanopartículas específicas como adulterante en recubrimientos a base de quitosano. A partir de ahí, como nano relleno con carácter antibacteriano14, la nanoplata (Ag) se ha dopado con quitosano. La adición de Ag no solo podría mejorar la propiedad de barrera de la película de quitosano, sino también mejorar su efecto antibacteriano, que se ha demostrado que mejora el efecto de conservación del recubrimiento. Sin embargo, la fácil agregación y la estructura simple de las partículas de Ag pueden disminuir la estabilidad y durabilidad de la película de quitosano, que se ha verificado que mejoran mediante el depósito de nanopartículas específicas. El dióxido de titanio (TiO2) es un compuesto de óxido metálico típico con excelentes propiedades como estabilidad química, baja toxicidad y costos razonables. Estas propiedades funcionales confieren alTiO2 un gran potencial en muchos campos de investigación15. Por ejemplo, las partículas deTiO2 podrían servir como aditivos en dispositivos médicos y biomateriales debido a su adhesividad y actividades bactericidas. Sin embargo, la aplicación real de las partículas de TiO2 está limitada en gran medida por su termodinámica inestable y sus tendencias de aglomeración. Por lo tanto, se ha propuesto el dopaje de materiales funcionales específicos en TiO2 para lograr el efecto combinativo de la actividad antibacteriana, la mejora de la dispersabilidad y la termoestabilidad.
En este estudio, se sintetizan compuestos antibacterianos de Ag/TiO2 y se aplican en un recubrimiento de quitosano para la conservación de huevos. Las imágenes SEM se utilizan para analizar la estructura y morfología de las partículas de Ag/TiO2 y las cáscaras de huevo. El rendimiento de conservación del recubrimiento se evalúa y compara por pérdida de peso, unidad de Haugh, pH de albúmina y morfologías de cáscara de huevo. Este estudio demuestra la posibilidad y el potencial de los recubrimientos de quitosano mezclados con nano compuestos en la conservación de alimentos.
Protocolo
1. Síntesis de compuestos nano Ag/TiO2
- Para preparar el sol de nanoplata, combine 100 mL de solución de AgNO3, 100 mL de agente protector y 50 mL de NaBH4 en un rompedor de 500 mL.
- Mezcle ácido acético y ácido metanoico (grado analítico) en una proporción de volumen de 1:1 para obtener 100 mL de solución de ácido complejo como precursor del agente protector. Diluir la solución ácida con agua desionizada (18 MΩ-cm) hasta 500 mL como agente protector.
- Añada la solución de AgNO3 (0,3 mol/L) en el agente protector resultante bajo agitación vigorosa, hasta que los solutos de AgNO3 se dispersen uniformemente en la solución protectora. Añadir 0,4 g de NaBH4 para obtener el Ag sol bien disperso después de hacer reaccionar la mezcla durante 1 h a temperatura ambiente.
PRECAUCIÓN: El tamaño de partícula de la nanoplata se puede ajustar mediante la concentración de agente protector y la velocidad de agitación en el paso 1.1.2.
- Combine el Ag en una solución de etanol de titanato de tetrabutilo (TBOT) bajo agitación y luego agregue 80 mL de catalizador ácido gota a gota.
- Combine 500 μL de ácido bencenosulfónico (BA) y ácido acético glacial (AA) para obtener la solución mezclada (BA y AA en la proporción de volumen de 1:2). Diluir la solución en 100 mL de agua desionizada (18 MΩ•cm) para preparar el catalizador ácido.
- Agregue el Ag sol resultante en la solución predispersa de etanol de titanato de tetrabutilo (TBOT) (2,5 de TBOT en una solución de etanol de 100 mL) y revuelva durante 1 h para obtener el sol mezclado. A continuación, añadir el sol gota a gota en 80 mL de catalizador ácido, y agitar durante 4 h a 70 °C.
- Agitar continuamente la mezcla durante 48 h a temperatura ambiente para producir el compuesto final de Ag/TiO2 .
CATIÓN: La agitación vigorosa puede causar salpicaduras de gotas de solución. Use dispositivos de protección para garantizar la seguridad, como una mascarilla protectora oral-nasal, una bata de laboratorio y guantes. No existe un estándar estricto para la velocidad de rotación en los procedimientos mencionados anteriormente.
2. Preparación del recubrimiento de quitosano
- Disuelva el quitosano en ácido acético al 1% (vol) y agite durante 24 h a 25 °C para preparar la solución de recubrimiento (asegúrese de que la concentración de quitosano sea del 0,5% (peso) en la solución resultante.
- Añadir partículas de Ag/TiO2 a la suspensión por separado (0, 0,5, 1 y 1,5 g de Ag/TiO2 en 50 g de solución de quitosano, respectivamente), para obtener soluciones de 0%, 1%, 2% y 3% (en peso) de Ag/TiO 2-quitosano, denotadas como Ag/TiO2-CS0, Ag/TiO2-CS1, Ag/TiO 2-CS2 y Ag/TiO2-CS3, respectivamente.
PRECAUCIÓN: No existe un estándar estricto para la velocidad de rotación en los procedimientos mencionados anteriormente.
3. Observación con microscopía electrónica de barrido (SEM)
- Cortar la cáscara de huevo experimental en trozos (dimensiones cuadradas de unos 2-3 mm).
- Inmovilice los pedazos de cáscara de huevo en un trozo de metal con un adhesivo conductor (es decir, cinta conductora de carbono de doble cara u otros materiales similares). Utilice guantes durante la preparación de la muestra para evitar cualquier contaminación de la muestra de las manos. Marque la muestra (por ejemplo, con un rasguño en forma de L con un cortador de rotulador de diamante).
- Alternativamente, aplique un recubrimiento pulverizado con material conductor (~ 10 nm de grosor) para evitar los efectos de carga.
- Adquirir al menos tres micrografías SEM de alta resolución (idealmente, un mínimo de cinco) desde una vista superior de la muestra. Asegúrese de que cada imagen muestre un área de al menos 25 μm x 25 μm, con una relación de resolución de 20 μm. Evite tomar imágenes de regiones de superficie con defectos macroscópicos de superficie.
- Utilice los siguientes parámetros SEM: tensión de funcionamiento de 30 kV. La resolución de la segunda imagen electrónica puede alcanzar los 2 nm mediante el uso de un cañón de electrones de emisión de campo en un microscopio electrónico de barrido de alto grado (la densidad de corriente del haz de iones es de aproximadamente 10,5 A / cm2).
- Observe la posición exacta de cada imagen con respecto al marcador en forma de L.
4. Experimentos de conservación de óvulos
NOTA: Los huevos recién puestos son huevos de gallina proporcionados por una granja local en Shenzhen, China.
- Examinar los huevos experimentales excluyendo los huevos con grietas, mácula o arenas en sus superficies para garantizar un proceso experimental de conservación de huevos propicio.
- Divida los huevos recién puestos en cinco grupos con 30 huevos en cada grupo. Diseñe los cuatro grupos recubiertos, que están recubiertos por el quitosano, Ag/TiO 2-quitosano dopado con 0%, 1%, 2% y 3% (wt) como Ag/TiO 2-CS0, Ag/TiO 2-CS1, Ag/TiO2-CS2 y Ag/TiO2-CS3, respectivamente.
- Llevar a cabo el proceso de recubrimiento para sumergir los huevos en diferentes soluciones de recubrimiento durante 5 min y secar a temperatura ambiente durante 24 h. Establezca los huevos lavados con agua (WE) como un experimento de control. Después de los tratamientos mencionados, almacenar los huevos tratados a 25 °C. Tome los cinco huevos marcados para medir la pérdida de peso, la unidad de Haugh, el pH de la albúmina y las morfologías de la cáscara del huevo para evaluar y comparar el rendimiento de la conservación.
- Obtener la pérdida de peso (%) del huevo calculando la diferencia de peso en porcentaje del huevo respecto al primer día. Mida el peso de los huevos de cada grupo cada 5 días.
- Calcule la unidad de Haugh para relacionar el peso del huevo con el espesor de la albúmina (Ecuación 1)12.
HU = 100 log (H-1,7W0,37+7,6) (1)
donde H representa la altura de la albúmina (mm) y W representa el peso del huevo (g).- De acuerdo con el valor de la unidad de Haugh, clasifique los huevos en grado AA, A y B cuando la unidad de Haugh de un huevo esté por encima de 72, entre 71-60 y por debajo de 60, respectivamente (los Estándares de los Estados Unidos para la Calidad de los Huevos de Cáscara Individuales).
- Separe la albúmina de la yema y use un medidor de pH digital para medir los valores de pH de la albúmina.
- Observe las morfologías de las superficies de las cáscaras de huevo utilizando un microscopio electrónico de barrido después de la pulverización catódica de platino de las muestras.
CATIÓN: Las cáscaras de huevo son sustancias quebradizas que no pueden soportar impactos violentos. Por lo tanto, tenga cuidado de evitar dañar las cáscaras de huevo. Además, los procedimientos del paso 4.3.4 son los mismos que los del paso 3.
Resultados
El tamaño de partícula de los compuestos Ag/TiO2 oscila entre 100 y 300 nm, lo que se ve afectado por las condiciones de síntesis (Figura 1).

Figura 1: Imágenes SEM de partículas compuestas de Ag/TiO2 a diferentes relaciones de resolución (500 nm). Haga clic aquí para ver una versión más grande de esta figura.
Las pérdidas de peso de las diferentes muestras de huevos durante el almacenamiento se muestran en la Tabla 1. El aumento continuo de la pérdida de peso se debe al escape de albúmina CO2 y vapor de agua a través de los poros de las cáscaras de huevo, lo que conduce al deterioro de la calidad del huevo. Las pérdidas de peso de los huevos WE son mucho mayores que las de otros grupos, lo que indica la capacidad protectora de los recubrimientos a base de quitosano para la calidad de los huevos. Después del recubrimiento con quitosano, las grietas en la cáscara del huevo disminuyen visiblemente, lo que limita la pérdida deCO2 y vapor de agua.
| Tiempo de almacenamiento (día) | Pérdida de peso (% en peso) | ||||
| NOSOTROS | Ag/TiO 2-CS0 | Ag/TiO 2-CS1 | Ag/TiO 2-CS2 | Ag/TiO 2-CS3 | |
| 6 | 0,78±0,09c | 0,69±0,09c | 0,53±0,12A | 0,49±0,21a,b | 0,48±0,06A |
| 11 | 1,85±0,13b | 1,54±0,18c | 1,34±0,15A | 1.28±0.13a,b | 1,26±0,21 A |
| 16 | 2,53±0,21 mil millones | 2,34±0,27 C | 1,95±0,21b | 1,93±0,35 A | 1,89±0,38A |
| 21 | 4.01±0.25c | 3,63±0,32 mil millones | 3.21±0.09b | 3.18±0.22a | 3.09±0.16a |
| 26 | 4,86±0,34b | 4.18±0.25b | 4,09±0,39b | 4.05±0.29a | 3.98±0.21a,b |
| 31 | 5,62±0,41 A | 5,01±0,51b | 4,76±0,48 A | 4.69±0.17a | 4,58±0,35 A |
| En la misma fila con diferentes letras superíndices son significativamente diferentes. | |||||
Tabla 1: Variación de la pérdida de peso de los diferentes huevos durante el tiempo de almacenamiento.
Además, los recubrimientos de quitosano dopados con partículas de Ag/TiO2 son más eficaces para sellar los poros y formar capas densas, lo que conduce a una pérdida de peso considerablemente inhibida. Cuanto mayor sea la dosis de las partículas de Ag/TiO2 , más fuerte será el efecto del recubrimiento correspondiente para reducir elCO2 y la pérdida de vapor (Figura 2).

Figura 2: Imágenes SEM de las superficies de cáscara de huevo cruda y superficies de cáscara de huevo tratadas con quitosano en los días 0, 11, 16 y 31. (A) las superficies de la cáscara de huevo cruda; (B) superficies de cáscara de huevo tratadas con quitosano. Haga clic aquí para ver una versión más grande de esta figura.
La unidad de Haugh se calcula por los cambios relacionados con la edad de las proteínas blancas, lo que refleja la variación del adelgazamiento de la albúmina, que está estrechamente relacionada con la proteólisis de la proteína y el pH de la albúmina. La disminución más rápida y los valores invariablemente más bajos de la unidad de Haugh en el grupo WE que en los grupos de recubrimiento de quitosano indican la capacidad protectora efectiva del quitosano. Los huevos en los grupos tratados con quitosano mantienen el grado A superior durante 26 días, mientras que el grupo WE se degrada a grado B después del día 6. Los valores de la unidad de Haugh en Ag/TiO 2-CS1 son siempre los más altos entre todos los grupos tratados, lo que indica que: (i) la adición de partículas de Ag/TiO2 contribuye a un efecto sinérgico con el quitosano, que son más eficaces para la estabilización del recubrimiento y el control bacteriano; mientras que (ii) el exceso de partículas de Ag/TiO2 destruiría la estructura estratificada del recubrimiento de quitosano, lo que llevaría a una peor capacidad de conservación. De acuerdo con los resultados de la Tabla 2, el quitosano dopado con partículas de Ag/TiO2 al 1% (pt) exhibe el mejor rendimiento para retrasar el deterioro de las proteínas de albúmina, extendiendo así la vida útil hasta en 30 días.
| Tiempo de almacenamiento (día) | Unidad Haugh | ||||
| NOSOTROS | Ag/TiO 2-CS0 | Ag/TiO 2-CS1 | Ag/TiO 2-CS2 | Ag/TiO 2-CS3 | |
| 6 | 73,23±0,68 C | 80,32±0,59 mil millones | 83.34±0.12a,b | 81.60±1.41a | 77.06±0.35a |
| 11 | 69.86±3.25c | 75,64±1,27 mil millones | 77.18±2.45a,b | 76.05±3.13a,b | 74.32±1.41a |
| 16 | 67.31±2.43b | 73,88±2,06 mil millones | 75.36±1.34a | 75.61±2.15a | 71.53±2.18a |
| 21 | 62.93±5.32c | 71.06±3.88c | 73.20±3.09a | 72.94±3.52a | 69.35±1.34a,b |
| 26 | 58,55±2,89 mil millones | 69.85±1.53c | 71.85±2.39a | 70.34±4.19a,b | 66.21±2.10a |
| 31 | 55.24±3.04a | 65,26±0,51 A | 69.31±3.18a | 68.96±1.17a | 62.64±4.03a |
| En la misma fila con diferentes letras en superíndice son significativamente diferentes | |||||
Tabla 2: Variación de la unidad de Haugh de diferentes huevos durante el tiempo de almacenamiento.
La variación del pH de la albúmina es causada por la evacuación de CO2, lo que conduce a un aumento lento de los valores de pH con el tiempo de almacenamiento. El pH de la albúmina de los huevos WE aumenta bruscamente en 10 días y alcanza hasta 9,5 a los 30 días. La degradación de las proteínas en grasa y peptona conduce a una disminución del pH. Después de ser protegida por un recubrimiento de quitosano, el pH de la albúmina presenta tendencias similares dentro de los 20 días, que se estabilizan en torno a un pH de 8,0-8,2. Después del día 20, los valores de pH de Ag/TiO 2-CS0 y Ag/TiO2-CS1 muestran una ligera fluctuación en torno a pH 8,2 y se estabilizan entre pH 7,5-8,0 para Ag/TiO2-CS2 y Ag/TiO2-CS3. El pH relativamente estable de la albúmina de los grupos tratados en comparación con el grupo WE ilustra la reducción efectiva de la pérdida deCO2 en la albúmina (Figura 3). La adición de la partícula Ag/TiO2 promueve la estabilidad del quitosano, que podría mantener una buena estabilidad hasta los 31 días (Figura 4).
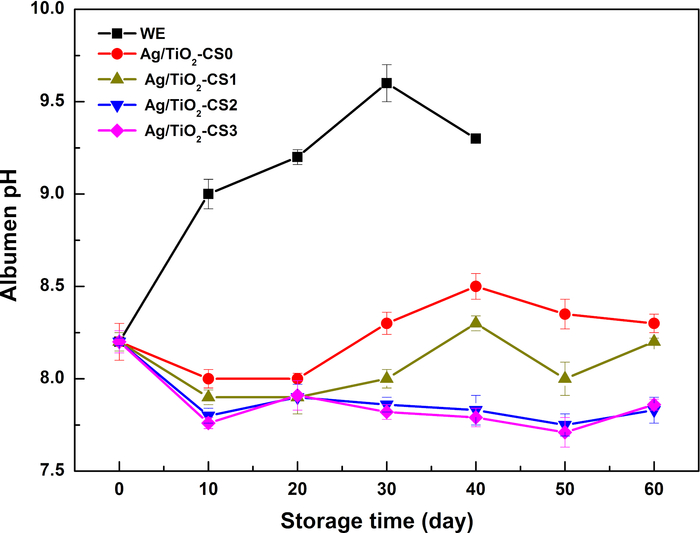
Figura 3: Cambios en el pH de la albúmina de diferentes huevos durante el tiempo de almacenamiento. Haga clic aquí para ver una versión más grande de esta figura.

Figura 4: Imágenes SEM de superficies de cáscara de huevo recubiertas de Ag/TiO2-CS en los días 0, 11, 16 y 31. (A) Ag/TiO 2-CS1; (B) Ag/TiO 2-CS2; (C) Ag/TiO 2-CS3. Haga clic aquí para ver una versión más grande de esta figura.
Discusión
Los problemas de conservación de la calidad de la proteína del huevo podrían aliviarse con el recubrimiento de quitosano, que ha demostrado ser una forma eficaz de prolongar la vida útil del huevo. Sin embargo, el uso de un solo recubrimiento de quitosano crea varios problemas, como la inestabilidad, lo que limita el período de conservación y la aplicación real de recubrimientos a base de quitosano. En particular, se ha propuesto el dopaje de nanopartículas antibacterianas específicas en quitosano para prolongar aún más la vida útil. En este estudio, las partículas de Ag/TiO2 se sintetizan con éxito y se dopan en un recubrimiento de quitosano, lo que podría extender el período de conservación a al menos 30 días.
Las imágenes SEM se utilizan para analizar la estructura y morfología de las partículas Ag/TiO2 , así como la morfología de las cáscaras de huevo recubiertas. Los rendimientos de conservación de los recubrimientos compuestos se evalúan mediante la pérdida de peso, la unidad de Haugh, el pH de la albúmina y las morfologías de la cáscara de huevo de las muestras. La adopción de compuestos de Ag/TiO2 contribuye a un efecto sinérgico con el quitosano, lo que podría prolongar aún más el período de conservación.
Los tamaños de partícula de los compuestos de Ag / TiO2 están en el rango de 100-300 nm (controlados por la condición de síntesis), lo que podría bloquear los poros en la parte superior de la cáscara de huevo y mejorar el rendimiento de conservación. Sin embargo, el exceso de partículas de Ag/TiO2 destruiría la estructura en capas del recubrimiento de quitosano, lo que resultaría en una menor capacidad de conservación.
En la actualidad, los rendimientos del recubrimiento de quitosano en este estudio, sin embargo, están limitados por las especies y concentraciones de partículas existentes, lo que requiere optimización en estudios futuros.
Los métodos de este estudio demuestran nuevos materiales de recubrimiento, que podrían mezclarse con nanopartículas específicas en el precursor del recubrimiento, para lograr efectos combinativos de la nanopartícula y el precursor, así como para preparar nuevos recubrimientos multifuncionales en el campo de la conservación de alimentos.
Divulgaciones
Los autores no tienen nada que revelar.
Agradecimientos
Este trabajo contó con el apoyo del Laboratorio Clave de Guangxi de la Fundación de Ahorro de Energía Nueva Energía y Edificios (No. 19-J-21-17, 19-J-21-30), el Proyecto de Investigación Científica de las Universidades de Guangxi (2020KY06029) y el Fondo Conjunto de Innovación (LZJ2020003) de la Universidad Tecnológica de Wuhan y la Universidad del Tíbet.
Materiales
| Name | Company | Catalog Number | Comments |
| acetate | Aladdin | 64-19-7 | GR, 99.8% |
| Benzenesulfonic acid | Aladdin | 03/11/1998 | 98% |
| Chitosan | Aladdin | 9012-76-4 | <200 mPa•s |
| Deionized water | prepared by ourselves | - | 18 MΩ•cm |
| Electronic precision balance | Sartorius | BSA124S-CW | |
| Ethanol | Aladdin | 64-17-5 | ≥99.8% |
| Formate | Aladdin | 64-18-6 | Standard for GC, >99% |
| pH meter | HeYi | PHS-25 | |
| Scanning electron microscope | Hiatchi | SU8010 | |
| Silver nitrate (AgNO3) | Aladdin | 7761-88-8 | ≥99.9% |
| Sodium borohydride (NaBH4 ) | Aladdin | 16940-66-2 | 98% |
| Temperature humidity chamber | YiHeng | LHS-50CH | |
| Titanium butoxide (TBOT) | Aladdin | 5593-70-4 | CP,98% |
Referencias
- Kuroli, S., Kanoo, T., Itoh, H., Ohkawa, Y. Nondestructive measurement of yolk viscosity in lightly heated chicken shelleggs. Journal of Food Engineering. 205, 18-24 (2017).
- Kostogrys, R. B., et al. Effect of dietary pomegranate seed oil on laying hen performance and physicochemical properties of eggs. Food Chemistry. 221, 1096-1103 (2017).
- Morsy, M. K., Sharoba, A. M., Khalaf, H. H., El-Tanahy, H. H., Cutter, C. N. Efficacy of antimicrobial pullulan-based coating to improve internal quality and shelf-life of chicken eggs during storage. Journal of Food Science. 80, 1066-1074 (2015).
- Damaziak, K., et al. Effect of dietary canthaxanthin and iodine on the production performance and egg quality of laying hens. Journal of Poultry Science. , (2018).
- Sert, D., Aygun, A., Demir, M. K. Effects of ultrasonic treatment and storage temperature on egg quality. Journal of Poultry Science. 90, 869-875 (2011).
- Yaceer, M., Aday, M. S., Caner, C. Ozone treatment of shell eggs to preserve functional quality and enhance shelf life during storage. Journal of the Science of Food and Agriculture. 96, 2755-2763 (2016).
- Viswanathan, K., Priyadharshini, M. L. M., Nirmala, K., Raman, M., Raj, G. D. Bactericidal paper trays doped with silver nanoparticles for egg storing applications. Bulletin of Materials Science. 39, 819-826 (2016).
- Aygun, A., Sert, D. Effects of vacuum packing on eggshell microbial activity and egg quality in table eggs under different storage temperatures. Journal of the Science of Food and Agriculture. 93, 1626-1632 (2013).
- Ryu, K. N., No, H. K., Prinyawiwatkul, W. Internal quality and shelf life of eggs coated with oils from different sources. Journal of Food Science. 76, 325-329 (2011).
- Figueiredo, T. C., et al. Effects of packaging, mineral oil coating, and storage time on biogenic amine levels and internal quality of eggs. Journal of Poultry Science. 93, 3171-3178 (2014).
- Caner, C., Ydceer, M. Efficacy of various protein-based coating on enhancing the shelf life of fresh eggs during storage. Journal of Poultry Science. 94, 1665-1677 (2015).
- Xu, D., Wang, J., Ren, D., Wu, X. Y. Effects of chitosan coating structure and changes during storage on their egg preservation performance. Coatings. 8, 317(2018).
- Kopacic, S., Bauer, W., Walzl, A., Leitner, E., Zankel, A. Alginate and chitosan as a functional barrier for paper-based packaging materials. Coatings. 8, 235(2018).
- Sagnelli, D., et al. Cross-linked amylose bio-plastic:A transgenic-based compostable plastic alternative. International Journal of Molecular Sciences. 18, 2075(2017).
- Megan, T., Robert, C. P., Ivan, P. P., Clara, P. Nanostructured titanium dioxide coatings prepared by aerosol assisted chemical vapour deposition (AACVD). Journal of Phothchemistry and Photobiology A-Chemistry. 400, 112727(2020).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados