Method Article
Un flujo de trabajo para determinar cuantitativamente las variaciones específicas de la lesión de la degeneración macular relacionada con la edad en la autofluorescencia del fondo de ojo
En este artículo
Resumen
Esta investigación describe un flujo de trabajo para determinar y comparar los niveles de autofluorescencia de regiones individuales de interés (p. ej., drusas y depósitos de drusas subretinianas en la degeneración macular relacionada con la edad [DMAE]) al tiempo que se tienen en cuenta los niveles variables de autofluorescencia en todo el fondo de ojo.
Resumen
Las imágenes de autofluorescencia del fondo de ojo (FAF) permiten el mapeo no invasivo de los fluoróforos intrínsecos del fondo ocular, en particular el epitelio pigmentario de la retina (EPR), ahora cuantificable con el advenimiento de la autofluorescencia cuantitativa (QAF) basada en la oftalmoscopia láser de barrido confocal. Se ha demostrado que la FAC está generalmente disminuida en el polo posterior en la degeneración macular asociada a la edad (DMAE). La relación entre la FAQ y diversas lesiones de la DMAE (drusas, depósitos de drusas subretinianas) aún no está clara.
En este artículo se describe un flujo de trabajo para determinar el QAF específico de la lesión en la DMAE. Se utiliza un enfoque de imagen in vivo multimodal, que incluye, entre otros, la tomografía de coherencia óptica de dominio espectral (SD-OCT), la exploración del volumen macular y el QAF. Mediante el uso de plug-ins FIJI personalizados, la imagen QAF correspondiente se alinea con la imagen del infrarrojo cercano de la exploración SD-OCT (puntos de referencia característicos; es decir, bifurcaciones de vasos). La foveola y el borde de la cabeza del nervio óptico se marcan en las imágenes OCT (y se transfieren a la imagen QAF registrada) para un posicionamiento preciso de las cuadrículas de análisis.
Las lesiones específicas de la DMAE se pueden marcar en BScans OCT individuales o en la propia imagen QAF. Los mapas normativos de QAF se crean para tener en cuenta la variación de la media y la desviación estándar de los valores de QAF a lo largo del fondo de ojo (se promediaron imágenes de QAF de un grupo representativo de DMAE para crear mapas de DMAE de QAF estándar estándar de la retina). Los plug-ins registran las coordenadas X e Y, la puntuación z (una medida numérica que describe el valor de QAF en relación con la media de los mapas de AF en términos de desviación estándar de la media), el valor de intensidad media, la desviación estándar y el número de píxeles marcados. Las herramientas también determinan las puntuaciones z de la zona limítrofe de las lesiones marcadas. Este flujo de trabajo y las herramientas de análisis mejorarán la comprensión de la fisiopatología y la interpretación clínica de las imágenes de FA en la DMAE.
Introducción
Las imágenes de autofluorescencia del fondo de ojo (FAF) proporcionan un mapeo no invasivo de los fluoróforos naturales y patológicos del fondo de ojo1. La autofluorescencia (FA) azul (excitación de 488 nm) más común excita los gránulos de lipofuscina y melanolipofuscina del epitelio pigmentario de la retina (EPR)2,3,4. La distribución y el aumento/disminución de los gránulos juegan un papel central en el envejecimiento normal y en diversas enfermedades de la retina, incluida la degeneración macular asociada a la edad (DMAE)5.
Un desarrollo adicional de la FAF, la autofluorescencia cuantitativa del fondo de ojo (QAF), permite ahora la determinación precisa de las intensidades de AF retiniana resueltas topográficamente 4,6. Al incorporar una referencia en la vía óptica del dispositivo de imágenes FAF, las intensidades de AF se pueden comparar entre dispositivos, puntos de tiempo y sujetos. Esta técnica ha supuesto un cambio de paradigma con respecto a un presunto factor patogénico en la DMAE, que durante mucho tiempo se especuló que se debía a una acumulación excesiva de lipofuscina en las células del EPR7. Sin embargo, la cuantificación histológica y clínica de la FA ha revelado una disminución de la FA en la DMAE (debido a la redistribución y pérdida de los gránulos de lipofuscina y melanolipofuscina autofluorescentes), en lugar del aumento propuesto de la FA 8,9,10.
La monitorización de la fibrilación auricular tiene implicaciones clínicas. Von der Emde et al. y otros han demostrado que la FA no solo disminuye, sino que también disminuye aún más en el curso de la DMAE en ojos de alto riesgo e intermedio para la DMAE 8,9. Además, los estudios histológicos sugieren que la mayoría de las células del EPR afectadas por DMAE muestran un comportamiento característico con la agregación y extrusión de gránulos antes de la pérdida de células del EPR por subducción, descamación, migración o atrofia13,14,15,16. Esto indica además que la pérdida de FA podría ser un desencadenante o una señal sustituta de una progresión inminente de la enfermedad.
Hasta el momento, los estudios de QAF solo han evaluado la FA a nivel mundial en el polo posterior, utilizando sistemas de coordenadas polares de cuadrícula prefabricados (por ejemplo, QAF8/Delori Grid)17. El uso de cuadrículas prefabricadas para medir el AF da como resultado múltiples valores de AF en áreas predeterminadas por ojo de un sujeto. Investigar los valores de FA de esta manera podría pasar por alto cambios locales en áreas con FA patológicamente alterada, por ejemplo, en la DMAE encima o cerca de drusas o depósitos de drusas subretinianas (SDD). Las drusas, y en mayor medida los SDD, se asocian con un alto riesgo de desarrollar DMAE tardía y pérdida de la visión. Las drusas, en particular, tienen un ciclo típico de aumento de tamaño a lo largo de muchos años y pueden deteriorarse rápidamente antes de la atrofia. Es concebible que, por ejemplo, la FA global disminuya en la DMAE, pero aumente o se reduzca aún más en y alrededor de estas lesiones focales específicas relacionadas con la enfermedad.
Los diferentes patrones locales de FA también podrían tener relevancia pronóstica para la progresión de la enfermedad. Por ejemplo, los niveles de autofluorescencia podrían usarse para evaluar si las drusas están aumentando de tamaño o si ya están en regresión a la atrofia. Ya se ha demostrado que la alteración de los patrones perilesionales de la FA en la atrofia geográfica tiene un gran impacto en la progresión de la atrofia a lo largo del tiempo18. Además, los patrones de autofluorescencia local podrían revelar más detalles sobre la salud del EPR. A menudo, la tomografía de coherencia óptica (OCT) muestra hiperreflectancia en el coriocapilar, aunque la capa de EPR aparece intacta. Un enfoque multimodal que combine los valores locales de QAF y OCT podría ayudar a diferenciar las lesiones con un alto riesgo de alteración del EPR y atrofia inminente.
Una de las razones por las que no se han realizado análisis espacialmente resueltos en los estudios es porque el software del fabricante más utilizado no proporciona una herramienta para este tipo de análisis. Las propiedades de la FA de diferentes lesiones dependientes del estadio de la enfermedad de DMAE podrían explicar aún más la patogénesis de la DMAE. Por lo tanto, sería deseable contar con una herramienta para medir la FA regional específica de la lesión. Para comparar con precisión las lesiones que se localizan en toda la retina, el flujo de trabajo necesita una forma de tener en cuenta los diferentes grados de FA en el fondo de ojo humano19. A nivel central, la FA es característicamente más baja debido a los efectos de sombreado del pigmento macular y a los diferentes recuentos de gránulos20,21.
La FA alcanza su punto máximo a ~9° (distancia a la fóvea en todas las direcciones) y disminuye en mayor medida periféricamente4. Por lo tanto, si se compararan los valores absolutos de los niveles de FA de las drusas blandas (localizadas en la fóvea y parafóvea en las zonas de baja FA) y las SDD (situadas paracentralmente en las zonas de FA alta), los resultados no serían comparables22. Inspirados en el trabajo de Pfau et al. y en el concepto de pérdida de sensibilidad (corrección de la sensibilidad medida en DMAE para la colina de visión [disminución de la sensibilidad retiniana con la distancia a la fóvea] de controles sanos) para la perimetría controlada por fondo de ojo, la FA se compara con los valores estandarizados de FA a lo largo de la mácula23,24. Los resultados se presentan como puntuaciones z (medición numérica de la relación del valor de una región de interés con la media).
El objetivo de este estudio es evaluar el uso de una nueva herramienta para medir los niveles locales de FAQ en diferentes tipos de lesiones en pacientes con DMAE. Esta herramienta está diseñada para medir los niveles de autofluorescencia de las lesiones identificadas en las OCT. Esto permite la evaluación de los niveles de autofluorescencia local en lesiones, como drusas blandas o SDD, y permite el seguimiento de los cambios en la FA de las lesiones a lo largo del tiempo. La utilidad potencial de esta herramienta es permitir un nuevo biomarcador estructural que estima la salud del EPR y puede tener valor pronóstico para las lesiones investigadas.
Protocolo
El estudio se realizó de acuerdo con la Declaración de Helsinki y fue aprobado por el Comité de Ética de la Universidad de Bonn (código de protocolo 305/21). Se obtuvo el consentimiento informado por escrito de todos los sujetos involucrados en el estudio. Requerimos que todos los participantes en el video firmaran formularios de autorización que nos otorgaran permiso para usar su imagen e información personal en la creación de un video en línea.
1. Adquisición de imágenes de autofluorescencia cuantitativa (QAF)
- Para una adquisición precisa de imágenes con el dispositivo QAF, asegúrese de que el participante esté sentado cómodamente frente al dispositivo. Pida al participante que presione la barbilla y la frente contra la barbilla y el reposacabezas. Ajuste la altura de la mentonera hasta que el ángulo lateral del párpado esté a la misma altura que la marca roja.
- Asegúrese de que la imagen se enfoque en el modo de infrarrojo cercano girando la rueda del dispositivo de grabación hasta que los vasos pequeños estén enfocados. Acérquese al ojo moviendo la cámara hacia adelante hasta que las esquinas de la imagen se iluminen uniformemente. Como regla general, ajuste el enfoque al equivalente esférico. Reduzca el enfoque antes de la obtención de imágenes QAF en una o dos dioptrías, ya que el QAF azul utiliza una longitud de onda más corta, y cambie el modo del dispositivo QAF del modo infrarrojo cercano al modo QAF.
- Vuelva a ajustar y aumentar la iluminación y ajuste el enfoque de la imagen hasta que los pequeños vasos más cercanos a la fóvea estén enfocados y la imagen se ilumine brillantemente sin puntos rojos (lo que indica una sobreiluminación). Decolore el fotopigmento esperando al menos 30 s en el modo QAF antes de la adquisición de la imagen para permitir que la excitación continua de la luz azul blanquee el pigmento fotorreceptor en el campo de visión de la configuración de la cámara.
- Para capturar imágenes, presione adquisición de imágenes en el panel táctil del dispositivo de imágenes ; asegúrese de capturar más de una imagen QAF en caso de parpadeo o movimientos oculares repentinos durante la adquisición.
NOTA: El flujo de trabajo también requiere imágenes de tomografía de coherencia óptica de dominio espectral (SD-OCT). La adquisición de imágenes de OCT se explica en otro lugar, ya que es ampliamente utilizada en la práctica clínica25.
2. Exportación de imágenes
- Para esta canalización de análisis, asegúrese de que las imágenes QAF y OCT estén en el formato de archivo de lenguaje de marcado extensible (XML). En el visor de HEYEX, haga clic con el botón derecho en la imagen QAF/OCT deseada y seleccione Exportar | como XML en el menú desplegable.
3. Plug-ins de código abierto para el análisis QAF: instalación de la canalización
NOTA: El software QAF presentado es un plug-in de código abierto denominado "Spectralis pipeline" creado para el software de código abierto ImageJ (expansión FIJI)26.
- Para acceder al complemento, abra FIJI, seleccione Ayuda y, a continuación, Actualizar en el menú desplegable y, a continuación, haga clic en Administrar sitios de actualización para agregar el sitio de actualización de Creative Computation "https://sites.imagej.net/CreativeComputation/" a los sitios de actualización preexistentes.
- Descargue los plug-ins y, a continuación, reinicie FIJI. Ahora, la canalización Spectralis está instalada. Los diferentes plug-ins de Spectralis se encuentran en el menú desplegable Plugins | Spectralis o Plugins | SpectralisBatch.
4. Configuración: almacenamiento de datos
NOTA: Para permitir un flujo de trabajo fluido, se recomienda configurar la estructura de carpetas de la siguiente manera. Primero, configure una carpeta para cada tema de estudio. Oculus dexter (OD) y oculus sinister (OS) se refieren al ojo derecho e izquierdo, respectivamente, y estas abreviaturas se utilizan en todo este flujo de trabajo.
- Para cada ojo examinado de cada sujeto de estudio, configure una carpeta para un OCT, denominados OD_OCT y OS_OCT, respectivamente. Deje que la canalización de Spectralis almacene automáticamente su salida del complemento "Mark_BScans_OCT" como valores separados por tabulaciones en estas carpetas.
- Para las imágenes QAF, cree dos carpetas denominadas OD_QAF y OS_QAF.
- Cree carpetas adicionales si se utilizan otras modalidades de imágenes multimodales. Asegúrese de que la estructura de carpetas resultante se parezca a la estructura que se indica a continuación:
CASE_ID
OD_OCT
OD_QAF
OD_other_imaging_modality
OS_OCT
OS_QAF
OS_other_imaging_modality
5. Conversión del archivo XML QAF en una imagen QAF (plug-in utilizado: QAF_xml_reader)
- Los archivos de exportación XML de Spectralis QAF se almacenan en formato rojo-verde-azul (RGB), limitados a una escala de 0 a 255 (que representa los valores de AF medidos) e incluyen regiones de calibración "estándar" y "negra". El plug-in "QAF_xml_reader" produce una imagen QAF. Para ello, abra el menú desplegable de complementos , seleccione Spectralis | QAF_XML_Reader y descarte la pantalla de apertura.
- Aparecerá una nueva ventana que muestra el mensaje Elija un directorio que contenga una exportación QAF XML de Spectralis:. Seleccione el directorio y haga clic en Seleccionar.
- Introduzca el factor de calibración de referencia (RCF) del dispositivo QAF (incluido en la información de la imagen QAF) y la edad del paciente en el momento en que se tomó la imagen.
- La siguiente ventana se llama Parámetros QAF. Si el paciente es pseudofáquico en el momento de la adquisición de la imagen, seleccione la edad 20 en su lugar (esto tiene el efecto de no aplicar corrección de edad). Después de hacer clic en Aceptar, cuando aparezca una ventana emergente con la etiqueta Asignar a 8 bits, introduzca el valor mínimo de QAF (qafMin) y el valor máximo de QAF (qafMax) para una imagen QAF codificada por colores. En caso de que qafMin y qafMax sean desconocidos, utilice la configuración predeterminada, haga clic en Aceptar y observe la imagen original etiquetada como Datos QAF sin procesar que aparece, así como la imagen QAF de 32 bits y la imagen QAF codificada por colores de 8 bits.
NOTA: La imagen QAF codificada por colores se utiliza únicamente con fines ilustrativos; la imagen QAF de 32 bits con valores QAF reales se utiliza para un análisis posterior.
6. Registro de imágenes QAF con la imagen OCT (plug-in utilizado: Register_OCT_2)
NOTA: Este paso es necesario para alinear con precisión la imagen OCT con la imagen QAF, de modo que las lesiones en las imágenes QAF y los BScan OCT estén alineadas.
- Accede al plug-in a través del menú desplegable Plugins | Spectralis, o crear una tecla de acceso rápido para acceder a los diferentes plug-ins utilizados. Para lograr esto, seleccione Register_OCT_2 en Complementos | Atajos | Agregue un acceso directo y elija la tecla de acceso rápido deseada.
- Después de abrir el complemento, haga clic en Aceptar en la primera ventana que aparece. A continuación, aparecerá una ventana que contiene el mensaje: Elija un directorio que contenga la exportación XML de Spectralis OCT: en la ventana principal de ImageJ. Seleccione la carpeta que contiene la exportación XML de Spectralis OCT y haga clic en Abrir.
NOTA: Ahora se cargará la OCT, lo que, dependiendo de la potencia de procesamiento de la computadora que se esté utilizando, puede demorar hasta 2 minutos. - A continuación, espere a que aparezca una ventana que contiene el mensaje Guardar imágenes registradas en: . Seleccione el directorio donde se almacenará EnFaceStack (archivo de imagen alineado) y haga clic en Abrir.
- Espere a que aparezca una ventana emergente que contenga el mensaje Elija una imagen para agregar a EnFaceStack: para que aparezca, seleccione la imagen QAF de 32 bits para alinear la imagen con la SD-OCT y haga clic en Abrir. Si se incluyen todas las imágenes necesarias en este EnFaceStack , seleccione Cancelar.
- Cuando la siguiente ventana pida al usuario que seleccione una etiqueta para EnFaceStack, seleccione la etiqueta QAF prefabricada; alternativamente, ingrese el nombre deseado de la modalidad en el cuadro Otro. Seleccione Aceptar para registrar la imagen.
NOTA: No incluya espacios u otros signos de puntuación en el campo Otros . - Observa las tres ventanas que aparecen. El primero está etiquetado como Localizador y muestra la SD-OCT como una imagen del ojo izquierdo (OS ). La segunda ventana se denomina QAF o una de las otras modalidades seleccionadas anteriormente como el ojo izquierdo (OS) o derecho (OD) original. La última ventana se llama Landmarks, que pide seleccionar de uno a tres puntos de referencia en cada imagen.
- Alinee las dos imágenes seleccionando de uno a tres puntos de referencia por imagen: bifurcaciones de recipientes u otras características ubicadas en ambas modalidades. Acérquese (use el carácter de teclado " +" para acercar y " -" para alejar) antes de seleccionar el punto de referencia. Asegúrese de que los puntos de referencia seleccionados estén distribuidos vertical y horizontalmente en la imagen. Una vez que se hayan anotado todos los puntos de referencia, seleccione Aceptar en la pestaña Puntos de referencia y Cancelar en el siguiente mensaje.
- Cuando aparezca una ventana en la que se le pregunte ¿Desea ver los resultados ?, seleccione Sí para comprobar si la imagen se ha alineado correctamente. Para ello, haz zoom en una pequeña embarcación y coloca el cursor a su lado, luego desplázate hacia arriba o hacia abajo para comprobar cuánto se mueve la embarcación en relación con el cursor. Si la alineación no es precisa, elimine el archivo ".tiff" en el directorio OD_QAF y reinicie el proceso desde el inicio del paso 2.
NOTA: Dado que las marcas en Mark_BScans_OCT deben ser precisas, la alineación entre la imagen SD-OCT y QAF también debe ser muy precisa. La alineación perfecta de píxeles se puede lograr en la mayoría de las imágenes, aunque en algunos casos la alineación se limita a una precisión de tres o cuatro píxeles.
7. Creación de una imagen QAF promediada para la comparación (plug-in utilizado: StandardRetina/BatchStandardRetina)
NOTA: Los valores de QAF dependen en gran medida de la ubicación de la retina (p. ej., sombreado central causado por el pigmento macular). Por lo tanto, los valores de QAF de las drusas deben compararse con los valores de QAF estándar de la misma región. Como requisito previo para el análisis, StandardRetina crea un mapa de cara de imágenes QAF promediadas (por ejemplo, de una cohorte de control con coincidencia de edad). El mapa de cara resultante muestra un mapa píxel por píxel de un valor promedio de QAF para la retina central.
- Hay dos formas de crear retinas estándar dentro de la canalización de Spectralis: la primera, AddToStandardRetina_OCT, permite un nuevo caso a la vez en el mapa de rostro, mientras que la segunda, BatchStandardRetina, agrega varios casos a la vez.
- Para agregar una imagen a la vez, seleccione Complementos | Espectralis | AddToStandardRetina_OCT y descarte la pantalla de apertura. Cuando aparezca una ventana que muestre el texto Elija un directorio que contenga una exportación XML de OCT de Spectralis, seleccione la carpeta y haga clic en Seleccionar para abrir el BScan.
- Cuando aparezca una nueva ventana que muestre el mensaje Elija un directorio que contenga imágenes EnFace registradas:, seleccione la carpeta adecuada y haga clic en Seleccionar.
- Observe las tres ventanas que aparecen, una etiquetada como EnFaceStack que muestra las imágenes apiladas de la carpeta seleccionada en el segundo paso, la segunda etiquetada Bscan Stack que muestra el OCT BScan y una tercera ventana que aparece en el medio etiquetada como Elegir modalidad. Seleccione una modalidad de EnFaceStack.
- Seleccione una modalidad y observe la nueva ventana que aparece con el mensaje Elija un directorio que contenga StandardRetina. Si aún no existe un directorio que contenga un StandardRetina, seleccione una carpeta vacía para crear un nuevo StandardRetina.
- Examine el nuevo StandardRetina, desplácese hacia arriba y hacia abajo y mueva el cursor para ver la media y la desviación estándar de esa ubicación específica. Haga clic en el botón ¿Aceptar? Para agregar la foto más reciente a StandardRetina o descartarla.
- Para agregar varias imágenes a la vez, use Batch_QAF_StandardRetina.
- Primero, prepare un archivo "manifest.txt" en la misma carpeta que los ID de caso y asegúrese de que enumere la ruta relativa desde la ubicación del archivo .txt hasta OCT y EnFaceStack. Separe los dos con un espacio de tabulación y asegúrese de que no haya espacios en blanco adicionales delante y detrás de los nombres. El archivo debe parecerse a esta configuración:
pathToOCT_1>pathToEnFaceStack_1>001/OD-OCT>001/OD-QAF
pathToOCT_2>pathToEnFaceStack_2>002/OD-OCT>002/OD-QAF - Crea el archivo en un software de hoja de cálculo y guárdalo como un archivo txt. Asegúrese de que todas las rutas de acceso contengan el QAF de segmento (letras de caracteres) para que el archivo de manifiesto funcione correctamente. Los plug-ins se encuentran en el menú desplegable Plugins | SpectralisBatch-Batch | QAF_StandardRetina.
- Cierre la pantalla de apertura y espere a que se abra una nueva ventana que muestre el mensaje Seleccione la retina estándar inicial. Seleccione una carpeta con un StandardRetina preexistente o seleccione una carpeta vacía para crear un nuevo StandardRetina.
- Busque un mensaje con la etiqueta Seleccionar modalidad para que aparezca; el valor predeterminado es QAF. Asegúrese de que el nombre de archivo de la modalidad respectiva coincida exactamente con el nombre de archivo de un segmento en cada EnFaceStack nombrado en el archivo de manifiesto. A continuación, cuando se abra una ventana en la que se pida al usuario que elija un archivo de manifiesto (descrito anteriormente), haga clic en Cancelar si no se va a agregar ningún otro archivo de manifiesto a este StandardRetina o seleccione otro archivo de manifiesto. Examine el nuevo StandardRetina en una nueva ventana con la etiqueta ¿Aceptar?, y decida si desea agregar el último lote a StandardRetina o descartar el último lote.
NOTA: El proceso de combinar todos los QAF en una StandardRetina puede llevar un tiempo.
- Primero, prepare un archivo "manifest.txt" en la misma carpeta que los ID de caso y asegúrese de que enumere la ruta relativa desde la ubicación del archivo .txt hasta OCT y EnFaceStack. Separe los dos con un espacio de tabulación y asegúrese de que no haya espacios en blanco adicionales delante y detrás de los nombres. El archivo debe parecerse a esta configuración:
8. Anotación de regiones de interés para el análisis (plug-in utilizado: Mark_BScans_OCT)
- Para marcar lesiones (como drusas), abra Plugins | Espectralis | Mark_BScans_OCT y descarte el mensaje de apertura. Busque una nueva ventana con la etiqueta Elija un directorio que contenga una exportación XML de OCT de Spectralis para que aparezca. Elija la carpeta que tiene la OCT deseada y haga clic en Aceptar.
- Después de que FIJI haya cargado la OCT, observe la nueva ventana con la etiqueta Elija un directorio que contenga imágenes de cara registradas para que aparezcan. Seleccione el directorio que contiene EnFaceStack y haga clic en Seleccionar.
- Ahora aparecen tres nuevas ventanas, una con la etiqueta EnFaceStack, otra con la etiqueta BscanStack y otra con el nombre Parámetros de usuario.
- La ventana Parámetros de usuario solicita al usuario que introduzca los siguientes parámetros: ID de caso, que aparecerá en el nombre del archivo csv de salida, ancho de banda en mm, ancho de línea de superficie, ancho de línea de BScan y opacidad de máscara de región.
- El parámetro ancho de banda en mm determina el ancho de cada isocasco en milímetros ( mm ). Utilice el ancho de línea de Enface para cambiar el ancho de línea de las lesiones marcadas en la ventana etiquetada como EnFaceStack.
- El ancho de línea de BScan determina el ancho de línea en la ventana Bscan Stack. Tenga en cuenta que establecer este parámetro en 1 es la mejor configuración de ancho de línea para la mayoría de los casos.
- Elija entre una máscara facial o un mapa de distancia que se muestra en una ventana separada para decidir si se deben colorear las bandas interiores. A continuación, haga clic en Listo en la ventana Marcar en BScan del plug-in.
- A continuación, cuando se le pida que seleccione un StandardRetina preexistente, seleccione la carpeta que contiene el StandardRetina y haga clic en Seleccionar. Tenga en cuenta que si se selecciona una StandardRetina , el Mark_BScans_OCT de salida seleccionará la puntuación z del modo (de un valor QAF medido en comparación con StandardRetina). Si se prefiere el valor QAF sin procesar , haga clic en Cancelar y espere una nueva ventana etiquetada como Mensaje que advierte que los resultados serán valores sin procesar, no puntuaciones z.
- La ventana Parámetros de usuario solicita al usuario que introduzca los siguientes parámetros: ID de caso, que aparecerá en el nombre del archivo csv de salida, ancho de banda en mm, ancho de línea de superficie, ancho de línea de BScan y opacidad de máscara de región.
- Busque una nueva ventana emergente que le pida que elija un directorio que contenga el estado guardado con los datos guardados. Si existe un archivo guardado, haga clic en el directorio que contiene los sectores | Seleccione. En caso de que no se vaya a guardar el progreso, seleccione cancelar. Busque una nueva ventana con la etiqueta Marcar en BScan y, en un menú desplegable, seleccione guardar, ignorar, listo y marcar.
- Marcar: Comience a anotar las regiones de interés en el BScan, con comandos similares a los del plug-in "Register_OCT_2" explicado anteriormente. Para marcar una región, seleccione iniciar haciendo clic con el botón derecho y arrastrando el cursor del ratón hasta el final de la lesión, asegúrese de que la marca esté seleccionada en la ventana Marcar en B-Sscan y haga clic en Aceptar. La región de interés ahora está marcada en este BScan.
- Ignorar: Seleccione Ignorar en la ventana Marcar en BScan y haga clic en Aceptar para ignorar la marca.
- Salvar: Seleccione guardar en la ventana Marcar en BScan y haga clic en Aceptar para que aparezca una nueva ventana, que contenga el mensaje de seleccionar un directorio para guardar el estado. Seleccione una carpeta ya existente o cree una nueva. Abra los archivos ya existentes iniciando "Mark_BScans_OCT" y seleccione el directorio que contiene el estado guardado cuando aparezca la ventana Elegir un directorio que contenga el estado guardado.
NOTA: No se pueden almacenar varios estados de guardado en un directorio; guardar estados de una configuración regional a otra no se puede cambiar fácilmente (por ejemplo, ALEMÁN a EE. UU.). - Hecho: Seleccione hecho en la ventana Marcar en BScan y haga clic en Aceptar para que aparezca una nueva ventana con la etiqueta elegir modalidad .
- Cuando aparezca un mensaje etiquetado como traer la modalidad correcta en la parte superior de la pila de enface, coloque la modalidad llamada QAF en la parte superior, que se alineó con "Register_OCT_2". Para ello, desplácese por EnFaceStack, seleccione la ventana En face Stack o haga clic en la flecha izquierda o derecha. Tenga en cuenta que el nombre de la modalidad se muestra en la esquina superior izquierda.
- Para inspeccionar y marcar mejor las lesiones, amplíe la ventana de Bscan. Haga clic en la ventana B-Scan , apunte el mouse en la dirección en la que desea acercar y presione la tecla + ; Para alejar la imagen, presione la tecla -.
- Desplácese por la pila de BScan desplazándose hacia arriba o hacia abajo con el ratón, arrastrando la barra de la parte inferior hacia la izquierda o hacia la derecha para desplazarse por el escaneo, o seleccionando el marco de B-Scan y haciendo clic en las teclas de flecha izquierda y derecha del teclado. Tenga en cuenta que la línea roja en la ventana de EnFaceStack y en la parte superior izquierda de la ventana de BScan donde se muestra el número de BScan (por ejemplo, 31/120) proporciona una descripción general del área actual en la pila de BScan.
- Haga clic en Aceptar para crear un nuevo archivo .tsv en la carpeta "OD_OCT" o "OS_OCT" correspondiente. Tenga en cuenta que el nombre del archivo .tsv se compondrá de "Mark_Bscans_OCT" más el ID del caso que se ingresó, la lateralidad y la modalidad que se eligió en el último paso de Mark_Bscans_OCT. Además, los "iso-cascos" codificados por colores de las drusas ahora se mostrarán en EnFaceStack.
Resultados
Visualización de la salida
Para analizar adecuadamente y sacar conclusiones de los resultados, es importante comprender el archivo de salida de Mark_Bscans_OCT. Las tres primeras columnas se etiquetan después del identificador del caso, la lateralidad del archivo y la modalidad de imagen que se eligió. La cuarta columna se denomina por modo y se denomina puntuación z. Tenga en cuenta que al momento de escribir este texto, Mark BScans solo puede calcular todas las lesiones de una sola vez; Las filas se refieren a isocascos, cuyas distancias desde el borde exterior de la lesión se especifican en las columnas inferior y superior de la hoja de cálculo. Los isocascos miden la FA en puntuaciones z (en el caso de QAF) en una circunferencia específica alrededor de la lesión. Tenga en cuenta que el valor mínimo de un píxel en un isocasco se puede encontrar en las columnas etiquetadas como min, las columnas etiquetadas como mediana, máximo, medio y stdev, respectivamente, contienen la mediana, el máximo, el valor medio y la desviación estándar de la media de los valores de píxel en unisocasco. La columna n contiene el número total de píxeles de un isocasco. En la figura 1 se muestra una drusa blanda singular marcada de un paciente masculino de 84 años con degeneración macular asociada a la edad intermedia (DMAEi).
La Figura 2 muestra el ojo izquierdo de un paciente representativo con SDD marcados con la herramienta QAF-Workflow (Figura 3). Los SDD en este paciente se asociaron con una reducción de la FA (z-score = -0,4 ± 0,2). De manera similar, los isocascos alrededor del SDD demostraron una AF reducida (por ejemplo, el isocasco más cercano = -0,3 ± 0,3) en comparación con el StandardRetina. Una explicación plausible para este fenómeno podrían ser los efectos de sombra (translucidez reducida) de las lesiones de SDD en el EPR. El uso de las SDD fue ejemplar. La herramienta también permite evaluar los niveles locales de FA en otras lesiones, como las drusas. Además, la herramienta permite realizar un seguimiento de los cambios en la FA de las lesiones a lo largo del tiempo.
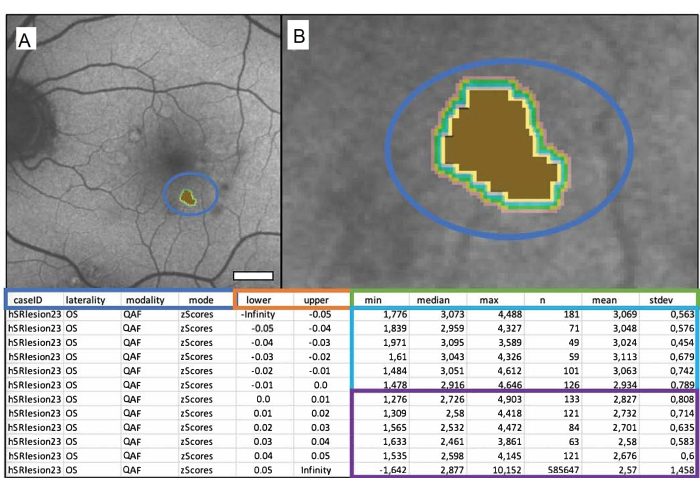
Figura 1: Una drusa blanda marcada singular de un paciente masculino de 84 años con degeneración macular asociada a la edad intermedia (DMAEi). (A) La imagen QAF de un ojo izquierdo con las drusas marcadas. (B) Primer plano de las drusas: centro marrón que representa las drusas marcadas y bandas de colores que representan los isocascos circundantes. En la tabla siguiente se muestra el archivo de salida. Los valores de drusas QAF se comparan con los valores QAF correspondientes de la excentricidad correspondiente de la StandardRetina. Esto da como resultado puntuaciones z que representan la desviación de la media de las áreas no afectadas. El cuadro azul muestra de izquierda a derecha: el ID del caso, la lateralidad del ojo, la modalidad utilizada y la salida deseada (en este caso, puntuaciones z). Las columnas dentro del cuadro naranja muestran los límites del área medida en milímetros (inferior = límite inferior, superior = límite superior). El cuadro verde etiqueta las columnas que muestran las mediciones de QAF. De izquierda a derecha, contienen el mínimo, la mediana, el máximo, el número de píxeles, la media y la desviación estándar de la media. Cada fila representa un isocasco, las filas dentro del cuadro azul representan los valores dentro de la lesión, y las filas dentro del cuadro púrpura muestran los isocascos que rodean cada lesión (de arriba a abajo a medida que aumenta la distancia a la lesión). Barra de escala = 1 mm. Haga clic aquí para ver una versión más grande de esta figura.
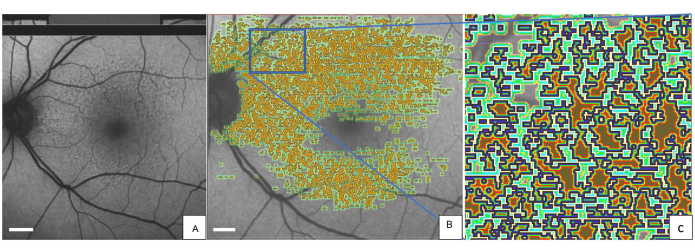
Figura 2: SDD marcados en una imagen de QAF de una paciente femenina de 80 años con DMAE temprana . (A) Los SDD se pueden ver en la imagen de QAF. La misma imagen QAF se muestra con anotaciones impresas de SDD. (B) Alrededor de cada lesión marcada, los iso-cascos se representan con un código de colores (verde claro, verde oscuro y rojo). (C) Una versión ampliada del rectángulo azul. El borde exterior de cada SDD está marcado en azul. Abreviaturas: QAF = autofluorescencia cuantitativa; DMAE = degeneración macular asociada a la edad; SDD = depósito de drusenoides subretinianos. Barra de escala = 1 mm. Haga clic aquí para ver una versión más grande de esta figura.
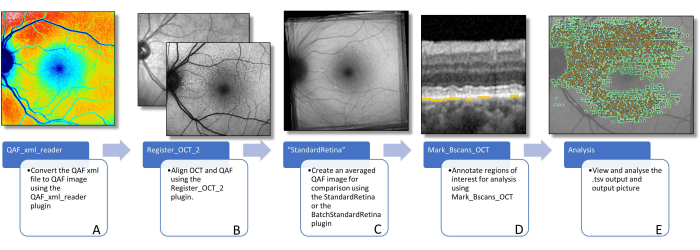
Figura 3: Flujo de trabajo para determinar la FA de las lesiones. En esta figura se visualizan los complementos de software necesarios para determinar la FA específica de la lesión. (A) La imagen muestra una imagen QAF codificada por colores que se puede utilizar para visualizar la distribución de los valores QAF, pero no debe utilizarse para un análisis posterior. (B) Se muestra una imagen QAF en primer plano, con la imagen infrarroja del escaneo SD-OCT en el fondo. Se supone que esto visualiza la alineación utilizando bifurcaciones de vasos. Esto se puede hacer usando el complemento Register_OCT_2. (C) Un StandardRetina que se utiliza para medir los valores de puntuación z de las lesiones. StandardRetinas se puede crear mediante StandardRetina/BatchStandardRetina. (D) Se muestra un BScan con flechas azules que apuntan a los SDD, que están resaltadas por líneas amarillas (nota: las lesiones siempre están marcadas debajo del EPR, independientemente de la ubicación en la dirección z). (E) Todas las lesiones marcadas se ven impresas en una imagen QAF (ver Figura 1). Los dos últimos pasos se realizan con el complemento Mark_BScans_OCT. Abreviaturas: AF = autofluorescencia; QAF = autofluorescencia cuantitativa; SDD = depósito de drusenoides subretinianos; IR = infrarrojo; EPR = epitelio pigmentario de la retina; SD-OCT = tomografía de coherencia óptica de dominio espectral. Haga clic aquí para ver una versión más grande de esta figura.
Discusión
Este flujo de trabajo proporciona una guía paso a paso para utilizar herramientas complementarias FIJI de código abierto para determinar y comparar la FA de lesiones específicas de DMAE. Los plug-ins proporcionan plantillas fáciles de usar que no requieren ningún conocimiento de codificación y pueden ser aplicadas por médicos sin soporte técnico27. Hasta donde sabemos, estas herramientas son únicas en su tipo para la cuantificación de la FA específica de la lesión.
Los valores de QAF varían naturalmente a lo largo de la retina, siendo los valores más altos en la periferia y más bajos en la mácula debido a la distribución desigual de la lipofuscina y la melanolipofuscina dentro de la retina, la baja FA de los vasos y la distribución desigual del pigmento macular. Debido a la alta variación de los niveles naturales de QAF en la retina, el análisis directo de los valores absolutos de QAF de las lesiones no es un enfoque prometedor. Por ejemplo, una lesión hipoautofluorescente en la periferia podría tener valores absolutos de QAF más altos que los niveles de fluorescencia fisiológica de la mácula. El uso de una Retina Estándar y el uso de puntuaciones z para medir los niveles de fluorescencia de las drusas corrigen esta varianza natural de los valores de QAF.
Una puntuación z es una medida numérica de la relación del valor de una región de interés con la media en StandardRetina. Se calcula restando la media de un individuo de la media de la retina estándar en la misma ubicación y luego dividiendo el resultado por la desviación estándar. Esta estandarización permite la comparación de diferentes imágenes QAF, ya que la puntuación z indica cuántas desviaciones estándar difiere un valor de la media. Una puntuación z positiva indica que el valor está por encima de la media, mientras que una puntuación z negativa indica que está por debajo de la media.
Es importante tener en cuenta que puede haber posibles escollos que deben tenerse en cuenta. Si bien este método tiene en cuenta la cantidad variable de niveles de FA a lo largo del fondo de ojo, es posible que aún no sea la forma más precisa de medir y comparar la FA de un EPR. Los individuos tienen diferentes niveles y topografía del pigmento lúteo macular, y las lesiones pueden afectar también a la translucidez de la retina suprayacente28,29. Por lo tanto, es plausible que la reducción de la FA medida en áreas de SDD (ver resultados representativos) sea consecuencia de los efectos de sombreado en lugar de la disminución de los fluoróforos en el RPE30,31,32.
Actualmente estamos trabajando en un flujo de trabajo para tener en cuenta la reflectividad de la retina, el grosor y el pigmento macular cuantificado (utilizando AF verde y azul) con modelos mixtos lineales. Además, hasta ahora, el QAF utiliza un factor de corrección dependiente de la edad para tener en cuenta la opacificación lenticular que no tiene en cuenta las diferencias interindividuales en la opacificación lenticular de los participantes de una edad similar33. Por lo tanto, actualmente estamos trabajando en un flujo de trabajo para un factor de corrección personalizado de la autofluorescencia lenticular y la opacificación. Para extraer de forma fiable la información de la FA de las lesiones pequeñas, se necesita una fiabilidad adecuada test-retest de las imágenes de QAF. Para diferenciar aún más aquellas imágenes QAF en las que es viable un análisis más detallado, estamos investigando "índices de fiabilidad de imágenes QAF" que pueden predecir la fiabilidad test-retest de las imágenes QAF. En la etapa actual, el enfoque prudente es adquirir imágenes duplicadas e investigar la fiabilidad de la repetición de la prueba de la FA específica de la lesión.
El método presentado para analizar adicionalmente los isocascos de las lesiones fue técnicamente difícil de implementar, ya que los isocascos de las lesiones vecinas se fusionan. Las áreas de isocascos fusionados podrían caracterizarse de forma distintiva dependiendo de la lesión que se considere. Nuestra solución fue considerar todas las lesiones de un tipo como una lesión y analizar su periferia como un isocasco articular. Este método, sin embargo, reduce drásticamente la capacidad de medir los isocascos de drusas individuales y podría considerarse un escollo adicional de esta técnica. En el futuro, podrían facilitarse el análisis de la FA en la circunferencia de las lesiones en el futuro métodos más sofisticados para tener en cuenta los isocascos fusionados o la notificación suspendida de la FA en las zonas de isocascos fusionados.
Utilizamos la DMAE como enfermedad modelo para este estudio. El flujo de trabajo también se puede adaptar para estudiar lesiones en otras enfermedades. Hasta ahora, el QAF se ha utilizado en muchas enfermedades coriorretinianas, incluida la enfermedad recesiva de Stargardt, las enfermedades asociadas a Bestrophin-1, varias formas de retinosis pigmentaria, retinopatía externa oculta zonal aguda, pseudoxantoma elástico y otras 17,33,34,35,36,37 . Dado que este flujo de trabajo utiliza software de código abierto, animamos a otros a duplicar este trabajo para determinar la FA específica de la lesión y ampliar nuestro conocimiento de los trastornos de la retina. En resumen, presentamos un flujo de trabajo para determinar y comparar los niveles de FA de diferentes lesiones retinianas a lo largo de la mácula. Este flujo de trabajo allana el camino para un análisis más profundo de la FA y podría facilitar el desarrollo de nuevos biomarcadores en la DMAE y más allá.
Divulgaciones
Leon von der Emde informa haber recibido pagos de Heidelberg Engineering. Merten Mallwitz no reporta ninguna información financiera. Kenneth R. Sloan tampoco reporta ninguna divulgación financiera. Frank G. Holz informa de consultoría/pagos personales para Acucela, Alcon (C), Gyroscope Allergan Apellis, Bayer Bioeq/Formycon, CenterVue, Roche/Genentech, Geuder, Ivericbio, NightStarX, Novartis, Optos, Oxurion, Pixium Vision, Stealth BioTherapeutics, Zeiss y el centro de lectura GRADE. Thomas Ach reporta pagos personales y de consultoría para Bayer, Apellis, Roche y Novartis.
Agradecimientos
Este trabajo fue financiado por la beca de la Sociedad Alemana de Oftalmología (DOG) para estudiantes de doctorado (MW) y el NIH/NEI 1R01EY027948 (TA).
Materiales
| Name | Company | Catalog Number | Comments |
| BatchStandardRetina plugin | n.a. | n.a. | n.a. |
| FIJI (Image J) | n.a. | n.a. | n.a. |
| Mark_Bscans_OCT plugin | n.a. | n.a. | n.a. |
| Microspft office | Microsoft | n.a. | n.a. |
| QAF_xml_reader plugin | n.a. | n.a. | n.a. |
| Register_OCT_2 plugin | n.a. | n.a. | n.a. |
| Spectralis | Heidelberg Engineering | n.a. | QAF extension |
| StandardRetina plugin | n.a. | n.a. | n.a. |
Referencias
- Schmitz-Valckenberg, S., et al. Fundus autofluorescence imaging. Progress in Retinal and Eye Research. 81, 100893 (2021).
- Bermond, K., et al. Autofluorescent granules of the human retinal pigment epithelium: phenotypes, intracellular distribution, and age-related topography. Investigative Ophthalmology and Visual Science. 61 (5), 35 (2020).
- Bermond, K., et al. Autofluorescent organelles within the retinal pigment epithelium in human donor eyes with and without age-related macular degeneration. Investigative Ophthalmology and Visual Science. 63 (1), 23 (2022).
- Delori, F., et al. Quantitative measurements of autofluorescence with the scanning laser ophthalmoscope. Investigative Ophthalmology and Visual Science. 52 (13), 9379-9390 (2011).
- Fleckenstein, M., et al. Age-related macular degeneration. Nature Reviews Disease Primers. 7 (1), 31 (2021).
- Greenberg, J. P., et al. Quantitative fundus autofluorescence in healthy eyes. Investigative Ophthalmology and Visual Science. 54 (8), 5684-5693 (2013).
- Sparrow, J. R., Boulton, M. RPE lipofuscin and its role in retinal pathobiology. Experimental Eye Research. 80 (5), 595-606 (2005).
- vonder Emde, L., et al. Natural history of quantitative autofluorescence in intermediate age-related macular degeneration. Retina. 41 (4), 694-700 (2021).
- Reiter, G. S., et al. Longitudinal changes in quantitative autofluorescence during progression from intermediate to late age-related macular degeneration. Retina. 41 (6), 1236-1241 (2021).
- Gliem, M., et al. Quantitative fundus autofluorescence in early and intermediate age-related macular degeneration. JAMA Ophthalmology. 134 (7), 817-824 (2016).
- Hussain, R. M., Gregori, N. Z., Ciulla, T. A., Lam, B. L. Pharmacotherapy of retinal disease with visual cycle modulators. Expert Opinion on Pharmacotherapy. 19 (5), 471-481 (2018).
- Ammar, M. J., Hsu, J., Chiang, A., Ho, A. C., Regillo, C. D. Age-related macular degeneration therapy: a review. Current Opinion in Ophthalmology. 31 (3), 215-221 (2020).
- Ach, T., et al. Lipofuscin redistribution and loss accompanied by cytoskeletal stress in retinal pigment epithelium of eyes with age-related macular degeneration. Investigative Ophthalmology and Visual Science. 56 (5), 3242-3252 (2015).
- Zanzottera, E. C., Messinger, J. D., Ach, T., Smith, R. T., Curcio, C. A. Subducted and melanotic cells in advanced age-related macular degeneration are derived from retinal pigment epithelium. Investigative Ophthalmology and Visual Science. 56 (5), 3269-3278 (2015).
- Cao, D., et al. Hyperreflective foci, optical coherence tomography progression indicators in age-related macular degeneration, include transdifferentiated retinal pigment epithelium. Investigative Ophthalmology and Visual Science. 62 (10), 34 (2021).
- Zanzottera, E. C., et al. The Project MACULA retinal pigment epithelium grading system for histology and optical coherence tomography in age-related macular degeneration. Investigative Ophthalmology and Visual Science. 56 (5), 3253-3268 (2015).
- Sparrow, J. R., Duncker, T., Schuerch, K., Paavo, M., de Carvalho, d. R. L. Lessons learned from quantitative fundus autofluorescence. Progress in Retinal and Eye Research. 74, 100774 (2020).
- Schmitz-Valckenberg, S., et al. Correlation between the area of increased autofluorescence surrounding geographic atrophy and disease progression in patients with AMD. Investigative Ophthalmology and Visual Science. 47 (6), 2648-2654 (2006).
- Ach, T., Bermond, K. Autofluorescence of the human retinal pigment epithelium in normal aging and in age-related macular degeneration: histology and clinical correlation. Klinische Monatsblatter Fur Augenheilkunde. 236 (5), 672-681 (2017).
- Pollreisz, A., et al. Visualizing melanosomes, lipofuscin, and melanolipofuscin in human retinal pigment epithelium using serial block face scanning electron microscopy. Experimental Eye Research. 166, 131-139 (2018).
- Bernstein, P. S., et al. meso-zeaxanthin: The basic and clinical science underlying carotenoid-based nutritional interventions against ocular disease. Progress in Retinal and Eye Research. 50, 34-66 (2016).
- Göbel, A. P., Fleckenstein, M., Heeren, T. F. C., Holz, F. G., Schmitz-Valckenberg, S. In-vivo mapping of drusen by fundus autofluorescence and spectral-domain optical coherence tomography imaging. Graefe's Archive for Clinical and Experimental Ophthalmology. 254 (1), 59-67 (2016).
- Pfau, M., et al. Mesopic and dark-adapted two-color fundus-controlled perimetry in geographic atrophy secondary to age-related macular degeneration. Retina. 40 (1), 169-180 (2020).
- vonder Emde, L., et al. Mesopic and dark-adapted two-color fundus-controlled perimetry in choroidal neovascularization secondary to age-related macular degeneration. Translational Vision Science and Technology. 8 (1), 7 (2018).
- Aumann, S., Donner, S., Fischer, J., Müller, F. Optical coherence tomography (OCT): principle and technical realization. High Resolution Imaging in Microscopy and Ophthalmology: New Frontiers in Biomedical Optics. , 59-85 (2019).
- Schindelin, J., et al. FIJI: an open-source platform for biological-image analysis. Nature Methods. 9 (7), 676-682 (2012).
- Kleefeldt, N., et al. Quantitative fundus autofluorescence: advanced analysis tools. Translational Vision Science and Technology. 9 (8), 2 (2020).
- Hong, I. H., Jung, W. H., Lee, J. H., Chang, I. B. Macular pigment optical density in the Korean population: a cross sectional study. Journal of Korean Medical Science. 35 (5), e30 (2020).
- Putnam, C. M. Clinical imaging of macular pigment optical density and spatial distribution. Clinical and Experimental Optometry. 100 (4), 333-340 (2017).
- Zweifel, S. A., Spaide, R. F., Curcio, C. A., Malek, G., Imamura, Y. Reticular pseudodrusen are subretinal drusenoid deposits. Ophthalmology. 117 (2), 303-312 (2010).
- Curcio, C. A., et al. Subretinal drusenoid deposits in non-neovascular age-related macular degeneration: morphology, prevalence, topography, and biogenesis model. Retina. 33 (2), 265-276 (2013).
- Spaide, R. F. Outer retinal atrophy after regression of subretinal drusenoid deposits as a newly recognized form of late age-related macular degeneration. Retina. 33 (9), 1800-1808 (2013).
- Reiter, G. S. Influence of lens opacities and cataract severity on quantitative fundus autofluorescence as a secondary outcome of a randomized clinical trial. Scientific Reports. 11 (1), 12685 (2021).
- Gliem, M., et al. Quantitative fundus autofluorescence in pseudoxanthoma elasticum. Investigative Ophthalmology and Visual Science. 58 (14), 6159-6165 (2017).
- Burke, T. R., et al. Quantitative fundus autofluorescence in recessive Stargardt disease. Investigative Ophthalmology and Visual Science. 55 (5), 2841-2852 (2014).
- Armenti, S. T., Greenberg, J. P., Smith, R. T. Quantitative fundus autofluorescence for the evaluation of retinal diseases. Journal of Visualized Experiments. (109), 53577 (2016).
- Pröbster, C., et al. Quantitative fundus autofluorescence in the developing and maturing healthy eye. Translational Vision Science and Technology. 10 (2), 15 (2021).
- Duncker, T., et al. Quantitative fundus autofluorescence and optical coherence tomography in PRPH2/RDS- and ABCA4-associated disease exhibiting phenotypic overlap. Investigative Ophthalmology and Visual Science. 56 (5), 3159-3170 (2015).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados