Method Article
Bioimaging enregistré des nanomatériaux pour la surveillance des services diagnostiques et thérapeutiques
Dans cet article
Résumé
Méthodes de bio-imagerie utilisées pour évaluer la biodistribution des cellules de nanoparticules sont applicables pour la surveillance thérapeutique et diagnostique de composés nanoformulated. Les méthodes décrites ici sont sensibles et spécifiques lorsqu'ils sont évalués par des coregistration histologique. Les méthodologies de fournir une voie de translation des rongeurs à des applications humaines.
Résumé
Nanomedications peut être transporté par le sang monocytes-macrophages dans le système réticuloendothélial (SER; rate, le foie des ganglions lymphatiques), et de mettre fin organes. Ces derniers comprennent le poumon, RES, et le cerveau et sont opérationnels au cours de type virus d'immunodéficience humaine un (VIH-1) infection. D'entrée des macrophages dans les tissus est notable dans les domaines de VIH-1 actifs réplication et des sites d'inflammation. Afin d'évaluer le potentiel des macrophages comme nanovecteurs, superparamagnétiques d'oxyde de fer et / ou de drogue particules chargées ont été enduits de tensioactifs parentérale injecté dans le VIH-1 souris encéphalitique. Cela a été fait pour évaluer quantitativement particule et de biodistribution des médicaments. Imagerie par résonance magnétique des résultats de test (IRM) ont été validés par coregistration histologique et le traitement d'image améliorée. Maladie d'organe Fin tant caractérisée par l'histologie du cerveau altéré ont été évalués par IRM. La démonstration de la migration robuste de nanoformulations dans les zones d'encéphalite focale offre «preuve de concept» pour l'utilisation de techniques avancées de bio-imagerie pour suivre la migration des macrophages. Surtout, les aberrations histopathologiques dans le cerveau en corrélation avec les paramètres bio-imagerie faisant l'utilité générale de l'IRM dans les études sur la distribution cellulaire dans la maladie faisable. Nous postulons que l'utilisation de ces méthodes peuvent fournir un indice en temps réel du fardeau de la maladie et l'efficacité thérapeutique avec un potentiel de translation pour les humains.
Protocole
1. Présentation
La distribution sélective des médicaments et des macromolécules thérapeutiques (peptides, protéines et acides nucléiques) à des sites cellulaires et tissulaires de la maladie active et continue des infections microbiennes permettra d'améliorer les réponses pharmaceutiques cours de la maladie 1-3. Un site en particulier cellulaire est le macrophage qui est à la fois très mobile et le système immunitaire engageant et est une cible cohérente principal pour le virus de l'immunodéficience humaine (VIH) 4. Fait important, l'inflammation des macrophages engagés sous-tend également un large éventail de troubles qui incluent dégénératives, inflammatoires, infectieuses et les maladies cancéreuses, et la mobilité de la cellule à la maladie sous-jacente des sites progression des lésions des tissus 5-9. Fait important, l'utilisation des macrophages par le sang en tant que drogue, macromolécule, et les transporteurs signal a attiré l'attention ces dernières pour son potentiel de translation. Cependant, une obstruction importante dans la réalisation des potentiels thérapeutiques est la barrière hémato-encéphalique (BHE) parmi d'autres barrières tissulaires qui sont imperméables à toute une gamme de macromolécules et des protéines. Ces obstacles, néanmoins, ne permettre le passage de cellule. Tous ensemble, il est projeté que dans le cours naturel des macrophages maladies périphériques que les barrières de contournement peut transporter de la drogue formulée, marqueurs, et des peptides à des sites d'infection ou d'inflammation. Néanmoins, ces technologies restent seulement dans le développement. C'est grâce à nos œuvres à médiation cellulaire de livraison peuvent être développés pour des applications diagnostiques et thérapeutiques et des applications telles sont soutenus par des modèles de laboratoire et les animaux de maladies humaines 10-12.
2. Les préparatifs des nanomatériaux
Préparation des nanomatériaux pour la livraison de drogue et les études de biodistribution est le sujet d'un manuscrit en parallèle dans ce numéro (manuscrit en parallèle de référence). Toutes les procédures pour la fabrication de nanoparticules cristallines sont effectuées dans une hotte à flux laminaire. Toutes les surfaces sont désinfectés avant usage avec de l'alcool à 70%. Cela comprend surface de travail, de l'extérieur de gants et tout déversement. Tous sont couverts avec une solution d'alcool à 70% répliquent immédiatement avec des lingettes. Les gants sont jetés après usage et ne sont pas portés en entrant dans une zone autre laboratoire. Excipient, de drogue, de l'eau stérile avec / contenant des réactifs / tous pour la fabrication de médicaments chargés de particules sont seulement mis en aires de travail lorsque cela est nécessaire pour les procédures. Stérile pipettes enveloppées sont utilisés uniquement et jetés après usage dans un conteneur pour déchets biologiques dangereux. L'appareil humides prêts est désinfectée à l'alcool avant et après utilisation. La zone de travail est nettoyée immédiatement avant et après avec de l'alcool à 70%. Solution de nanoparticules est testé pour pyrogènes conformément aux directives de la FDA pour évaluer l'absence d'endotoxines bactériennes dans les solutions de particules médicament utilisé pour les animaux. En bref,
- Nanoformulations candidat pour l'utilisation in vivo sont répliqués en remplaçant le noyau de drogue ou de gouttelettes d'une taille de particules identiques ou un morceau moulu d'oxyde de fer superparamagnétique (SPIO) avant revêtement avec le surfactant approprié.
- Il est suivi par des mesures de taille, la charge, la forme et la cytotoxicité de déterminer si le système modèle SPIO a les mêmes propriétés que le médicament candidat nanoformulated.
- Enfin, des essais de chargement de cellules sont réalisées par incubation avec le modèle de nanoformultation candidat SPIO afin de déterminer la relaxivité dans les cellules en utilisant des fantômes composé de cellules marquées en suspension dans un gel d'agar. Phantoms sont préparés en triple exemplaire et sont préparés à une série de concentrations afin de quantifier la relaxivité due à l'absorption SPIO dans les cellules. Cela fournit un indice de sensibilité et détermine si le nanoformulations peuvent affecter l'état d'oxydation, et donc la visibilité de la SPIO en imagerie par résonance magnétique (IRM).
3. Méthodes et procédures: Préparation des animaux
- Injections / cathéters. Selon le temps d'intérêt, les injections peuvent exiger l'utilisation d'un cathéter pour injecter de l'animal au sein de l'IRM. Les cathéters sont préparés en utilisant une aiguille non magnétique et une extension de tuyau d'un diamètre minimum pour minimiser l'espace mort dans la ligne d'injection. Le cathéter doit être prérempli avec soit la solution contenant le nanomatériau doit être injecté ou une solution saline, selon l'espace mort et le volume total acceptable de l'injection. Si possible, l'injection peut être suivie d'un rinçage du sérum physiologique. Si les temps aiguë ne sont pas d'une extrême importance, un pré-scan peut être effectué, et l'injection peut se faire en dehors de l'aimant à une heure prédéterminée avant que le suivi des analyses pour les mesures de biodistribution. Les cathéters sont généralement inséré dans la veine de la queue pour les injections IV.
- L'anesthésie et la surveillance. Avant la numérisation, l'animal est placé dans une chambre pour induire une anesthésie. Cette chambre est préremplie avec l'isoflurane à 1,5% dans 70% nl'oxyde itrous et l'oxygène de 30% afin d'accélérer l'apparition de l'anesthésie chez l'animal et de minimiser la quantité de temps requise pour s'assurer que l'animal ne se réveille pas lors du retrait de la chambre. Une fois que l'animal est totalement anesthésié, l'animal est retiré de la chambre et placé dans le support stéréotaxique équipé pour surveiller le taux de respiration et la température de l'animal, tout en continuant à fournir l'isoflurane pendant la configuration et de numérisation.
- Les détenteurs des animaux et de réglage: Set-up comprend lubrifiant oculaire pour se protéger contre les ulcères cornéens. L'animal est légèrement enveloppé d'une gaze et la gaze est enregistrée en place pour minimiser les pertes de chaleur lors de la numérisation et de fournir une pression positive contre le moniteur de respiration. Les détenteurs d'animaux sont équipées de barres dents réglables, permettant un alignement vertical et horizontal de la tête. Ceci est particulièrement important pour les IRM à haut champ, comme une angulation de la tête en direction caudale-rostrale va causer des difficultés supplémentaires avec inhomogénéité de champ magnétique dû à la susceptibilité magnétique. Inhomogénéité de champ magnétique est délétère pour la qualité de haute T 2 * IRM ainsi que la spectroscopie 1 H par résonance magnétique (SRM 1 H) et par résonance magnétique Diffusion Tensor Imaging (DTI). En plus d'un bon positionnement de l'angle de la tête en direction caudale-rostrale, les rotations de la tête doit être évitée dans la mesure où c'est faisable. En tenant compte de la rotation du porte animales dans l'aimant prévoit des compensations pour les rotations mineures, qui peuvent survenir de l'animal à animal. Cela peut être diminuée en placement soigneux de la tête et d'attention à l'angulation avant d'insérer l'animal dans le système d'IRM.
- Calibrage et Shimming: Une fois que l'animal est dans le support et la bobine de surface est correctement placé sur la tête, la position initiale de l'animal est déterminé par un temps réel unidimensionnelle lecture en direction caudale-rostrale. Le signal est limité à la zone autour de la bobine de surface utilisé pour la réception, en limitant le besoin de l'interprétation des formes d'onde observées. Une fois la position initiale est déterminée, une image 3-localizer avion est pris pour déterminer la position exacte de l'animal dans le scanner et pour permettre le mouvement à la localisation précise nécessaire à la numérisation (s) d'intérêt. Elle est suivie par un ajustement de l'homogénéité du champ magnétique ou «calage» de l'aimant. Cela se fait par la cartographie de la distribution du champ et le calcul d'une correction déterminée avec précision spatiale basée sur les réponses mesurées d'une série d'électroaimants ou «bobines de shim" au sein du système conçu pour régler l'homogénéité sur le terrain. Calage est accompli en utilisant une séquence en écho de gradient multi-et le logiciel de cartographie développé par le Dr Hetherington 13. Régions de l'homogénéité sont adaptées à la région examinée par chaque méthode d'imagerie individuelles. Une fois calage est terminée, nous pouvons acquérir le scan (s) d'intérêt de l'animal.
4. Acquisition de données
- Haute Résolution T 2 * IRM pondérée. Biodistribution des nanoparticules contenant SPIO peut être déterminée en détectant les régions de perte de signal en haute résolution 3D T 2 * IRM pondérée. La région du cerveau est déterminée à partir de l'analyse de piste et prescrit sur les scans localizer ou des scans supplémentaires si nécessaire. AT 2 * scanner IRM pondérée avec une résolution de 150 microns isotrope est ensuite acquise. Une haute résolution de gradient 3D rappelé l'écho IRM de la tête de la souris est acquis à l'aide d'une bobine de 25 mm cage volume avec les paramètres d'acquisition des temps d'écho = 5 ms, temps de répétition = 50 ms, l'écho de 30%, angle de bascule = 35 degrés, des moyennes = 2, le champ de vision = 20 x 20 x 20 mm avec une résolution de 128 x 128 x 128 (voxel size = 150 x 150 x 150 um 3), le temps d'acquisition total = 30 min.
- Diffusion Tensor Imaging (DTI): les images du tenseur de diffusion sont des mesures quantitatives de l'orientation et l'ampleur de la diffusion de l'eau dans les cellules des tissus. En conséquence, la phase du signal est extrêmement sensible au mouvement, comme les scans sont sensibilisés ou «pondéré» pour le mouvement d'eau microscopiques. En conséquence, les acquisitions seul coup l'on souhaite éviter des décalages de phase entre les acquisitions de causer bavures du signal et la synchronisation respiratoire est nécessaire pour empêcher le mouvement brut lors de l'acquisition du signal. Par conséquent, une des voies respiratoires fermée écho de spin pondérées en diffusion d'imagerie écho planar (EPI) séquence IRM est employée. Encore une fois, calage de la région de l'analyse est très important, comme hors effets de la résonance au cours de l'évolution du signal provoque la mauvaise superposition des signaux de la fréquence, et donc la position, dans le plan de l'image. PEV paramètres d'acquisition comprend 14 tranches, 200 kHz, 96 x 96 dans l'acquisition avion rempli de zéros à 256 x 256, et une épaisseur de coupe de 0,5 mm. L'encodage de diffusion utilisé est un équilibre, schéma de polarité rotation-invariante et alternant icosaédrique (12 directionstions) 14,15. Le schéma de codage a été conçu pour réduire background-diffusion en gradient raccords 16. Diffusion pondération facteur b = 800 mm -2 s, δ = 4 ms, Δ = 15 ms, Gdmax = 40 g / cm, 200 ms temps de montée, 7 moyennes pour b = 0 acquisition, 3 moyennes pour chaque b = 800 encodage direction, pour un temps total d'acquisition de 20-40 min, en fonction de la fréquence respiratoire.
- Localisé 1 H spectroscopie par résonance magnétique (SRM 1 H): 1 H SRM peut être obtenue à partir des régions du cerveau prescrits sur des images acquises durant la session d'imagerie mêmes. Localisations anatomiques sont trouvés sur les images pour prescrire la région d'intérêt pour l'acquisition de spectres. Une fois que la région est identifiée, calage est effectué sur une région correspondant au volume de l'acquisition, vérifiée en utilisant un spectre d'eau localisée. Ensuite, la puissance des impulsions de suppression de l'eau sont optimisés, la fréquence de l'eau est mesurée pour assurer le signal de l'eau sur la résonance, et un spectre court test est acquis pour fournir un contrôle de qualité. Si les spectres sont de qualité insuffisante, les paramètres système, y compris les radiofréquences (RF) de puissance et les paramètres de cale, sont vérifiées. Enfin, si la qualité est encore insuffisante, un deuxième avion 3-localisateur est exécuté pour s'assurer que l'animal n'a pas bougé de l'analyse initiale. Dans notre expérience, cela donne un très haut degré de reproductibilité et la précision des acquisitions spectroscopiques. Enfin, les spectres sont acquis en blocs courts avec réarmement de la fréquence du système entre les acquisitions d'éliminer les effets de la dérive du champ magnétique et d'assurer la reproductibilité et la qualité des numérisations finales. A la fin de l'acquisition, un spectre seule impulsion de l'eau à un gain du préamplificateur prédéfini est utilisé comme une référence quantitative l'amplitude du signal.
- Histologie et d'imagerie îlot: Après la séance d'IRM final dans la série temporelle des expériences, la souris est perfusé, le cerveau est enlevé et embarqué dans un bloc de l'OCT, composé qui a été assombri l'aide d'une goutte d'encre de Chine. Le bloc est placé dans un cryostat pour le tranchage et l'analyse histologique. Images sont acquises îlot en utilisant un appareil photo numérique (Canon EOS 300D Digital Rebel avec un Canon EFS 60mm f/2.8 ultrasons Macro USM) monté à l'avant du cryostat avec un support personnalisé et déclenché par un interrupteur à distance. Les images numériques sont acquises toutes les 50 micromètres à travers le volume du cerveau entier. Les tranches sont numérotées afin de permettre l'enregistrement dans le volume après traitement histologique et la coloration. Tranches îlot individuels ont été alignés pour reconstruire le volume 3D en utilisant le bloc décrit pour rendre compte de la gigue dans la position de la tête du cryostat. Le volume du cerveau est alors automatiquement segmentées en utilisant l'algorithme région à base de graines de plus en plus dans le logiciel Analyser (AnalyzeDirect, Lexena, KS).
5. Analyses de données
- Détection par IRM SPIO: SPIO provoque une perte de signal en T 2 * IRM pondérée; marqueur et, comme tel, le vide de signal IRM est une question sensible, mais non spécifique pour la présence de SPIO dans les tissus. La sensibilité dépend de la résolution spatiale de l'IRM et la taille de la particule SPIO, avec une particule microns seule taille détectées avec une résolution de 100 microns isotrope. Dans ces œuvres, une résolution de 150 microns isotrope avec 200 particules nanométriques de taille SPIO sont utilisés. Pour fournir à la fois sensibilité et la spécificité de la présence de SPIO dans le cerveau, les souris ont été scannés avant l'injection des cellules SPIO étiquetés pour permettre la soustraction d'images à utiliser pour l'identification positive des cellules dans le cerveau à des points plus tard. 3D IRM ont été subimaged utilisant la méthode de niveau de contrainte mis au point dans notre laboratoire comme décrit précédemment 17. Volume du cerveau ont ensuite été recalées Subimaged, l'intensité du signal normalisé, et les volumes soustraits à détecter des régions dans le volume du cerveau avec une perte de signal (présence de SPIO), ce qui n'était pas le long des bords pour éliminer positifs faux signal de toute les erreurs d'enregistrement sous-pixel.
- Coregistration d'histologie et de l'IRM: coregistration entre l'histologie et l'IRM a été accompli en utilisant l'image comme un îlot de référence commun. Cette approche réduit la complexité du problème majeur de corriger le rétrécissement asymétrique des tranches de tissu lors de la préparation et la coloration d'un problème à deux dimensions comme décrit dans nos précédents travaux 18,19. Ici, l'IRM et l'histologie de détection des macrophages dans le cerveau contenant SPIO ont montré une excellente corrélation spatiale, avec une surestimation du volume prévu par la perte de signal IRM et une plus grande sensibilité à quelques cellules démontré par l'histologie 12. Précis de co-localisation de ces deux signaux permet une mesure de la précision des coregistration et la déformation de l'histologie de retour aux formes originales des tranches.
- Région d'intérêt (ROI) Analyses de DTI: DTI scans sont généralement analysées par la sélection d'un ROI anatomique pour détermine les propriétés de diffusion moyenne du tissu dans une sous-structure anatomique particulière.
Analyses de la diffusion de données pondérées sont effectuées en utilisant des programmes personnalisés écrits en IDL (Interactive Data Language, ITT Visual Information Solutions, Boulder, CO), comme décrit précédemment 15,20. Analyses de produire des cartes de la diffusivité tenseur (λ 1, λ 2, λ 3), la diffusivité moyenne (D av) où: D av = (λ 1 + λ 2 + λ 3) / 3 et de l'anisotropie fractionnelle (FA), où: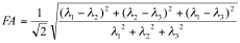
Transversale (λ ⊥ = (λ 2 + λ 3) / 2) et longitudinale (λ ll = λ 1) les composantes du tenseur de diffusion ont été obtenus comme décrit par ailleurs 21. Une fois les cartes sont construites, ROIs sont dessinés sur T 2 superposées IRM pondérée avec des cartes de couleur codée directionnalité λ 1. Exemples des régions choisies pour l'analyse dans le modèle murin VIH sont affichés dans la figure 1. - Analyse spectroscopique: Quantification des composés métaboliques contribuant aux pics de SRM cérébrale 1 H est déterminée en utilisant l'une des diverses méthodes d'ajustement de courbe. Une variété de techniques d'ajustement de courbe ont été développés. Dans notre laboratoire, nous utilisons une méthode d'ajustement dans le domaine temporel (QUEST) 22 au 23 jMRUI logiciel de traitement de signal qui est une combinaison linéaire de spectres métabolite individuels qui contribuent à le spectre final. Nous utilisons une base ensemble de 22 métabolites individuels potentiels facteurs contributifs. Les spectres de base sont simulées et vérifiée à l'aide des spectres de solutions de métabolites individuels. Un exemple d'un résultat ajustement de la courbe d'un seul spectre est montré dans la figure 2.
6. Les résultats représentatifs
Exemples de DTI et 1HMRS sont présentés dans les figures 1 et 2. D'autres exemples d'1H MRS 24-26 et 27 DTI résultats peuvent être vus dans nos précédentes publications. Exemples de préinjection T 2 * IRM pondérée avec une superposition de l'emplacement des cellules marquées en jaune est montré dans la figure 3. La souris avait étiqueté les monocytes macrophages dérivés injectée dans la veine de la queue. Cinq jours plus tard, T 2 * IRM pondérée a été acquise et traitée comme décrit ci-dessus. La souris a été préparé par l'injection de macrophages humains infectés par le VIH dans le cerveau, ce qui est considéré comme une ligne de monocytes de souris détectée macrophages dérivés. D'autres exemples de détection des deux cellules marquées et coregistration l'histologie peut être vu dans nos publications antérieures 10,12.
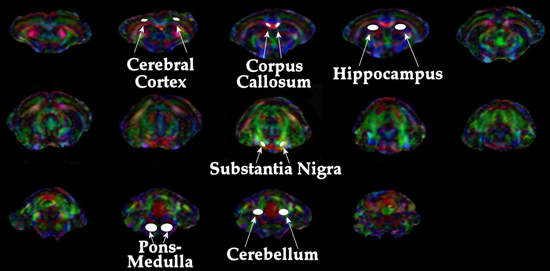
Figure 1. Représentation des régions analysées pour les métriques DTI.
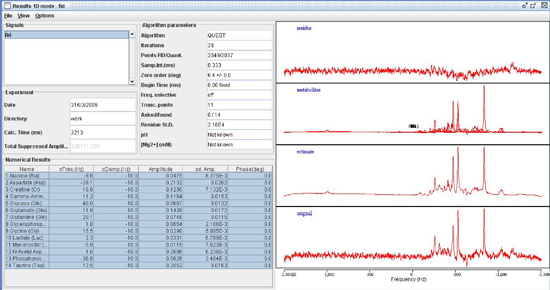
Figure 2. Montage spectroscopique utilisant QUEST dans la suite jMRUI traitement du signal.
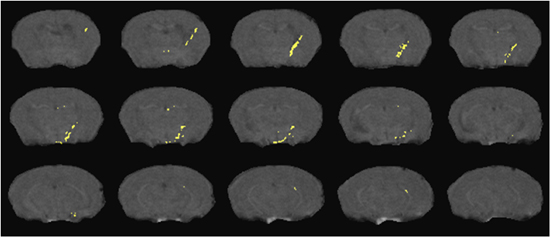
Figure 3. Détection de cellules étiquetées SPIO migrer du sang périphérique dans une région du cerveau avec une encéphalite focale. Positions cellulaire (jaune) tranches représentant superposition d'un T 2 * l'acquisition IRM pondérée comme détaillé dans le texte.
Discussion
L'enregistrement précis de l'histologie avec des résultats d'imagerie in vivo est une étape critique dans le développement de biomarqueurs d'imagerie pour la détection et à la tenue d'une maladie neuronale. Certaines mesures d'imagerie sont susceptibles d'être corrélés avec les changements morphologiques brute, y compris les changements dans les propriétés de relaxation magnétique des tissus utilisés pour détecter la présence de la maladie de la substance blanche et des cancers. D'autres méthodes plus subtiles, telles que le DTI, sont susceptibles de détecter les premiers changements cellulaires qui peuvent ne pas être détectable que des modifications histologiques causés par la maladie n'apparaissent que plus tard, les stades de la maladie. Marqueurs autres encore, tels que les marqueurs spectroscopiques, peuvent être des indicateurs de changements précoces et réversibles, qui précèdent, même les plus subtiles altérations cellulaires.
Biodistribution peut être déterminée de façon non invasive utilisant une variété de méthodes. La première des méthodes non invasives sont la tomographie par émission de positons (TEP), la tomographie d'émission (SPECT), l'imagerie optique et IRM. La médecine nucléaire basée imagerie (PET et SPECT) ont été utilisés au fil des ans pour la biodistribution de nombreux, mais ces méthodes sont limitées par la demi-vie de l'radiotraceurs utilisés pour l'étiquetage des composés ou des nanomatériaux, en particulier pour les traceurs TEP. L'imagerie optique peut être utilisé pour les petits rongeurs, mais ne peuvent pas être traduits à l'utilisation humaine à l'exception des régions facilement accessibles tels que les tumeurs de surface due à l'absorption de lumière et de diffusion de la lumière. En outre, il est difficile de quantifier les signaux optiques pour ces mêmes raisons. L'IRM utilise les balises persistants tels que SPIO qui peuvent être suivis dans le corps au cours d'une période de plusieurs semaines. Cela, aussi, doit être utilisé avec prudence, car l'étiquette peut être transférée à des cellules différentes ou être réabsorbé par le corps.
La spécificité de détection pour SPIO en IRM peuvent être fournis par une variété de méthodes. Les méthodes de détection, qui fournissent des signaux positifs que négatifs, sont utilisés pour améliorer la spécificité de l'IRM pour la détection de la présence de SPIO dans les tissus. La méthode de soustraction utilisée dans ce travail a été utilisé par d'autres, ainsi que 28. D'autres approches incluent la détection hors 29-31 résonance, la phase d'imagerie sensible qui produit un schéma particulier près vides SPIO 32, et zéro l'image temps d'écho qui utilise pondération T1 à produire une intensité de signal positif dans la région de SPIO 33. L'avancement de ces méthodes pour améliorer la quantification des étiquettes, la sensibilité et la spécificité est un domaine de recherche active d'aujourd'hui.
Déclarations de divulgation
Remerciements
Le travail a été soutenu par des subventions 1K25MH089851, 1P01DA028555-01A1, 2R01 NS034239, 2R37 NS36126, P01 NS31492, P20RR 15635, P01MH64570 et P01 NS43985 de la National Institutes of Health. Les auteurs remercient Mme Robin Taylor pour la lecture critique du manuscrit et un support exceptionnel des graphiques et littéraires. Les auteurs tiennent également à remercier Erin McIntyre, Melissa Mellon, et Lindsay Rice, pour leur soutien technique.
matériels
| Name | Company | Catalog Number | Comments |
| Isoflurane | |||
| Medical Oxygen | |||
| Isoflurane vaporizer | |||
| Rodent gas anesthesia mask | |||
| MRI compatible Stereotactic head holder | |||
| Syringe | |||
| Polyethylene catheter tubing | |||
| Non-magnetic needle | |||
| Eye lubricant | |||
| Gauze | |||
| Tape | |||
| Perfusion media | |||
| OCT compound for embedding tissue | |||
| MRI system | |||
| Digital Camera | |||
| Tissue Sectioning Cryostat |
Références
- Nowacek, A., Gendelman, H. E. NanoART neuroAIDS and CNS drug delivery. Nanomedicine (Lond). 4, 557-574 (2009).
- Nowacek, A., Kosloski, L. M., Gendelman, H. E. Neurodegenerative disorders and nanoformulated drug development. Nanomedicine (Lond). 4, 541-555 (2009).
- Nowacek, A. S., Miller, R. L., McMillan, J. NanoART synthesis, characterization, uptake, release and toxicology for human monocyte-macrophage drug delivery. Nanomedicine (Lond). 4, 903-917 (2009).
- Herbein, G., Varin, A. The macrophage in HIV-1 infection: from activation to deactivation. Retrovirology. 7, 33-33 (2010).
- Qian, B. Z., Pollard, J. W. Macrophage diversity enhances tumor progression and metastasis. Cell. 141, 39-51 (2010).
- Nathan, C., Ding, A. Nonresolving inflammation. Cell. 140, 871-882 (2010).
- McNeill, E., Channon, K. M., Greaves, D. R. Inflammatory cell recruitment in cardiovascular disease: murine models and potential clinical applications. Clin Sci (Lond). 118, 641-655 (2010).
- Bondeson, J. Activated synovial macrophages as targets for osteoarthritis drug therapy. Curr Drug Targets. 11, 576-585 (2010).
- Benoit, L. A., Holtzman, M. J. New immune pathways from chronic post-viral lung disease. Ann N Y Acad Sci. 1183, 195-210 (2010).
- Beduneau, A., Ma, Z., Grotepas, C. B. Facilitated monocyte-macrophage uptake and tissue distribution of superparmagnetic iron-oxide nanoparticles. PLoS One. 4, e4343-e4343 (2009).
- Dou, H., Grotepas, C. B., McMillan, J. M. Macrophage delivery of nanoformulated antiretroviral drug to the brain in a murine model of neuroAIDS. J Immunol. 183, 661-669 (2009).
- Liu, Y., Uberti, M. G., Dou, H. Ingress of blood-borne macrophages across the blood-brain barrier in murine HIV-1 encephalitis. J Neuroimmunol. 200, 41-52 (2008).
- Hetherington, H. P., Chu, W. J., Gonen, O., Pan, J. W. Robust fully automated shimming of the human brain for high-field 1H spectroscopic imaging. Magn Reson Med. 56, 26-33 (2006).
- Hasan, K. M., Parker, D. L., Alexander, A. L. Comparison of gradient encoding schemes for diffusion-tensor MRI. J Magn Reson Imaging. 13, 769-780 (2001).
- Hasan, K. M., Basser, P. J., Parker, D. L., Alexander, A. L. Analytical computation of the eigenvalues and eigenvectors in DT-MRI. J Magn Reson. 152, 41-47 (2001).
- Neeman, M., Freyer, J. P., Sillerud, L. O. A simple method for obtaining cross-term-free images for diffusion anisotropy studies in NMR microimaging. Magn Reson Med. 21, 138-143 (1991).
- Uberti, M. G., Boska, M. D., Liu, Y. A semi-automatic image segmentation method for extraction of brain volume from in vivo mouse head magnetic resonance imaging using Constraint Level Sets. J of Neurosci Methods. 179, 338-344 (2009).
- Liu, Y., Uberti, M. G., Dou, H., Mosley, R. L., Gendelman, H. E., Boska, M. D. An Image Warping Technique for Rodent Brain MRI-Histology Registration Based On Thin-Plate Splines with Landmark Optimization. Proc Soc Photo Opt Instrum Eng. 7259, 72592-K-72597-K (2009).
- Uberti, M. G., Liu, Y., Dou, H., Mosley, R. L., Gendelman, H. E., Boska, M. Registration of in vivo MR to histology of rodent brains using blockface imaging. Proc Soc Photo Opt Instrum Eng. 7262, 726213-726213 (2009).
- Basser, P. J., Mattiello, J., LeBihan, D. Estimation of the effective self-diffusion tensor from the NMR spin echo. J Magn Reson B. 103, 247-254 (1994).
- Hasan, K. M., Narayana, P. A. Retrospective measurement of the diffusion tensor eigenvalues from diffusion anisotropy and mean diffusivity in DTI. Magn Reson Med. 56, 130-137 (2006).
- Ratiney, H., Sdika, M., Coenradie, Y., Cavassila, S., Ormondt, D. v. a. n., Graveron-Demilly, D. Time-domain semi-parametric estimation based on a metabolite basis set. NMR Biomed. 18, 1-13 (2005).
- Naressi, A., Couturier, C., Castang, I., Beer, R. d. e., Graveron-Demilly, D. Java-based graphical user interface for MRUI, a software package for quantitation of in vivo/medical magnetic resonance spectroscopy signals. Comput Biol Med. 31, 269-286 (2001).
- Boska, L. e. w. i. s., Destache, T. B., J, C. Quantitative 1H magnetic resonance spectroscopic imaging determines therapeutic immunization efficacy in an animal model of Parkinson's disease. J Neurosci. 25, 1691-1700 (2005).
- Mosley, R. L., Benner, E. J., Kadiu, I. Neuroinflammation, Oxidative Stress and the Pathogenesis of Parkinson's Disease. Clin Neurosci Res. 6, 261-281 (2006).
- Nelson, J. A., Dou, H., Ellison, B. Coregistration of quantitative proton magnetic resonance spectroscopic imaging with neuropathological and neurophysiological analyses defines the extent of neuronal impairments in murine human immunodeficiency virus type-1 encephalitis. J Neurosci Res. 80, 562-575 (2005).
- Boska, H. a. s. a. n., Kibuule, K. M., D, . Quantitative diffusion tensor imaging detects dopaminergic neuronal degeneration in a murine model of Parkinson's disease. Neurobiol Dis. 26, 590-596 (2007).
- Liu, W., Frank, J. A. Detection and quantification of magnetically labeled cells by cellular MRI. Eur J Radiol. 70, 258-264 (2009).
- Balchandani, P., Yamada, M., Pauly, J., Yang, P., Spielman, D. Self-refocused spatial-spectral pulse for positive contrast imaging of cells labeled with SPIO nanoparticles. Magn Reson Med. 62, 183-192 (2009).
- Stuber, M., Gilson, W. D., Schar, M. Positive contrast visualization of iron oxide-labeled stem cells using inversion-recovery with ON-resonant water suppression (IRON). Magn Reson Med. 58, 1072-1077 (2007).
- Suzuki, Y., Cunningham, C. H., Noguchi, K. In vivo serial evaluation of superparamagnetic iron-oxide labeled stem cells by off-resonance positive contrast. Magn Reson Med. 60, 1269-1275 (2008).
- Kim, Y. B., Bae, K. H., Yoo, S. S., Park, T. G., H, P. a. r. k. Positive contrast visualization for cellular magnetic resonance imaging using susceptibility-weighted echo-time encoding. Magn Reson Imaging. 27, 601-610 (2009).
- Zhou, R., Idiyatullin, D., Moeller, S. SWIFT detection of SPIO-labeled stem cells grafted in the myocardium. Magn Reson Med. 63, 1154-1161 .
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon