Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Préparation Facile de dérivés quinazoline 4-substitué
Dans cet article
Résumé
A protocol for facile preparation of 4-substituted quinazoline derivatives from 2-aminobenzophenones, thiourea and dimethyl sulfoxide is presented.
Résumé
Rapporté dans le présent document est une méthode très simple pour la préparation directe de dérivés de quinazoline 4-substitués à partir d'une réaction entre substitués 2-aminobenzophénones et thiourée en présence de diméthylsulfoxyde (DMSO). Ceci est un système de réaction complémentaire unique dans lequel la thiourée est soumis à une décomposition thermique pour former le carbodiimide et le sulfure d'hydrogène, où les anciens réagit avec le 2-aminobenzophénone pour former quatre-phenylquinazolin-2 (1H) -imine intermédiaire, tandis que le sulfure d'hydrogène réagit avec du DMSO pour donner méthanethiol ou une autre molécule contenant du soufre, qui fonctionne alors comme un agent réducteur pour réduire complémentaire 4-phenylquinazolin-2 (1H) -imine intermédiaire en 4-phényl-1,2-dihydroquinazolin-2-amine. Par la suite, l'élimination de l'ammoniac à partir de 4-phényl-1,2-dihydroquinazolin-2-amine donne substitué dérivé quinazoline. Cette réaction donne généralement de quinazoline en tant que produit unique résultant de 2-aminobenzophénone comme contrôlé par CG / SMl'analyse, le long avec une petite quantité de molécules contenant du soufre tels que le diméthyl disulfure de diméthyle trisulfure, etc. La réaction se termine habituellement en 4-6 heures à 160 ° C dans une petite échelle, mais peut durer plus de 24 heures lorsqu'elle est effectuée à grande échelle. Le produit de réaction peut être facilement purifié par lavage avec de l'eau hors du DMSO suivi par une Chromatographie sur colonne ou la chromatographie en couche mince.
Introduction
Quinazolines substituées comme un type unique d'hétérocycles, sont connues pour une variété d'activités biologiques, y compris les antibiotiques, une antidépresseur, anti-hypertensive 2 anti-inflammatoire 3,4, 3 antipaludéen, 5 et anti-tumorale, notamment 6 . Ce qui est quinazolines plus, 4-substitué, par exemple, 4-aryl-quinazolines, ayant une activité anti-Plasmodium 7 ont été reconnues comme des récepteurs du facteur de croissance épidermique (EGFR) des inhibiteurs de tyrosine kinase, 8 dépresseurs du SNC, 9 et des antibiotiques contre Staphylococcus résistant à la méthicilline aureus et résistant à la vancomycine Enterococcus faecalis. 10 en raison de son large spectre d'activités biologiques, procédés de synthèse pour quinazolines substituées ont été largement explorée. A titre d'exemple, plus de 25 procédés de synthèse ont déjà été rapportés pour la préparation de 4-phenylquinazolines. 11 Repprocédés repré- comprennent la formation de 4-phenylquinazolines de 2-aminobenzophénones et du formamide en présence d'éthérate de trifluorure de bore (BF 3 · Et 2 O) 12 ou de l'acide formique, 13 ou de la réaction des 2-aminobenzophénones de urotropine et du bromoacétate d'éthyle, ou 14 la réaction avec l'aldéhyde et l'acétate d'ammonium en présence d'un agent oxydant. 15
Différent des réactions ci-dessus en utilisant le réactif sensible à l'humidité (par exemple, BF 3 · Et 2 O) ou un réactif coûteux (par exemple, urotropine et du bromoacétate d'éthyle), un procédé facile et peut convertir 2-aminobenzophénones en 4-phenylquinazolines correspondant dans du diméthylsulfoxyde ( DMSO) en présence de thiourée a été explorée. Des études mécanistiques largement sur cette réaction indiquent qu'il est une réaction complémentaire dans laquelle la thiourée subit une décomposition thermique pour former le carbodiimide etsulfure d'hydrogène, où carbodiimide réagit avec la 2-aminobenzophénone pour former quatre-phenylquinazolin-2 (1H) -imine intermédiaire, tandis que le DMSO est utilisé non seulement en tant que solvant, mais également le réactif pour produire la réduction de réactif quand il réagit avec l'hydrogène sulfuré sulfure de (également résultant de la thiourée). Ensuite, les agents réducteurs contenant du soufre, de réduire le 4-phenylquinazolin-2 (1H) -imine intermédiaire pour former la 4-phényl-1,2-dihydroquinazolin-2-amine qui est soumis à l'élimination de l'ammoniac pour former quatre-phénylquinazoline. Cette réaction est habituellement effectuée à une température de 135 à 160 ° C, et peut être facilement réalisée au moyen d'un chauffage à bain d'huile traditionnels sur plaque chauffante ou sous irradiation de micro-ondes. Cette réaction est généralement illustré sur la Figure 1 ci-dessous.
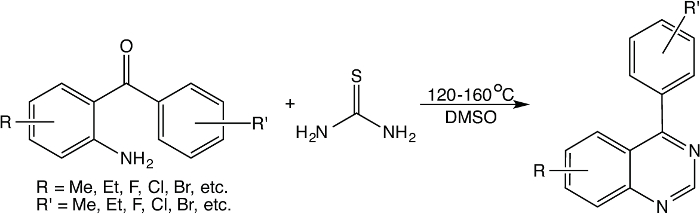
Figure 1: Une réaction générale entre 2-aminobenzophénone etthiourée dans le DMSO. S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.
Protocole
Attention: S'il vous plaît consulter toutes les fiches de données de sécurité des matériaux pertinents (FS) avant utilisation. Tandis que des 2-aminobenzophénones sont inodores, des molécules contenant du soufre sont produits dans cette réaction. Par conséquent, bon état de la ventilation doit toujours être utilisé. S'il vous plaît utiliser toutes les pratiques de sécurité approprié lors de l'exécution des réactions à la température supérieure à 140 ° C, la pression peut dépasser 5 bars, enregistrée sous irradiation micro-ondes. Lorsque la température est fixée à 160 ° C, la pression la plus élevée enregistrée est de 21 bars, ce qui est presque la limite supérieure du réacteur à micro-ondes peut gérer. Bien que la pression ne se pose pas lorsque la réaction est effectuée dans un bain d'huile sous reflux, une bonne ventilation doit toujours être utilisé.
1. Préparation de la 4-phénylquinazoline à petite échelle Sous Micro-ondes irradiation
- Préparation d'un mélange pour réaction
- Ajouter une barre d'agitation magnétique compatible avec un tube de réaction à micro-ondes 2-5 ml.
- Utilisez balance analytique et peser 0,0866 g de 2-aminobenzophénone (poudre jaune), 0,0988 g de thiourée (cristal blanc, 3 équivalents) dans le tube de réaction ci-dessus.
Remarque: Le rapport optimal entre 2-aminobenzophénone et la thiourée est de 1: 3. - Transfert 5 ml de DMSO dans le tube de réaction.
Remarque: La quantité de DMSO est assez souple, 5 ml de DMSO est juste assez pour répondre à l'exigence minimale de volume pour l'absorption correcte de micro-ondes selon le guide du fabricant. Toutefois, en vertu des conditions thermiques, il faut beaucoup moins de solvant pour la réaction de cette ampleur. - Scellez le tube de réaction avec une capsule en aluminium compatible contenant du caoutchouc admission à membrane.
- Agiter vigoureusement le tube sur un vortex pendant 1-2 min pour dissoudre les réactifs.
Remarque: Thiourea peut pas dissoudre complètement dans le DMSO à la température ambiante, mais il va se dissoudre complètement lorsque la chaleur est appliquée. - Utiliser une micro-seringue pour retirer 5 ul de mélange réactionnel à une 2 ml de verreÉCHANTILLONNAGE tube contenant 0,35 ml d'acétate d'éthyle (EtOAc) pour la chromatographie en phase gazeuse / spectrométrie de masse (GC / MS) d'analyse avant que la réaction commence.
- Formation de 4-phénylquinazoline Sous irradiation micro-ondes
- Allumez réacteur à micro-ondes, mettre le tube de réaction à micro-ondes dans l'un des supports de tubes huit.
- Paramètres de la réaction d'installation grâce à l'écran tactile, comme l'emplacement du tube (par exemple, à partir de puits 1 à 8), type de tube (par exemple, 2-5 ml), la température de réaction (à 150 ° C), la durée de pré-agitation (1 min), le niveau d'absorption de micro-ondes (haute), la vitesse d'agitation (600 rpm), et le temps de réaction (5 h).
- Une fois que tous les paramètres sont configurés correctement, cliquez sur le bouton "run", le robot va automatiquement chercher le tube de réaction du porte-tube (ou bien) et le mettre dans le trou de chauffage. Ensuite, le réacteur à micro-ondes se déroulera la réaction selon les paramètres définis précédemment.
- Lorsque l'irradiation de micro-ondes est terminée, wAttendez que la température tombe à près de 30 ° C, le robot va chercher le tube de réaction et de le remettre au détenteur initial.
- Utilisez micro-seringue pour prélever 5 pi de mélange réactionnel (solution jaune clair, pas de substance insoluble observé) et l'ajouter à un autre tube d'échantillonnage en verre de 2 ml contenant 0,35 ml de EtOAc pour l'analyse GC / MS.
- L'analyse CG / SM indique que la réaction est terminée seulement la moitié, mis en place la réaction à micro-ondes de la même tube pendant encore 5 heures à la même température.
Remarque: Le temps de réaction varie en fonction de la quantité de matière première utilisée, la concentration de la solution de réaction, les groupes substituants en 2-aminobenzophénones, et plus important encore, la température de réaction. Par exemple, une réaction de 0,3 g de 2-aminobenzophénone dans 3 ml de DMSO terminera en 6 heures à 160 ° C, mais dure plus de 14 heures à 140 ° C sous irradiation micro-ondes à la fois et le chauffage de la plaque chauffante. Il est également recommandé de surveiller la réaction périodiquement avec GC ou analyse CG / SM. Les personnes sans accès à GC ou GC / MS devraient alors utiliser la chromatographie sur couche mince (CCM) pour surveiller la réaction, bien qu'il soit pas le meilleur outil.
- GC / MS L'analyse du mélange réactionnel
- Assurez-vous que GC / MS est configuré correctement selon le protocole du fabricant.
- Mettre les tubes de prélèvement de verre sur le plateau échantillonneur automatique.
- Cliquez sur "GCMS_3" raccourci sur l'écran pour lancer le programme d'acquisition de données qui contrôle et coordonne les fonctions de l'injecteur, GC et spectromètre de masse. Charger une méthode appropriée en cliquant sur la "méthode" sur le menu déroulant et en sélectionnant «Méthode de charge." La méthode choisie contient tous les paramètres nécessaires à la fois pour GC et quadruple spectromètre de masse pour analyser les échantillons cibles. S'il n'y a pas une telle méthode, créer une méthode nécessaire.
- Pour un nouvel échantillon, si modifier certains des paramètres du GC pour convenir à un échantillon particulier, mettre en évidence le "Modifier entire Méthode "en cliquant sur" Méthode "du menu déroulant et modifier les paramètres pertinents en conséquence. Les paramètres de GC qui sont souvent modifiés sont la température initiale et la durée pour maintenir cette température, le taux d'augmentation de la température, la température finale et la durée pour maintenir la température, la quantité d'injection, le temps de laver l'aiguille d'injection avant et après l'injection, le temps d'équilibration et post exécution, et la température après l'exécution.
- Pour cette expérience, régler la température de GC initiale à 70 ° C (1 min), avec une vitesse d'augmentation de température à 20 ° C / min, et la température finale de 250 ° C (5 min). Utiliser une durée totale de 15 min. Utiliser un volume d'injection de 2 pl, avec 4 pré-lavage et 4 après-lavages de l'aiguille. Utiliser de l'hélium pur comme gaz porteur utilisé dans ces conditions.
Remarque: Une méthode pour l'analyse GC / MS contient les paramètres pré-établis afin de fonctionner à la fois GC et instruments MS. Les paramètres for GC comprennent la température initiale du four pour chauffer la colonne de GC et le nombre de minutes de conserver cette température, le taux d'élever la température du four, la température finale du four et le nombre de minutes de conserver la température finale avant la L'analyse GC se termine; la quantité d'échantillon injectée; le taux de division du gaz porteur; le nombre de fois pour laver l'aiguille avant que l'échantillon est injecté; et le nombre de fois pour laver l'aiguille après que l'échantillon est injecté, etc. Le choix des températures initiale et finale, ainsi que le taux d'élever la température dépend de la nature de l'échantillon analysé. D'une manière générale, des molécules non polaires de bas point d'ébullition sont analysés à température relativement basse initiale.
- Réglez le spectromètre de masse Selon le protocole du fabricant.
- Une fois une méthode de fonctionnement est sélectionné, cliquez sur "Instrument" au-dessus du menu déroulant, et sélectionnez "Tune MSD." Ensuite, une autre fenêtreapparaît en face de la fenêtre d'acquisition de données. On peut choisir soit «Tune MSD» ou «QuickTune", et cliquez sur le bouton "OK" pour démarrer le processus de réglage de spectromètre de masse. L'option "QuickTune" prend environ 3 min pour terminer, alors que l'option «Tune MSD" dure environ 10 min. Dans des circonstances normales, l'option "QuickTune" est assez bon pour calibrer le spectromètre de masse avec une précision allant jusqu'à 0,1 Dalton. Le processus de réglage permettra de mesurer l'abondance relative du pic 69, 219 et 502 de la perfluorotributylamine (PFTBA) ainsi que la quantité de N 2, O 2, H 2 O, CO 2, etc.
Remarque: Le spectromètre de masse doit être étalonné tous les deux jours afin d'avoir une mesure précise de la masse. L'accord est d'ajuster les paramètres pour le spectromètre de masse fonctionne correctement, telles que la tension de quadruple, vide de détecteur de masse, le bruit de fond, les sommets standard afin d'évaluer le spectromètre de masse,etc. On peut choisir soit autotune ou le mode de réglage manuel de calibrer le spectromètre de masse, soit en sélectionnant l'option «Tune MSD" "QuickTune" ou.
- Une fois une méthode de fonctionnement est sélectionné, cliquez sur "Instrument" au-dessus du menu déroulant, et sélectionnez "Tune MSD." Ensuite, une autre fenêtreapparaît en face de la fenêtre d'acquisition de données. On peut choisir soit «Tune MSD» ou «QuickTune", et cliquez sur le bouton "OK" pour démarrer le processus de réglage de spectromètre de masse. L'option "QuickTune" prend environ 3 min pour terminer, alors que l'option «Tune MSD" dure environ 10 min. Dans des circonstances normales, l'option "QuickTune" est assez bon pour calibrer le spectromètre de masse avec une précision allant jusqu'à 0,1 Dalton. Le processus de réglage permettra de mesurer l'abondance relative du pic 69, 219 et 502 de la perfluorotributylamine (PFTBA) ainsi que la quantité de N 2, O 2, H 2 O, CO 2, etc.
- Acquérir le MS GC / données
- Modifier la séquence d'acquisition de données. Cliquez sur le "Séquence" au-dessus du menu déroulant pour sélectionner "Séquence d'édition", et une nouvelle fenêtre apparaît, dans laquelle les informations sur les échantillons doit être entrée, tels que le type de l'échantillon (échantillon, blanc, l'étalonnage, QC , etc.), l'emplacement du flacon d'échantillon (de 1 à 100), le nom de l'échantillon, le nom du fichier de données, les commentaires de l'échantillon, etc. Lorsque toutes les informations échantillon a été entrée, cliquer sur le bouton "OK". Puis cliquez sur le "Séquence" au-dessus du menu déroulant pour sélectionner "Save Sequence sous .." et entrez le nom de la séquence dans un dossier approprié.
- Acquérir les données GC / MS. Cliquez sur le "Séquence" au-dessus du menu déroulant pour sélectionner "l'ordre d'exécution", choisissezun «répertoire des fichiers de données" appropriée pour enregistrer les données acquises, puis cliquez sur le bouton "ordre d'exécution" pour démarrer le processus d'acquisition de données.
- Analyser les GC / MS Résultats
Remarque: Les molécules peuvent être caractérisées par les minutes sont éluées de la colonne de GC, que l'on appelle le temps de rétention. Dans les mêmes conditions de GC (à savoir les paramètres de GC mentionnés ci-dessus), le temps de rétention d'une molécule particulière est très reproductible. Le composé peut être confirmée par son spectre de masse. On peut facilement identifier un composé en termes de temps de rétention et le spectre de masse, et de vérifier la pureté d'un composé ainsi.- Double cliquez sur le raccourci "GCMS_3 analyse des données" sur l'écran pour faire apparaître le logiciel qui traite délibérément les données acquises de la GC / MS machine.
- Au cours du processus d'acquisition de données, pour voir le résultat instantané de l'échantillon analysé, cliquez sur "Fichier" dans le menu déroulant et Highlig basht "prendre un instantané" pour obtenir le spectre de GC synchronisée de l'échantillon. Souvent, les gens vont traiter les données après le processus d'acquisition complète. Dans ce cas, cliquez sur "Fichier" dans le menu déroulant pour sélectionner "Fichier de données de charge" et sélectionnez le bon fichier de données, ou parcourir le répertoire de données et double cliquez sur le fichier de données, afin de montrer l'ensemble du spectre de l'échantillon de GC. Une ligne verticale apparaît à l'endroit où la souris est pointée vers l'intérieur de la fenêtre du spectre GC.
- Passez la souris au centre d'un pic où la ligne verticale frappe le point du pic le plus élevé, et double cliquez sur le bouton droit de la souris pour faire apparaître le spectre de masse de l'échantillon dans une nouvelle fenêtre ci-dessous la fenêtre du spectre GC. On peut agrandir le spectre de masse en maintenant le bouton gauche et sélectionnez la région pour agrandir pour le détail de spectre de masse.
- Identifier les composés par un double clic sur le bouton droit de la souris dans la fenêtre du spectre de masse pour obtenir deux nouvelles fenêtres. Le petitpare-brise avec un nom de "PBM Résultats de la recherche: C: Database W8N08.L" fait apparaître 20 molécules de la base de données qui correspondent probablement le spectre de masse analysé, et classe les 20 molécules dans l'ordre de leurs similitudes. La grande fenêtre arrière contient deux volets, dont le panneau supérieur affiche le spectre de masse initiale du pic analysé à l'intérieur du spectre de GC, et le panneau inférieur affiche le spectre de masse de la molécule sélectionnée dans la liste de la petite fenêtre avant. Souvent, les composés organiques courants peuvent être confirmée en comparant son spectre de masse avec le spectre de masse à collectées dans la base. Bien que les nouveaux composés ou des molécules non collectées dans la base de données ne peuvent pas être directement confirmées, leurs identités peuvent être obtenus grâce à la mise en correspondance d'un poids moléculaire prévu et fragments possibles avec leurs structures.
- Identifier le même composé dans différents échantillons en comparant son temps de rétention sur le spectre de GC. Dans les mêmes conditions d'acqu de donnéesisition, le même composé devrait apparaître avec le même temps de rétention sur le spectre de GC.
- Analyser la pureté de l'échantillon en cliquant sur le "Chromatogramme" sur le menu déroulant, en soulignant soit "Intégrer" ou "AutoIntegrate", et en sélectionnant "Pourcentage Rapport".
- Imprimer à la fois le spectre de GC et le spectre de masse correspondant aux pics à l'intérieur du spectre de GC en mode portrait ou paysage en sélectionnant "Configuration d'imprimante" quand un seul clic "Fichier" dans le menu déroulant. En outre, imprimer les spectres directement en format pdf en sélectionnant un convertisseur de pdf.
- Extraction du mélange réactionnel
Remarque: Le processus d'isolation a été réalisée dans une hotte, aussi petite quantité de molécules contenant du soufre avec odeur désagréable sont générés dans cette réaction.- Ouvrir le tube de réaction à micro-ondes avec le fabricant fourni pince, et transférer le mélange réactionnel dans un 125 ml ampoule à décanter. UNEjj 20 ml d'EtOAc à cet entonnoir suivis par 10 ml d'eau.
Remarque: Si la solution réactionnelle est laissée à température ambiante pendant un jour, longue aiguille cristaux de forme peut apparaître dans la solution en fonction de la concentration de la solution. Ainsi, il est sage de laisser le mélange de réaction à grande échelle à la température ambiante pour former cristal et isoler le produit des cristaux directement si le temps est pas un facteur. - Agiter l'ampoule à décanter énergiquement et drainer la couche aqueuse inférieure. Puis ajouter encore 10 ml d'eau pour l'ampoule à décanter, et répéter ce processus.
- Concentrer la solution EtOAc restant jusqu'à environ 1 ml par évaporation rotative.
- Ouvrir le tube de réaction à micro-ondes avec le fabricant fourni pince, et transférer le mélange réactionnel dans un 125 ml ampoule à décanter. UNEjj 20 ml d'EtOAc à cet entonnoir suivis par 10 ml d'eau.
- La purification du 4-phénylquinazoline par CCM preparative
- Transférer la solution concentrée avec de l'EtOAc à une pipette Pasteur 20 cm x 20 cm plaque de CCM preparative de telle sorte que la bande d'échantillon sur la plaque de CCM est inférieur à 1 cm de large et est d'environ 1 cm du bord. Trempez cette plaque à un glass chambre contenant 150 ml d'hexane et d'EtOAc (2: 1). Regardez le mouvement de frontière solvant approcher le haut de la plaque de CCM, et retirer la plaque lorsque frontière solvant est d'environ 1 cm du bord supérieur.
- Dessinez deux lignes droites sur la plaque TLC avec un crayon pour marquer l'endroit avant échantillon est chargé. En outre, tremper la plaque de CCM dans la chambre de verre de telle sorte que la bande d'échantillon se trouve en bas, mais encore d'environ 2 mm au-dessus du niveau du solvant.
- Sous ultra-violet (UV), utiliser un crayon pour marquer la bande avec la fluorescence verte, et gratter la bande marquée sur la plaque TLC à un papier de pesage (avec une mobilité relative de R f = 0,68, hexane / EtOAc = 2 :1).
Remarque: En raison de la sensibilité élevée de l'absorption UV, on peut observer plusieurs bandes faibles sur la plaque. Cependant, les bandes très haut correspondent souvent à des molécules contenant du soufre, tels que le disulfure de diméthyle, trisulfure de diméthyle; autres bandes au-dessous de 4 phénylquinazoline sont visible mais leur montant sont trop peu pour être isolé et caractérisé. - Pour une pipette en verre rempli de laine de verre, de transférer la poudre de gel de silice rayé à la pipette en pliant le papier pesant diagonale pour permettre à la poudre de gel de silice tombe dans la pipette, puis appuyez sur la pipette contre une surface dure pour emballer le gel de silice étanche . Laver la pipette avec de l'acétone (8-15 ml) dans un flacon à scintillation de 2-tambour.
- Transférer 0,35 ml de la solution d'acétone élue à un autre tube en verre d'échantillonnage de 2 ml pour une analyse GC / MS, directement et sécher la solution restante de l'acétone sur un évaporateur rotatif. Mettez toute la fiole à scintillation contenant le composé purifié dans un dessiccateur à vide pour un séchage supplémentaire.
Remarque: Jusqu'à cette étape, le produit est purifié et peut être utilisée pour une caractérisation plus poussée (par exemple, la résonance magnétique nucléaire (RMN)) ou des transformations supplémentaires.
- Transférer la solution concentrée avec de l'EtOAc à une pipette Pasteur 20 cm x 20 cm plaque de CCM preparative de telle sorte que la bande d'échantillon sur la plaque de CCM est inférieur à 1 cm de large et est d'environ 1 cm du bord. Trempez cette plaque à un glass chambre contenant 150 ml d'hexane et d'EtOAc (2: 1). Regardez le mouvement de frontière solvant approcher le haut de la plaque de CCM, et retirer la plaque lorsque frontière solvant est d'environ 1 cm du bord supérieur.
2. Préparation de la 4-phénylquinazoline in à petite échelle par l'intermédiaire Plaque chauffante chauffage
Remarque: Les procédures pour l'analyse GC / MS du mélange réactionnel, extraction du mélange réactionnel, et la purification des produits de réaction sont très similaires à ceux décrits dans la section 1 (1.1.1-1.3.4, 1.4.1-1.4.3 et 1.5.1-1.5.5, respectivement), de sorte que la plupart de ces étapes sera omise ci-après.
- Préparation d'un mélange réactionnel pour le chauffage de la plaque chauffante
- Peser 0,0240 g de 2-aminobenzophénone et 0,0280 g de thiourée dans un flacon de 2 ml en verre, puis de transférer 0,5 ml de DMSO à la même flacon, et fermer le flacon avec un bouchon à vis.
Remarque: La quantité de DMSO utilisée sous cette condition est bien inférieure à celle sous irradiation micro-ondes. En raison de petite échelle de cette réaction, l'agitation magnétique est pas plus nécessaire, donc pour l'agitation de la solution de vortex pour dissoudre les réactifs. Cependant, dans une échelle relative de réaction importante, par exemple, dans deux tambours flacon à scintillation ou un flacon à fond rond, sous agitation magnétiqueest encore nécessaire.
- Peser 0,0240 g de 2-aminobenzophénone et 0,0280 g de thiourée dans un flacon de 2 ml en verre, puis de transférer 0,5 ml de DMSO à la même flacon, et fermer le flacon avec un bouchon à vis.
- Préparation du 4-phénylquinazoline par chauffage Plaque
- Inside hotte, mettre un bloc de chauffage au-dessus de plaque de cuisson, et la température réglée à 160 ° C.
- Lorsque la température atteint 160 ° C, à insérer le flacon de verre dans l'un des puits dans le bloc chauffant. Avec environ une demi-heure d'intervalle, de prendre du flacon et de la main secouer pendant 2-3 sec, et le remettre au bien nouveau. Après 6 heures, sortir du flacon et de le laisser à l'intérieur de la hotte pour refroidir.
- Transfert 5 pi du mélange de réaction à un autre tube d'échantillonnage en verre de 2 ml contenant 0,35 ml de EtOAc, et soumettre l'échantillon à analyser GC / MS.
- Une fois la réaction terminée, travailler sur le produit tel que décrit dans l'article 1. Voir les détails dans la section 1.1.1-1.3.4, 1.4.1-1.4.3, et 1.5.1-1.5.5 pour analyse GC / MS, extraction du mélange réactionnel et la purification du produit, respectivement.
Résultats
L'analyse GC du mélange réactionnel avant la réaction, 5 heures après la réaction sous irradiation de micro-ondes, et 10 heures après la réaction sous irradiation de micro-ondes à 150 ° C sont présentés dans la figure 2, qui illustre bien le procédé de cette réaction sans solvant. Les spectres de masse de 2-aminobenzophénone et 4-phénylquinazoline sont présentés sur la figure 3 et la figure 4, respectivement. Un mé...
Discussion
Cette réaction de nettoyage (comme représenté sur la figure 2) apparaît très intéressante tant au début de la masse moléculaire du produit est augmenté de seulement 9 par rapport à celle du produit de départ (comme représenté sur la Figure 3 et la Figure 4). Cela semble impossible parce que le poids atomique du carbone est 12. Très probablement, l'introduction d'un atome de carbone dans une molécule va augmenter le poids moléculaire d'au moin...
Déclarations de divulgation
Except for the contents described in patent (pending), the authors have nothing else to disclose.
Remerciements
The financial support from the National Science Foundation (NSF, grant number 0958901), the Robert Welch Foundation (Welch departmental grant BC-0022 and the Principal Investigator grant BC-1586), and the University of Houston-Clear Lake (FRSF grant) are greatly appreciated.
matériels
| Name | Company | Catalog Number | Comments |
| 2-Aminobenzophenone | Alfa Aesar | A12580 | 98% purity, with tiny impurity as seen on Figure 1(A) in the manuscript. |
| Thiourea | Acros | 138910010 | 1 kg package, 99%, extra pure |
| Dimethyl Sulfoxide | Acros | 326880010 | Methyl sulfoxide, 99.7+%, Extra Dry, AcroSeal® |
| N,N-Dimethylformamide | Acros | 348430010 | N,N-Dimethylformamide, 99.8%, Extra Dry over Molecular Sieve, AcroSeal® |
| Ethyl Acetate | Acros | 610170040 | Ethyl acetate, used as solvent for GC/MS analysis |
| Preparative TLC plate | Sigma-Aldrich | Z740216 SIGMA | PTLC (Preparative TLC) Glass Plates from EMD/Merck KGaA |
| Rotavapor | Buchi | Rotavapor R-205 | Use to dry solvent |
| Microwave Reactor | Biotage | Initiator+ | Use to carry out chemical reaction under microwave irradiation |
| Hotplate | IKA | RCT basic | use to carry out thermal chemical reaction |
Références
- Kamal, A., Reddy, K. L., Devaiah, V., Shankaraiah, N., Rao, M. V. Recent Advances in the Solid-Phase Combinatorial Synthetic Strategies for the Quinoxaline, Quinazoline and Benzimidazole Based Privileged Structures. Mini-Rev. Med. Chem. 6 (1), 71-89 (2006).
- Spirkova, K., Stankovsky, S. Some Tricyclic Annelated Quinazolines. Khim. Geterotsikl. Soedin. (10), 1388-1389 (1995).
- Connolly, D. J., Cusack, D., O'Sullivan, T. P., Guiry, P. J. Synthesis of Quinazolinones and Quinazolines. Tetrahedron. 61 (43), 10153-10202 (2005).
- Baba, A., et al. Studies on Disease-Modifying Antirheumatic Drugs: Synthesis of Novel Quinoline and Quinazoline Derivatives and Their Anti-Inflammatory Effect. J. Med. Chem. 39 (26), 5176-5182 (1996).
- Gama, Y., Shibuya, I., Simizu, M. Novel and Efficient Synthesis of 4-Dimethylamino-2-Glycosylaminoquinazolines by Cyclodesulfurization of Glycosyl Thioureas with Dimethylcyanamide. Chem. Pharm. Bull. 50 (11), 1517-1519 (2002).
- Wakeling, A. E., et al. Specific Inhibition of Epidermal Growth Factor Receptor Tyrosine Kinase by 4-Anilinoquinazolines. Breast Cancer Res Treat. 38 (1), 67-73 (1996).
- Verhaeghe, P., et al. Synthesis and Antiplasmodial Activity of New 4-Aryl-2-Trichloromethylquinazolines. Bioorg. Med. Chem. Lett. 18 (1), 396-401 (2008).
- Kitano, Y., Suzuki, T., Kawahara, E., Yamazaki, T. Synthesis and Inhibitory Activity of 4-Alkynyl and 4-Alkenylquinazolines: Identification of New Scaffolds for Potent Egfr Tyrosine Kinase Inhibitors. Bioorg. Med. Chem. Lett. 17 (21), 5863-5867 (2007).
- Goel, R. K., Kumar, V., Mahajan, M. P. Quinazolines Revisited: Search for Novel Anxiolytic and Gabaergic Agents. Bioorg. Med. Chem. Lett. 15 (8), 2145-2148 (2005).
- Parhi, A. K., et al. Antibacterial Activity of Quinoxalines, Quinazolines, and 1,5-Naphthyridines. Bioorg. Med. Chem. Lett. 23 (17), 4968-4974 (2013).
- Brown, D. J. . Chemistry of Heterocyclic Compounds, Volume 55: Quinazolines, Supplement I. , (1996).
- Yang, C. -. H., et al. Color Tuning of Iridium Complexes for Organic Light-Emitting Diodes: The Electronegative Effect and -Conjugation Effect. J. Organomet. Chem. 691 (12), 2767-2773 (2006).
- Byford, A., Goadby, P., Hooper, M., Kamath, H. V., Kulkarni, S. N. O-Aminophenyl Alkyl/Aralkyl Ketones and Their Derivatives. Part V. An Efficient Synthetic Route to Some Biologically Active 4-Substituted Quinazolines. Ind. J. Chem. B. 27 (4), 396-397 (1988).
- Blazevic, N., Oklobdzija, M., Sunjic, V., Kajfez, F., Kolbah, D. New Ring Closures of Quinazoline Derivatives by Hexamine. Acta Pharmaceut. Jugo. 25 (4), 223-230 (1975).
- Panja, S. K., Saha, S. Recyclable, Magnetic Ionic Liquid Bmim[Fecl4]-Catalyzed, Multicomponent, Solvent-Free, Green Synthesis of Quinazolines. RSC Adv. 3 (34), 14495-14500 (2013).
- Wang, Z. D., Eilander, J., Yoshida, M., Wang, T. Mechanistic Study of a Complementary Reaction System That Easily Affords Quinazoline and Perimidine Derivatives. Eur. J. Org. Chem. (34), 7664-7674 (2014).
- Wang, D. Z., Yoshida, M., George, B. Theoretical Study on the Thermal Decomposition of Thiourea. Comput. Theoret. Chem. 1017, 91-98 (2013).
- Zhang, P., et al. Inhibitory Effect of Hydrogen Sulfide on Ozone-Induced Airway Inflammation, Oxidative Stress, and Bronchial Hyperresponsiveness. Am. J. Respir. Cell Mol. Biol. 52 (1), 129-137 (2015).
- Yan, J., et al. One-Pot Synthesis of Cdxzn1-Xs-Reduced Graphene Oxide Nanocomposites with Improved Photoelectrochemical Performance for Selective Determination of Cu2+. RSC Adv. 3 (34), 14451-14457 (2013).
- Keith, J. D., Pacey, G. E., Cotruvo, J. A., Gordon, G. Experimental Results from the Reaction of Bromate Ion with Synthetic and Real Gastric Juices. Toxicology. 221 (2-3), 225-228 (2006).
- Timchenko, V. P., Novozhilov, A. L., Slepysheva, O. A. Kinetics of Thermal Decomposition of Thiourea. Russ. J. Gen. Chem. 74 (7), 1046-1050 (2004).
- Wang, S., Gao, Q., Wang, J. Thermodynamic Analysis of Decomposition of Thiourea and Thiourea Oxides. J. Phys. Chem. B. 109 (36), 17281-17289 (2005).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon