Method Article
Réhabilitation motrice structurée après transferts sélectifs de nerf
Dans cet article
Résumé
Ici, nous présentons un protocole pour la réadaptation motrice des patients présentant des dommages graves de nerf et la chirurgie sélective de transfert de nerf. Il vise à restaurer la fonction motrice en proposant plusieurs étapes dans l'éducation des patients, la thérapie de stade précoce après la chirurgie et les interventions pour la réadaptation après la ré-innervation réussie de la cible du nerf.
Résumé
Après des lésions nerveuses graves, les transferts sélectifs de nerf fournissent une occasion de reconstituer la fonction motrice et sensorielle. La récupération fonctionnelle dépend à la fois de la ré-innervation réussie des cibles dans la périphérie et du processus de réapprentissage moteur impliquant la plasticité corticale. Bien qu'il existe un nombre croissant de méthodes pour améliorer la réadaptation, leur mise en œuvre systématique en milieu clinique demeure un défi en raison de leur complexité et de leur longue durée. Par conséquent, des recommandations pour des stratégies de réadaptation sont présentées dans le but de guider les médecins et les thérapeutes à travers le processus de réadaptation à long terme et de fournir des instructions étape par étape pour soutenir le réapprentissage moteur.
Directement après la chirurgie de transfert de nerf, aucune fonction motrice n'est présente, et la thérapie devrait se concentrer sur la promotion de l'activité dans les secteurs sensoriel-moteurs de cortex de la partie paralysée de corps. Après environ deux à six mois (selon la gravité et la modalité des blessures, la distance de régénération nerveuse et de nombreux autres facteurs), la première activité motrice peut être détectée par électromyographie (EMG). Dans cette phase de réadaptation, la rétroaction multimodale est utilisée pour réapprendre la fonction motrice. Ceci est particulièrement critique après les transferts de nerf, car les modèles d'activation de muscle changent dû à la connexion neurale altérée. Enfin, la force musculaire devrait être suffisante pour surmonter la gravité / résistance des muscles antagonistes et la raideur articulaire, et des tâches plus fonctionnelles peuvent être mises en œuvre dans la réadaptation.
Introduction
Les transferts sélectifs de nerf fournissent une occasion pour reconstituer la fonction de moteur après des dommages de nerf quand la récupération par l'utilisation de la neurolyse, la réparation de nerf, ou la greffe de nerf ne peut pas s'attendre1,2. Les indications possibles pour des transferts de nerf sont des dommages distales graves de nerf, des dommages avulsion-type, le manque des racines nerveuses disponibles pour la greffe, les cicatrices étendues au site de blessure et la reconstruction retardée3,4. Après la blessure de nerf moteur, la reconstruction est time-critical car la dégénérescence du tissu de muscle et des plaques d'extrémité de moteur permettent seulement la re-innervation réussie de muscle dans 1-2 ans après blessure5,6. Ici, les transferts de nerf s'offrent l'avantage d'un temps de réinnervation relativement court après la chirurgie, car ils permettent la coaptation nerveuse près de la cible. Cette procédure, également connue sous le nom de neurotisation, implique la redirection chirurgicale d'un nerf intact (nerf de distributeur) à la partie distale du nerf receveur. Comme cette connexion est distale au site endommagé du nerf receveur, elle permet de contourner le segment nerveux blessé7.
Comme les voies neurales sont modifiées après la chirurgie de transfert de nerf, les patients ne peuvent pas être traités avec les protocoles postopératoires standard de thérapie autrement employés après réparation directedenerf 8,9. Tandis que les axones de distributeur se développent dans la nouvelle cible, ils prennent en charge une fonction qu'ils n'ont pas euavant tandis que cortically toujours étant relié à leur fonction originale. Par exemple, le transfert de nerf ulnaire Oberlin est utilisé pour restaurer la flexion du coude après des dommages irréparables au tronc supérieur ou aux racines nerveuses C5 et C61. Comme le montre la figure 1, il s'agit de transférer un ou plusieurs fascicles du nerf ulnaire à la branche motrice musculo-cutanée du muscle du biceps10. Cependant, après la re-innervation réussie, ces fascicles du nerf ulnaire sont cortiquement toujours liés à leur fonction précédente de flexion de doigt et/ou d'enlèvement et de flexion ulnaire du poignet. Sur le plan fonctionnel, cela implique qu'au début de la réadaptation, le patient doit se concentrer sur la fonction nerveuse précédente (fermeture de la main) afin d'activer et de renforcer le muscle receveur (contraction du biceps). Cette approche est également connue sous le nom d'« approche de réadaptation axée sur l'activation des donneurs »9.
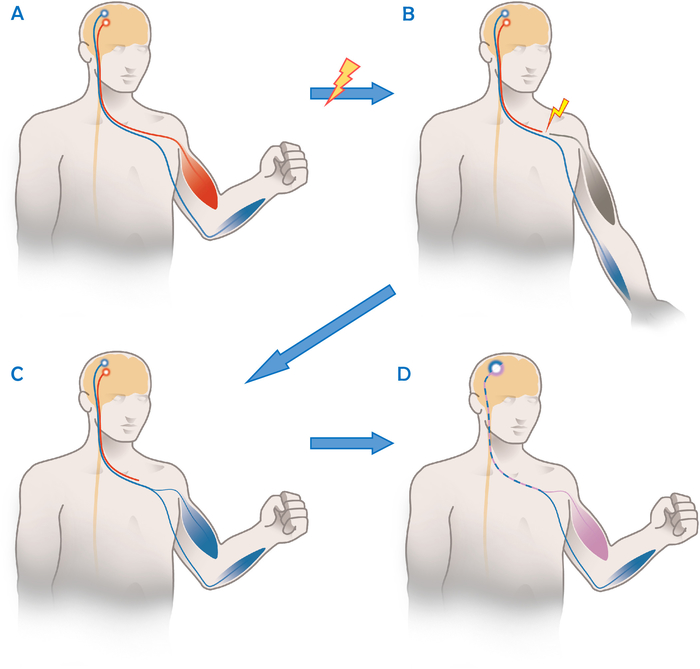
Figure 1 : Illustration schématique du principe fonctionnel d'un transfert de nerf ulnaire à musculocutané. (A) Chez une personne en bonne santé, il y a une séparation claire entre l'activité dans le cortex moteur pour les fonctions de différents nerfs/articulations comme ici le nerf musculo-cutané (rouge) et le nerf ulnaire (bleu). (B) Après une blessure du nerf musculo-cutané, le muscle du biceps ne peut pas être activé, tandis que le nerf ulnaire non blessé (en bleu) fonctionne toujours. (C). Après le transfert et la réinnervation du nerf de l'Oberlin, les fascicles du nerf ulnaire contrôlent les muscles du biceps ainsi que tous les autres muscles anatomiquement innervés par le nerf ulnaire. Avant la réorganisation corticale se produit, les deux muscles sont activés ensemble car il n'y a pas de séparation corticale entre ces fibres nerveuses (en bleu). (D) Avec la réadaptation réussie, le patient a appris à employer certains axones corticaux pour les fonctions « normales » de nerf ulnaire (en bleu), alors que d'autres (en pourpre) contrôlent maintenant le muscle de biceps. Cela permet un mouvement indépendant des deux groupes musculaires. Veuillez cliquer ici pour voir une version plus grande de ce chiffre.
Bien que la compréhension de ce concept soit le fondement d'une réadaptation réussie, le réapprentissage de nouveaux modèles moteurs peut être difficile pour les patients et les cliniciens. Ceci est dû à la longue durée de la réadaptation, à la complexité de la régénération et de la réinnervation des nerfs et à la quantité limitée d'activité musculaire directement observable pendant la réinnervation précoce8. Outre les changements dans le système nerveux périphérique, les chirurgiens et les thérapeutes sont de plus en plus sensibilisés à la pertinence des changements dans le système nerveux central (SNC), c'est-à-d. la réorganisation du moteur manuel et des zones corticales sensorielles conséquence de la dénervation11. Lorsque l'entrée neuronale au SNC est privée, la zone corticale associée diminue dans une certaine mesure au détriment des zones adjacentes12. La restauration de la fonction dépend donc de la récupération centrale de sa représentation dans le cerveau. Au cours des dernières années, l'utilisation des méthodes de biofeedback8 et des approches pour soutenir la réorganisation corticale13,14,15 a conduit à des possibilités étendues dans la réadaptation après les transferts de nerfs. Cependant, en raison de la complexité de la thérapie post-chirurgicale, il est important de fournir les bonnes interventions au bon moment13.
Par conséquent, l'objectif de ce protocole structuré pour la réadaptation après transferts sélectifs de nerf est de fournir une approche faisable et holistique pour soutenir la récupération de moteur. Il est basé sur les recommandations actuelles et l'expérience des auteurs avec son intégration dans un cadre clinique. Le protocole vise à guider les médecins, les ergothérapeutes et les physiothérapeutes ainsi que d'autres professionnels de la santé tout au long du processus de réadaptation durable.
Ce protocole structuré pour la réadaptation motrice a été évalué dans une étude de faisabilité8 dans cinq patients présentant des dommages brachial de plexus comme indiqué dans le tableau1. Tous ont reçu plusieurs transferts de nerf (certains en combination avec des greffes de nerf) pour reconstituer la fonction supérieure d'extrémité. Par conséquent, par souci de clarté, lorsqu'ils décrivent des interventions spécifiques dans ce protocole, ils se réfèrent au membre supérieur. Dans le détail, nous prenons le transfert de nerf ulnaire d'Oberlin10 comme exemple, qui a été exécuté dans les patients 1-3. Pour cela, nous nous référons à des parties du nerf ulnaire comme étant le nerf du donneur et le nerf musculo-cutané étant le nerf receveur. Ainsi, les muscles du biceps et de la brachialis sont les muscles receveurs qui sont réinnervés par des parties du nerf ulnaire. Fonctionnellement, cela signifie qu'à la suite d'une activation du donneur axée approche9, mouvements associés à l'activité nerveuse ulnaire (comme la fermeture des mains ou l'enlèvement ulnaire du poignet) sont utilisés pour l'activation du muscle du biceps directement après ré-innervation. Cependant, des exercices basés sur cette approche peuvent être effectués dans d'autres parties du corps ainsi. Si des considérations spéciales sont nécessaires pour mettre en œuvre cela dans d'autres parties du corps (par exemple, l'extrémité inférieure), cela est souligné dans le protocole.
Indépendamment de la partie du corps affectée, les séances de thérapie ne devraient pas dépasser 30 min car les muscles deviennent facilement fatigués peu de temps après la ré-innervation8 et la formation réussie exige l'engagement et la concentration complètes d'un patient.
Protocole
L'étude a été approuvée par le comité local d'éthique de la recherche (numéro: 1009/2014) et réalisée conformément à la Déclaration d'Helsinki. Tous les patients ont fourni le consentement éclairé écrit pour participer à cette étude.
1. Éducation des patients
-
En dépit de n'importe quelle information précédente donnée au patient, employer la première séance post-chirurgicale de consultation/thérapie pour expliquer en détail le type de blessure, aussi bien que la chirurgie exécutée.
- Visualisez les transferts de nerfs, qui ont été effectués, sur un schéma ou une impression à partir d'une figure d'anatomie.
- Expliquez comment la voie neuronale altérée exige d'abord de penser au modèle de mouvement original d'un nerf.
- Donnez au patient un plan de réadaptation approximative et une idée des résultats qui pourraient être réalistes à quel moment.
- Si le patient souffre des conséquences négatives de la blessure sur un niveau psychologique16,17 ou a besoin de soutien pour faire face au stress ou à la douleur, contactez un psychologue.
-
Demandez au patient d'expliquer l'impact des transferts de nerfs dans ses propres mots pour savoir comment il a compris le concept.
- Si nécessaire, répétez certaines explications et répondez à des questions ouvertes.
- Si l'établissement de réadaptation dispose d'un dépliant commettant les faits les plus importants, remettez-le au patient (voir Le dossier supplémentaire par exemple).
-
Discutez d'un programme à domicile avec le patient.
- Expliquez qu'une fréquence élevée de formation est importante pour de bons résultats, et donc les exercices à domicile font partie intégrante de la réadaptation.
- Discutez avec le patient de la façon dont il pense que cela peut être mieux abordé. Ainsi, donner au patient le pouvoir d'assumer la responsabilité de sa propre réadaptation.
- Distribuez le programme d'exercices à domicile discuté sous une forme écrite. Assurez-vous qu'il ne contient que des exercices qui ont déjà été effectués au cours d'une séance de thérapie.
- Afin de préserver l'observance au fil du temps, demandez régulièrement au patient ce qu'il ressent au sujet du programme à domicile et discutez de la façon dont il devrait être modifié pour être faisable et significatif pour le patient.
2. Amélioration de la re-présentation corticale de la partie du corps Denervated
REMARQUE: Les techniques de réadaptation suivantes favorisent l'activation du moteur denervated et des secteurs corticaux sensoriels pour regagner la représentation corticale de la partie paralysée de corps. Pendant cette phase, aucune contraction musculaire active n'est possible.
- Suivre une approche pour la formation de latéralisation (discrimination gauche/droite) telle que décrite par Mosely et coll.18.
- Préparer les cartes montrant les extrémités gauche et droite dans un ordre aléatoire (extrémité supérieure, si l'extrémité supérieure est affectée et l'extrémité inférieure pour les lésions nerveuses des extrémités inférieures). Montrez-les au patient dans un ordre aléatoire.
- Demandez au patient si une extrémité gauche ou droite est montrée. Alors que la vitesse d'environ 2 s / carte est normale18, donner au patient au moins 15 s pour répondre, si nécessaire.
- Donnez au patient la rétroaction, et si nécessaire, le temps de comprendre pourquoi la réponse était mauvaise.
- Faites-le pendant 5 à 10 min pour éviter la fatigue. Demandez au patient de le faire à la maison ainsi, deux fois par jour pendant 5-10 min.
- Instruisez le patient à imaginer les mouvements de la partie du corps paralysée, bien qu'aucune sortie motrice ne soit prévue.
- Assurez-vous que le patient est dans un environnement calme sans aucune distraction.
- Demandez au patient quels mouvements de l'extrémité paralysée sont faciles à imaginer.
- Instruisez le patient à imaginer ces mouvements pendant environ 5 minutes avec le moment exact en fonction de la capacité du patient à se concentrer pleinement sur ces mouvements imaginés.
- Dans le processus de traitement, demandez au patient d'imaginer des mouvements plus complexes ainsi.
- Comme un exercice à domicile, demandez au patient d'imaginer ces mouvements 5 à 10 min, deux fois par jour.
- Utilisez la thérapie miroir pour créer l'illusion du mouvement actif de la partie paralysée19,20.
- Placez un miroir debout ou une boîte miroir devant le thérapeute et le patient. Placez-le sur un bureau pour l'extrémité supérieure ou sur le sol pour l'extrémité inférieure.
- Expliquez que la thérapie de miroir fonctionne en faisant usage de la réflexion du côté sonore pour créer l'image du mouvement simultané du côté sonore et de l'extrémité dénervated19,21. Démontrer rapidement cela avec l'extrémité supérieure ou inférieure du thérapeute.
- Placez le miroir médially en face du patient d'une manière qu'il / elle voit le reflet du côté sonore exactement où l'extrémité blessée est attendue. Assurez-vous que toute l'extrémité blessée est couverte par le miroir (boîte), c'est-à-dire qu'elle ne peut pas être vue par le patient.
- Demandez-lui quels mouvements il peut facilement imaginer. Instruisez le patient à effectuer ces mouvements avec le côté sonore tout en regardant le miroir. Commencez par des mouvements lents.
- Instruisez le patient à déplacer les deux côtés pendant 5 à 10 min. Expliquez que le côté blessé ne bougera pas, mais qu'il est toujours important de générer l'illusion d'un mouvement simultané des deux côtés.
- Dans le processus de traitement, encouragez le patient à effectuer également des mouvements qu'il/elle ne peut pas imaginer facilement pour augmenter graduellement la difficulté.
- Comme un exercice à domicile, demandez au patient d'effectuer / imaginer ces mouvements 5 à 10 min, deux fois par jour.
REMARQUE: Avec les autres exercices pour améliorer la réorganisation corticale, cela représente environ 20 min du programme à domicile, deux fois par jour. Demandez au patient si cela est faisable. Sinon, choisissez une ou deux de ces interventions en fonction des préférences du patient et réduisez le temps de formation à un montant gérable.
- Comme il n'y a pas de mouvement actif prévu dans les premiers mois après la chirurgie, assurez-vous que l'aire de répartition du mouvement (ROM) est préservée dans toutes les articulations.
- Laissez le patient déplacer activement toutes les articulations.
- Instruisez le patient à l'exécuter tous les jours par lui-même.
- En outre, dans les mains ou les chevilles paralysées utilisent des attelles ou des orthèses pour stabiliser les articulations dans une position qui évite les contractures des articulations, des ligaments et des tendons (comme la position intrinsèque plus pour la main22). Si nécessaire, fabriquer une attelle à main ou assurez-vous que les patients obtiennent un dispositif bien ajusté. Chez les patients dont l'épaule est instable et/ou qui n'ont pas de flexion du coude, utilisez une élincage15.
- Selon les besoins du patient, inclure des exercices pour la symétrie du corps, la stabilité du tronc, et la posture. En particulier, si la fonction de la main est gravement altérée, inclure la formation des activités d'une seule main et de fournir au patient avec des dispositifs d'assistance.
3. Activation motrice à l'aide d'une approche latérale du donneur
- Commencer cette partie de la réadaptation dès que la première contraction volontaire du muscle réinnervated peut être détectée, qui peut habituellement être prévue dans les 3-5 mois après la chirurgie (voir le tableau 2).
- Configurez un système de biofeedback EMG de surface en le déballant sur une table, en branchant tous les câbles et en appuyant sur le bouton d'alimentation. Il peut s'agit d'un appareil autonome ou d'un appareil connecté à un ordinateur. Si un ordinateur est utilisé, connectez l'appareil à l'ordinateur et démarrez le logiciel approprié.
- Préparer la peau du patient pour réduire l'impédance23. Pour ce faire, en rasant soigneusement la partie corporelle respective et/ou en enlevant délicatement les cellules mortes de la peau avec un gel peeling et/ou une serviette en papier humide. Expliquer rapidement la fonctionnalité du système au patient.
- Demandez au patient de penser aux mouvements dont les nerfs du donneur étaient à l'origine responsables (p. ex., fermeture de la main si le nerf ulnaire a été utilisé) et palpez le muscle receveur.
- Placez une électrode EMG de surface sur la position exacte, où la contraction musculaire peut être palpée. Tandis que l'EMG de surface peut être détecté avec des électrodes humides et sèches, dans cette expérience des électrodes sèches sont préférées pour l'essai car elles peuvent être facilement déplacées sur la peau pour modifier la position d'électrode. Même si aucun mouvement ne peut être palpé, vérifiez l'activité EMG régulièrement dans les 3-6 premiers mois après la chirurgie.
REMARQUE: La ré-innervation peut être confirmée, si l'amplitude du signal pendant l'activation est à plusieurs reprises 2-3 fois plus élevé que le bruit de fond pendant la relaxation8. - Si cela ne peut pas être confirmé, modifier légèrement la position de l'électrode et essayer d'autres commandes motrices liées au nerf du donneur (p. ex., enlèvement ulnaire ou flexion du poignet, si le nerf ulnaire a été utilisé comme donneur). Sinon, continuer avec les interventions pour l'activation corticale et tester à nouveau après quelques semaines.
- Entraînez l'activation des muscles nouvellement ré-innervés avec le biofeedback de sEMG.
- Comme première étape de la formation d'activation de muscle, éduquez le patient sur la fonction du biofeedback de sEMG et expliquez les principes de l'approche d'activation de distributeur.
- Allumez le système de biofeedback et placez l'électrode EMG de surface sur la peau du patient au-dessus du muscle pour afficher l'activation musculaire du patient.
- Assurez-vous que le patient est confortablement assis et demandez au patient de penser aux modèles de mouvement liés au nerf du donneur tout en ramassant les signaux sEMG du muscle receveur. Si un système avec la possibilité d'ajuster les gains de signal est utilisé, configurez-le de manière à ce que l'amplitude du signal soit suffisamment élevée pour être facilement observée. Au début, cela nécessite généralement une amplification élevée.
- Dès que le patient peut activer le muscle de façon répétée, demandez-lui de se détendre complètement après l'activation musculaire, ce qui correspond à des amplitudes EMG proches de zéro. La relaxation complète est souvent difficile à réaliser pour le patient et peut prendre un certain temps. Demandez au patient d'activer à plusieurs reprises le muscle et de le détendre complètement.
- Essayez différents repères de mouvement et positions d'électrodes afin de trouver la plus haute amplitude. Après avoir trouvé une bonne combinaison, maintenez-le le reste de la session.
- Fournir au patient un programme structuré d'exercice à domicile comprenant la quantité de formation par semaine (10-20 min de formation concentrée par jour est recommandé) et des instructions exactes de ce qu'il faut former. S'il est possible pour le patient d'utiliser un dispositif pour le biofeedback sEMG à la maison, encouragez ce8. Mettre à jour le programme d'exerciceà ezons régulièrement.
- Dès que le patient se sent confiant avec la configuration sEMG, introduire des commandes motrices, y compris l'activation du nerf du donneur et la fonction réelle du muscle receveur. Pour un patient avec un transfert de nerf ulnaire d'Oberlin au muscle de biceps, ceci signifie penser à la fermeture de main et à la flexion de coude en même temps.
MISE EN GARDE: Dans les patients où une branche de nerf d'un muscle antagoniste a été transférée, ne se concentrent que sur la fonction de nerf de distributeur et omettent cette étape. - Entraînez l'activation musculaire avec et sans biofeedback sEMG jusqu'à ce que la force musculaire soit suffisante pour surmonter la gravité ou la résistance des muscles antagonistes. En outre, répétez les interventions pour l'activation du cortex moteur.
4. Réapprendre le modèle de mouvement original
- Dès que le muscle est assez fort pour surmonter la gravité ou la résistance des muscles antagonistes et la raideur articulaire, concentrez la thérapie sur le réapprentissage du modèle de mouvement original du nerf receveur. Cela signifie qu'un patient après le transfert de nerf ulnaire d'un Oberlin doit enfin apprendre à fléchir le coude sans aucun mouvement de la main et inversement, déplacer la main sans flexion du coude.
- Encouragez le patient à activer légèrement le muscle receveur sans le mouvement dans les muscles à l'origine innervé par le nerf du donneur.
- Soutenez ceci en utilisant le biofeedback de sEMG avec deux canaux. Placez une électrode bipolaire sur la peau au-dessus du muscle réinnervated et mettez l'autre sur la peau au-dessus du muscle de nerf de distributeur original. Cela permet au patient de voir simultanément l'activation des deux muscles. Encouragez le patient à activer le muscle receveur et à s'assurer que le muscle du donneur est détendu avec une amplitude de signal EMG faible.
- Faites savoir au patient que la séparation du signal est généralement plus facile avec une légère activation musculaire et que la co-contraction indésirable des deux muscles est commune au début de l'entraînement.
- En utilisant la même configuration sEMG, demandez au patient d'activer le muscle du donneur sans l'activation du muscle ré-innervé et de surveiller les stratégies souhaitables/indésirables entraînant une meilleure / pire séparation des signaux. Encouragez les stratégies qui appuient la séparation du signal.
- Si les deux signaux peuvent être séparés par de légères contractions musculaires, demandez au patient d'effectuer des contractions plus fortes.
- Dès qu'une bonne séparation du signal lors de l'utilisation du biofeedback sEMG peut être observée, demandez au patient d'effectuer des mouvements séparés de « donneur » et de « receveur » sans rétroaction.
- Comme cette phase est exigeante sur le plan cognitif et que la répétition est d'une grande importance pour le réapprentissage moteur, assurez-vous que le patient dispose d'un programme d'exercice à domicile approprié. Encore une fois, encouragez l'utilisation de dispositifs de biofeedback sEMG à la maison, si possible.
- Avec une fonction motrice accrue, encouragez le patient à accomplir des tâches plus complexes, y compris une force musculaire accrue ou une précision améliorée. Commencez également des exercices de renforcement « classiques », si nécessaire.
- Enfin, concentrez-vous sur les activités de la vie quotidienne et celles qui sont nécessaires à la maison, à l'environnement de travail et à l'exécution des sports du patient.
- Dans les transferts de nerf des membres inférieurs, commencer l'entraînement de démarche en mettant l'accent sur l'évitement des mouvements compensatoires indésirables.
- Demandez au patient de marcher le long d'un couloir et d'analyser la démarche en fonction des principes de l'analyse de la démarche observationnelle24,25.
- Définir les écarts par rapport au modèle physiologique de démarche et les analyser en ce qui concerne l'origine (p. ex., quel muscle peut être faible) et la connexion entre les uns et les autres (p. ex., comment la cinématique de la hanche affecte la cinématique du genou et vice versa). Si nécessaire, pour obtenir des éclaircissements, effectuez des tests supplémentaires (p. ex., pour la force musculaire ou la mobilité articulaire).
- Élaborer un plan de traitement basé sur vos résultats24,25.
- Évaluer les interventions pendant que le patient les fait, ainsi que les progrès de la thérapie au fil du temps. Si nécessaire, effectuez une autre analyse de la démarche et/ou modifiez les interventions.
- Voir le patient trois, six et douze mois après la sortie de la réadaptation pour en savoir plus sur le succès de la thérapie à long terme et la satisfaction du patient. Si nécessaire et demandé par le patient fournir des séances de formation supplémentaires.
- Évaluer, si l'objectif fonctionnel, qui a été discuté avec le patient avant la chirurgie / au début de la réadaptation pourrait être atteint.
REMARQUE : Pour certains patients, cela pourrait être un rétablissement entièrement fonctionnel, tandis que pour d'autres, le retour d'une fonction minimale pourrait être suffisant.- Demandez au patient s'il est satisfait des résultats de la réadaptation et précisez que cela est très subjectif et qu'il n'est pas nécessairement reflété par les notes des instruments d'évaluation des résultats.
- Si le patient n'est pas satisfait des résultats, informez le patient sur d'autres stratégies (chirurgicales) pour améliorer la fonction, ainsi que la possibilité d'utiliser des orthèses fonctionnelles pour compenser la force musculaire limitée.
Résultats
Le protocole de réadaptation décrit a été mis en œuvre dans un cadre clinique à l'Université médicale de Vienne et sa faisabilité a été évaluée dans une étude précédente8.
Comme indiqué dans notre publication précédente8, cinq patients ont participé à l'essai pour évaluer la faisabilité et les résultats d'un tel programme pour la réadaptation motrice après des lésions nerveuses périphériques complexes. Les caractéristiques du patient, y compris les blessures et la reconstruction chirurgicale effectuée, se trouvent dans le tableau 1. Tous les patients inclus ont souffert des dommages brachial graves de plexus. Ainsi, la récupération de moteur sans intervention chirurgicale a été jugée peu probable et la suture directe de nerf n'était pas possible dans n'importe lequel des cas. Les transferts de nerf exécutés ont été choisis selon l'anatomie intacte, et si possible, des transferts de nerf des muscles agonistiques ont été exécutés. Ceci a été fait pour réduire la charge cognitive pendant le réapprentissage de moteur.
Afin d'évaluer les résultats moteurs, la force musculaire des patients a été évaluée avant la chirurgie reconstructive et après la sortie de la réadaptation en utilisant le British Medical Research Council (BMRC) échelle26.
Les résultats présentés dans le tableau 2 montrent que tous les patients avaient une fonction améliorée de l'épaule et du coude après la réadaptation, ce qui leur permet de fléchir le bras contre la gravité. Ceci est en ligne avec la recherche antérieure, rapportant qu'une majorité de patients regagnent la fonction utile d'épaule et de coude après des transferts sélectifs de nerf et la réadaptation3,27,28. Cependant, deux des patients présentant un transfert ulnaire de nerf d'Oberlin inclus dans cette étude, ont regagné la force pleine de flexion de coude (M5), qui est meilleure que décrite par Bertelli et Ghizoni (2004)29 qui ont employé la même méthode chirurgicale. Cependant, Ray et coll. (2011)28 pourraient également montrer le plein rétablissement de la fonction de coude dans certains des patients soignés dans leur centre. Par conséquent, les résultats moteurs présentés sont semblables ou légèrement meilleurs que ceux décrits dans la littérature. Ceci indique que ce protocole contribue à de bons résultats dans les muscles proximal, où la ré-innervation des muscles est probable.
Cependant, dans les parties plus distales du corps, la pleine fonction ne pouvait pas être récupérée pour tous les patients, ce qui est en ligne avec d'autres recherches3,30. Bien que nous croyons que la rééducation motrice à l'aide d'un protocole d'entraînement structuré peut faciliter la réadaptation motrice par la récupération centrale de la représentation de la main dans le cerveau, elle a une influence limitée sur les processus périphériques nécessaires pour le ré-innervation des muscles après la chirurgie de transfert de nerf. Ainsi, les auteurs proposent l'utilisation de ce protocole, si la ré-innervation périphérique de nerf est prévue, mais ne croient pas qu'il favorise la régénération de nerf au niveau périphérique.
| Affaire nr. | Sexe, Age (années) | Type d'accident | Type de Lésion | Chirurgies reconstructives pour la restauration de la fonction des membres supérieurs | ||||
| 1 | m, 68 | Accident de moto | Polytraumatisme; Plexopathie brachiale mondiale | Greffes de nerf pour combler le défaut de MCN ; greffes de nerf thoracodorsal pour combler le défaut du nerf axillaire ; greffes de nerf pour la reconstruction postérieure de tronc ; Transfert de nerf ulnaire d'Oberlin à la branche motrice de MCN à la tête courte du biceps | ||||
| 2 | m, 56 ans | Accident de vélo | Avulsion de racine de nerf de C5-C6 | Transfert de nerf ulnaire d'Oberlin à la branche motrice de MCN pour la restauration de la fonction de biceps ; transfert de la branche motrice radiale de triceps au nerf axillaire | ||||
| 3 | m, 62 | Accident de vélo | Dommages importants au tronc supérieur du BP ; blessure de traction de C7 | Transfert de nerf XI-à-suprascapular ; transfert de bout en bout du nerf phrénétique à C7; transfert de fascicle de nerf ulnaire à la branche motrice de biceps de MCN ; transfert du fascicle médian de nerf à la branche motrice de brachialis de MCN ; transfert de fascicle du nerf radial au nerf axillaire | ||||
| 4 | f, 22 ans | Accident | Avulsion de racine de nerf de C7 ; dommages causés au C8 et au T1 | Greffes nerveuses de C5 et C6 au MCN, nerf médian et radial; greffes nerveuses de C8 au nerf médian, radial et ulnaire; greffes de nerf de T1 au nerf ulnaire | ||||
| 5 | f, 43 ans | Traumatisme sémineux des années après l'OBPL | Blessure de traction du tronc supérieur et médial du BP | Greffes nerveuses pour combler les défauts de C5, C6 et C7 pour restaurer la fonction du coude et la stabilité de l'épaule; transfert du fascicle médian de nerf à la branche de moteur brachial de MCN | ||||
Tableau 1 : Caractéristiques du patient. Veuillez noter les abréviations suivantes : BP et plexus brachial; MCN - nerf musculo-cutané; OBPL - lésion de plexus brachique obstétrical ; OP - opération; XI - nerf accessoire spinal. Ce tableau est adapté de Sturma et coll. (2018)8.
| Affaire nr. | Fonction des membres supérieurs, y compris les grades BMRC à la ligne de base | Fonction des membres supérieurs, y compris les grades BMRC au suivi | Temps entre la chirurgie de transfert de nerf et la première activité volontaire de sEMG | non. de sessions de thérapie au total (30 min chacun) | ||||
| 1 | Muscle deltoïde: 0 | Muscle deltoïde: 2 | 5 mois | 25 | ||||
| Flexion du coude: 0 | Flexion du coude: 3 | |||||||
| Triceps muscle: 0 | Triceps muscle: 2 | |||||||
| Aucune fonction active de main | Extension du poignet: 1 | |||||||
| Extension du doigt: 2 | ||||||||
| 2 | Flexion du coude: 1 | Flexion du coude: 5 | 4 mois | 22 | ||||
| Muscle deltoïde: 2- | Muscle deltoïde: 5 | |||||||
| 3 | Flexion du coude: 0 | Flexion du coude: 5 | 3 mois | 30 | ||||
| Muscle deltoïde: 0 | Muscle deltoïde: 4 | |||||||
| Triceps muscle: 3 | Triceps muscle: 5 | |||||||
| Extension du poignet : 3 | Extension du poignet: 5 | |||||||
| Flexion des doigts : 3 | Flexion des doigts: 5 | |||||||
| 4 | Flexion du coude: 0 | Flexion du coude : 3 | 5 mois | 20 | ||||
| Triceps muscle: 0 | Triceps muscle: 2 | |||||||
| Aucune fonction active de main | Flexion du poignet: 3 | |||||||
| Flexion des doigts (partie FDP ulnaire): 3 | ||||||||
| 5 | Flexion du coude: 0 | Flexion du coude: 3 | 4 mois | 18 | ||||
| Muscle deltoïde: 2 | Muscle deltoïde: 2 | |||||||
| Triceps muscle: 3 | Triceps muscle: 4 | |||||||
| Moyenne (SD) | 4,2 à 0,75 mois | De 23 à 4,20 | ||||||
Tableau 2 : Résultats moteurs du protocole de réhabilitation. Il n'y avait aucune altération fonctionnelle des muscles non inclus dans le tableau. Dans tous les patients, la fonction d'épaule et de coude ont été altérées à la ligne de base et améliorées au suivi. En outre, le temps entre la chirurgie et la première activité volontaire de sEMG, aussi bien que le nombre de sessions de thérapie pour chaque patient sont présentés. Ce tableau est adapté de Sturma et coll. (2018)8.
Fichier supplémentaire. Veuillez cliquer ici pour télécharger le fichier.
Discussion
Récemment, les transferts de nerfont ont été de plus en plus utilisés pour restaurer la fonction après des lésions nerveuses proximales graves avec des résultats prometteurs1,4,31,32. Cependant, bien qu'il y ait un consensus sur le fait que des programmes de formation structurés sont nécessaires pour promouvoir les changements neuroplastiques bénéfiques33,34,35, il n'y a pas de protocole structuré disponible pour décrire le moteur la réadaptation s'approche après des transferts de nerfs étape par étape. Par conséquent, le but du protocole présenté était de fournir des instructions détaillées pour la réadaptation post-chirurgicale pour embrasser des changements corticaux et pour augmenter des résultats chirurgicaux. Contrairement à d'autres protocoles9,36, la visualisation de l'activité musculaire via la surface EMG biofeedback est un élément clé dans le protocole présenté.
Dans le cadre de la thérapie, l'éducation des patients est une étape critique car le patient doit comprendre la procédure chirurgicale plutôt complexe et être éduqué sur les activités améliorant l'état de santé afin d'être activement impliqué dans le long processus de réadaptation8 , 13 (en) , 37. Il est largement entendu dire que la répétition est fondamentale et que des exercices quotidiens à domicile sont nécessaires pour renforcer une représentation corticale bien établie de la main8,34,38,39 . Outre l'information pure de patient, les auteurs recommandent fortement une approche patient-centrée pour la réadaptation. Cela implique en outre le traitement du patient comme une personne unique, la participation du patient dans les soins, une bonne communication clinicien-patient et l'autonomisation du patient. En réadaptation médicale, cette approche influence positivement la satisfaction des patients et les résultats40. En ce qui concerne la réadaptation motrice elle-même, il est recommandé de commencer les interventions avant la ré-innervation des muscles et de suivre une approche axée sur l'activation du donneur9. Pour s'assurer que l'activité musculaire est détectée le plus tôt possible, des dispositifs de biofeedback EMG peuvent être utilisés. Bien que les auteurs soient conscients que les dispositifs de biofeedback EMG ne sont pas encore de norme clinique,leur utilisation est fortement recommandée car ils permettent de commencer la réadaptation active précoce de moteur et de fournir la rétroaction valable sur les muscles nouvellement re-innervé8.
Les principes décrits dans ce protocole peuvent être appliqués pour différents types de transferts de nerfs, bien que des modifications au sein du protocole puissent être nécessaires. Tandis que le réapprentissage moteur est relativement facile si des muscles/nerfs synergiques ont été employés, l'utilisation des muscles/nerfs antagonistes exige un temps plus long de réadaptation et l'utilisation du biofeedback pourrait être d'une importance encore plus grande3,8. Particulièrement dans les cas où un plus grand nombre de répétitions est nécessaire, les protocoles futurs pourraient également inclure des jeux sérieux pour maintenir la motivation patiente41.
Comme le moment de la régénération des nerfs et la quantité de récupération dépend énormément des blessures et des interventions chirurgicales, il n'y a pas de calendrier strict pour la réadaptation. Au lieu de cela, le thérapeute est invité à procéder en fonction des signes de récupération motrice comme indiqué dans le protocole. De la même manière, il est important de noter que le succès de la chirurgie de transfert de nerf est basé sur de nombreux facteurs comprenant le type et la sévérité de la blessure, les qualifications et l'expertise du chirurgien aussi bien que l'âge, l'état de santé, la cognition et la motivation du patient8 , 13 (en) , 42 Ans, états-unis ( , 43. Bien que la réadaptation soit un pilier principal pour retrouver la fonction après des dommages graves de nerf, même le meilleur programme pour la rééducation de moteur ne peut pas améliorer la fonction, s'il y a la régénération périphérique inadéquate de nerf et la re-innervation de muscle. Ainsi, les auteurs recommandent fortement de voir les patients régulièrement ensemble au sein d'une équipe multidisciplinaire pour être en mesure de discuter si le rétablissement se passe comme prévu ou si des interventions médicales supplémentaires sont nécessaires. Cependant, particulièrement après des dommages graves tels que c8 et Th1 avulsions de racinede nerf, les résultats réalistes pourraient ne pas inclure le plein rétablissement de la fonction d'extrémité 3,30. Dans ces cas, l'équipe clinique doit communiquer ceci au patient dès qu'un pronostic réaliste peut être indiqué (environ un an après les transferts de nerf). À ce stade, d'autres possibilités dans la réadaptation, les dispositifs d'assistance ou les interventions chirurgicales (comme les transferts de tendon) doivent être discutées. Dans les cas, où absolument aucune fonction de la main ne revient, le remplacement du membre sans fonction par un dispositif prothétique peut être considéré comme une option ainsi44,45. Ceci n'est toutefois recommandé qu'en dernier recours et après une évaluation physique et psychologique approfondie46.
Tandis que l'accent de la chirurgie périphérique de nerf se trouve habituellement sur la reconstruction de la fonction motrice, les transferts sensoriels de nerf sont parfois employés pour reconstituer la sensation dans la main après la blessure médiane ou ulnaire grave de nerf4,47. Semblable aux transferts de nerf moteur, ceci crée les voies neurales sensorielles altérées et a comme conséquence des sensations qui sont senties comme si elles provenaient de la zone précédente d'innervation du nerf de distributeur. Même si aucun transfert sensoriel de nerf n'a été exécuté, il peut toujours être changé/sensation réduite dû à la blessure elle-même27 ou dû à la morbidité de donateur-côté48. Dans ces cas, la rééducation en temps opportun peut aider à améliorer la fonction sensorielle49, et de réduire l'hypersensibilité indésirable et la douleur qui se produit souvent après de telles blessures. Pour assurer une bonne fonction motrice et sensorielle, les auteurs recommandent fortement de compléter la rééducation motrice avec des approches thérapeutiques sur mesure pour promouvoir la réorganisation dans le cortex sensoriel correspondant ainsique 39,50, 51. En ce qui concerne la rééducation sensorielle, il est recommandé de commencer les interventions avant la ré-innervation de la peau49,52,53. Cela peut inclure la substitution de la sensation par d'autres sens comme la vision53 ou la rétroaction auditive54, ainsi que l'utilisation du chevauchement des zones d'innervation sensorielle27,52. Dès que le patient a retrouvé une certaine sensibilité, la gnose tactile et la reconnaissance d'objets peuvent être formées, tout en maintenant une grande quantité d'entrée sensorielle34. Les matériaux typiques qui peuvent être utilisés pour cela, comprennent des assiettes autofaites avec différentes surfaces à reconnaître avec les yeux fermés (voir la figure 2) ou une boîte remplie de haricots/ lentilles/riz (voir figure 3).

Figure 2 : Différentes surfaces peuvent être utilisées pour soutenir le rétablissement de la sensibilité. Habituellement, le patient est invité à les toucher avec les deux mains d'abord, alors qu'il / elle pourrait essayer par la suite de reconnaître les différentes surfaces sans vision en utilisant seulement la main avec une sensibilité limitée. Veuillez cliquer ici pour voir une version plus grande de ce chiffre.
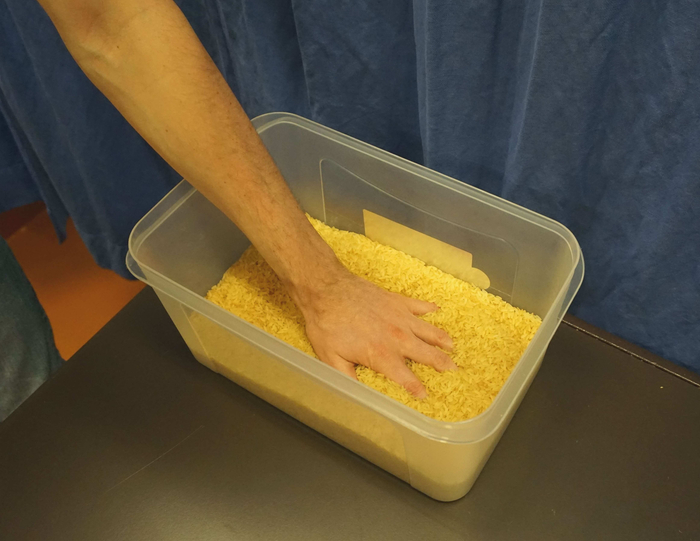
Figure 3: Une boîte remplie de riz pour la rééducation sensorielle de la main. En thérapie, le patient peut mettre sa main avec une sensibilité réduite soigneusement dans cette boîte et déplacer lentement la main. Pour attirer l'attention du patient, le thérapeute peut mettre quelques petits objets (p. ex., blocs de bois ou trombones) dans cette boîte et demander à les trouver sans contrôle visuel. Veuillez cliquer ici pour voir une version plus grande de ce chiffre.
Cependant, tant dans la rééducation sensorielle que dans la rééducation motrice, il n'y a que peu de preuves concernant le choix des interventions nécessaires pour favoriser une bonne récupération34. Cela limite la validité du protocole de réadaptation proposé, comme pour d'autres protocoles. Bien que le protocole décrit ait été évalué dans le cadre d'une étude de faisabilité et que les résultats moteurs soient semblables ou légèrement meilleurs que ceux rapportés dans la littérature8, cette étude a été réalisée sur une petite taille d'échantillon et sans groupe témoin. Il est donc impossible de comparer les résultats, les avantages et les inconvénients de ce protocole par rapport aux précédents. D'autres recherches doivent inclure des études contrôlées afin de comparer les avantages possibles de l'utilisation du biofeedback EMG de surface aux approches conventionnelles.
Déclarations de divulgation
Les auteurs n'ont rien à révéler.
Remerciements
Cette étude a été financée par la Christian Doppler Research Foundation du Conseil autrichien pour la recherche et le développement technologique et le Ministère fédéral autrichien de la science, de la recherche et de l'économie. Nous remercions Petra Gettinger pour son aide dans la préparation du tournage et Aron Cserveny pour la préparation des illustrations incluses dans le manuscrit et le dépliant de réhabilitation. Frontiers in Neuroscience a accordé la permission de reproduire les données présentées dans l'article original.
matériels
| Name | Company | Catalog Number | Comments |
| EMG electrodes | Otto bock Healthcare, Duderstadt, Germany | electrodes 13E202 = 50 | The EMG electrodes used in this study were bipolar and included a ground and a 50 Hz filter. They were used with the Moby. |
| Folding Mirror Therapy Box (Arm/Foot/Ankle) | Reflex Pain Management Therapy Store | This box was used for mirror therapy. | |
| Myoboy | Otto bock Healthcare, Duderstadt, Germany | Myoboy | This EMG Biofeedback device that can be used as stand alone device or with a computer. While this device was used in the presented pilot study, other (cheaper) devices for sEMG biofeedback training are available as well. |
| Recognise[TM] Flash Cards | noigroup | If no self-made cards for left-right discrimination are used, these can be purchased from noigroup.com. There, a mobile app for training is available as well. |
Références
- Rohde, R. S., Wolfe, S. W. Nerve transfers for adult traumatic brachial plexus palsy (brachial plexus nerve transfer). HSS Journal. 3 (1), 77-82 (2007).
- Ray, W. Z., Mackinnon, S. E. Management of nerve gaps: Autografts, allografts, nerve transfers, and end-to-side neurorrhaphy. Experimental Neurology. 223 (1), 77-85 (2010).
- Tung, T. H., Mackinnon, S. E. Nerve Transfers: Indications, Techniques, and Outcomes. The Journal of Hand Surgery. 35 (2), 332-341 (2010).
- Isaacs, J., Cochran, A. R. Nerve transfers for peripheral nerve injury in the upper limb. Bone Joint Journal. 101 (2), 124-131 (2019).
- Terzis, J. K., Papakonstantinou, K. C. The surgical treatment of brachial plexus injuries in adults. Plastic and Reconstruction Surgery. 106 (5), (2000).
- Ray, W. Z., Mackinnon, S. E. Clinical Outcomes Following Median to Radial Nerve Transfers. The Journal of Hand Surgery. 36 (2), 201-208 (2011).
- Liu, Y., Lao, J., Gao, K., Gu, Y., Xin, Z. Outcome of nerve transfers for traumatic complete brachial plexus avulsion: results of 28 patients by DASH and NRS questionnaires. Journal of Hand Surgery European. 37 (5), 413-421 (2012).
- Sturma, A., Hruby, L. A., Prahm, C., Mayer, J. A., Aszmann, O. C. Rehabilitation of Upper Extremity Nerve Injuries Using Surface EMG Biofeedback: Protocols for Clinical Application. Frontiers in Neuroscience. 12 (906), (2018).
- Kahn, L. C., Moore, A. M. Donor Activation Focused Rehabilitation Approach: Maximizing Outcomes After Nerve Transfers. Hand Clinics. 32 (2), 263-277 (2016).
- Oberlin, C., et al. Nerve transfer to biceps muscle using a part of ulnar nerve for C5-C6 avulsion of the brachial plexus: anatomical study and report of four cases. Journal of Hand Surgery American. 19 (2), 232-237 (1994).
- Karl, A., Birbaumer, N., Lutzenberger, W., Cohen, L. G., Flor, H. Reorganization of motor and somatosensory cortex in upper extremity amputees with phantom limb pain. Journal of Neurosciences. 21 (10), 3609-3618 (2001).
- Makin, T. R., Bensmaia, S. J. Stability of Sensory Topographies in Adult Cortex. Trends in Cognitive Science. 21 (3), 195-204 (2017).
- Novak, C. B., Lvonder Heyde, R. Rehabilitation of the upper extremity following nerve and tendon reconstruction: when and how. Seminars in Plastic Surgery. 29 (1), 73-80 (2015).
- Lundborg, G. Brain plasticity and hand surgery: an overview. Journal of Hand Surgery Bristish. 25 (3), 242-252 (2000).
- Novak, C. B. Rehabilitation Following Motor Nerve Transfers. Hand Clinics. 24 (4), 417-423 (2008).
- Miller, C., Peek, A. L., Power, D., Heneghan, N. R. Psychological consequences of traumatic upper limb peripheral nerve injury: A systematic review. Hand Therapy. 22 (1), 35-45 (2016).
- Bailey, R., Kaskutas, V., Fox, I., Baum, C. M., Mackinnon, S. E. Effect of Upper Extremity Nerve Damage on Activity Participation, Pain, Depression, and Quality of Life. The Journal of Hand Surgery. 34 (9), 1682-1688 (2009).
- Moseley, G. L. . The graded motor imagery handbook. , (2012).
- Ramachandran, V. S., Rogers-Ramachandran, D. Synaesthesia in phantom limbs induced with mirrors. Proceedings of the Royal Society of Biological Sciences. 263 (1369), 377-386 (1996).
- Rothgangel, A. S., Braun, S. M., Beurskens, A. J., Seitz, R. J., Wade, D. T. The clinical aspects of mirror therapy in rehabilitation. International Journal of Rehabilitation Research. 34 (1), 1-13 (2011).
- Ramachandran, V. S., Hirstein, W. The perception of phantom limbs. The D. O. Hebb lecture. Brain. 121 (Pt 9), 1603-1630 (1998).
- Hubatka, G., Meyer, V. E. Immobilization of the injured hand. Helvetica Chirurgica Acta. 47 (1-2), 81-84 (1980).
- Merletti, R., Parker, P. A. Electromyography: Physiology, Engineering, and Non-Invasive Applications. Wiley IEEE-Press Verlag. , (2004).
- Götz-Neumann, K. . Gehen verstehen. Ganganalyse in der Physiotherapie. , (2016).
- Perry, J., Burnfield, J. M. . Gait Analysis: Normal and Pathological Function. , (2010).
- James, M. A. Use of the Medical Research Council muscle strength grading system in the upper extremity. The Journal of Hand Surgery American. 32 (2), 154-156 (2007).
- Bertelli, J. A., Ghizoni, M. F., Loure Iro Chaves, D. P. Sensory disturbances and pain complaints after brachial plexus root injury: a prospective study involving 150 adult patients. Microsurgery. 31 (2), 93-97 (2011).
- Ray, W. Z., Pet, M. A., Yee, A., Mackinnon, S. E. Double fascicular nerve transfer to the biceps and brachialis muscles after brachial plexus injury: clinical outcomes in a series of 29 cases. Journal of Neurosurgery. 114 (6), 1520-1528 (2011).
- Bertelli, J. A., Ghizoni, M. F. Reconstruction of C5 and C6 brachial plexus avulsion injury by multiple nerve transfers: spinal accessory to suprascapular, ulnar fascicles to biceps branch, and triceps long or lateral head branch to axillary nerve. The Journal of Hand Surgery American. 29 (1), 131-139 (2004).
- Wong, A. H., Pianta, T. J., Mastella, D. J. Nerve transfers. Hand Clinics. 28 (4), 571-577 (2012).
- Colbert, S. H., Mackinnon, S. E. Nerve Transfers for Brachial Plexus Reconstruction. Nerve Transfers. 24 (4), 341-361 (2008).
- Brown, J. M., Mackinnon, S. E. Nerve Transfers in the Forearm and Hand. Nerve Transfers. 24 (4), 319-340 (2008).
- Beisteiner, R., et al. New type of cortical neuroplasticity after nerve repair in brachial plexus lesions. Archives in Neurology. 68 (11), 1467-1470 (2011).
- Novak, C. B., von der Heyde, R. L. Evidence and techniques in rehabilitation following nerve injuries. Hand Clinics. 29 (3), 383-392 (2013).
- Dahlin, L. B., Andersson, G., Backman, C., Svensson, H., Bjorkman, A. Rehabilitation, Using Guided Cerebral Plasticity, of a Brachial Plexus Injury Treated with Intercostal and Phrenic Nerve Transfers. Frontiers in Neurology. 8, 72 (2017).
- Hill, J., et al. . The stages of rehabilitation following motor nerve transfer surgery. , (2019).
- Vikstrom, P., Carlsson, I., Rosen, B., Bjorkman, A. Patients' views on early sensory relearning following nerve repair-a Q-methodology study. The Journal of Hand Therapy. 31 (4), 443-450 (2018).
- Anastakis, D. J., Malessy, M. J., Chen, R., Davis, K. D., Mikulis, D. Cortical plasticity following nerve transfer in the upper extremity. Hand Clinics. 24 (4), 425-444 (2008).
- Oud, T., Beelen, A., Eijffinger, E., Nollet, F. Sensory re-education after nerve injury of the upper limb: a systematic review. Clinical Rehabilitation. 21 (6), 483-494 (2007).
- Plewnia, A., Bengel, J., Korner, M. Patient-centeredness and its impact on patient satisfaction and treatment outcomes in medical rehabilitation. Patient Education Counselling. 99 (12), 2063-2070 (2016).
- Prahm, C., Kayali, F., Sturma, A., Aszmann, O. PlayBionic: Game-Based Interventions to Encourage Patient Engagement and Performance in Prosthetic Motor Rehabilitation. Physical Medicine & Rehabilitation. 10 (11), 1252-1260 (2018).
- Rosen, B., Lundborg, G., Dahlin, L. B., Holmberg, J., Karlson, B. Nerve repair: correlation of restitution of functional sensibility with specific cognitive capacities. Journal of Hand Surgery. 19 (4), 452-458 (1994).
- Lundborg, G., Rosen, B. Sensory relearning after nerve repair. Lancet. 358 (9284), 809-810 (2001).
- Aszmann, O. C., et al. Bionic reconstruction to restore hand function after brachial plexus injury: a case series of three patients. Lancet. 385 (9983), 2183-2189 (2015).
- Hruby, L. A., et al. Algorithm for bionic hand reconstruction in patients with global brachial plexopathies. Journal of Neurosurgery. , 1-9 (2017).
- Hruby, L. A., Pittermann, A., Sturma, A., Aszmann, O. C. The Vienna psychosocial assessment procedure for bionic reconstruction in patients with global brachial plexus injuries. PloS One. 13 (1), e0189592 (2018).
- Soldado, F., Bertelli, J. A., Ghizoni, M. F. High Median Nerve Injury: Motor and Sensory Nerve Transfers to Restore Function. Hand Clinics. 32 (2), 209-217 (2016).
- Li, X. M., et al. Donor-side morbidity after contralateral C-7 nerve transfer: results at a minimum of 6 months after surgery. Journal of Neurosurgery. 124 (5), 1434-1441 (2016).
- Rosen, B., Lundborg, G. Sensory re-education after nerve repair: aspects of timing. Handchirurgie Mikrochirurgie Plastiche Chirurgie. 36 (1), 8-12 (2004).
- Jerosch-Herold, C. Sensory relearning in peripheral nerve disorders of the hand: a web-based survey and delphi consensus method. Journal of Hand Therapy. 24 (4), 292-298 (2011).
- Rosén, B., Lundborg, G., Skirven, T. M., Osterman, A. L., Fedorczyk, J. M., Amadio, P. C. . Rehabilitation of the Hand and Upper Extremity. 6, (2011).
- Daniele, H. R., Aguado, L. Early compensatory sensory re-education. Journal of Reconstructive Microsurgery. 19 (2), 107-110 (2003).
- Rosen, B., et al. Enhanced early sensory outcome after nerve repair as a result of immediate post-operative re-learning: a randomized controlled trial. Journal of Hand Surgery European Volume. 40 (6), 598-606 (2015).
- Rosen, B., Lundborg, G. Early use of artificial sensibility to improve sensory recovery after repair of the median and ulnar nerve. Scandinavian Journal of Plastic and Reconstructive Surgery and Hand Surgery. 37 (1), 54-57 (2003).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon