Method Article
Caractéristiques d’imagerie de la sclérose systémique associée à la maladie pulmonaire interstitielle
Dans cet article
Résumé
Ici, nous présentons des recommandations pratiques pour effectuer la tomographie calculée à haute résolution thoracique pour diagnostiquer et évaluer la maladie pulmonaire interstitielle systémique liée à la sclérose.
Résumé
Le diagnostic précoce de la maladie pulmonaire interstitielle liée à la sclérose systémique (SSc-ILD) est important pour permettre l’administration d’un traitement avec un délai minimal. Cependant, le diagnostic de SSc-ILD est difficile parce que les symptômes clés ne sont pas spécifiques. La tomographie calculée à haute résolution (HRCT) de la poitrine est reconnue comme une méthode d’imagerie sensible pour diagnostiquer et évaluer SSc-ILD. L’exposition des patients aux rayonnements ionisants peut être considérée comme une limitation, bien que des mesures méthodologiques puissent être prises pour modérer cela. Nous présentons des recommandations pratiques pour effectuer des analyses hrct et interpréter les résultats. Les principales caractéristiques de SSc-ILD sur HRCT incluent un modèle non spécifique de pneumonie interstitielle (NSIP) avec des opacités périphériques de sol-verre et la bronchiectasis de traction étendue. Malgré les similitudes entre SSc-ILD et la fibrose pulmonaire idiopathique (IPF), hrct peut être utilisé pour différencier ces conditions: dans SSc-ILD par rapport à IPF, il ya une plus grande proportion d’opacité du verre moulu et la fibrose est moins grossière. Un oesophage dilaté, rempli d’air avec le diamètre >10 mm, suggestif de la dysmotilité oesophagienne est généralement vu dans SSc-ILD. La taille d’artère pulmonaire plus grande que l’aorte ascendante adjacente suggère l’hypertension pulmonaire coexistante. Les nodules doivent être surveillés en raison du risque accru de cancer du poumon. Une grande partie de la maladie sur HRCT (≥20%) ou un score élevé de fibrose suggère un risque accru de mortalité. HrCT est au cœur du diagnostic de SSc-ILD, et les évaluations en série peuvent être utiles pour surveiller la progression de la maladie ou la réponse au traitement.
Introduction
La sclérose systémique (SSc) est une maladie auto-immune complexe, hétérogène. Il peut se manifester comme vasculopathie, phénomène de Raynaud et la fibrose de la peau et des organes internes1. SSc est classé en sous-types comme suit: limitée cutanée, cutanée diffuse, sclérodermie sinusoïdée (sans implication de la peau), et SSc chevauchement syndrome1.
SSc n’est pas hérité à la mode mendéle, mais les facteurs génétiques semblent influencer la susceptibilité à la maladie. Les taux d’incidence diffèrent d’un groupe ethnique à l’autre et sont augmentés chez les personnes ayant des antécédents familiaux de la maladie2,3. Les facteurs de risque environnementaux semblent également exister, avec une exposition élevée à la silice ou aux solvants organiques semblant augmenter l’occurrence de SSc4. La prévalence mondiale du SSc est d’environ 1 sur 10 0001. Plus de femelles que d’hommes sont touchées par SSc, avec des rapports féminins/hommes rapportés allant entre 3:1 et 8:1, et le groupe d’âge avec l’incidence la plus élevée de la maladie est 45-54 ans5.
Le poumon est le deuxième organe viscéral le plus fréquemment affecté chez les patients atteints de SSc6. Il y a deux principales manifestations pulmonaires de SSc : la maladie pulmonaire interstitielle (ILD), et l’hypertension pulmonaire7. Ild est généralement fibrotique; il se produit dans environ 80% des patients présentant SSc et est plus commun dans la sclérodermie cutanée diffuse que dans la forme limitée de la maladie1,8. L’hypertension pulmonaire peut se manifester sous forme d’hypertension artérielle pulmonaire isolée (HAP, qui a une prévalence de 13–35% dans SSc) ou d’hypertension pulmonaire résultant de la participation ventriculaire gauche/dysfonctionnement diastolique ou ILD/hypoxémie7. Les profils d’anticorps diffèrent entre les patients atteints de SSc-ILD et ceux atteints de SSc-PAH. Par exemple, la présence d’anticorps anti-Scl-70 est associée à SSc-ILD8, tandis que les anticorps anticentromères sont plus fréquents chez les patients atteints de HAP que chez ceux qui n’ont pas de HAP9.
Les symptômes de SSc-ILD incluent la dyspnée, la toux, la douleur thoracique, et la limitation d’exercice. ILD est un contributeur majeur à la morbidité dans SSc10,11,12. Par conséquent, les coûts annuels des soins de santé toutes causes confondues ont été signalés plus élevés chez les patients atteints de SSc-ILD que chez ceux atteints de SSc et d’aucun IDD : 31 285 à 55 446 $ contre 18 513 à 23 268 $, respectivement13$
SSc-ILD est la principale cause de mortalité chez les patients atteints de SSc, représentant 30 à 35% des décès dans ce groupe10,14. La survie médiane chez les patients atteints de SSc-ILD a été signalée à 5–8 ans10,15; à titre de comparaison, environ 76 % de la population totale atteinte de SSc survit pendant plus de 10 ans à la suite de l’apparition de la maladie16. Les prédicteurs significatifs de la mortalité dans SSc-ILD incluent l’âge, la capacité vitale forcée (FVC), la capacité de diffusion de base du poumon pour le monoxyde de carbone (DLCO), l’étendue de la maladie sur la tomographie calculée à haute résolution (HRCT), la présence d’hypertension pulmonaire et les niveaux de Kerbs von den Lungren 6 (KL-6) antigène17,18.
Le diagnostic précoce est important pour permettre le traitement d’être administré avec un délai minimal et, chez les patients présentant un phénotype progressif, la progression de la maladie peut potentiellement être ralentie. Cependant, le diagnostic de SSc-ILD est difficile parce que les symptômes non spécifiques de la toux, de la dyspnée et de la fatigue peuvent être confondus avec d’autres aspects de SSc, tels que la maladie cardiaque et la participation musculo-squelettique. Les évaluations pour diagnostiquer les ILD comprennent : présentation clinique, histoire, statut de tabagisme, fonction pulmonaire, imagerie, et dans certains cas, biopsie pulmonaire. L’affirmation du diagnostic SSc-ILD nécessite plusieurs investigations, qui sont souvent utilisées en combinaison19. Les évaluations les plus fréquemment utilisées comprennent les tests de fonction pulmonaire et HRCT20,21,22,23. D’autres méthodes d’imagerie, telles que la radiographie thoracique et l’imagerie par rayonnement (p. ex., imagerie par résonance magnétique [IRM], échographie pulmonaire) peuvent également être utilisées22. Les tests de fonction pulmonaire sont utilisés pour évaluer la gravité de l’ILD et surveiller son cours. Cependant, l’utilisation des tests de fonction pulmonaire seul est d’une utilité limitée pour diagnostiquer SSc-ILD24,25. HRCT de la poitrine est considéré comme le moyen non invasif le plus sensible de faciliter le diagnostic différentiel de SSc-ILD19. Les résultats de base du HRCT, ainsi que les changements au fil du temps, peuvent être utilisés pour prédire l’évolution future des maladies pulmonaires et la réponse potentielle à la thérapie26.
L’exposition aux rayonnements avec hrct est parfois considérée comme un facteur limitant pour le dépistage régulier27,28; limiter le nombre de tranches est une méthode potentielle pour réduire le risque de rayonnement, et la dose peut également être réduite en diminuant soit la tension ou le courant29,30,31. Par ailleurs, différentes méthodes d’évaluation peuvent être envisagées. Par exemple, l’IRM semble avoir un certain potentiel d’évaluation et de suivi des patients atteints deLIL 22. Dans une étude utilisant des images d’IRM pondérées en T2 avec synchronisation respiratoire, hrct a été exécuté en parallèle comme évaluation « or-natio » ; 100% de sensibilité et 60% de spécificité ont été rapportés avec l’IRM pour déterminer la présence d’ILD32. Un accord similaire entre l’IRM et le HRCT dans la détection et la catégorisation de l’ILD a été rapporté dans une autre étude33. Malgré les résultats prometteurs, l’IRM est actuellement une méthodologie de recherche et elle n’est pas encore prête pour une utilisation clinique généralisée.
Ici, nous fournissons un aperçu pratique de l’interprétation des résultats de l’imagerie, en mettant l’accent sur hrct, pour diagnostiquer la participation pulmonaire dans SSc, déterminer le pronostic, et aussi explorer les développements futurs qui peuvent améliorer les méthodes d’imagerie et l’interprétation des résultats. Les images hrct des cas représentatifs sont incluses dans le document.
Protocole
1. Analyse HRCT
- Effectuer le balayage d’acquisition de HRCT volumétrique de la poitrine36. Les agents de contraste ne sont pas requis36,37.
- Obtenez les acquisitions suivantes avec les paramètres indiqués au tableau 136,37.
- Acquérir un balayage inspirateur de supination (volumétrique) des apices de poumon à la base pulmonaire.
- Acquérir un balayage expiraratoire de supination (séquentiel avec des écarts de 10 à 20 mm) de 2 cm sous les apites pulmonaires à la base pulmonaire.
- Acquérir une option inspiratory sujette (séquentielle avec des écarts de 10 à 20 mm) de la carina à la base pulmonaire.
- Donnez des instructions respiratoires au patient avant chaque acquisition36,37. Pour un scan inspirateur, dites : « Prenez une profonde respiration... et laissez-le sortir. Prenez dans une autre respiration profonde .... et laissez-le sortir. Prenez une autre respiration profonde, et retenez votre souffle. Continuez à retenir votre souffle »37.
- Obtenir des scans inspiratoires à pleine inspiration35,36.
- Utilisez la colimation la plus fine, le temps de rotation le plus court et la hauteur la plus élevée pour vous assurer que les images sans mouvement sont obtenues36. Les paramètres de numérisation suggérés sont détaillés dans le tableau 137.
- Pour une qualité optimale des scans volumétriques, obtenez des images de section mince (<2 mm) avec reconstruction à haute résolution spatiale35,36.
- Examiner les analyses immédiatement après l’acquisition et répéter si l’un ou l’autre artefact de mouvement est présent ou l’inspiration inadéquate s’est produite37.
2. Rapports
- Préparer un rapport d’interprétation.
- Partagez le rapport et les images du HRCT avec l’équipe soignante du patient et ajoutez-les aux dossiers médicaux du patient.
Résultats
Diagnostic
Les principales caractéristiques de SSc-ILD sur hrct incluent généralement un modèle non spécifique de pneumonie interstitielle (NSIP) avec des opacités périphériques de verre de sol et une bronchiectasis de traction étendue (figure 1 et figure 2). Les opacités en verre moulu ont une large étiologie et sont souvent non spécifiques40,41,42. La prédominance centrale ou la distribution périphérique avec l’épargne subpleural est très suggestive du NSIP (Figure 3).
Typiquement, les modèles d’ILD dans les images de HRCT incluent des réticulations avec la distorsion architecturale ayant pour résultat la bronchiectasis/bronchiolectasis de traction (compatible avec une forme fibrotique de NSIP). En effet, la bronchiectasie de traction et la bronchiolectasis de traction sont souvent les caractéristiques prédominantes de SSc-ILD (Figure 4)43. D’autres résultats peuvent inclure le nid d’abeilles (figure 5; plus fréquent dans les formes limitées de SSc), l’épaississement septal interlobulaire et les lignes intralobulaires, et les micronodules40,44. Le nid d’abeille se réfère aux espaces aériens cystiques groupés de diamètre généralement constant (~3–10 mm) avec des murs épais et bien définis31. Les bronchiectasies de nid d’abeille et de traction sont des caractéristiques clés de la pneumonie interstitielle habituelle (UIP) sur HRCT. Bien que ce modèle soit le plus souvent associé à la fibrose pulmonaire idiopathique (IPF), le prototype de fibrosing ILD avec un phénotype progressif, il peut parfois être vu chez les patients atteints de SSc-ILD10. Récemment, plusieurs signes ont été identifiés chez les patients atteints d’ILD liés à la maladie des tissus conjonctifs (y compris SSc-ILD) et le modèle uIP sur HRCT, mais pas chez ceux atteints de FPI. Il s’agit du signe de bord droit (c.-à-d. l’isolement de la fibrose aux bases pulmonaires avec une délimitation marquée dans le plan craniocaudal sans extension substantielle le long des marges latérales des poumons sur les images coronales), le signe prédominant (ou exubérant) de nid d’abeille (>70% des parties fibrotiques du poumon), et le signe antérieur du lobe supérieur (c.-à-d. concentration de la fibrose dans l’aspect antérieur des lobes supérieurs, avec l’épargne relative des autres aspects des lobes supérieurs, et la participation concomitante de lobe inférieur)45. Le signe de bord droit a également été associé à la pathologieNSIP 46, qui est le modèle principal de CT dans SSc-ILD10.
L’œsophage dilaté rempli d’air est fréquemment observé chez les patients atteints de SSc (Figure 6)47,48,49 et chez les patients atteints de SSc-ILD47,48. Bien qu’il n’y ait pas de limite d’âge supérieure acceptée où un oesophage dilaté peut ne plus aider à différencier SSc-ILD et IPF, un oesophage dilaté peut être plus difficile à interpréter chez les patients de plus de 65 ans en raison de l’incidence croissante des troubles de la motilité oesophagienne. La lymphadénopathie mediastinale (habituellement réactive), dans laquelle l’axe court du ganglion lymphatique dépasse 10 mm, est également souvent observée chez les patients atteints de SSc-ILD47,50. La taille de l’artère pulmonaire supérieure à l’aorte ascendante adjacente suggère une hypertension pulmonaire coexistante (figure 6), même chez les patients sans maladie pulmonaire fibrotique51,52,53. Les zones de consolidation suggèrent l’infection superposée, l’aspiration, l’organisation de la pneumonie, l’hémorragie ou la malignité. Les nodules doivent être surveillés en raison du risque accru de cancer du poumon dans SSc-ILD7; le cancer primaire le plus commun à survenir dans les patients avec SSc-ILD est adénocarcinome7,54.
SSc-ILD partage un certain nombre de similitudes cliniques, mécanistes et pathologiques avec IPF15,55. Cependant, certaines caractéristiques radiologiques permettent la différenciation de ces deux ILD15,45. Dans SSc-ILD, par rapport à l’IPF, il y a une plus grande proportion d’opacité de verre moulu et la fibrose est moins grossière. Dans les cas d’UIP dans SSc, le nid d’abeilles peut être observé dans plus de 70% du tissu fibrotique-poumon - le signe exubérant de nid d’abeille56,57. En outre, le signe à quatre coins (également connu sous le nom de signe antérieur du lobe supérieur) est significativement plus commun dans SSc-ILD que dans IPF ; il s’agit d’un modèle d’inflammation et/ou de fibrose focalement ou de façon disproportionnée impliquant les lobes supérieurs antérolatéraux bilatéraux et les lobes inférieurs postérieurs58.
Les radiographies thoraciques peuvent d’abord détecter l’ILD; cependant, ils n’offrent pas la résolution de contraste suffisante pour le diagnostic fiable. Dans les radiographies thoraciques de patients atteints de SSc-ILD, le modèle le plus fréquent est la réticulation basale prédominante59. D’autres caractéristiques peuvent inclure la bronchiectasie visible, la perte de volume et le nid d’abeilles. Comme avec HRCT, la présence d’un oesophage dilaté rempli d’air peut être utile pour soutenir le diagnostic de SSc-ILD47.
Pronostic
Plusieurs résultats différents d’imagerie ont été montrés pour être associés au pronostic dans SSc-ILD. Le risque de mortalité a été rapporté pour être plus élevé dans les patients avec une étendue de maladie d’au moins 20% sur HRCT (la survie de 10 ans était 43% contre 67%, respectivement, dans les patients avec l’étendue de la maladie au-dessus contre en dessous du seuil de 20%)60. De même, un score élevé de fibrose sur hrct (basé sur l’étendue de la réticulation et du nid d’abeilles) a été associé à une augmentation de la mortalité61. Les grands diamètres oesophagiens sont associés à une sévérité accrue de l’ILD et à une diminution de laDLCO 48. La densité pulmonaire et le diamètre de l’artère pulmonaire peuvent potentiellement être utilisés pour prédire le risque d’hypertension pulmonaire62. Des paramètres informatisés et quantitatifs de CT pourraient également être exploités pour identifier le risque de déclin ou de mortalité de la fonction pulmonaire des patients. Une étude a suggéré que l’étendue de l’ILD, quantifiée à partir de HRCT, pourrait être utilisée pour prédire la baisse de la FVC sur 12 mois63. Dans une autre étude, les paramètres quantitatifs de CT de coffre ont fourni des résultats de risque de mortalité qui étaient compatibles avec les modèles cliniques de prévision64. Malgré leur potentiel apparent, les biomarqueurs basés sur l’imagerie sont actuellement mieux considérés au niveau de la population, car leur utilité clinique chez les patients individuels n’a pas été établie.
Réponse au traitement
Le cyclophosphamide et le mofetil mycophénolate procurent des avantages modestes chez les patients atteints de SSc-ILD. Dans l’étude historique sur les poumons de Sclérodermie I, le traitement cyclophosphamide a conduit à une progression plus lente de la fibrose par rapport au placebo65. Plus récemment, l’étude sur les poumons de Sclérodermie II a rapporté une efficacité similaire et une meilleure tolérabilité avec le mycophénolate mofetil par rapport au cyclophosphamide66. Cependant, il reste un besoin d’amélioration des options de traitement pour les patients atteints de SSc-ILD. Les thérapies actuellement étudiées comprennent les anticorps monoclonaux (p. ex. rituximab, abituzumab), les agents antifibrotiques (p. ex., nintedanib, pirfenidone), l’inhibiteur direct de la thrombine dabigatran, l’inhibiteur du protéasome bortezomib et la transplantation hématopoïétique de cellules souches19,67.
Analyses hrct en série montrant la progression de la maladie chez un patient atteint de SSc-ILD
Les évaluations hrct effectuées à différents points de temps peuvent être utilisées pour étudier la progression de la maladie. La figure 7 montre deux séries d’images axiales et coronales hrct de coffre prises 10 ans d’intervalle dans un patient avec SSc-ILD. Les images axiales et coronales initiales (Figure 7A,B) de la poitrine HRCT montrent l’opacité et la réticulation prédominantes basilar de sol-verre avec la bronchiectasis de traction douce et l’épargne subpleural compatible avec NSIP dans ce patient avec SSc. Ce dernier ensemble d’images (Figure 7C, D) prises 10 ans plus tard, montrent une réticulation accrue et la bronchiolectasis de traction aux bases pulmonaires avec diminution de l’opacité du verre moulu sur les images axiales et coronales (Figure 7C,D) de la poitrine CT compatible avec une légère aggravation de la fibrose pulmonaire. Les balayages en série de HRCT peuvent également être utilisés pour surveiller la réponse de traitement68,69,70; ceci a été démontré dans l’étude de poumon de Sclérodermie II, dans laquelle les scores de diagnostic par ordinateur-aidé basés sur des balayages de HRCT ont été utilisés pour comparer l’efficacité du cyclophosphamide avec le mofetil de mycophénolate dans les patients présentant SSc-ILD68.
| Phase | Détecteur Collimation | Tension (kV) | Courant (mAs) | numériser Intervalle | Terrain | Rotation | Courant de tube Modulation |
| Supine inspiratoire | Hélicoïdale 1,2 mm | 120 (peut être abaissé) | 230 (peut être abaissé) | N/A | ~1.0 | 0,5 seconde ou plus rapide | Sur |
| Expiration de la supination | Axial 2 x 1,0 mm | 120 | 150 | 20 mm | N/A | 1,0 seconde | Sur |
| Inspirateur enclin | Axial 2 x 1,0 mm | 120 | 150 | 20 mm | N/A | 1,0 seconde | Sur |
Tableau 1 : Paramètres d’acquisition de tomographie calculée37. N/A = non applicable.
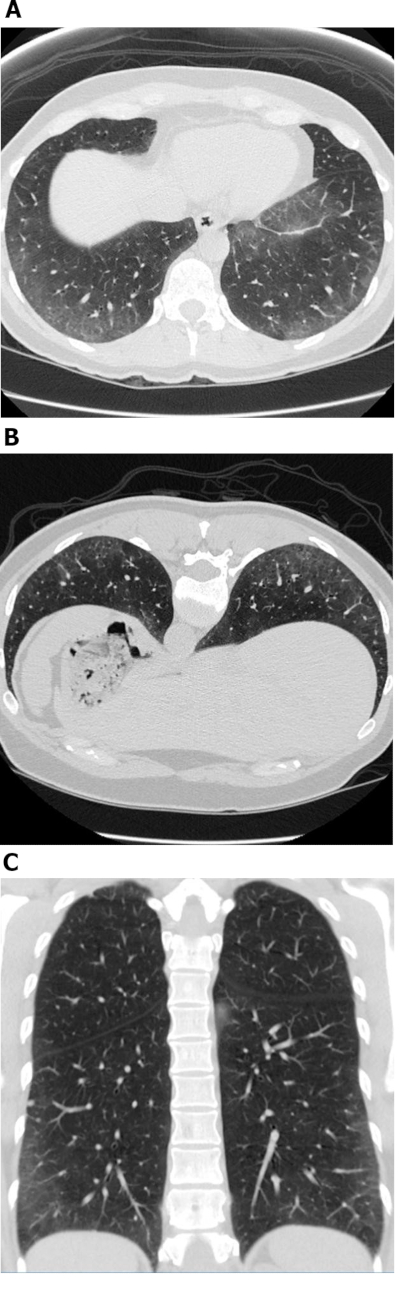
Figure 1: Sclérose systémique avec un modèle cellulaire de la maladie du NSIP. Les images de tomographie calculée à haute résolution (Axial( A ), sujettes (B) et coronales (C) montrent toutes de vastes opacités périphériques et basales prédominantes en verre au sol; ce sont des observations typiques avec NSIP. Le manque de bronchiectasis de traction est suggestif d’un modèle nsip cellulaire de la maladie. NSIP = pneumonie interstitielle non spécifique. Veuillez cliquer ici pour voir une version plus grande de ce chiffre.
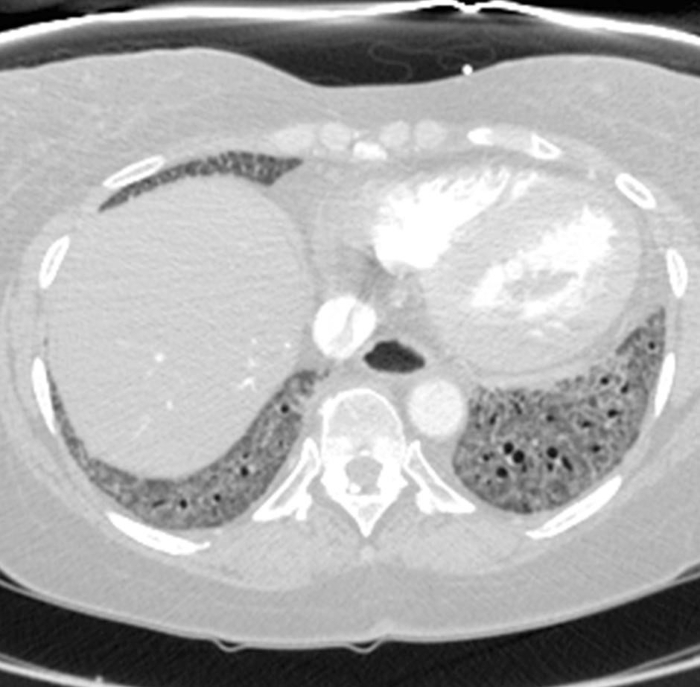
Figure 2: Sclérose systémique avec un modèle de pneumonie interstitielle non spécifique fibrotique de la maladie. L’image de tomographie calculée axiale montre des opacités étendues, basales-prédominantes de sol-verre avec la bronchiectasis associée de traction. Notamment, l’œsophage montre une dilatation marquée; c’est typique de la sclérodermie. Veuillez cliquer ici pour voir une version plus grande de ce chiffre.
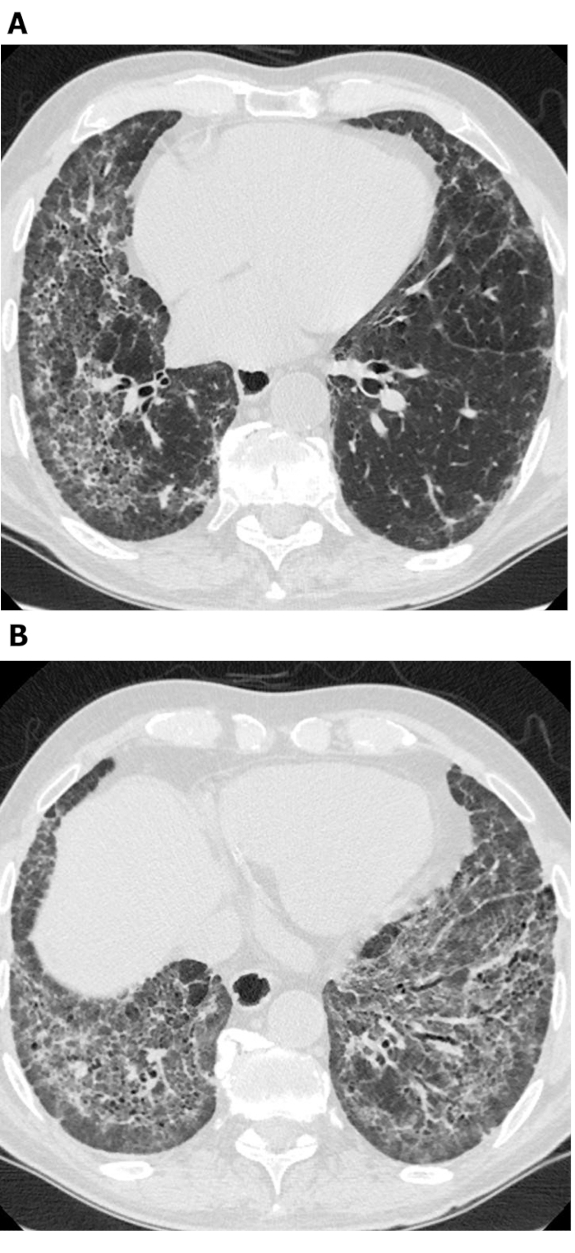
Figure 3: Sclérose systémique avec un modèle fibrotique NSIP. Les images de tomographie calculée à haute résolution axiales (A et B) montrent de vastes opacités en verre moulu, une réticulation, une distorsion architecturale et une bronchiectasie de traction. Notamment, l’épargne subpleural est apparente; ceci est typique du NSIP et est vu dans environ 50% de tous les cas. NSIP = pneumonie interstitielle non spécifique. Veuillez cliquer ici pour voir une version plus grande de ce chiffre.
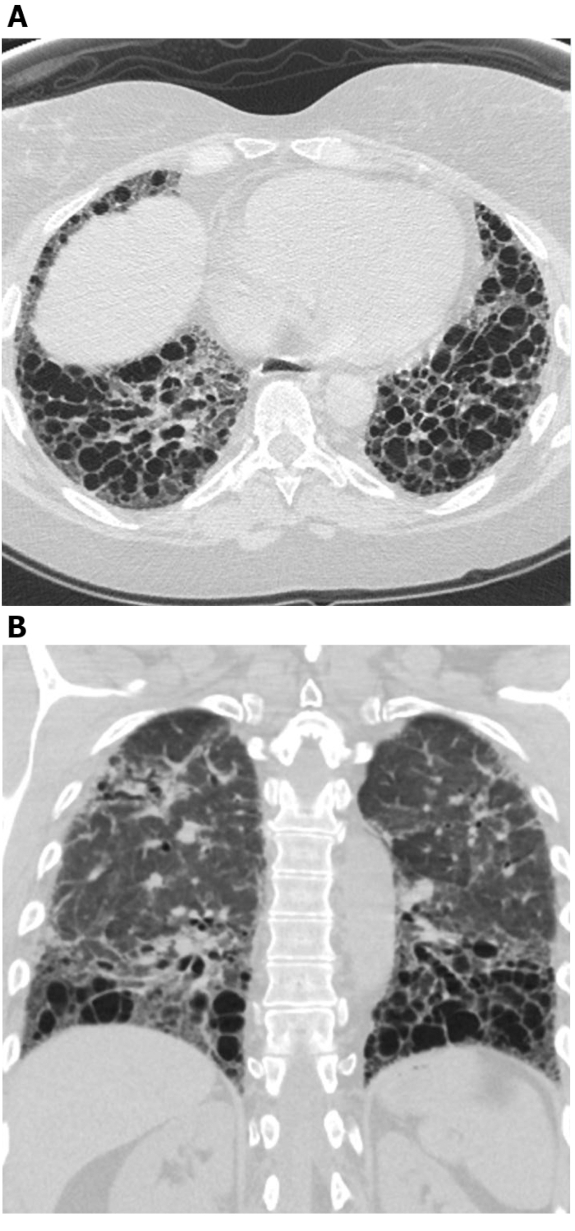
Figure 4: Sclérose systémique avec bronchiectasis de traction exubérante. Les images de tomographie calculée à haute résolution de la zone axiale (A) et coronale (B) montrent une bronchiectasie de traction prédominante de zone pulmonaire moyenne et inférieure étendue. Bien que cela puisse être confondu avec le nid d’abeilles, les zones cystiques se connectent les unes avec les autres et épargnent le poumon sous-pleural immédiat ; c’est typique de la bronchiectasie. Veuillez cliquer ici pour voir une version plus grande de ce chiffre.
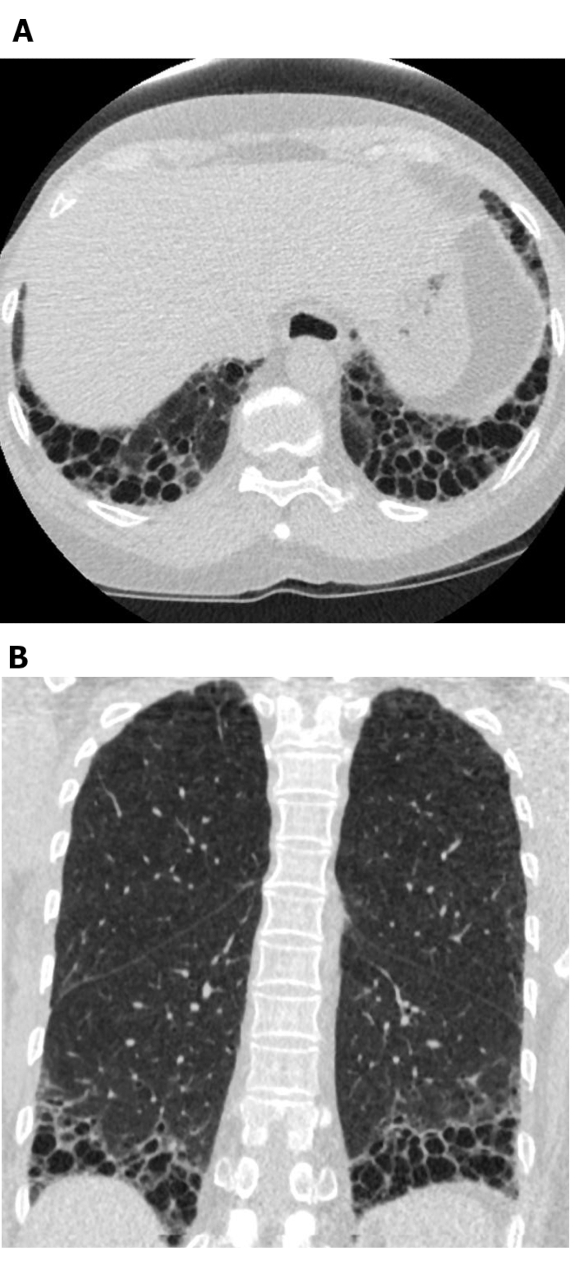
Figure 5: Sclérose systémique avec un modèle uIP de la fibrose pulmonaire. Les images de tomographie calculée axiale (A) et coronale (B) montrent des bronchiectasies périphériques et basaux prédominantes de nid d’abeille et de traction en accord avec le modèle typique d’UIP de la fibrose pulmonaire. Notez l’œsophage dilaté (attribuable à la sclérodermie) et le nid d’abeilles « exubérant » (suggestif de l’ILD lié à la maladie des tissus conjonctifs plutôt qu’à la fibrose pulmonaire idiopathique). UIP = pneumonie interstitielle habituelle. Veuillez cliquer ici pour voir une version plus grande de ce chiffre.
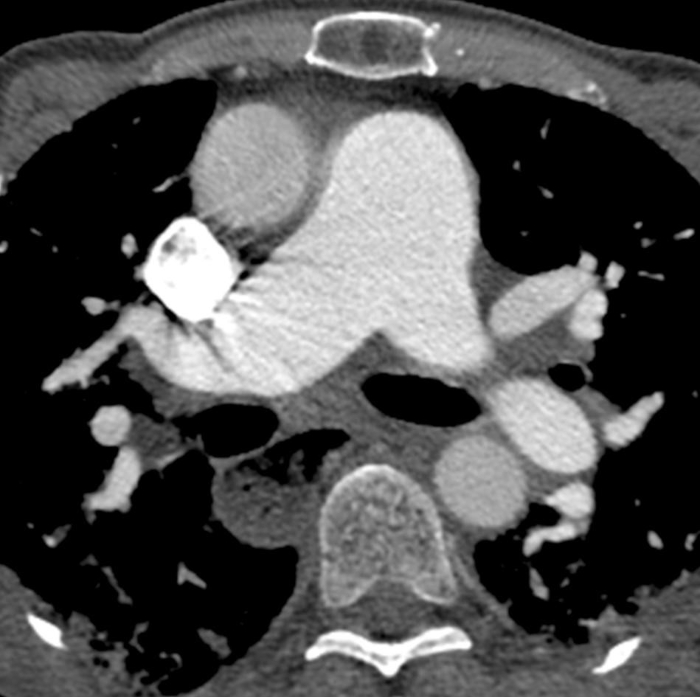
Figure 6: Sclérose systémique avec hypertension pulmonaire et œsophage dilaté. La tomographie calculée de coffre contrastée montre l’agrandissement marqué du tronc pulmonaire, avec une plus grande mesure que l’aorte ascendante adjacente qui suggère l’hypertension pulmonaire sous-jacente. L’œsophage est nettement dilaté; ceci est attribuable à la sclérodermie. Veuillez cliquer ici pour voir une version plus grande de ce chiffre.
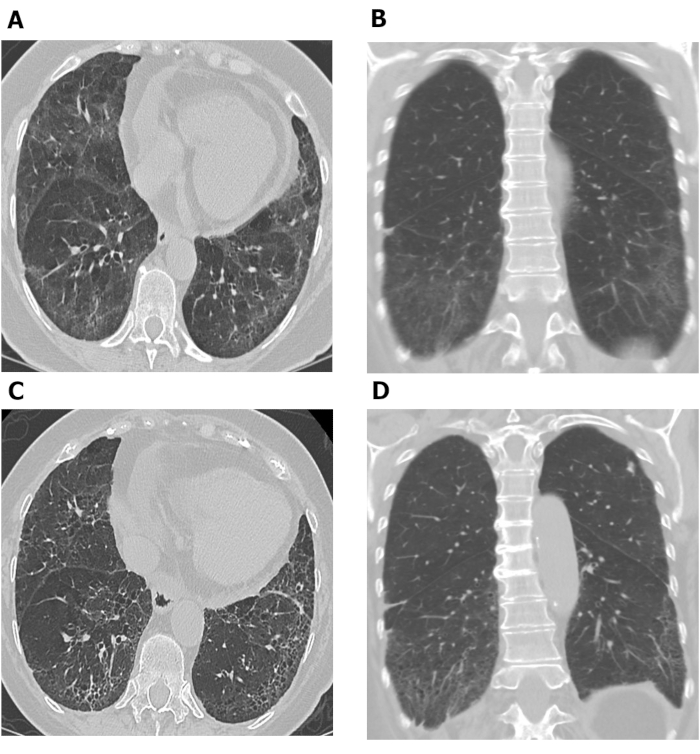
Figure 7: Images en série de HRCT de coffre montrant la progression de la fibrose pulmonaire dans le patient avec SSc-ILD. Les images axiales (A) et coronales (B) de la poitrine HRCT montrent l’opacité et la réticulation prédominantes basilaires de sol-verre avec la bronchiectasis de traction douce et l’épargne subpleural compatible avec la pneumonie interstitielle non spécifique dans ce patient avec SSc. Après 10 ans, la réticulation accrue et la bronchiolectasis de traction aux bases de poumon avec la diminution de l’opacité de sol-verre sont observées sur les images axiales (C) et coronal (D) de HRCT de coffre, compatibles avec l’aggravation douce de la fibrose pulmonaire. HRCT = tomographie calculée à haute résolution; SSc-ILD = maladie pulmonaire interstitielle associée à la sclérodermie systémique. Veuillez cliquer ici pour voir une version plus grande de ce chiffre.
Discussion
Bien que le HRCT soit actuellement la méthode d’imagerie définitive pour diagnostiquer et évaluer SSc-ILD, il utilise des rayonnements ionisants et est relativement coûteux. Les radiographies thoraciques peuvent être entreprises à la place, bien que celles-ci ne facilitent pas le diagnostic différentiel dans la même mesure que hrct, et une radiographie normale de coffre n’élimine pas la possibilité de l’ILD. Peut-être la meilleure utilisation des radiographies thoraciques est de surveiller la maladie progressive entre les balayages de HRCT et pour l’exclusion de la maladie compliquée, telle que la pneumonie infectieuse, dans le cadre de l’aggravation aiguë des symptômes.
Une limitation perçue de hrct est l’exposition de rayonnement. Comme décrit précédemment, de nouvelles méthodes de ct scans peuvent permettre de réduire l’exposition aux radiations31, et en outre, les scanners CT actuels fournissent une gamme de techniques avancées qui offrent la possibilité à l’avenir de réduire l’exposition aux rayonnements à des niveaux de radiographie presque thoracique. Alternativement, des méthodes d’imagerie telles que l’IRM ou l’échographie pulmonaire pourraient potentiellement être utilisées pour éviter d’exposer le patient à la radiation à l’avenir32,71,72,73. Nous croyons que, bien qu’il y ait des considérations de risque-bénéfice associées à l’utilisation d’imagerie, les avantages de la CT dans le diagnostic et la gestion des patients l’emportent de loin sur les risques potentiels.
Les données d’imagerie, en particulier hrct, fournissent sans doute l’information la plus importante pour permettre le diagnostic de SSc-ILD. L’examen détaillé des modèles et des dispositifs des balayages de HRCT est habituellement suffisant pour distinguer SSc-ILD d’autres maladies pulmonaires, avec l’avantage d’éviter la nécessité d’une procédure invasive de biopsie.
L’évaluation visuelle des balayages de HRCT introduit un degré de subjectivité et la possibilité de variabilité inter-observateur. Les méthodes informatiques d’interprétation de l’analyse hrct ont été étudiées comme une approche possible pour améliorer la précision63,74. Par exemple, des approches quantitatives pour l’évaluation de la fibrose pulmonaire ou l’étendue de la maladie peuvent être utilisées pour évaluer la réponse au traitement68,,70,75. Cependant, ces méthodes ne sont pas largement utilisées dans la pratique clinique quotidienne en ce moment.
Nous espérons que l’information présentée dans ce manuscrit servira de guide pratique pour aider les médecins à utiliser des balayages de HRCT pour diagnostiquer SSc-ILD et déterminer le pronostic. Les méthodes améliorées pour obtenir des images et pour interpréter des balayages ont le potentiel de réduire l’exposition des patients aux rayonnements et d’améliorer la précision diagnostique/pronostique.
Déclarations de divulgation
Jonathan Chung ne déclare aucun conflit d’intérêts potentiel en ce qui concerne la recherche décrite, la paternité et/ou la publication de cet article; Christopher Walker déclare la réception des redevances d’Amirsys (Elsevier); et Stephen Hobbs déclare la réception des redevances d’Elsevier et Wolters Kluwer Health. La publication en libre accès de cet article est parrainée par Boehringer Ingelheim Pharmaceuticals, Inc.
L’auteur(s) répond aux critères d’auteur recommandés par le Comité international des rédacteurs en chef de revues médicales (ICMJE). Les auteurs n’ont reçu aucune compensation directe liée au développement de la vidéo. Le support d’écriture médicale pour le script vidéo a été fourni par Leon Newman, PhD, de GeoMed, une compagnie d’Ashfield, qui a été contractée et financée par Boehringer Ingelheim Pharmaceuticals, Inc. (BIPI). Le BIPI a eu l’occasion d’examiner la vidéo finale pour l’exactitude médicale et scientifique ainsi que pour des considérations de propriété intellectuelle.
Remerciements
Les auteurs répondent aux critères d’auteur recommandés par le Comité international des rédacteurs en chef de revues médicales (ICMJE). Les auteurs n’ont reçu aucune compensation directe liée à l’élaboration du manuscrit. L’aide à la rédaction a été fournie par Ken Sutor, BSc, de GeoMed, une société Ashfield, qui fait partie d’UDG Healthcare plc, qui a été contractée et financée par Boehringer Ingelheim Pharmaceuticals, Inc. (BIPI). Le BIPI a eu l’occasion d’examiner le manuscrit pour des raisons médicales et scientifiques ainsi que pour des considérations de propriété intellectuelle.
matériels
| Name | Company | Catalog Number | Comments |
| CT scanners | Philips | NA | Multiple |
Références
- Denton, C. P., Khanna, D. Systemic sclerosis. Lancet. 390 (10103), 1685-1699 (2017).
- Arnett, F. C., et al. Familial occurrence frequencies and relative risks for systemic sclerosis (scleroderma) in three United States cohorts. Arthritis & Rheumatism. 44 (6), 1359-1362 (2001).
- Barnes, J., Mayes, M. D. Epidemiology of systemic sclerosis: incidence, prevalence, survival, risk factors, malignancy, and environmental triggers. Current Opinion in Rheumatology. 24 (2), 165-170 (2012).
- Marie, I., Gehanno, J. F. Environmental risk factors of systemic sclerosis. Seminars in Immunopathology. 37 (5), 463-473 (2015).
- Silman, A. J. Epidemiology of scleroderma. Annals of the Rheumatic Diseases. 50, 846-853 (1991).
- Scholand, M. B., et al. Interstitial lung disease in systemic sclerosis: diagnosis and management. Rheumatology. 1, 008 (2012).
- Solomon, J. J., et al. Scleroderma lung disease. European Respiratory Review. 22 (127), 6-19 (2013).
- Walker, U. A., et al. Clinical risk assessment of organ manifestations in systemic sclerosis: a report from the EULAR Scleroderma Trials And Research group database. Annals of the Rheumatic Diseases. 66 (6), 754-763 (2007).
- Hinchcliff, M., Fischer, A., Schiopu, E., Steen, V. D., Investigators, P. Pulmonary hypertension assessment and recognition of outcomes in scleroderma (PHAROS): baseline characteristics and description of study population. The Journal of Rheumatology. 38 (10), 2172-2179 (2011).
- Giacomelli, R., et al. Interstitial lung disease in systemic sclerosis: current and future treatment. Rheumatology International. 37 (6), 853-863 (2017).
- Sanchez-Cano, D., et al. Interstitial lung disease in systemic sclerosis: data from the spanish scleroderma study group. Rheumatology International. 38 (3), 363-374 (2018).
- Silver, K. C., Silver, R. M. Management of systemic-sclerosis-associated interstitial lung disease. Rheumatic Diseases Clinics of North America. 41 (3), 439-457 (2015).
- Fischer, A., Kong, A. M., Swigris, J. J., Cole, A. L., Raimundo, K. All-cause healthcare costs and mortality in patients with systemic sclerosis with lung involvement. The Journal of Rheumatology. 45 (2), 235-241 (2018).
- Tyndall, A. J., et al. Causes and risk factors for death in systemic sclerosis: a study from the EULAR Scleroderma Trials and Research (EUSTAR) database. Annals of the Rheumatic Diseases. 69 (10), 1809-1815 (2010).
- Herzog, E. L., et al. Review: interstitial lung disease associated with systemic sclerosis and idiopathic pulmonary fibrosis: how similar and distinct. Arthritis & Rheumatology. 66 (8), 1967-1978 (2014).
- Rubio-Rivas, M., Royo, C., Simeon, C. P., Corbella, X., Fonollosa, V. Mortality and survival in systemic sclerosis: systematic review and meta-analysis. Seminars in Arthritis and Rheumatism. 44 (2), 208-219 (2014).
- Stock, C., et al. Serum KL-6 as a marker of disease progression in SSc-ILD. European Respiratory Journal. 52, (2018).
- Winstone, T. A., et al. Predictors of mortality and progression in scleroderma-associated interstitial lung disease: a systematic review. Chest. 146 (2), 422-436 (2014).
- Khanna, D., et al. Ongoing clinical trials and treatment options for patients with systemic sclerosis-associated interstitial lung disease. Rheumatology (Oxford). 58 (4), 567-579 (2019).
- Behr, J., Furst, D. E. Pulmonary function tests. Rheumatology (Oxford). 47, 65-67 (2008).
- Hax, V., et al. Clinical algorithms for the diagnosis and prognosis of interstitial lung disease in systemic sclerosis. Seminars in Arthritis and Rheumatism. 47 (2), 228-234 (2017).
- Molberg, O., Hoffmann-Vold, A. M. Interstitial lung disease in systemic sclerosis: progress in screening and early diagnosis. Current Opinion in Rheumatology. 28 (6), 613-618 (2016).
- Raghu, G., Goldman, L., Schafer, A. I. Interstital lung disease. Goldman-Cecil Medicine. , 575-588 (2016).
- Showalter, K., et al. Performance of forced vital capacity and lung diffusion cutpoints for associated radiographic interstitial lung disease in systemic sclerosis. The Journal of Rheumatology. 45 (11), 1572-1576 (2018).
- Suliman, Y. A., et al. Brief report: pulmonary function tests: high rate of false-negative results in the early detection and screening of scleroderma-related interstitial lung disease. Arthritis & Rheumatology. 67 (12), 3256-3261 (2015).
- Roth, M. D., et al. Predicting treatment outcomes and responder subsets in scleroderma-related interstitial lung disease. Arthritis & Rheumatology. 63 (9), 2797-2808 (2011).
- Kalra, M. K., Maher, M. M., Rizzo, S., Kanarek, D., Shepard, J. A. Radiation exposure from chest CT: issues and strategies. Journal of Korean Medical Science. 19 (2), 159-166 (2004).
- Siegel, J. A., Pennington, C. W., Sacks, B., Welsh, J. S. The birth of the illegitimate linear no-threshold model: an invalid paradigm for estimating risk following low-dose radiation exposure. American Journal of Clinical Oncology. 41 (2), 173-177 (2018).
- Frauenfelder, T., et al. Screening for interstitial lung disease in systemic sclerosis: performance of high-resolution CT with limited number of slices: a prospective study. Annals of the Rheumatic Diseases. 73 (12), 2069-2073 (2014).
- Kubo, T., et al. Radiation dose reduction in chest CT: a review. American Journal of Roentgenology. 190 (2), 335-343 (2008).
- Nguyen-Kim, T. D. L., et al. The impact of slice-reduced computed tomography on histogram-based densitometry assessment of lung fibrosis in patients with systemic sclerosis. Journal of Thoracic Disease. 10 (4), 2142-2152 (2018).
- Muller, C. S., Warszawiak, D., Paiva, E. D. S., Escuissato, D. L. Pulmonary magnetic resonance imaging is similar to chest tomography in detecting inflammation in patients with systemic sclerosis. Revista Brasileira de Reumatologia English Edition. 57 (5), 419-424 (2017).
- Pinal-Fernandez, I., et al. Fast 1.5 T chest MRI for the assessment of interstitial lung disease extent secondary to systemic sclerosis. Clinical Rheumatology. 35 (9), 2339-2345 (2016).
- Sverzellati, N. Highlights of HRCT imaging in IPF. Respiratory Research. 14, 3 (2013).
- Lynch, D. A., et al. Diagnostic criteria for idiopathic pulmonary fibrosis: a Fleischner Society White Paper. The Lancet Respiratory Medicine. 6 (2), 138-153 (2018).
- Raghu, G., et al. Diagnosis of idiopathic pulmonary fibrosis. An official ATS/ERS/JRS/ALAT clinical practice guideline. American Journal of Respiratory and Critical Care Medicine. 198 (5), 44-68 (2018).
- . Exam: CT thorax for interstitial lung disease Available from: https://www.pulmonaryfibrosis.org/docs/default-source/medical-community-documents/ct-chest-for-ild-protocol.pdf?sfvrsn=0 (2019)
- Doyle, T. J., Hunninghake, G. M., Rosas, I. O. Subclinical interstitial lung disease: why you should care. American Journal of Respiratory and Critical Care Medicine. 185 (11), 1147-1153 (2012).
- Peroni, D. G., Boner, A. L. Atelectasis: mechanisms, diagnosis and management. Paediatric Respiratory Reviews. 1 (3), 274-278 (2000).
- Branley, H. M. Pulmonary fibrosis in systemic sclerosis: diagnosis and management. Respiratory Medicine CME. 3, 10-14 (2010).
- Engeler, C. E., Tashjian, J. H., Trenkner, S. W., Walsh, J. W. Ground-glass opacity of the lung parenchyma: a guide to analysis with high-resolution CT. American Journal of Roentgenology. 160 (2), 249-251 (1993).
- Goldin, J. G., et al. High-resolution CT scan findings in patients with symptomatic scleroderma-related interstitial lung disease. Chest. 134 (2), 358-367 (2008).
- Strollo, D., Goldin, J. Imaging lung disease in systemic sclerosis. Current Rheumatology Reports. 12 (2), 156-161 (2010).
- Pandey, A. K., et al. Significance of various pulmonary and extrapulmonary abnormalities on HRCT of the chest in scleroderma lung. Indian Journal of Radiology and Imaging. 23 (4), 304-307 (2013).
- Chung, J. H., et al. CT Features of the usual interstitial pneumonia pattern: differentiating connective tissue disease-associated interstitial lung disease from idiopathic pulmonary fibrosis. American Journal of Roentgenology. 210 (2), 307-313 (2018).
- Zhan, X., et al. Differentiating usual interstitial pneumonia from nonspecific interstitial pneumonia using high-resolution computed tomography: the "Straight-edge Sign". Journal of Thoracic Imaging. 33 (4), 266-270 (2018).
- Farrokh, D., Abbasi, B., Fallah-Rastegar, Y., Mirfeizi, Z. The extrapulmonary manifestations of systemic sclerosis on chest high resolution computed tomography. Tanaffos. 14 (3), 193-200 (2015).
- Salaffi, F., et al. Relationship between interstitial lung disease and oesophageal dilatation on chest high-resolution computed tomography in patients with systemic sclerosis: a cross-sectional study. La Radiologia Medica. 123 (9), 655-663 (2018).
- Vonk, M. C., et al. Oesophageal dilatation on high-resolution computed tomography scan of the lungs as a sign of scleroderma. Annals of the Rheumatic Diseases. 67 (9), 1317-1321 (2008).
- Chowaniec, M., Skoczynska, M., Sokolik, R., Wiland, P. Interstitial lung disease in systemic sclerosis: challenges in early diagnosis and management. Reumatologia. 56 (4), 249-254 (2018).
- McCall, R. K., Ravenel, J. G., Nietert, P. J., Granath, A., Silver, R. M. Relationship of main pulmonary artery diameter to pulmonary arterial pressure in scleroderma patients with and without interstitial fibrosis. Journal of Computer Assisted Tomography. 38 (2), 163-168 (2014).
- Pandey, A. K., et al. Predictors of pulmonary hypertension on high-resolution computed tomography of the chest in systemic sclerosis: a retrospective analysis. Canadian Association of Radiologists Journal. 61 (5), 291-296 (2010).
- Raymond, T. E., Khabbaza, J. E., Yadav, R., Tonelli, A. R. Significance of main pulmonary artery dilation on imaging studies. Annals of the American Thoracic Society. 11 (10), 1623-1632 (2014).
- Colaci, M., et al. Lung cancer in scleroderma: results from an Italian rheumatologic center and review of the literature. Autoimmunity Reviews. 12 (3), 374-379 (2013).
- Distler, O., et al. Design of a randomised, placebo-controlled clinical trial of nintedanib in patients with systemic sclerosis-associated interstitial lung disease (SENSCIS). Clinical and Experimental Rheumatology. 35 (4), 75-81 (2017).
- Desai, S. R., et al. CT features of lung disease in patients with systemic sclerosis: comparison with idiopathic pulmonary fibrosis and nonspecific interstitial pneumonia. Radiology. 232 (2), 560-567 (2004).
- Mira-Avendano, I., et al. Interstitial lung disease and other pulmonary manifestations in connective tissue diseases. Mayo Clinic Proceedings. 94 (2), 309-325 (2019).
- Walkoff, L., White, D. B., Chung, J. H., Asante, D., Cox, C. W. The four corners sign: a specific imaging feature in differentiating systemic sclerosis-related interstitial lung disease from idiopathic pulmonary fibrosis. Journal of Thoracic Imaging. 33 (3), 197-203 (2018).
- Kotnur, M. R., Suresh, P., Reddy, V. S., Sharma, T., Salim, N. A. Systemic sclerosis with multiple pulmonary manifestations. Journal of Clinical & Diagnostic Research. 10 (6), 16-17 (2016).
- Goh, N. S., et al. Interstitial lung disease in systemic sclerosis: a simple staging system. American Journal of Respiratory and Critical Care Medicine. 177 (11), 1248-1254 (2008).
- Takei, R., et al. Radiographic fibrosis score predicts survival in systemic sclerosis-associated interstitial lung disease. Respirology. 23 (4), 385-391 (2018).
- Bakker, M. E., et al. Lung density and pulmonary artery diameter are predictors of pulmonary hypertension in systemic sclerosis. Journal of Thoracic Imaging. 32 (6), 391-397 (2017).
- Khanna, D., et al. Predictors of lung function decline in scleroderma-related interstitial lung disease based on high-resolution computed tomography: implications for cohort enrichment in systemic sclerosis-associated interstitial lung disease trials. Arthritis Research & Therapy. 17, 372 (2015).
- Ariani, A., et al. Quantitative chest computed tomography is associated with two prediction models of mortality in interstitial lung disease related to systemic sclerosis. Rheumatology (Oxford). 56 (6), 922-927 (2017).
- Goldin, J., et al. Treatment of scleroderma-interstitial lung disease with cyclophosphamide is associated with less progressive fibrosis on serial thoracic high-resolution CT scan than placebo: findings from the scleroderma lung study. Chest. 136 (5), 1333-1340 (2009).
- Tashkin, D. P., et al. Mycophenolate mofetil versus oral cyclophosphamide in scleroderma-related interstitial lung disease (SLS II): a randomised controlled, double-blind, parallel group trial. The Lancet Respiratory Medicine. 4 (9), 708-719 (2016).
- Distler, O., et al. Nintedanib for Systemic Sclerosis-Associated Interstitial Lung Disease. New England Journal of Medicine. 380, 2518-2528 (2019).
- Cappelli, S., et al. Interstitial lung disease in systemic sclerosis: where do we stand. European Respiratory Review. 24 (137), 411-419 (2015).
- Goldin, J. G., et al. Longitudinal changes in quantitative interstitial lung disease on CT after immunosuppression in the Scleroderma Lung Study II. Annals of the American Thoracic Society. 5 (11), 1286-1295 (2018).
- Wangkaew, S., Euathrongchit, J., Wattanawittawas, P., Kasitanon, N. Correlation of delta high-resolution computed tomography (HRCT) score with delta clinical variables in early systemic sclerosis (SSc) patients. Quantitative Imaging in Medicine and Surgery. 6 (4), 381-390 (2016).
- Kim, H. J., et al. Transitions to different patterns of interstitial lung disease in scleroderma with and without treatment. Annals of the Rheumatic Diseases. 75 (7), 1367-1371 (2016).
- Tardella, M., et al. Ultrasound B-lines in the evaluation of interstitial lung disease in patients with systemic sclerosis: cut-off point definition for the presence of significant pulmonary fibrosis. Medicine (Baltimore). 97 (18), 0566 (2018).
- Hassan, R. I., et al. Lung ultrasound as a screening method for interstitial lung disease in patients with systemic sclerosis. Journal of Clinical Rheumatology. , (2018).
- Wang, Y., Gargani, L., Barskova, T., Furst, D. E., Cerinic, M. M. Usefulness of lung ultrasound B-lines in connective tissue disease-associated interstitial lung disease: a literature review. Arthritis Research & Therapy. 19 (1), 206 (2017).
- Ariani, A., et al. Quantitative CT indexes are significantly associated with exercise oxygen desaturation in interstitial lung disease related to systemic sclerosis. The Clinical Respiratory Journal. 11 (6), 983-989 (2017).
- Kim, H. J., et al. Quantitative texture-based assessment of one-year changes in fibrotic reticular patterns on HRCT in scleroderma lung disease treated with oral cyclophosphamide. European Radiology. 21 (12), 2455-2465 (2011).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon