Method Article
Échographie Doppler veineuse-artérielle continue lors d’une provocation de précharge
Dans cet article
Résumé
La courbe Frank-Starling-Sarnoff est cliniquement importante et décrit la relation entre la précharge cardiaque et le débit. Ce rapport illustre une nouvelle méthode de vélocimétrie Doppler artérielle jugulaire et carotidienne simultanée en tant que substituts transitoires de la précharge et du débit cardiaques, respectivement; cette approche est rendue possible par l’échographie Doppler portable sans fil.
Résumé
Un défi de précharge (PC) est une manœuvre clinique qui, premièrement, augmente le remplissage cardiaque (c.-à-d. la précharge) et, deuxièmement, calcule le changement dans le débit cardiaque. Fondamentalement, un PC est une approche au chevet du patient pour tester la courbe Frank-Starling-Sarnoff (c.-à-d. la « fonction cardiaque »). Normalement, cette courbe a une pente raide telle qu’un petit changement dans la précharge cardiaque génère un changement important dans le volume de l’AVC (SV) ou le débit cardiaque. Cependant, dans divers états pathologiques, la pente de cette relation s’aplatit de telle sorte que l’augmentation du volume dans le cœur entraîne peu d’augmentation du SV. Dans ce scénario pathologique, une précharge cardiaque supplémentaire (p. ex. liquide intraveineux) est peu susceptible d’être physiologiquement efficace et pourrait entraîner des dommages si la congestion des organes évolue. Par conséquent, l’inférence à la fois de la précharge cardiaque et du débit est cliniquement utile car elle peut guider la réanimation liquidienne intraveineuse (IV). En conséquence, l’objectif de ce protocole est de décrire une méthode pour suivre simultanément les substituts de la précharge cardiaque et de la sortie à l’aide d’une nouvelle échographie portable sans fil lors d’un défi de précharge bien validé.
Introduction
À sa fondation, la courbe Frank-Starling-Sarnoff décrit la relation entre la précharge cardiaque et le débit 1,2,3,4. Historiquement, cette courbe est représentée en traçant la pression auriculaire droite sur l’abscisse et le débit cardiaque ou volume de l’AVC (SV)5 en ordonnée. L’évaluation de la pente de cette courbe est cliniquement importante car la relation entre le remplissage cardiaque et le débit est dynamique; Ainsi, la pente de la courbe informe la stratégie de réanimation 1,4. Plus précisément, si la pente de la courbe Frank-Starling-Sarnoff (c.-à-d. « fonction cardiaque ») est raide, l’augmentation de la précharge (p. ex. administration de liquide intraveineux) augmente le rendement. En revanche, si la pente de la courbe de la fonction cardiaque est peu profonde, l’apport de liquide intraveineux (IV) n’augmente pas la SV2.
Savoir quand le liquide IV augmente ou n’augmente pas le SV est important afin que le clinicien traitant puisse éviter le liquide physiologiquement inefficace4,6, en d’autres termes, le scénario dans lequel l’administration de liquide IV à un patient n’augmente pas la SV 7,8. L’identification de cet état clinique relativement courant est obtenue via un défi de précharge (PC), qui est une manœuvre clinique qui « teste » la pente de la courbe de la fonction cardiaque3. Un PC est obtenu en augmentant rapidement le remplissage cardiaque et en mesurant le changement dans SV9. Comme ci-dessus, le liquide IV peut agir comme un PC, tout comme les manœuvres gravitationnelles telles que déplacer la tête sous le niveau du cœur (c.-à-d. positionnement de Trendelenburg)10 ou passer d’une position semi-couchée à une position couchée avec les jambes surélevées (c.-à-d. une élévation passive des jambes)11. En fait, le lèvement passif des jambes (DPP) est un PC bien accepté et bien validé qui est utilisé dans les unités de soins intensifs modernes et recommandé par les experts avant l’administration de liquide IV pendant la réanimation de la septicémie 4,12. Fait important, il est suggéré que pendant le DPP, le clinicien mesure à la fois la précharge cardiaque (p. ex., le changement de la pression auriculaire droite) et le débit (p. ex., le changement de SV) pour tester adéquatement la courbe de la fonction cardiaque13. Cependant, le premier est rarement effectué car les mesures simultanées sont lourdes et un cathéter invasif placé dans l’oreillette droite est souvent nécessaire.
Les substituts échographiques du remplissage et du débit cardiaques ont gagné en popularité au cours des dernières décennies, en particulier dans les services d’urgence et les unités de soins intensifs 2,14. Plus précisément, l’évaluation simultanée d’une grande veine et d’une grosse artère agit comme substitut de la précharge et du débit cardiaques, respectivement 2,15. Par exemple, des changements morphologiques dans la grande veine Doppler ont été trouvés pour suivre la pression auriculaire droite - cela est vrai pour la jugulaire interne 16,17,18, hépatique et veine porte 19, veine cavesupérieure 20, veine caveinférieure 21, veines fémorales 22 et même veines intrarénales 23. Ainsi, la vélocimétrie Doppler veineuse fonctionne comme un substitut pour le remplissage cardiaque2. Cependant, le Doppler d’une grosse artère peut suivre transitoirement les changements dans le débit cardiaque. Par exemple, les mesures du temps systolique commun de l’artère carotide 24,25, de la vitesse 26,27,28 et du débit 29,30 se sont révélées prometteuses pour détecter les changements de SV.
Une nouvelle échographie Doppler sans fil, portable et à ondes continues qui fait sonner simultanément la veine jugulaire interne et l’artère carotide commune a déjà été décrite 14,15,27,28,31,32,33,34,35,36 . Ici, une méthode utilisant cet appareil lors d’un PC clinique couramment utilisé - la levée de jambe passive - est illustrée. De plus, les morphologies Doppler jugulaire interne et artérielle carotidienne commune pendant la PC sont décrites comme des substituts possibles de la précharge et du débit cardiaques, respectivement. Ce protocole est cliniquement important car il fournit une base à la fois pratique et physiologique pour l’étude future des patients. Par exemple, les patients hospitalisés (p. ex. milieu périopératoire, septicémie, gravement malade) et les patients externes (p. ex. insuffisance cardiaque congestive, dialyse) pourraient être surveillés par la méthode ou les modifications de celle-ci décrite ci-dessous.
Protocole
Lors de l’exécution d’un défi de précharge à l’aide du système d’échographie Doppler portable sans fil, l’utilisateur doit prendre en compte un certain nombre d’étapes critiques. Un consentement écrit et éclairé a été obtenu pour ce protocole; l’étude a été examinée et approuvée par le Comité d’éthique de la recherche d’Horizon Santé-Nord. Les procédures suivies étaient conformes aux normes éthiques locales du comité de l’expérimentation humaine et à la Déclaration d’Helsinki de 1975.
1. Identifier un patient approprié
- Identifiez un patient sur lequel l’échographie Doppler portable sera placé. Assurez-vous que le patient est calme et relativement immobile pour minimiser la phonation et la déglutition pendant toute la durée de l’évaluation (1-5 min).
- Placez le patient en position semi-couchée ou semi-Fowler dans le lit d’hôpital ou la civière. Plus précisément, ajustez le lit de manière à ce que le torse soit à un angle de 30 à 45 ° au-dessus de l’horizontale.
2. Obtention des signaux Doppler de l’artère carotide et de la jugulaire interne
- Allumez l’échographie Doppler portable en appuyant sur le bouton rond au centre de l’appareil à ultrasons. Des lumières bleues autour de la périphérie du bouton clignotent, signalant que l’appareil est allumé et prêt à être jumelé avec un appareil intelligent.
- Activez l’application dédiée sur l’appareil intelligent. Appuyez sur le bouton de démarrage de l’application Smart Device. Observez la liste affichée sur l’application montrant les appareils à ultrasons détectables et portables à proximité physique de l’appareil intelligent. Faites correspondre le numéro apposé sur la face de l’appareil à ultrasons souhaité à l’appareil indiqué dans la liste des applications. Appuyez sur connecter pour coupler l’appareil à ultrasons souhaité à l’application.
- Confirmez que l’appareil à ultrasons souhaité est jumelé en observant des lumières blanches clignotantes autour du bouton au centre de l’appareil. Appuyez sur Corriger sur l’application Smart Device pour terminer le couplage.
- Appliquez une petite quantité de gel à ultrasons sur la grande face du coin du transducteur à l’arrière de l’appareil à ultrasons.
REMARQUE: L’application de gel produit un artefact de signal Doppler caractéristique, qui peut être vu sur l’application Smart Device. - Appuyez sur la grande face du coin du transducteur pour vous assurer que l’appareil est actif et couplé à l’application Smart Device. Assurez-vous que le volume de l’application Smart Device est activé en appuyant sur le bouton de l’icône de volume dans le coin supérieur droit de l’affichage de l’application.
- Avec le cou du patient légèrement étendu, notez la proéminence laryngée et tenez l’appareil à ultrasons de sorte que la grande face du coin du transducteur soit orientée vers le bas vers le cœur du patient. Placez le coin de l’appareil sur la face latérale de la proéminence laryngée du patient. Recherchez une réponse audio et visuelle sur l’application Smart Device : la partie supérieure de l’application affichera un spectre de forme d’onde pour l’artère carotide et la veine jugulaire. La partie inférieure de l’application quantifie le temps d’écoulement corrigé (ccFT) pour chaque cycle cardiaque, affiché sous forme de barres vertes.
- Faites glisser latéralement la face du transducteur sur le cou du patient à partir d’un plan perpendiculaire défini par la trachée jusqu’à ce que le spectre Doppler carotidien soit détecté visuellement et sonorement sur l’application Smart Device.
REMARQUE: Chez la plupart des patients, les spectres Doppler audio et visuels de l’artère carotide et de la veine jugulaire sont détectés à quelques centimètres de la bordure laryngée latérale.
3. Optimisation de l’artère carotide et des signaux Doppler jugulaires internes
- Tout en maintenant l’appareil en place, observez le spectre Doppler carotidien et ses caractéristiques sur le dessus de l’écran de l’application. Un bon signal Doppler de l’artère carotide est identifié par sa course ascendante caractéristique avec un bon rapport signal sur bruit et une encoche dicrotique claire, qui délimite l’extrémité de la systole mécanique. L’application commencera automatiquement à tracer le spectre Doppler une fois qu’un signal suffisamment fort est obtenu, indiqué par une ligne blanche autour du maximum de la forme d’onde.
- Tout en maintenant l’appareil en place, observez les mesures de vitesse à l’aide de l’échelle située en haut à gauche de l’écran de l’appareil intelligent. En utilisant l’auto-traçage sur l’artère carotide maximum, assurez-vous que la trace est dans une plage typique. La vitesse systolique maximale de l’artère carotide est généralement comprise entre 50 cm/s et 120 cm/s, et la vitesse diastolique terminale est généralement inférieure à 20 cm/s.
- Faites glisser lentement l’appareil à ultrasons latéralement légèrement de quelques millimètres tout en regardant l’encoche dicrotique sur le spectre artériel pour vous assurer qu’un nadir de vitesse clair est observé de manière fiable. Si la vitesse dicrotique de l’encoche devient difficile à voir, répétez cette étape, mais faites glisser l’appareil à ultrasons médialement.
- Répétez les étapes 3.1-3.3 sur l’artère carotide controlatérale pour évaluer la présence d’une vitesse d’encoche dicrotique plus claire.
- Après avoir observé la présence d’une vitesse d’encoche dicrotique claire sur les deux artères carotides, sélectionnez le côté du cou auquel l’appareil sera collé. Choisissez le côté avec la vitesse d’encoche dicrotique la plus évidente. Si les deux côtés du cou ont des vitesses d’encoche dicrotiques également acceptables, choisissez le côté du cou avec le spectre Doppler jugulaire interne le plus robuste.
4. Adhérence de l’appareil à ultrasons au cou
- Préparez-vous à coller l’appareil à l’artère carotide choisie en notant visuellement où sur le cou le meilleur signal a été obtenu. Si nécessaire, utilisez un stylo de marquage de la peau pour identifier la position de placement optimale. Soulevez l’appareil du cou et retirez le support protecteur de l’adhésif fixé à l’appareil à ultrasons.
- Observez la face du transducteur sur l’appareil à ultrasons et déterminez s’il reste une quantité suffisante de gel à ultrasons. Si nécessaire, réappliquez une petite quantité de gel à ultrasons sur le visage du transducteur. Retirez l’excès de gel à ultrasons du cou qui peut être resté pendant la découverte du signal, car cela peut interférer avec l’adhérence de l’appareil.
- Remettez le dispositif au cou à l’endroit identifié à l’étape 4.1, avec la grande face du coin du transducteur pointant vers le bas vers le cœur. Lissez les ailes de l’adhésif sur le cou. Retirez le support protecteur des extrémités de l’adhésif après avoir serré; Placez le filmage contre la peau pour fixer complètement l’appareil au cou. Surveillez les spectres carotidien et jugulaire tout au long de l’adhésion pour vous assurer que le signal n’est pas perdu.
5. Effectuer un défi de précharge via un levage passif de la jambe (DPP)
- Assurez-vous que le patient est en position semi-couchée sur le lit d’hôpital ou la civière, comme indiqué à l’étape 1.2.
- Effacez les données de l’application Smart Device en appuyant sur Redémarrer sur l’application Smart Device. Appuyez sur Commencer l’évaluation sur l’application Smart Device pour obtenir les mesures de base pour le levage passif des jambes (DPP). Commencez par 30 à 60 s de repos avec le patient en position semi-couchée sur le lit d’hôpital ou la civière. Recherchez un marqueur affiché dans la partie inférieure de l’affichage de l’application pour indiquer le début de l’évaluation.
- Préparer les mesures nécessaires pour effectuer un DPP (p. ex., obtenir de l’aide infirmière supplémentaire au besoin).
- Une fois prêt à effectuer un DPP, appuyez sur marquer l’intervention sur l’application de l’appareil intelligent pour signifier le début du défi de préchargement (dans ce cas, un DPP). Recherchez un marqueur affiché sur la partie inférieure de l’affichage de l’application pour indiquer le début de l’intervention. Effectuer un DPP; Sans toucher le patient, repositionnez le lit d’hôpital ou la civière de manière à ce que le torse soit déplacé vers le bas vers l’horizontale et que les jambes soient soulevées à 30-45 ° au-dessus de l’horizontale.
REMARQUE: L’utilisateur doit prendre grand soin de garder le patient complètement passif pendant cette manœuvre. - Gardez le patient en position PLR pendant 90-120 s.
REMARQUE: Tout au long de la manœuvre, il est impératif que le patient garde son cou complètement immobile afin de ne pas modifier l’angle d’insonation entre la face du transducteur et les vaisseaux du cou. Si nécessaire, stabilisez manuellement le cou du patient. - Observer le spectre Doppler jugulaire sur l’application de l’appareil intelligent pendant l’intervention; Évaluer les changements dans la vitesse veineuse jugulaire absolue et son profil comme substitut de la pression veineuse jugulaire.
- Observer l’évolution des barres vertes sur l’application smart device lors de l’intervention; évaluer les changements dans le ccFT avant et après le début du défi de précharge. L’application Smart Device quantifie automatiquement le ccFT pour chaque cycle cardiaque et le représente sous la forme d’une barre verte.
- Une fois l’intervention terminée, appuyez sur fin d’évaluation sur l’application Smart Device. Recherchez un marqueur qui sera affiché dans la partie inférieure de l’affichage de l’application pour indiquer la fin de l’évaluation.
- Ramener le patient à sa position de base, semi-couchée.
- Si vous le souhaitez, appuyez sur Enregistrer sur l’application Smart Device pour enregistrer l’évaluation et exporter les fichiers de données (voir les notes de données supplémentaires pour plus de détails).
6. Observer les changements dans le temps d’écoulement corrigé de la carotide (ccFT) sur l’application d’appareil intelligent après l’évaluation terminée
- Observez les changements évalués dans le ccFT affichés dans une case jaune en bas à droite de l’application.
REMARQUE: L’application Smart Device quantifie automatiquement les changements de ccFT entre les mesures de référence enregistrées et les mesures de provocation / intervention avant charge. - Appuyez sur enregistrer sur l’application et attendez que les données soient divisées en fichiers suivants: deux fichiers au format .txt contenant des données IQ et Tick du matériel de l’appareil Doppler; un fichier au format PKL contenant les informations du spectrogramme (utilisez-le pour visualiser les données collectées en temps réel en ligne); et deux fichiers au format .json contenant les informations de session (telles que la date et l’heure, les paramètres matériels de l’appareil intelligent, les paramètres utilisateur, etc.) et des calculs en temps réel par cycle cardiaque.
Résultats
En ce qui concerne l’interprétation de l’échographie Doppler veineuse-artérielle continue au cours d’une provocation avant charge, les réponses physiologiques générales sont illustrées à la figure 1, à la figure 2, à la figure 3 et à la figure 4.
Premièrement, chez un patient ayant une courbe de la fonction cardiaque verticale normale, une légère augmentation de la précharge cardiaque (p. ex., telle que déduite par le Doppler veineux jugulaire) s’accompagne d’une augmentation relativement importante du volume de l’AVC (p. ex., comme indiqué par l’augmentation de la CCFT)2,14,36; c’est ce qu’illustre la figure 1. L’inférence de changements dans la pression veineuse jugulaire (JVP) à partir du spectre Doppler jugulaire pendant le défi de précharge mérite quelques précisions. Encore une fois, cette variable physiologique est un substitut de la précharge cardiaque ou du remplissage. Normalement, la veine jugulaire est affaissée en position verticale lorsque la pression veineuse jugulaire est inférieure à la pression atmosphérique. Dans le spectre Doppler, cela se traduit par une vitesse relativement élevée (c’est-à-dire généralement plus de 50 cm/s) avec des pulsations minimales et une faible amplitude (c’est-à-dire l’intensité ou la « luminosité » du signal jugulaire). Ensuite, si la pression veineuse jugulaire augmente pendant la manœuvre, la veine arrondit en diamètre, sa vitesse diminue (c’est-à-dire généralement à moins de 50 cm / s), l’intensité (c’est-à-dire la « luminosité ») augmente et la forme d’onde devient plus pulsatile 2,14,36. Comme le montre la figure 1, le changement dans la morphologie Doppler veineuse indique que la veine jugulaire a augmenté en diamètre (c.-à-d. vitesse de chute, amplitude croissante) et commence à suivre les déviations de pression auriculaire droites. Bien que non illustré, avec une augmentation de la pression auriculaire droite, l’onde « v » au cours de la systole tardive peut cliver l’onde monophasique vue sur la figure 1 en une onde de vitesse systolique « s » et une onde de vitesse diastolique « d » 2,14,36. Dans des données non encore publiées chez des volontaires sains, nous avons observé que la morphologie Doppler veineuse jugulaire était la mesure échographique veineuse la plus précise pour distinguer les états de précharge faible des états de précharge élevés.
En revanche, une réponse anormale est illustrée à la figure 2. Un exemple clinique de cette physiopathologie est un patient hypovolémique, veino-dilaté, septique avec un dysfonctionnement cardiaque septique évolutif 2,15,36. Un tel patient a un retour veineux diminué (ce qui réduit la précharge cardiaque, c’est-à-dire la pression veineuse auriculaire ou jugulaire droite) et simultanément une fonction cardiaque déprimée 2,15,35,36. Par conséquent, au départ, ce patient présente une morphologie Doppler veineuse continue et à faible JVP qui augmente (c.-à-d. devient plus pulsatile) pendant la provocation précharge sans augmentation significative du ccFT. Cela décrit efficacement une pente aplatie de la courbe de la fonction cardiaque.
Les résultats du Doppler veineux-artériel continu pourraient également alerter le clinicien traitant des problèmes avec le DPP lui-même. Par exemple, dans certaines situations, le DPP peut ne pas recruter suffisamment de sang veineux des membres inférieurs et de la circulation splanchnique pour générer une provocation de préchargephysiologiquement efficace 4. Sans évaluer le remplissage cardiaque, cela pourrait entraîner un DPP « faussement négatif ». Cependant, si le clinicien constate peu de réponse ccFT (c.-à-d. en tant que substitut du volume de l’AVC) associée à aucun changement dans le Doppler veineux (c.-à-d. en tant que substitut de la précharge), cela pourrait annoncer un DPP inefficace, comme le montre la figure 3.
Enfin, il est essentiel que la manœuvre du DPP soit fidèle à son homonyme, ce qui signifie qu’il n’y a pas d’effort de la part du patient lorsque le torse tombe et que les jambes s’élèvent13. Cela évite les écoulements adrénergiques, qui peuvent augmenter la fonction cardiaque indépendamment du retour veineux; cependant, comme décrit à la figure 4, ce scénario indésirable peut être indiqué par les paramètres d’une augmentation du volume de course dans le signal artériel couplée à une morphologie Doppler veineuse, suggérant une diminution de la pression veineuse.
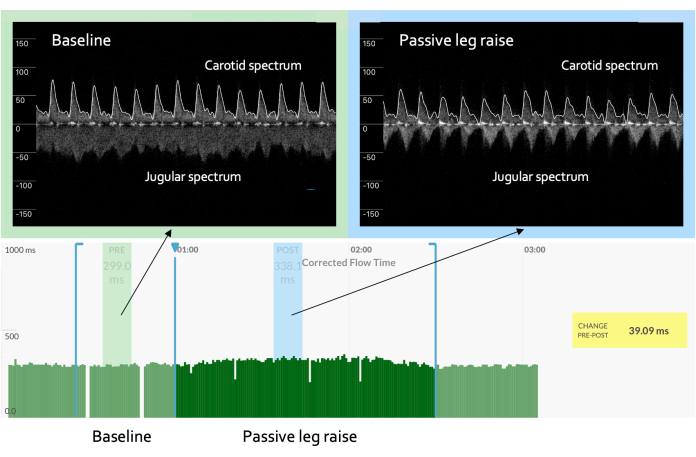
Figure 1 : Augmentation de la pente de la courbe de la fonction cardiaque. Dans un exemple de résultat « normal » ou « attendu », la forme d’onde veineuse progresse d’une vitesse élevée, d’une faible amplitude et d’une non-pulsatile à une vitesse plus faible, une amplitude plus élevée et un caractère pulsatile. La forme d’onde veineuse pulsatile peut être marquée par un signal monophasique, comme on le voit ici. Concomitamment, la forme d’onde Doppler artérielle montre une augmentation du ccFT par rapport à la ligne de base, ce qui suggère que l’augmentation de la précharge cardiaque est compensée par une augmentation du débit cardiaque. Ces réponses, prises ensemble, indiquent une courbe de « fonction cardiaque » avec une pente raide. L’axe des y sur le spectre représente la vitesse en centimètres par seconde. La vitesse positive est vers le cerveau (par exemple, l’artère carotide), tandis que la vitesse négative est vers le cœur (par exemple, la vitesse jugulaire). L’axe des x sur le spectre est le temps. Veuillez cliquer ici pour voir une version agrandie de cette figure.
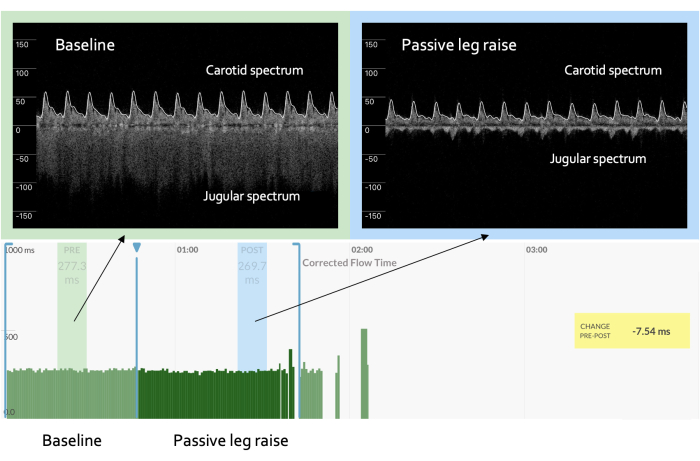
Figure 2 : Pente aplatie de la courbe de la fonction cardiaque. Une réponse « anormale » lors d’un défi de précharge est marquée par une forme d’onde Doppler veineuse qui évolue comme ci-dessus mais avec une réponse artérielle qui ne révèle aucun changement significatif ou même une diminution du ccFT par rapport à la ligne de base, comme on le voit ici. Cette constellation de signes veineux et artériels implique une courbe de la fonction cardiaque plate ou, potentiellement, altérée avec une précharge accrue. Veuillez cliquer ici pour voir une version agrandie de cette figure.
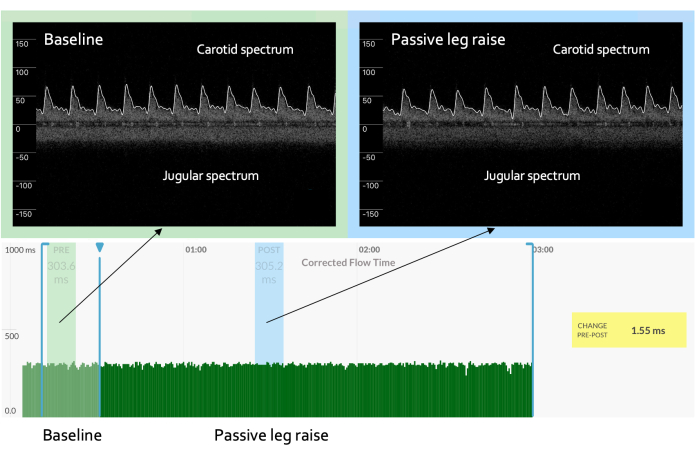
Figure 3 : Aucun changement dans le Doppler veineux. Un défi de précharge qui ne montre aucun changement significatif dans la forme d’onde Doppler veineuse pourrait représenter un changement inadéquat dans le remplissage cardiaque, ce qui signifie qu’aucun changement dans le spectre artériel n’est attendu. Veuillez cliquer ici pour voir une version agrandie de cette figure.
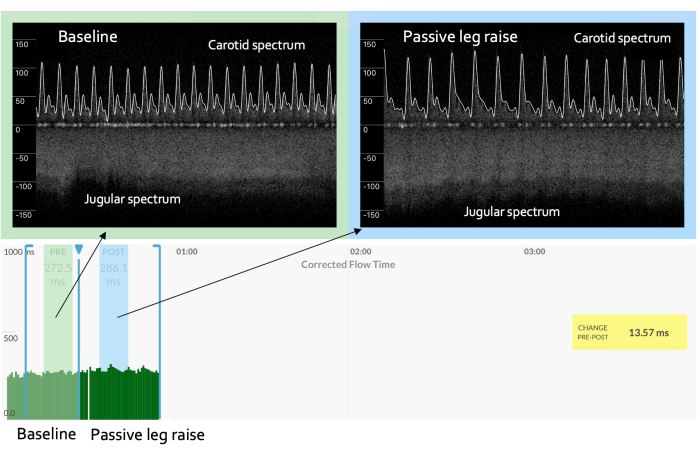
Figure 4 : Chute de la précharge lors d’un défi de précharge. Une provocation précharge qui montre une augmentation de la vitesse veineuse et une augmentation significative des mesures Doppler artérielles peut signifier une augmentation du tonus adrénergique (c.-à-d. stimulation sympathique) de sorte que la fonction cardiaque augmente indépendamment du retour veineux. Cette circonstance pourrait être le résultat d’une augmentation de jambe « non passive », par exemple, si le patient s’efforce de changer la position de son corps. Veuillez cliquer ici pour voir une version agrandie de cette figure.
Figure 5 : L’appareil sur un volontaire. Veuillez cliquer ici pour voir une version agrandie de cette figure.
Discussion
L’objectif principal de cette expérience visuelle est de décrire un protocole permettant de suivre simultanément les substituts de la précharge cardiaque et de la sortie pendant un PC bien validé à l’aide d’une échographie portable sans fil. L’objectif n’est pas de décrire un protocole d’étude spécifique chez les patients, en soi. Cependant, la description du Doppler veineux et artériel continu sert de base pratique et physiologique pour concevoir des études chez des patients nécessitant à la fois une réanimation (p. ex. période périopératoire, septicémie) ou une déréanimation (p. ex. insuffisance cardiaque congestive, dialyse, incapacité à libérer de la ventilation mécanique)15,36.
La méthode décrite utilise un échographie Doppler portable à ondes continues qui fait sonner simultanément une veine et une artère majeures pour déduire la fonction cardiaque au cours d’un PC15. La sélection d’un patient approprié et coopératif et la garantie d’un changement d’angle minimal entre les vaisseaux et le transducteur tout au long de l’évaluation sont essentielles à cette méthode. De plus, assurer une vitesse d’entaille dicrotique claire et cohérente est primordial pour permettre la mesure cohérente du temps systolique. Enfin, l’utilisateur doit apprécier la morphologie Doppler veineuse et sa variation à travers un spectre de pression veineuse jugulaire (JVP), comme discuté ci-dessus dans les résultats représentatifs.
En tant que modification de la méthode décrite, au lieu d’un DPP, le PC pourrait consister en une perfusion rapide de liquide intraveineux9, en déplaçant un patient complètement couché sur le dos de l’horizontale à la tête vers le bas de 15 à 30° (c.-à-d. positionnement de Trendelenburg)10, ou des manœuvres respiratoires telles que l’occlusion expiratoire en fin d’expiration34. Ces approches sont bénéfiques en ce sens qu’il y a moins de mouvements du patient et, ostensiblement, un risque réduit de changement d’angle pendant l’évaluation. En général, le dépannage de tous les PC avec l’échographie portable nécessite un positionnement stable du cou, un adhésif supplémentaire pour sécuriser l’angle d’insonation, la prolongation de l’évaluation lorsque des artefacts de phonation ou de déglutition se produisent, le repositionnement de l’appareil ou l’ajout de gel à ultrasons pour optimiser le couplage acoustique au patient31.
Il y a des limites à la méthode d’inférence cardiovasculaire décrite dans ce manuscrit. En ce qui concerne le signal veineux jugulaire, la morphologie Doppler est un substitut de la pression veineuse jugulaire, qui est elle-même un substitut de la pression auriculaire droite37,38,39,40. Par conséquent, il n’y a aucune certitude que la précharge cardiaque est augmentée sur la base des seuls changements Doppler veineux. Néanmoins, la forme d’onde Doppler veineuse varie sa morphologie en fonction des déviations de pression de l’oreillette droite17,18,41 ; Cela a été observé dans plusieurs grandes veines en plus de la jugulaire. Par exemple, les évaluations de la veine cave supérieure et inférieure et des veines hépatique, portale, intrarénale et fémorale estiment toutes qualitativement la pression veineuse42. Plus précisément, l’onde de vitesse veineuse proéminente pendant la systole est formée par la descente x de la pression auriculaire droite et l’onde de vitesse diastolique par la descente y de la pression auriculaire droite. Le nadir de vitesse entre la systole et la diastole est dû à la pression auriculaire droite « v wave"16,17,18,42.
De plus, alors que la durée de la systole mécanique est directement proportionnelle au volume de la course, le temps systolique, semblable à la SV, est médié par la fréquence cardiaque, la précharge, la postcharge et la contractilité43. Alors que l’équation ccFT corrige la fréquence cardiaque, une limitation de la ccFT en tant que substitut du volume de l’AVC est qu’elle est déterminée par d’autres entrées hémodynamiques. Néanmoins, il a été démontré que des augmentations du ccFT d’au moins 7 ms 24 ou de +2% à 4% détectent avec précision une augmentation de 10% du SV chez les patients gravement malades 24, les volontaires sains effectuant une manœuvre de modification de la précharge44,45 et les volontaires sains subissant une réanimation simulée d’hémorragie modérée à sévère27. De plus, ccFT a été utilisé pour suivre avec précision l’évolution des SV dans la population chirurgicale élective pendant les manœuvres respiratoires46. Ainsi, en supposant que la post-charge et la contractilité sont relativement constantes pendant un PC focalisé, le ccFT varie principalement en raison des changements dans le SV.
De plus, les contre-indications absolues et relatives de cette approche n’ont pas encore été élaborées, en particulier chez les patients. Comme nous l’avons mentionné précédemment, la contre-indication la plus courante est probablement l’incapacité de coopérer (p. ex., délire, parole, mouvement, rigueur). Cela est vrai pour de nombreux moniteurs de signes vitaux modernes, bien que l’échographie portable soit particulièrement sensible à la phonation et aux mouvements du cou. En conséquence, l’appareil fonctionne très bien chez les patients intubés et paralysés en salle d’opération; Une étude utilisant le dispositif sur des patients recevant un pontage aortocoronarien électif est actuellement en cours de recrutement. Une variation physiologique entre les artères carotides opposées chez un patient particulier est possible; cependant, cette préoccupation est atténuée parce que, dans le paradigme PC, le patient agit comme son propre contrôle (c.-à-d. une intervention pré-post). Par conséquent, nous prévoyons que même si les différents côtés du cou (figure 5) peuvent produire des signaux Doppler veineux et artériels légèrement différents, le changement devrait être cohérent, à moins d’anomalies unilatérales importantes (p. ex. sténose). Les limitations physiques peuvent également poser des problèmes (p. ex. cathéters centraux, colliers cervicaux-rachidiens, sangles de trachéotomie, traumatisme, cous courts ou cyphose cervicale grave). Les contre-indications physiologiques telles que la sténose carotidienne modérée à sévère, la sténose aortique, l’arythmie et les schémas respiratoires anormaux sont également potentiellement préoccupantes. En général, cependant, un DPP avec des mesures en temps réel du débit cardiaque est résistant à bon nombre de ces problèmes, y compris l’arythmie 4,11. L’appareil est actuellement à l’étude chez les patients respirant spontanément dans les services d’urgence et dans la salle d’opération; La proportion de signaux inutilisables sera tirée de ces données.
L’importance de la méthode décrite ci-dessus est que l’échographie adhérée peut échantillonner des minutes de données continues, tandis que les approches portatives sont généralement limitées à quelques cycles cardiaques48,49. De plus, le logiciel pour l’échographie portable mesure le coefficient de variation Doppler artériel. À partir de là, une « fenêtre intelligente » est mise en œuvre pour échantillonner un nombre suffisant de cycles cardiaques au départ et pendant l’intervention; Cet instrument statistique adapte la précision de mesure à chaque défi de précharge47. De plus, étant donné que l’échographie portable reste apposée sur le patient, le risque de facteurs humains50,51 qui augmentent la variabilité de mesure est diminué; Cela vaut pour l’insonation artérielle et veineuse. Un autre aspect important de cette méthode est que l’évaluation Doppler veineuse et artérielle contemporaine permet au clinicien d’évaluer indirectement la précharge cardiaque au cours d’une manœuvre dynamique; Ceci est recommandé par les experts dans le domaine13 mais rarement effectué car la mesure de la bonne pression auriculaire est lourde. En conséquence, le Doppler veineux-artériel continu pendant un PC donne une image plus profonde de la fonction cardiaque au chevet du patient. Bien que cette méthode décrite ci-dessus puisse être utilisée pour juger de la réanimation liquidienne intraveineuse, elle est également prometteuse pour évaluer la « déréanimation »15,52 ou prédire le sevrage de la ventilation mécanique 53 et devrait être explorée dans de futures recherches cliniques. Par exemple, la diurèse des patients présentant une surcharge volumique peut être révélée par des signes de chute de la pression auriculaire droite dans le signal Doppler veineux à mesure que le retrait du volume progresse. De plus, si le patient reçoit un DPP avant et après la dialyse, le changement dans les mesures Doppler artérielles devrait indiquer une augmentation de la fonction cardiaque, comme indiqué précédemment52.
Une méthode de Doppler veino-artériel continu au cours d’un PC est mieux accomplie en suivant les six étapes générales décrites ci-dessus dans la section protocole. Un nouveau système d’échographie Doppler portable et sans fil contribue à ce paradigme en adhérant à un patient et en permettant un angle d’insonation relativement fixe lors du changement de précharge. Fondamentalement, le Doppler veineux-artériel simultané, instantané peut élaborer les deux axes de la relation Frank-Starling-Sarnoff et, par conséquent, donner de nouvelles perspectives sur la fonction cardiaque. Ceci est particulièrement important lors de la prise en charge de patients gravement malades; Cette nouvelle approche pourrait améliorer l’administration et le retrait des volumes. Bien que la discussion ci-dessus soit largement limitée aux applications hospitalières, des utilisations ambulatoires supplémentaires dans les domaines de l’insuffisance cardiaque congestive, de l’insuffisance rénale chronique et de l’hypertension pulmonaire sont également possibles. En conséquence, le Doppler veineux-artériel continu peut débloquer des canaux d’exploration imprévus au sein de l’hémodynamique et des disciplines médicales connexes.
Déclarations de divulgation
J.E.S.K., S.O.G., D.J., L.M.H., E.R., G.C., J.K.E. travaillent pour Flosonics Medical, la start-up qui construit l’échographie Doppler portable; R.A. et B.N. ne déclarent aucun intérêt concurrent.
Remerciements
Aucun.
matériels
| Name | Company | Catalog Number | Comments |
| FloPatch | Flosonics | ||
| iPad | Apple | ||
| ultrasound gel |
Références
- Berlin, D. A., Bakker, J. Starling curves and central venous pressure. Critical Care. 19 (1), 55 (2015).
- Kenny, J. -. E. S. Assessing fluid intolerance with Doppler ultrasonography: A physiological framework. Medical Sciences. 10 (1), 12 (2022).
- Monnet, X., Marik, P. E., Teboul, J. -. L. Prediction of fluid responsiveness: An update. Annals of Intensive Care. 6 (1), 111 (2016).
- Monnet, X., Shi, R., Teboul, J. -. L. Prediction of fluid responsiveness. What's new. Annals of Intensive Care. 12 (1), 46 (2022).
- Kenny, J. -. E. S., Barjaktarevic, I. Letter to the editor: Stroke volume is the key measure of fluid responsiveness. Critical Care. 25 (1), 104 (2021).
- Malbrain, M. L., et al. Principles of fluid management and stewardship in septic shock: It is time to consider the four D's and the four phases of fluid therapy. Annals of Intensive Care. 8 (1), 66 (2018).
- Douglas, I. S., et al. Fluid response evaluation in sepsis hypotension and shock: A randomized clinical trial. Chest. 158 (4), 1431-1445 (2020).
- Latham, H. E., et al. Stroke volume guided resuscitation in severe sepsis and septic shock improves outcomes. Journal of Critical Care. 42, 42-46 (2017).
- Barthélémy, R., et al. Accuracy of cumulative volumes of fluid challenge to assess fluid responsiveness in critically ill patients with acute circulatory failure: A pharmacodynamic approach. British Journal of Anaesthesia. 128 (2), 236-243 (2021).
- Ma, G. -. G., et al. Change in left ventricular velocity time integral during Trendelenburg maneuver predicts fluid responsiveness in cardiac surgical patients in the operating room. Quantitative Imaging in Medicine and Surgery. 11 (7), 3133 (2021).
- Monnet, X., et al. Passive leg raising predicts fluid responsiveness in the critically ill. Critical Care Medicine. 34 (5), 1402-1407 (2006).
- Bentzer, P., et al. Will this hemodynamically unstable patient respond to a bolus of intravenous fluids. JAMA. 316 (12), 1298-1309 (2016).
- Monnet, X., Teboul, J. -. L. Passive leg raising. Intensive Care Medicine. 34 (4), 659-663 (2008).
- Kenny, J. -. &. #. 2. 0. 1. ;. S. Functional hemodynamic monitoring with a wireless ultrasound patch. Journal of Cardiothoracic and Vascular Anesthesia. 35 (5), 1509-1515 (2021).
- Kenny, J. -. &. #. 2. 0. 1. ;. S., et al. Inferring the Frank-Starling curve from simultaneous venous and arterial Doppler: Measurements from a wireless, wearable ultrasound patch. Frontiers in Medical Technology. 3, 676995 (2021).
- Sivaciyan, V., Ranganathan, N. Transcutaneous doppler jugular venous flow velocity recording. Circulation. 57 (5), 930-939 (1978).
- Ranganathan, N., Sivaciyan, V., Pryszlak, M., Freeman, M. R. Changes in jugular venous flow velocity after coronary artery bypass grafting. The American Journal of Cardiology. 63 (11), 725-729 (1989).
- Ranganathan, N., Sivaciyan, V. Jugular venous pulse descents patterns - Recognition and clinical relevance. CJC Open. , (2022).
- Abu-Yousef, M. M. Normal and respiratory variations of the hepatic and portal venous duplex Doppler waveforms with simultaneous electrocardiographic correlation. Journal of Ultrasound in Medicine. 11 (6), 263-268 (1992).
- Appleton, C. P., Hatle, L. K., Popp, R. L. Superior vena cava and hepatic vein Doppler echocardiography in healthy adults. Journal of the American College of Cardiology. 10 (5), 1032-1039 (1987).
- Reynolds, T., Appleton, C. P. Doppler flow velocity patterns of the superior vena cava, inferior vena cava, hepatic vein, coronary sinus, and atrial septal defect: A guide for the echocardiographer. Journal of the American Society of Echocardiography. 4 (5), 503-512 (1991).
- Abu-Yousef, M. M., Kakish, M., Mufid, M. Pulsatile venous Doppler flow in lower limbs: Highly indicative of elevated right atrium pressure. American Journal of Roentgenology. 167 (4), 977-980 (1996).
- Iida, N., et al. Clinical implications of intrarenal hemodynamic evaluation by Doppler ultrasonography in heart failure. JACC: Heart Failure. 4 (8), 674-682 (2016).
- Barjaktarevic, I., et al. Ultrasound assessment of the change in carotid corrected flow time in fluid responsiveness in undifferentiated shock. Critical Care Medicine. 46 (11), 1040-1046 (2018).
- Mackenzie, D. C., et al. Ultrasound measurement of carotid flow time changes with volume status. Critical Care. 18 (1), 131 (2014).
- Pace, R., et al. Carotid vs aortic velocity time integral and peak velocity to predict fluid responsiveness in mechanically ventilated patients. A comparative study. Minerva Anestesiologica. 88 (5), 352-360 (2021).
- Kenny, J. -. &. #. 2. 0. 1. ;. S., et al. Carotid artery velocity time integral and corrected flow time measured by a wearable Doppler ultrasound detect stroke volume rise from simulated hemorrhage to transfusion. BMC Research Notes. 15 (1), 7 (2022).
- Kenny, J. -. &. #. 2. 0. 1. ;. S., et al. Carotid Doppler ultrasonography correlates with stroke volume in a human model of hypovolaemia and resuscitation: analysis of 48 570 cardiac cycles. British Journal of Anaesthesia. 127 (2), 60-63 (2021).
- Marik, P. E., Levitov, A., Young, A., Andrews, L. The use of bioreactance and carotid Doppler to determine volume responsiveness and blood flow redistribution following passive leg raising in hemodynamically unstable patients. Chest. 143 (2), 364-370 (2013).
- Effat, H., Hamed, K., Hamed, G., Mostafa, R., El Hadidy, S. Electrical cardiometry versus carotid Doppler in assessment of fluid responsiveness in critically ill septic patients. Egyptian Journal of Critical Care Medicine. 8 (4), 96-113 (2021).
- Kenny, J. -. &. #. 2. 0. 1. ;. S., et al. A novel, hands-free ultrasound patch for continuous monitoring of quantitative Doppler in the carotid artery. Scientific Reports. 11, 7780 (2021).
- Kenny, J. S., et al. A wireless wearable Doppler ultrasound detects changing stroke volume: Proof-of-principle comparison with trans-esophageal echocardiography during coronary bypass surgery. Bioengineering. 8 (12), 203 (2021).
- Kenny, J. -. E. S., et al. A wearable patch to assess changes in carotid blood velocity during passive leg raising. European Journal of Anesthesiology. 36, 223 (2019).
- Kenny, J. &. #. 2. 0. 1. ;. S., et al. A wearable carotid Doppler tracks changes in the descending aorta and stroke volume induced by end-inspiratory and end-expiratory occlusion: A pilot study. Health Science Reports. 3 (4), 190 (2020).
- Kenny, J. -. E. S., Eibl, J. K., Mackenzie, D. C., Barjaktarevic, I. Guidance of intravenous fluid by ultrasound will improve with technology. Chest. 161 (2), 132-133 (2021).
- Kenny, J. -. &. #. 2. 0. 1. ;. S., Munding, C. E., Eibl, A. M., Eibl, J. K. Wearable ultrasound and provocative hemodynamics: A view of the future. Critical Care. 26 (1), 329 (2022).
- Guarracino, F., et al. Jugular vein distensibility predicts fluid responsiveness in septic patients. Critical Care. 18 (6), 647 (2014).
- Hossein-Nejad, H., Mohammadinejad, P., Ahmadi, F. Internal jugular vein/common carotid artery cross-sectional area ratio and central venous pressure. Journal of Clinical Ultrasound. 44 (5), 312-318 (2016).
- Lipton, B. Estimation of central venous pressure by ultrasound of the internal jugular vein. The American Journal of Emergency Medicine. 18 (4), 432-434 (2000).
- Donahue, S. P., Wood, J. P., Patel, B. M., Quinn, J. V. Correlation of sonographic measurements of the internal jugular vein with central venous pressure. The American Journal of Emergency Medicine. 27 (7), 851-855 (2009).
- Tang, W. W., Kitai, T. Intrarenal venous flow: A window into the congestive kidney failure phenotype of heart failure. JACC: Heart Failure. 4 (8), 683-686 (2016).
- McNaughton, D. A., Abu-Yousef, M. M. Doppler US of the liver made simple. Radiographics. 31 (1), 161-188 (2011).
- Boudoulas, H. Systolic time intervals. European Heart Journal. 11, 93-104 (1990).
- Kenny, J. -. &. #. 2. 0. 1. ;. S., et al. Diagnostic characteristics of 11 formulae for calculating corrected flow time as measured by a wearable Doppler patch. Intensive Care Medicine Experimental. 8 (1), 54 (2020).
- Kenny, J. -. &. #. 2. 0. 1. ;. S., et al. A carotid Doppler patch accurately tracks stroke volume changes during a preload-modifying maneuver in healthy volunteers. Critical Care Explorations. 2 (1), 0072 (2020).
- Kimura, A., Suehiro, K., Juri, T., Tanaka, K., Mori, T. Changes in corrected carotid flow time induced by recruitment maneuver predict fluid responsiveness in patients undergoing general anesthesia. Journal of Clinical Monitoring and Computing. 36 (4), 1069-1077 (2021).
- Kenny, J. -. &. #. 2. 0. 1. ;. S., et al. Carotid Doppler measurement variability in functional hemodynamic monitoring: An analysis of 17,822 cardiac cycles. Critical Care Explorations. 3 (6), 0439 (2021).
- Kenny, J. -. &. #. 2. 0. 1. ;. S., Barjaktarevic, I. Timing and measurement variability are critical when using carotid Doppler to infer hemodynamics. Ultrasound in Medicine and Biology. 46 (12), 3485-3486 (2020).
- Kenny, J., Cannesson, M., Barjaktarevic, I. Minimizing measurement variability in carotid ultrasound evaluations. Journal of Ultrasound in Medicine. 40 (4), 855-856 (2020).
- Lui, E. Y., Steinman, A. H., Cobbold, R. S., Johnston, K. W. Human factors as a source of error in peak Doppler velocity measurement. Journal of Vascular Surgery. 42 (5), 972-979 (2005).
- Gill, R. W. Measurement of blood flow by ultrasound: Accuracy and sources of error. Ultrasound in Medicine and Biology. 11 (4), 625-641 (1985).
- Chebl, R. B., et al. Corrected carotid flow time and passive leg raise as a measure of volume status. American Journal of Emergency Medicine. 37 (8), 1460-1465 (2019).
- Dres, M., et al. Passive leg raising performed before a spontaneous breathing trial predicts weaning-induced cardiac dysfunction. Intensive Care Medicine. 41 (3), 487-494 (2015).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon