A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
מבחני photobleaching (FRAP & FLIP) כדי למדוד Dynamics חלבון הכרומטין בתוך החיים בתאי גזע עובריים
In This Article
Summary
אנו מתארים שיטות photobleaching כולל שחזור הקרינה לאחר photobleaching (FRAP) והפסד הקרינה photobleaching (FLIP) כדי לעקוב אחר הדינמיקה חלבון הכרומטין בתוך גזע עובריים (ES) התאים. הכרומטין הדינמיקה חלבון, אשר נחשב אחד האמצעים ללמוד פלסטיות הכרומטין, מוגברת בתאים pluripotent.
Abstract
שחזור הקרינה לאחר photobleaching (FRAP) והפסד הקרינה photobleaching (FLIP) לאפשר את לימוד הדינמיקה חלבון בתאים חיים עם רזולוציה במרחב ובזמן טוב. כאן אנו מתארים כיצד לבצע FRAP מבחני FLIP של חלבונים הכרומטין, כולל H1 ו HP1, בעכבר גזע עובריים (ES) התאים. בניסוי FRAP, תאים transfected, או transiently או ביציבות, עם חלבון של עניין התמזגו עם חלבון פלואורסצנטי ירוק (GFP) או נגזרים ממנו (YFP, CFP, שרי וכו '). ב, תאים transfected fluorescing, קרן לייזר ממוקדת הלבנה אינטנסיבי באזור קטן יחסית של עניין (ROI). אורך גל לייזר נבחרה על פי חלבון פלואורסצנטי המשמש היתוך. אור לייזר בלתי הפיך הלבנה אות הניאון של מולקולות ROI ו, מיד לאחר הלבנה, ההתאוששות של האות ניאון באזור מולבן - מתווכת על ידי החלפתו של מולקולות מולבן עם מולקולות מולבן - מנוטר באמצעות לשגות הדמיה הזמן. עקומות שנוצר התאוששות הקרינה לספק מידע על ניידות של החלבון. אם מולקולות ניאון הם נייח, ההחלמה לא הקרינה יקויימו. בגישה משלים, אובדן הקרינה photobleaching (FLIP), קרן הלייזר הלבנה באותו מקום שוב ושוב את עוצמת האות נמדדת במקום אחר בתא fluorescing. ניסויים FLIP ולכן למדוד דעיכה אות ולא התאוששות פלואורסצנטי מועילים כדי לקבוע ניידות חלבון, כמו גם חלבון מדלג בין תאים סלולריים. מחייב חלוף הוא רכוש משותף של הכרומטין הקשורים חלבונים. אמנם חלק גדול של כל חלבון הכרומטין חייב הכרומטין בכל רגע נתון על מצב יציב, מחייב הוא חולף וחלבונים הכרומטין ביותר יש תחלופה גבוהה על הכרומטין, עם זמן מגורים בסדר גודל של שניות. מאפיינים אלה הם קריטיים ליצירת גמישות גבוהה בביטוי הגנום 1. ניסויים photobleaching ולכן הם יעילים במיוחד כדי לקבוע פלסטיות הכרומטין באמצעות GFP-Fusion גירסאות של חלבונים מבניים הכרומטין, במיוחד בתאי גזע עובריים, שם החליפין הדינמי של חלבונים הכרומטין (כולל חלבון heterochromatin 1 (HP1), היסטון H1 מקשר ו ההיסטונים הליבה) גבוה מ בתאים הבדיל 2,3.
Protocol
1. ציפוי תאים ES
ט = 0 שעות
MEF ציפוי
- סמל ההדמיה לחיות טוב 8-μ-שקופיות (ibidi: מינכן, גרמניה) עם ג'לטין או בכוסות החדרים לכסות (Lab-Tek, רוצ'סטר, ניו יורק) או זכוכית התחתונה מנות התרבות (MatTek: אשלנד, MA). השאירו דקות 5-30 ו לשאוב משם את הג'לטין חינם.
- זרעי 22,000 MEFs / גם בנפח 250 סך μl של DMEM [בתוספת 10% בסרום שור העובר (FBS)]. אפשר לתאים לגדול בתרבית רקמה אינקובטור (37 ° C, CO2 5%).
ט = 6 שעות
ES ציפוי התא
- לשאוב DMEM.
- Seed כל MEF מצופה היטב / טוב בנפח 250 סך μl של התקשורת ES תא עם 15,000 תאים R1 [בתוספת סרום ESC כיתה 10% שור העובר (FBS), נתרן pyruvate 1 מ"מ, 0.1 mM חומצות אמינו חיוניות, β 0.1 מ"מ mercaptoethanol, 1000 ו - U / ml גורם ללוקמיה מעכבות (LIF)], כדי להשיג 30% עד 50% מפגש למחרת.
2. Transfecting תאים ES
T = 24 שעות
חלוף transfection
- החזר את תא התקשורת ES עם 250 μl / גם של מדיה תא טרי ES.
- בתוך צינור 1.5-ml בדיקה סטרילית, להוסיף 100 μl בסרום חינם התקשורת [Opti-ממ (Gibco)], ולאחר מכן להוסיף 10 Transit-LT1 μl מגיב transfection (Mirus) ישירות לתוך התקשורת החופשית בסרום. מערבבים על ידי pipetting עדין דגירה בטמפרטורת החדר למשך 50-20 דקות.
- הוסף GFP 1.5 מיקרוגרם היתוך DNA פלסמיד (H1e, H1o או HP1) אל מעבר בדילול-LT1 מגיב. מערבבים על ידי pipetting עדין דגירה בטמפרטורת החדר למשך 15-30 דקות.
- הוסף μl 13.5 / היטב לתערובת transfection. מערבולת 8-μ-שקופיות היטב על מנת להבטיח פיזור אפילו. אחרי 24 שעות להחליף את תא התקשורת הישנה ES עם 250 μl של התקשורת תא טרי ES.
3. ביצוע FRAP ו FLIP
ט = 48-72 שעות
- הניסוי יכול להתבצע על כל confocal מיקרוסקופ סורק לייזר (CLSM) אבל מאז בניסוי FRAP / FLIP נורמלי, תמונות רצופות רבים נרכשים, מומלץ להשתמש במיקרוסקופ ספינינג דיסק confocal, המאפשרת מהירות הרכישה מבטיחה כי לא מדגם לא רצויים הלבנת תתרחש לאחר האירוע הראשוני הלבנת מכוונת. כאן, אנו ממליצים להשתמש המהפכה ספינינג מערכת דיסק confocal (www.Andor.com), עם ראש המז"פ-X דיסק ספינינג Yokogawa. מערכת זו יש את היכולת כפול photobleach באמצעות מודול מיוחד FRAPPA עם מערכת סריקה נקודה, כדי לעבור במהירות את האור כדי לאסוף את התמונות באמצעות דיסק מסתובב. 3 חלבונים fluorescing הנפוץ ביותר המשמש photobleaching ניסויים GFP, YFP ושרי. אם ה-GFP או YFP משמשים, ~ 488 ננומטר לייזר נדרשת. עבור שרי, שימוש בלייזר ~ 560 ננומטר. בכל מקרה, אנו ממליצים להשתמש לייזרים של מצב מוצק. לאחר שלב אוטומטית שימושי אבל לא חובה. מאז תאים חיים הם צילמו, חיוני להשתמש קאמרית סביבתיים (אנו משתמשים אחד מן LIS, שוויץ), שליטה חמצן, לחות, טמפרטורה ו-CO 2. FRAP מבוצע באמצעות לייזר בעוצמה מקסימלית תוך ההדמיה נעשית עם כוח לייזר המינימלי הנדרש (בדרך כלל באזור של 10%, כאשר רמת הקרינה היא נאותה).
שים את התאים עם אור ניאון של אורך הגל המתאים ובחרו תא להביע GFP באמצעות עדשה 60x טבילה שמן. להבטיח חלוקה subcellular הנכון. מדי פעם, כאשר רמות ביטוי גבוהות מדי, לוקליזציה של החלבון עשוי "לשפוך" אל תאים אחרים כגון nucleolus. תאים כאלה לא צריכים להיות נבחרים. - עכשיו להגדיר פרוטוקול הדמיה: אוספים 3-5 מסגרות לפני photobleaching, אז photobleach ב euchromatin או heterochromatin (כפי שנצפו מרוכז GFP מוקדים) ולאסוף 90-120 מסגרות לאחר photobleach, עם מרווחי 250-1000 ms: H1e-GFP, 1000 ms, H1o HP1 ו-GFP, 250 ms (מרווח הזמן משתנה על פי הדינמיקה חלבון, שבו חלבונים דינמי מאוד לדרוש מרווח זמן קצר יותר). בדרך כלל אנחנו משתמשים עוצמת הלייזר 8-10% עבור photobleaching עם דופק לייזר של μseconds 20-40 (1-2 חזרות), אבל מספרים אלה יכולים להשתנות בהתאם החלבון לנתח את רמות הביטוי. כאשר photobleaching מתאים, אתה צריך לראות "חור שחור" של הקרינה GFP שלך. החור השחור הוא בהדרגה מחדש מלא התאוששות בעקבות הקרינה. למרות דיסק ספינינג יכול לקבל עד כ -60 תמונות לשנייה (עם עוצמת הקרינה טוב כאשר התקרבות על תא בודד), לא מומלץ להשתמש במערכת במהירויות גבוהות כאלה, בשל איכות התמונה נמוכה phototoxicity גדל פוטנציאל.
- לצורך ניסוי FLIP, להגדיר פרוטוקול הדמיה שונים: אוספים 3-5 מסגרות לפני הלבנה, ולאחר מכן להתחיל לחזור הלבנה באותו מקום בעת איסוף התמונות. עבור H1e-GFP, אקונומיקה כל 5 שניות, עבור H1o-GFP, אקונומיקה כל 2 שניות, ועל HP1-GFP אקונומיקה כל 1 שניות. Bleachד לאסוף תמונות שוב ושוב לאורך הניסוי כולו.
- עבור טכניקה או, לחזור על התהליך על 20-30 תאים. למטרות סטטיסטיות, חזור על הניסוי 3 פעמים או יותר, רצוי בימים שונים. באוכלוסיות הומוגנית ההגדרות הנכונות, סטיית התקן היא נמוכה בדרך כלל (<5%).
עבור FRAP והן FLIP, בגודל ובצורה של האזור מולבן משפיע על הדינמיקה ההתאוששות חייבת להישאר קבועה בתוך ניסוי. כמו כן, כאשר שני תאים מושווים, פרוטוקולים זהים יש להשתמש בתאים יש לנתח ברצף באותו היום כמו לייזר כוח ומצבים אחרים עשויים להשתנות והם עלולים להשפיע על תוצאות הניסוי.
4. FRAP ולהפוך ניתוח נתונים
- בכל מסגרות FRAP שנאספו, למדוד את עוצמת הקרינה את ההחזר על ההשקעה (ROI b = שטח מולבן), האזור רקע (ROI bg), והשטח לא מולבן גרעיני (ROI nb) כפונקציה של זמן לפני ואחרי הלבנה. כאשר אזור מחומצן הוא זניח בגרעין כולו ניתן לבחור למטרות נורמליזציה.
- עבור כל נקודת זמן, לנרמל את הנתונים לפי הנוסחה: (ROI ב - ROI bg) / (ROI nb - ROI bg) / (pbROI ב - pbROI bg) / (pbROI nb - pbROI bg), pb מציין מראש מולבן. במשך מראש אקונומיקה תמונות אתה צריך לקבל ערך של כ 1. התמונה הראשונה לאחר להלבין את יציין את עומק Bleach. הפחת את הערך 1 עבור הערך Bleach בפועל עומק. חזור על הפעולה עבור כל תא וממוצע 20-30 תאים כל ניסוי.
- בכל מסגרות FLIP שנאספו, למדוד את עוצמת הקרינה באזור הלא מולבן הגרעיני, ואזור רקע (ROI nb = לא מולבן באזור, ROI bg רקע =). חישוב נתונים FLIP דומה עקומת FRAP, רק את ההחזר על ההשקעה ניתחו (ROI nb) צריך להיות שונה מאשר באזור מולבן בפועל, אשר אינו משמש לצורך חישוב: (ROI nb - ROI bg) / (pbROI nb - pbROI bg) . אפשר גם להשתמש בתא השכן (ROI = n התא השכן) למטרות נורמליזציה: (ROI nb - ROI bg) / (n ROI - החזר על השקעה bg) / (pbROI nb - pbROI bg) / (n pbROI - pbROI bg ).
לאחר איסוף הנתונים, ניתן להתאים את נתוני הניסוי על הדמיית מחשב. זה מאפשר חישוב, עם הקרבה טוב, את החלק היחסי ניידים, חלק נייח לבין חצי מקסימלית. אנחנו לא נדון בהיבטים מתמטיים וניתוחים סטטיסטיים של FRAP כאן מפנים את הקורא פרסומים מעולה אחרים 4-9. עומק אקונומיקה מתייחס למרחק (על ציר y) בין האות (100%) מראש אקונומיקה התמונה הראשונה אחרי אקונומיקה, שבר ניידים מתייחס למרחק (על ציר ה-Y) בין עומק אקונומיקה את האות כאשר התאושש קינטיקה מגיע הרמה, ואת חלק נייח מתייחס למרחק (על ציר ה-Y) בין האות התאושש מראש אקונומיקה (100%) אות (ראה איורים 1B ו -2). מעבר לניתוח זה, יש מודלים מתמטיים טוב כדי להתאים את הנתונים. עבור המעריך אחת, את המשוואה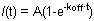
כאשר t הוא הזמן, הוא חלק ניידים, 1-A הוא חלק נייח ו k את זה ניתוק תמידי, יכול לשמש כדי להתאים את הנתונים, הערכה ישירה של שיעור הנחה של הכריכה (k כבוי) ניתן המתקבל, כמו גם עבור הפרמטר A, אשר יכול לשמש כדי לחשב את שיעור העמותה.
5. נציג תוצאות:
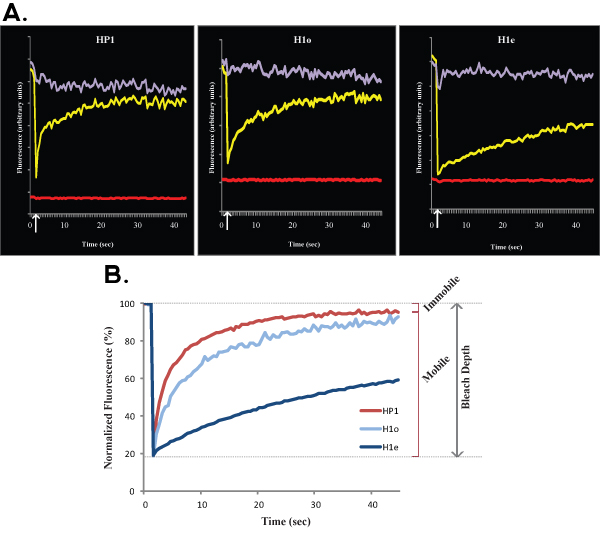
באיור 1. ונציג B להראות FRAP הקימורים של HP1 (משמאל), H1o (באמצע) ו H1e (מימין) בתאי גזע עובריים R1. עבור איור פשטות ובהירות 1A מציגה את הנתונים הגולמיים של תא בודד לפני נורמליזציה כלשהי בחישוב. עקומת צהוב מתאים באזור מולבן, עקומת סגול המתאים לאזור הלא מולבן הגרעיני (כאשר אזור מחומצן הוא זניח הגרעין כולו ניתן לבחור למטרות נורמליזציה), ואת הקו האדום מתאים פלואורסצנציה הרקע, אשר מינימלי במקרה זה. החץ האנכי מייצג את הזמן אקונומיקה. נתונים מנורמל ממוצעים של מוצג באיור 1B. הערה התאוששות איטית של H1 (בכחול) לעומת HP1 (אדום). כמו כן, הגרסה H1e (כחול כהה) היא איטית יותר מאשר הגרסה H1o (תכלת). שברים נייד נייח ו Bleach עומק מצוינים עבור HP1.
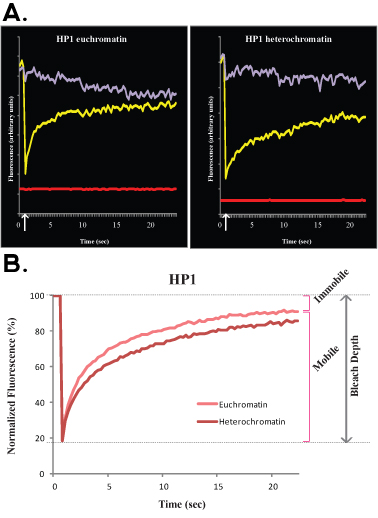
איור 2. A ו-B להראות נציג FRAP עקומות השוואת euchromatin (משמאל) עם heterochromatin (מימין) של HP1 R1 בתאי גזע עובריים. בדומה איור 1, איור 2 א מראה הנתונים הגולמיים של תא בודד, עקומת צהוב מתאים באזור מולבן, עקומת סגול המתאים לאזור הלא מולבן הגרעינית, ואת הקו האדום מתאים פלואורסצנציה הרקע. החץ האנכי מייצג את הזמן אקונומיקה. נתונים מנורמל ממוצעים של מוצג תרשים 2B. הערה התאוששות איטית של heterochromatin (אדום כהה) לעומת euchromatin (אור אדום). שברים נייד נייח ו Bleach עומק מצוינים עבור euchromatin.
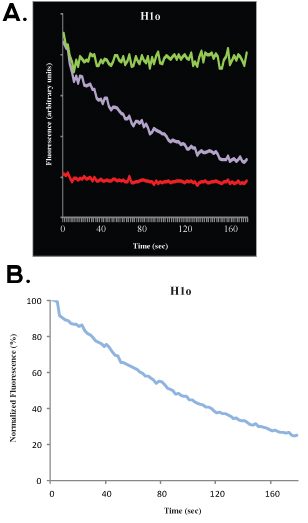
איור 3.. הניסוי FLIP אופייני H1o תאים R1 ES מוצג באיור 3 א (גולמיים, בלתי מנורמל נתונים) ו-B (נתונים ממוצעים של מנורמל). בניסוי זה את עקומת סגול המתאים לאזור הלא מולבן הגרעיני, הקו הירוק מתאים גרעין התא השכנות הקו האדום מתאים פלואורסצנציה הרקע.
Discussion
שלא כמו בשיטות הזמינות ביותר, אשר כרוך הכרומטין מטוהרים מן אוכלוסיות תאים או תאים קבוע, ניסויים FRAP בעקבות שינויים הדינמיקה חלבון הכרומטין בתאים חיים. מצאנו הדינמיקה הכרומטין חלבון להיות אינדיקטור טוב עבור פלסטיות הכרומטין. עם זאת, מכיוון שהיא דורשת פיוזינג את הגן של...
Disclosures
Acknowledgements
אנו מודים לחברי מעבדה משורר, במיוחד שי מלצר, עדי Alajem, Edupuganti ראגו רם, באדי סרי Sailaja, אנה Mattout ואלווה בירן, הערות ביקורתיות עבור בעיות הירי ניסויים photobleaching על בסיס יומי. EM מהווה ח ר 'יוסף בל בראון מרצה בכיר למדעי החיים והוא נתמך על ידי הקרן הלאומית למדע (ISF 943/09), את משרד הבריאות (6007) האיחוד האירופי (IRG-206872 ו 238176), למלחמה בסרטן Research Foundation, מענקים פנימי רפואי יישומי של האוניברסיטה עברית ואת הפסיכו המכון הישראלי.
Materials
| Name | Company | Catalog Number | Comments |
| שם מגיב | חברה | מספר קטלוגי | |
|---|---|---|---|
| DMEM | סיגמא | D5671 | |
| לטין | מרק | 1.04078 | |
| Opti-ממ | Gibco | 31985 | |
| Transit-LT1 | Mirus | MIR2300 | |
| 8-μ היטב-שקופיות | ibidi | 80826 |
References
- Phair, R. D. Global nature of dynamic protein-chromatin interactions in vivo: three-dimensional genome scanning and dynamic interaction networks of chromatin proteins. Mol Cell Biol. 24, 6393-6402 (2004).
- Meshorer, E., Girard, L. . Imaging chromatin in embyonic stem cells in StemBook. , (2008).
- Meshorer, E. Hyperdynamic plasticity of chromatin proteins in pluripotent embryonic stem cells. Dev Cell. 10, 105-116 (2006).
- Bancaud, A., Huet, S., Rabut, G., Ellenberg, J. . Fluorescence perturbation techniques to study mobility and molecular dynamics of proteins in live cells: FRAP, photoactivation, photo conversion, and FLIP. , (2009).
- Dundr, M., Misteli, T. Measuring dynamics of nuclear proteins by photobleaching. Curr Protoc Cell Biol. Chapter 13, Unit 13-Unit 13 (2003).
- Ellenberg, J. Nuclear membrane dynamics and reassembly in living cells: targeting of an inner nuclear membrane protein in interphase and mitosis. J Cell Biol. 138, 1193-1206 (1997).
- Lenser, T., Weisshart, K., Ulbricht, T., Klement, K., Hemmerich, P. Fluorescence fluctuation microscopy to reveal 3D architecture and function in the cell nucleus. Methods Cell Biol. 98, 2-33 (2010).
- Mueller, F., Mazza, D., Stasevich, T. J., McNally, J. G. FRAP and kinetic modeling in the analysis of nuclear protein dynamics: what do we really know. Curr Opin Cell Biol. 22, 403-411 (2010).
- Phair, R. D., Misteli, T. Kinetic modelling approaches to in vivo imaging. Nat Rev Mol Cell Biol. 2, 898-907 (2001).
- Poser, I. BAC TransgeneOmics: a high-throughput method for exploration of protein function in mammals. Nat Methods. 5, 409-415 (2008).
- Sigal, A. Generation of a fluorescently labeled endogenous protein library in living human cells. Nat Protoc. 2, 1515-1527 (2007).
- Cohen, A. A. Dynamic proteomics of individual cancer cells in response to a drug. Science. 322, 1511-1516 (2008).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved