A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
מדידה של הפצות לחות תלת-ממדיות בתאים חיים באמצעות הדמיה וניתוח FRET היפרספקטרליים
In This Article
Summary
בשל יחס אות לרעש נמוך (SNR) של חיישנים מבוססי העברת אנרגיית תהודה של Fӧrster (FRET), מדידת אותות המחנה הייתה מאתגרת, במיוחד בשלושה ממדים מרחביים. כאן, אנו מתארים מתודולוגיית דימות וניתוח FRET היפרספקטרלית המאפשרת מדידה של התפלגות המחנה בשלושה ממדים מרחביים.
Abstract
AMP מחזורי הוא שליח שני המעורב במגוון רחב של פעילויות תאיות ופיזיולוגיות. מספר מחקרים מצביעים על כך שאותות המחנה ממודרים, וכי המידור תורם לאותת על הספציפיות בתוך מסלול האיתות של המחנה. הפיתוח של biosensors מבוססי העברת אנרגיה תהודה Fӧrster (FRET) קידם את היכולת למדוד ולדמיין אותות cAMP בתאים. עם זאת, מדידות אלה מוגבלות לעתים קרובות לשני ממדים מרחביים, מה שעלול לגרום לפרשנות שגויה של נתונים. עד כה, היו רק מדידות מוגבלות מאוד של אותות המחנה בשלושה ממדים מרחביים (x, Y ו- z), בשל המגבלות הטכניות בשימוש בחיישני FRET המציגים מטבעם יחס אות לרעש נמוך (SNR). בנוסף, גישות הדמיה מסורתיות המבוססות על מסנן אינן יעילות לעתים קרובות למדידה מדויקת של אותות המחנה באזורים תת-תאיים מקומיים בשל מגוון גורמים, כולל הצלבה ספקטרלית, עוצמת אות מוגבלת ופלואורסצנטיות אוטומטית. כדי להתגבר על מגבלות אלה ולאפשר שימוש בביוסנסורים מבוססי FRET עם פלואורופורים מרובים, פיתחנו גישות דימות וניתוח FRET היפרספקטרליות המספקות ספציפיות ספקטרלית לחישוב יעילות FRET והיכולת להפריד באופן ספקטי אותות FRET מפלואורסצנטיות אוטומטית מבלבלת ו / או אותות מתוויות פלואורסצנטיות נוספות. כאן, אנו מציגים את המתודולוגיה ליישום הדמיית FRET היפרספקטרלית, כמו גם את הצורך לבנות ספרייה ספקטרלית מתאימה כי הוא לא undersampled ולא דגימת יתר לבצע unmixing ספקטרלי. בעוד אנו מציגים מתודולוגיה זו למדידה של התפלגות טמפ תלת מימדית בתאי אנדותל מיקרו-וסקולריים ריאתיים (PMVECs), מתודולוגיה זו יכולה לשמש לחקר הפצות מרחביות של המחנה במגוון סוגי תאים.
Introduction
אדנוסין מונופוספט מחזורי (באנגלית: Adenosine monophosphate) הוא שליח שני המעורב בתהליכים תאיים ופיזיולוגיים מרכזיים, לרבות חלוקת תאים, זרם סידן, שעתוק גנים והתמרת אותות. גוףגדל והולך של ראיות מצביע על קיומם של תאי המחנה בתא שדרכו מושגת הספציפיות של האיתות 1,2,3,4,5,6,7. עד לאחרונה, מידור המחנה הסיק בהתבסס על השפעות פיזיולוגיות או תאיות ברורות הנגרמות על ידי אגוניסטים קולטנים שונים מצמידי G8,9,10,11. לאחרונה, בדיקות הדמיית פלואורסצנטיות מבוססות FRET סיפקו גישות חדשות למדידה ותצפית ישירה של אותות המחנה בתא12,13,14.
העברת אנרגיית תהודה של Förster (FRET) היא תופעה פיזית שבה העברת אנרגיה מתרחשת בין מולקולות תורם ומקבל בצורה לא רדיאטורית כאשר המולקולות נמצאות בסמיכות15,16. עם התפתחותם של אינדיקטורים פלואורסצנטיים מבוססי FRET, תופעה פיזית זו שימשה ביישומים ביולוגיים לחקר אינטראקציות חלבון-חלבון17, חלבון שיתוף לוקליזציה18, Ca+2 איתות19, ביטויגנים 20, חלוקת תאים21 ואיתות נוקלאוטיד מחזורי. מחווני המחנה מבוסס FRET מורכבים בדרך כלל מתחום כריכת המחנה, פלואורופור תורם ופלואורופור מקובל22. לדוגמה, חיישן H188 cAMP12,22 המשמש במתודולוגיה זו מורכב מתחום כריכת המחנה המתקבל מ- Epac, בין פלואורופורים בצבע טורקיז (תורם) ונוס (מקבל). בתנאים בסיסיים (לא מאוגדים), טורקיז ונוגה נמצאים באוריינטציה כך FRET מתרחשת בין הפלורופורים. בעת קשירת המחנה לתחום הכריכה, מתרחש שינוי קונפורמציה כך שטורקיז ונוגה מתרחקים זה מזה וכתוצאה מכך ירידה ב- FRET.
גישות הדמיה מבוססות FRET מציעות כלי מבטיח לחקירה והדמיה של אותות המחנה בתוך התא. עם זאת, טכניקות הדמיה מיקרוסקופיות מבוססות FRET הנוכחיות מצליחות לעתים קרובות רק באופן חלקי בהשגת עוצמת אות מספקת כדי למדוד FRET בבהירות מרחבית תת-תאית. זאת בשל מספר גורמים, כולל עוצמת האות המוגבלת של כתבי FRET רבים, רמת הדיוק הגבוהה הנדרשת לכימות מדויק של שינויים ביעילות FRET, ונוכחות של גורמים מבלבלים, כגון autofluorescence הסלולר23,24. התוצאה היא לעתים קרובות תמונה FRET כי הוא מוטרד על ידי SNR חלש, מה שהופך את הדמיה של שינויים תת תאיים FRET קשה מאוד. בנוסף, חקירה של אותות המחנה המותאמים לשפות הפליא בוצעה כמעט אך ורק בשני ממדים מרחביים בלבד והתפלגות המחנה צירי נחשבה לעתים רחוקות25. סביר להניח שהסיבה לכך היא ש-SNR נמוך עכב את היכולת למדוד ולדמיין מעברי צבע של המחנה בשלושה ממדים מרחביים. כדי להתגבר על מגבלות של שימוש בחיישני FRET עם SNR נמוך, יישמנו גישות הדמיה וניתוח היפרספקטרליות כדי למדוד FRET בתאים בודדים25,26,27.
גישות הדמיה היפרספקטרליות פותחו על ידי נאס"א כדי להבדיל בין אובייקטים יבשתיים הנמצאים בתמונותלווין 28,29. טכניקות אלה תורגמו מאז לשדה מיקרוסקופיה פלואורסצנטית30, עם מספר מערכות מיקרוסקופ קונפוקליות מסחריות המציעות גלאים ספקטרליים. בהדמיית פלואורסצנטיות מסורתית (לא ספקטרלית), המדגם מתרגש באמצעות מסנן פסים או קו לייזר, והפליטה נאספה באמצעות מסנן פסים שני, שנבחר לעתים קרובות כדי להתאים את אורך הגל של פליטת השיא של הפלואורופור(ים). לעומת זאת, גישות הדמיה היפרספקטרליות מבקשות לדגום פרופיל ספקטרלי מלא של פליטת פלואורסצנטיות26,31,32 או עירור33,34 במרווחי זמן ספציפיים אורך גל. במחקרים הקודמים שלנו, הראינו כי גישות הדמיה וניתוח היפרספקטרליות יכולות להציע כימות משופר של אותות FRET בתאים בהשוואה לטכניקות הדמיה FRET מבוססות מסנן מסורתיות26. כאן, אנו מציגים מתודולוגיה לביצוע חלוקות וניתוח FRET תלת-ממדיות (x, Y, z ו- λ) כדי למדוד ולדמיין התפלגותamp בשלושה ממדים מרחביים. גישות אלה אפשרו הדמיה של מעברי צבע מרחביים של cAMP הנגרמים על-ידי אגוניסט בתאים בודדים25. מעניין, בהתאם אגוניסט, מעברי צבע המחנה עשוי להיות גלוי בתאים. המתודולוגיה המוצגת כאן משתמשת בהסרת ההסרה הספקטרלית של רקע לא אחיד ואוטלואורסצנטיות תאית כדי לשפר את הדיוק של מדידות FRET. בעוד מתודולוגיה זו מודגמת בתאי אנדותל מיקרו וסקולריים ריאתיים (PMVECs) באמצעות biosensor FRET cAMP, המתודולוגיה יכולה בקלות להיות שונה לשימוש עם כתבי FRET חלופיים או קווי תאים חלופיים.
Protocol
פרוטוקול זה עוקב אחר נהלים שאושרו על ידי אוניברסיטת דרום אלבמה מוסדית לטיפול בבעלי חיים ושימוש בוועדה.
1. הכנת תאים, דגימה וריאגנט להדמיה
- לבודד תאי אנדותל מיקרו וסקולריים ריאתי חולדה (PMVECs) כמתואר בעבר35.
הערה: תאים היו מבודדים ותרבית על ידי הליבה תרבית התא באוניברסיטת דרום אלבמה, נייד, AL על 100 מ"מ תרבית תאים צלחות. - זרע PMVECs מבודד על כיסויי זכוכית עגולה 25 מ"מ ולתת להם לגדול באינקובטור ב 37 °C (37 °F) עד התאים להשיג לפחות 80% השפעה (לפחות 24 שעות).
הערה: תאים וסוג התא עשויים להשתנות ממחקר למחקר ולכן יש לעקוב אחר הליכי תרבית תאים ספציפיים לתאים כדי לזרוע ולגדל תאים. פרוטוקול זריעת תאים ופולחן המשמש במחקרים אלה זמין כמידע משלים בקובץ בשם "תרבות File_Cell משלימה ו Transfection". - נצלו PMVECs עם ביו-סנסור FRET ודגרה למשך 48 שעות ב-37 °C (75 °F).
הערה: הפרוטוקול כדי transfect PMVECs מתואר גם בקובץ מידע משלים בשם "תרבות File_Cell משלימה transfection". - ביום ההדמיה, חימם את המאגר של טיירוד ל 37 °C (50 °F) באמבט מים.
הערה: המאגר של טיירוד מורכב מ- 145 מ"מ NaCl, 4 מ"מ KCl, 10 מ"מ HEPES, 10 מ"מ גלוקוז, 1 מ"מ MgCl2 ו- 1 mM CaCl2 - הר כיסוי המכיל תאים שהודבקו לתא תא ואבטח את החלק העליון עם אטם הרכבה כדי למנוע דליפה.
- נגב את החלק התחתון של כיסוי באמצעות מחיקת משימה עדינה לניקוי כל מדיה עודפת או תאים דבקים.
- הוסף 800 μL של חיץ עובד ו 4 μL של תווית גרעינית 5 mM לתא התא וסלע בעדינות במשך 5 - 10 שניות.
הערה: בעת הוספת פתרונות חוצץ או ריאגנט לכיסויים המותקנים בתא התא, הקפד להוסיף את הפתרון בעדינות ובצד תא התא כדי לא לפרק תאים דבקים. הוספת 4 μL של תווית גרעינית 5 mM ל 800 μL של חוצץ עושה 25 μM ריכוז סופי של תווית גרעינית. עבור תאים דבקים באופן רופף כגון תאי HEK293, מערבבים תחילה תווית גרעינית ומאגר בתקנה ולאחר מכן מוסיפים לכיסויים המותקנים בתא התא. פעולה זו תמנע הרמת התאים מהכיסוי. - לכסות את תא התא עם רדיד אלומיניום כדי להגן מפני אור ודגורה במשך 10 דקות בטמפרטורת החדר.
- הכנה ריאגנט: להוסיף 1 μL של 50 mM forskolin כדי 199 μL של חוצץ. זה יפיק ריכוז סופי של forskolin של 50 מיקרומטר כאשר נוסף לתאים שהוכנו עם 800 μL של חוצץ. 1 μL של DMSO ב 199 μL של חוצץ צריך גם להיות מוכן לשמש כשליטת רכב.
הערה: במחקרים אלה, forskolin משמש מפעיל אדניל ציקלאז כדי לעורר ייצור המחנה. אם תרצה, מתודולוגיה זו יכולה להשתנות בקלות כדי לאפשר טיפול עם ריאגנטים חלופיים לגירוי או עיכוב אדניל ציקלאז, פוספודיזטראזים וכו '.
2. רכישת תמונות
- השתמש במיקרוסקופ קונפוקלי המצויד בגלאי ספקטרלי.
הערה: כל שלבי רכישת התמונות המתוארים כאן פותחו באמצעות מערכת מיקרוסקופ ניקון A1R זמינה מסחרית. ייתכן שיהיה צורך להתאים שלבים אלה אם משתמשים במיקרוסקופ ספקטרלי חלופי. ודא כי כל הציוד מופעל לפחות 30 דקות לפני תחילת הניסוי כדי להגיע לתנאי הפעלה יציבים. - בחר את המטרה טבילת מים 60x ולהוסיף טיפת מים למטרה.
הערה: להדמיה של תאים חיים ברזולוציה גבוהה, מומלץ להשתמש במטרה צמצם מספרי גבוה. עיין ברשימת החומרים לקבלת מידע אודות המטרה המשמשת במחקרים אלה. - הנח את תא התא הטעון (משלב 1.7) על שלב המיקרוסקופ.
- בחר את המסנן DFT (DAPI/FITC/TRITC) שהוגדר על-ידי כוונון ידית המסנן בצד ימין של המיקרוסקופ.
- הפעל את המיקרוסקופ במצב פלואורסצנטיות רחבת שדה באמצעות העינים כדי לבחור שדה תצוגה המכיל תאים המבטאים את חיישן FRET המחנה.
הערה: ודא שהעוצמה הממוצעת של אות FRET באורך הגל של שיא פליטת התורם או המקבל בתא הנבחר היא לפחות 100 יחידות עוצמה (A.U.) או לפחות פי 4 מהאות הבסיסי של אזור ללא תאים מתבטאים. ניתן לאשר זאת באמצעות מציג פרופיל הספקטרום הזמין בתוכנת רכיבי NIS. כאשר מחפשים תא עם אות טוב, מומלץ להשליך תאים בהירים מדי (הם עלולים להיות בסכנה). - פתחו תוכנת NIS, עברו למצב קונפוקל, פתחו את כפתור ההשתלבות בלייזר ולחצו על Live.
- השתמש בידית המוקד כדי להתמקד בתאים על-ידי התבוננות בתצוגה המקדימה על המסך.
- קבע תצורה של הגדרות התקן, רכישה וערימת z בתוכנה, כמתואר להלן.
- הגדרות רכישה:
הערה: ניתן להחיל הגדרות רכישת מצלמה והתקן באמצעות תמונה שנרכשה בעבר. פתח את התמונה, לחץ באמצעות לחצן העכבר הימני ובחר 'שימוש חוזר בהגדרות המצלמה'.- פתח את תפריט הגדרות A1, סמן את התיבות המתאימות לקווי לייזר של 405 ננומטר ו- 561 ננומטר, בחר SD לגלאי ספקטרלי, בחר 10 לרזולוציה ו- 31 לערוצים.
הערה: תפריט הגדרות A1 מוצג כסמל גלגל שיניים קטן בפינה הימנית העליונה של חלון הגדרות A1 Plus. לייזר 405 ננומטר משמש להתרגשות תורמים ולייזר 561 ננומטר משמש לתסיסת גרעינית. - הגדר את טווח אורך הגל (410 - 730 ננומטר) על-ידי בחירת ערכי אורך גל התחלה וסיום.
- לחץ על סמל binning/skip בתפריט הגדרות A1 ובחר בתיבה ממוספרת 15 ולאחר מכן לחץ על אישור בתפריט הגדרות A1.
הערה: זה כדי להסיר את ערוץ אורך הגל המתאים לייזר עירור 561 ננומטר (זה בדרך כלל ערוץ אורךהגל 15). חשוב לא להשתמש בפס אורך הגל הזה כדי למנוע אות נמוך באופן מלאכותי, אשר יכול ליצור חפץ ספקטרלי. האות נמוך יותר ברצועה זו בגלל האצבע המכנית המכסה את אלמנט הגלאי כדי להגן עליו מפני נזק לייזר. - הגדר את עוצמות הלייזר ל- 8% ו- 2% עבור לייזרי 405 ננומטר ו- 561 ננומטר, בהתאמה, Si Hv (רווח גלאי) ב- 149, ורדיוס חור סיכה של 2.4 יחידות דיסק אוורירית (AU).
הערה: ייתכן שיהיה להתאים את עוצמות הלייזר בהתאם לגיל המכשיר ומצב הלייזרים. אם התאמת עוצמות לייזר בין דגימות שונות או קבוצות ניסוי, חשוב לשמור על אותו יחס של עוצמות לייזר (למשל, 8:2). בנוסף, חשוב לבחור בעוצמת לייזר שאינה כה בהירה עד כדי יצירת ליבנה מהירה. יש להתאים את רווח הגלאי כדי למקסם את עוצמת האות תוך מזעור רעש הגלאי. עבור מחקרים אלה, רווח של 149 שימש. גודל חור סיכה של 2.4 AU נבחר כאיזון בין רכישת תמונות עם יחס אות לרעש מספיק (SNR) לבין שמירה על חתך אופטי (confocality). עלייה בגודל חור הסיכה מגדילה את SNR אך מקטינה את הקונפוצליות. - הגדר את מהירות הסריקה ל- 0.25 מסגרות ספקטרליות לשניה, בחר את הסמל המתאים ל- חד-כיווני לכיוון הסריקה, הזן 4 לספירה והגדר 1024 x 1024 עבור גודל הסריקה.
הערה: אותות FRET חלשים, ומהירות סריקה איטית נדרשת לעתים קרובות. באמצעות מהירות סריקה של 0.25, רכישת מחסנית z ספקטרלית הושלמה בתוך ~ 3 דקות. מהירות הסריקה יכולה להיות מוגברת או מופחתת בהתאם פלואורופורים בשימוש. לדוגמה, עבור פלואורופורים בהירים יותר כמו eGFP, ניתן להשתמש במהירות סריקה מהירה יותר (2 פריימים לשנייה). המספר שהוזן תחת ספירה תואם למסגרת המהווה ערך ממוצע של 4, המסייע בהפחתת רעש במהלך רכישת תמונה. עבור דוגמאות יציבות מאוד והיכן שהזמן אינו אילוץ, ניתן להשתמש בערכי ממוצע גבוהים יותר (עד 16) כדי להשיג תמונות עם SNR משופר.
- פתח את תפריט הגדרות A1, סמן את התיבות המתאימות לקווי לייזר של 405 ננומטר ו- 561 ננומטר, בחר SD לגלאי ספקטרלי, בחר 10 לרזולוציה ו- 31 לערוצים.
- הגדר פרמטרי רכישת z-stack:
הערה: ייתכן שיהיה צורך להתאים את הערכים שהוזנו בשלבים 2.10 כדי להתאים לשינויים בכריכה או בריכוז של תוויות פלואורסצנטיות, סוג התווית, מספר התוויות בהן נעשה שימוש, קו התא ושינויים אחרים בהכנת הדגימה שעשויים להשפיע על צפיפות תיוג התאים ו/או על הפלואורסצנטיות הסלולרית. בעת התאמת פרמטרי הרכישה, יש לנקוט זהירות כדי להשיג SNR מספיק תוך מזעור ההלבנה. בנוסף, בעת קביעת התצורה של בדיקה FRET ספקטרלי, יש לנקוט זהירות כדי להבטיח כי הפרמטרים לעבוד היטב על פני כל קבוצות הטיפול. מומלץ להפעיל ניסוי של כל קבוצת טיפול עם הגדרות הפרמטר המוצעות כדי להבטיח כי SNR מספיק והלבנת תמונות ממוזערת.- פתח את חלון הרכישה של ND על-ידי לחיצה על תצוגה → בקרת רכישה → רכישת ND.
- הזן את הנתיב/היעד ואת שם הקובץ כדי לשמור את קובץ ND בחלון המוקפץ.
- סמן את התיבה המתאימה לסדרת z.
- לחץ על חי בחלון הגדרות A1 פלוס. פעולה זו תפתח חלון צפייה חי.
- התאם את ידית המוקד במיקרוסקופ כדי לבחור את החלק העליון של התא ולחץ על עליון בחלון הרכישה של ND כדי להגדיר את המיקום הנוכחי כחלק העליון.
הערה: מומלץ להתמקד מעט מעל החלק העליון של התא כדי להבטיח שכל התא נדגם בסידרת z. - התאם את ידית המוקד במיקרוסקופ כדי לבחור את החלק התחתון של התא ולחץ על Bottom בחלון הרכישה של ND כדי להגדיר את המיקום הנוכחי כתחתית.
הערה: התמקד מעט מתחת לתחתית התא כדי להבטיח שכל התא יידגם. - הזן 1 מיקרומטר עבור גודל שלב, בחר בחלק העליון התחתון עבור כיוון סריקת z ולחץ על הפעל בחלון רכישת ND כדי להשיג מחסנית z.
הערה: גודל השלב קובע את מספר פרוסות z שנרכשו בהתאם למיקומים העליונים והתחתונים (כלומר, המרחק שעבר). גודל שלב של 1 מיקרומטר נבחר כפשרה בין מהירות הדמיה, דגימת ציר z והלבנת תמונות. באמצעות קוטר חור הסיכה הקונפוקל של 2.4 AU ואת המטרה טבילת מים 60x הביא עובי סעיף אופטי של 1.73 מיקרומטר. לפיכך, גודל שלב 1 מיקרומטר הוא מעט מתחת קריטריוני הדגימה Nyquist, אבל זה פשרה שנעשתה כדי להפחית את הזמן הדרוש כדי לרכוש z-מחסנית. עבור דגימות יציבות מאוד, אשר מהירות אינה קריטית, צעד קטן יותר z-ציר ואולי קוטר חור קונפוקלי קטן יותר עשוי לשמש כדי להגדיל את רזולוציית ציר z. החלק התחתון אמור להניב תוצאות דומות וניתן להשתמש בו כדי להעריך את כל ההשפעות של ליחתום תמונות שעלולות להתרחש במהלך סריקת z.
- הגדר את מערכת המיקוד המושלמת (PFS) אם היא זמינה:
הערה: PFS מאפשר למערכת לפצות על תנודות בעומק המוקד במהלך רכישת תמונה. ניתן להשתמש בשלבים הבאים כדי להגדיר PFS, וצעדים אלה עשויים להשתנות מעט בהתאם לגירסת ניקון A1R ולגרסת רכיבי NIS בהם נעשה שימוש.- סמן מצב סימטרי המוגדר על-ידי סמל הטווח בחלון הרכישה של ND.
- הפעל את לחצן PFS על הפנים הקדמיות של המיקרוסקופ (ודא שידית המראה הדיכרואית הממוקמת במקטע שמתחת לשלב המדגם היא 'ב').
- הגדיר מחדש את החלק העליון (סובב נגד כיוון השעון) והתחתון (סובב בכיוון השעון) באמצעות הידית בחזית של בקר היסט PFS.
- הגדר מיקום z/z יחסי על-ידי לחיצה על 'יחסי' בחלון הרכישה של ND.
- לחץ על זיכרון על הפנים הקדמיות של המיקרוסקופ, כך שהתוכנה תשנן את עומק z היחסי.
- לאחר השלמת רכישת z-stack, הוסיפו בעדינות את ריאגנט הרצוי (forskolin או בקרת רכב) באמצעות פיפטה והמתינו 10 דקות.
הערה: הוסף את ריאגנט בעדינות רבה כדי לא להפריע לתאים או להזיז את המיקום של תא התא בתוך שלב המיקרוסקופ XY; מומלץ לוודא בתצוגה חיה או בתמונה שלאחר מכן ששדה הראייה לא השתנה במהלך הוספת ריאגנט. זמן ההמתנה של 10 דקות הוא שהטיפול בסלקולין ייכנס לתוקף. אם נעשה שימוש בטיפול אלטרנטיבי, ייתכן שיהיה צורך להתאים את זמן ההמתנה. - לאחר 10 דקות, שנה את שם הקובץ ולחץ על הפעל בחלון הרכישה של ND.
- חזור על שלבים 2.11 – 2.13 כמפורט לעיל עבור לפחות 5 כיסויים כדי להשיג תוצאות מספיקות לניתוח סטטיסטי (n = 5 עבור כל קבוצת טיפול – forskolin ובקרת רכב).
- הכן דוגמאות וריק מדגם כדי לבנות את הספריה הספקטרלית ולרכוש תמונות ספקטרליות באמצעות הגדרות רכישה דומות כפי שמתואר בשלבים 2.9 ו- 2.10.
3. ניתוח תמונה
הערה: תמונות אלה ישמשו לבניית ספרייה ספקטרלית המכילה את הספקטרום הטהור של כל הבאים הבודדים הקיימים במחקר. המברים הסופיים בספרייה הספקטרלית עשויים להשתנות ממחקר למחקר אם משתמשים בפלואורופורים שונים. הליך מפורט לבניית הספרייה הספקטרלית מסופק בקובץ מידע משלים בשם "ספריית File_Spectral משלימה". כאן, אנו מתארים ייצוא נתונים לקבצים .tiff, ביטול ספקטרלי ליניארי, מדידות יעילות FRET, שחזור תלת מימדי ואומדן רמות המחנה. ניתוח תמונה יכול להתבצע באמצעות ניתוח תמונות ופלטפורמות תכנות שונות כגון ImageJ, פייתון, MATLAB או CellProfiler. במחקרים אלה, סקריפטים MATLAB שימשו.
- יצא נתוני תמונה:
- צור תיקיות חדשות עם אותו שם קובץ המתאים לתמונות הערימה z הספקטרליות שנרכשו בשלבים 2.13 ו- 2.14.
הערה: השלבים הבאים המתוארים לייצוא נתונים ספציפיים עבור רכיבי NIS AR גירסה 4.30.01. שלבים אלה עשויים להשתנות מעט בהתאם לגירסת התוכנה. - לחץ על קובץ, שיפתח חלון קובץ. עיין ובחר את קובץ התמונה הספקטרלי שנרכש בשלב 2.12 ולחץ על פתח.
- לאחר טעינת הקובץ, לחץ על קובץ→ ייבוא/ייצוא→ ייצוא מסמך ND.
- בחלון המוקפץ: עיין ובחר את התיקיה שנוצרה בשלב 3.1.1, בחר תבנית תמונה מתויגת (TIF) עבור סוג קובץ ולאחר מכן בחר תמונת מונו עבור כל ערוץ ושמור על עומק סיביות.
הערה: קידומת הקובץ תיווצר מראש; שנה ערך זה לנוחות. סדר האינדקס ישתנה בהתאם לערוצים שנבחרו, ועליו להציג "z, c" עבור יצירת אינדקס לפי מיקום z-slice תחילה ומספר רצועת אורך גל שני. ודא שהתיבות המתאימות להחלת LUTs או להוספת שכבות-על או לשמות נקודות שימוש לא נבחרו. - לחץ על יצא כדי לייצא את קבצי ה- tiff לתיקיית יעד כקבצי tiff בודדים.
- חזור על שלבים 3.1.2 – 3.1.5 כדי לייצא קבצי תמונה ספקטרליים שנרכשו בשלב 2.13.
- צור תיקיות חדשות עם אותו שם קובץ המתאים לתמונות הערימה z הספקטרליות שנרכשו בשלבים 2.13 ו- 2.14.
- ביטול ספקטרלי ליניארי:
- פתח את תוכנת התכנות.
הערה: סקריפט תכנות שפותח בהתאמה אישית כדי לבטל את ה- unmix תמונות ספקטרליות גולמיות מסופק באתר האינטרנט של אוניברסיטת דרום אלבמה BioImaging ו- BioSystems, תחת הכרטיסיה משאבים (https://www.southalabama.edu/centers/bioimaging/resources.html). - פתח את הקובץ שכותרתו "ביטול מיקסינג ליניארי.m" ולחץ על לחצן ההפעלה בסרגל הכלים של העורך.
- עיינו ובחרו את התיקיה המכילה את רצף הקבצים המיוצא *.tif שנוצר על ידי תוכנת NIS Elements.
- לחץ על אישור כדי להמשיך, אשר יפתח חלון חדש בשם אורך גל ו Z-Slice.
- העתק את שם הקובץ של הקובץ הראשון (ללא z-slice ומספר ערוץ) בתיקיה שנבחרה בשלב 3.2.4 והדבק אותו בשלב הראשון של תיבת הדו-שיח שכותרתה "הזן את שם התמונה".
- הזינו את מספר הערוצים בשלב השני שכותרתו "הזן את מספר רצועות אורך הגל", מספר פרוסות z בשלב השלישי שכותרתו "הזן את מספר פרוסות Z" ולחץ על אישור.
הערה: מספר רצועות אורכי הגל עשוי להשתנות אם מתבצעים שינויים בהגדרות הרכישה, כגון התאמת טווח אורך הגל או גודל צעד אורך הגל. מספר פרוסות Z עשוי להשתנות גם בהתאם לגובה התא. - עיין ובחר את קובץ אורך הגל בשם "Wavelength.mat" בחלון המוקפץ שכותרתו "בחר את קובץ המידע אורך הגל" ולחץ על פתח.
- עיין ובחר בקובץ "Library.mat" בחלון המוקפץ החדש שכותרתו "בחר את קובץ הספריה הספקטרלית", לחץ על פתח והמתן עד לסיום ביטול ה- Slicexing של הפרוסות.
הערה: קובץ Library.mat הוא קובץ המכיל ספקטרום טהור עבור כל פלואורופור endmember יחד עם autofluorescence התא וחתימות ספקטרליות רקע. במקרה זה, פלואורופור סוף השנה כוללים טורקיז, ונוס ו- DRAQ5. חתימות ספקטרליות ברקע כוללות פלואורסצנטיות תאית או מטריצה, פלואורסצנטיות מכסה, וכיסוי עקיפה. קובץ Wavelength.mat הוא קובץ המכיל מידע ערוץ אורך גל המשמש לרכישת התמונה הספקטרלית. קובץ ספריה לדוגמה וקובץ אורך גל זמינים באתר Bioimaging ו- Biosystems (ראה את הפתק מתחת ל- 3.2.1). לקבלת מידע נוסף על אופן יצירת ספריה ספקטרלית וקבצי אורך גל, עיין בקובץ מידע משלים בשם "ספריית File_Spectral משלימה". תמונות לא מעורבות המתאימות לכל פרוסת z יישמרו בתיקיה הנקראת "לא מעורב" שנוצרה במהלך תהליך ביטול המיקסם בתוך התיקיה שנבחרה בשלב 3.2.3.
- פתח את תוכנת התכנות.
- חישוב יעילות FRET:
- פתח את קובץ ה- Script של התוכנית הנקרא "multiFRRCF.m" ולחץ על הפעל.
הערה: קובץ תכנות זה זמין מאתר הביואימציה והביו-מערכות של אוניברסיטת דרום אלבמה (ראה הערה בשלב 3.2.1). - הזן את מספר הניסויים הניסיוניים שיש לנתח בתיבת הדו-שיח המוקפצת הנקראת "כמה תיקיות לריס" ולחץ על אישור.
הערה: יש לשמור נתוני תמונה מכל ניסוי בתיקיית תמונה נפרדת שאינה מעורבת. שלב זה פשוט מאפשר לקוד הניתוח לעבור בלולאה על תיקיות רבות כשלב לחיסכון בזמן. - עיין ובחר את התיקיות הלא מעורבות ולחץ על אישור.
הערה: מספר הפעמים שהחלון המוקפץ "חפש תיקיה" נפתח תלוי במספר שהוזן בתיבת הדו-שיח "כמה תיקיות לריסים" בשלב הקודם. עיין ובחר את התיקיות אחת אחרי השנייה. - בחלון המוקפץ החדש, הזן את המידע הבא בתיבות המתאימות: גורם קנה המידה הוא 12.4, הסף הוא 5.6, X, Y ותדירות Z הם 5, 5 ו- 1 בהתאמה, ואלגוריתם ההחלקה הוא גאוס.
הערה: גורם קנה המידה הוא ערך בפיקסלים/מיקרומטר וישמש לשינוי קנה המידה של דגימת כיוון Z לזו של כיוון XY. גורם קנה המידה מתקבל מגודל פיקסל התמונה, המסופק בדרך כלל כמטא-נתונים בתמונה עבור רוב מערכות המיקרוסקופ הקונפוקליות. לדוגמה, אם התמונה נרכשת עם מרווח של 0.08 מיקרומטר/פיקסלים, גורם קנה המידה צריך להיות 12.5 פיקסלים/מיקרומטר. ערך הסף ישמש לסף התמונות וליצור מסיכה בינארית של התא. יצרנו רשימה של ערכים אופטימליים המבוססים על עוצמת התורם+מקבל התמונות. השתמש ב- 4.5 כערך סף אם לתמונה יש עוצמת תורם+קבלה בהירה ורקע נמוך, ערך בין 5.6 ל- 6.5 עבור תמונות בעלות עוצמת תורם+קבלה מתונה בלבד ו/או רקע גבוה יותר, וערך של 7.5 ומעלה עבור תמונות בעלות עוצמת תורם+מקבל נמוכה מהרקע. ערך התדירות מתאים למרווח, במספר הפיקסלים, שבו הניקוד מתבצע בשלבים הבאים. לדוגמה, אם עומק Z של התא הוא 17 מיקרומטר עם גודל של 1 מיקרומטר שלב ומקדם קנה מידה של 12.5 פיקסלים/מיקרומטר משמש בכיוון XY, עומק ערכת הנתונים של התמונה התלת-ממדית יידגם מחדש ב- 212 פיקסלים (כיוון Z). בהתבסס על ערך תדר Z שהוזן (לדוגמה, פיקסל אחד), ערכת נתוני התמונה התלת-ממדית תיחתך מחדש החל מראש ערכת נתוני התמונה ולאחר מכן תעבור במרווחים של פיקסל אחד כלפי מטה. התוצאה היא 212 תמונות שנמסרו. אם הוזנו מרווח זמן גדול יותר של ערך תדר עבור תדר Z, ייווצרו פחות תמונות עם שרידים. תמונות שנחסכות נשמרות בשלבים הבאים. - לחץ על הפעל והמתן עד לביצוע כל מדידות FRET והשרידים.
הערה: תיקיה נפרדת נוצרת בספריית האב שאליה נשמרות תמונות יעילות FRET בגווני אפור ותמונות יעילות FRET צבעוניות (מפת צבעים מוחלת). לדוגמה, כל תמונות FRET בגווני אפור ובמפות צבע השזורות בכיוון X (מישור YZ) נשמרות בתיקיה הנקראת "Resliced_XFRET". - חזור על הניתוח עם הגדרות דומות לכל הניסויים – לפני ואחרי טיפולי forskolin ובקרות רכב.
הערה: שלבים המוזכרים בסעיף 3.3 מתארים את הערכים שיש להזין עבור קובץ ה- Script של תיכנות ניתוח FRET מותאם אישית כדי ליצור נתוני תמונה תלת-ממדיים של FRET. עם זאת, סקריפט זה מבצע מספר פעולות במהלך הפעלה, כולל: טעינת נתוני תמונה, יצירת ערימות תמונה, החלקה, חישובי יעילות FRET, יצירה והחלה של מסיכת גבול תא, שחזור תמונה תלת-ממדי, הוספת תמונות תלת-ממדיות במרווחי זמן שצוינו (תדרים), החלת מפת צבעים להמחשה חזותית של שינויי FRET ושמירת נתוני התמונה שהוחזרו לאותה ספריה. פרטים נוספים נכללו כהערות בקובץ ה- Script של התוכנית.
- פתח את קובץ ה- Script של התוכנית הנקרא "multiFRRCF.m" ולחץ על הפעל.
4. מיפוי יעילות FRET לרמות המחנה
- פתח את קובץ התיכנות בשם 'Mapping_FRET Efficiency_to_cAMP_concentration.m' ולחץ על הפעל בחלון הראשי.
הערה: הקובץ זמין באתר BioImaging ו- BioSystems (ראה הערה מתחת ל- 3.2.1). קובץ זה קורא תמונות יעילות FRET בגווני אפור וממיר אותן לרמות המחנה בהתבסס על עקומה אופיינית. עקומה אופיינית זו משתמשת בקשר גומלין של המחנה לפראט המתועד בספרות15,36 המתואר על-ידי משוואת היל (המשוואה השלישית המוצגת להלן). עם זאת, Kd של הבדיקה בתאים שלמים קשה להעריך והנחנו שזה יהיה 1 μM בחישובים שלנו. לפיכך, התוצאות מוצגות כפונקציה של Kd. (כלומר, [amp] = x* Kd). משוואות המשמשות למדידת יעילות FRET ומיפוי FRET לרמות המחנה מוצגות להלן: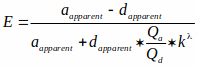
כאשר E הוא יעילות FRET, ו- d נראה לעין הם עוצמות פיקסלים לא מעורבות של תמונות קבלה ותורם, בהתאמה.
Qa ו- Qd הם תשואות קוונטיות של מקבל ותורם. שים לב ש- Qa ו- Qd מתבטלים כאשר המשוואה עבור kλ משולבת במשוואת היעילות FRET, kλ הוא גורםתיקון: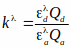
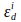
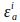 והם מקדמי הכחדה של תורם ומקבל באורך גל עירור התורם, i (405nm).
והם מקדמי הכחדה של תורם ומקבל באורך גל עירור התורם, i (405nm).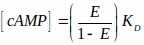
E הוא יעילות FRET ו- KD = קבוע דיסוציאציה = 1 מיקרומטר. - נווטו ובחרו בתמונת FRET הראשונה בקנה מידה אפור (שנשמרה בשלב 3.3.5) ולחצו על הלחצן 'אשר'.
- פתח את תמונות FRET/cAMP כדי לבדוק את התפלגות אותות המחנה בשלושה ממדים.
תוצאות
פרוטוקול זה מתאר את השימוש בגישות הדמיה וניתוח FRET היפרספקטרליות למדידת שיפועי המחנה בשלושה ממדים מרחביים בתאים חיים. ישנם מספר שלבים מרכזיים המעורבים ביצירת תוצאות אלה, שעבורם נדרשת תשומת לב זהירה בעת ניתוח וכימות הנתונים. צעדים מרכזיים אלה כוללים בניית ספריה ספקטרלית מתאימה, ביטול ספקט...
Discussion
הפיתוח של BIOSENSors FRET אפשר מדידה והדמיה של אותות נוקלאוטיד מחזורי בתאים בודדים, ויש הבטחה גדולה לדמיין אירועי איתות תת תאיים13,22,37,38. עם זאת, השימוש בביו-סנסורים FRET מציג מספר מגבלות, כולל מאפייני אות לרעש נמוכים של כתבי FRET מב...
Disclosures
ד"ר לייסלי וריץ' חושפים עניין פיננסי בחברת סטארט-אפ, SpectraCyte, LLC, שהוקמה כדי למסחר טכנולוגיות הדמיה ספקטרליות. עם זאת, כל ההליכים המתוארים בפרוטוקול זה נערכו באמצעות מוצרים זמינים מסחרית שאינם משויכים ל- SpectraCyte, LLC.
Acknowledgements
המחברים רוצים להכיר ד"ר קס Jalink (המכון לסרטן הולנד ומרכז ואן Leeuwenhoek למיקרוסקופיה מתקדמת, אמסטרדם, הולנד) על כך שסיפק לנו את H188 cAMP FRET biosensor וקני טרינה (המכללה להנדסה, אוניברסיטת דרום אלבמה) על עזרה טכנית בהפחתת הזמן שנדרש כדי להפעיל את תסריטי התכנות המפותחים בהתאמה אישית שלנו.
המחברים רוצים להכיר במקורות המימון: איגוד הלב האמריקאי (16PRE27130004), הקרן הלאומית למדע; (1725937) NIH, S100D020149, S10RR027535, R01HL058506, P01HL066299).
Materials
| Name | Company | Catalog Number | Comments |
| Attofluor Cell Chamber | Invitrogen | A7816 | Attofluor contains steel cell chambers and a rubber O-ring. Cell chamber holds the coverslip and O-ring provides a lock in mechanism to hold the buffer in cell chamber with out leakage |
| Dimethyl Sulfoxide (DMSO) | Fisher Scientific | BP231-100 | Solvent used to prepare stock solution forskolin. |
| DRAQ5 Fluoroscent Probe Solution | Thermo Scientific | 62252 | Nuclear label |
| Dulbecco Modified Eagle Medium (DMEM) | Gibco | 11965-092 | Contains nutrients and growth factors for the cells to grow and divide in the culture dishes. |
| Fetal Bovine Serum (FBS) | Sigma | F6178 | Growth factor suppliment that is added to culture medium, DMEM |
| Forskolin | Sigma | F3917 | Adenyly cyclase activator. |
| H188 Cyclic AMP FRET biosensor | Netherland Cancer Institute, Dr. K. Jalink | Gift | Plasmid encoding Turquoise (donor fluorophore), Venus (acceptor fluorophore), and binding domain obtained from Epac. |
| Image J | image.net | Free download | Another image processing platform used to extact spectral information and image processing. |
| Integrating Sphere | Ocean Optics | FOIS-1 | Used to measure illumination intensity of the laser line at different laser intensities (?). |
| Laminin Mouse Protein, Natural | Invitrogen | 23017-015 | Coverslips are coated with laminin and this helps in cell attachment, growth and motility of the cell. |
| Lipofectamine 3000 Transfection Kit | Invitrogen | L3000-015 | Transfection reagent used to transfect cells with H188 FRET biosensor |
| MATLAB | Mathworks | R2019a | Image processing operations (linear unmixing and FRET efficiency calculations) are performed by writing custom programs in MATLAB programming environment |
| Nikon A1R confocal microscope | Nikon Instruments | Nikon A1R | Spectral image acquisition is performed using confocal microscope. |
| Nikon Elements Software | Nikon Instruments | Software dongle | used to export and handle nd2 image files (multidimensional image files) that are aquired using Nikon A1R |
| NIST-Traceable Calibration Lamp | Ocean Optics | LS-1-CAL-INT | A lamp with a known spectrum for use as a standard |
| PBS pH 7.4 (1X) | Gibco | 10010-023 | coomonly used buffer suring cell culture |
| Pulmonary Microvascular Endothelial Cells (PMVECs) | In house - Cell culture core, Univeristy of South Alabama | Isolated from Rat pulmonary microvasculature | PMVECs form inner lining of a blood vessel. |
| Penicillin-Streptomycin (10,000 U/ml) | Gibco | 15140-122 | antibiotics are added to culture medum to prevent contamination of the cells. |
| Pre-Cleaned Gold Seal Micro Slides | Clay Adams | 3010 | Microscope slides used for cell fixation |
| ProLong Diamond Antifade Mounting Media | Invitrogen | P36961 | If samples are fixed using antifade mountant, then the later protects fluoroscent dyes and chromophores from fading. |
| Spectrometer | Ocean Optics | QE65000 | Used to measure spectral response of the light source (?) |
| Trypsin-EDTA (0.25%) | Gibco | 25200-056 | Digests the protein-protein bond between the cell and cell matrix and helps to disscociate and lift the cells during cell plating. |
| Tyrodes Buffer | Made in-house | Made in-house | Tyrodes buffer is used to make working solutions and to maintain cells in aqueous solution during image acquisition. |
| 6 Well Cell Culture Plate | Corning | 3506 | Laminin coated coverslips are placed in 6-well culture dish (one coverlisps/well). Cells along with medium is added into each well. |
| 25 mm Round Microscope Cover Slips | Fisher Scientific | 12545102 | Cells were grown on round glass coverslips |
| 60X Ojective | Nikon Instruments | Plan Apo VC 60X/1.2 WI ∞/0.15-0.18 WD 0.27 | water immersion and commonly used objective for cells |
References
- Corbin, J. D., Sugden, P. H., Lincoln, T. M., Keely, S. L. Compartmentalization of adenosine 3':5'-monophosphate and adenosine 3':5'-monophosphate-dependent protein kinase in heart tissue. The Journal of Biological Chemistry. 252, 3854-3861 (1977).
- Terrin, A., et al. PGE1 stimulation of HEK293 cells generates multiple contiguous domains with different [cAMP]: role of compartmentalized phosphodiesterases. The Journal of Cell Biology. 175, 441-451 (2006).
- Bacskai, B. J., et al. Spatially resolved dynamics of cAMP and protein kinase A subunits in Aplysia sensory neurons. Science. 260, 222-226 (1993).
- Iancu, R. V., Ramamurthy, G., Harvey, R. D. Spatial and temporal aspects of cAMP signalling in cardiac myocytes. Clinical and Experimental Pharmacology & Physiology. 35, 1343-1348 (2008).
- Brunton, L. L., Hayes, J. S., Mayer, S. E. Functional compartmentation of cyclic AMP and protein kinase in heart. Advances in Cyclic Nucleotide Research. 14, 391-397 (1981).
- Hohl, C. M., Li, Q. Compartmentation of cAMP in adult canine ventricular myocytes. Relation to single-cell free Ca2+ transients. Circulation Research. 69, 1369-1379 (1991).
- Rich, T. C., et al. A uniform extracellular stimulus triggers distinct cAMP signals in different compartments of a simple cell. Proceedings of the National Academy of Sciences of the United States of America. 98, 13049-13054 (2001).
- Sayner, S. L., Alexeyev, M., Dessauer, C. W., Stevens, T. Soluble adenylyl cyclase reveals the significance of cAMP compartmentation on pulmonary microvascular endothelial cell barrier. Circulation Research. 98, 675-681 (2006).
- Rich, T. C., Tse, T. E., Rohan, J. G., Schaack, J., Karpen, J. W. In vivo assessment of local phosphodiesterase activity using tailored cyclic nucleotide-gated channels as cAMP sensors. The Journal of General Physiology. 118, 63-78 (2001).
- Blackman, B. E., et al. PDE4D and PDE4B function in distinct subcellular compartments in mouse embryonic fibroblasts. Journal of Biological Chemistry. 286, 12590-12601 (2011).
- Sayner, S. L., et al. Paradoxical cAMP-induced lung endothelial hyperpermeability revealed by Pseudomonas aeruginosa ExoY. Circulation Research. 95, 196-203 (2004).
- Klarenbeek, J., Jalink, K. Detecting cAMP with an EPAC-based FRET sensor in single living cells. Methods in Molecular Biology. 1071, 49-58 (2014).
- Surdo, N. C., et al. FRET biosensor uncovers cAMP nano-domains at β-adrenergic targets that dictate precise tuning of cardiac contractility. Nature Communications. 8, 15031 (2017).
- Ponsioen, B., et al. Detecting cAMP-induced Epac activation by fluorescence resonance energy transfer: Epac as a novel cAMP indicator. EMBO Reports. 5, 1176-1180 (2004).
- Vogel, S. S., Thaler, C., Koushik, S. V. Fanciful FRET. Science's STKE. 2006, (2006).
- Clegg, R. M. The History of FRET: From conception through the labors of birth. Reviews in Fluorescence. 3, (2006).
- Giepmans, B. N. G., Adams, S. R., Ellisman, M. H., Tsien, R. Y. The fluorescent toolbox for assessing protein location and function. Science. 312, 217-224 (2006).
- Manzella-Lapeira, J., Brzostowski, J. A. Imaging protein-protein interactions by Förster resonance energy transfer (FRET) microscopy in live cells. Current Protocols in Protein Science. 93, 58 (2018).
- Cooper, D. M. F., Mons, N., Karpen, J. W. Adenylyl cyclases and the interaction between calcium and cAMP signalling. Nature. 374, 421-424 (1995).
- Sassone-Corsi, P. Coupling gene expression to cAMP signalling: role of CREB and CREM. The International Journal of Biochemistry & Cell Biology. 30, 27-38 (1998).
- Rebhun, L. I. Cyclic nucleotides, calcium, and cell division. International Review of Cytology. 49, 1-54 (1977).
- Klarenbeek, J., Goedhart, J., Van Batenburg, A., Groenewald, D., Jalink, K. Fourth-generation Epac-based FRET sensors for cAMP feature exceptional brightness, photostability and dynamic range: characterization of dedicated sensors for FLIM, for ratiometry and with high affinity. PLOS ONE. 10, 0122513 (2015).
- Leavesley, S. J., Rich, T. C. FRET: signals hidden within the noise. Cytometry Part A. 85, 918-920 (2014).
- Rich, T. C., Webb, K. J., Leavesley, S. J. Can we decipher the information content contained within cyclic nucleotide signals. The Journal of General Physiology. 143, 17-27 (2014).
- Annamdevula, N. S., et al. Spectral imaging of FRET-based sensors reveals sustained cAMP gradients in three spatial dimensions. Cytometry Part A. 93 (10), 1029-1038 (2018).
- Leavesley, S. J., Britain, A. L., Cichon, L. K., Nikolaev, V. O., Rich, T. C. Assessing FRET using spectral techniques. Cytometry Part A. 83, 898-912 (2013).
- Leavesley, S. J., Rich, T. C. Overcoming limitations of FRET measurements. Cytometry Part A. 89, 325-327 (2016).
- Fink, D. J. Monitoring Earcths Resources from Space. Technology Review. 75, 32-41 (1973).
- Goetz, A. F. H., Vane, G., Solomon, J. E., Rock, B. N. Imaging Spectrometry for Earth Remote Sensing. Science. 228, 1147-1153 (1985).
- Bücherl, C. A., Bader, A., Westphal, A. H., Laptenok, S. P., Borst, J. W. FRET-FLIM applications in plant systems. Protoplasma. 251, 383-394 (2014).
- Chen, Y., Mauldin, J. P., Day, R. N., Periasamy, A. Characterization of spectral FRET imaging microscopy for monitoring nuclear protein interactions. Journal of Microscopy. 228, 139-152 (2007).
- Zimmermann, T., Rietdorf, J., Girod, A., Georget, V., Pepperkok, R. Spectral imaging and linear un-mixing enables improved FRET efficiency with a novel GFP2-YFP FRET pair. FEBS Letters. 531, 245-249 (2002).
- Griswold, J. R., Annamdevula, N., Deal, J., Rich, T., Leavesley, S. Estimating FRET Efficiency using Excitation-Scanning Hyperspectral Imaging. Biophysical Journal. 112, 586 (2017).
- Favreau, P. F., et al. Excitation-scanning hyperspectral imaging microscope. Journal of Biomedical Optics. 19, 046010 (2014).
- King, J., et al. Structural and functional characteristics of lung macro- and microvascular endothelial cell phenotypes. Microvascular Research. 67, 139-151 (2004).
- Thaler, C., Koushik, S. V., Blank, P. S., Vogel, S. S. Quantitative multiphoton spectral imaging and its use for measuring resonance energy transfer. Biophysical Journal. 89, 2736-2749 (2005).
- Agarwal, S. R., et al. Compartmentalized cAMP signaling associated with lipid raft and non-raft membrane domains in adult ventricular myocytes. Frontiers in Pharmacology. 9, 332 (2018).
- Johnstone, T. B., Agarwal, S. R., Harvey, R. D., Ostrom, R. S. cAMP signaling compartmentation: Adenylyl cyclases as anchors of dynamic signaling complexes. Mol Pharmacol. , (2017).
- Zhang, J., Li, H., Chai, L., Zhang, L., Qu, J., Chen, T. Quantitative FRET measurement using emission-spectral unmixing with independent excitation crosstalk correction. Journal of Microscopy. 257, 104-116 (2015).
- Zhang, J., Lin, F., Chai, L., Wei, L., Chen, T. IIem-spFRET: improved Iem-spFRET method for robust FRET measurement. Journal of Biomedical Optics. 21, 105003 (2016).
- Levy, S., et al. SpRET: highly sensitive and reliable spectral measurement of absolute FRET efficiency. Microscopy and Microanalysis. 17, 176-190 (2011).
- West, S. J., et al. Hyperspectral Measurements Allow Separation of FRET Signals from Non-Uniform Background Fluorescence. Biophysical Journal. 112, 453 (2017).
- Annamdevula, N. S., et al. An approach for characterizing and comparing hyperspectral microscopy systems. Sensors. 13, 9267-9293 (2013).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved