Method Article
A Quantitative Analysis Fitness Workflow
* Questi autori hanno contribuito in egual misura
In questo articolo
Riepilogo
Fitness Quantitative Analysis (QFA) è una serie complementare di metodi sperimentali e computazionali per la stima convenienze coltura microbica. QFA stima l'effetto di mutazioni genetiche, farmaci o altri trattamenti applicati sulla crescita microbica. Esperimenti di scala dall'analisi focalizzata di singole culture a migliaia di colture in parallelo possono essere progettati.
Abstract
Fitness Quantitative Analysis (QFA) è un flusso di lavoro sperimentale e computazionale per confrontare convenienze delle colture microbiche cresciute in parallelo 1,2,3,4. QFA può essere applicato alle osservazioni focalizzate su singole culture, ma è molto utile per genome-wide interazione genetica o studiando schermi di droga fino a migliaia di culture indipendenti. Il metodo sperimentale è centrale l'inoculazione di indipendenti, diluiti colture liquide microbiche su piastre di agar solido che vengono incubate e regolarmente fotografato. Fotografie di ciascun punto temporale vengono analizzati, producendo quantitativi stime di densità cellulari, che vengono utilizzati per costruire curve di crescita, consentendo misure quantitative di fitness da derivati. Convenienze della cultura può essere paragonato a quantificare e classificare i punti di forza di interazione genetica o sensibilità di droga. L'effetto sul fitness cultura di eventuali trattamenti aggiunto in agar substrato (ad esempio piccole molecole, antibiotici o sostanze nutritive), ovvero applicati alle piastre esternely (ad esempio irradiazione UV, temperatura) può essere quantificato QFA.
Il flusso di lavoro QFA produce crescita stime analoghi a quelli ottenuti mediante misurazione spettrofotometrica della paralleli colture liquide in lettori di piastre da 96 pozzetti o 200-bene. È importante sottolineare che, QFA ha un throughput significativamente più alto rispetto a tali metodi. Culture QFA crescere su una superficie solida agar e sono pertanto ben aerato durante la crescita senza la necessità di mescolamento o agitazione.
Il throughput QFA non è così elevata come quella di alcuni Array sintetico genetica (SGA) metodi di screening 5,6. Tuttavia, poiché le culture QFA sono fortemente diluiti prima di essere inoculato su agar, QFA in grado di catturare le curve di crescita più complete, tra cui esponenziale e le fasi di saturazione 3. Ad esempio, le osservazioni curva di crescita consentire tempi di duplicazione di coltura per stimare direttamente con elevata precisione, come discusso in precedenza 1.
Qui vi presentiamo unospecifico protocollo QFA applicata a migliaia di S. cerevisiae culture che vengono automaticamente gestite da robot durante l 'inoculazione, incubazione e di imaging. Qualsiasi di queste fasi automatizzate può essere sostituito da un equivalente, procedura manuale, con associata una riduzione nella velocità, e si presentano anche un protocollo inferiore manuale velocità. Gli stessi strumenti software QFA possono essere applicati alle immagini catturate in entrambi flusso di lavoro.
Abbiamo una vasta esperienza applicando QFA alle culture del lievito nascente S. cerevisiae ma ci aspettiamo che QFA si rivelerà altrettanto utile per l'esame delle culture del lievito di fissione S. pombe e culture batteriche.
Protocollo
Manuale QFA Protocol (per ceppi di S. cerevisiae)
1. Coltura dei lieviti Ceppi
- Fino a 96 ceppi di lievito indipendenti sono coltivate in 200 microlitri di ricchi di liquidi in un piatto da 96 pozzetti cultura. I ceppi sono coltivati a saturazione in un incubatore a temperatura controllata.
- A 96 pin, 1/8 "di diametro manuale replica Plater (SIGMA-R 2508) è sterilizzato prima immergendo il Plater replica in 100% etanolo, fiammeggiante e poi lasciare raffreddare.
- 200 pl di acqua sterile è disposto in una piastra a 96 pozzetti coltura. Le culture saturi sono agitati (Eppendorf MixMate, 30 sec, 750 rpm) e diluita immergendo lo strumento sterilizzato pin nei ceppi saturi tre volte e poi nel piatto contenente l'acqua una volta.
- Lo strumento pin è ri-sterilizzati per 1,2.
- Lo strumento pin sterilizzato viene utilizzato per individuare la coltura diluita su piastre di agar venduti per immersione nella piastra contenente la cultura diluito tre volte in trasferire l'utensile perno di una piastra rettangolare agar solido.
- Le piastre rettangolari agar solido vengono incubati a una temperatura adeguata, prima di essere ripreso manualmente utilizzando un S & P Robotics spImager. Metodi alternativi di acquisizione delle immagini può essere utilizzato anche come un FujiFilm LAS4000, o una meno costosa fotocamera reflex digitale se si ha cura di garantire un'illuminazione uniforme e piastra di posizionamento coerente rispetto alla macchina fotografica.
- Il metodo è adattabile ad un numero inferiore di colture parallele come 48, che può essere montato su petri tonde se si ha cura di assicurare lo stesso angolo rispetto alla termocamera durante ogni fotografia.
Fully Automated QFA Protocol (per i ceppi di S. cerevisiae)
2. Coltura dei lieviti Ceppi
- Inizia con una matrice rettangolare di ceppi di lievito indipendenti che crescono su agar solido. In questo esempio, i ceppi di partenza sono il risultato di attraversare una temperaturainterrogazione mutazione sensibile con la Collezione di eliminazione lievito (YDC) di Synthetic Array genetica (SGA). Finali piastre SGA sono formato nel 1536. Si tratta di 16 righe per 24 colonne di colonie e culture che rappresentano quattro repliche di 384 ceppi di lievito indipendenti. Vedere la Figura 1 per i layout della piastra.
- 384 ceppi fuori di 1536 vengono trasferiti usando un robot S & P Robotics Inc BM3-SC robot con un perno 96, 1-mm pintool diametro del perno sterile in quattro piastre di coltura a 96 pozzetti contenenti 200 microlitri di terreni selettivi (Figura 1). Pintool pulizia e sterilità viene raggiunto da sequenzialmente lavaggio in acqua sterile per due volte (una volta con una spazzola rotante per rimuovere i detriti), 70% etanolo (con sonicazione) e infine etanolo 100%.
- Le colture sono coltivate a saturazione (per tre giorni a 20 ° C in questo esempio, vedi Figura 1).
3. Spotting lieviti
- Utilizzando un Beckman Biomek FX, culture saturi unonuovamente risospeso nel vortex su un Teleshake Variomag (in senso antiorario a 1000rpm per 20 secondi) e diluita di circa 1:70 da appuntare in 200 microlitri di acqua sterile utilizzando una sterile 96 pin strumento robotico pin (V & P scientifico magnetica di montaggio pintool, 2 diametro del perno mm). Strumento pulizia Pin e sterilità viene raggiunto da lavaggio in acqua sterile, lavaggio in 70% etanolo (con un pennello per rimuovere i detriti) e infine immersione in etanolo 70% seguita da essiccazione.
- Culture diluito sono macchiati su piastre di agar solidi in formato 384 utilizzando lo stesso strumento pin robotica (vedi Figura 1) dopo la pulizia e la sterilizzazione.
- Dopo pinning, le piastre vengono trasferiti ad una temperatura controllata Cytomat, incubatore umidificato con carosello automatico e portello di accesso.
4. Image Capture
- L'S & P Robotics automatica imager rimuove ripetutamente i piatti dall'incubatore Cytomat, toglie il coperchio della piastra, li colloca proprio in virtù di un allegared, illuminato in modo uniforme lo spazio sotto una Canon EOS Rebel Ti DSLR 35 mm, cattura l'immagine a 5184 x 3456 px risoluzione, sostituisce il coperchio della piastra, e li restituisce alla giostra incubatore. Una immagine viene catturata immediatamente successivo trasferimento iniziale per l'incubatore per consentire uno zero misura crescita punto nel tempo (background). Robot manipolazione e la fotografia prende 2 minuti per ogni piatto.
- Con una giostra a pieno carico, la massima frequenza raggiungibile immagine piastra di cattura è una fotografia ogni sei ore. Le piastre vengono incubate per un massimo di sei giorni (fino a saturazione colonia crescita. Figura 1 mostra tre immagini tipiche di un tempo portate a 20 ° C.
- Ai fini di monitoraggio, le piastre sono denominati in base al nome incubatore, temperatura, numero di lotto unico sequenziale e la posizione nell'incubatrice. I nomi delle immagini sono una concatenazione di targa e il timestamp e vengono costruite dopo la cattura di immagini (ad esempio K000011_030_010_2011-09-22_09-47-54.jpg, File Type FT1, Tabella 1).
5. Cattura di metadati Sperimentale
I file di metadati descritti in questa sezione sono delimitati da tabulazioni file di testo che vengono generati manualmente (ad esempio utilizzando il software foglio di calcolo). Il file di descrizione Sperimentale (FT2, Tabella 1) è unico per ogni esperimento, ma la descrizione Library (FT3, tabella 1) può essere ri-usato estensivamente, una volta costruito.
- L'esperimento è descritto nel file di descrizione Sperimentale (FT2, Tabella 1) contenente le colonne di codici a barre (o targa generato automaticamente), timestamp esperimento di partenza, il trattamento piatto, il contenuto di agar solido, screen name, la biblioteca, il numero di targa (per le biblioteche piastre multiple) e una ripetizione quadranti numerici (si veda la Figura 1) per scalare verso il basso dal 1536 formato a 384 in formato.
- La biblioteca ceppo di lievito è descritto con un file di libreria per la descrizione (FT3, Tabella 1) che indichi il genotipo cresciuto in ogni luogo della cultura in ogni piatto di una biblioteca. Esso contiene colonne per: nome della libreria, ORF, numero di targa, riga piastra, colonna a piatti e una colonna opzionale note.
- Un optional di file standard nome del gene (FT4, tabella 1) che descrive il nome standard gene (ad esempio RAD9) associato ad ogni sistematica ORF y-numero (ad esempio YDR217C) identificare i ceppi di essere proiettati può essere fornita. Questo file contiene due colonne: nome ORF & Gene.
6. Analisi dei dati
Il flusso di lavoro QFA computazionale richiede l'accesso a un sistema ragionevolmente potente workstation multicore computer (ad esempio un Dell Precision T3500 con Xeon quad-core 2,67 GHz e 12GB RAM) su cui è installata l'immagine Colonyzer strumento di analisi software 3,4 e il pacchetto QFA R 7 , entrambi i quali sono documentati online, sono disponibili gratuitamente ed eseguito su una vasta gamma di sistemi operativi.
- Esegui Colonyzer con ciascuna delle immagini catturate piastra come input, generando un file di output Colonyzer (FT5 Tabella 1) per ogni immagine catturata. I file di output Colonyzer stime di densità specifica cultura, area cultura, forma e colore per ciascuno dei 384 punti sulla piastra immaginata. Nome del file in uscita viene automaticamente copiato dal nome del file immagine di origine (ad esempio la fotografia piastra K000011_030_010_2011-09-22_09-47-54.jpg (FT1, tabella 1) corrisponde al file di output Colonyzer K000011_030_010_2011-09-22_09-47-54.dat ( FT5, Tabella 1)).
- Usando il pacchetto QFA R, caricare i metadati sperimentale (FT2, Tabella 1) e file di output (Colonyzer FT5 Tabella 1). Questi dati vengono uniti in R frame di dati (che può essere esportato come QFA prime file di testo (dati FT6, Tabella 1)) per ulteriori analisi.
- Il pacchetto R QFA contiene le funzioni per raccogliere timecourses densità cellulari per ogni cultura, per adattarsi generalizzato lomodelli di popolazione gistic alle osservazioni e di plot sia (vedi figure 2 e 3 per esempi). I valori dei parametri componibili vengono scritti i file di parametri QFA logistica FT7 (Tabella 1). Vedi QFA documentazione del pacchetto R per ulteriori dettagli.
- Il pacchetto R QFA contiene anche funzioni per il controllo della qualità: le colonie di bordo vengono scartati a causa della maggiore disponibilità di sostanze nutritive ai bordi della piastra e difficoltà di analisi di immagine in prossimità di pareti piastra, culture che non hanno il SGA e la visualizzazione di genotipi collegamento con screen-specifici geni marcatori sono eliminati dalle analisi.
- Diverse misure quantitative di fitness sono derivati da parametri logistici modello di popolazione per ogni cultura. Questi includono i tassi massimi di raddoppiamento della popolazione (MDR) e il numero di divisioni da inoculazione di saturazione (MDP). Per ogni insieme di culture repliche (di genotipo unico per esempio) e per ogni definizione di fitness, statistiche riassuntive diverse stime fitness sono compnon distribuiti: media e mediana fitness, palestra deviazione standard e il numero di repliche osservato. Statistiche di riepilogo vengono emessi QFA file Riassunto Fitness (FT8, Tabella 1) per ulteriori analisi, ad esempio, il calcolo dei punteggi di interazione FT9 genetiche (Tabella 1).
7. Risultati rappresentativi
La figura 2 mostra una curva tipica crescita di colture 384 QFA crescita a 20 ° C su agar solido come quantificata Colonyzer, con aumento della densità delle cellule prima diventando rilevabile dopo circa 2 giorni. Questo ritardo è probabilmente un effetto combinato di una fase di coltura ritardo dopo l'inoculazione su un supporto solido e un limite inferiore di rilevamento per densità cellulare. 308 La Figura 3 mostra le curve di crescita simili catturate da una singola piastra. Figura 4 mostra il confronto di due genoma schermi QFA per inferire geneticapunti di forza di interazione (adattato da 1). Il pacchetto R QFA 7 include anche funzioni per la produzione di figura 3 e per l'output graduatorie dei genotipi esaminati e stime di forza di interazione genetica (GIS), insieme ad un valore di q (Tasso False Discovery (FDR) corretta p-value) per la significato di GIS osservato.

Figura 1. Schema di inoculo robotica di ceppi di lievito in 384-spot in formato. Questa procedura inizia con 1536 culture indipendenti per piastra (a sinistra). In questo esempio tipico, colonie nelle posizioni 1,1, 1,2, 2,1 e 2,2 (colore rosso) sono quattro repliche dello stesso genotipo HIS3 :: culture KANMX in giallo, sempre sul bordo della piastra. , hanno un vantaggio di crescita a causa della mancanza di concorrenza e non sono quindi esaminati da QFA. Uno di questi replicati (ad esempio 1,1) viene inoculato in terreno di coltura liquido in piastra a 96 pozzetti s utilizzando un 96-pin strumento che inocula 96 di 1536 colonie ogni volta. Per inoculare un replicato per ciascuno dei 384 delezioni geniche, quattro diversi quadranti "" (indicata come rosso, blu, verde e viola) vengono inoculate in quattro diverse piastre da 96 pozzetti contenenti mezzo di crescita. Dopo una crescita a saturazione (ad esempio 3 giorni a 20 ° C), le colture sono diluite in acqua, poi i quattro quadranti da una ripetizione sono macchiati nel 384 formato su una piastra di agar solido (a destra) lo stesso modello come la targa originale SGA (come indicato dal colore). Il processo può essere ripetuto per verificare altri repliche: 1,2, 2,1 e 2,2. Esempio time-lapse immagini a destra sono stati catturati 0,5, 2 e 3,5 giorni dopo l'inoculazione. Adattato dalla figura complementare 1 2. Clicca qui per ingrandire la figura .
018/4018fig2.jpg "/>
Figura 2. Un singolo robot-catturato QFA curva di crescita. A) QFA curva di crescita di un ceppo di lievito cresce su agar contenente galattosio a 20 ° C. Le immagini sono state catturate roboticamente circa ogni 2 ore. Fase esponenziale a questa temperatura è osservabile per circa 1,5 giorni, con aumento della densità di cultura prima di diventare rilevabile circa 2 giorni dopo l'inoculazione. Un modello generalizzato logistico era adatto ai dati osservati (curva grigia). Parametri del modello automaticamente installati dal pacchetto QFA R sono presentati: K (capacità di carico (AU)), r (tasso di crescita (d -1)), g (densità di inoculo (AU)), v (simmetria crescita). B) Per quanto riguarda pannello A, tracciata con la densità cellulare su una scala logaritmica. Clicca qui per ingrandire la figura .
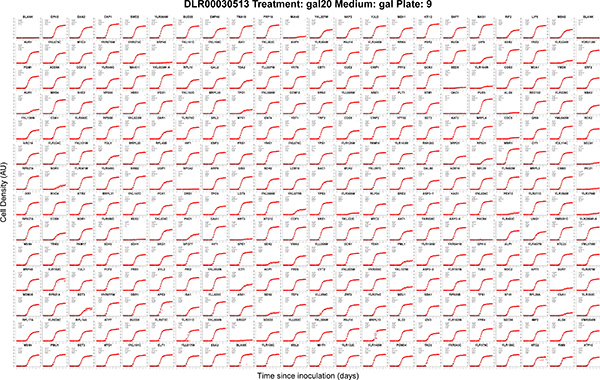
Figura 3. Automaticamente gene curve di crescita nominale catturato in parallelo da una singola a 384 in formato piatto. Ogni pannello mostra le stime di densità delle cellule (croci rosse) e fit modello (curve nere) per le culture indipendenti etichettati in base al nome o gene ORF y numero cresciuto in una procedura QFA. Questa piastra esempio è stato fotografato dal robot e coltivate in un incubatore automatizzato a 20 ° C. Metadati sperimentale vengono automaticamente inclusi nel titolo figura: targa, trattamento lamiera, terreno di agar e la targa biblioteca. Componibili valori dei parametri del modello vengono inoltre automaticamente stampato su ciascun pannello (vedi figura 2). Culture di Edge sono stati spogliati dalle analisi QFA, lasciando i 308 culture in questo grafico (vedi QFA Protocol 5.4). Poiché colture bordo non vengono analizzati in QFA, queste posizioni di coltura sono tipicamente riempiti con ceppi di controllo neutro (pGAL-HIS3 in questo caso). La versione originale di questa figura, in uscita dal pacchetto QFA R, è in. Formato pdf ed è quindi infinitamente stradale e ricercabili da query di testo.:/ / Www.jove.com/files/ftp_upload/4018/4018fig3.pdf "target =" _blank "> Clicca qui per ingrandire la figura.

Figura 4. Confrontando convenienze da due schermi QFA per dedurre l'interazione genetica. Questo grafico mostra il confronto del fitness di delezioni di lievito in erba (yfgΔ) in combinazione con la mutazione neutra ura3Δ o sensibile alla temperatura CDC13-1 mutazione e cresciuto al semi-permissivo temperatura per CDC13- 1 (27 ° C). Fitness è stato calcolato come il prodotto della frequenza massima e raddoppio raddoppio massimo potenziale 1. Maggior parte dei ceppi di delezione crescono bene quando combinato con la mutazione neutro ura3Δ, come previsto e hanno idoneità elevata, ma delezioni combinati con CDC13-1 hanno una vasta gamma di convenienze. Le linee di luce blu si incrociano a maggioposizione e della mutazione neutra his3Δ, la linea continua è un modello di regressione lineare di indipendenza genetica (fitness atteso CDC13-1 yfgΔ mutanti dato fitness ura3Δ yfgΔ mutanti) e la linea tratteggiata è la linea di parità di forma fisica. Le eliminazioni di colore verde di migliorare notevolmente il difetto fitness CDC13-1 ceppi. Le eliminazioni di colore rosso in modo significativo sopprimere lo stesso difetto. Distanza verticale di qualsiasi mutazione CDC13-1 yfgΔ dalla linea continua indica la forza di interazione tra genetica CDC13-1 e yfgΔ alle condizioni piastra. Si noti che alcuni dei più forti soppressori di CDC13-1 sono preventivamente individuati geni checkpoint, RAD17, DDC1 e RAD24 e la nucleasi EXO1 nella parte superiore destra. Geni la cui cancellazione riduce il fitness comprendono YKU80 (che codifica per la riparazione del DNA e dei telomeri capping proteine Yku80) nei pressi della in basso a destra. Si noti inoltre che alcuni gruppi di geni che funzionano insieme tendono ad essere collocati su questo terreno. Tre gruppi di esempio sono evidenziate in blu SPE1, SPE2 e SPE3: geni di sintesi spermidina, RAD17 DDC1 e RAD24: componenti di codifica del morsetto checkpoint di scorrimento e fissaggio loader checkpoint, Mre11, RAD50 e XRS2: il complesso MRX, coinvolti in DDR e EST1 e EST3: geni coinvolti nella regolazione della lunghezza dei telomeri. Adattato da 1B supplementare figura 1, i dati grezzi da cui è stato generato questo terreno può essere scaricato da qui: http://research.ncl.ac.uk/colonyzer/AddinallQFA/ . Clicca qui per ingrandire la figura .
Tabella 1. Elettronici Files QFA. Tutti i file elencati (ad eccezione FT1) sono delimitati da tabulazioni file di testo e può essere costruito o leggere utilizzando qualsiasi editor di testo o fogli di calcolo. Per ulteriori dettagli sulla costruzione di file di metadati QFA e interpretazione precisa della produzione QFA vedere il pacchetto di documentazione QFA R 7 e la documentazione del software Colonyzer 3.
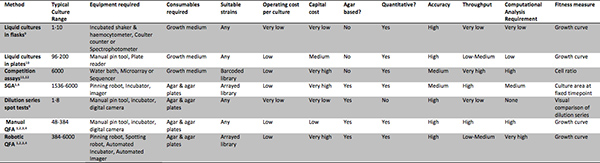
Tabella 2. Metodi per valutare l'idoneità della cultura. Una sintesi delle caratteristiche e richiedonomenti di un certo numero di metodi per valutare l'idoneità microbica cultura. Una revisione da Blomberg 8 contiene confronto più dettagliato di alcune di queste. Clicca qui per ingrandire la figura .
Discussione
QFA è in molti sensi una diretta discendente di tre stabiliti banco scala tecniche microbiologiche: la cultura del test di diluizione in loco della serie 9, la determinazione della curva di crescita in colture liquide gassose 9 e placcatura replica 13. Questi tre metodi sono riassunte e confrontati con QFA ed altre tecniche ad alta produttività in Tabella 2. Considerando che la diluizione, saggi punti in serie di definire un ceppo di idoneità come la sua capacità di formare colonie in una serie di colture derivate da una serie di diluizioni di inoculo, QFA fitness ceppo misure con osservazioni ripetute di una singola cultura per costruire una curva di crescita. Quantificare il fitness da singole culture permette di molti ceppi di più per essere esaminate simultaneamente, in condizioni identiche. Replica di array di culture permette ripetute prove su collezioni estensimetri, più utile quando si verifica per le differenze culturali di fitness in ambienti diversi o sfondi genetici. Il protocollo QFA presentatoqui usa costose attrezzature robotiche di replicare, inoculare, incubare le piastre di agar e di immagini, adatto per osservare la crescita di migliaia di culture indipendenti (robotica QFA, Tabella 2). Tuttavia, poiché QFA si basa su consolidati, tradizionali tecniche di laboratorio, può anche essere effettuata molto più basso sostituendo assistenza robot con operazioni manuali (manuale QFA, Tabella 2). Manuale QFA coinvolge la replicazione e inoculo delle colture su piastre di agar con uno strumento manuale pin e il trasferimento manuale dei piatti da e per un incubatore per la fotografia. Lo stesso flusso di analisi computazionale può essere applicata per generare curve di crescita di entrambi disegno sperimentale.
QFA stime fitness sembrano essere relativamente preciso. In figura 4, le convenienze medi di quattro gruppi di esempio funzionalmente delezioni di geni correlati sono evidenziati. La vicinanza dei membri di ciascuna classe funzionale gene correlato in due indisfondi ent genetiche ura3Δ e CDC13-1) indica la riproducibilità dei QFA stime fitness. Ad esempio, solo 3 delezioni geniche (su un massimo di 4.300) separare i tre membri del complesso MRX conservato.
Throughput elevato alternative QFA per testare le caratteristiche di crescita di ceppi microbici includono SGA 5,6, schermi concorrenza librerie a barre 11,12 e schermi cattura cinetica densità ottica in lettori di piastre spettrofotometrici 10 che sono riassunti nella Tabella 2 e descritto più dettagliatamente altrove 8 . QFA e piastre SGA, in cui le culture crescono su superfici solide (agar agar metodi basati, Tabella 2) possono essere gestite in modo rapido e facilmente robot. Solid culture superficie dell'agar sono ben aerati in tutta la crescita e le cellule possono crescere in colture fisse, consentendo microbi socievoli di crescere in una comunità 14. Lasciato intatto, una comunità microbicheffect proprie micro-ambienti, tossine secernono come etanolo, ed eventualmente di segnalazione tra cellule. Tuttavia, continua mescolanza di culture liquidi, necessari per raggiungere una adeguata aerazione, artificialmente sconvolge le comunità microbiche e le loro micro-ambienti che possano pregiudicare il loro modalità di crescita. Cross-contaminazione è meno di una preoccupazione nei metodi di agar solido poiché non vi è meno possibilità di schizzi di liquidi tra le cellule che trasportano le culture. Se la contaminazione avviene per stranieri aerodispersi microbi nei saggi agar solido, spesso può essere rilevata mediante ispezione visiva delle piastre di agar solido e contabilizzati o rimosso.
Velocità QFA è significativamente superiore a quello dei metodi parallele liquido in due modi. Prima di tutto, e il QFA (SGA), piatti, colture inoculate sono imballate insieme più densamente, dando culture più indipendenti per piastra. In QFA ci sono culture in genere 308, senza contare le culture non-sperimentali bordo (Figura 1) COMconfrontato in parallelo colture liquide con 96 o 100 culture per piastra. In secondo luogo, gli esperimenti QFA può essere scalata a un numero maggiore di piastre. Considerando che il numero di piastre analizzati in un singolo esperimento QFA è limitato soltanto dallo spazio disponibile in una stanza incubatore o calda, la frequenza minima consentita l'acquisizione di immagini e la frequenza massima di acquisizione ottenibile, il numero di piastre in un esperimento crescita liquido è fortemente limitata dalla capacità del lettore di piastre (tipicamente uno o due piastre), o del raccoglitore collegato al lettore di piastre (normalmente 25-50 piastre). Abbiamo recentemente effettuato un esperimento completamente automatizzato QFA su 123 piastre, ciascuna con 308 culture sperimentali, dando 37,884 culture contemporanee. Stimiamo che il numero massimo raggiungibile di culture indipendenti che crescono in liquido è 96 (culture / piastra) x 50 (piastre / raccoglitore) = 4800, che è di circa dieci volte inferiore rispetto alla nostra velocità QFA. Un'alternativa per schermi coltura liquidi è quello di utilizzare molti gro automatizzatowth dispositivi in parallelo (tabella 1 dal recensione di Blomberg 8), ciascuno avente una capacità di una o due piastre. Il controllo della temperatura in ogni dispositivo è indipendente, e quindi le condizioni non sono identici, ma assumendo che siano, questo flusso di lavoro richiederebbe almeno 190 di tali dispositivi in modo che corrisponda il throughput QFA (assumendo 200 colture liquide per dispositivo).
In sintesi, QFA è un flusso di lavoro di alta qualità che può essere utilmente applicato per raccogliere fenotipi crescita quantitativa sia in piccoli esperimenti su scala mirati e high-throughput schermi. E 'sufficientemente flessibile per essere applicato efficacemente con diversi requisiti per le apparecchiature robotica. La componente di calcolo del flusso di lavoro si basa su QFA liberamente disponibile, il codice open source.
Divulgazioni
Non ci sono conflitti di interesse dichiarati.
Riconoscimenti
Ringraziamo tutti i membri del nostro laboratorio e del Centro per la Biologia Sistema Integrato di Invecchiamento e Nutrizione (CISBAN) per il supporto e le discussioni utili. Questo studio è stato supportato da biotecnologia e Biological Sciences Research Council (BBSRC) (BB/C008200/1) e il Wellcome Trust (075.294, 093.088).
Materiali
| Name | Company | Catalog Number | Comments |
| Nome del reagente / attrezzature | Azienda | Numero di catalogo | Comments |
| Replica Plater | Sigma | R-2508 | 96 pin manuale pintool con 1/8 pin diametro " |
| Mescolare Mate | Eppendorf | 5353 000.014 | |
| Biomek FX | Beckman | A31842 | |
| Teleshake | Thermo Scientific | 50095890 | Installato su Biomek FX |
| BM3-SC | S & P Robotics Inc | BM3-SC | 192 ripiano giostra rotante |
| spImager | S & P Robotics Inc | spImager | Manuale di imaging ad alta risoluzione |
| spImager con Cytoma | S & P Robotics Inc | Costume | Temperatura controllata automatizzato di imaging ad alta risoluzione |
| Cytomat 6001 con scambiatore di calore | Thermo Scientific | 51022222 | Collegato al spImager |
| Ecoline RE207 | Lauda | RE207 | Collegato al Cytomat |
| spImager con il carosello | S & P Robotics Inc | Costume | Automated imaging ad alta risoluzione |
| Robot strumento dispositivo pin per FP12pins | V & P Scientific | AFIX96FP12 | N / A |
| 96 x FP12 pin | V & P Scientific | FP12 | 50,4 mm di lunghezza, 17 mm di lunghezza esposto pin |
| Docking Station per lo strumento di Pin | V & P Scientific | VP425 | Base docking station rimosso per consentire l'essiccazione fan dei perni |
| Pin Spazzola di pulizia | V & P Scientific | VP425 | N / A |
| Replica Plater | Sigma | R-2508 | Pin utensile manuale |
| Nunc OmniTray con coperchio | Nunc | 734-0490 | N / A |
| 96 piastre di polistirene e sterili | Greiner BioOne | 655161 | N / A |
| 96 coperchi in polistirene e sterili | Greiner BioOne | 656171 | N / A |
Tabella 3. Reagenti e attrezzature specifiche.
Riferimenti
- Addinall, S. G., Holstein, E., Lawless, C., Yu, M., Chapman, K., et al. Quantitative Fitness Analysis shows that NMD proteins and many other protein complexes suppress or enhance distinct telomere cap defects. PLoS Genetics. 7 (4), e1001362 (2011).
- Addinall, S. G., Downey, M., Yu, M., Zubko, M. K., Dewar, J., et al. A genomewide suppressor and enhancer analysis of cdc13-1 reveals varied cellular processes influencing telomere capping in Saccharomyces cerevisiae. Genetics. 180, 2251-2266 (2008).
- Lawless, C., Wilkinson, D., Young, A., Addinall, S., Lydall, D. Colonyzer: automated quantification of micro-organism growth characteristics on solid agar. BMC Bioinformatics. 11, 287-28 (2010).
- Tong, A. H., Evangelista, M., Parsons, A. B., Xu, H., Bader, G. D., et al. Systematic genetic analysis with ordered arrays of yeast deletion mutants. Science. 294, 2364-2368 (2001).
- Costanzo, M., Baryshnikova, A., Bellay, J., Kim, Y., Spear, E. D., et al. The genetic landscape of a cell. Science. 327, 425-431 (2010).
- Blomberg, A. Measuring growth rate in high-throughput growth phenotyping. Curr. Opin. Biotechnol. 22 (1), 94-102 (2011).
- Maringele, L., Lydall, D. EXO1-dependent single-stranded DNA at telomeres activates subsets of DNA damage and spindle checkpoint pathways in budding yeast yku70Δmutants. Genes and Dev. 16 (15), 1919-1933 (2002).
- Warringer, J., Blomberg, A. Automated screening in environmental arrays allows analysis of quantitative phenotypic profiles in Saccharomyces cerevisiae. Yeast. 20, 53-67 (2003).
- Hillenmeyer, M., Fung, E., Wildenhain, J., Pierce, S., Hoon, S., Lee, W., Proctor, M., St. Onge, R., Tyers, M., Koller, D., Altman, R., Davis, R., Nislow, C., Giaever, G. The chemical genomic portrait of yeast: uncovering a phenotype for all genes. Science. 320 (5874), 362-365 (2008).
- Smith, A. M., Durbic, T., Oh, J., Urbanus, M., Proctor, M., Heisler, L. E., Giaever, G., Nislow, C. Competitive Genomic Screens of Barcoded Yeast Libraries. J. Vis. Exp. (54), e2864 (2011).
- Lederberg, J., Lederberg, E. M. Replica plating and indirect selection of bacterial mutants. J. Bacteriol. 63, 399-406 (1952).
- Queller, C. Behavioural ecology: The social side of wild yeast. Nature. 456, 589-590 (2008).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon