Method Article
Количественный анализ рабочих процессов Фитнес
* Эти авторы внесли равный вклад
В этой статье
Резюме
Количественный анализ Фитнес (КФД) является дополнительной серии экспериментальных и расчетных методов для оценки приспособленности микробной культуры. КФД оценивает влияние генетических мутаций, наркотиков или других прикладных процедур на микроб роста. Эксперименты масштабирование от целенаправленного анализа одной культуры до тысячи параллельных культур могут быть разработаны.
Аннотация
Quantitative Fitness Analysis (QFA) is an experimental and computational workflow for comparing fitnesses of microbial cultures grown in parallel1,2,3,4. QFA can be applied to focused observations of single cultures but is most useful for genome-wide genetic interaction or drug screens investigating up to thousands of independent cultures. The central experimental method is the inoculation of independent, dilute liquid microbial cultures onto solid agar plates which are incubated and regularly photographed. Photographs from each time-point are analyzed, producing quantitative cell density estimates, which are used to construct growth curves, allowing quantitative fitness measures to be derived. Culture fitnesses can be compared to quantify and rank genetic interaction strengths or drug sensitivities. The effect on culture fitness of any treatments added into substrate agar (e.g. small molecules, antibiotics or nutrients) or applied to plates externally (e.g. UV irradiation, temperature) can be quantified by QFA.
The QFA workflow produces growth rate estimates analogous to those obtained by spectrophotometric measurement of parallel liquid cultures in 96-well or 200-well plate readers. Importantly, QFA has significantly higher throughput compared with such methods. QFA cultures grow on a solid agar surface and are therefore well aerated during growth without the need for stirring or shaking.
QFA throughput is not as high as that of some Synthetic Genetic Array (SGA) screening methods5,6. However, since QFA cultures are heavily diluted before being inoculated onto agar, QFA can capture more complete growth curves, including exponential and saturation phases3. For example, growth curve observations allow culture doubling times to be estimated directly with high precision, as discussed previously1.
Here we present a specific QFA protocol applied to thousands of S. cerevisiae cultures which are automatically handled by robots during inoculation, incubation and imaging. Any of these automated steps can be replaced by an equivalent, manual procedure, with an associated reduction in throughput, and we also present a lower throughput manual protocol. The same QFA software tools can be applied to images captured in either workflow.
We have extensive experience applying QFA to cultures of the budding yeast S. cerevisiae but we expect that QFA will prove equally useful for examining cultures of the fission yeast S. pombe and bacterial cultures.
протокол
Руководство КФД протокола (для штаммов S. CEREVISIAE)
1. Штаммы культивирования дрожжей
- До 96 независимых штаммов дрожжей культивируют в 200 мкл богатых жидких сред в 96-и культуре блюдо. Штаммы выращиваются на насыщение контролем температуры инкубатора.
- 96 контактный, 1/8 "Диаметр руководства реплики посева (SIGMA R-2508) стерилизуют первым погружением реплики посева на 100% этанола, пламенный, а затем оставить для охлаждения.
- 200 мкл стерильной воды одетые в 96-и культуру пластину. Насыщенный культуры встряхивали (Eppendorf MixMate, 30 сек, 750 оборотов в минуту) и разбавляют путем погружения стерилизованных инструментов булавку в насыщенном штаммов в три раза, то в пластины, содержащей воду один раз.
- Вывод инструмент повторно стерилизовать как в 1.2.
- Стерилизованного инструмента вывод использоваться для определения разбавленных культуры на проданы пластины агара путем погружения в пластины, содержащей разбавленную культуру в три разап. передачи контактный инструмент для прямоугольных пластин твердого агара.
- Прямоугольной плашки агар инкубируют при соответствующей температуре, прежде чем отображаемого вручную с помощью S & P Robotics spImager. Альтернативные методы захвата изображения могут быть также использованы такие как FujiFilm LAS4000 или менее дорогих цифровых зеркальных камер, если приняты меры для обеспечения равномерного освещения и последовательное позиционирование пластины по сравнению с изображениями камеры.
- Метод адаптируется к меньшим числом параллельных культур, таких как 48, которые могут быть установлены на круглой чашки Петри, если приняты меры, чтобы обеспечить такой же угол относительно изображения камеры при каждой фотографии.
Полностью автоматизированная КФД протокола (для штаммов S. CEREVISIAE)
2. Штаммы культивирования дрожжей
- Начните с прямоугольный массив независимых штаммов дрожжей, растущие на твердом агаре. В этом примере, начиная штаммы являются результатом пересечения температурычувствительным мутации запрос коллекции дрожжей удалений (YDC) на синтетическое Генетические Array (SGA). Окончательный SGA пластины в 1536 году формат. Это 16 строк на 24 столбцов колоний / культур, представляющих четыре повторяет из 384 независимых штаммов дрожжей. См. Рисунок 1 пластина макетов.
- 384 штаммов из 1536 переданы робототехники использования S & P Robotics Inc BM3-SC робота с 96-контактный, 1 мм, диаметр оправки стерильной pintool на четыре 96-луночного культуры пластины, содержащие 200 мкл селективной среде (рис. 1). Pintool чистота и стерильность достигается путем последовательной промывкой в стерильной воде в два раза (один раз с вращающейся щеткой, чтобы удалить остатки), 70% этанола (с ультразвуком) и, наконец, 100% этанола.
- Культуры выращиваются на насыщение (в течение трех дней при температуре 20 ° C в этом примере, см. Рисунок 1).
3. Зрительные дрожжевых культур
- Использование Beckman Biomek FX, насыщенной культурповторно ресуспендируют по встряхивая на Teleshake Variomag (против часовой стрелки на 1000rpm в течение 20 секунд) и разбавляют примерно 1:70, закрепив в 200 мкл стерильной воды с помощью стерильного 96 контактный робота инструмент контактный (V & P Научные магнитном основании pintool, 2 мм диаметр оправки). Pin чистоты и стерильности инструмента достигается промывкой в стерильной воде, стиральная в 70% этанола (с щеткой для удаления мусора) и, наконец, погружение в 70% этанола с последующей сушкой.
- Разводненная культуры заметили на твердых пластинах агара в 384 формате, используя тот же инструмент робота-контактный (см. Рисунок 1) после очистки и стерилизации.
- После фиксации, пластины передается Cytomat с контролируемой температурой, увлажненный инкубатор с автоматической карусели и входной люк.
4. Image Capture
- S & P Robotics автоматизированных изображений неоднократно снимает плиты из Cytomat инкубатор, снимает пластинку крышкой, ставят их именно под заключитег, равномерно освещенное пространство под Canon EOS Rebel Ti 35 DSLR, захватывает изображение 5184 х 3456 пикселей резолюции, заменяет пластину крышки, и возвращает их в инкубатор карусели. Один снимок сделан сразу после первоначальной передачи в инкубатор, чтобы обеспечить нулевой момент времени рост измерения (фон). Обработка робота и фотографии занимает 2 минуты в тарелке.
- При полной загрузке карусели, максимально достижимая пластины изображений частотой один снимок каждые шесть часов. Пластины инкубируют в течение шести дней (до колонии насыщение роста. На рисунке 1 показаны три типичных изображений с временной ход при температуре 20 ° C.
- Для целей учета и контроля пластин названы в соответствии с инкубатор имя, температуры, индивидуальный порядковый номер партии и положении в инкубаторе. Изображение имена объединения табличку и метку времени и автоматически построена на захват изображения (например, K000011_030_010_2011-09-22_09-47-54.jpg, тип файла FT1, таблица 1).
5. Захват экспериментальной метаданными
Метаданные файлов, описанных в данном разделе, разделенных табуляцией текстовые файлы, которые созданы вручную (например, с использованием электронных таблиц). Экспериментальные файл Описание (FT2, таблица 1) является уникальным для каждого эксперимента, но библиотека Описание (FT3, таблица 1) можно использовать повторно после создания широко.
- Эксперимент описан в экспериментальной файл Описание (FT2, табл.1), содержащие столбцы для штрих-кодов (или автоматически генерируются табличке), эксперимент, начиная метки, плиты лечение, содержание твердой среде агара, псевдоним, библиотека, номерного знака (для библиотек несколько пластин) и повторить номер квадранта (см. рисунок 1), сворачивают с 1536 до 384 формат формат.
- Библиотека штамм дрожжей описывается файл библиотеки Описание (FT3, Table1) о том, генотип, выращенного в культуре каждого места в каждой пластине библиотеки. Он содержит столбцы: имя библиотеки, ORF, номерной знак, плиты строка, столбец пластины и дополнительный столбец примечаний.
- Дополнительный стандартный файл Имя Гена (Т4, таблица 1), описывающий стандартное имя гена (например, RAD9), связанные друг с систематическим ORF у-номер (например, YDR217C) выявление штаммов проходит проверку могут быть предоставлены. Этот файл содержит две колонки: ORF и Гена имя.
6. Анализ данных
КФД вычислительных рабочих требуется доступ к достаточно мощный многоядерный компьютер рабочей станции (например, Dell Precision T3500 с Xeon четырехъядерных процессоров 2,67 ГГц процессор и 12 Гб оперативной памяти), на котором установлен анализа Colonyzer образ программного 3,4 и пакет КФД R 7 , оба из которых описаны в Интернете, находятся в свободном доступе и работает на различных операционных систем.
- Запуск Colonyzer с каждым из захваченных изображений пластины в качестве входных данных, генерироваться Colonyzer выходного файла (FT5 табл. 1) для каждого изображения в плен. Выходные файлы Colonyzer указать культуры оценки плотности, области культуры, форма и цвет для каждого из 384 мест на отображаемой пластины. Выходной файл будет автоматически скопирована из файла исходного изображения (например, плита фотографии K000011_030_010_2011-09-22_09-47-54.jpg (FT1, таблица 1) соответствует файл Colonyzer выход K000011_030_010_2011-09-22_09-47-54.dat ( FT5, таблица 1)).
- Использование пакета КФД R, загрузить экспериментальные метаданных (FT2, табл.1) и Colonyzer выходных файлов (FT5 табл. 1). Эти данные будут объединены в R кадров данных (которые могут быть экспортированы в текстовый КФД сырье файлы данных (FT6, таблица 1)) для последующего анализа.
- Пакет КФД R содержит функции для сбора timecourses плотности клеток для каждой культуры, чтобы соответствовать вот обобщенныхgistic модели населения наблюдений и сюжет как (см. рис 2 и 3 для примера). Встроенная значения параметров записываются в файлы КФД логистических параметров (FT7 табл. 1). Смотрите КФД R пакет документации для получения дополнительной информации.
- Пакет КФД R также содержит функции для контроля качества: край колонии удаляются за счет большей доступности питательных веществ на плите края и трудности с анализа изображений у стены пластины, культуры, которая не SGA и генотипов отображения связей с экрана конкретных генов-маркеров удаляются из анализа.
- Некоторые количественные показатели фитнес выводятся из логистических населения параметров модели для каждой культуры. Они включают максимальную населения удвоение ставки (MDR) и число делений от прививки к насыщению (MDP). Для каждого набора повторных культур (уникальных генотипов, например) и для каждого определения пригодности, несколько сводная статистика фитнес оценки Compраспределенных: среднее и среднее фитнес, фитнес-стандартное отклонение и количество дубликатов наблюдалось. Сводные статистические данные выводятся на КФД Фитнес Основная файлов (FT8, таблица 1) для дальнейшего анализа, например, расчет генетического оценки взаимодействия (FT9 табл. 1).
7. Представитель Результаты
На рисунке 2 показана одна типичная кривая роста из 384 культур КФД растущий при 20 ° С на твердом агаре как количественно Colonyzer, с увеличением плотности клеток став сначала обнаружить после примерно 2 дня. Эта задержка, скорее всего, комбинированный эффект фазы культуры отставание после прививки на твердой среде и нижний предел обнаружения плотности клеток. На рисунке 3 показано 308 подобных кривых роста захваченных из одной пластины. Рисунок 4 показывает сравнение двух генома КФД экранов вывести генетическуюВзаимодействие сильных (адаптировано из 1). КФД R пакет 7 также включает в себя функции для получения 3 и вывести рейтинг из списка рассматриваются генотипов и оценки генетической силы взаимодействия (ГИС), вместе с д-значение (False Discovery Rate (FDR) исправлены р-значения) для значение наблюдаемых ГИС.

Рисунок 1. Схема робота прививки штаммов дрожжей в 384 местах формате. Эта процедура начинается с 1536 независимой культуры в пластине (слева). В этом типичном примере колонии в положении 1,1, 1,2, 2,1 и 2,2 (красного цвета) четыре повторов того же генотипа HIS3 :: KANMX культур в желтом, растущих на краю тарелки. , имеют преимущество роста из-за отсутствия конкуренции и поэтому не рассматриваются КФД. Одна из них повторяет (например, 1,1) засевают в жидких средах рост в 96-луночного планшета с помощью 96-контактный инструмент, который прививает 96 из 1536 колоний каждый раз. Для того, чтобы привить один репликации для каждого из 384 генов удаления, четыре различных "квадранта" (обозначается как красный, синий, зеленый и фиолетовый) засевают на четыре 96-луночных содержащие питательные среды. После роста к насыщению (например, 3-х дней при температуре 20 ° C), культуру разводят в воде, затем четыре квадранта от одного повтора были замечены в 384-формате на твердую пластину агара (справа) в той же схеме, что и исходная пластина SGA (как указано на цвет). Этот процесс можно повторить, чтобы проверить другие повторяет: 1,2; 2,1 и 2,2. Пример покадровой изображения справа были захвачены 0,5, 2 и 3,5 дня после прививки. По материалам дополнительный рисунок 1 2. Нажмите здесь, чтобы увеличить рисунок .
018/4018fig2.jpg "/>
Рисунок 2. Один робот захватили КФД кривой роста.) КФД кривая роста дрожжей, растущих на агар, содержащий галактозу при 20 ° C. Изображения были захвачены робототехники примерно каждые 2 часа. Экспоненциальная фаза при этой температуре наблюдается примерно 1,5 дня, с увеличением плотности культуры став сначала обнаруживается примерно через 2 дня после прививки. Обобщенной логистической модели подходят к наблюдаемым данным (серая кривая). Параметры модели автоматически устанавливается в пакете КФД R представлены: K (пропускная способность (АС)), т (темп роста (г -1)), г (посевной плотности (АС)), V (рост симметрия). Б) Что касается панели, построенные с плотность клеток на логарифмической шкале. Нажмите здесь, чтобы увеличить рисунок .
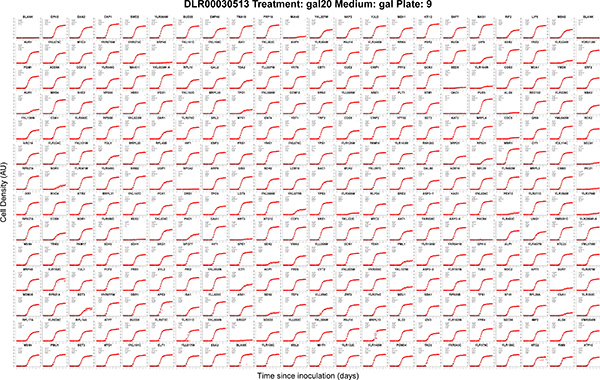
Рисунок 3. Автоматически ген рейтингу кривые роста захватили параллельно с одной 384-формат пластин. Каждая панель показывает плотность клеток оценки (красный крест) и модель подходит (черная кривая) для независимых культур помечены имя ген или ORF у-число выросло в порядке КФД. Этот пример пластины изображено робота и вырос в автоматическом инкубаторе при температуре 20 ° C. Экспериментальные метаданных, автоматически включаются в показатель название: таблички, плиты лечения, агар и количество библиотек пластины. Встроенная значений параметров модели и автоматически печатается на каждой панели (см. Рисунок 2). Пограничный культуры были вырезаны из анализа КФД, в результате чего 308 культур в этом участке (см. КФД протокола 5.4). С краю культуры не анализируются в КФД этих местах культуры, как правило, заполнены с нейтральным штаммов контроля (pGAL-HIS3 в данном случае). Оригинальная версия этой фигуры, выход из пакета КФД R, в. PDF формате, и поэтому бесконечно масштабируемые и поиска по тексту запроса.:/ / Www.jove.com/files/ftp_upload/4018/4018fig3.pdf "целевых =" _blank "> Нажмите здесь, чтобы увеличить цифру.

Рисунок 4. Сравнение приспособленности с двумя экранами КФД вывести генетических взаимодействий. Этот график показывает сравнение фитнес бутонизации удаление дрожжей (yfgΔ) в сочетании с нейтральной мутации ura3Δ или чувствительных к температуре cdc13-1 мутации и выросло на полу-разрешительной температура cdc13- 1 (27 ° C). Фитнес был рассчитан как произведение максимальной скорости удвоения и максимальный потенциал удвоения 1. Большинство штаммов удаление хорошо растут в сочетании с нейтральной мутации ura3Δ, как и ожидалось, имеют высокую пригодность, но удаление в сочетании с cdc13-1 имеют широкий диапазон приспособленности. Голубой линии пересекаются в гоэлектронной расположение нейтральных мутаций his3Δ, сплошная линия является линейной регрессионной модели генетической независимости (ожидается пригодности cdc13-1 yfgΔ мутантов данного пригодности ura3Δ yfgΔ мутанты) и пунктирная линия является линией равных фитнеса. Удаления зеленого цвета значительно повысить фитнес дефект cdc13-1 штаммов. Удаления красного цвета существенно подавить тот же дефект. Расстояние по вертикали от любой мутации cdc13-1 yfgΔ из сплошной линией указывает на силу взаимодействия между генетическими cdc13-1 и yfgΔ под пластиной условиях. Заметим, что некоторые из самых сильных супрессоров cdc13-1, ранее идентифицированных генов контрольно-пропускной пункт, RAD17, DDC1 и RAD24 и нуклеазы EXO1 в верхнем правом углу. Генов, удаление снижает фитнес включает YKU80 (кодирование репарации ДНК и белков теломер укупорки Yku80) вблизи правом нижнем углу. Также обратите внимание, что некоторые группы генов, которые работают вместе, как правило, размещаться на этом участке. Три кластера пример выделены SPE1 синий, SPE2 и SPE3: спермидина синтез генов, RAD17, RAD24 и DDC1: кодирование компонентов контрольно-пропускной пункт скольжение зажима и контрольно-пропускной пункт зажим погрузчик, MRE11, RAD50 и XRS2: комплекс MRX, участвующих в DDR и EST1 И EST3: гены, участвующие в регуляции длины теломер. По материалам дополнительный рисунок 1В 1, исходные данные, из которой этот участок был сгенерирован может быть загружен отсюда: http://research.ncl.ac.uk/colonyzer/AddinallQFA/ . Нажмите здесь, чтобы увеличить рисунок .
Таблица 1. Электронные КФД файлов. Перечислены все файлы (за исключением FT1) являются табуляции текстовых файлов и могут быть построены или прочитать с помощью любого текстового редактора или электронных таблиц. Для получения дополнительной информации о строительстве КФД файлы метаданных и точной интерпретации выходной КФД см. пакет КФД R 7 и документация документация Colonyzer программного обеспечения 3.
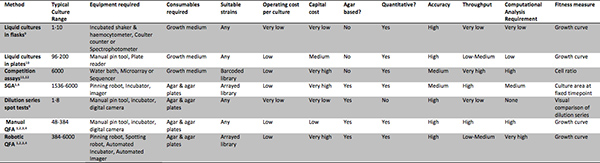
Таблица 2. Методы оценки культуры фитнеса. Обзор возможностей и требуютments ряд методов для оценки микробной фитнес-культуры. Обзор Blomberg 8 содержит более подробное сравнение некоторых из них. Нажмите здесь, чтобы увеличить рисунок .
Обсуждение
КФД является во многих отношениях прямой потомок трех установленных скамейке масштабе микробиологические методы: культура разведения серии тестов месте 9, кривая роста определения в газированных жидких культурах 9 и реплики покрытия 13. Эти три метода кратко и по сравнению с КФД и других высокопроизводительных методов в таблице 2. В то время как разведение тесты серии месте определить пригодность штамма, как его способность к образованию колоний в ряде культур, выращенных из ряда разведений посевной, КФД меры деформации фитнес на повторных наблюдений одного культуры для построения кривой роста. Количественная фитнес от одной культуры позволяет многие другие штаммы должны быть рассмотрены одновременно, в одинаковых условиях. Репликация массивов культур позволяет повторное тестирование штамма коллекций, наиболее полезным при тестировании культуры фитнес различия в различных средах или генетического происхождения. КФД протокол представленЗдесь используются дорогие роботы оборудования для репликации, прививать, инкубировать и плиты изображение агар, подходит для наблюдения роста тысяч независимых культур (робот КФД, таблица 2). Однако, поскольку КФД основана на установленных, традиционные методы лабораторию, он также может быть проведена гораздо дешевле заменить роботом с помощью ручных операций (ручной КФД, таблица 2). Руководство включает в себя КФД репликации и прививки культур на агар пластины с использованием ручного инструмента контактный и ручной передачи пластин и из инкубатора для фотографии. То же самое вычислительных рабочих анализа могут быть применены для создания кривых роста либо из эксперимента.
КФД фитнес оценки кажутся сравнительно точно. На рисунке 4, средние приспособленности четырех например кластеров функционально связанных удаления гена выделены. Непосредственной близости от членов каждого класса функционально связанных генов в двух независимыхЛОР-генетического фона (ura3Δ и cdc13-1) указывает на воспроизводимость КФД оценки пригодности. Например, только 3 гена удаления (из возможных 4300) отделяют три члена сохраняющийся комплекс MRX.
Высокая пропускная способность альтернативы КФД для проверки характеристик роста штаммов микроорганизмов включают SGA 5,6, конкуренция экраны в штрих библиотеки 11,12 и экранов захвата оптического кинетики плотности в спектрофотометрических читатели пластины 10, которые приведены в таблице 2 и более подробно описаны в другом месте 8 . КФД и SGA плит, где культуры растут на твердых поверхностях агара (агар на основе методов, таблица 2) могут быть обработаны быстро и легко робота. Твердые поверхности агара культур, хорошо газированной протяжении роста и клетки могут расти в основной культуры, что позволяет общительный микробов расти в обществе 14. Остаются нетронутыми, микробных сообществffect свой микро-среды, выделяя токсины, такие как этанол, и, возможно, сигналов между клетками. Тем не менее, непрерывного перемешивания жидких культур, необходимых для достижения адекватной аэрации, искусственно разрушает микробные сообщества и микро-среды, которые могут повлиять на их режимы роста. Кросс-загрязнение меньше беспокойства в твердом методы агар, поскольку существует меньше возможностей для проведения брызг жидкости клеток между культурами. Если заражение происходит в результате иностранной воздушно-капельным путем микробов в твердых анализов агар, его часто можно обнаружить при визуальном осмотре твердых пластин агара и приходится или удалены.
КФД пропускная способность значительно выше, чем у параллельного жидкости методами в двух направлениях. Прежде всего, по КФД (и SGA) пластин, привитых культур упакованы вместе более плотно, давая более независимой культуры в тарелку. В КФД там, как правило, 308 культур, не считая неэкспериментальных край культур (рис. 1) комсравнению с параллельным жидких культур с 96 или 100 культур в тарелку. Во-вторых, КФД эксперименты могут быть соизмеримы с гораздо большим количеством пластин. В то время как количество пластин проанализированы в одном эксперименте КФД ограничивается только места в инкубаторе или теплой комнате, минимально допустимая частота захвата изображения и максимально достижимая частота захвата, количество пластин в жидкости эксперимент рост сильно ограниченным по возможности ридер (как правило, одну или две тарелки), или укладчик прикреплены к ридер (обычно 25-50 пластин). Недавно мы провели полностью автоматизирован КФД эксперимент на 123 пластин, каждая с 308 экспериментальных культурах, давая 37884 одновременных культур. Мы считаем, что максимально достижимое количество независимых культур, растущих в жидкость 96 (культур / пластина) х 50 (плиты / укладчик) = 4800, что составляет примерно в десять раз меньше, чем наши КФД пропускной способности. Альтернатива для жидкости экранами культуры является использование многих автоматизированных Грут-го устройства параллельно (табл. 1 из обзора Blomberg 8), каждая из которых имеет емкость одной или двумя пластинами. Регулирование температуры в каждом устройстве не зависит, и поэтому условия не являются идентичными, но при условии, что они есть, это рабочий процесс потребует не менее 190 таких устройств в соответствии с КФД пропускная способность (при условии 200 жидких культур на устройство).
Таким образом, КФД является высококачественным рабочим процессом, который может быть с пользой применены для сбора количественных фенотипов роста в малых масштабах сосредоточены экспериментов и высокую пропускную способность экранов. Он достаточно гибок, чтобы эффективно применяться с различными требованиями к роботизированным оборудованием. Вычислительных компонент рабочего процесса КФД основана на свободном доступе, с открытым исходным кодом.
Раскрытие информации
Нет конфликта интересов объявлены.
Благодарности
Мы выражаем глубокую признательность всем членам нашей лаборатории и Центра по разработке системы биологии старения и питания (CISBAN) за поддержку и полезные обсуждения. Это исследование было поддержано биотехнологии и биологических наук Исследовательского Совета (СИББН) (BB/C008200/1) и Wellcome Trust (075294, 093088).
Материалы
| Name | Company | Catalog Number | Comments |
| Название реагента / оборудование | Компания | Номер по каталогу | Комментарии |
| Реплика Платер | Сигма | R-2508 | 96 контактный ручной pintool с 1/8 "Диаметр контактов |
| Смешайте Mate | Эппендорф | 5353 000.014 | |
| Biomek FX | Beckman | A31842 | |
| Teleshake | Thermo Scientific | 50095890 | Установленный на Biomek FX |
| BM3-SC | S & P Robotics Inc | BM3-SC | 192 полка вращающаяся карусель |
| spImager | S & P Robotics Inc | spImager | Высокое разрешение изображения руководства |
| spImager с Cytomв | S & P Robotics Inc | Обычай | Температура контролируется автоматизированной высоким разрешением |
| Cytomat 6001 с теплообменником | Thermo Scientific | 51022222 | В приложении к spImager |
| Эколайн RE207 | Лауда | RE207 | В приложении к Cytomat |
| spImager с карусели | S & P Robotics Inc | Обычай | Автоматизированная высоким разрешением |
| Робот контактный инструмент приспособления для FP12pins | V & P Научные | AFIX96FP12 | N / A |
| 96 х FP12 контакты | V & P Научные | FP12 | 50,4 мм, 17 мм подвергаются контактный длину |
| Док-станция для контактов инструмента | V & P Научные | VP425 | Док-станция базы удалены, чтобы вентилятор сушки контакты |
| Прикрепите очистки кистей | V & P Научные | VP425 | N / A |
| Реплика Платер | Сигма | R-2508 | Ручной инструмент контактных |
| Nunc OmniTray с крышкой | Nunc | 734-0490 | N / A |
| 96 стерильных пластин из полистирола | Greiner BioOne | 655161 | N / A |
| 96 стерильной крышкой из полистирола | Greiner BioOne | 656171 | N / A |
Таблица 3. Специальные реагенты и оборудование.
Ссылки
- Addinall, S. G., Holstein, E., Lawless, C., Yu, M., Chapman, K., et al. Quantitative Fitness Analysis shows that NMD proteins and many other protein complexes suppress or enhance distinct telomere cap defects. PLoS Genetics. 7 (4), e1001362 (2011).
- Addinall, S. G., Downey, M., Yu, M., Zubko, M. K., Dewar, J., et al. A genomewide suppressor and enhancer analysis of cdc13-1 reveals varied cellular processes influencing telomere capping in Saccharomyces cerevisiae. Genetics. 180, 2251-2266 (2008).
- Lawless, C., Wilkinson, D., Young, A., Addinall, S., Lydall, D. Colonyzer: automated quantification of micro-organism growth characteristics on solid agar. BMC Bioinformatics. 11, 287-28 (2010).
- Tong, A. H., Evangelista, M., Parsons, A. B., Xu, H., Bader, G. D., et al. Systematic genetic analysis with ordered arrays of yeast deletion mutants. Science. 294, 2364-2368 (2001).
- Costanzo, M., Baryshnikova, A., Bellay, J., Kim, Y., Spear, E. D., et al. The genetic landscape of a cell. Science. 327, 425-431 (2010).
- Blomberg, A. Measuring growth rate in high-throughput growth phenotyping. Curr. Opin. Biotechnol. 22 (1), 94-102 (2011).
- Maringele, L., Lydall, D. EXO1-dependent single-stranded DNA at telomeres activates subsets of DNA damage and spindle checkpoint pathways in budding yeast yku70Δmutants. Genes and Dev. 16 (15), 1919-1933 (2002).
- Warringer, J., Blomberg, A. Automated screening in environmental arrays allows analysis of quantitative phenotypic profiles in Saccharomyces cerevisiae. Yeast. 20, 53-67 (2003).
- Hillenmeyer, M., Fung, E., Wildenhain, J., Pierce, S., Hoon, S., Lee, W., Proctor, M., St. Onge, R., Tyers, M., Koller, D., Altman, R., Davis, R., Nislow, C., Giaever, G. The chemical genomic portrait of yeast: uncovering a phenotype for all genes. Science. 320 (5874), 362-365 (2008).
- Smith, A. M., Durbic, T., Oh, J., Urbanus, M., Proctor, M., Heisler, L. E., Giaever, G., Nislow, C. Competitive Genomic Screens of Barcoded Yeast Libraries. J. Vis. Exp. (54), e2864 (2011).
- Lederberg, J., Lederberg, E. M. Replica plating and indirect selection of bacterial mutants. J. Bacteriol. 63, 399-406 (1952).
- Queller, C. Behavioural ecology: The social side of wild yeast. Nature. 456, 589-590 (2008).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены