Method Article
アクティブポルト大静脈シャントを使用して、ブタ肝臓調達と同所移植の技術
要約
Experimental animal research plays a pivotal role in the development of clinical transplantation practice. The porcine orthotopic liver transplantation model (OLTx) closely resembles human conditions and is frequently used in clinically oriented research. The following protocol contains all information for a reliable porcine OLTx model using an active porto-caval-jugular shunt.
要約
The success of liver transplantation has resulted in a dramatic organ shortage. Each year, a considerable number of patients on the liver transplantation waiting list die without receiving an organ transplant or are delisted due to disease progression. Even after a successful transplantation, rejection and side effects of immunosuppression remain major concerns for graft survival and patient morbidity.
Experimental animal research has been essential to the success of liver transplantation and still plays a pivotal role in the development of clinical transplantation practice. In particular, the porcine orthotopic liver transplantation model (OLTx) is optimal for clinically oriented research for its close resemblance to human size, anatomy, and physiology.
Decompression of intestinal congestion during the anhepatic phase of porcine OLTx is important to guarantee reliable animal survival. The use of an active porto-caval-jugular shunt achieves excellent intestinal decompression. The system can be used for short-term as well as long-term survival experiments. The following protocol contains all technical information for a stable and reproducible liver transplantation model in pigs including post-operative animal care.
概要
同所性肝移植(OLTx)は、末期肝疾患や進行肝細胞癌患者のための唯一の治療選択肢です。過去25年の間、待機リストの候補の数は徐々に増加し、現在までのところ利用可能な移植片の数を超えています。ほとんどの移植領域では、肝移植の待機リストに患者〜20の30%が臓器移植を受けることなく死ぬかによる疾患の進行に上場を廃止しています。戦略は、このように、利用可能な移植片の数は、必死に必要とされる、ドナーのプールを増加させました。拡張基準臓器配分、長期の移植片の保存、および免疫寛容の誘導は、依然として主要な臨床課題1-3を表します。したがって、実験的OLTx調査は、臨床OLTxの練習を最適化するために極めて重要です。
ブタOLTxがlを含む多くの方法で人間OLTxに似ている十分に確立された実験モデルでありますアイバーサイズ、解剖学、生理学4-6。したがって、このような外科技術、生理学、免疫学、保存、および虚血 - 再灌流傷害などの研究分野における標準的な実験方法となりました。グラフト調達、レシピエント肝切除、及び、特に、血管再構築の多くの技術が文献5に記載されています。適切な技術の選択は、研究者の好みや技術的能力に応じて変化します。
人間のシナリオとは対照的に、肝外性の段階の間に内臓の混雑は、ブタOLTxにおける重要な問題です。その後の腸管虚血およびうっ血性血管損傷は、このように、実験7-9の成功を豚の生存を危険にさらすと、重度の血行動態不安定性を引き起こす可能性があります。そのため、十分な腸解凍が特に少ない技術的に洗練された実験的な設定では、必須です。
米国る肝外性の相の期間中、アクティブポルト大静脈 - 頚シャントは、腸の混雑を避けるために信頼性の高いオプションです。システムは、初期の再灌流実験ならびに長期生存のシナリオのために使用することができます。以下のプロトコルは、肝切除とエンドツーエンドの血管再構成技術、および術後ケアを含むドナー肝臓調達、受信者動作を含むブタの安定かつ再現性の肝移植モデル、に関するすべての情報が含まれています。
プロトコル
すべての動物は医学研究と健康、オンタリオ州、カナダの国立研究所によって公開 '' '実験動物の管理のためのガイド」のため国立協会によって定式化' ''実験動物管理の原則」に準拠して人道的なケアを受け。トロント一般研究所の動物管理委員会は、すべての研究を承認しました。
1.オルガン検索
- 移植前1週間のための研究施設では30と35キロの間にハウスの雄ヨークシャーブタ(灌流の結果10,11変更することができます)と住宅事情に動物を順応さストレス誘発物理的反応を防止することができます。前麻酔の導入に6時間の最小値のための豚を高速です。
- ケタミン(25 mgの/ kg)を、アトロピン(0.04ミリグラム/ kg)を、およびミダゾラム(0.15ミリグラム/ kg)を混合物の筋肉内(IM)注射によるドナー豚を麻酔。
- 挿管の前に、豚が自発的にイソフルランの5%を投与した酸素の2 Lを呼吸することを確認します。仰臥位では、声帯の痙攣を回避するために挿管前に2%リドカイン2分で声帯をスプレー。 35キロの豚については、6.5のFR気管チューブを使用しています。室内空気の3〜5ミリリットルで気管チューブをブロックします。
- 挿管後、正しい挿管を確認するためにカプノメトリを使用しています。豚の尾のパルス酸素濃度計によって心拍数と酸素飽和度を監視します。 2%のイソフルラン気化器を下げます。
- 最小限の肺胞内濃度(MAC)値によって麻酔の深さを調整します。 2.5 MAC - 2を目指します。 16呼吸/分および10の一回換気量 - - 15ミリリットル/ kg体重14に人工呼吸器を設定します。
- 乳酸リンゲル液(200ミリリットル/時間)の注入を可能にするために、耳静脈のいずれかで18 G静脈内(IV)カテーテルを配置します。豚をスクラブし、滅菌ドレープでそれをカバーしています。
- 無菌状態を確認した後、正中開腹folloを作ります左側拡張によって結婚。左側に移動する前に、大小の腸をカバーするためにタオルを使用してください。
- 焼灼を使用して、鎌状靱帯と三角靱帯を分割します。
- 電気メスを使用して、右側の振動板からの肝臓をリリース。静脈とダイヤフラムとの間の上部のためのはさみを使用しています。右側の副腎静脈と左サイドの腎静脈の分岐まで肝臓下の静脈を解剖。
- 互いに肝臓下静脈および遠位大動脈を分離します。脊椎に大動脈の枝を連結。付着組織から腎動脈を分離し、無料。 2-0タイで各腎動脈を囲みます。
- 左腎静脈への頭蓋、大動脈および腸間膜動脈を解剖。 2-0のタイとの腸間膜動脈を囲みます。
- 腸間膜動脈に腹膜頭蓋を開いた後、慎重に腹腔動脈に向かって大動脈に従ってください。 VEのポータルに尾側に腹腔動脈を解剖で;どの分岐後方腹腔動脈から、脾臓、左胃動脈を囲みます。門脈から腹腔動脈を解剖。
- 膵臓および門脈の間腹膜切開により門脈をリリース。門脈に膵臓から排出静脈を縛ります。
- 肝十二指腸間膜から胆管を分離し、遠位連結後、それを分割します。
- リンパ管の漏れを防止するために肝十二指腸間膜内リンパ管を結紮。ネクタイの間に胃十二指腸動脈と右胃動脈を分割します。小さい静脈を結紮。
- 心と腹腔トランク間のダイアフラムの背後にある大動脈を解剖。腹腔動脈の頭蓋大動脈の周りに2-0ネクタイを配置します。
- 胆嚢を削除し、胆嚢床からの出血を焼灼。
- 絞りを開きます。心臓内ヘパリン1,000 IU / kgのドナー体重を管理またはIV達成するために、5%(> 2.5 MAC)にイソフルランを設定より深い麻酔レベル。循環死(DCD)モデルの後のドナーについては、ヘパリン投与後40 mvalのKCl 3分の心臓内注射により心停止を誘発します。温虚血の出発点として、心停止を設定します。
- 腎臓、脾臓、腸間膜、左胃動脈の周りに予め設定された関係を縛ります。腎臓および腸骨動脈との間に遠位大動脈を縛るとオルガンフラッシュラインと大動脈にカニューレを挿入。
- として近位できるだけ門脈を縛ると別の器官フラッシュラインでそれにカニューレを挿入。
- 近位大動脈の周りに予め設定されたネクタイを閉じた後、大動脈(圧力バッグ)と門脈(重力駆動)を介して二重の灌流を用いた冷ウィスコンシン大学(UW)の溶液2Lで肝臓をフラッシュします。
- 長い残りのすべての船を残し、肝臓を切除。肝上大静脈の周りに寛大な横隔膜リムのままにしておきます。氷上で滅菌臓器袋に肝臓を置きます。
- バック表作成、CLの間にSatinskyクランプを使用して、肝上大静脈をAMPおよび門脈流出が透明になるまで逆行下部下大静脈を介して肝臓にUW液約0.5リットルで2回洗浄します。
- 大動脈および腹腔トランクのすべての動脈枝を縛ります。 UW液12の残りの0.5リットルで動脈背表圧力灌流を行います。
- UW液を用いて胆管をフラッシュします。
- まともなサイズに横隔膜パッチをトリミングします。すべて閉じて横隔静脈 - 通常3,1それぞれ左右、および1後部 - 4-0モノフィラメントポリプロピレンステッチを使用して。
- 臓器袋を閉じて、氷の上に、肝臓を格納します。
2.受信者の肝切除
- ケタミン(25 mgの/ kg)を、アトロピン(0.04ミリグラム/ kg)を、およびミダゾラム(/ kgの0.15 mg)を混合物の筋肉内注射することにより、受信者の豚を麻酔。
- 加熱マットの上に手術台に仰臥位で豚を配置します。豚のwiをカバー熱循環毛布番目。
- 挿管の前に、豚が自発的にイソフルランの5%を投与した酸素の2 Lを呼吸することを確認します。声帯のけいれんを避けるために挿管前に2%リドカイン2分で声帯をスプレーしてください。 35キロの豚については、6.5のFR気管チューブを使用しています。室内空気の3〜5ミリリットルで気管チューブをブロックします。
- 挿管後、正しい挿管を確認するためにカプノメトリを使用しています。豚の尾のパルス酸素濃度計によって心拍数と酸素飽和度を監視します。ブタの鼻の中に温度プローブを配置し、固定します。 2%( - 2.5 MAC 2を目標)にイソフルラン気化器を下げます。 16呼吸/分および10の一回換気量 - - 15ミリリットル/ kg体重14に人工呼吸器を設定します。
- 麻酔下ながら乾燥を防ぐために、目に軟膏を使用してください。
- 左外頚静脈にシース誘導因子(8.5神父)を挿入するセルジンガー法13を使用してください。アクティブポータル大静脈 - 頸静脈バイパスのために、この後、カテーテルを使用してください。
- セルジンガーtechniquを使用してくださいeは右外頸静脈への完全非経口栄養(TPN)は、カテーテル(9.5神父)を挿入します。
- 無菌条件下で、右頸動脈を切開し、侵襲的動脈圧モニタリングのためのポリプロピレンカテーテル(18 G)を挿入します。緊急連結を可能にするために2-0絹のネクタイと動脈を囲みます。
- 麻酔の深さを維持するために - (8 / kg /時間のIV 5) - (MAC 2 1.5)とプロポフォールを追加し、1%のイソフルラン気化器を下げてください。鎮痛のために、クエン酸フェンタニル(最も好ましい、2μgの/ kg /時間)またはレミフェンタニル(第二希望、15μgの/ kg /時間)の連続静脈内注入を使用しています。
- 皮膚切開前に、セフロキシムとメトロニダゾールivの500 mgの1,000 mgを得。 150ミリリットル/時で5%グルコースを乳酸リンゲル液を用いて、輸液ポンプを設定します。
- 頭頸部領域に熱循環毛布を置きます。豚をスクラブし、滅菌ドレープでそれをカバーしています。
- 無菌条件下で、正中開腹術を行います。腹部Rを挿入etractor右上腹部への十分なアクセスを取得します。
- falciforme靭帯と焼灼を使用して三角靱帯を分割します。
- 複数のステップでは、ネクタイの間に肝臓に近い肝十二指腸間膜を分割します。特定し、分割し、肝動脈と胆管の分岐をマークします。
- 胃十二指腸動脈の分割まで逆行肝動脈を解剖。ブルドッグクランプが後クランプするための胃十二指腸動脈に総肝動脈の近位の周りにフィットすることを確認してください。
- 付着組織から門脈を解放します。
- 電気メスを使用して右側の後腹膜から大静脈を動員。静脈とダイヤフラムとの間の上部のためのはさみを使用してください。右側の副腎静脈と左サイドの腎静脈の分岐まで肝臓下の静脈を解剖。
- 脾臓の門を公開します。ほぼ中間脾臓の長さに沿って、注意深く明確付着腹膜層からの脾動脈と静脈F。 4 2-0シルクネクタイと脾動脈と静脈の両方を囲みます。
- 門脈に向かって遠位方向に向い、脾静脈にカテーテルの先端にある2つの追加の穴と8.5のFRシースデューサを挿入します。 2-0の関係のいずれかでの挿入に遠位カテーテルを修正し、別の2-0タイでの挿入に静脈近位を閉じます。オープン他の2の関係を残します。
- 、カテーテルから血液を描くの生理食塩水10mlで、それをフラッシュして、カテーテルのクランプを閉じます。
- 近位に遠心ポンプヘッドからなるバイパスへの生理食塩水、頚管(3/16 ")、およびポータルブランチ(3/16両方からの流入」)と大静脈の枝(1/4"、ルアーロックコネクタを埋めます開口部)。大静脈チューブの近位端にチューブクランプを置きます。
- ポータルとの両方のシース導入器カテーテル( 図1)へのバイパスの頸静開口部を接続し、conneをシール金属ホースクランプリングとction。そのポンプ位置に遠心ポンプヘッドを置きます。
- クロスクランプの前にトラネキサム酸およびヘパリン3分IVの万IU 1,000 mgを得。肝外性の相の時間のために2mg / kg /時間にプロポフォール注入率を低下させます。動脈圧と豚の反応性にイソフルラン濃度を調整します。
- シースイントロデューサカテーテルおよびクロスクランプ門脈の両方のクランプを開きます。血液が受動的にバイパスを介して実行されていることを確認してください。
- 約1,500回/分で遠心ポンプを起動します。 A)豚がcardiovascularly安定であり、b)はバイパスが約500 ml /分で実行されている場合、クロスクランプを続けます。豚は、クロスクランプ、代替ボリューム(クリスタロイド又はコロイド)と強心薬剤(小丸薬でノルエピネフリン)を許容しない場合。
- クロスデBakey·ベッククランプを使用して、腎静脈にちょうど頭蓋肝臓下の大静脈をクランプします。肝臓TISSにしっかりと圧力をかけますUEは、残存血液の一部を絞り出します。尾側の肝臓を後退しながらSatinskyクランプを使用して、横隔膜リムを含む肝上大静脈をクロスクランプ。
- 肝組織との境界で直接肝上大静脈をカットします。次に、肝門部付近の門脈をカット。
- 肝臓下静脈クランプの約4センチ頭蓋、大静脈の前壁に穴をカット。この穴に、ルアーロックを前方に向けてバイパス「大静脈開口部のコネクタを配置。
- 1-0シルクネクタイと肝臓下静脈にコネクタを固定します。そして、バイパスの大静脈枝のチューブクランプを開きます。
- 最後に、既存のポルト頚バイパスに加えて、大静脈、頚静脈バイパスを可能にするために肝臓下静脈クランプを開きます。 1100ミリリットル/分 - 約2,500回/分頚側のバイパス流出は900との間にあるようにポンプ速度を上げます。
- その残りのCの肝臓を切除肝臓下のバイパスコネクタに頭蓋onnection、バイパス接続を確保絆が切断されていないことを保証します。よじれを避けるために慎重に管バイパスを配置します。免疫抑制を初期化するために、メチルプレドニゾロンの500 mgを得。
3.船舶の復興
- 肝上大静脈の開口で、受信者側のすべての3つの横隔静脈口近くに4-0モノフィラメントポリプロピレン縫合糸を使用して。受信者側の肝上大静脈の両方の隅に内外二重武装4-0モノフィラメントポリプロピレン縫合糸をステッチ。
- アイスボックスからドナー臓器袋を取り出します。 、臓器袋を開けドナーの肝臓を除去し、腹腔内に配置します。
- 肝上大静脈のエンドツーエンドの吻合のために、受信者側に適合するように、ドナー肝上大静脈をトリミング。受信者側コーナーステッチの内側の針を使用して、suprahの各辺の内外コーナーステッチを行いますepaticドナー静脈。
- 一緒に右の縫合糸の両端を撃ちました。次に左側の縫合糸の両方の終末を結ぶ、レシピエントとドナー静脈の両方の小孔を近似します。
- 短い端を撮影して、次のタイに戻って壁を受信者の静脈の外内側のステッチを行います。理想的には、静脈壁を外転、後壁の上に実行してください。
- 右側に達した後、同じ縫合糸で2-3前壁ステッチを追加し、この縫合結末を撃ちました。左隅からの残りの縫合糸を使用して前壁の上に実行します。一緒に背中と前壁に使用される両方の縫合糸を結びます。右コーナーで他の二つの縫合糸終末を結びます。
- 適切な長さにドナー門脈をトリミングした後、6-0モノフィラメントポリプロピレン縫合糸を使用して、同様の方法で、エンドツーエンドの門脈吻合を行います。まもなく前壁で終了する前に、別のフラッシュラインと肝臓下の静脈の内腔を挿管し、生理食塩水1LでUW液を洗い流しますRTで肝臓下cavaportal静脈から。
- 吻合を完了し、成長因子のおよそ0.5cmに残して、縫合糸を結びます。別のデBakey-ベックはドナー肝臓下静脈へクランプ置きます。
- 肝上大静脈クランプを開き、出血を確認してください。そして、ポータルクランプを開くことによって、肝臓を再灌流。
- 止血ステッチのための6-0モノフィラメントポリプロピレン縫合糸を使用してください。約1,500回/分にバイパスポンプの回転数を減少させ、ポータルシース導入カテーテルのクランプを閉じます。
- 肝臓下の大静脈の受信者側がReclamp、バイパスの大静脈部分にチューブクランプを置きます。遠心ポンプを停止します。
- 大静脈コネクタの絆をカットし、それを削除します。頸静脈カテーテルを介して豚にバイパスからの残りの血液を返します。
- 頸静脈カテーテルのクランプを閉じ、バイパスを外します。ヘパリンに拮抗するために硫酸プロタミンの100 mgを得。パイの特別な注意を払ってくださいこれらのステップの間にGの血行動態。圧力サポートと代謝性アシドーシスの代替重炭酸ナトリウムのためのカテコールアミンを使用しています。
- 5-0モノフィラメントポリプロピレン縫合糸を用いて、上記のように再び肝臓下静脈のエンドツーエンドの吻合を実行します。両方のクランプを解除することにより肝臓下の下の静脈を再灌流。
- ドナーの腹腔動脈の周りの大動脈パッチをトリミングします。総肝動脈に近い受信者胃十二指腸動脈を縛ります。胃十二指腸動脈の接合部の近位に総肝動脈にブルドッグクランプを置きます。接合部の周りの血管組織を使用して、ポッツはさみと小さな動脈パッチをトリミング。
- ヘパリン化生理食塩水10mlでドナー肝動脈をフラッシュし、別のブルドッグは、出血をバック避けるために、さらに遠位クランプ置きます。 6-0モノフィラメントポリプロピレン縫合糸を使用して、実行中のパラシュート法で動脈小孔のエンドツーエンドの吻合。最初OPEによって再灌流寧遠位した後、近位ブルドッグクランプ。
- 上述の技術を使用して実行されている2 6-0モノフィラメントポリプロピレン縫合糸で胆管のエンドツーエンドの吻合。ブタ胆管は非常に壊れやすく、簡単に涙ためperibiliary組織の大部分が含まれていることを確認してください。
- 止血のためにチェックした後、脾静脈からシース導入カテーテルを取り除きます。残りの2タイで近位端および遠位端を閉じます。
- サイズ1モノフィラメント吸収性縫合糸で腹壁を閉じます。いずれかのスキンステープラーまたは実行中の2-0縫合糸で皮膚を閉じます。
4.術後相
- 豚を暖かく保つために加熱パッドと熱循環ブランケットを使用してください。
- 毎時サンプル血液ガス。注入速度を増加させることによって脱水を調整します。
- 麻酔を離乳させます。別の2時間豚を換気します。
- VEの左頸静脈からのシース導入カテーテルを削除である。プレス数分の出血を防ぐためにしっかりとしました。
- 豚の首の側にトンネルTPNカテーテルを皮下に。 2-0縫合糸で固定します。
- 豚は、カテコールアミンのサポートなしで血行力学的に安定であれば、2時間後に動脈ラインを削除します。穿刺側は出血していないことを確認してください。それ以外の場合は、動脈を閉じずに、動脈の穴の周りに6-0巾着ステッチを作ります。切開部位を閉じます。
- 豚は、独立して呼吸することができたら、換気を停止します。気管チューブからの換気チューブを外します。豚が十分に呼吸している場合、繰り返し確認してください。
- 加熱ランプを備えた単一の動物ペンに腹臥位で豚を配置します。抜管はかつて豚は、独立して、彼の頭を保持することができます。それは胸骨横臥位を維持するのに十分な意識を取り戻したまで無人動物を放置しないでください。ハウス全体術後期間の別々の豚。
- 提供します術後に十分な静脈内鎮痛薬(例えば、ブプレノルフィン0.01から0.05ミリグラム/ kgのすべての6時間)。
- 豚は、独立して飲まれない場合は、十分なボリュームIVを置き換えます
- (毎朝250mgの術後日(POD)1朝、その後125 mg)で免疫抑制としてメチルプレドニゾロンを続行します。上POD2から一日二回の2mg / kg、経口セファロスポリン起動します。
- メトロニダゾール500mgの1日2回セファゾリン1,000mgのと同様に、一日一回POD3までパントプラゾール20mgを投与します。
- 密接に豚を監視します。それは苦痛の兆候を示している場合、それを生け贄に捧げることを躊躇しないでください(例えば、無気力、再注輸は、永続的なアシドーシスや低血糖症、または出血または腹膜炎の徴候を飲みます)。安楽死のために、肝上大静脈を切断することにより、深いイソフルラン麻酔(5%、> 2.5 MAC)の下に豚を放血。
結果
最初の移植の研究では、心臓鼓動ドナーモデルでは(HBD、n = 5)をDCDモデルと比較した(n = 10)、その場で暖かい虚血の45分に暴露しました。両方のグループでは、移植片は、調達後10時間氷上で保存しました。
HBDグループでは、受信者のブタの100%が移植後5日目のフォローアップの最後まで生存しました。 DCDグループでは、受信者の豚の50%が減少し、術後肝機能の結果として、凝固の問題や代謝代償に起因する5日間生存しました。
すべての血液サンプルは、中心静脈カテーテルから採取しました。遠心分離後、血清試料を入手し、肝細胞傷害(アスパラギン酸アミノトランスフェラーゼ、AST)、胆管の機能(総ビリルビンおよびアルカリホスファターゼ)、および肝機能(INR)を分析しました。 5 -各マーカーの時間経過を図2に示されています。
ASTレベルは、24時間(DCDグループ内のHBDグループ内の1414±538 U / Lと2296±1313 U / L、P = 0.13)の後にピークに達し、5日後にはほぼ正常値に戻りました。 HBD群(162±54 U / L、P = 0.27)と比較した場合、同様に、アルカリホスファターゼ値が顕著に(224±111 U / L)DCDグループ内の36時間後に増加しました。総ビリルビンが(≤10マイクロモル/ Lを通じて)HBDグループで安定であったが、それは徐々に5日目までDCD群では増加した(23±31マイクロモル/ L、P = 0.43)。 DCDグループ中のビリルビン値の大きな標準偏差は、このグループの独特の不均一性胆管損傷を示しています。肝機能のマーカーとしてのINRは、AST値と同様の傾向を示しました。値は、24時間でピークに達し、5日後にはほぼ正常値に回復しました。 HBDグループはDCD群と比較して1.47±0.34でピークと低い値を示した(ピーク1.70±0.36、P = 0.32)。
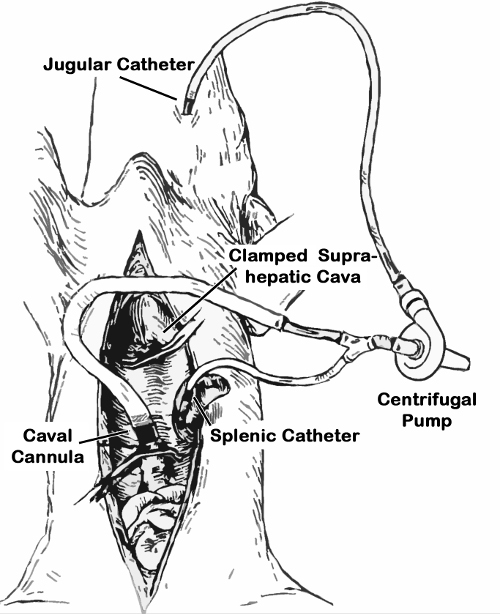
ポルト大静脈-頸静シャントの図1のスキーム。バイパスが乳酸リンゲル液で満たされています。次に、大静脈部分はチューブクランプでクランプされ、頸静脈および脾臓部分があらかじめ設定されたカテーテルに接続され、バイパスが開かれ、遠心ポンプは、門脈クランプ後に開始されます。肝切除後、バイパスの大静脈部分が挿入され、腎静脈へ、肝臓下大静脈断端に頭蓋確保します。チューブクランプは、ポータル伸張に加えて、大静脈伸長を可能にするために解放されます。
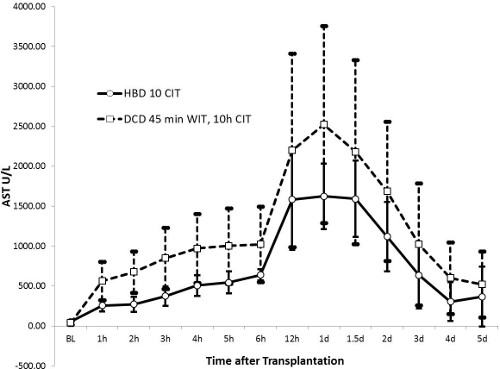
図2.アスパラギン酸アミノトランスフェラーゼ(AST)(HBDはn = 5、DCDのn = 10)。ASTは、肝細胞損傷の敏感なマーカーです。ピーク後方ER 24時間より少ない肝再灌流傷害を示唆し、DCD群よりもHBDが低いです。小さい標準偏差はHBD群でより均質な結果を示しています。
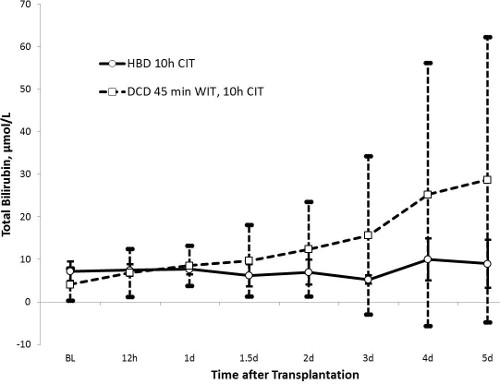
図3.総ビリルビン(HBDはn = 5、DCDのn = 10)。総ビリルビンは、胆汁クリアランスと胆管の完全性のマーカーとして、HBDグループでは10マイクロモル/ L以下の値で安定して均質な傾向を示しています。 DCDグループ中のビリルビン曲線は実験群の一部のみで胆管損傷を示唆し、時間をかけて徐々に増加し、高い標準偏差を示しています。
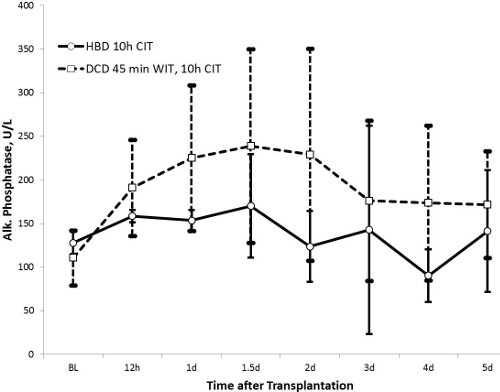
図4アルカリホスファターゼ(HBD N = 5、DCD N = 10)。アルカリホスファターゼI胆管損傷の指標です。 HBD基の値は小さい胆管の損傷を意味するDCD群のそれよりも低いです。
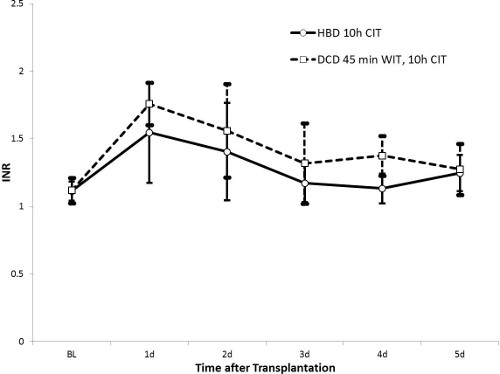
図5 INR(HBD N = 5、DCD N = 10)。高INR値は、凝固因子の放出の減少に起因する肝機能の低下を示しています。 HBDとDCD両方のグループでは、INR値は、肝機能の回復を示唆し、5日目移植後正常値に戻ります。 HBDグループの値が低く表示されます。
ディスカッション
実験ブタOLTxは、臨床シナリオの集中治療資源のない研究の設定のための挑戦的な手順です。可能性のある合併症は、血行動態不安定、出血、臓器虚血、低体温、および代謝、ならびに呼吸器、代償があります。いずれの研究グループでは、外科的手法5と同様に豚麻酔14,15の十分な手続き訓練が代表と再現性のある結果を得るために必須です。
多くの技術的な機微は、特に、血管再建段階5について 、文献に記載されています。上記のOLTxプロトコルは人間OLTx似静脈-交換モデルに必要な情報を提供します。得られた結果は、両方のHBDとDCDモデルで信頼性の高い動物の生存および移植片の回復を示しています。プロトコルは、グラフト再灌流EXPEで使用短期生存のシナリオに適用可能ですriments、例えば、ならびに耐性の研究と長期生存モデルにおいて。
ブタOLTxの一つの大きな障害は、静脈と門脈クロスクランプの比較的低い許容範囲です。肝外性の段階の間に内臓渋滞があっても、臓器再灌流7後に不可逆的なショックの点に主要な腸管虚血や血行動態不安定になる可能性があり、静脈高血圧および毛細管損傷を引き起こします。大静脈を完全に肝実質内に埋め込まれているので、静脈温存ピギーバック手順は実行可能ではありません。静脈再建段階中の大静脈の完全閉塞は、豚の血行動態の安定性を損ないます。いくつかの報告は、ブタOLTx未満25分16,17の合計静脈と門脈閉塞の間に達成することができることを示しているが、血管再建の時間ポルト静脈-頸静バイパス技術は、より安全で実用的な選択肢7- 9,18。目でEの著者の経験は、受動ポルト頚バイパスは肝外性の相の間に安定した豚の血行動態を維持する最適ではありません。肝臓下の静脈と門脈の両方の活性伸長を含むバイパスモデルは、予期せぬ合併症に延長しても、クランプ時間は肝上大静脈と門脈吻合の穏やかな再構築フェーズを可能にします。ポータルバイパスカテーテルが除去されると以前の報告7に反して、脾臓摘出は必須ではありません。脾動脈と静脈の両方が十分に灌流近位半分を残して約途中脾臓の長さに沿って閉じられています。によるバイパス断線に出血や空気塞栓症などの合併症は、バイパスを慎重に配置され、適切に固定されていることを確実にすることによって回避されています。
長期生存OLTx実験では、胆管吻合は、その高い合併症率19に弱点を考えられています。胆管組織は非常に壊れやすいとネブラスカ処理されている場合は、特に注意をEDS。多くの異なる吻合技術が5,19に記載されています。エンドツーエンドの吻合は、技術的に容易で、最小限の合併症19と関連しています。 peribiliary結合組織の大きなセクションを含む非切断針と連続縫合糸が結節縫合よりも優れていることが表示されます。中断された縫合糸の単一の縫い目が結ばれるとき胆管が不要張力下に置かれます。これは、組織の涙と連続した胆汁漏れになることがあります。縫合材料 - 吸収性または非吸収性の - ブタが終了するまでの限られた寿命を与え、通常は重要ではありません。数ヶ月にわたって長期生存モデルでは、吸収性縫合糸 - 人間OLTxのようには - が好ましいです。
特定のケアは、術後のフォローアップで撮影する必要があります。十分な栄養と流体供給、信頼性のある鎮痛プロトコル、および適切な免疫抑制政権は義務です。長期的な実験のために、免疫抑制は特に重要であると思われます。他の哺乳動物に比べて、豚はOLTx 20,21の後に驚くほど低い免疫拒絶率を示しています。円形細胞浸潤は、移植後の第2週の間に最大であり、さらには免疫抑制せずに自然に減少します。拒絶反応はほとんどブタOLTx 22後の死亡原因ではありません。しかし、ここで述べたステロイドIVおよびカルシニューリン阻害剤の経口投与することを含む、免疫抑制プロトコルで、移植片拒絶はOLTx後約4日で開始トランスアミナーゼの軽度の増加によって示され、見かけ上のポータルフィールド円形細胞浸潤を確認しました。カルシニューリン阻害剤は経口23,24又は静脈25,26のいずれかを挙げることができます。両方の方法には欠点があります。でも経口適用助剤と、胃腸管に到達する実際の量は、とらえどころのないままになります。一方、連続的な静脈内注入でアクティブな動物と豚のペンは困難です。したがって、静脈内アプリケーションは、潜在的な毒性効果とともに高い薬物濃度ピークになり、ボーラスとして実行する必要があります。それにもかかわらず、アプリケーションの両方の方法は、長期生存を可能にするように思われます。
臨床設定と同様に、術後ストレス潰瘍の予防が推奨されます。消化性潰瘍の術後の出血が頻繁な問題であり、障害肝機能27に関連し得ます。両方OLTx群で消化管出血のいくつかのケースの後、著者は、パントプラゾールとの定期的な予防を始めて以来、任意の消化管出血を経験しませんでした。
臨床手術室内の条件に匹敵する手術滅菌条件の厳格な保守、およびその結果としての抗生物質の予防は、感染性合併症のリスクを減少させます。
結論として、この記事のProvides研究設定でブタOLTxプログラムを確立するための実用的な情報。十分な献身、練習、およびチームワークは、学習期間を減少させる信頼性のある結果を生成するために、コストおよび研究動物の数を減少させるために重要です。
開示事項
The authors have nothing to disclose.
謝辞
The study was supported by research grants from the Roche Organ Transplant Research Foundation (ROTRF) and Astellas. Markus Selzner was supported by an ASTS Career Development Award. Matthias Knaak was supported by the Astellas Research Scholarship. We thank Uwe Mummenhoff and the Birmingham family for their generous support.
資料
| Name | Company | Catalog Number | Comments |
| Atropine Sulphate 15 mg/30ml | Rafter 8 Products | 238481 | |
| Buprenorphine 0.3 mg/ml | RB Pharmaceuticals LDT | N/A | |
| Cefazolin 1 g | Pharmaceutical Partners of Canada Inc. | 2237138 | |
| Cyclosporin Oral Solution 5,000 mg/50 ml | Novartis Pharmaceuticals Canada Inc. | 2150697 | |
| Fentanyl Citrate 0.25 mg/5 ml | Sandoz Canada Inc. | 2240434 | |
| Heparin 10,000 iU/10 ml | Leo Pharma A/S | 453811 | |
| Isoflurane 99.9%, 250 ml | Pharmaceutical Partners of Canada Inc. | 2231929 | |
| Ketamine Hydrochloride 5000 mg/50 ml | Bimeda-MTC Animal Health Inc. | 612316 | |
| Lactated Ringer’s + 5% Dextrose, 0.5 L | Baxter Corporation | 61131 | |
| Lacteted Ringer’s, 1 L | Baxter Corporation | 61085 | |
| Metronidazole 500 mg/100 ml | Baxter Corporation | 870420 | |
| Midazolam 50 mg/10 ml | Pharmaceutical Partners of Canada Inc. | 2242905 | |
| Pantoprazole 40 mg | Sandoz Canada Inc. | 2306727 | |
| Potassium Chloride 40 mEq/20 ml | Hospira Healthcare Corporation | 37869 | |
| Propofol 1,000 mg/100 ml | Pharmascience Inc. | 2244379 | |
| Protamine Sulfate 50 mg/5 ml | Pharmaceutical Partners of Canada Inc. | 2139537 | |
| Saline 0.9%, 1 L | Baxter Corporation | 60208 | |
| Sodium Bicarbonate 50 mEq/50 ml | Hospira Healthcare Corporation | 261998 | |
| Solu-Medrol 500 mg | Pfizer Canada Inc. | 2367963 | |
| Tranexamic Acid 1,000 mg/10 ml | Pfizer Canada Inc. | 2064413 | |
| University of Wisconsin Solution, SPS-1 | Organ Recovery Systems | SPS-1 | |
| Xylocaine Endotracheal 10 mg/50 ml | AstraZeneca | 2003767 | |
| Appose ULC 35 W skin stapler | Covidien Canada | 803712 | |
| Maxon, 1 | Covidien Canada | 606173 | |
| Sofsilk, 0 | Covidien Canada | S606 | |
| Sofsilk, 2-0 | Covidien Canada | S405 | |
| Sofsilk, 3-0 | Covidien Canada | S404 | |
| Surgipro II, 4-0 | Covidien Canada | VP581X | |
| Surgipro II, 5-0 | Covidien Canada | VP725X | |
| Surgipro II, 6-0 | Covidien Canada | VP733X | |
| Catheter i.v, 18 G | BD Canada | 381147 | |
| Cook TPN catheter, 9.5 Fr | Cook Medical Company | C-TPNS-9.5-90 | |
| PSI Kit for sheath catheter, 8.5 Fr | Arrow International | ASK-09803-UHN | |
| Infusion Pump Line | Smith Medical ASD Inc. | 21-0442-25 | |
| Liver Admin Set (flush line) | CardioMed Supplies Inc | 17175 | |
| Mallinckrodt, Tracheal Tube, 6.5 mm | Covidien Canada | 86449 | |
| Med-Rx Suction Connecting Tube | Benlan Inc. | 70-8120 | |
| Organ Bag | CardioMed Supplies Inc | 2990 | |
| Suction Tip | Tyco Healthcare Group LP | 8888501023 | |
| Valleylab, Cautery Pencil | Covidien Canada | E2515H | |
| Valleylab, Patient Return Electrode | Covidien Canada | E7507 | |
| Bypass Connector 3/8” x 1/4“ | Raumedic AG | 955083-001 | |
| Bypass Connector 3/8” x 3/8” Luer Lock | Raumedic AG | 955163-001 | |
| Bypass Connector Y 3/8” x 3/8” x 1/4” | Raumedic AG | 961360-002 | |
| Bypass Tubing 1/4” x 1/16” | Raumedic AG | 039505-010 | |
| Bypass Tubing 3/8” x 3/32” | Raumedic AG | 039535-005 | |
| Rotaflow Centrifugal Pump | Maquet-Dynamed | HC 2821 | |
| Stainless Steel Hose Clamp Ring, 5mm | Oetiker | 16700007 | |
| Abdominal Retractor | Medite GmbH | N/A | |
| De Bakey – Beck, Infrahepatic Cava Clamp | Aesculap Inc. | FB519R | |
| Deithrich, Atraumatic Clamp (Portal Vein) | Aesculap Inc. | FB525R | |
| Gregory Bulldog Clamp, curved | Aesculap Inc. | FB382R | |
| Gregory Bulldog Clamp, straight | Aesculap Inc. | FB381R | |
| Potts – De Martel, Scissors | Aesculap Inc. | BC648R | |
| Satinsky, Suprahepatic Cava Clamp | Aesculap Inc. | FB605R | |
| Symetrical Tubing Clamp | Codman Instruments | 198010 | |
| Anesthesia Machine, Optimax | Moduflex Anesthesia Equipment | SN5180 | |
| Bypass Flow meter, HT 110 | Transonic Systems Inc. | HT110B11106 | |
| Flow meter probe, H6XL | Transonic Systems Inc. | H6Xl689 | |
| Heat Therapy Pump, T/Pump | Gaymar Industries Inc | TP500-G89D19 | |
| Infusion Pump 3,000 | SIMS Graseby LTD. | SN300050447 | |
| Isoflurane Vapor 19.1 | Draeger Medical Canada Inc. | N/A | |
| Monitor, Datex AS 3 | Instrumentarium Corp./ Hitachi | D-VHC14-23-02 | |
| Rotaflow Centrifugal Drive Unit | Maquet-Dynamed | 952301 | |
| Rotaflow Console | Maquet-Dynamed | 706035 | |
| Temperature Therapy Pad | Gaymar Industries Inc | TP26E | |
| Valleylab Force Tx | Valleylab Inc. | 216151480 | |
| Ventilator, AV 800 | DRE Medical Equipment | 40800AVV | |
| Warm Touch, Patient Warming System | Nellcor/ Covidien Canada | 5015300A |
参考文献
- Mehrabi, A., Fonouni, H., Muller, S. A., Schmidt, J. Current concepts in transplant surgery: liver transplantation today. Langenbecks Arch. Surg. 393 (3), 245-260 (2008).
- Qiu, J., Ozawa, M., Terasaki, P. I. Liver transplantation in the United States. Clin. Transpl. , 17-28 (2005).
- Chalstrey, L. J. Technique of orthotopic liver transplantation in the pig. Br. J. Surg. 58 (3), 585-588 (1971).
- Esmaeilzadeh, M. Technical guidelines for porcine liver allo-transplantation: a review of literature. Ann. Transplant. 17 (2), 101-110 (2012).
- Calne, R. Y. Observations of orthotopic liver transplantation in the pig. Br. Med. J. 2 (5550), 478-480 (1967).
- Memsic, L., Quinones-Baldrich, W., Kaufman, R., Rasool, I., Busuttil, R. W. A comparison of porcine orthotopic liver transplantation using a venous-venous bypass with and without a nonpulsatile perfusion pump. J. Surg. Res. 41, 33-40 (1986).
- Torres, O. J. Hemodynamic alterations during orthotopic liver experimental transplantation in pigs. Acta. Cir. Bras. 23 (2), 135-139 (2008).
- Battersby, C., Hickman, R., Saunders, S. J., Terblanche, J. Liver function in the pig. 1. The effects of 30 minutes' normothermic ischaemia. Br. J. Surg. 61 (1), 27-32 (1974).
- Smith, A. C., Swindle, M. M. Preparation of swine for the laboratory. Ilar. J. 47 (4), 358-363 (2006).
- Swindle, M. M., Smith, A. C. Best practices for performing experimental surgery in swine. J. Invest. Surg. 26 (2), 63-71 (2013).
- Moench, C., Moench, K., Lohse, A. W., Thies, J., Otto, G. Prevention of ischemic-type biliary lesions by arterial back-table pressure perfusion. Liver Transpl. 9 (3), 285-289 (2003).
- Koski, E. M., Suhonen, M., Mattila, M. A. Ultrasound-facilitated central venous cannulation. Crit. Care Med. 20 (3), 424-426 (1992).
- Lange, J. J., Hoitsma, H. F., Meijer, S. Anaesthetic management in experimental orthotopic liver transplantation in the pig. Eur. Surg. Res. 16 (6), 360-365 (1984).
- Kaiser, G. M., Heuer, M. M., Fruhauf, N. R., Kuhne, C. A., Broelsch, C. E. General handling and anesthesia for experimental surgery in pigs. J. Surg. Res. 130 (1), 73-79 (2006).
- Heuer, M. Liver transplantation in swine without venovenous bypass. Eur. Surg. Res. 45 (1), 20-25 (2010).
- Gruttadauria, S. Porcine orthotopic liver autotransplantation: facilitated technique. J. Invest. Surg. 14 (2), 79-82 (2001).
- Falcini, F. Veno-venous bypass in experimental liver transplantation: portal-jugular versus caval-portal-jugular. G. Chir. 11 (4), 206-210 (1990).
- Filipponi, F., Benassai, C., Falcini, F., Martini, E., Cataliotti, L. Biliary tract complications in orthotopic liver transplantation: an experimental study in the pig. Ital. J. Surg. Sci. 19 (2), 131-136 (1989).
- Terblanche, J. Orthotopic liver homotransplantation: an experimental study in the unmodified pig. S. Afr. Med. J. 42 (20), 486-497 (1968).
- Calne, R. Y. Prolonged survival of liver transplants in the pig. Br. Med. J. 4 (5580), 645-648 (1967).
- Battersby, C., Egerton, W. S., Balderson, G., Kerr, J. F., Burnett, W. Another look at rejection in pig liver homografts. Surgery. 76 (4), 617-623 (1974).
- Net, M. The effect of normothermic recirculation is mediated by ischemic preconditioning in NHBD liver transplantation. Am. J. Transplant. 5 (10), 2385-2392 (2005).
- Guarrera, J. V. Hypothermic machine perfusion of liver grafts for transplantation: technical development in human discard and miniature swine models. Transplant Proc. 37 (1), 323-325 (2005).
- Minor, T. Hypothermic reconditioning by gaseous oxygen improves survival after liver transplantation in the pig. Am. J. Transplant. 11 (12), 2627-2634 (2011).
- Kelly, D. M. Porcine partial liver transplantation: a novel model of the 'small-for-size' liver graft. Liver Transpl. 10 (2), 253-263 (2004).
- Meijer, S., Hoitsma, H. F., Visser, J. J., de Lange, J. J. Long term survival following orthotopic liver transplantation in pigs; with special reference to gastric ulcer complications. Neth. J. Surg. 36 (6), 168-171 (1984).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved