Method Article
활성 포르토 대정맥 션트를 사용하여 돼지 간 조달 및 동소 이식 이식의 기술
요약
Experimental animal research plays a pivotal role in the development of clinical transplantation practice. The porcine orthotopic liver transplantation model (OLTx) closely resembles human conditions and is frequently used in clinically oriented research. The following protocol contains all information for a reliable porcine OLTx model using an active porto-caval-jugular shunt.
초록
The success of liver transplantation has resulted in a dramatic organ shortage. Each year, a considerable number of patients on the liver transplantation waiting list die without receiving an organ transplant or are delisted due to disease progression. Even after a successful transplantation, rejection and side effects of immunosuppression remain major concerns for graft survival and patient morbidity.
Experimental animal research has been essential to the success of liver transplantation and still plays a pivotal role in the development of clinical transplantation practice. In particular, the porcine orthotopic liver transplantation model (OLTx) is optimal for clinically oriented research for its close resemblance to human size, anatomy, and physiology.
Decompression of intestinal congestion during the anhepatic phase of porcine OLTx is important to guarantee reliable animal survival. The use of an active porto-caval-jugular shunt achieves excellent intestinal decompression. The system can be used for short-term as well as long-term survival experiments. The following protocol contains all technical information for a stable and reproducible liver transplantation model in pigs including post-operative animal care.
서문
동소 이식 간 이식 (OLTx)는 말기 간 질환 또는 고급 간암 환자 만 치료 방법이다. 지난 25 년 동안, 대기리스트에 후보들의 수는 점차 증가하고 지금까지 가능한 이식편의 수를 초과하고있다. 대부분의 이식 지역에서는 간 이식 대기자 명단에 환자의 20-30%는 장기 이식을받지 않고 사망 또는 인해 질병의 진행에 상장 폐지된다. 전략 따라서, 가능한 이식편의 수, 절실히 요구되는, 도너 풀을 증가시키고있다. 확장 기준 기관 할당, 장기 이식 보존 및 면역 관용의 유도는 여전히 주요 임상 과제 1-3을 나타냅니다. 따라서, 실험 OLTx 연구는 임상 OLTx 연습을 최적화하기 위해 중요한 것입니다.
돼지 OLTx는 L을 포함하여 여러 가지 방법으로 인간의 OLTx 유사한 잘 확립 된 실험 모델이버 크기, 해부학, 생리학 4-6. 따라서, 이러한 수술 기법, 생리학, 면역학, 보존, 및 허혈 재관류 손상으로 연구 분야에서 표준 실험 방법이되었다. 이식 조달,받는 사람 간절하고, 특히, 혈관 재건의 수많은 기술 문헌 5에 기재되어있다. 적절한 기술의 선택은 연구자의 선호 및 기술 능력에 따라 달라집니다.
인간 시나리오와 대조적으로, anhepatic 단계에서 내장의 정체 돼지 OLTx에서 중요한 문제를 나타낸다. 후속 창자 허혈 및 울혈 혈관 손상, 즉, 실험 7-9의 성공을 돼지 생존을 위태롭게 심한 혈역학 적 불안정성을 야기하고있다. 따라서, 충분한 장 압축 해제는 특히 덜 기술적으로 세련된 실험 설정에서, 필수입니다.
우리anhepatic 단계의 기간 동안 활성 포르토 - 대정맥 - 경정맥 션트를 보내고하는 것은 장내 혼잡을 피하기 위해 신뢰할 수있는 옵션입니다. 시스템은 초기 재관류 실험뿐 아니라 장기 생존율 시나리오에 사용될 수있다. 다음 프로토콜은 간 절제술 및 엔드 - 투 - 엔드 혈관 재건 기술 및 수술 후 관리를 포함하여 기증자 간 조달,받는 사람 연산 포함 돼지 안정적이고 재현성 간 이식 모델에 대한 모든 정보가 포함되어 있습니다.
프로토콜
모든 동물의 건강, 온타리오, 캐나다의 국립 연구소에 의해 게시 된 의료 연구 및 '실험 동물의 관리에 대한 가이드'에 대한 국가 사회에 의해 공식화 ''실험 동물 관리의 원칙 '을 준수 인도적인 치료를받은 . 토론토 일반 연구소의 동물 관리위원회는 모든 연구를 승인했다.
1. 장기 검색
- 이식 전 일주의 연구 시설에서 30과 35kg 사이 주택의 남성 요크셔 돼지 (관류의 결과 10, 11 변경할 수)과 주거 조건에 동물을 순응하는 스트레스에 의한 물리적 인 반응을 방지합니다. 이전 마취의 유도에 6 시간의 최소 돼지를 빠르게.
- 케타민 (25 ㎎ / ㎏), 아트로핀 (0.04 ㎎ / ㎏) 및 미다 졸람 (0.15 ㎎ / ㎏)의 혼합물을 근육 내 (IM) 주사에 의해 도너 피그를 마취.
- 삽관에 앞서, 돼지는 자발적으로 5 %의 이소 플루 란을 투여 산소 2 L 통풍 보장. 앙와위에서 성대 경련을 방지하기 위해 삽관 전에 2 % 리도카인 2 분으로 성대를 스프레이. 35kg의 돼지를 들어, 6.5 프랑의 기관 튜브를 사용합니다. 실내 공기 5 ㎖ - 3 기관 튜브를 차단.
- 삽관 후, 올바른 삽관을 확인 capnometry를 사용합니다. 돼지의 꼬리에 맥박 산소 측정기에 의한 심박수와 산소 포화도를 모니터링합니다. 2 % 이소 플루 란 기화기를 낮 춥니 다.
- 최소 폐포 농도 (MAC) 값을 기준으로 마취의 깊이를 조정; 2.5 MAC - 2 목표로하고 있습니다. 16 호흡 / 분 및 10의 호흡량 - - 15 ㎖ / ㎏ 체중 (14)에 인공 호흡기를 설정합니다.
- 젖산 링거 용액 (200 ㎖ / 시간)의 주입을 허용하도록 귀 정맥 중 하나에 18 G 정맥 카테터를 놓는다. 돼지 스크럽 멸균 커튼으로 커버.
- 무균 조건을 확인한 후, 중간 선 개복술의 FOLLO을왼쪽 측면 확장에 의해 결혼. 왼쪽에 이동하기 전에 크고 작은 창자를 충당하기 위해 수건을 사용합니다.
- 낫 모양의 인대와 소작을 사용하여 삼각 인대를 나눕니다.
- 전기 소작을 이용하여 우측의 진동판 간 릴리스; 맥과 다이어프램의 상부에 가위를 사용합니다. 우측 부신 정맥 및 좌측 신장 정맥 지점까지 infrahepatic 카바 해부.
- infrahepatic 맥과 서로 원위부 대동맥을 분리; 척추 대동맥 가지를 결찰; 분리 및 부착 조직에서 무료로 신장 동맥. 2-0 동점 각각 신장 동맥을 둘러싸고 있습니다.
- 두개골 왼쪽 신장 정맥, 대동맥 및 장간막 동맥을 해부하다. 2-0 넥타이 장간막 동맥을 둘러싸고 있습니다.
- 장간막 동맥에 복막 두개골을 연 후, 조심스럽게 복강 트렁크쪽으로 대동맥을 따릅니다. 적이 포털에 꼬리 쪽 복강 트렁크를 해부하다에; 어느 지점 후방 복강 트렁크 오프 비장과 왼쪽 위 동맥을 둘러싸고 있습니다. 포털 정맥 오프 복강 트렁크를 해부하다.
- 췌장과 문맥 사이의 복강 절개하여 문맥을 놓습니다. 포털 정맥에 췌장에서 배출 정맥을 묶어.
- hepatoduodenal 인대에서 담관을 분리하고 원심 결찰 후 나눕니다.
- 림프 누출을 방지하기 위해 hepatoduodenal 인대 내 림프관을 결찰. 관계 사이의 위 십이지장 동맥과 오른쪽 위의 동맥을 나눈다. 작은 혈관을 결찰.
- 심장과 복강 트렁크 사이의 조리개 뒤에 대동맥을 해부하다. 복강 트렁크에 대동맥 두개골 주위에 2-0 동점을 놓습니다.
- 담낭을 제거하고 담낭 침대에서 출혈을 소작.
- 다이어프램을 엽니 다. intracardially 헤파린 1,000 IU / kg의 기증자 무게를 관리 또는 IV 달성하기 위해 5 % (> 2.5 MAC)에 이소 플루 란을 설정깊은 마취 수준. 순환 죽음 (DCD) 모델 후 기증자의 경우, 헤파린 투여 후 40 mval KCl을 3 분의 intracardial 주사로 심장 마비를 유도한다. 따뜻한 허혈의 시작점으로 설정 심정지.
- 신장, 비장, 장간막, 왼쪽 위 동맥 주위 이전에 설정 한 관계를 묶어. 신장과 장골 동맥 사이에 원심 대동맥을 묶고 기관 플러시 라인 대동맥을 cannulate.
- 같은 근위 가능한 포털 정맥을 묶어 다른 기관 플러시 라인을 cannulate.
- 근위 대동맥 주위에 미리 설정된 넥타이를 닫은 후, 대동맥 (압력 가방)과 문맥 (무게 중심)를 통해 듀얼 관류를 사용하여 위스콘신 (UW) 솔루션의 차가운 대학의 2 L로 간을 세척하십시오.
- 오래 남아있는 모든 혈관을 떠나 간을 절제. suprahepatic 정맥 주위에 관대 한 횡격막 림을 남겨주세요. 얼음에 멸균 장기 가방에 간을 놓습니다.
- 다시 테이블 준비, CL 동안Satinsky 클램프를 사용하여 suprahepatic 맥을 앰프와 포털 정맥 유출이 깨끗해질 때까지 역행 낮은 하대 정맥을 통해 간에게 UW 용액의 약 0.5 L와 두 번째로 세척하십시오.
- 대동맥과 복강 트렁크의 모든 동맥 가지를 묶어. UW 솔루션 (12)의 나머지 0.5 L와 동맥 백 테이블 압력 관류를 수행합니다.
- UW 용액을 사용하여 담관 플러시.
- 알맞은 크기로 횡격막 패치를 낸다. 모든 횡격막 정맥을 닫습니다 - 보통 (3), 각 1 왼쪽과 오른쪽, 1 후방 - 4-0 모노 필라멘트 폴리 프로필렌 바늘을 사용.
- 장기 가방을 닫고 얼음에 간을 저장합니다.
2.받는 사람 절제술
- 케타민 (25 ㎎ / ㎏), 아트로핀 (0.04 ㎎ / ㎏) 및 미다 졸람 (/ kg 0.15 mg)의 혼합물의 IM 주사에 의해받는 돼지를 마취.
- 난방 매트 위에 수술대에 앙와위에서 돼지를 놓습니다. 돼지 위스콘신 커버열 순환 담요를 토륨.
- 삽관에 앞서, 돼지는 자발적으로 5 %의 이소 플루 란을 투여 산소 2 L 통풍 보장. 성대 경련을 방지 삽관 전에 2 % 리도카인 2 분으로 성대 스프레이. 35kg의 돼지를 들어, 6.5 프랑의 기관 튜브를 사용합니다. 실내 공기 5 ㎖ - 3 기관 튜브를 차단.
- 삽관 후, 올바른 삽관을 확인 capnometry를 사용합니다. 돼지의 꼬리에 맥박 산소 측정기에 의한 심박수와 산소 포화도를 모니터링합니다. 놓고 돼지의 주둥이에 온도 프로브를 고정합니다. 2 % (- 2.5 MAC 2 목표)에 이소 플루 란 기화기를 낮 춥니 다. 16 호흡 / 분 및 10의 호흡량 - - 15 ㎖ / ㎏ 체중 (14)에 인공 호흡기를 설정합니다.
- 마취 동안 건조를 방지하기 위해 눈에 연고를 사용합니다.
- 왼쪽 외부 경정맥에 시스 유도 (8.5 프랑)을 삽입 Seldinger 기술 (13)를 사용합니다. 활성 포털 대정맥 - 경정맥 우회 나중에이 카테터를 사용합니다.
- Seldinger의 techniqu를 사용하여전자는 오른쪽 외부 경정맥에 총 정맥 영양 (TPN) 카테터 (9.5 프랑)를 삽입합니다.
- 멸균 조건 하에서, 우측 경동맥을 해부 침습적 동맥압 모니터링 폴리 프로필렌 카테터 (18 G)를 삽입한다. 비상 결찰을 허용 2-0 실크 넥타이와 동맥을 둘러싸고 있습니다.
- 1 % 이소 플루 란 기화기를 줄이십시오 (1.5-2 MAC)과 프로포폴 추가 - 마취의 깊이를 유지하기 위해 (5 ~ 8 ㎎ / ㎏ / 시간의 IV)를. 진통제를 들어, 연속 정맥 펜타닐 시트 레이트의 주입 (가장 바람직한, 2 μg의 / ㎏ / 시간) 또는 레미 펜타닐 (두 번째 선택, 15 μg의 / ㎏ / 시간)를 사용합니다.
- 피부 절개하기 전에 세푸 1,000 mg의 메트로니다졸 IV의 500 mg의를 제공합니다. 150 ㎖ / 시간에서 5 % 포도당 링거 락 테이트를 사용하여 주입 펌프를 설정합니다.
- 머리와 목 영역으로 열 순환 담요를 놓습니다. 돼지 스크럽 멸균 커튼으로 커버.
- 무균 조건에서 중간 선 개복술을합니다. 복부 R 삽입etractor 오른쪽 윗부분에 충분한 액세스를 얻을 수 있습니다.
- falciforme 인대와 소작을 사용하여 삼각 인대를 나눕니다.
- 여러 단계에서 관계 사이의 간 가까이 hepatoduodenal 인대를 나눕니다. 식별, 분할 및 간동맥과 담즙 덕트의 분기를 표시합니다.
- 위 십이지장 동맥의 부문까지 역행 간 동맥을 해부하다. 불독 클램프 나중에 클램핑 십이지장 동맥에 공통 간 동맥의 근위부에 맞는지 확인하십시오.
- 부착 조직에서 포털 정맥을 무료로 제공됩니다.
- 전기 소작을 사용하여 우측에서 복막 대정맥을 동원. 맥과 다이어프램의 상부에 가위를 사용합니다. 우측 부신 정맥 및 좌측 신장 정맥 지점까지 infrahepatic 카바 해부.
- 비장의 폐문을 노출. 약 반 비장의 길이, 신중 명확한 따라부착 된 복막 층에서 비장 동맥과 정맥 F. 4 2-0 실크 넥타이와 모두 비장 동맥과 정맥을 둘러싸고 있습니다.
- 포털 정맥쪽으로 원심 가리키는, 비장 정맥에 카테터의 팁이 추가 구멍 8.5 프랑 시스 유도를 삽입합니다. 2-0 관계의 하나의 삽입에 원심 카테터를 수정하고 다른 2-0 타이를 삽입하여 정맥의 근위부를 닫습니다. 열려있는 다른 두 관계를 둡니다.
- , 카테터에서 혈액을 채취 식염수 10 ㎖로 세척하고, 카테터의 클램프를 닫습니다.
- ""(과 대정맥 분기 (1/4 포털 분기 3/16) 모두에서, 유입 원심 펌프 헤드, 경정맥 튜브 (3/16) "의 근위부에, 루어 잠금 커넥터로 구성된 바이 패스에 식염수를 채우 개방). 대정맥 튜브의 기단부에 튜브 클램프를 넣습니다.
- 포털 모두 칼집 도입기 카테터 (그림 1)에 바이 패스의 경정맥 개방을 연결하고도없고 밀봉금속 호스 클램프 링 ction의. 그 펌프의 위치로 원심 펌프 헤드를 놓습니다.
- 트라 넥 삼산 1,000 mg의 크로스 클램핑 전에 헤파린 3 분 IV의 10,000 IU를 제공합니다. anhepatic 단계의 시간을 2 ㎎ / ㎏ / 시간에 프로포폴 주입 속도를 줄입니다. 동맥 압력과 돼지의 반응성에 이소 플루 란 농도를 조정합니다.
- 외장 도입기 카테터 및 크로스 클램프 포털 정맥 모두의 클램프를 엽니 다. 그 피가 수동적으로 바이 패스를 통해 실행되어 있는지 확인합니다.
- / 분 약 1,500 원의 원심 펌프를 시작합니다. ) 돼지 cardiovascularly 안정 및 b) 바이 패스는 약 500 ml / 분에서 실행중인 경우 크로스 클램핑을 계속합니다. 돼지는 크로스 클램핑, 대체 볼륨 (결정질 또는 콜로이드)과 inotrope 에이전트 (작은 boli에서 노르 에피네프린)을 허용하지 않습니다.
- 크로스 드 Bakey - 벡 클램프를 사용하여 신장 혈관에 바로 두개골 infrahepatic 대정 맥을 클램프. 간, 담배 마는에 확고한 압력을 적용UE는 남은 혈액의 일부를 짜내합니다. 꼬리 쪽 간을 후퇴하면서 Satinsky 클램프를 사용하여 횡격막 림을 포함 suprahepatic 대정 맥을 크로스 클램프.
- 간 조직과의 경계에 직접 suprahepatic 대정 맥을 잘라. 이어서, 간 폐문 근처 문맥을 잘랐다.
- infrahepatic 맥 클램프의 약 4cm의 두개골은 대정맥의 앞쪽 벽에 구멍을 잘라. 이 구멍에, 루어 잠금 장치가 전방으로 향하게 바이 패스 '대정맥 개방의 커넥터를 배치합니다.
- 1-0 실크 넥타이와 infrahepatic 맥에 커넥터를 고정합니다. 그런 다음, 바이 패스의 대정맥 지점의 튜브 클램프를 엽니 다.
- 마지막으로, 기존의 포르토 경정맥 우회 이외에 대정맥-경정맥 바이 패스를 허용하기 infrahepatic 카바 클램프를 연다. 약 2,500 원 / 분에 펌프 속도를 증가 등 경정맥 측에 바이 패스 유출 (900) 사이에 있는지 - 1,100 ml / 분.
- 남아있는 C에서 간 절제를 통해서만 이루어진다 infrahepatic 바이 패스 커넥터 두개골, 보장 바이 패스 연결을 고정하는 관계가 절단되지 않습니다. 꼬임을 방지하기 위해주의 깊게 튜브 바이 패스를 놓습니다. 면역 억제를 초기화하는 메틸 프레드니솔론 500mg을주세요.
3. 선박 재건
- 가까운 4-0 모노 필라멘트 폴리 프로필렌 봉합사, suprahepatic 맥의 구멍에서 수신자 측에 3 횡격막 정맥 오스티 사용. 수신자 측의 suprahepatic 맥의 양쪽 모서리에 내부 - 외부를 두 번 무장 4-0 모노 필라멘트 폴리 프로필렌 봉합 스티치.
- 얼음 상자에서 기증자의 장기 가방을 제거합니다. , 장기 가방을 열고 기증자의 간을 제거하고 복강에 배치합니다.
- suprahepatic 정맥의 종단 문합 들어, 수신자 측에 맞게 도너 suprahepatic 대정맥 트림. 수신자 측 코너 스티치 내측의 바늘을 사용하여, suprah의 측면 각각에 내외부 모서리 스티치를 할epatic 기증자 맥.
- 함께 오른쪽 봉합사의 양쪽 끝 샷. 다음 왼쪽 봉합사의 양쪽 끝을 묶어,받는 사람과 기증자 맥 모두 오스티에 근접.
- 짧은 끝을 촬영 한 다음 넥타이 다시 벽을받는 정맥의 외부 - 내부 스티치을한다. 이상적으로 정맥 벽을 everting, 후면 벽을 통해 실행합니다.
- 오른쪽에 도달하면 같은 봉합사와 2-3 전면 벽 바늘을 추가,이 봉합 결말을 촬영. 왼쪽 구석에 남아있는 봉합사를 사용하여 전면 벽을 통해 실행합니다. 함께 앞면과 뒷면 벽에 사용되는 두 봉합을 묶어. 오른쪽 모서리에있는 다른 두 봉합 끝을 묶어.
- 적당한 길이로 도너 간문맥 트리밍 후 6-0 모노 필라멘트 폴리 프로필렌 봉합을 사용하여, 동일한 방식으로 엔드 - 투 - 엔드 포털 정맥 문합을 수행한다. 바로 앞 벽 마무리하기 전에, 다른 플러시 라인 infrahepatic 맥의 루멘을 삽관 및 생리 식염수 1 L로 UW 솔루션을 플러시실온에서 infrahepatic cavaportal 정맥을 통해.
- 문합을 완료하고 성장 인자의 약 0.5 센티미터를 남겨두고 봉합을 묶어. 다른 데 Bakey- 벡 기증자 infrahepatic 맥에 고정 넣습니다.
- suprahepatic 맥 클램프를 열고 출혈이 있는지 확인합니다. 그리고, 포털 클램프를 개방함으로써 간 재관류.
- 지혈 스티치를 위해 6-0 모노 필라멘트 폴리 프로필렌 봉합사를 사용합니다. 약 1,500 원 / 분에 바이 패스 펌프의 속도를 낮추고 포털 시스 도입기 카테터의 클램프를 닫습니다.
- infrahepatic 대정 맥의 수신자 측 Reclamp 및 바이 패스의 대정맥 부분에 튜브 클램프를 넣어. 원심 펌프를 중지합니다.
- 대정맥 커넥터의 관계를 잘라 제거합니다. 경정맥 카테터를 통해 돼지 바이 패스에 남아있는 혈액을 돌려줍니다.
- 경정맥 카테터의 클램프를 닫고 바이 패스 연결을 끊습니다. 헤파린을 적대시하는 프로타민 황산의 100 mg을주세요. 파이의 특별한주의이 단계 동안 G의 혈역학; 대사성 산증에 대한 압력 지원 및 대체 중탄산 나트륨에 대한 카테콜아민을 사용합니다.
- 5-0 모노 필라멘트 폴리 프로필렌 봉합을 이용하여, 전술 한 바와 같이 다시 infrahepatic 카바 종단 문합을 수행한다. 두 클램프를 풀어 infrahepatic 낮은 맥을 재관류.
- 기증자의 복강 트렁크 주위 aortal 패치를 낸다. 일반 간장 동맥 근처에받는 사람 십이지장 동맥을 묶어. 위 십이지장 동맥의 교차점에 근위 일반적인 간동맥에 불독 클램프를 넣습니다. 접합 주위의 혈관 조직을 사용하여, 포츠 가위와 작은 동맥 패치를 낸다.
- 헤파린 식염수 10 mL로 기증자 간 동맥을 세척하고 다른 불독 더 원심 클램프 출혈 다시 않도록했습니다. 6-0 모노 필라멘트 폴리 프로필렌 봉합사를 사용하여, 실행 낙하산 기법에서 동맥 오스티의 종단을 문합. 처음 OPE에 의해 재관류닝 원위부 후 근위 불독 클램프.
- 전술 한 기술을 사용하여 실행이 6-0 모노 필라멘트 폴리 프로필렌 봉합 담관 종단을 문합. 돼지 담관이 매우 취약하고 쉽게 눈물 때문에 peribiliary 조직의 큰 부분이 포함되어 있는지 확인합니다.
- 지혈을 검사 한 후, 비장 정맥에서 시스 도입기 카테터를 제거합니다. 나머지 2 타이 근위 및 원위 끝을 닫습니다.
- 크기 1 모노 필라멘트 흡수성 봉합사와 복부 벽을 닫습니다. 피부 스테이플러 또는 실행중인 2-0 봉합사로 피부를 닫습니다.
4. 수술 후 단계
- 돼지을 따뜻하게 유지하기 위해 가열 패드와 열 순환 담요를 사용합니다.
- 시간당 샘플 혈액 가스. 주입 속도를 증가시킴으로써 탈수를 조정한다.
- 마취를 유아. 또 다른 2 시간 동안 돼지를 환기 시키십시오.
- 적이 왼쪽 경정맥에서 시스 도입기 카테터를 제거인치를 눌러 몇 분 출혈을 방지하기 위해 단단히하십시오.
- 터널 돼지 목의 측면에 TPN 카테터 피하. 2-0 봉합사로 고정합니다.
- 돼지가 카테콜아민 지원하지 혈역학 적으로 안정된 경우 2 시간 후 동맥 라인을 제거합니다. 구멍 측이 출혈되지 않았는지 확인합니다. 그렇지 않으면, 동맥을 닫지 않고 동맥 구멍 주위에 6-0 지갑 문자열 스티치를합니다. 절개 사이트를 닫습니다.
- 돼지는 독립적으로 숨을 쉴 수있게되면 환기를 중지합니다. 기관 튜브의 환기 튜브를 분리합니다. 돼지가 충분히 호흡 경우 반복적으로 확인합니다.
- 가열 램프를 구비 한 단일 동물 펜에 발생하기 쉬운 위치에 돼지를 놓습니다. Extubate은 돼지 한 번 독립적으로 자신의 머리를 보유 할 수 있습니다. 이 흉골 드러 누움을 유지하기 위해 충분한 의식을 회복 할 때까지 무인 동물을 두지 마십시오. 집 전체 수술 후 기간에 대해 개별적으로 돼지.
- 제공수술 후 충분한 정맥 진통제 (예, 부 프레 노르 핀 0.01-0.05 ㎎을 / kg을 매 6 시간).
- 돼지는 독립적으로 마시지 않는 경우, 충분한 볼륨 IV를 대체
- 면역 억제 등의 메틸 프레드니솔론 (250 mg을 수술 후 하루 (POD) 1 아침 후 125 mg을 매일 아침을) 계속합니다. 에 POD2에서 하루에 두 번 2 ㎎ / ㎏ 포 팔로 스포린 시작합니다.
- 메트로니다졸 500 mg의 회 cefazoline 1,000 ㎎,뿐만 아니라 회까지 POD3 판토 프라 졸 20mg을 관리].
- 밀접하게 돼지를 모니터링합니다. 그것은 고통의 흔적을 보여줍니다 경우를 희생하는 것을 망설이지 말라 (예를 들어, 혼수, refusion는 지속적 산증 또는 저혈당, 또는 출혈이나 복막염의 흔적을 마실). 안락사를 들어, suprahepatic 정맥을 절단하여 깊은 이소 플루 란 마취 (5 %> 2.5 MAC)에서 돼지에게서 피를 뽑다.
결과
첫 번째 이식 연구, 심장 박동 기증자 모델에서 (HBD, N = 5) 현장에서 따뜻한 국소 빈혈의 45 분에 노출 된 DCD 모델 (N = 10)과 비교 하였다. 두 군에서, 이식편은 구매 후 10 시간 동안 얼음 상에 유지 하였다.
HBD 그룹에서받는 사람 돼지의 100 %가 이식 후 5 일에 추적이 끝날 때까지 살아 남았다. DCD 그룹에서받는 돼지의 50 %가 감소 수술 후 간 기능의 결과로서, 응고 문제 또는 대사 부전에 기인 5 일간 생존.
모든 혈액 샘플 중심 정맥 카테터로부터 수거 하였다. 원심 분리 후, 혈청 샘플을 수득하고, 간세포 손상 (아스파 테이트 아미노 트란스 퍼 라제, AST), 담도 함수 (총 빌리루빈 및 알칼리 포스파타제), 및 간 기능 (INR)에 대해 분석 하였다. 5 - 각 마커의 시간 과정은 그림 2에 표시됩니다.
AST 수치는 24 시간 (DCD 그룹의 HBD 그룹의 1414 ± 538 U / L 및 2296 ± 1313 U / L, P = 0.13) 이후에 피크에 도달, 5 일 후에 거의 정상치로 돌아왔다. 마찬가지로, 알칼리 포스파타제 값은 현저 DCD 그룹에서 36 시간 HBD 그룹 (162 ± 54 U / L, p = 0.27)에 비해 (224 ± 111 U / L) 후에 증가 하였다. 총 빌리루빈이 HBD 그룹의 안정적인 동안 (10 μmol에 걸쳐 / L ≤), 서서히 5 일 (23 ± 31 μmol / L, P = 0.43)까지 DCD 그룹에서 증가했다. DCD 그룹의 빌리루빈 값의 큰 표준 편차는이 그룹의 특유의 이질성 담즙 부상을 보여줍니다. 간 기능의 마커로서 INR은 AST 값과 유사한 경향을 보였다. 값은 24 시간에 뾰족 5 일 후 거의 정상 값으로 변경되었다. HBD 그룹 DCD 그룹에 비해 1.47 ± 0.34으로 낮은 피크 값을 가지고 있었다 (피크 1.70 ± 0.36, p = 0.32).
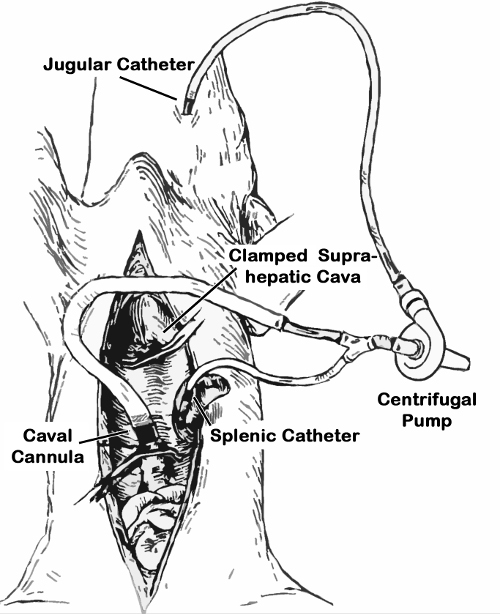
그림 포르토 - 대정맥 - 경정맥 션트 1. 계획. 바이 패스 락 테이트 링거액으로 가득합니다. 그 후 대정맥 부는 튜브 클램프 클램프, 경정맥 및 비장 부를 미리 설정된 카테터에 연결되어 바이 패스가 개방되고, 원심 펌프는 포털 정맥 클램핑 후에 시작된다. 간 절제술 후, 바이 패스의 대정맥 일부가 삽입되고 신장 정맥, infrahepatic 대정맥 밑둥에 두개골 확보했다. 호스 클램프는 포털 신장 이외에 대정맥 감압 있도록 해제된다.
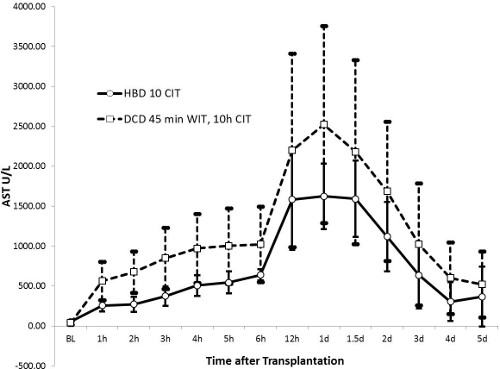
2. 아스 파르 테이트 아미노 전이 효소 (AST)도 (HBD N = 5, DCD를 N = 10). AST는 간세포 손상의 민감한 마커입니다. 피크 후미ER은 24 시간 이하 간 재관류 손상을 시사 DCD 군보다 HBD 낮다; 작은 표준 편차는 HBD 그룹의보다 균일 결과를 나타낸다.
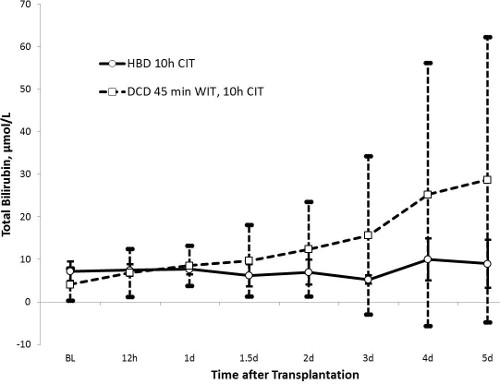
그림 3. 총 빌리루빈 (HBD N = 5, DCD N = 10). 총 빌리루빈은 담즙의 통관 및 담관의 무결성의 마커로, HBD 그룹의 10 μmol / L 이하의 값으로 안정적이고 균일 한 경향을 보여줍니다. DCD 그룹 빌리루빈 곡선은 실험군의 일부만에 담도 부상을 시사 시간에 걸쳐 점진적으로 증가시키고, 높은 표준 편차를 나타낸다.
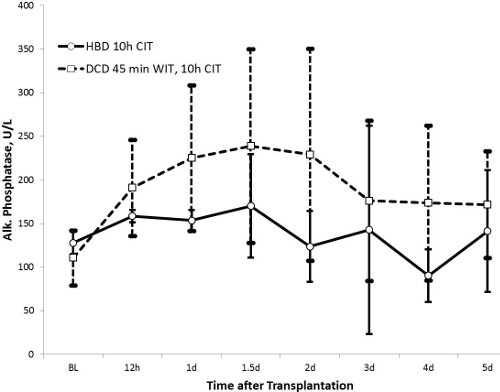
그림 4. 알칼리 포스 파타 아제 (HBD N = 5, DCD N = 10). 알칼리 포스 파타 아제 나담도 손상의 지표를에요. HBD 그룹의 숫자가 적은 담도 부상을 의미 DCD 그룹의 그것보다 낮다.
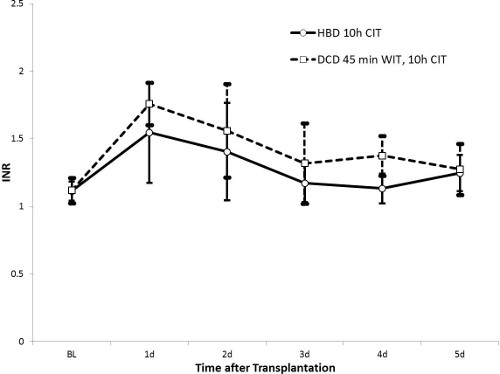
도 5 INR (HBD N = 5, DCD N = 10). INR 높은 값은 응고 인자의 방출을 감소 인해 간세포 감소 기능을 나타낸다. 모두 HBD 및 DCD 그룹, INR 값은 간 기능의 회복을 제안, 오일 이식 후 정상 값으로 돌아갑니다. HBD 그룹의 값은 낮은 나타납니다.
토론
실험 돼지 OLTx은 임상 시나리오의 집중 치료 자원이없는 연구 설정에 대한 도전적인 절차입니다. 가능한 합병증은 혈역학 적 불안정, 출혈, 장기 허혈, 저체온증, 대사뿐만 아니라 호흡기, 부전을 포함한다. 어떤 연구 군의 경우, 수술 기법 5뿐만 아니라 돼지 마취 14,15 충분한 절차 훈련 대표 재현 가능한 결과를 달성하기 위해 필수적이다.
많은 기술적 미묘 특히 혈관 재구성 단계 5에 관한 문헌에 기재되어있다. 위에서 설명한 OLTx 프로토콜은 인간의 OLTx을 닮은 맥 - 대체 모델에 대한 필요한 정보를 제공합니다. 제공된 결과는 모두 HBD 및 DCD 모델에서 신뢰할 수있는 동물의 생존과 이식 복구를 보여줍니다. 프로토콜은 그래프트 expe의 재관류에 사용 단기 생존 시나리오에서 적용될 수있다riments, 예를 들면,뿐만 아니라 내성 연구 장기 생존 모델.
돼지 OLTx 하나의 큰 장애물은 정맥과 문맥 크로스 클램핑의 상대적으로 가난한 허용합니다. anhepatic 단계에서 내장의 정체도 장기 재관류 7 후 돌이킬 수없는 충격의 점에 큰 장 허혈 및 혈역학 적 불안정을 초래할 수 정맥 고혈압과 모세 혈관에 손상을 일으킴. 대정맥 완전히 간 실질에 매립되어 있기 때문에, 카바 보존 피기 백 절차는 가능하지 않다. 정맥 재건 단계에서 대정맥의 총 폐색은 돼지의 혈역학 적 안정성을 손상. 몇몇 보고서 돼지 OLTx 미만 25 분 (16, 17)의 총 정맥과 간문맥 폐색 동안 달성 될 수 있음을 보여준다하더라도, 혈관 재구성 시간 포르토 카바 - 경정맥 바이 패스 기술은 더욱 안전하고 실용적인 옵션 7- 인 9,18. 일에전자 저자의 경험은, 수동적 인 포르토 - 경정맥 바이 패스는 anhepatic 단계에서 안정 돼지 혈역학을 유지하는 최적 없습니다. infrahepatic 정맥과 문맥 모두의 활성 압축 해제를 포함한 바이 패스 모델은, 예기치 못한 합병증도 확장 클램핑 시간 suprahepatic 대정맥과 포털 문합 진정 재건 단계에 있습니다. 포털 우회 카테터가 제거 될 때 초기 리포트 7과는 달리, 비장 절제술은 필수 아니다. 모두 비장 동맥과 정맥은 비장의 길이가 충분히 관류 근위 반을 떠나 함께 중간에 대해 닫혀있다. 때문에 바이 패스 분리에 출혈이나 공기 색전증 등의 합병증은 바이 패스 신중하게 배치하고 적절하게 고정하도록함으로써 피할 수 있습니다.
장기 생존 OLTx 실험에서, 담관 문합으로 인해 높은 합병증 (19)에 약점으로 간주됩니다. 담즙의 조직은 매우 깨지기 및 북동입니다EDS 특별한주의가 때 처리되고. 많은 다른 문합 5,19 기법을 설명 하였다. 엔드 - 투 - 엔드 문합 기술적 쉽고 최소한 19 합병증과 관련된다. peribiliary 결합 조직의 큰 부분을 포함하여 비 절삭 바늘로 연속 봉합이 중단 된 봉합 우수한 것으로 보인다. 단속 봉합 스티치 단일 매듭이 때 담관 불필요한 장력하에 배치된다. 이 조직의 눈물과 연속 담즙 누출의 원인이 될 수 있습니다. 봉합사 - 흡수성 또는 비 흡수성은 - 돼지가 종료 될 때까지 그 수명이 제한을 주어, 일반적으로 중요하지 않다. 몇 개월 이상 장기 생존 모델의 경우, 흡수성 봉합사 - 인간 OLTx에 등이 -이 바람직하다.
특정 치료는 수술 후 추적 관찰에주의해야합니다. 충분한 영양과 유체 공급, 신뢰할 수있는 통증 완화 프로토콜, 그리고 적절한 면역 억제정권은 필수입니다. 장기간 실험을 위해, 면역 억제제는 특히 중요 나타난다. 다른 포유류에 비해 돼지는 OLTx (20, 21) 이후 놀라 울 정도로 낮은 면역 거부 반응 속도를 보여줍니다. 라운드 셀 침투는 이식 후 두 번째 주 동안 최대이며, 심지어 면역 억제하지 않고 자발적으로 감소. 거부는 거의 돼지 OLTx 22 후 사망의 원인입니다. 그러나, 면역 억제 프로토콜이 여기에 언급 관리 스테로이드 IV 및 칼시 뉴린 억제제 포를 포함하여, 이식 거부는 OLTx 후 약 4 일째부터 트랜스 아미나의 온화한 증가에 의해 표시되며 명백한 포털 필드 라운드 세포의 침윤에 의해 확인. 칼시 뉴린 억제제들 중 PO 23,24 또는 25,26 IV 될 수있다; 두 방법 모두 단점이있다. 심지어 구두 응용 프로그램 보조기구, 위장관에 도달하는 실제 금액은 애매 남아있다. 한편, 연속적인 정맥 주입에활성 동물 돼지 펜 어렵다. 따라서, IV 응용 프로그램은 잠재적 인 독성 효과와 함께 높은 약물 농도 피크 결과 러스로 수행해야합니다. 그럼에도 불구하고, 어플리케이션의 두 방법은 장기간의 생존을 허용하도록 나타난다.
임상 환경과 유사하게, 수술 후 스트레스 궤양 예방하는 것이 좋습니다. 소화성 궤양 수술후 출혈 빈번한 문제이며 손상된 간 기능 (27)에 관련 될 수있다. 모두 OLTx 그룹의 위장관 출혈의 몇 가지 경우 후, 저자는 판토 프라 졸과 정기적 인 예방을 시작했고, 그 이후로 어떤 위장관 출혈을 경험하지 않았다.
임상 수술실의 조건에 비해 수술 중 무균 조건, 및 그에 따른 예방 적 항생제의 엄격한 유지 보수, 감염성 합병증의 위험을 감소시킨다.
결론적으로,이 문서에 Provides 연구 환경에서 돼지 OLTx 프로그램을 설정하기위한 실질적인 정보를 제공합니다. 충분한 헌신, 관행 및 팀워크 위해서는, 학습 기간을 감소시키는 신뢰성있는 결과를 생성하기 위해, 비용 및 연구 동물의 수를 줄이기 위해 중요하다.
공개
The authors have nothing to disclose.
감사의 말
The study was supported by research grants from the Roche Organ Transplant Research Foundation (ROTRF) and Astellas. Markus Selzner was supported by an ASTS Career Development Award. Matthias Knaak was supported by the Astellas Research Scholarship. We thank Uwe Mummenhoff and the Birmingham family for their generous support.
자료
| Name | Company | Catalog Number | Comments |
| Atropine Sulphate 15 mg/30ml | Rafter 8 Products | 238481 | |
| Buprenorphine 0.3 mg/ml | RB Pharmaceuticals LDT | N/A | |
| Cefazolin 1 g | Pharmaceutical Partners of Canada Inc. | 2237138 | |
| Cyclosporin Oral Solution 5,000 mg/50 ml | Novartis Pharmaceuticals Canada Inc. | 2150697 | |
| Fentanyl Citrate 0.25 mg/5 ml | Sandoz Canada Inc. | 2240434 | |
| Heparin 10,000 iU/10 ml | Leo Pharma A/S | 453811 | |
| Isoflurane 99.9%, 250 ml | Pharmaceutical Partners of Canada Inc. | 2231929 | |
| Ketamine Hydrochloride 5000 mg/50 ml | Bimeda-MTC Animal Health Inc. | 612316 | |
| Lactated Ringer’s + 5% Dextrose, 0.5 L | Baxter Corporation | 61131 | |
| Lacteted Ringer’s, 1 L | Baxter Corporation | 61085 | |
| Metronidazole 500 mg/100 ml | Baxter Corporation | 870420 | |
| Midazolam 50 mg/10 ml | Pharmaceutical Partners of Canada Inc. | 2242905 | |
| Pantoprazole 40 mg | Sandoz Canada Inc. | 2306727 | |
| Potassium Chloride 40 mEq/20 ml | Hospira Healthcare Corporation | 37869 | |
| Propofol 1,000 mg/100 ml | Pharmascience Inc. | 2244379 | |
| Protamine Sulfate 50 mg/5 ml | Pharmaceutical Partners of Canada Inc. | 2139537 | |
| Saline 0.9%, 1 L | Baxter Corporation | 60208 | |
| Sodium Bicarbonate 50 mEq/50 ml | Hospira Healthcare Corporation | 261998 | |
| Solu-Medrol 500 mg | Pfizer Canada Inc. | 2367963 | |
| Tranexamic Acid 1,000 mg/10 ml | Pfizer Canada Inc. | 2064413 | |
| University of Wisconsin Solution, SPS-1 | Organ Recovery Systems | SPS-1 | |
| Xylocaine Endotracheal 10 mg/50 ml | AstraZeneca | 2003767 | |
| Appose ULC 35 W skin stapler | Covidien Canada | 803712 | |
| Maxon, 1 | Covidien Canada | 606173 | |
| Sofsilk, 0 | Covidien Canada | S606 | |
| Sofsilk, 2-0 | Covidien Canada | S405 | |
| Sofsilk, 3-0 | Covidien Canada | S404 | |
| Surgipro II, 4-0 | Covidien Canada | VP581X | |
| Surgipro II, 5-0 | Covidien Canada | VP725X | |
| Surgipro II, 6-0 | Covidien Canada | VP733X | |
| Catheter i.v, 18 G | BD Canada | 381147 | |
| Cook TPN catheter, 9.5 Fr | Cook Medical Company | C-TPNS-9.5-90 | |
| PSI Kit for sheath catheter, 8.5 Fr | Arrow International | ASK-09803-UHN | |
| Infusion Pump Line | Smith Medical ASD Inc. | 21-0442-25 | |
| Liver Admin Set (flush line) | CardioMed Supplies Inc | 17175 | |
| Mallinckrodt, Tracheal Tube, 6.5 mm | Covidien Canada | 86449 | |
| Med-Rx Suction Connecting Tube | Benlan Inc. | 70-8120 | |
| Organ Bag | CardioMed Supplies Inc | 2990 | |
| Suction Tip | Tyco Healthcare Group LP | 8888501023 | |
| Valleylab, Cautery Pencil | Covidien Canada | E2515H | |
| Valleylab, Patient Return Electrode | Covidien Canada | E7507 | |
| Bypass Connector 3/8” x 1/4“ | Raumedic AG | 955083-001 | |
| Bypass Connector 3/8” x 3/8” Luer Lock | Raumedic AG | 955163-001 | |
| Bypass Connector Y 3/8” x 3/8” x 1/4” | Raumedic AG | 961360-002 | |
| Bypass Tubing 1/4” x 1/16” | Raumedic AG | 039505-010 | |
| Bypass Tubing 3/8” x 3/32” | Raumedic AG | 039535-005 | |
| Rotaflow Centrifugal Pump | Maquet-Dynamed | HC 2821 | |
| Stainless Steel Hose Clamp Ring, 5mm | Oetiker | 16700007 | |
| Abdominal Retractor | Medite GmbH | N/A | |
| De Bakey – Beck, Infrahepatic Cava Clamp | Aesculap Inc. | FB519R | |
| Deithrich, Atraumatic Clamp (Portal Vein) | Aesculap Inc. | FB525R | |
| Gregory Bulldog Clamp, curved | Aesculap Inc. | FB382R | |
| Gregory Bulldog Clamp, straight | Aesculap Inc. | FB381R | |
| Potts – De Martel, Scissors | Aesculap Inc. | BC648R | |
| Satinsky, Suprahepatic Cava Clamp | Aesculap Inc. | FB605R | |
| Symetrical Tubing Clamp | Codman Instruments | 198010 | |
| Anesthesia Machine, Optimax | Moduflex Anesthesia Equipment | SN5180 | |
| Bypass Flow meter, HT 110 | Transonic Systems Inc. | HT110B11106 | |
| Flow meter probe, H6XL | Transonic Systems Inc. | H6Xl689 | |
| Heat Therapy Pump, T/Pump | Gaymar Industries Inc | TP500-G89D19 | |
| Infusion Pump 3,000 | SIMS Graseby LTD. | SN300050447 | |
| Isoflurane Vapor 19.1 | Draeger Medical Canada Inc. | N/A | |
| Monitor, Datex AS 3 | Instrumentarium Corp./ Hitachi | D-VHC14-23-02 | |
| Rotaflow Centrifugal Drive Unit | Maquet-Dynamed | 952301 | |
| Rotaflow Console | Maquet-Dynamed | 706035 | |
| Temperature Therapy Pad | Gaymar Industries Inc | TP26E | |
| Valleylab Force Tx | Valleylab Inc. | 216151480 | |
| Ventilator, AV 800 | DRE Medical Equipment | 40800AVV | |
| Warm Touch, Patient Warming System | Nellcor/ Covidien Canada | 5015300A |
참고문헌
- Mehrabi, A., Fonouni, H., Muller, S. A., Schmidt, J. Current concepts in transplant surgery: liver transplantation today. Langenbecks Arch. Surg. 393 (3), 245-260 (2008).
- Qiu, J., Ozawa, M., Terasaki, P. I. Liver transplantation in the United States. Clin. Transpl. , 17-28 (2005).
- Chalstrey, L. J. Technique of orthotopic liver transplantation in the pig. Br. J. Surg. 58 (3), 585-588 (1971).
- Esmaeilzadeh, M. Technical guidelines for porcine liver allo-transplantation: a review of literature. Ann. Transplant. 17 (2), 101-110 (2012).
- Calne, R. Y. Observations of orthotopic liver transplantation in the pig. Br. Med. J. 2 (5550), 478-480 (1967).
- Memsic, L., Quinones-Baldrich, W., Kaufman, R., Rasool, I., Busuttil, R. W. A comparison of porcine orthotopic liver transplantation using a venous-venous bypass with and without a nonpulsatile perfusion pump. J. Surg. Res. 41, 33-40 (1986).
- Torres, O. J. Hemodynamic alterations during orthotopic liver experimental transplantation in pigs. Acta. Cir. Bras. 23 (2), 135-139 (2008).
- Battersby, C., Hickman, R., Saunders, S. J., Terblanche, J. Liver function in the pig. 1. The effects of 30 minutes' normothermic ischaemia. Br. J. Surg. 61 (1), 27-32 (1974).
- Smith, A. C., Swindle, M. M. Preparation of swine for the laboratory. Ilar. J. 47 (4), 358-363 (2006).
- Swindle, M. M., Smith, A. C. Best practices for performing experimental surgery in swine. J. Invest. Surg. 26 (2), 63-71 (2013).
- Moench, C., Moench, K., Lohse, A. W., Thies, J., Otto, G. Prevention of ischemic-type biliary lesions by arterial back-table pressure perfusion. Liver Transpl. 9 (3), 285-289 (2003).
- Koski, E. M., Suhonen, M., Mattila, M. A. Ultrasound-facilitated central venous cannulation. Crit. Care Med. 20 (3), 424-426 (1992).
- Lange, J. J., Hoitsma, H. F., Meijer, S. Anaesthetic management in experimental orthotopic liver transplantation in the pig. Eur. Surg. Res. 16 (6), 360-365 (1984).
- Kaiser, G. M., Heuer, M. M., Fruhauf, N. R., Kuhne, C. A., Broelsch, C. E. General handling and anesthesia for experimental surgery in pigs. J. Surg. Res. 130 (1), 73-79 (2006).
- Heuer, M. Liver transplantation in swine without venovenous bypass. Eur. Surg. Res. 45 (1), 20-25 (2010).
- Gruttadauria, S. Porcine orthotopic liver autotransplantation: facilitated technique. J. Invest. Surg. 14 (2), 79-82 (2001).
- Falcini, F. Veno-venous bypass in experimental liver transplantation: portal-jugular versus caval-portal-jugular. G. Chir. 11 (4), 206-210 (1990).
- Filipponi, F., Benassai, C., Falcini, F., Martini, E., Cataliotti, L. Biliary tract complications in orthotopic liver transplantation: an experimental study in the pig. Ital. J. Surg. Sci. 19 (2), 131-136 (1989).
- Terblanche, J. Orthotopic liver homotransplantation: an experimental study in the unmodified pig. S. Afr. Med. J. 42 (20), 486-497 (1968).
- Calne, R. Y. Prolonged survival of liver transplants in the pig. Br. Med. J. 4 (5580), 645-648 (1967).
- Battersby, C., Egerton, W. S., Balderson, G., Kerr, J. F., Burnett, W. Another look at rejection in pig liver homografts. Surgery. 76 (4), 617-623 (1974).
- Net, M. The effect of normothermic recirculation is mediated by ischemic preconditioning in NHBD liver transplantation. Am. J. Transplant. 5 (10), 2385-2392 (2005).
- Guarrera, J. V. Hypothermic machine perfusion of liver grafts for transplantation: technical development in human discard and miniature swine models. Transplant Proc. 37 (1), 323-325 (2005).
- Minor, T. Hypothermic reconditioning by gaseous oxygen improves survival after liver transplantation in the pig. Am. J. Transplant. 11 (12), 2627-2634 (2011).
- Kelly, D. M. Porcine partial liver transplantation: a novel model of the 'small-for-size' liver graft. Liver Transpl. 10 (2), 253-263 (2004).
- Meijer, S., Hoitsma, H. F., Visser, J. J., de Lange, J. J. Long term survival following orthotopic liver transplantation in pigs; with special reference to gastric ulcer complications. Neth. J. Surg. 36 (6), 168-171 (1984).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유