このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
Hの測定
要約
A multidimensional gas chromatography method for the analysis of dissolved hydrogen sulfide in liquid crude oil samples is presented. A Deans switch is used to heart-cut light sulfur gases for separation on a secondary column and detection on a sulfur chemiluminescence detector.
要約
原油サンプル中の溶存硫化水素の分析のための方法は、ガスクロマトグラフィーを用いて実証されます。効果的に干渉を除去するために、二次元の列の構成は、第二列(ハートカット)に最初から硫化水素を移送するために用いられるのDeansスイッチで、使用されます。液体の粗サンプルは、最初のジメチルポリシロキサンカラムで分離され、軽いガスは、ハートカット、さらに他の光硫黄種から硫化水素を分離することができる結合した多孔質層オープンチューブラー(PLOT)カラムで分離されています。硫化水素は、次いで、選択の追加の層を追加すること、硫黄化学発光検出器で検出されます。硫化水素の分離および検出に続いて、システムは、粗試料中に存在する高沸点炭化水素を除去し、クロマトグラフィーの完全性を維持するためにバックフラッシュされます。溶存硫化水素は、1.1から500 Pに液体試料中の定量化されています午後には、サンプルの範囲に幅広い適用性を実証します。この方法はまた、正常0.7 9,700 ppmでの硫化水素の測定と、原油のヘッドスペースとプロセスガスバッグからガスサンプルの分析に適用されています。
概要
健康と安全規制と経済は油の品質の関数であるとして、原油の正確な分析は、石油・ガス産業のために不可欠です。粗製のサンプルの輸送を保護するためには、放出または漏出の場合に実施される安全規則を開発するために、粗サンプルの特性を決定する必要があります。具体的には、硫化水素の定量化(H 2 S)が原因で、気相中でその高い毒性のために、重要です。 100 ppmのような低いエクスポージャーは致命的なことができ(http://www.cdc.gov/niosh/idlh/7783064.html)1,2。粗製サンプル中の溶解H 2 Sは、一般的に3,4腐食性であると考えられ、そして油5-7を治療するために用いられる触媒を不活性化することができます。原油からのH 2 Sの除去は、ストリーム理想的であるが、溶解したH 2 Sを測定する方法がなければ、除去処置の成功を評価することは困難です。これらの理由のため、このプロトコルはdissoを測定するために開発されましたこのようなカナダのオイルサンド原油などの重質原油試料中のH 2 SをLVED。
標準的な方法の数は軽い石油又は燃料ベースのサンプル中のH 2 Sの定量化のために存在するが、どれも一般的に、カナダのオイルサンドから抽出された重い原油を使用するために検証されていません。 H 2 Sおよびメルカプタンユニバーサル石油製品(UOP)メソッド163 8によって滴定技術を用いて決定されるが、この方法は、滴定曲線の手動読み取りから得られるユーザ解釈バイアスを被ります。石油(IP)法570の研究所は、燃料油試料9と、シンプルさと携帯性から利益を加熱する専門のH 2 S・アナライザを使用していますが、重いサンプル10と正確さを欠いています。米国材料試験協会(ASTM)方法D5623は、軽油の液体中でのH 2 Sを測定するための極低温冷却および硫黄選択的検出をガスクロマトグラフィー(GC)を使用しています11,12。この規格は、したがって、それは、本明細書で論じるプロトコルの基礎として使用され、周囲の分離を使用するように向上させることができ、また、重い原油に適用します。
GCは、石油試料の分析のために頻繁に使用される技術です。サンプルは、熱い入口で気化され、そして分離は、気相で起こります。それは簡単に入口での加熱時に液体試料から放出されるようなガス相分離は、H 2 Sの分析のためのGC最適です。 GC法が作成され、使用される温度プログラムに応じて、異なるサンプルに合わせて調整、列が実装され、多次元クロマトグラフィー13-15を使用することができます。 GCを用いて、H 2 Sを測定するための最近の発展の数がありました。ルオンら多次元GCおよびディーンズスイッチングを使用して、光と中間留分中のH 2 Sと他の光硫黄化合物の測定値を示したが、この方法ではない持っていますまだ重い原油16に適用され。ディ三蔵らはまた、GCを用いて、ガソリン中のH 2 Sを定量化し、しかし、それはまた、重い原油に使用され、サブ周囲冷却17を必要とされていません。ここで紹介する方法は、10分(ルオン)と40分(ディ三蔵)に比べて、5分の完了分析時間で、これらの従来の方法より節約かなりの時間を示しています。残念ながら、精度を比較するために私たちの研究室でこれらのメソッドの実装が原因で機器や時間の制約することはできませんでした。
多次元GCは、ユーザーが2つの列の選択ではなく、単一の列を利用することができます。従来のGCでは、分離は、1列で発生します。多次元GCの場合には、試料を分離し、選択性を向上させる、二つの異なるカラムで分離されています。学部長のスイッチは、二次元の列構成を採用するために使用される一つの装置です。スイッチは悲惨に外部バルブを使用しています2出口ポート18〜20のいずれかにスイッチ上の入口からCTガス流。最初のカラムからの流出物は、いずれかの方向に向けることができます。この場合、光硫黄ガスは、多孔質層開管の最初の分離から「ハートカット」21 Hの分離に優れていることが示されている二次分離のために(PLOT)カラムである他の光硫黄ガスから2 S (http://www.chem.agilent.com/cag/cabu/pdf/gaspro.pdf)22-24。硫黄化学発光検出器は、硫黄化合物の選択性を提供し、心臓カット中PLOTカラムに転送されていてもよい任意の他の軽質ガスからの干渉の可能性を排除し、検出のために使用されます。原油サンプルからの炭化水素は、第一次元カラムに保持され、バックフラッシュ手順の間に削除されます。これは、任意の汚染25-27からPLOTカラムを保護します。このアプローチは、正常肛門のために実装されています変圧器油28における酸化防止剤のysis。
本明細書において、二次元GC法は、重質原油サンプル中の溶解H 2 Sの分析および定量化のために使用されます。この方法は、H 2 S濃度の広い範囲にわたって適用可能であることが示され、また、気相サンプル中のH 2 Sを測定することができます。
Access restricted. Please log in or start a trial to view this content.
プロトコル
注意:使用する前に、材料に関連するすべての物質安全データシート(MSDS)を参照してください。特に、CS 2は非常に可燃性であり、適切に保存され、処理されるべきです。 H 2 Sガスは非常に毒性があり、かつ任意の容器又はH 2 Sを含むガスバッグを開いたり、正しく通気換気フードの外側で処理されるべきではありません。原油サンプルでの作業は必ず完全個人用保護具(手袋、安全メガネ、白衣、ズボンと閉じたつま先の靴)で行われるべきであり、すべての粗サンプルを換気フードに、オープンした転送して処理する必要があります。認定ガス基準は、有効期限と製造業者から配信され、最も正確な結果のケアのための期限が切れていない基準を使用するように注意する必要があります。
標準の調製
- 標準液
- 自動ピペットを用いて、50 mlのvolumetrに二硫化炭素(CS 2)の10μLを分注しますICフラスコ。 HPLC(高速液体クロマトグラフィー)等級のトルエンで標線までメスフラスコを埋めます。フラスコに蓋をし、5回の最小値を反転して旋回することにより溶液を混合。これは、500 ppmの株式校正ソリューションです。
- 分析の各日には、キャリブレーションのためにCS 2の4バイアルを準備します。 4 1.5ミリリットルのオートサンプラーバイアルにラベルを付け、バイアルトレイに置きます。
- 自動ピペットを用いて、各バイアルに500 ppmのストックCS 2溶液200μlを分注します。第二の自動ピペットを用いて、4バイアルのそれぞれにHPLCグレードのトルエン800μLを分注します。すぐにCS 2、トルエンを分配した後、各バイアルに蓋をし 、混合する3回転倒。これらは、100ppmの校正標準です。
- ガス基準
- 通気換気フードに認定された校正ガスのガスボンベを移動し、ガスバッグに取り付けるための装着されているレギュレータを取り付けます。
- なしを開きます空のガスバッグにzzleガスボンベのレギュレータにガスバッグを取り付けます。
- レギュレータを閉じた状態で、上部反時計回りにノブを回して、ガスボンベを開きます。
- ガスの定常流がガス袋をいっぱいになるまで反時計回りにレギュレータのノブを回します。ガスバッグがいっぱいになると、ガスの流れを遮断するために、レギュレータのノブを時計回りに回します。
- ガスバッグにノズルを閉じて、レギュレータからそれを切り離します。トップ時計回りにノブを回して、ガスボンベを閉じます。残りのガスをパージし、レギュレータは、もはやそれに任意のガスを持っているときに再びそれを閉じていない、圧力を解放するために、レギュレータを開きます。
2.機器セットアップ
- メソッドのパラメータ
- 以下の手順を使用して、各システムが固有の圧力設定になりますように学部長は、ガスクロマトグラフに設置列に応じて切り替えて設定します。
- 計算上のDeansスイッチ電卓プログラムを開きます R、入力カラム寸法、キャリアガス、温度、使用する所望の流量及び検出器( 図1参照 )【選択演算部は、入口と、圧力制御モジュール(PCM)のために必要な圧力を定義し、リストリクタチューブの長さが必要とされます学部長スイッチ及び炎イオン化検出器(FID)の間に設置しました。これらの圧力およびメソッドファイルに入力してください。
- ディーンズスイッチの計算からの情報および表1に記載されている情報は、プログラム気体または液体の分析のいずれかの適切なパラメータを持つメソッドファイルを使用します。メソッドファイルを保存します。
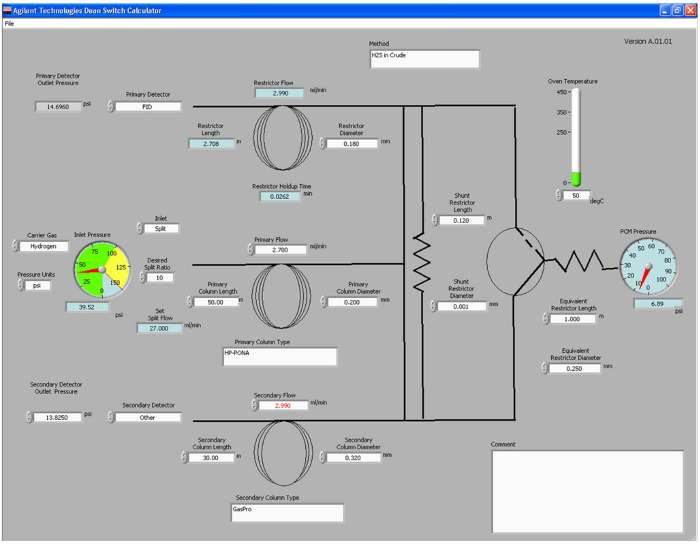
図1.ディーンズは、電卓を切り替える。学部長のスクリーンショットは、電卓プログラムを切り替えます。ユーザ調整可能なパラメータは、ホワイトボックスに示されており、出力パラメータは、青色のボックスに示されています。EF = "https://www.jove.com/files/ftp_upload/53416/53416fig1large.jpg"ターゲット= "_空白">この図の拡大版をご覧になるにはこちらをクリックしてください。
- 列のインストール
- 楽器、オーブンや注入口はRTであることを確認してください。ディーンズスイッチへの入口とPCM供給流れへのガス流をオフにします。
- 製造元の指示に従うことで、スプリット/スプリットレス注入口とディーンズスイッチ、ディーンズ間のPLOTカラムスイッチと硫黄化学発光検出器(SCD)、およびリストリクタチューブ(ステップ2.1.2で決定された長さ)の間にジメチルポリシロキサンカラムをインストールディーンズスイッチとFID。
- ガスクロマトグラフのソフトウェアを使用して、注入口およびPCMへのキャリアガスの流れをオンにし、各列の端部に及び学部長スイッチで継手に近接して、電子漏れ検出器を通過させることにより、リークのためのシステムをテストします。リークはDETに光および/または音の通知で示されていますエクター。
- 漏れがある場合は、ゆっくり電子漏れ検出器でフィッティングし、再テストを締めます。オーブンのドアを閉じ、ガスクロマトグラフオーブンや注入口ヒーターをオンにします。
- (カラムのドキュメントにあります)PLOTカラムの温度上限にオーブン温度を上昇させることによってカラムとリストリクタチューブのベークアウトを実行します。オーブンは3時間この温度で最低座ってすることができます。
- ベークアウトが完了すると、必要に応じて締め付け、電子漏れ検出器を備えたガス漏れをRT、オーブン内部の再テスト接続にオーブンを冷却します。
- ガスクロマトグラフを制御するソフトウェアを使用して、事前にプログラムされたメソッドファイルをロードします。機器は、分析のための準備ができています。

図2.ガスクロマトグラフオーブン。ConfiguratiGCオーブン内の列配置の上。 FID:炎イオン化検出器、SCD:硫黄化学発光検出器は、 この図の拡大版をご覧になるにはこちらをクリックしてください。
- 適切ディーンズスイッチタイミングの決定
- ディーンズスイッチはガスクロマトグラフにおけるバルブによって制御されます。メソッドのパラメータのバルブタイミング点セクションを見つけます。ソフトウェアでは、「オン」にスイッチを設定し、バルブが再度の「上に」0.5分の「オフ」、およびバルブを回す第2のイベントを回すから始まる、ディーンズスイッチを制御するバルブの時間イベントを作成3.0分。本明細書では「オフ」位置は、カラム流出液は、SCDに搬送される方向に対応します。
- 、換気フード中で(ヘリウム中でH 2 Sの量を知られている)校正ガスを含むガスバッグを配置そして、ガスバッグのノズルにゴム製の乳首または同等の浸透性カバーを配置します。ガスバッグにノズルを開きます。
- 250μlの気密ガラスシリンジを使用して、袋の上にゴム製の乳首を穿刺し、校正ガスの250μLを撤回。入口隔膜を注射器に蓋をし、ガスクロマトグラフに注射器を運びます。
- シリンジからセプタムキャップを外します。手動で迅速に同時にソフト取得を開始する、ガスクロマトグラフに校正ガスを注入します。 H 2 Sは、SCDの信号トレースのピークとして表示されます。このピークの保持時間を記録します。 。
- 、ハートカットウィンドウの時間を短縮開始時に1つの側面( すなわち、連続的な注射用の0.1分によってイベント「オン」バルブを減少させます)。 H 2 Sのピークがクロマトグラムから消失するまで、このように続けています。この時に0.2分を追加し、ハートカットウィンドウの上限として、それを注意してください。
- PERFピークが見えなくなるまで徐々に連続的な注射用バルブ「オフ」イベントの時間を増加させない、時間ウィンドウの下端に同じ手順をORM。この時点から0.2分を減算し、ハートカットウィンドウの下限とそれを注意してください。
- /「オン」と「オフ」バルブを保存する方法ファイルにコマンド。
3.装置のキャリブレーション
- 液体
- 液体オートサンプラは、ガスクロマトグラフのスプリット/スプリットレス注入口にインストールされていることを確認してください。オートサンプラトレイにバイアル位置1-4で4以前に作成した検量バイアルを置きます。
- ガラスピペットを用いて、HPLCグレードトルエンでバイアルを充填し、オートサンプラトレイの洗浄溶媒用バイアルの位置に配置します。オートサンプラトレイの廃棄物のバイアルまたはリザーバが空であることを確認してください。
- この方法は、ガスクロマトに接続されているソフトウェアの液相分析用に設定された負荷しますグラフ;両検出器が上とガスクロマトグラフがレディ状態であることになっていることを確認してください。
- この方法によれば、バイアルごとに1つの注入を行い、ガスクロマトグラフに付属のソフトウェアを使用して、各クロマトグラムでのCS 2ピークを統合するために、ガスクロマトグラフソフトウェアを使用してください。
- 表計算プログラムを使用して、キャリブレーション溶液(100ppm以下)の濃度によってCS 2ピークの面積数を除算し、次に硫黄の原子当たりの応答を与えるために2で、これを分割することによりSCDの平均応答ファクターを計算します。
- ガス
- 液体オートサンプラ塔は、ガスクロマトグラフから削除されたことを確認し、ガス分析のための適切な方法をロードします。両検出器の電源が入っていること、およびガスクロマトグラフがレディ状態にあることを確認してください。
- 2.3.4へのステップ2.3.2で説明したように校正ガスを注入します。
- 校正ガスAの手動注入を繰り返し3回の最小。
- Hを3回の注射で2 Sのピークを統合すると、表計算プログラムを使用して、Hの濃度によってH 2 Sのピークの平均面積を分割することによってH 2 Sの平均応答ファクターを計算するために、ガスクロマトグラフのデータ分析ソフトウェアを使用ガスバッグ内の2 S。
4.サンプル分析
- 液体
- ガラスピペットを用いて、少量(<1 ml)を転送することによって、注射のための原油を評価します。粗生成物をガラスピペットに残っ有意な残基で転送された場合、粗生成物をニート注入することができます。粗生成物をガラスピペットでかなりの量を残す場合4.1.2に記載したように、希釈します。きちんと注入することができる原油、ガスクロマトグラフのオートサンプラーバイアルに原油の〜1ミリリットルを転送し、バイアルをキャップ。
- 、オートサンプラーバイアルに自動ピペットで原油の0.75ミリリットルを転送することにより、高粘度原油を希釈ND HPLCグレードのトルエンの等量を添加します。十分に溶液を混合するために振とうしながら、バイアルをキャップし、反転します。
- オートサンプラートレイに充填したバイアルを配置し、ガスクロマトグラフのソフトウェア上の液体の分析方法をロードします。
- ガスクロマトグラフのソフトウェアと以前に設定した方法( 表1)を使用して 、バイアルごとに3つの繰り返し注入を実行するためにオートサンプラを使用しています。
- ガス
- 頭隙
- 分析しようとする原油の450ミリリットルと500ミリリットル琥珀色のガラス瓶を埋めます。ボトルの上部にセプタム張りのキャップを取り付けます。通気換気フード内の任意の粗転送手順を実行します。
- 温度制御された環境(30℃で、すなわち、水浴)で分析するボトル(複数可)を置きます。注:原油サンプルが使用されたサンプルに応じて行使されるべきで高温とケアで揮発性になることがあります。
- 1 mlのガラス製ガスタイトシリンジを用いて、穿刺セプタムトップとヘッドスペース内のガスを構築する必要がある場合は圧力解放のための手段を提供するために、ボトルの上部に注射器を残します。
- 軽く液体とヘッドスペースとの間でのH 2 Sを平衡化時間後にボトルを持ち上げると揺れ、24時間、温度制御された環境でボトル(複数可)のままにしておきます。
- ヘッドスペースガスを分析するために、セプタムトップを穿刺し、気密ガラスシリンジにガスのμLを撤回。
- 入口セプタムの切れ端でシリンジの端をキャップとガスクロマトグラフに注射器を運びます。手動で迅速に同時にデータ収集を開始するためのソフトウェアを起動し、注入口にガスを注入します。
- ガスの3反復注入の最小値を取得するには、この手順を繰り返します。 H 2 Sのピークがあまりにも濃厚ではなく、検出器の規模である場合、スケールのピークを持って来るためにガスの小さい注射器での手順を実行します( 図3参照 ); 私は。E。、100μlあるいは25μlの。
- ガスバッグ
- 分析すべきガスバッグのノズルにゴム製の乳首または同等の浸透性カバーを配置し、通気換気フードにガスバッグを配置します。
- ガス分析のための適切な方法は、ガスクロマトグラフのソフトウェアにロードされていることを確認し、ガスクロマトグラフの準備ができた状態であること。
- ガスバッグにノズルを開き、250μlのガスタイトシリンジでニップルの上部に穴を開ける。ガスの250μlのシリンジを埋める、注射器を撤回し、ガスバッグにノズルを閉じます。
- 入口セプタムの切れ端でシリンジの端をキャップとガスクロマトグラフに注射器を輸送し、手動で同時にデータ収集を開始するためのソフトウェアを起動し、入口にガスを注入します。
- ガスの3反復注入の最小値を取得するには、この手順を繰り返します。 H 2 Sのピークの濃度が濃すぎると検出器の規模ではない場合(複数可EE 図3)、規模でピークをもたらすためにガスの小さい注射器での手順を実行し、すなわち、100μlあるいは25μlの。
- 頭隙
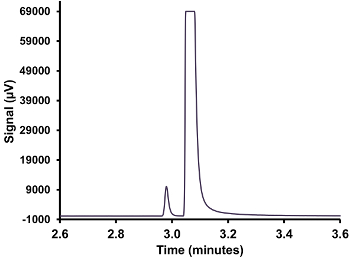
図3.過負荷状態のH 2 Sのピークとガスクロマトグラム。30℃に保持された液体粗試料のヘッドスペースからガス注入、SCDの過負荷を証明している。 この図の拡大版をご覧になるにはこちらをクリックしてください。
5.データ解析
- 液体
- H 2 Sのピーク保持時間を決定する(だけ繰り返す必要が機器構成が変更された場合)
- ノーない液体の粗でのGCオートサンプラーバイアルを埋めるためにガラスピペットを使用してくださいT希釈を必要とし、バイアルをキャップ。
- ガスクロマトグラフのソフトウェア上の液体の分析のために適切なメソッドをロードし、液体オートサンプラ塔が設置されていることを確認。
- オートサンプラートレイに液体粗試料を置き、原油の一回の注射を行います。
- H 2 S含有ガス(ヘリウム中の2.5%)の750μlのガラスガスタイトシリンジを埋めます。オートサンプラートレイからバイアルを取り外し、ガスが充填された注射器でバイアルのキャップにセプタムを穿刺し、バイアル内の試料の表面下の注射器の端部に配置します。粗試料を通って泡にガスを注射器のプランジャーを押し下げます。
- バックオートサンプラトレイにバイアルを置き、スパイクサンプルの単回注射を行うためにオートサンプラーを指示するためにソフトウェアを使用しています。
- ガスクロマトグラフに付随するソフトウェアを使用して、H 2 Sスパイク前後のクロマトグラムを比較します。大きなピークは、事前にする必要があります最初のクロマトグラムには存在しなかった第二のクロマトグラムで送信されました。このピークの保持時間を記録する( 図4参照)。
- 分析
- H 2 S(ステップ5.1.1.6で述べた保持時間を使用して同定する)は、各クロマトグラムにおいて( 図5)のピーク面積を積分し、各サンプルについての平均ピーク面積を計算するためにガスクロマトグラフに付随するデータ分析ソフトウェアを使用スプレッドシートプログラム。
- 3.1節で求めた応答因子を使用して、PPMに存在するH 2 Sの量を与える応答係数によってサンプルの平均ピーク面積を分割します。希釈したサンプルについて、希釈されていないサンプル( 図6)中のH 2 Sの量を与えるために適切な希釈係数により濃度を掛けます。
- H 2 Sのピーク保持時間を決定する(だけ繰り返す必要が機器構成が変更された場合)
/ "/ 53416 / 53416fig4.jpgをアップロード>
H 2 S 2つは変化を示すクロマトグラムは、H 2 Sとの粗試料をスパイクするとき期待重ねて図4.原油サンプルがスパイク 、この図の拡大版をご覧になるにはこちらをクリックしてください。
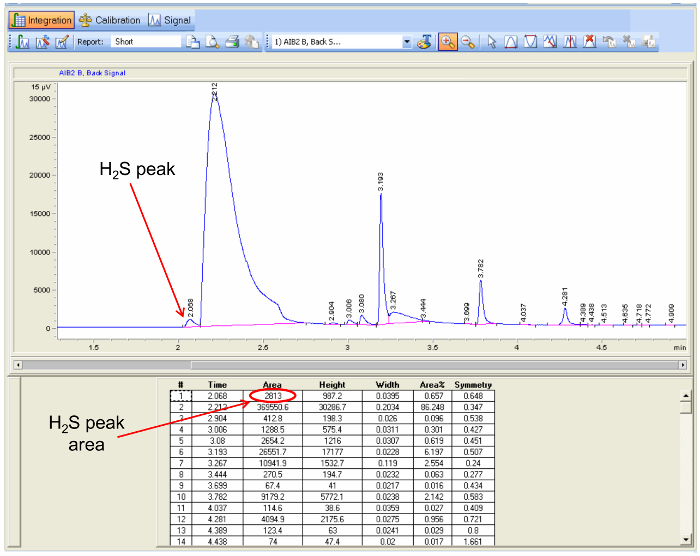
図5.ガスクロマトグラムデータ解析のH 2 Sの濃度を決定するために使用される試料とピーク面積中のH 2 Sのピークの位置を強調し、データ解析プログラムの。スクリーンショット拡大表示するにはここをクリックしてくださいこの図のバージョン。彼をクリックしてくださいこの図の拡大版を表示するために再。
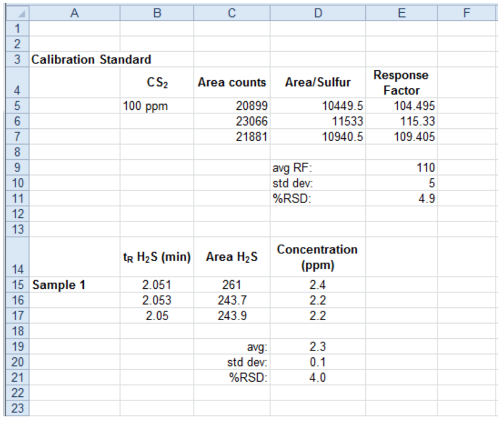
データ分析のための図6.サンプルスプレッドシート。キャリブレーション標準のピークの面積と試料ピークの面積を用いて、H 2 Sの濃度を計算する方法の例を示す表計算プログラムのスクリーンショット。 ご覧になるにはこちらをクリックしてくださいこの図の拡大版。
- ガス
- 3.2節で校正するために使用されるH 2 Sのピークの保持時間を一致させることによって、各クロマトグラム中のH 2 Sのピークを特定します。
- 収集されたデータにそれぞれH 2 Sのピークのピーク面積を積分し、各試料の平均ピーク面積を計算するためにガスクロマトグラフに付随するデータ分析ソフトウェアを使用。
- 応答因子determinを使用edは3.2で、ppm単位の存在するH 2 Sの量を与える応答係数による試料の平均ピーク面積を分割します。 250μlのシリンジ中に存在するH 2 Sの量を与えるために適切な希釈係数により濃度を掛け、小さいシリンジ容量を用いた試料(すなわち、(250μL/ 25μLシリンジ25μL)。
Access restricted. Please log in or start a trial to view this content.
結果
液体と気体の両方のサンプルについてのH 2 Sの信頼性のある定量化を得るために、適切なキャリブレーションが必要です。キャリブレーションの注射とサンプル注入のために、H 2 Sのピークは、隣接するピークと重複するべきではなく、再現性のピーク面積を持っている必要があります。 図3ガスは、この方法はあまりにも集中している気体試料の注入を示してい?...
Access restricted. Please log in or start a trial to view this content.
ディスカッション
H 2 Sの最適な測定を達成するために、この方法は、学部長スイッチ、バックフラッシュおよび硫黄化学発光検出器(SCD)を用います。ジメチルポリシロキサンカラムは、一次元GCカラムとして使用され、それらはPLOTカラムを汚染しないように、試料中に存在する重質炭化水素の移動を遅延させる働きをします。この効果は、クール(50°C)最初の分離によって強化されます。ライトガ...
Access restricted. Please log in or start a trial to view this content.
開示事項
The authors have nothing to disclose.
謝辞
The authors would like to acknowledge support from the Government of Canada's interdepartmental Program of Energy Research and Development, PERD 113, Petroleum Conversion for Cleaner Air. N.E.H would like to acknowledge her Natural Sciences and Engineering Research Council of Canada Visiting Fellowship.
Access restricted. Please log in or start a trial to view this content.
資料
| Name | Company | Catalog Number | Comments |
| Deans switch | Agilent | G2855A | Or equivalent flow switching device |
| Restrictor tubing | Agilent | 160-2615-10 | Fused silica, deactivated, 180 µm |
| HP-PONA column | Agilent | 19091S-001 | |
| GasPro column | Agilent | 113-4332 | |
| Sulfur chemiluminescence detector, 355 | Agilent/Sievers | G6603A | |
| H2S calibration standard, in He | Air Liquide | Custom order | 211 ppm H2S |
| CS2 | Fisher Scientific | C184-500 | |
| Toluene, HPLC grade | Fisher Scientific | T290-4 | |
| Gas bag, 2 L | Calibrated Instruments, Inc. | GSB-P/2 | Twist on/off nozzle |
| 250 µl gas tight syringe | Hamilton | 81130 | |
| 500 ml amber glass bottle | Scientific Specialties | N73616 | |
| Open top screw caps | Scientific Specialties | 169628 | |
| Tegrabond disc for screw caps | Chromatographic Specialties | C889125C | 25 mm, 10/90 MIL |
| 1 ml gas tight syringe | Hamilton | 81330 | |
| 2.5% H2S in He gas standard | Air Liquide | Custom order |
参考文献
- Guidotti, T. L. Hydrogen sulphide. Occ. Med. 46, 367-371 (1996).
- Reiffenstein, R. J., Hulbert, W. C., Roth, S. H. Toxicology of Hydrogen Sulfide. Annu. Rev. Pharmacol. Toxicol. , 109-134 (1992).
- Qi, Y., et al. Effect of Temperature on the Corrosion Behavior of Carbon Steel in Hydrogen Sulphide Environments. Int. J. Electrochem. Sci. 9, 2101-2112 (2014).
- Ma, H., et al. The influence of hydrogen sulfide on corrosion of iron under different conditions. Corros. Sci. 42, 1669-1683 (2000).
- Kallinikos, L. E., Jess, A., Papayannakos, N. G. Kinetic study and H2S effect on refractory DBTs desulfurization in a heavy gasoil. J. Catal. 269, 169-178 (2010).
- Liu, B., et al. Kinetic investigation of the effect of H2S in the hydrodesulfurization of FCC gasoline. Fuel. 123, 43-51 (2014).
- Si, X., Xia, D., Xiang, Y., Zhou, Y. Effect of H2S on the transformation of 1-hexene over NiMoS/γ-Al2O3 with hydrogen. J. Nat. Gas Chem. 19, 185-188 (2010).
- Hydrogen Sulfide and Mercaptan Sulfur in Liquid Hydrocarbons by Potentiometric Titration. , ASTM International. West Conshohocken, PA. UOP 163-10(2010).
- Standard Test Method for Determination of Hydrogen Sulfide in Fuel Oils by Rapid Liquid Phase Extraction. , ASTM International. West Conshohocken, PA. ASTM D7621-10(2010).
- Lywood, W. G., Murray, D. H2S in Crude Measurement Report. , Canadian Crude Quality Technical Association. (2012).
- Standard Test Method for Sulfur Compounds in Light Petroleum Liquids by Gas Chromatography and Sulfur Selective Detection. , ASTM International. West Conshohocken, PA. ASTM D7621-10(2009).
- Liu, W., Morales, M. Detection of Sulfur Compounds According to ASTM D5623 in Gasoline with Agilent's Dual Plasma Sulfur Chemiluminescence Detector (G6603A) and an Agilent 7890A Gas Chromatograph. , Agilent Technologies. (2008).
- Barman, B. N., Cebolla, V. L., Membrado, L. Chromatographic Techniques for Petroleum and Related Products. Crit. Rev. Anal. Chem. 30, 75-120 (2000).
- Rodgers, R. P., McKenna, A. M. Petroleum Analysis. Anal. Chem. 83, 4665-4687 (2011).
- Nizio, K. D., McGinitie, T. M., Harynuk, J. J. Comprehensive multidimensional separations for the analysis of petroleum. J. Chromatogr. A. 1255, 12-23 (2012).
- Luong, J., Gras, R., Shellie, R. A., Cortes, H. J. Tandem sulfur chemiluminescence and flame ionization detection with planar microfluidic devices for the characterization of sulfur compounds in hydrocarbon matrices. J. Chromatogr. A. 1297, 231-235 (2013).
- Di Sanzo, F. P., Bray, W., Chawla, B. Determination of the Sulfur Components of Gasoline Streams by Capillary Column Gas Chromatography with Sulfur Chemiluminescence Detection. J. High Res. Chromatog. 17, 255-258 (1994).
- Deans, D. R. A new technique for heart cutting in gas chromatography. Chromatographia. 1, 18-22 (1968).
- Hinshaw, J. V. Valves for Gas Chromatography, Part III: Fluidic Switching Applications. LC GC N. Am. 29, 988-994 (2011).
- Seeley, J. V., Micyus, N. J., Bandurski, S. V., Seeley, S. K., McCurry, J. D. Microfluidic Deans Switch for Comprehensive Two-Dimensional Gas Chromatography. Anal. Chem. 79, 1840-1847 (2007).
- Tranchida, P. Q., Sciarrone, D., Dugo, P., Mondello, L. Heart-cutting multidimensional gas chromatography: A review of recent evolution, applications, and future prospects. Anal. Chim. Acta. 716, 66-75 (2012).
- Armstrong, D. W., Reid, G. L. III, Luong, J. Gas Separations: A Comparison of GasPro™ and Aluminum Oxide PLOT Columns for the Separation of Highly Volatile Compounds. Curr. Sep. 15, 5-11 (1996).
- Ellis, J., Vickers, A. K., George, C. Capillary Column Selectivity and Inertness for Sulfur Gas Analysis in Light Hydrocarbon Streams by Gas Chromatography. Fuel Chemistry Division Preprints. 47, 703-704 (2002).
- Ji, Z., Majors, R. E., Guthrie, E. J. Porous layer open-tubular capillary columns: preparations, applications and future directions. J. Chromatogr. A. 842, 115-142 (1999).
- Luong, J., Gras, R., Shellie, R. A., Cortes, H. J. Applications of planar microfluidic devices and gas chromatography for complex problem solving. J. Sep. Sci. 36, 182-191 (2013).
- Hildmann, F., Kempe, G., Speer, K. Application of the precolumn back-flush technology in pesticide residue analysis: A practical view. J. Sep. Sci. 36, 2128-2135 (2013).
- Gray, B. P., Teale, P. The use of a simple backflush technology to improve sample throughput and system robustness in routine gas chromatography tandem mass spectrometry analysis of doping control samples. J. Chromatogr. A. 1217, 4749-4752 (2010).
- Hayward, T., Gras, R., Luong, J. Characterization of selected oxidation inhibitors in transformer oils by multidimensional gas chromatography with capillary flow technology. Anal. Methods. 6, 8136-8140 (2014).
- Hutte, R. S., Johansen, N. G., Legier, M. F. Column Selection and Optimization for Sulfur Compound Analyses by Gas Chromatography. J. High Res. Chromatog. 13, 421-426 (1990).
- Yan, X. Unique selective detectors for gas chromatography: Nitrogen and sulfur chemiluminescence detectors. J. Sep. Sci. 29, 1931-1945 (2006).
- Araujo, P. Key aspects of analytical method validation and linearity evaluation. J. Chromatogr. B. 877, 2224-2234 (2009).
Access restricted. Please log in or start a trial to view this content.
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved