Method Article
아실 염화물과 칼륨 Alkynyltrifluoroborate 소금에서 Ynones의 금속이 합성
요약
The goal of this manuscript is to demonstrate a straightforward method for the preparation of ynones from acyl chloride and potassium alkynyltrifluoroborate salt starting materials. The one-pot reaction proceeds rapidly in the presence of boron trichloride without exclusion of air and moisture.
초록
Ynones are a valuable functional group and building block in organic synthesis. Ynones serve as a precursor to many important organic functional groups and scaffolds. Traditional methods for the preparation of ynones are associated with drawbacks including harsh conditions, multiple purification steps, and the presence of unwanted byproducts. An alternative method for the straightforward preparation of ynones from acyl chlorides and potassium alkynyltrifluoroborate salts is described herein. The adoption of organotrifluoroborate salts as an alternative to organometallic reagents for the formation of new carbon-carbon bonds has a number of advantages. Potassium organotrifluoroborate salts are shelf stable, have good functional group tolerance, low toxicity, and a wide variety are straightforward to prepare. The title reaction proceeds rapidly at ambient temperature in the presence of a Lewis acid without the exclusion of air and moisture. Fair to excellent yields may be obtained via reaction of various aryl and alkyl acid chlorides with alkynyltrifluoroborate salts in the presence of boron trichloride.
서문
The intention of this video is to demonstrate a straightforward approach for the preparation of compounds containing an ynone functional group from convenient starting materials. Ynones are valuable building blocks in organic chemistry that have been shown to have biomedical and material significance. Ynones are precursors to valuable organic functional groups including pyrimidines,1,2 quinolones,3 furans,4 pyrazoles,5,6 flavones,7 oximes,8 and chiral propargylic alcohols.9-11 A more convenient method for the preparation of ynones has been sought as a result of the drawbacks of traditional methods including poor functional group tolerance and tedious synthetic routes.
The reaction of metal12,13 and metalloid14 acetylides with acyl chlorides is one common route for the preparation of ynones. Alternatively, the synthesis of ynones from acyl chloride can be achieved via two-step procedures using Weinreb amides and organolithium or Grignard reagents.15 Another prevalent approach includes the addition of organolithium or Grignard reagents to an aldehyde, which is followed by the oxidation of a secondary alcohol to the corresponding ketone.16-19 Poor functional group tolerance of metal acetylides and the need to purify synthetic intermediates after each step are main deficiencies of the aforementioned methods. Transition-metal-catalyzed carbonylative couplings have recently emerged as an alternative approach for the preparation of ynones.20-22 Unfortunately, in addition to cost and toxicity associated with transition metals, metal-catalyzed carbonylative reactions often require elevated CO pressures and suffer from the presence of an undesired Sonogashira coupling byproduct. Given their utility in organic synthesis as well as the drawbacks associated with traditional synthetic methods, the development of a more straightforward method for the preparation of ynones is appealing.
Potassium organotrifluoroborate salts have recently emerged as versatile reagents in organic synthesis. Advantages including ease of preparation,23 inherent stability, low toxicity, and good functional group tolerance have made organotrifluoroborate salts attractive synthetic reagents.24-27 Organotrifluoroborate salts have been used primarily as a bench-stable equivalent of boronic acids for palladium-catalyzed Suzuki-Miyaura coupling.26 Recently, following a seminal work by Matteson and co-workers,28 Bode, Molander and others have highlighted the utility of organotrifluoroborates as reagents in non-metal catalyzed reactions.29-33 The field of transition-metal-free reactions of trifluoroborates is still in its infancy stage. Given the great potential for use of organotrifluoroborate salts in non-metal catalyzed organic synthesis, we sought to develop a novel method for the preparation of ynones from acyl chlorides and alkynyltrifluoroborate salts.
프로토콜
Ynone 1. 합성
- 분석 저울을 사용하여, 원하는 alkynyltrifluoroborate 칼륨 염 (1.5 당량) 0.15 밀리몰 무게 및 자기 교반 막대가 장착 된 깨끗한 유리 병에 추가.
- 트리 플루오의 0.3 M 용액을 수득 바이알에 무수 DCM 0.5를 가하여, 바늘 장착 된 유리 플런저 주사기를 사용.
주 :이 새로운 방법이기 때문에, 반응이 개념의 증거에 대해 수행되었다. 폐기물을 감소시키기 위해 그들 소규모로 수행되었다. 반응은 필요에 따라 더 큰 수익률을 생산하기 위해 확장 할 수 있습니다. - 유리 주사기를 사용하여 교반하면서 주위 온도 (20 ℃)에서 반응 용기에 1.0 M 삼염화 붕소 용액 0.15 밀리몰 (1.5 당량, 150 μL) 적가 하였다. 캡을 교체합니다. 홀드 또는 반응 용액을 초음파 처리기에 흘수선 아래에 오도록 캡핑 반응 용기 클램프. 20 ° C에서 30 초 동안 용액 및 주파수 O 초음파 처리F 40 kHz에서.
- 추가로 20 분 동안 실온 (20 ℃ 온도)에서 반응 용액을 교반 하였다. alkynyltrifluoroborate 출발 물질의 특성에 따라 색의 변화를 관찰한다. 황갈색에 흰색 또는 짙은 갈색, 빨강, 또는 보라색의 색상 변화는 일반적입니다.
- 교반하면서 주위 온도에서 약병 (20 ° C)에 원하는 아실 클로라이드 (1.0 당량)의 0.1 밀리몰 추가. 대안 적으로, 자기 교반 막대로 충전 플라스크에, 반응 용기의 내용을 전송하여 아실 클로라이드 0.1 밀리몰. 캡을 교체합니다. 30 분 동안 상온 (20 ° C에서)에서 반응 용액을 교반 하였다.
주 : 일반적으로, 매우 어두운 색 변화는 반응이 일어나는 지표이다. - 박층 크로마토 그래피 (TLC) (34)를 사용하여 적절한 아실 클로라이드 표준 비교함으로써 반응의 진행을 감시한다.
주 : 출발 물질의 특성에 따라서는, 반응물을 마칠 수 없다.CYL 클로라이드 출발 물질이 방법을 사용하여 현재까지 제조 ynones의 모든 최종 생성물보다 높은 주행 반점이 관찰되었다.- 작은 유리 병에 1 ㎖의 에틸 아세테이트로 출발 물질 아실 클로라이드의 약 10 ㎎을 희석하여 아실 클로라이드 표준을 준비한다.
- 감시인 TLC를 사용하여 TLC 플레이트의 시작 라인에서 반응 액에 표준 스팟. 반응 용액 및 표준 모두 공동 스폿은 여전히 반응 액에 존재하는 출발 물질이 존재 하는지를 판정하는 데 유용 할 수있다.
- 시행 착오에 의해 적당한 TLC 이동상을 결정합니다. 제품 (1A)의 제조를위한, 이동상 1:30 에틸 아세테이트로 이루어진 : ynone 생성물 및 염화 벤조일을 약 0.5 내지 0.8의 R의 F 값에 헥산 결과 각각 출발 물질.
- UV 빛 아래 개발 된 TLC 판을 시각화. 눈에 보이는 지점을 표시하기 위해 연필을 사용합니다.
2. 수성 후
- 반응 용기에 차가운 물 (대략 41 ° C)의 1 ml에 첨가하여 반응을 켄 칭하고. 파스퇴르 피펫을 사용하여, 깨끗한 용액을 분리 깔때기에 옮긴다. 또한, 10 ml의 냉수로 분리 깔때기의 내용물을 희석시키고, 15 ml의 에틸 아세테이트로 한 번 생성물을 추출한다.
- 하부 수층을 버리고 물 10 ㎖ 및 염수 10 mL로 1 회 유기층을 추가 1 회 세척 하였다. 깨끗한 삼각 플라스크에 유기층을 수집하고 황산 마그네슘으로 건조. 중력 여과하여 깨끗한 둥근 바닥 플라스크에 넣고 용액을 필터.
Ynone 3. 정제
- 박층 크로마토 그래피를 사용하여 생성물의 플래쉬 크로마토 그래피 정제를위한 적합한 이동상을 결정한다. 약 0.5의 고정 요소 (R의 F)는 나머지 개시로부터 생성물을 분리하는 것은 일반적으로 충분재료와면 제품을 보내고.
참고 제품 저급 R의 F 값을 가지고 분리 불량의 경우, 덜 극성 인 용매 계 등을 사용할 수있다. 1 ~ 5 : 30의 범위에있는 혼합물을 에틸 아세테이트 : 출발 물질, 헥산의 극성에 따라 한 것은 일반적으로 적합하다. - 적절한 이동상 젖은 열 포함 된 실리카를 준비합니다. 제품 및 용리액의 첨가시 교란 실리카을 방지하기 위해 칼럼의 상부에 모래의 층을 추가한다.
- 40 ° C에서의 욕 온도 및 120 rpm으로 설정된 회전 회전 증발기를 사용하여 후 처리 액을 증발시켰다. 이동상 2 mL에 플라스크의 내용물을 조심스럽게 용해시키고 컬럼 상 균일 용액을로드. 실리카이 젖어 있지만, 용매 라인은 실리카의 높이를 초과하지 않도록하십시오. 일부 용매 제품 실리카상에서 용출되도록 허용. 모바일 위상과 반복의 작은 금액을 추가합니다.
- COL 채우기3.1 단계에서 결정된 이동상과 UMN; 제품 (1A)의 경우, 30 : 1의 헥산 : 에틸 아세테이트 혼합물을 적절하다. 정제 공정의 속도를 플래쉬 크로마토 그래피를 사용하여 시험관에서 분획을 수집한다. 단순히 공기 배출구에 튜브와 어댑터를 연결합니다. 용리액 적당한 속도로 컬럼을 통해 흐르도록 공기 압력을 조정한다.
- TLC 플레이트 상 컬럼 분획의 각 스팟. 선택적으로, 기준으로서 아실 클로라이드 표준 자리. 이동상 단계 1.8에서 적절하다고 사용하여 TLC를 개발한다. 생성물을 아실 클로라이드 표준보다 낮은 R f를이 예상되는 것을주의 UV 광 하에서 눈에 보이는 반점이있는 표시한다.
- 큰 둥근 바닥 플라스크에 보이는 관광 명소를 포함하는 모든 분수를 수집합니다. 출발 물질보다 낮은 R f를 가진 두 개 이상의 지점이 존재하는 경우, 별도의 플라스크에서 그들을 모은다. 회전 증발기를 사용하여 용매를 증발시키고, 운데 수집 재료를 건조2 시간 동안 높은 진공 r에.
- 필요한 경우, 더 열악한 전자 아실 클로라이드 출발 물질로부터 제조 ynone 생성물을 정제하기 위해 작은 열에 펜탄 세척을 수행한다. 소규모, 이는 열로 파스퇴르 피펫을 이용하여 수행 될 수있다.
- 펜탄 습식 실리카 컬럼 상 클로로포름, DCM, 또는 디 에틸 에테르의 최소 하중에 생성물을 용해시키고. 용출 1-2 칼럼 칼럼을 통해 펜탄 길이와 폐기물 비이커에 모은다.
- 디 에틸 에테르 또는 에틸 아세테이트를 사용하여 칼럼으로부터 펜탄 ynone 순수한 생성물을 용리시킨다. 별도의 플라스크에서 용리액을 증발시켜 수집하고, 2 시간 이상 동안 고 진공하에 놓는다. NMR 분광법에 의한 특성화를 위해 제품의 약 10 mg을 얻었다.
Ynone 4. 특성
- 특성화 1 H, 13 C NMR 분광법을 이용하여 최종 생성물의 순도를 평가. 34일반적으로, 카르 보닐 탄소의 화학적 이동은 13 C NMR 스펙트럼의 177 ppm의 근처에 나타난다. ynone 기능 그룹의 두 SP 탄소 87, 93 ppm의 근처 특성 피크로 표시됩니다.
- ynone 생성물의 특성 카보 닐 피크를 식별하기 위해 적외선 분광기 (34)를 사용한다. 인접 삼중 결합으로부터 전자 비편 재화 보통 보닐 피크가 1,600 내지 1,650cm을 표시 -1, 전자 화합물의 특성에 따라 발생.
- 생성물의 분자량을 결정하고 또 고해상도 질량 분석기를 이용하여 신원을 검증한다. 34
결과
초기의 노력은 페닐 아세틸렌 트리 플루오 S1 및 벤조일 클로라이드 (도 1)로부터 ynone (1a)의 제조 주위 집중 하였다. 표 1은 최적화 단계는 다양한 루이스 산, 용매뿐만 아니라, 반응에 물의 효과 시험 스크리닝 포함 행한다 도시 . 이어서, 반응의 범주는 아실 클로라이드의 다양한 존재 (도 2)에서 최적화 된 조건에 톡시 메틸 트리 플루오로 페닐 아세틸렌을 제출 탐구되었다. 우수한 수율 디스트는 아실 클로라이드 기판의 특성에 따라 획득 될 수있다. 반응의 범위는 상기 alkynyltrifluoroborate 염의 몇몇 추가적인 예시의 제조를 통해 평가되었다. (3)가 발전 조건 하에서 ynones의 제조에 사용될 수있는 다른 alkynyltrifluoroborate 염의 선택된 예를 도시한다. 중독의 파생 상품alkynyltrifluoroborate 염 지방족 유도체는 약간 덜 반응 수득 겸손 수익률 것으로 판명 동안 우수한 수율 좋은에서 해당 ynone 제품을 여유 치환기를 기부 메틸 트리 플루오로 베어링 전자 ylacetylene.
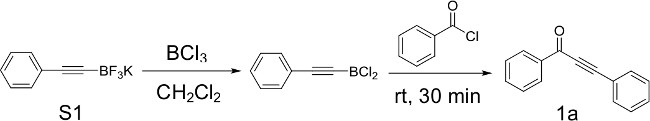
도 1 :. dichloroborane 반응성 중간체의 형성을 포함 ynone (1a)의 제조 조건을 나타내는 페닐 아세틸렌 및 메틸 트리 플루오로 벤조일 클로라이드 S1 스킴 Ynone (1a)의 제조.
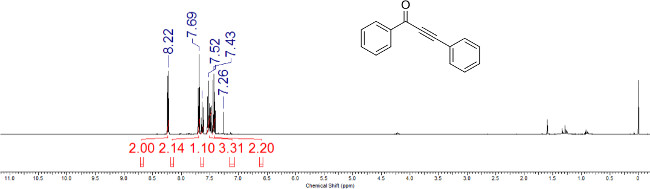
그림 2 :. ynone (1a)의 대표 1 H NMR 스펙트럼 화학 변화와 특성 양자의 상대적 통합이 표시되어 있습니다.
: FO 아가씨 = "jove_content" 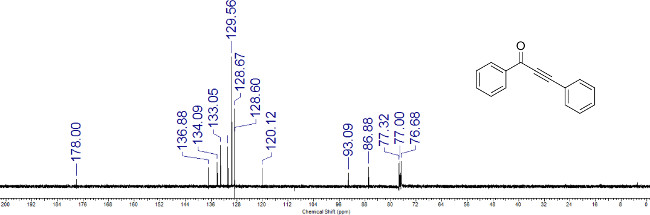
그림 3 :. ynone (1a)의 대표 (13) C NMR 스펙트럼 특성 탄소의 화학적 이동이 표시되어 있습니다.
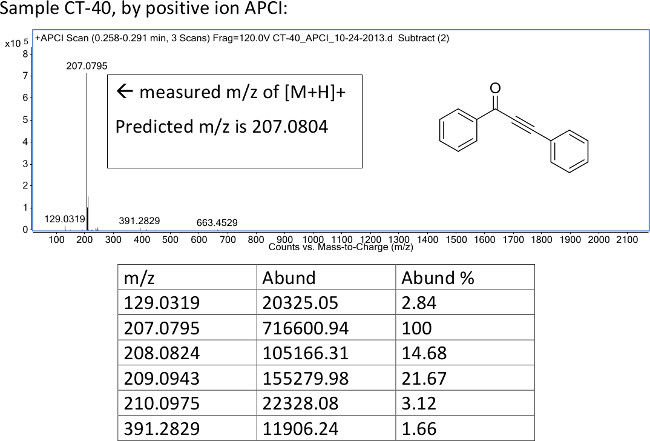
도 4 :. 대기압 화학적 이온화를 통해 얻어진 ynone (1a)의 주제 스펙트럼 HRMS [M + H]의 측정 된 m / z 값 + 이온이보고된다.
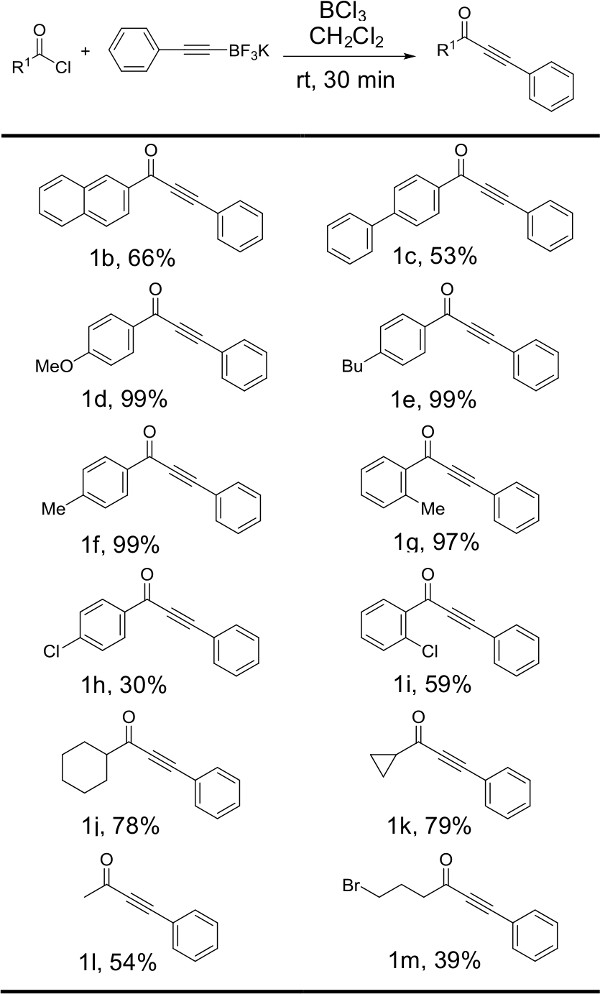
그림 5 : 정체성을 변화시켜 생산 된 제품에 대한 아실 클로라이드와 phenylacetylenetrifluoroborate 소금 S1의 반응 구조 및 수익률.아실 클로라이드 출발 물질로 설명된다. 반응은 아실 클로라이드 1 당량, 1.5 당량의 칼륨 phenylacetylenetrifluoroborate S1, 및 1.5 당량의 삼염화 붕소를 사용하여 실행 하였다.
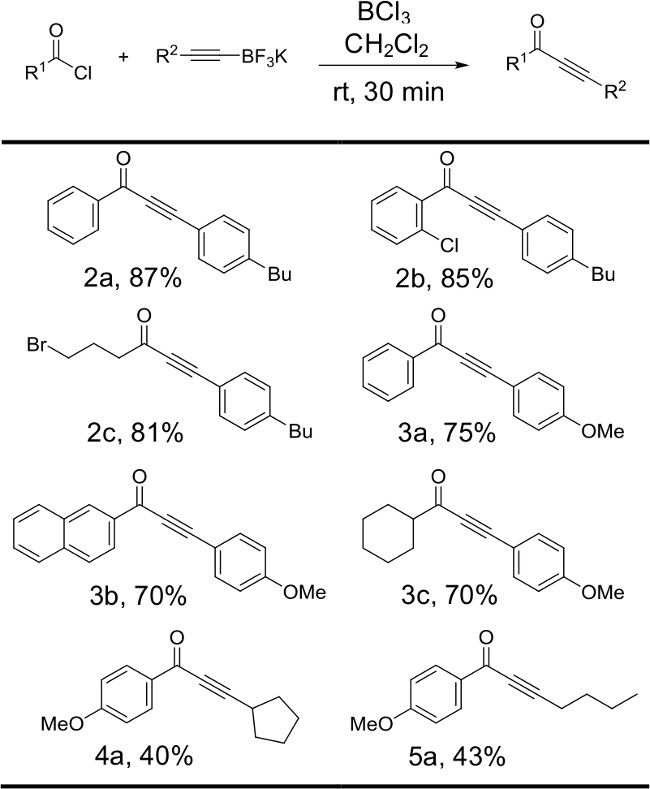
도 6 :. 아실 클로라이드 구조 alkynyltrifluoroborate 출발 물질의 신원을 변화시켜 제조 된 제품의 수율과 다양 alkynyltrifluoroborates의 반응이 예시된다. 반응은 아실 클로라이드 1 당량, 2.5 당량 칼륨 organotrifluoroborate 소금과 2.5 당량 삼염화 붕소 실행되었다.
| 기입 | 루이스 산 | 루이스 산 (당량) | 조건 | 수율 (%) |
| 1 B </ SUP> | 그런가 2 | 16.5 | CH 2 CL 2 | 0 |
| 이 | SiCl4를 | (1) | CH 2 CL 2 | 자취 |
| 3 | BF 3 · OET 2 | (1) | CH 2 CL 2 | 자취 |
| 4 B | 50ml을 | (1) | CH 2 CL 2 | (24) |
| 5 ℃ | 의 AlCl 3 | (1) | CH 2 CL 2 | (62) |
| 6 D | 의 AlCl 3 | (1) | CH 2 CL 2 | (66) |
| 7 전자 | 의 AlCl 3 | (1) | CH 2 CL 2 | (60) |
| 8 | 의 AlCl 3 | (1) | THF | 자취 |
| 9 | 의 AlCl 3 | (1) | 톨루엔 | 자취 |
| (10) | 의 AlCl 3 | 이 | ClCH 2 CH 2 CL | (33) |
| (11) | 의 AlCl 3 | (1) | DMSO | 자취 |
| (12) | 의 AlCl 3 | 이 | 아세토 니트릴 | 자취 |
| (13) | 의 AlCl 3 · 6H 2 O | (1) | CH 2 CL 2 | 0 |
| (14) (B) | BCL 3 | 1.5 | CH 2 CL 2 | 67 |
| (15) | BBR 3 | (1) | CH 2 CL 2 | (20) |
표 1 :. 생성물 ynone 1A는 (A)의 제조 조건의 최적화 수율 반응 조건 및 루이스 산 촉매의 변동에 따라도 1a. 반응은 1 당량 벤조일 클로라이드 및 1 당량 칼륨 phenylacetylenetrifluoroborate (S1)에 수행 하였다. 1.5 당량의 S1 ㄴ. C 무수 조건. D 반응물 공기 하에서 비 - 건조 된 유리기구에서 수행 하였다. 예를 무수 조건 + 물 1 μL.
토론
표 1은 대응 ynone 생성물을 형성 벤조일 클로라이드와 메틸 트리 플루오로 페닐 아세틸렌의 반응 조건을 최적화하기 위해 취해지는 단계를 도시한다. 처음에 organodifluoroboranes organotrifluoroborates 변환 공지 촉매 시험 하였다. 불행히도 실리카겔, 사염화 규소 35, 36, 31, 32, 삼 불화 붕소 원하는 ynone의 형성 (표 1, 항목 1-3)을 촉진하지 않았다. 증명 염소화 루이스 산 촉매의 사용은 더 성공적한다. 원하는 ynone (1a)의 낮은 수율은 철 (III) 클로라이드 촉매 (표 1, 항목 4)의 존재를 얻었다. 다음에, 알루미늄 (III) 클로라이드가 프리델 - 크래프트 (Friedel-Crafts)의 아 실화에 oxocarbenium 이온 형성을 촉진하기 위해 그 노포 능력의 결과로서 조사 하였다. 알루미늄 (III) 클로라이드 촉매 때 37-39 목적 생성물을 62 % 수율로 수득 하였다 EMPloyed.
또한 최적화는 공기와 수분이 반응의 수율 (표 1, 항목 5-7)에 거의 영향을 미칠 것으로 나타났다. 결과적으로, 후속 반응은 공기의 존재 하에서 비 - 건조 된 유리기구에서 수행 하였다. 용매를 최적화하기위한 시도는 디클로로 메탄 (DCM)을 반응 (표 1, 엔트리 8-12)에 특히 적합 않은 것을 확인했다. 알루미늄 (III) 클로라이드에 의해 촉매 반응의 결과 불일치 대체 촉매의 탐사를 자극했다. 시판의 알루미늄 (III) 클로라이드 수화물은 반응 조건 (표 1, 항목 13)에서 완전히 불활성이었다. 이것은 알루미늄 (III) 클로라이드 수화물의 형성이 반응을 저해하는 것이 좋은 지표이다. 삼염화 붕소는 더 일관성 (표 1, 항목 14)와 유사한 수율을 생산하는 것으로 확인되었다.
칼륨의 상호 작용시 alkynyltriflu삼염화 붕소와 oroborate는 organodichloroborane 이상의 반응성 종을 형성한다. (40)이 초기 단계를 진행할 ynone의 아실 클로라이드와 반응 형성에 중요하다. organotrifluoroborate 염을 DCM에 용해되지 않기 때문에, 반응은 이종 혼합물로 이루어진다. 삼염화 붕소의 첨가 후, 반응 용액을 메틸 트리 플루오로 할 수 염의 표면적을 증가시킴으로써 dichloroborane 반응성 종의 형성을 촉진하기 위하여 초음파 처리를한다. 반응 혼합물에 초음파의 적용은 캐비테이션 기포의 발생을 통한 기계적인 효과를 야기한다. 초음파 동안, 캐비테이션의 붕괴는 높은 온도와 압력의 지역화 된 영역에서 유체 결과에 거품. (41) 충격 파도 고체 메틸 트리 플루오로 소금의 운동 에너지의 증가의 결과로 미세 난류를 만드는 것이 생산된다. 초음파 프로모션 기간 동안 시스템의 에너지의 증가트리 플루오로 보레이트 염 TES 조각화 삼염화 붕소와 상호 작용할 가능한 표면적을 증가 얻어진. 종래 아실 클로라이드 출발 물질의 첨가로 반응 혼합물을 초음파 처리 더 강제 조건이나 반응 시간을 길게 할 필요없이 alkynyldichloroborane 반응성 종의 효율적인 형성을 보장한다.
도 2는 메틸 트리 플루오로 페닐 아세틸렌은 최적 반응 조건 하에서 아실 클로라이드와 반응시켜 다양한 때 얻어지는 결과가 보여준다. 중립 방향족 (1B, 1C)과 지방족 (1J-1) 아실 염화물 합성 유용 수익률에 해당 ynones를 제출. 전자 구인 그룹이 비교적 완만 한 금리 (1H, 1I, 1m) 발생하면서 전자 기부 그룹에게 (1D-g)가있는 그 아실 클로라이드는 우수한 수익률을 제공합니다. Intere전자 흡인 성기가 오르토 위치 (1I, 59 %)에 위치 될 때 stingly, 상당한 수율 증가가 유사한 파라 비교 관찰은 아실 클로라이드 (1H, 30 %) 치환. 오르토 위치의 치환기의 입체 상호 작용함으로써, 방향족 고리의 전자 회수 특성을 상쇄 평면으로부터 카보 닐 작용기를 강제 할 수있다. 그것은 4 bromobutyryl 클로라이드 39 % 수율의 목적 생성물을 수득 1m 반응 것을 주목할 가치가있다. 우리가 알기로는,이 알킬 브로마이드 관능기를 견딜 ynones의 합성을위한 제 1 프로토콜이다. 출발 물질 아실 클로라이드는 중성 또는 전자 결핍 때 때때로 지방족 불순물 양성자 NMR에 나타난다. 이는 상기 생성물을 정제하기 위해 펜탄 세척을 필요로 할 수있다. 가능한 반면, 제 정화 단계 중에 S 펜탄 세척을 수행하는 경제적이지 못하다인스 펜탄, 헥산에 비해 비용이 많이 든다. 이러한 파스퇴르 피펫 컬럼으로 작은 규모 별도로 이차 정제를 완료하면 상당히 요구 펜탄의 양을 감소시킨다.
도 3은 반응의 수율에 alkynyltrifluoroborate 염의 신원 효과를 나타낸 것이다. 일반적으로, 방향족 고리상의 메틸 트리 플루오로 페닐 아세틸렌 염 베어링 전자공 여성 치환기의 유도체는 우수한 수율 (C-2A, 3A-C)으로 좋은에서 원하는 ynones을 생산하는 방향족 및 지방족 아실 클로라이드와 반응시켰다. 지방족 alkynyltrifluoroborate 염은 반응성이 적은 기판 것을 입증했다. hexynyl- 및 cyclopentylethynyltrifluoroborate 염 전자 풍부한 벤조일 클로라이드 유도체 (4A, 5A)와 반응했을 때 겸손 금리가 얻어졌다.
결론적으로, 제제 O위한 신규 한 방법에있어서F 아실 염화 칼륨 alkynyltrifluoroborate 염에서 ynones이 개발되었다. 적당한에서 아실 클로라이드의 성질에 따라,이 방법에 우수한 대별 ynones의 합성에 대해 얻어진 수율은 출발 물질 트리 플루오. 일반적으로 전자 공 여성 치환기를 갖는 화합물에 관한 출발 물질과 전자 구인 중성 작용기를 함유 출발 물질보다 더욱 용이하게 반응을 겪는다. 이 접근법의 값은 방법의 단순한 작동 및 관능기 공차에있다. 이 간단, 원 - 포트 (one-pot) 반응은 공기 및 습기의 배제없이 삼염화 붕소의 존재하에 주위 온도에서 신속하게 진행한다. 이 편리한 방법은 아실 클로라이드와 alkynyltrifluoroborate 다양한 염들로부터 우수한 수율로 완만 ynones의 제조에 사용될 수있다.
공개
The authors declare that they have no competing financial interests.
감사의 말
This work was supported by the UOIT start-up fund. We thank Mr. Matthew Baxter (UOIT) for his assistance in the laboratory.
자료
| Name | Company | Catalog Number | Comments |
| Sonicator | VGT | 1860QT | Ultrasonic cleaner. Similar sonication devices may be used. |
| Dichloromethane | Sigma | 270997 | Anhydrous |
| Boron trichloride solution | Sigma | 178934 | 1 M solution in DCM |
| Acyl chloride | Sigma | Various | Acyl chlorides from other suppliers such as Alfa Aesar may be used. Caution: refer to MSDS for safety information. |
| Potassium alkynyltrifluoroborate salt | N/A | N/A | Synthesized23 from terminal alkyne |
| Ethyl acetate | ACP | E-2000 | ACS grade |
| Hexanes | ACP | H-3500 | ACS grade |
| Pentane | Sigma | 236705 | Anhydrous |
| Magnesium sulfate | Sigma | M7506 | |
| Filter paper | Whatman | 1093 126 | Student grade. This speceific variety is not necessary. |
| Silica Gel 60 | EMD | 1.11567.9026 | Particle size 0.040-0.063 |
참고문헌
- Bannwarth, P., Valleix, A., Grée, D., Grée, R. Flexible Synthesis of Pyrimidines with Chiral Monofluorinated and Difluoromethyl Side Chains. J. Org. Chem. 74, 4646-4649 (2009).
- Karpov, A. S., Merkul, E., Rominger, F., Müller, T. J. Concise Syntheses of Meridianins by Carbonylative Alkynylation and a Four‐Component Pyrimidine Synthesis. Angew. Chem. Int. Ed. 44, 6951-6956 (2005).
- Arcadi, A., Aschi, M., Marinelli, F., Verdecchia, M. Pd-catalyzed regioselective hydroarylation of α-(2-aminoaryl)-α, β-ynones with organoboron derivatives as a tool for the synthesis of quinolines: experimental evidence and quantum-chemical calculations. Tetrahedron. 64, 5354-5361 (2008).
- Lee, C. G., Lee, K. Y., Lee, S., Kim, J. N. Chemical transformation of Baylis–Hillman adducts: the reaction of methyl 3-arylamino-2-methylene-3-phenylpropanoates in polyphosphoric acid. Tetrahedron. 61, 1493-1499 (2005).
- Kirkham, J. D., Edeson, S. J., Stokes, S., Harrity, J. P. Synthesis of Ynone Trifluoroborates toward Functionalized Pyrazoles. Org. Lett. 14, 5354-5357 (2012).
- Mohamed Ahmed, M. S., Kobayashi, K., Mori, A. One-pot construction of pyrazoles and isoxazoles with palladium-catalyzed four-component coupling. Org. Lett. 7, 4487-4489 (2005).
- Awuah, E., Capretta, A. Access to Flavones via a Microwave-Assisted, One-Pot Sonogashira− Carbonylation− Annulation Reaction. Org. Lett. 11, 3210-3213 (2009).
- She, Z., et al. Synthesis of Trisubstituted Isoxazoles by Palladium (II)-Catalyzed Cascade Cyclization–Alkenylation of 2-Alkyn-1-one O-Methyl Oximes. J. Org. Chem. 77, 3627-3633 (2012).
- Corey, E., Helal, C. J. Novel electronic effects of remote substituents on the oxazaborolidine-catalyzed enantioselective reduction of ketones. Tetrahedron Lett. 36, 9153-9156 (1995).
- Matsumura, K., Hashiguchi, S., Ikariya, T., Noyori, R. Asymmetric transfer hydrogenation of α, β-acetylenic ketones. J. Am. Chem. Soc. 119, 8738-8739 (1997).
- Midland, M. M., McDowell, D. C., Hatch, R. L., Tramontano, A. Reduction of. alpha.,. beta.-acetylenic ketones with B-3-pinanyl-9-borabicyclo [3.3. 1] nonane. High asymmetric induction in aliphatic systems. J. Am. Chem. Soc. 102, 867-869 (1980).
- Logue, M. W., Moore, G. L. Cuprous trimethylsilylacetylide. Preparation and reaction with acid chlorides. J. Org. Chem. 40, 131-132 (1975).
- Normant, J. Organocopper (I) Compounds and Organocuprates in Synthesis. Synthesis. , 63-80 (1972).
- Logue, M. W., Teng, K. Palladium-catalyzed reactions of acyl chlorides with (1-alkynyl) tributylstannanes. A convenient synthesis for 1-alkynyl ketones. J. Org. Chem. 47, 2549-2553 (1982).
- Nahm, S., Weinreb, S. M. N-Methoxy-N-methylamides as effective acylating agents. Tetrahedron Lett. 22, 3815-3818 (1981).
- Baba, T., Kizuka, H., Handa, H., Ono, Y. Reaction of ketones or aldehydes with 1-alkynes over solid-base catalysts. Appl. Catal., A. 194, 203-211 (2000).
- Brown, H. C., Garg, C. P. A simple procedure for the chromic acid oxidation of alcohols to ketones of high purity. J. Am. Chem. Soc. 83, 2952-2953 (1961).
- Nishimura, T., Onoue, T., Ohe, K., Uemura, S. Palladium (II)-catalyzed oxidation of alcohols to aldehydes and ketones by molecular oxygen. J. Org. Chem. 64, 6750-6755 (1999).
- Pu, L. Asymmetric alkynylzinc additions to aldehydes and ketones. Tetrahedron. 59, 9873-9886 (2003).
- Kim, W., Park, K., Park, A., Choe, J., Lee, S. Pd-Catalyzed Selective Carbonylative and Non-carbonylative Couplings of Propiolic Acid: One-Pot Synthesis of Diarylalkynones. Org. Lett. 15, 1654-1657 (2013).
- Kobayashi, T., Tanaka, M., Sakakura, T. Palladium(ii) Complex-catalysed Formation of a-Keto Acids via Double Carbonylation of Organic. Halides J. Chem. Soc., Chem. Commun. , 837-838 (1985).
- Mohamed Ahmed, M. S., Mori, A. Carbonylative Sonogashira coupling of terminal alkynes with aqueous ammonia. Org. Lett. 5, 3057-3060 (2003).
- Vieira, A. S., et al. Nucleophilic Addition of Potassium Alkynyltrifluoroborates to d-Glucal Mediated by BF3· OEt2: Highly Stereoselective Synthesis of α-C-glycosides. Org. Lett. 10, 5215-5218 (2008).
- Darses, S., Genet, J. -. P. Potassium organotrifluoroborates: new perspectives in organic synthesis. Chem. Rev. 108, 288-325 (2008).
- Darses, S., Genet, J. P. Potassium trifluoro (organo) borates: new perspectives in organic chemistry. Eur. J. Org. Chem. 2003, 4313-4327 (2003).
- Molander, G. A., Ellis, N. Organotrifluoroborates: Protected Boronic Acids That Expand the Versatility of the Suzuki Coupling Reaction. Acc. Chem. Res. 40, 275-286 (2007).
- Stefani, H. A., Cella, R., Vieira, A. S. Recent advances in organotrifluoroborates chemistry. Tetrahedron. 63, 3623-3658 (2007).
- Matteson, D. S., Kim, G. Y. Asymmetric alkyldifluoroboranes and their use in secondary amine synthesis. Org. Lett. 4, 2153-2155 (2002).
- Dumas, A. M., Bode, J. W. . Synthesis of Acyltrifluoroborates. Org. Lett. 14, 2138-2141 (2012).
- Dumas, A. M., Molander, G. A., Bode, J. W. Amide‐Forming Ligation of Acyltrifluoroborates and Hydroxylamines in Water. Angew. Chem. Int. Ed. 51, 5683-5686 (2012).
- Mitchell, T. A., Bode, J. W. Synthesis of Dialkyl Ethers from Organotrifluoroborates and Acetals. J. Am. Chem. Soc. 131, 18057-18059 (2009).
- Vo, C. -. V. T., Mitchell, T. A., Bode, J. W. Expanded substrate scope and improved reactivity of ether-forming cross-coupling reactions of organotrifluoroborates and acetals. J. Am. Chem. Soc. 133, 14082-14089 (2011).
- Zeng, J., Vedachalam, S., Xiang, S., Liu, X. -. W. Direct C-Glycosylation of Organotrifluoroborates with Glycosyl Fluorides and Its Application to the Total Synthesis of (+)-Varitriol. Org. Lett. 13, 42-45 (2010).
- Lehman, J. W. The student's lab companion: laboratory techniques for organic chemistry: standard scale and microscale. Pearson College Div. , (2008).
- Molander, G. A., Cavalcanti, L. N., Canturk, B., Pan, P. -. S., Kennedy, L. E. Efficient Hydrolysis of Organotrifluoroborates via Silica Gel and Water. 74, 7364-7369 (2009).
- Molander, G. A., Ellis, N. Organotrifluoroborates: protected boronic acids that expand the versatility of the Suzuki coupling reaction. Acc. Chem. Res. 40, 275-286 (2007).
- Calloway, N. The Friedel-Crafts Syntheses. Chem. Rev. 17, 327-392 (1935).
- Gore, P. The Friedel-Crafts acylation reaction and its application to polycyclic aromatic hydrocarbons. Chem. Rev. 55, 229-281 (1955).
- Groves, J. The Friedel–Crafts acylation of alkenes. Chem. Soc. Rev. 1, 73-97 (1972).
- Kim, B. J., Matteson, D. S. Conversion of alkyltrifluoroborates into alkyldichloroboranes with tetrachlorosilane in coordinating solvents. Angew. Chem. 116, 3118-3120 (2004).
- Thompson, L., Doraiswamy, L. Sonochemistry: science and engineering. Ind. Eng. Chem. Res. 38, 1215-1249 (1999).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유