Method Article
마우스의 분절 대퇴 임계 크기 결함 모델의 설립은 플레이트 고정술에 의해 안정화
요약
Although mouse models are invaluable tools for bone tissue engineering, models of long bone defects are sparse. This need motivated development of the present protocol which uses a locking plate with four screws and a dedicated jig to perform and stabilize a reproducible, femoral, critical-size defect with low morbidity.
초록
The use of tissue-engineered bone constructs is an appealing strategy to overcome drawbacks of autografts for the treatment of massive bone defects. As a model organism, the mouse has already been widely used in bone-related research. Large diaphyseal bone defect models in mice, however, are sparse and often use bone fixation which fills the bone marrow cavity and does not provide optimal mechanical stability. The objectives of the current study were to develop a critical-size, segmental, femoral defect in nude mice. A 3.5-mm mid-diaphyseal femoral ostectomy (approximately 25% of the femur length) was performed using a dedicated jig, and was stabilized with an anterior located locking plate and 4 locking screws. The bone defect was subsequently either left empty or filled with a bone substitute (syngenic bone graft or coralline scaffold). Bone healing was monitored noninvasively using radiography and in vivo micro-computed-tomography and was subsequently assessed by ex vivo micro-computed-tomography and undecalcified histology after animal sacrifice, 10 weeks postoperatively. The recovery of all mice was excellent, a full-weight-bearing was observed within one day following the surgical procedure. Furthermore, stable bone fixation and consistent fixation of the implanted materials were achieved in all animals tested throughout the study. When the bone defects were left empty, non-union was consistently obtained. In contrast, when the bone defects were filled with syngenic bone grafts, bone union was always observed. When the bone defects were filled with coralline scaffolds, newly-formed bone was observed in the interface between bone resection edges and the scaffold, as well as within a short distance within the scaffold.
The present model describes a reproducible critical-size femoral defect stabilized by plate osteosynthesis with low morbidity in mice. The new load-bearing segmental bone defect model could be useful for studying the underlying mechanisms in bone regeneration pertinent to orthopaedic applications.
서문
대규모 골간 골 결손은 정형 외과 의사에게 큰 도전입니다. 현재 금 표준 치료로 간주자가 골 이식과 골 교체, 제한된 공급에 수확 관련 사망률과 관련이있다. 이러한 이유로 osteoconductive 지지체 골수 간엽 줄기 세포를 결합 조직 공학 뼈 구조는 정형 외과에서자가 이식을위한 대안으로 탐구하고있다.
현재까지 대부분의 연구 등 (예 : 개, 돼지, 양, 1-3 만, 작은 동물 모델에서 소성을, 분절, 임계 크기 골 결손 이러한 구조의 예비 평가 임상 적 관련 동물 모델에서 수행 된 생쥐)는 여러 가지 장점 수 : 동물의 다수가 조작 될 수있다 (II) (I) 낮은 비용; (ⅲ) 대형 동물 모델에 대하여, 마우스 균주 균질성 골격 흡수 A의 각각의 변화를 제한ND 골 형성하고; (IV)가 가장 중요한 특정 항체 및 유전자 대상 동물의 가용성은 뼈의 치유에 관여하는 생물학적 과정의 평가를 할 수 있습니다. 마지막으로, 쥐의 면역 결핍 균주의 사용은 마우스의 이상 면역 반응없이 이식 또는 인간 유래의 세포를 사용하여 연구를 할 수 있습니다.
상기의 장점에도 불구하고, 마우스에서 대규모 골간 골 결손 모델은 드물다. 이러한 모델은 대부분 (따라서 시험 될 재료의 양을 제한하는) 골수 공동을 채운다 골수 핀 뼈 고정을 사용하고 또한 회전 및 축 안정 2,4-7를 제공하지 않음으로써 재현성을 방해한다.
본 연구의 목적은 (ⅰ) 정확하고 재현성있는 잠금 플레이트 osteosynth에 의해 안정화된다 재현, 중요한 크기, 분절, 쥐에서 대퇴 결함 모델을 설명하기 위해, 임상 뼈 비 노조 상황을 흉내 낸입니다안정성이 높은 생체 역학적 환경 8-10을 제공 ESIS; (ⅱ)이 전위 골 대체물과 본 모델을 도시하고 골 형성은 그것이 사용될 수있는 분석을 설명하는 데.
프로토콜
윤리 진술 : 본 연구에 사용 된 마우스는 "케어 및 사용 실험 동물의"(지침 63분의 2,010 / 유럽 연합 (EU)과 유럽 협약 ETS 123)에 대해 유럽위원회가 발표 한 지침에 따라 처리 하였다. 실험 프로토콜은 의학 Lariboisière 세인트 루이스의 학부의 윤리위원회 (CEEA LV / 2010-01-04)에 의해 승인되었다.
1. 동물
- 무 흉선 마우스 (10 주 이전)를 사용합니다. 음성 대조군으로 비어 결함과 6 마우스의 최소한의 번호를 사용합니다.
2. 공사장 공중 발판 준비
- Syngenic 이식 준비
- 6 동물의 최소 개수와 대조군을 제공하는 결함을 채우기 위해 뼈 isograft를 사용한다.
- 수확하여 구하는 뼈 동종 이식편을 이식은 결함이 산호 발판 "그룹 (일 가득"비어 또는 결함 "중 하나에 속하는 마우스에서 대퇴골 뼈를 절제뼈 isograft) (11)를 수집하는 별도의 동물의 사용은 피하는 것이다.
- 인산염 완충 식염수 (PBS)로 절제 뼈를 세척 및 멸균 촉촉한 거즈 압축을 사용하여 유지.
- 산호 비계 준비
- 아크로 특검팀 : 천연 산호 만들어진 비계를 사용합니다. 산호 외골격 큐브, 6 동물의 최소 전위 골 대체 등 3 × 3 × 3mm.
- 원통형 손으로 각 산호 큐브 개척 (3.5 높이; 2mm 직경).
- , 고압 증기 멸균하여 각 지지체 (20 분 121 ° C)를 소독 멸균 PBS로 세척하고, 마우스에 이식하기 전에 24 시간 동안 완전 배지 (α-MEM)에 침지.
3. 마취 절차 및 진통
- 부 프레 노르 핀의 피하 주사 (0.1 밀리그램 / kg 동물 체중)에 의해 방지 진통, 마취 전 15 분을 제공한다.
- 동물에 연고를 적용동물이 마취 동안 눈을 매 30 분 건조를 방지한다.
- 저체온증을 방지하기 위해 온난화 패드에 마우스를 놓습니다.
- 수술시 마취 및 진통
- 복강 용액 함유 자일 라진 (8 ㎎ / ㎏) 및 케타민 (/ kg 100 mg)을 주입한다.
- 플로우 - 바이로 (50 ㎖ / 분), 산소를 제공한다.
- 유해 자극 (예., 회사 발가락 핀치)에 좋은 근육 이완과 동물 응답의 부족의 존재에 의해 마취의 적절한 깊이를 확인합니다.
- 피하 미생물 예방 등 enrofloxacin의 단일 용량 (0.05 ㎎ / ㎏)을 주입한다.
- 수술 후 진통
- 부 프레 노르 핀의 피하 주사 (0.1 ㎎ / ㎏) 3 일 연속 매 12 시간으로 수술 후 진통제를 제공합니다.
- 진단 이미징 절차 동안 마취
- anesthetizin에 마우스를 놓습니다g-상자, 다음 유도 각각 산소 약 4 %와 2 % 이소 플루 란을 이용하여 마취를 유지한다.
- 좋은 동물 근육의 휴식과 운동 부족에 의한 마취의 적절한 깊이를 확인합니다.
- 복구 조건
- 전체 복구 될 때까지 온난화 패드에 마우스를 유지
- 이 수술 후 흉골 드러 누움을 유지하기 위해 충분한 의식을 회복 할 때까지 무인 동물을 두지 마십시오.
- 완전히 회복 될 때까지 다른 동물의 회사에 수술을 한 동물을 반환하지 않습니다.
- 수술 후 조건
- 3 일 후 케이지에 4 쥐 호스트 처음 3 일 동안 별도로 마우스를 호스트.
- 물과 적응 식품 광고 무제한을 제공합니다. 포스트 수술 기간 동안 모든 활동의 제한없이, 체중 곰에 마우스를 허용합니다.
4. 수술 절차 :대퇴 분절 결함 모델 (11, 12)
- 마취 후, 확장의 왼쪽 뒷다리와 복부 드러 누움에 각 마우스를 놓습니다.
- 5 분 동안 10 % 포비돈 요오드를 사용하여 무균 수술 사지 스크럽하고 멸균 표면 (멸균 투명 드레이프는 절차 중에 호흡 움직임을 감시 할 수 있도록하기 위해 사용된다)을 만들 사지 하에서 멸균 드레이프를 배치했다. 케어는 절차를 수행하는 동안 수술 분야의 불임을 유지하기 위해 취해진 다.
- 뒷무릎 관절에 고관절로부터 연장, 대퇴골의 외측면에 걸쳐 17 mm 길이 방향 피부 절개 - 15합니다.
- 대퇴근을 절개는 광근의 근육을 lateralis와 팔뚝은 대퇴골 골간의 전체 길이를 노출 근육 대퇴 분할합니다. 주의 꼬리 쪽 좌골 신경을 보존하기 위해 수행되어야한다 말단 관절 캡슐 (그림 1).
- 대퇴골 골간 박람회를 향상시키기 위해물론, 둔부 근육과 팔뚝이 3 차 대전 자부에서 대퇴 가로로 쪼개다.
- 골간의 중간에서 대퇴골의 원형 절개를 수행합니다.
- 6 홀 티타늄 마이크로 잠금 플레이트를 적용 (최대 10 mm, 1.5 mm 폭, 무게 : 30 mg)을 전방 대퇴 쪽.
주 : 원추형 원통 부와 오목 된 판의 구멍 티탄 2mm 긴 잠금 나사 (태핑 수용은 0.47 mm 외경, 중량 : 5 ㎎, 헤드 나사의 저면으로는 내 로킹 가능하게 나사 고정 할 때 오프 비틀어 줄기에 연결되어 플레이트 구멍). - 0.3 mm의 드릴 비트 전용 엔진 파워 또는 약 500 mW의 12 2,500 rpm으로 작동 비 전용 엔진 출력)를 사용하여 플레이트의 가장 근위 구멍을 뚫는다.
- 전용 드라이버를 사용하여 첫 번째 나사를 삽입 한 다음 (그림 2)를 잠급니다.
참고 : t의 정렬 이후그 플레이트이 스크류 볼트의인가에 의해 결정되어, 상기 나사를 삽입 할 때 대퇴부에 평행 판을 배치하는 것이 중요하다. - 유사한 방식으로 상기 플레이트의 가장 후방 구멍을 드릴 나사 삽입하고 (도 3)를 잠글.
- 두 개의 다른 외부 나사를 삽입하지만 잠금을하지 않는다.
- 질리가 메디 오 - 측면 방향으로 뼈 주위에 밀접하게 본 0.22 mm의 와이어를 위치하게 한 후, 지그 (그림 4)의 슬롯에 삽입합니다.
- 마지막 두 나사의 줄기에 전용 지그를 삽입하고 플레이트 (그림 5) 이상에 적용합니다.
- 열 괴사를 방지하기 위해 (멸균 등장 성 식염수를 사용하여) 질리가 관개에 따라 본 사용하여 3.5 mm 길이 중반 골간 대퇴골 ostectomy을 수행합니다. 외과 의사의 조수 지그을했다. 외과 의사가 일정한 안정된 장력을 적용 할 수 있습니다. 톱 와이어를 복잡하게 얽힌하는 와이어의 중간 3 분의 2를 사용하지 않도록주의합니다. 예를 피하십시오직선 뼈 절단을 얻기 위해 운 운동 (도 6).
- ostectomy 후, 질리가 본 제거합니다. 연부 조직 손상을 피하기 위해, 한쪽 뼈 톱날 선 확대를 잘랐다.
- 지그를 제거하고이 마지막 나사 (그림 7)를 잠급니다.
- 어느 빈 분절의 결함을 떠나거나 수술 결함 내부 테스트 할 재료를 넣어를 입력합니다.
- 풍부하게 멸균 등장 성 식염수로 수술 부위를 씻어.
- 접시 위에 느슨하게 광근 lateralis 근육을 놓습니다. 간단한 연속 봉합 패턴과 5.0 glycomer 631 봉합사를 사용하여 근막과 피하 비행기를 닫습니다; 4.0 glycomer 631 봉합사를 사용하여 단순 단속 봉합 패턴 피부를 닫는다. 대안 적으로, 피부에 접착제를 사용하여 피부에 가까이하는 것도 가능하다.
뼈 재생의 생체 평가 5.
- 마취에서 마우스로, 방사선을 수행종래의 X 선을 모두 사용하여 길이 방식으로 평가 (26 kV로, 10 초; 2X 배율 20 라인 / mm 공간 해상도) 및 고해상도 마이크로 컴퓨터 단층 촬영 (μCT).
- μCT 분석 (0.5 mm 알루미늄 필터 0.7 º의 회전 단계 180 º의 단층 회전을 이용하여 40 msec의 노출 시간에서 50 kV로하고 478mA) 36 ㎛의 해상도로 화상을 취득. 상주 소프트웨어를 사용하여 이미지를 분석한다.
뼈 재생의 6 전의 VIVO 평가
- 텐 주 수술 후, 산소 이소 플루 란을 이용하여 마취를 유도 한 다음 바르비 투르 산염의 과량 (펜토 바르 비탈 1 ㎖)의 복강 내 주사하여 쥐를 희생.
- , 대퇴 뼈를 절제 근육 조직을 오버레이 제거, 4 일 동안 4 % 파라 포름 알데히드 (PH 7.4)에서 뼈 표본을 수정합니다.
- 파라 포름 알데히드의 fixa 후 각 절제 뼈 표본에서 플레이트와 나사를 제거기.
- 예 생체은 CT 분석 μ
- 75 % 알코올로 가득 폴리에틸렌 관의 각을 절제 고정 뼈를 놓고 생체 μCT를 사용하여 분석 할 수 있습니다.
- 80 kV의 100 μA (1000 msec의 노출 시간, 알루미늄 0.5 필터, 4 μm의 카메라 화소 크기 (7 ㎛의 복셀 사이즈 2400 X 4000)에서 0.9 º 각 회전 증분 평균 4 개의 프레임을 영상 획득.
- 상주 소프트웨어 해밍 여과 역 투영을 이용하여 3 차원 영상 (13 ㎛의 평균 복셀 사이즈)를 재구성한다.
- 골 형성의 정량적 분석을 위해, 결함에 대응 관심 결정된 일관성 영역 광물 조직 (45 계조 인덱스 하부 회색 임계 240 계조 인덱스 상부 회색 임계 값)의 양을 얻기 위해 상주 소프트웨어를 사용한다.
- 동일한 등록 각 마우스에 대해 동일한 방법으로 분석을 수행관심의 이온.
- 골유합 율 군간 관심 영역 광물 조직의 체적과 비교 - (95 %에서 및 p <0.05의 유의 수준 신뢰 구간) 일방 분석 시험을 사용한다.
- 조직 학적 분석
- 삽입 각각 잘라 내고, 메틸 메타 크릴 레이트 수지의 대퇴골을 고정 undecalcified 조직학을 위해 그것을 처리한다.
- 원형 수냉식 다이아몬드 톱을 사용하여 두꺼운 부분 (200 μm의)에 길이 각각의 뼈 표본을 잘라.
- 100 ㎛의 두께까지 각각의 뼈 시료 부를 연마하여 연마하고 Stevenel 블루 반 Gieson picrofuchsin 얼룩을 사용하여 염색.
참고 : 염색 한 후 세포를 광학 현미경에서 갈색 블루, 핑크 뼈, 산호에 나타납니다.
결과
전술 한 수술은 45 ~ 60 분에 지속되었다. Ostectomy 및 골 유합술은 외과 의사의 조수의 도움으로 있지만 확대 시스템을 사용하지 않고 수행이 용이했다. 어떤 수술 합병증은 발생하지 않았다. (18) 마우스 (11)에 대한 예비 연구에서 수술 후 방사선은 골 결손 길이 (3.43 ± 0.12 mm) 및 (뒷무릎 관절 캐비티 플레이트의 말단 부분 사이의 거리 = 2.65 ± 0.56 mm) 판 위치가 재현 하였다는 증거를 제공했다.
마취 관련 사망률은 5 %였다.
조작 된 사지의 기능 회복 수술 (애니메이션 그림 1) 후 일 이내에 관찰되었다 모든 동물과 전체 체중 부하에서 우수했다. 상기 p-에 사용되는 골 유합술 (플레이트 및 나사)의 무게재전송 연구는 마우스 체중의 약 0.1 %였다. 어떤 합병증 (예를 들면, 창상 감염, 이식 실패 골 이식 마이그레이션 등)은 발생하지 않았다. cagemates에 의한 없음 자기 부상이나 상해가 발생하지 않습니다.
수술에 의한 골 결손이 비어 때, 의미있는 골 형성 일관성 골 불유합으로 관찰되지 않았다. 대조적으로, 결함가 isograft 또는 산호 골격들로 채워지 때 관찰 된 근위 및 원위 골 가장자리로부터 연장되는 뼈를 새롭게 형성했다. 또한, 반면 골 형성은 동종 이식편을 이식 (그림 8), 그것은 단지이 재료로 충전 결함의 산호 골격 내부 관찰로 치료 대부분의 결함에 뼈 연속성의 재 설립을 허용했다. 사실, 더 뼈 거리 뼈 가장자리로부터 1mm 이상이 관찰되지 않았다. 모든 조직 학적으로 연골의 부재는 증거를 제공하는 결과를 분석달성 된 골 유합술의 안정성 (그림 9, 그림 10).
방사선 및 microCT는 골유합이 결함 왼쪽 빈 그룹의 동물 발생하지 않았 음을 증거를 제시 분석 10 주 주입을 게시 할 수 있습니다. microCT 분석에 의해 평가 광물 조직의 부피는 ± 0.3 mm 3 0.8이었고, 새로 형성된 뼈 대표했다. isograft와 산호 골격 그룹에서 골유합은 각각 4, 4 동물을 얻었다. microCT 분석에 의해 평가 광물 조직의 부피는 4.4 ± 0.9 mm 3 8.9 ± 0.7 mm 3. isograft와 산호의 골격이 모두 미네랄을 포함하기 때문에이 그룹에서, 그러나, 새로운 골 형성이 남아있는 이식 물질 (isograft 또는 산호 비계)에서 진정으로 구별 할 수 없었다. 봉 조합의 속도와 isograft 그룹에서 얻은 광물 조직의 볼륨 모두와산호 골격 그룹 (P <0.001) 결함 왼쪽 빈 그룹에 의한 것보다 훨씬이었다에서.
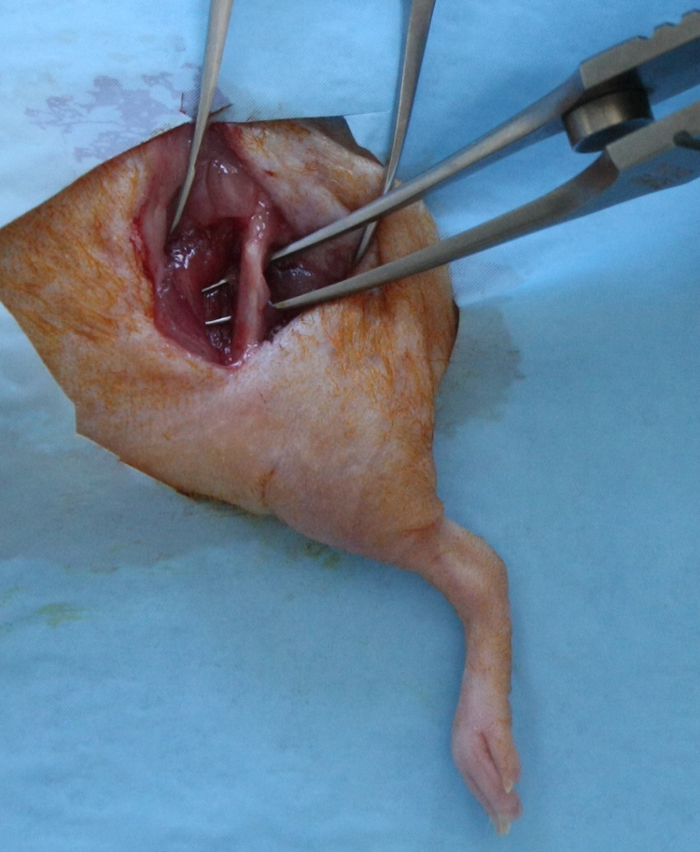
그림 1 :. 대퇴골 분절 결함의 생성을위한 외과 노출 15-17-mm 세로 피부 절개, 뒷무릎 관절에 고관절로부터 연장은, 대퇴골의 외측면에 걸쳐 만들어졌다. 대퇴근은 절개; 광근의 근육을 lateralis과 팔뚝 근육은 대퇴골 골간의 전체 길이를 노출 분리 된 대퇴. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
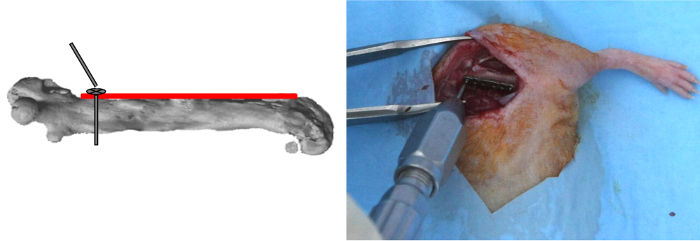
그림 2 : 플레이트위치 및 근위 나사 배치. 플레이트는 전방 대퇴 측에 적용 하였다. 상기 플레이트의 가장 근위 구멍 천공시켰다 제 1 나사가 잠겨, 다음, 삽입되었다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
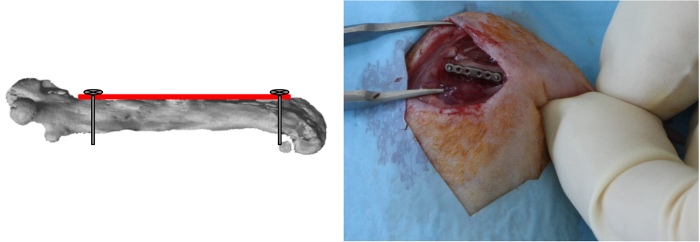
그림 3 :. 원위 나사 배치 판의 가장 말단 구멍을 뚫고하고 나사를 삽입하고 고정되었다. (조직 공학과 파트 C 2013, 19 (4), 271-280에서 허가 재판) 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
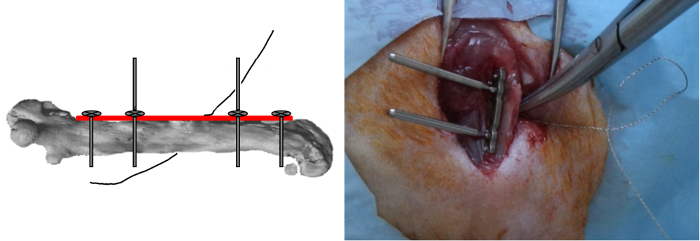
그림 4 : 질리가 위치를 보았다. 두 개의 다른 외부 나사를 삽입하지만 잠겨 있지 및 0.22 mm 질리 톱의 와이어가 메디 오 - 측면 방향으로 뼈 주위에 밀접하게 묶여 있었다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
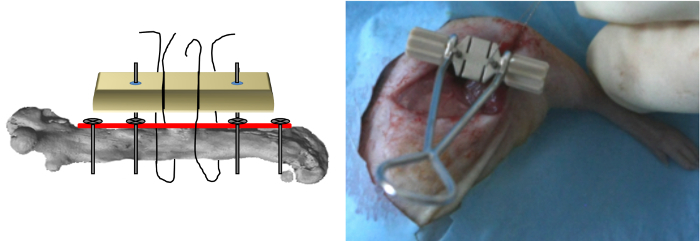
도 5 : 지그 위치 결정 지그 마지막 두 나사 스템에 삽입 판 위에 도포하고, 탄성 표면파의 와이어 후 지그의 슬롯에 삽입 하였다.. (조직 공학과 파트 C 2013, 19 (4), 271-280에서 허가 재판) 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 6 :. Ostectomy Ostectomy 수행하고 질리 톱은 철회되었다. (조직 공학과 파트 C 2013, 19 (4), 271-280에서 허가 재판) 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
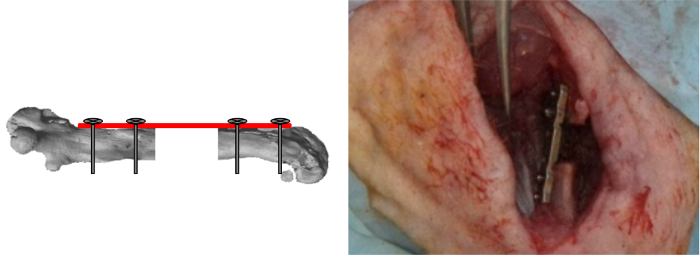
그림 7 :. 내부 나사가 잠금은 지그를 제거하고 마지막 두 나사를 고정했다. 분절 결함은 왼쪽 빈 또는 시험 물질로 채워진 중 하나였다. (조직 공학과 파트 C 2013, 19 (4), 271-280에서 허가 재판) 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
t = "그림 8"SRC = "/ 파일 / ftp_upload / 52940 / 52940fig8.jpg"/>
그림 8 : 대표 수술 후 방사선 사진과 쥐의 대퇴부 뼈의 시상 μCT 재건 각각의 결함과 대퇴 뼈 중 왼쪽 (AE) 빈, 또는 대규모 syngenic 골 이식 (FJ)로 채워진, 또는 대규모의 아크로 산호의 골격 가득 (KO. ); 즉시 수술 후 (A, F, K) 4 주 수술 N (B, G, L), 술 후 6 주 (C, H, M), 및 10주 수술 후 (D, E, I, J, 이후 , O) (플레이트 길이 = 10 mm)이다. (조직 공학과 파트 C 2013, 19 (4), 271-280에서 허가 재판) 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
파일 / ftp_upload / 52940 / 52940fig9.jpg "/>
. 그림 9 : 대표 방사선 사진, 본 연구에서 테스트 산호 발판으로 가득 결함의 μCT 재건 및 조직학 새로 형성된 뼈의 많은 양의 주변 뼈 가장자리와 산호의 골격 사이에-관찰되었다; 대조적으로, 작은 뼈는 지지체 내부에 존재했다. 얼룩 : Stevenel 블루와 폰 Gieson의 picrofuchsin. 이러한 조건에서, 뼈 세포 및 산호는 각각 적색, 청색, 갈색 염색. 스케일 바 = 500 μm의. ACS = 아크로 산호 골격; BN = 뼈. (조직 공학과 파트 C 2013, 19 (4), 271-280에서 허가 재판) 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
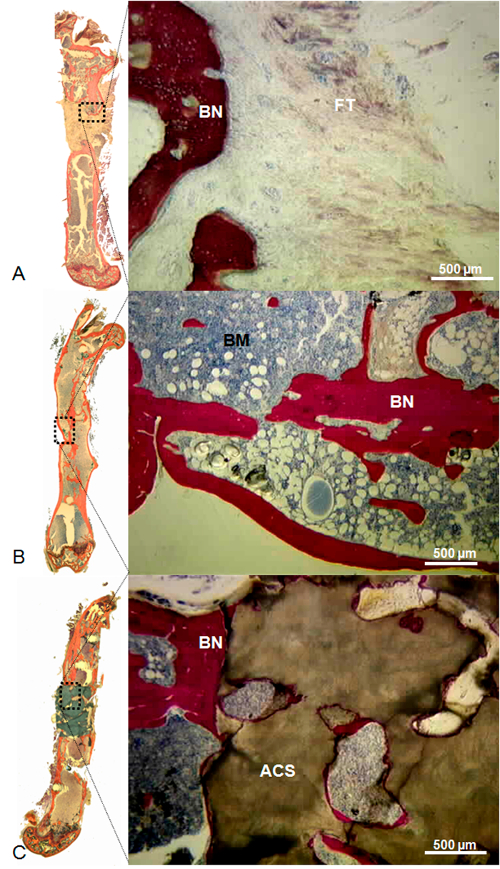
그림 10 : 파트 : 대규모 Syngenic 뼈 이식 (B)으로 가득하고, 산호 비계 (C)로 충전 된 결함 왼쪽 빈 (A)의 대의 적 조직학가. 결함에서 비어, 뼈의 라운딩은 수질 운하 충전과 깊은 풍부한 섬유 조직으로 에지 결함으로 관찰 하였다. 대규모 syngenic 골 이식 가득 결함에서 뼈의 연속성은 이식과 주변 뼈 가장자리 사이에 관찰되었다; 골수은 원래 공동 전반에 걸쳐 존재. 산호의 골격 가득 결함에 새로 형성된 뼈 주위의 뼈 가장자리와 산호의 골격 사이에 관찰되었다,하지만 작은 뼈는 지지체 내부에 존재했다. 얼룩 : Stevenel 블루와 폰 Gieson의 picrofuchsin. 이러한 조건에서, 뼈 세포 및 산호는 각각 적색, 청색, 갈색 염색. 스케일 바 = 500 mm이다. ACS, 산호 골격; BN, 뼈; BM, 골수; FT, 섬유 조직. (조직 공학과 파트 C 2013에서 허가 재판 19 (4), 271-280)OAD / 52940 / 52940fig10large.jpg "대상 ="_ 빈 ">이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

애니메이션 / 비디오 그림 1 : 마우스 하루 수술의 걸음 걸이의 대표적인 비디오. 베어링이 관찰되었다 전체 무게. 이 동영상을 보려면 여기를 클릭하십시오.
토론
정형 관련 재료 및 마우스 장치의 이소성 주입은 일반적으로 다양한 지지체 (13, 14)의 용량을 형성하는 뼈 평가를 행한다. 중요한 차이는 있지만 기본 골 형성 신호 요인과 호스트 뼈 형성 세포 분비의 상호 작용을 포함하여 자궁외 및 동 소성 모델 사이에 존재한다.
본 연구는 재현 쥐 큰 분절을 설정, 중요한 크기 대퇴 결함 (3.5 mm, 대퇴골 길이의 약 20~25%). 이러한 결함의 크기와 결과 판 고정술에 의해 제공되는 안정성을 고려하면,이 모델은 임상 적 발견 위축성 불유합 뼈 모방.
본 연구에서 선택한 수술 시간은 8 ~ 12 주 4,9,15,16 후 적절한 치료의 부족을 보여주는, 앞에서 설명한 비 노조 모델 마우스와 일치한다.
가장 중요한 것은, reprodu뼈 이식 대체물 cible 안정 고정술뿐만 아니라 안정성이 로킹 플레이트 및 ostectomy을 수행하는 지그 양자의 사용으로 유의 한 이환율 및 사망률 1,2-없이 얻었다. 이 결과는 또한 외부 고정 장치 또는 골수 손톱 하나가 4,5,17-24를 사용할 때보고 된 결과를 대조. 외부 전위 단점 포함 fixators 들어 : 강성 변동, 핀 책자의 감염, 핀 풀림은 핀 재료 (4 마우스 체중의 20 %)의 중량으로 인한 부상에서, 전위. 골수 못 들어 잠재적 인 단점은 다음과 같습니다 : 손톱과 관절 표면의 의원 성 손상과 수질 공동의 충전.
판 고정술 의해 안정화 다른 뮤린 분절, 임계 크기 결함 대퇴 1.5 내지 2 mm 길이 16,25 범위의 버어에 의해 생성 된 골 결손으로 설명되었다. 일에서전자 본 모델, 지그 및 톱 와이어의 사용은 큰 근육 외상없이 정확한 3.5 mm 길이의 ostectomy을 허용했다.
그러나, 하나는 고려 몇 가지 주요 포인트에 수행해야 할 절차를 수행하기에 성공하기 : 그렇지 않으면 플레이트가 너무 오래한다 (8 주에서 25g 또는 세 미만의 중 무게와 누드 마우스) 작은 마우스를 사용하지 마십시오. 대퇴 뼈에 접근 할 때, 꼬리 쪽 좌골 신경 말단 관절 캡슐을 모두 유지하기 위해주의를 기울입니다. 대퇴골의 전방 측면에 플레이트를 적용하고 판의 배향이 제 나사의인가에 의해 결정되기 때문에,이 제 나사를 삽입 할 때 대퇴부에 평행 판의 위치를 알아서.
ostectomy하기 전에 근육의 외상을 방지하기 위해 골간의 중간에서 대퇴골의 원형 절개를 수행하도록주의하십시오. ostectomy을 수행 할 때, 의사의 조수 단단히 가이드와 쉬르을 보유해야geon 일정한 안정 장력을인가하면서 (ii) 상기 선재의 중간 2/3을 사용하고, (ⅲ) 직선 뼈 절단을 얻기 위해 과도한 움직임을 방지하기 위해, 톱날 와이어 얽힌 않도록주의 (I)이어야한다.
본 모델은 골 이식이 사용됩니다 제공에 뼈 치유가 가능합니다. 또한,이 모델은 인간 기원의 이식 또는 세포 하나가 잘 표준화, 큰, 분절, 골 결손에 사용되는 골 교체 전략에 관여하는 메커니즘의 추가 연구를 할 수 있습니다.
또한, 정제 및 정형 관련 연구에서 동물의 사용 감소를 요구하는 현재의 추세에 맞춰,이 모델은 이러한 생물 발광 등의 생체 영상 기술과 함께 사용될 수있다. 이러한 비 침습적 방법은 동물의 희생 없이도 26 모두 이식 세포의 생존과 조직 치료를 모니터링 할 수 있습니다.
본 모델의 주요 제한 사항이 모두 있습니다하중 조건들이 완전히 인간 임상 발생들을 모방하지 않으므로 만들어진 골 결손의 볼륨. 모델의 다른 제한은 (I)의 생체 μCT 분석 전에 플레이트의 제거를 필요로 할 수 있으며, 길이 방사선 투과 검사 결과 해석을 복잡하게 판의 무선 불투명도이다 (ⅱ) 판의 강성을 조절하는 무능력을하는 골 형성 27-30에서 핵심 기계 매개 변수 일 수있다.
뼈 isograft 또는 (특히 탄산 칼슘) 미네랄 성분을 함유하는 다른 지지체를 사용할 때 새롭게 형성된 골밀도 부분적으로 중첩 한 것이기 때문에, 어떤 바이어스 마이크로 CT 분석 분할 공정에 도입되어, 또한 명심해야 isograft 밀도 또는 비계의 밀도 중 하나. 골 부피는 마이크로 CT 분석으로 수득 이러한 이유로 주로 광물 조직 (새로 형성된 뼈의 양을 반영 플러스뼈 대체) 11,26,31.
공개
저자는 더 경쟁 재정적 이해 관계가 없음을 선언합니다.
감사의 말
저자는 원고에 그녀의 소중한 의견 레나 Bizios을 감사드립니다.
자료
| Name | Company | Catalog Number | Comments |
| α-MEM , Minimum Essential Medium Eagle | Sigma-Aldrich, France | M4526 | 500 ml |
| Acropora sp. coral exoskeleton cubes, Biocoral® | Biocoral®, Inoteb, France | 3 x 3 x 3 mm cubes, autoclaving (121 °C for 20 min) sterilization | |
| Buprenorphine, Buprecare® | Axience, Pantin, France | 0.3 mg/ml | |
| Xylazine, Rompun® 2% | Bayer HealthCare, Puteaux, France | 20 mg/ml | |
| Ketamine, Ketamine 500® | Virbac, Carros, France | 50 mg/ml | |
| Isoflurane, Forène® | Abbott, Arcueil, France | ||
| Enrofloxacine, Baytril® 5% | Bayer HealthCare, Puteaux, France | 50 mg/ml | |
| Pentobarbital, Dolethal® | Vétoquinol, Lure, France | 182.2 mg/ml | |
| Anesthetizing box | Ugo Basile, Gemonio, Italy | 7900/10 | |
| Plastic transparent sterile drape, BusterOpCover 30 x 45 cm | Buster, Coveto, Montagu, France | 613867 | |
| 10% povidone iodine, Vétédine® Solution | Vétoquinol, Lure, France | 100 mg/ml | |
| Titanium micro- locking plate, MouseFix Plate XL | RISystem AG, Davos, Switzerland, http://www.risystem.com/ | RIS.401.120 | 6 holes, 10 mm long and 1.5 mm wide, autoclaving (121 °C for 20 min) sterilization or cold sterilzation (ethylene oxide) |
| 0.3 mm drill bit, Drill Bit 0.30 mm | RISystem AG, Davos, Switzerland, http://www.risystem.com/ | RIS.592.200 | autoclaving (121 °C for 20 min) sterilization or cold sterilzation (ethylene oxide) |
| Engine power | RISystem AG, Davos, Switzerland, http://www.risystem.com/ | AccuPen | Cold sterilzation (ethylene oxide) |
| Screw driver, Handrill | RISystem AG, Davos, Switzerland, http://www.risystem.com/ | RIS.390.130 | autoclaving (121 °C for 20 min) sterilization or cold sterilzation (ethylene oxide) |
| Self-tapping locking screws, MouseFix Screw 2 mm | RISystem AG, Davos, Switzerland, http://www.risystem.com/ | RIS.401.100 | 2 mm long, 0.47 mm outer diameter and 0.34 mm core diameter, autoclaving (121 °C for 20 min) sterilization or cold sterilzation (ethylene oxide) |
| Jig, MouseFix XL Drill and Saw Guide | RISystem AG, Davos, Switzerland, http://www.risystem.com/ | RIS.301.103 | 3.5 mm between the slots, autoclaving (121 °C for 20 min) sterilization or cold sterilzation (ethylene oxide) |
| 0.22-mm Gigli saws (0.22 mm Saws) | RISystem AG, Davos, Switzerland | ||
| 5.0 glycomer 631, Biosyn | Covidien, Vétoquinol, Lure, France | Tapper-cut needle | |
| 4.0 glycomer 631, Biosyn | Covidien, Vétoquinol, Lure, France | Tapper-cut needle | |
| X-ray, MX20 | Faxitron X-ray Corp, Edimex, Le Plessis Grammorie | ||
| In vivo high-resolution microcomputed tomography, Skyscan 1176 | Skyscan, Aartselaar, Belgium | ||
| Ex vivo high-resolution microcomputed tomography, Skyscan 1172 | Skyscan, Aartselaar, Belgium | ||
| Resident software: Nrecon (v1.6.9) / Ctan (v.1.14.4) | Skyscan, Aartselaar, Belgium |
참고문헌
- Auer, J. A., et al. Refining animal models in fracture research: seeking consensus in optimising both animal welfare and scientific validity for appropriate biomedical use. BMC Musculoskelet Disord. 8 (72), (2007).
- Histing, T., et al. Small animal bone healing models: standards, tips, and pitfalls results of a consensus meeting. Bone. 49 (4), 591-599 (2011).
- Horner, E. A., et al. Long bone defect models for tissue engineering applications: criteria for choice. Tissue Eng. Part B Rev. 16 (2), 263-271 (2010).
- Srouji, S., et al. A model for tissue engineering applications: femoral critical size defect in immunodeficient mice. Tissue Eng. Part C Methods. 17 (5), 597-606 (2011).
- Thompson, Z., Miclau, T., Hu, D., Helms, J. A. A model for intramembranous ossification during fracture healing. J Orthop Res. 20 (5), 1091-1098 (2002).
- Harris, J. S., Bemenderfer, T. B., Wessel, A. R., Kacena, M. A. A review of mouse critical size defect models in weight bearing bones. Bone. 55 (1), 241-247 (2013).
- Garcia, P., et al. The LockingMouseNail--a new implant for standardized stable osteosynthesis in mice. J. Surg. Res. 169 (2), 220-226 (2011).
- Garcia, P., Histing, T., Holstein, J. H., Pohlemann, T., Menger, M. D. Femoral non-union models in the mouse. Injury. 41 (10), 1093-1094 (2010).
- Garcia, P., et al. Development of a reliable non-union model in mice. J. Surg. Res. 147 (1), 84-91 (2008).
- Viateau, V., Logeart-Avramoglou, D., Guillemin, G., Petite, H., Conn, P. M. Animal Models for bone tisue enginering purposes. Sourcebook of models for biomedical research. , 725-738 (2008).
- Manassero, M., et al. A novel murine femoral segmental critical-sized defect model stabilized by plate osteosynthesis for bone tissue engineering purposes. Tissue Eng. Part C Methods. 19 (4), 271-280 (2013).
- Matthys, R., Perren, S. M. Internal fixator for use in the mouse. Injury. 40 Suppl 4, S103-S109 (2009).
- Becquart, P., et al. Ischemia is the prime but not the only cause of human multipotent stromal cell death in tissue-engineered constructs in vivo. Tissue Eng. Part A. 18 (19-20), 2084-2094 (2012).
- Deschepper, M., et al. Proangiogenic and prosurvival functions of glucose in human mesenchymal stem cells upon transplantation. Stem Cells. 31 (3), 526-535 (2013).
- Oetgen, M. E., Merrell, G. A., Troiano, N. W., Horowitz, M. C., Kacena, M. A. Development of a femoral non-union model in the mouse. Injury. 39 (10), 1119-1126 (2008).
- Liu, K., et al. A murine femoral segmental defect model for bone tissue engineering using a novel rigid internal fixation system. J Surg Res. 183 (2), 493-502 (2013).
- Zwingenberger, S., et al. Establishment of a femoral critical-size bone defect model in immunodeficient mice. J Surg Res. 181 (1), e7-e14 (2013).
- Cheung, K. M., et al. An externally fixed femoral fracture model for mice. J. Orthop Res. 21 (4), 685-690 (2003).
- Claes, L., et al. Hyperhomocysteinemia is associated with impaired fracture healing in mice. Calcif. Tissue Int. 85 (1), 17-21 (2009).
- Drosse, I., et al. Validation of a femoral critical size defect model for orthotopic evaluation of bone healing: a biomechanical, veterinary and trauma surgical perspective. Tissue Eng. Part C Methods. 14 (1), 79-88 (2008).
- Holstein, J. H., et al. Advances in the establishment of defined mouse models for the study of fracture healing and bone regeneration. J. Orthop. Trauma. 23 (5 Suppl), S31-S38 (2009).
- Johnson, K. D., August, A., Sciadini, M. F., Smith, C. Evaluation of ground cortical autograft as a bone graft material in a new canine bilateral segmental long bone defect model. J. Orthop. Trauma. 10 (1), 28-36 (1996).
- Meinig, R. P., Buesing, C. M., Helm, J., Gogolewski, S. Regeneration of diaphyseal bone defects using resorbable poly(L/DL-lactide) and poly(D-lactide) membranes in the Yucatan pig model. J. Orthop. Trauma. 11 (8), 551-558 (1997).
- Wu, J. J., Shyr, H. S., Chao, E. Y., Kelly, P. J. Comparison of osteotomy healing under external fixation devices with different stiffness characteristics. J. Bone Joint Surg. Am. 66 (8), 1258-1264 (1984).
- Xing, J., et al. Establishment of a bilateral femoral large segmental bone defect mouse model potentially applicable to basic research in bone tissue engineering. J. Surg. Res. 192 (2), 454-463 (2014).
- Manassero, M., et al. Comparison of Survival and Osteogenic Ability of Human Mesenchymal Stem Cells in Orthotopic and Ectopic Sites in Mice. Tissue Eng. Part A. 22 (5-6), 534-544 (2016).
- Bos, R. R., et al. Degradation of and tissue reaction to biodegradable poly(L-lactide) for use as internal fixation of fractures: a study in rats. Biomaterials. 12 (1), 32-36 (1991).
- Oest, M. E., Dupont, K. M., Kong, H. J., Mooney, D. J., Guldberg, R. E. Quantitative assessment of scaffold and growth factor-mediated repair of critically sized bone defects. J.Orthop. Res. 25 (7), 941-950 (2007).
- Pihlajamaki, H., Bostman, O., Tynninen, O., Laitinen, O. Long-term tissue response to bioabsorbable poly-L-lactide and metallic screws: an experimental study. Bone. 39 (4), 932-937 (2006).
- Rai, B., et al. Combination of platelet-rich plasma with polycaprolactone-tricalcium phosphate scaffolds for segmental bone defect repair. J. Biomed. Mater Res. A. 81 (4), 888-899 (2007).
- Komlev, V. S., et al. Kinetics of in vivo bone deposition by bone marrow stromal cells into porous calcium phosphate scaffolds: an X-ray computed microtomography study. Tissue Eng. 12 (12), 3449-3458 (2006).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유