Method Article
라이트 기반 효소 탈 카르 복 실화
요약
산화 적 변환에 대한 보조 인자 - 우리는 과산화수소의 광 촉매 작용으로 발생하는 프로토콜을 기술한다.
초록
산화 환원 효소가 가장 많이 적용되는 산업용 효소에 속한다. 그럼에도 불구하고, 그들은 누구의 공급 종종 비용이 많이 들고 도전 외부 전자가 필요합니다. 전자 도너의 NADH 또는 NADPH 재활용 추가적인 효소와 희생 기판의 사용을 요구한다. 흥미롭게도 몇 가지가 산화 환원 효소, 전자 공여체로서 과산화수소를 받아 들인다. 저렴하면서,이 시약들은 효소의 안정성을 감소시킨다. 이 문제에 대한 해결책은 보조 인자의 동일계에서 발생된다. 저농도 보조인의 지속적인 공급이 효소의 안정성을 손상시키지 않고 반응을 구동한다. 이 논문을위한 방법을 보여주는 광 촉매 헴 의존 지방산 라제 OleT JE의 예 과산화수소 시츄 생성한다. 지방산 라제 OleT JE는 지방산하는 종래 알려지지 효소에서 장쇄 1- 알켄을 생성하는 고유의 기능으로 인해 발견반응. 1 알켄 널리 가소제 및 윤활제를 위해 첨가제를 사용한다. OleT JE은 산화성 탈 카복실 화에 대해 과산화수소로부터 전자를 수용하는 것으로 나타났다. 과산화수소 손상 보조인의 동일계에서 생성 효소 및 낮은 수율 결과의 첨가는 이러한 문제를 회피하면서. photobiocatalytic 시스템 지방산 탈 카르 복 실화를위한 간단하고 효율적인 방식으로 생성 된 효소 활성 및 수율에 대한 명확한 이점을 나타낸다.
서문
기후 변화와 재생 자원의 예측 고갈은 우리 사회에 심각한 위협을 제기. 이러한 맥락에서, 효소 촉매는 지속 가능한 개발과 '친환경'화학 1 아직도 완전히 이용하지 가능성을 나타냅니다. 산화 환원 효소는 온화한 반응 조건에서 도입 및 관능기 변형을 촉매 가장 중요한 생체 촉매 (2)에 속해있는 능력을 가지고있다. 대부분의 산화 환원 변환은 NAD (P) H로 보조 인자의 외부의 공급을 필요로한다. 보조 인자 재생을위한 방법은 산업 규모에 적용되었습니다. 그러나, 여전히 고가의 제품에 주로 애플리케이션을 제한하는 높은 공정 비용을 초래한다. 흥미롭게도, 여러 퍼 옥시다아제 3,4 및 P450 모노 옥 시게나 제 (5)는 소위 과산화 션트를 통해 과산화 수소에서 전자를 받아들입니다. H 2 O 2가 저렴한 공동 시약이지만, 보도 harmf이고많은 효소에 대한 UL. 현장 형성에 정상 과산화수소의 낮은 농도는 효소의 작동 안정성을 손상시키지 않고 반응을 유도하기위한 실용적인 방법이다.
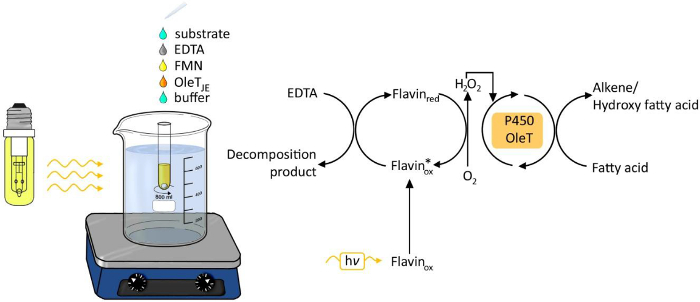
그림 OleT JE에 의해 지방산의 photobiocatalytic 탈 카르 복 실화 1. 실험 세트입니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
화학적 및 생물학적 과정을위한 에너지 소스로서 광을 이용 지난 년 6 증가 주목을 받고있다. 과산화수소의 광 생성 구동 독스 변형 (도 1)에 대한 과산화수소를 공급하는 간단하고 강력한 방법으로 떠오르고있다. 이러한 아데닌 월 플라 빈과 같은 광촉매onucleotide (FMN) 그런 oxyfunctionalization 효소 반응을위한 보조 인자로서 사용되는 과산화수소, 산소 분자의 환원을 허용한다. 가능한 전자 도너는 에틸렌 디아민 테트라 아세트산 (EDTA), 아스 코르 베이트 또는 저렴 포르 미 에이트이다. 이 방법은 퍼 옥시다아제 3,4 및 P450 모노 옥 시게나 제 (5)을 포함하여 2 O 2 의존성 효소, H에 대해 일반적으로 적용 할 수 있습니다.
최근 올레핀 8로 천연 지방의 변환을위한 신규 박테리아 라제 (7)의 어플리케이션을 조사 하였다. 이것은 바이오 기초 소스에서 널리 사용되는 플랫폼 화학 물질의 합성에 대해 지속 라우트 될 것이다. 그램 양성 세균 Jeotgalicoccus 특검팀에서 탈 카르복시 OleT JE. 지방산의 산화 적 탈 카르 복 실화를 촉매 제품 1- 알켄을 형성한다. OleT JE 밀접하게 세균 P450 모노 옥 시게나 제에 관한와 F 전자를 필요로한다반응에 ROM 과산화수소.
불행히도, 기재와 효소의 용액에 H 2 O 2를 첨가 아마도 인해 OleT JE의 안정성에 과산화수소의 해로운 효과, 낮은 변환 결과의 재현성이 나쁘고 결과. NADPH-환원 RhFred와 융합 단백질의 생성은 NADPH의 높은 가격과 비용 효율적인 재생을위한 전류 제한 가능성은 저렴 전자 공여체를 조사하기 위해 우리를 묻는 메시지가, 그럼에도 불구 NADPH 의존 탈 카르 복 실화 가능합니다. (9)을했다. P450 모노 옥 시게나 제와 OleT JE의 유사성에 의해 영감을, 우리는 H 2 O 2의 광 촉매 생성을 사용했다. 우리는 무 세포 추출물 또는 정제 된 효소 솔루션을 사용하여 (> 95 %까지) 높은 전환을 얻기 기쁘게했다.
지방산 탈 카르 복 실화의 예, 우리는 빛을 주도 enzym에 대한 일반적인 프로토콜을 제시보조 인자로서 광촉매로 과산화수소를 사용 FMN ATIC 산화 환원 변형. 제시된 방법은 E. 재조합 세포에서 효소의 생산을 포함 콜라이 효소의 정제, 1- 알켄의 합성 및 반응 생성물의 분석을위한 프로그램.
프로토콜
주의 : 사용하기 전에 모든 관련 물질 안전 보건 자료 (MSDS)를 참조하십시오. 이러한 합성에 사용되는 화학 물질 중 일부는 급성 독성 및 발암 성이다. 유해한 유기 용제, 특히 반응 생성물의 추출 및 지방산의 유도체를 포함하는 모든 단계는 개인 보호 장비 (안전 안경, 장갑, 실험실 코트, 전체 길이 바지, 폐쇄 발가락 신발을 사용하여 흄 후드에서 수행되어야한다 ). 이 연구에서 유전자 변형 생물체와 관련된 모든 작업은 안전 수준 (S1)의 유전자 변형 생물체의 취급에 대한 승인을 설치해야합니다.
E.에서 재조합 디카 르 복실 라 아제 OleT JE의 1 식 대장균
- 생산 균주의 제조
- Jeotgalicoccus에서 OleT JE의 합성 유전자를 준비하고 발현 벡터 PASK-IBA37plus 설명 된대로에 클로닝. (8)
참고 : 박테리아 대사, E.에서 효소에 의해 지방산의 저하를 방지하기 위해 지방산 분해 역기능 통로와 게이오 컬렉션에서 대장균 균주 JW5020 사용 하였다.
- Jeotgalicoccus에서 OleT JE의 합성 유전자를 준비하고 발현 벡터 PASK-IBA37plus 설명 된대로에 클로닝. (8)
- 재배 및 효소 발현의 유도
- E. 접종에 의해 사전 문화를 준비 테스트 튜브에 두 개의 3 ㎖ LB-매체 (100 μg의 ㎖의 -1 암피실린을 포함)를 LB 플레이트에서 대장균 JW5020 OleT 돌연변이. 선택을위한 매체로 원액에서 피펫 암피실린 (100 μg의 ㎖의-1) 및 180 rpm으로 진탕 배양기에서 15 시간 동안 37 ° C에서 품어.
- 1 L 쉐이크 플라스크에, 두 개의 200 ㎖의 LB-매체에 포함 된 암피실린 (100 μg의 ㎖의 -1) 전 문화 2 ㎖를 추가합니다. 배양은 37 ° C, 180 rpm으로 진행된다.
- OD600nm에서의 변화를 모니터링 접종 후. 외경 600 0.6 사이의 값에 도달하면D 0.8 (0.2 μg의 용액 1) 테트라 사이클린을 첨가함으로써 발현을 유도한다. 20 ° C에서 15 시간 180 rpm으로의 문화를 품어.
주 : OleT JE는 헴 보조 인자를 포함하기 때문에, δ 아미노 레 불린 산 (0.5 mM)을 종래의 유도에 첨가 팩터 합성을위한 전구체로 배양을 제공하기 위해 필요하다.
- 세포 용해
- 얼음에서 다음 단계를 수행합니다. 원심 분리기 튜브에 경사 또는 피펫 팅에 의해 문화를 전송하고 평등 한 분배를 보장하기 위해 스케일을 사용합니다. 4 ℃에서 12,000 XG에서 20 분 동안 문화를 원심 분리기.
- 조심스럽게 상층 액을 버리고 피펫 50 ml의 버퍼 (트리스의 50 mM, NaCl을 200 밀리미터, 산도 7.5)에 펠렛을 재현 탁하고 원추형 원심 관에 정지를 전송합니다.
- 4 ° C에서 4,000 XG에 15 분 동안 원심 분리 후, 상층 액을 버린다 피펫으로 3 ㎖ 버퍼에 각 펠렛을 재현 탁.
- 이렇게하여 세포 용해를 수행주기 사이에 1 분 일시 정지를 떠나 얼음 솔루션 (X 30 초 3주기)를 nicating. 원심 4 ℃에서 15,000 × g으로 20 분 동안 용액은 세포 파편을 제거하고, 피펫 팅하여 펠렛을 방해하지 않고 원추형 원심 분리 튜브에 상청을 전송한다. 펠렛을 폐기하십시오.
참고 : 작은 분자가 제거 된 후 하나의 용매 분획물이 생물 촉매에 직접 사용됩니다. 두 번째 분획은 태그가 그의 OleT JE의 정제에 사용한다.
- 세포 추출물의 작은 분자를 제거하여
- 생물 촉매의 조 추출물을 4 ℃에서 4,000 XG에서 10 kDa의 막 원심 분리기로 원심 분리 필터 장치로 무 세포 추출물을 3 ㎖를 피펫 팅에 의해 과산화수소의 형성 또는 전자 이동을 방해 할 수있는 작은 분자를 제거하여 이전. 3 mL의 트리스 -HCl 버퍼에 남아있는 단백질을 재현 탁.
- OleT의 정제
- 평형 완충액 (트리스 20 mM의, 염화나트륨 300 밀리미터, 이미 다졸 10 밀리미터)로 전 평형 된 그의 뿌르 니켈 NTA 스핀 열, 두 번째 세포 추출물의 3 ㎖를 적용합니다.
- 하단 플러그와 상부 스크류 캡과 열을 밀봉 수지는 무 세포 추출물과 동등하게 분산 될 때까지 가볍게 흔들어. 4 ℃에서 오버 헤드 진탕 기에서 30 분간로드 열을 품어.
- 2 분 동안 700 XG에 원심 분리하여 세척 완충액 1 ㎖ (트리스 20 mM의, 염화나트륨 300 밀리미터, 이미 다졸하는 20 mM, pH를 7.4)에 열을 씻으십시오. 두 번이 단계를 반복합니다.
- 신선한 원뿔 원심 분리 튜브에 열을 놓고 용출 버퍼의 1 ㎖ (트리스 20 mM의, 염화나트륨 300 밀리미터, 이미 다졸 250 밀리미터, 산도 7.4) OleT JE를 추가합니다. 2 분 동안 700 XG에 원심 분리기이 단계를 두 번 반복합니다.
참고 : 이미 다졸 니켈에 결합함으로써 열에서 OleT JE을 제거합니다. - 원심 분리 필터 장치로 용출 트랜스퍼 (10 kDa의의 MEMbrane)와 4 ° C에서 4,000 XG에 원심 분리기는 이미 다졸을 제거합니다.
- 물질 안전 보건 자료 페이지 (15 %). 9 섞어 SDS 버퍼 (최종 농도 1 배)로 용출 3 μL에 의해 효소의 순도를 확인하고 변성 5 분 동안 95 ° C에서 솔루션을 품어. 이어서 SDS 페이지에 총 금액을 적용합니다. 상업 단백질 표준을 사용하여 35mA에서 젤을 실행합니다. 50 kDa의에서 단백질을 감지합니다.
- 단백질 농도가 상용 가능한 BSA-키트를 사용 확인하십시오. 피펫 희석하여 단백질 시료 50 μL (1 : 100, 1 : 200, 1 : 500) 및 BSA 표준 (0, 20, 30, 40, 50, 60, 80, 100 mg을 용액 1) 96 웰 플레이트 . 브래드 포드 시약 200 μL를 추가 형광 계 15 분 후에 595 nm에서 흡광도를 측정하여 표준 곡선을 이용하여 농도를 구한다.
2. 라이트 촉매 생물 전환
- 과산화수소를 첨가하지 않은 생 촉매 반응
- 증류수 10 % (V / V) TERGITOL 0.0284 g 및 스테아르 산을 첨가하여 10 mM의 스테아린산 (M 연구 284.5 g 몰 -1)의 10 ㎖의 스톡 용액을 제조 하였다. 지방산이 완전히 용해 될 때까지 60 ° C로 가열 챔버 내의 용액을 가열한다.
- 생물 촉매 및 샘플링
- 50 mM의 EDTA, 0.01 mM의 FMN, 트리스 - 염산 완충액 0.5 mM의 스테아르 산을 포함하는 두 개의 2 ml의 반응 혼합물을 준비합니다. 충분한 산소 공급을위한 자기 교반 막대를 추가하고 25 ° C로 가열 수조의 유리 튜브를 배치합니다.
- 반응 혼합물의 각 정제 효소의 200 μg의 용액 -1 또는 10 % (v / v)의 무 세포 추출액을 첨가하고, 반응 튜브 15cm 거리에서 투명 유리 전구 (120 W)로 조명.
- 20 μl의 37 % HCl로 반응 중지 특정 시점 (0, 10, 30, 60, 120 분, 밤 이상) 200 μL 샘플을 가져 가라. 5 μL 미리스트 산을 추가 (10 mM의 재고 그래서내부 표준으로 lution).
- 반응 생성물의 분석
- 추출을 위해, 두 샘플을 500 ㎕의 에틸 아세테이트를 추가 13,000 x g에서 1 분간 원심 분리 튜브를 반전한다.
- 상층 액 400 μl를 벗고 용매를 완전히 증발 할 수 있습니다.
- (트리메틸 실릴) 트리 플루오로 아세트 아미드 (MSTFA) - N - 메틸 - 200 μL를 첨가하여 N trimethylsilylcarboxylic 산에 카르복시산 유도체 화. 에테르 트리메틸 수산기로 변환하기 위해 30 분 동안 60 ° C에서 상기 용액을 인큐베이션.
- GC / FID로 전환 결정
참고 : / FID를 GC를 사용하여 : 기판 (12.05 및 12.1 분 RT) 및 감소, α-와 β 히드 록시 스테아르 산 (11.15 분 RT) : 1 헵타 데센 (8.34 분 RT)의 형성을 결정합니다.- 340 ℃로 설정 아래의 주입 온도를 설명하는 온도 프로파일을 설정한다. 보류초기 오븐 온도는 3.5 분 동안 90 ° C에 있고, 그 후 45 ° C의 분 -1로 증가한다. 220 ° C에서 2 분 동안 온도를 유지. 45 ° C의 분 -1의 반복 된 증가 후 2 분 동안 280 ° C의 온도를 유지하고 분 -1 60 ° C로 증가한다.
참고 : 330 ° C의 최대 온도는 1.44 분 동안 유지된다. - 캐리어 가스 헬륨과 급격한 휘발 균질 혼합을 얻기 위해 (5)의 분할 비와, 샘플 4 μl를 주입한다.
주 : 증가하는 온도에 의존하여 기판 제품의 기상을 입력한다. 물질은 특정 체류 시간에서 컬럼을 통과 한 후 GC / FID 검출기에 의해 검출되고, 화면의 피크를 표시한다. 모니터의 피크 형성을 관찰한다. - 다음 식에 의해 형성된 생성물의 농도를 계산한다 :
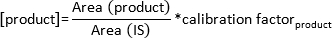
주 : 보정 계수가 유도 물질 및 해당 피크 면적의 알려진 양으로부터 표준 곡선을 계산함으로써 각각의 기판 및 제품이 열에 대한 구체적 결정되었다.
- 340 ℃로 설정 아래의 주입 온도를 설명하는 온도 프로파일을 설정한다. 보류초기 오븐 온도는 3.5 분 동안 90 ° C에 있고, 그 후 45 ° C의 분 -1로 증가한다. 220 ° C에서 2 분 동안 온도를 유지. 45 ° C의 분 -1의 반복 된 증가 후 2 분 동안 280 ° C의 온도를 유지하고 분 -1 60 ° C로 증가한다.
- GC / MS에 의해 올레핀 및 β-하이드 록시 산 봉우리를 식별합니다.
- GC / MS에 의해 올레핀 및 β-하이드 록시 산 봉우리를 식별합니다. 온도 프로파일을 설정합니다. 250 ° C까지 주입 온도를 설정합니다. 5 분 동안 100 ° C의 오븐 온도를 잡고 이후 20 ° C의 분 -1로 증가한다.
참고 : 최대 온도는 7.5 분 동안 유지된다. - 250 ° C의 질량 분석 검출기 온도를 설정하고 전자 충격 모드에서 50 ~ 500 m / z에서 검색합니다.
참고 : 전자 충격 이온화 질량 분석을 위해 앞으로 전달됩니다 라디칼 양이온의 형성의 결과로 하나의 전자를 제거합니다. 때문에 내 높은 intramolar 에너지 공유 결합에낮은 m / z의 조각을 만드는 분자 휴식. 이러한 단편은 물질에 특이적인 핑거 프린트를 형성한다. - 샘플 1 μl를 주입한다. 해당 핑거 (도 2) 11.4 분 체류 시간 후, 1- 헵타 데센을 검출한다.
- GC / MS에 의해 올레핀 및 β-하이드 록시 산 봉우리를 식별합니다. 온도 프로파일을 설정합니다. 250 ° C까지 주입 온도를 설정합니다. 5 분 동안 100 ° C의 오븐 온도를 잡고 이후 20 ° C의 분 -1로 증가한다.
결과
반응 혼합물에 과산화수소를 첨가 전환 (<10 %) 중저 결과 동안 과산화수소 시츄 생성에 80 % 전환으로 전환 증가했다. GC / MS에 의한 분석은 지방산으로부터 올레핀의 형성 (도 2)을 나타낸다.
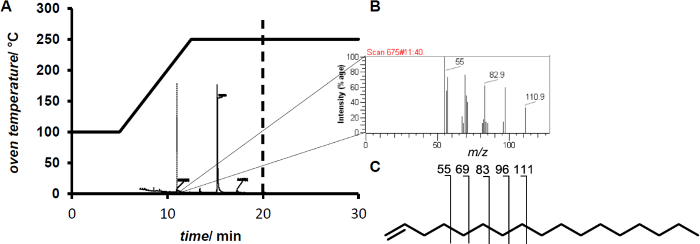
GC / MS 측정을위한 그림 2. (A) 온도 프로파일. 11.4 분 후, 1- 헵타 데센 용출 (B) 지문. (C) 1 헵타 데센에 대해 표시 단말기 올레핀 예시의 특성 보조 C n 개의 H 2N-1 조각 이온. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
빛 - 촉매 반응은 E.의 무 세포 추출물 높은 전환을 달성 대장균. 정제 된 효소 용액 농도 효소 및 전환 사이에 명확한 상관 관계를 보였다. 높은 전환으로 빛 수확 분자 FMN 리드의 농도를 증가. 그러나, 상기 과산화수소의 양이 충분히 가능하고 더 이상 제한 요소가 있음을 나타내는 반응을 촉진하지 않았다 10mM의 상기 농도를 증가시킨다.
지방산의 탈 카르 복 실화 외에도 OleT JE는 β 위치에서의 히드 록 실화를 촉매한다. 스테아르 산의 전환에있어서, 탈 카르 복 실화는 수산화보다 약 3 배 빠르다. 0.5 mM의 스테아르 산의 용액을 10 μM FMN를 이용한 전형적인 실험에서, 상기 기판의 99 %의 비율로 1- 헵타 데센, 2- 히드 록시 스테아르 산의 혼합물로 전환시켰다3.3 : 1 (그림 3) 8. 광 구동 생물 촉매의 기판 스펙트럼의 조사 생성물 혼합물에서 하이드 록실 지방산의 상대적인 양이 짧은 사슬 길이가 증가하면서 이상 아실 체인 지방산 들어 OleT JE 우선적 상기 탈 카르 복 실화를 촉매하는 것으로 나타났다. 미리스트 산 (C14)보다 짧은 지방산은 탈 카르 복 실화를 겪지 않았다.
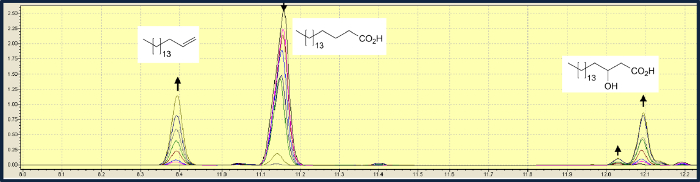
OleT JE 그림 3. 가스 크로마토 그래피 분석은 1 헵타 데센 (8.4 분), α-하이드 록시 스테아르 산 (12.04 분) β 히드 록시 스테아르 산 (12.1 분)에 스테아르 산 (11.15 분)의 탈 카르 복 실화를 매개 성. 2 시간의 시간에 걸쳐 촬영 한 샘플의 피크 면적의 변화가 표시됩니다. 경쟁하려면 여기를 클릭하십시오이 그림의 WA 더 큰 버전.
놀랍게도, 불포화 지방산 (C18 : 1d9 CIS) 올레산 및 리놀레산 (C18은 : 2d9d12) 시스 이중 결합의 꼬임 구성이 효소의 생산 결합 모드에서 수용 할 수없는 것을 나타내는 기재로 인정되지 않았다. 올레인산 (10 %)의 첨가는 또한 스테아르 산의 전환을 막았다. 흥미롭게도, 스테아르 산 (C18 : 1d9 트랜스) OleT JE에 의해 변환, 아직 다음 약간 낮은 활동 스테아르 산 하였다.
토론
과산화수소의 광 중심 세대 peroxygenases 3 포함한 다양한 산화 환원 변형을인가하고 10 chloroperoxidases P450 모노 옥 시게나 제 (5)는 수있다. 그것은 간단하고 실용적인 방법입니다. 장기적으로, 가시 광선의 사용은 에너지가 풍부한 반응을위한 지속 가능한 대안 화학 변환에 대한 태양 광을 활용하는 관점을 엽니 다.
이 방법은 정제 된 효소 또는 무 세포 추출물과 함께 적용 할 수있다. 후자는 적은 비용 및 작업이 필요하지만, 상기 조 추출물에서 작은 분자의 광 촉매 전환을 방해 할 수 있음을 유의해야한다. 실용적인 방법은 (a 원심 필터 유닛 또는 투석하여 원심 분리에 의해, 예)는 micromembrane 이러한 작은 구성 요소를 제거하는 것이다. 광 수확 FMN 분자의 농도는, 과산화수소의 농도를 결정한다. AFFINI에 따라산화 환원 효소의 타이,이 농도는 효소 활성에 대한 결정적이다. 또 다른 중요한 인자는 희생 전자 공여체 EDTA의 농도이다. 가장 중요한 파라미터는, 그러나, 효소의 작동 안정성 및 활동이다.
지방산 olefinization 화학 산업의 중요한 상품에 속해 올레핀으로 바이오 기초 지방산의 전환을위한 우아한 반응이다. 광 기반 생 촉매 탈 카복실 실온에서 지속성면에서 명확한 이점을 제공 중성 pH에서 수행 될 수있다.
우리의 결과는 과산화수소 인 시츄 생성에 하이 전환으로 효소의 안정성을 손상시키지 않고 보조인을 공급하는 전략을 보여준다. 보조 인자 재생을위한 본 발명의 방법은 농산물이나 석유 기반 화학 물질을 사용합니다. 라이트 기반의 반응은 신 재생 대안으로 부상하고있다. 미래연구 저렴 분자 희생 시약 EDTA를 교체하기위한 방법에 전용되며 광 수확 FMN 분자의 양을 감소.
공개
The authors declare that they have no competing financial interests.
감사의 말
R.K. and F.H. are grateful for the EU-commision for financial support within the Marie-Sklodowska ITN Biocascades (Nr. 634200).
자료
| Name | Company | Catalog Number | Comments |
| Chemicals | |||
| Ampicillin | Sigma Aldrich | 69-52-3 | |
| Bradford reagent | Roth | K015.1 | |
| BSA | Sigma Aldrich | 90604-29-8 | |
| DMSO | Sigma Aldrich | 67-68-5 | |
| Ethyl acetate | Fisher Chemical | 141-78-6 | |
| Ethylenediaminetetraacetic acid (EDTA) | Roth | 8043.1 | |
| Riboflavin 5-monophosphate sodium salt hydrate | Sigma Aldrich | 130-40-5 | |
| Hydrochlorid acid 37% | Sigma Aldrich | 7647-01-0 | |
| Hydrogen peroxide 30% | Sigma Aldrich | 7722-84-1 | |
| δ-Amino levulinic acid | Sigma Aldrich | 5451-09-2 | |
| N-Methyl-N-(Trimethylsilyl)trifluoro acetamide (MSTFA) | Sigma Aldrich | 24589-78-4 | |
| Myristic acid >99% | Sigma Aldrich | 208-875-2 | |
| Imidazole | Sigma Aldrich | 288-32-4 | |
| Sodium chloride | Fisher Chemical | 7647-14-5 | |
| Stearic acid >99% | Sigma Aldrich | 57-11-4 | |
| Tetracycline | Sigma Aldrich | 60-54-8 | |
| Tergitol | Sigma Aldrich | MFCD01779855 | |
| Tris(hydroxymethyl)-aminomethan | Sigma Aldrich | 77-86-1 | |
| Device | |||
| Incubator shaker | G-25CK | New Brunswick Scientific | |
| Ecotron | Infors HT | ||
| Centrifugation | Labofuge 400R | Heraeus | |
| RC 5B Plus | Sorvall | ||
| Fresco 17 | Thermo Scientific | ||
| Centrifugation rotors | SS34 | Sorvall | |
| SLA | Sorvall | ||
| Clean bench | Envirco | Ceag Schirp Reinraum technik | |
| Column GC-FID | CP-Sil 5CB (30 m x 0.25 mm x 0.25 µm) | Agilent Technologies | |
| Column GC-MS | FactorFour Capillary Coloumn (VF-5 ms + 5 m EZ Guard) | Varian | |
| GC-FID | GC-2010 plus | Shimadzu | |
| GC-MS | IST-40 | Varian | |
| Magnetic stirrer | RCT classic | IKA | |
| pH meter | SevenEasy | Mettler toledo | |
| Sonicator | Branson Sonifier 250 | Branson | |
| Spectral photometer | FLUOstar Omega | BMG Labtech | |
| Equipment | |||
| Affinity chromatography column | His Pur Ni-NTA spin column | Thermo Scientific | |
| Centricon | Vivaspin turbo 15 | VWR International | |
| Microtiter plates | 96 Well Multiply®PCR Plates | Sarstedt |
참고문헌
- Kourist, R., Domìnguez de Marìa, P., Miyamoto, K. Biocatalytic strategies for the asymmetric synthesis of profens - recent trends and developments. Green Chem. , 2607-2618 (2011).
- Holtmann, D., Fraaije, M. W., Arends, I. W., Opperman, D. J., Hollmann, F. The taming of oxygen: biocatalytic oxyfunctionalisations. Chemical Comm. 50, 13180-13200 (2014).
- Churakova, E., et al. Specific photobiocatalytic oxyfunctionalization reactions. Ang. Chem. In. Ed. 123, 10904-10907 (2011).
- Hollmann, F., Arends, I., Buehler, K. Biocatalytic Redox Reactions for Organic Synthesis: Nonconventional Regeneration Methods. ChemCatChem. 2, 762-782 (2010).
- Girhard, M., Kunigk, E., Tihovsky, S., Shumyantseva, V. V., Urlacher, V. B. Light-driven biocatalysis with cytochrome P450 peroxygenases. Biotechnol. Appl. Biochem. 60, 111-118 (2013).
- Bartsch, M., et al. Photosynthetic production of enantioselective biocatalysts. Microb. Cell. Fact. 14, 53 (2015).
- Rude, M. A., et al. Terminal olefin (1-alkene) biosynthesis by a novel P450 fatty acid decarboxylase from Jeotgalicoccus species. Appl. Environ. Microbiol. 77, 1718-1727 (2011).
- Zachos, I., et al. Photobiocatalytic decarboxylation for olefin synthesis. Chem. Comm. 51, 1918-1921 (2015).
- Liu, Y., et al. Hydrogen peroxide-independent production of α-alkenes by OleTJE P450 fatty acid decarboxylase. Biotechnol. Biofuels. 7, 28 (2014).
- Perez, D. I., Grau, M. M., Arends, I. W., Hollmann, F. Visible light-driven and chloroperoxidase-catalyzed oxygenation reactions. Chem. Comm. 40 (44), 6848-6850 (2009).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유