Method Article
Geração Teratoma na Cápsula do Testículo
Neste Artigo
Resumo
As células pluripotentes humanas estaminais (hPSCs) têm o potencial para tratar uma miríade de diferentes doenças. A utilidade destas células reside no facto de que eles podem diferenciar-se em qualquer tipo de célula no corpo. Descrevemos aqui o ensaio teratoma, que é usado para demonstrar a pluripotência das hPSCs.
Resumo
As células estaminais pluripotentes (PSC) têm a característica única que eles podem diferenciar em células de todas as três camadas germinais. Isto torna-os de uma ferramenta potencialmente útil para o tratamento de muitas doenças diferentes. Com o advento das células pluripotentes induzidas estaminais (iPSCs) e pesquisa de continuar com células estaminais embrionárias (hESCs), há uma necessidade de ensaios que possam demonstrar que uma linha de células particular é pluripotentes. Transmissão germinativa tem sido o padrão ouro para demonstrar a pluripotência das células-tronco embrionárias do rato (MESC) linhas 1,2,3. Utilizando este ensaio, os investigadores podem mostrar que uma linha de MESC pode fazer todos os tipos de células no embrião incluindo células germinativas 4. Com a geração de linhas humano ESC 5,6, o ensaio apropriado para provar pluripotência destas células era clara, uma vez CES humanos não podem ser testados para a transmissão da linha germinativa. Como um substituto, o ensaio de teratoma é actualmente utilizado para demonstrar a pluripotrência de células-tronco pluripotentes humanas (hPSCs) 7,8,9. Embora este ensaio tem vindo recentemente sob escrutínio e novas tecnologias estão sendo ativamente explorados, o ensaio de teratoma é o padrão ouro atual 7. Neste ensaio, as células em questão são injectados um rato imune comprometida. Se as células são pluripotentes, um teratoma desenvolverá eventualmente e secções do tumor irá mostrar tecidos a partir de todas as 3 camadas germinais 10. No ensaio de teratoma, hPSCs pode ser injetado em diferentes áreas do mouse. Os locais de injecção mais comuns incluem a cápsula testículo, a cápsula do rim, o fígado, ou para a perna por via subcutânea ou por via intramuscular 11. Descrevemos aqui um protocolo robusto para a geração de teratomas de hPSCs utilizando a cápsula testículo como o local para o crescimento do tumor.
Protocolo
Nota: Todos os procedimentos com animais devem ser aprovados pelo IACUC ou equivalente.
Todo o equipamento cirúrgico deve ser esterilizado antes da cirurgia. Luvas estéreis, cortinas e gaze deve ser usada.
1. Preparação antes da cirurgia
- Obtenha 6 semanas de idade Mus musculus CbySmn.CB17-Prkdc SCID / J camundongos machos ou estirpe imunocomprometidos outro rato.
- Esterilizar todos os instrumentos cirúrgicos, luvas e gaze.
- Dissociar hPSCs ser injetados com accutase.
- Contar as células e ressuspender 1.000.000 células por 20-30 uL em Matrigel diluído 1:1 em DMEM/F-12. Manter as células no gelo até terminar.
- Note-se que muitas vezes é útil para fazer uma corrida através do experimento, onde Trypan Blue é injectado. Isso vai ajudar a identificar problemas potenciais antes que as células são desperdiçados.
- No biotério, anestesiar o mouse de acordo com procedimentos aceitos de sua instituição. Em nossos experimentos, utilizamos uma AnesthESIA máquina com isoflurano. Os camundongos foram inicialmente colocadas em uma câmara de indução com o oxigênio 1l/min e 3-4% de isoflurano. Uma vez anestesiados, com um cone de nariz 1l/min oxigénio e 2-3% de isoflurano foi usado.
- Raspar o abdómen com tesouras, e limpar a parede anterior do abdómen do rato, a partir do centro do abdómen e de trabalho dos ponteiros do relógio para o exterior. Primeiro uso da solução de iodo-povidona, em seguida, lavar com etanol 70%. Repita 3 vezes, mudando esfregaços de cada vez. Transferir o animal a uma almofada de aquecimento para manter o animal quente no interior de uma cultura de tecidos ou capuz de dissecação.
- Fazer uma incisão 1 centímetro longitudinal através da pele e do peritoneu com tesouras cirúrgicas estéreis imediatamente abaixo do nível da articulação da anca.
- Enquanto mantém o peritônio com uma pinça, descem em direção ao quadril direito com outro forcept estéril e puxe o tecido adiposo branco, juntamente com testículos conectados.
- Coloque os testículos em gaze estéril.
- Encha uma tuberculina ou Hamilton (1cc) seringa wiº os hPSCs a ser injetado. Note que é uma boa idéia de incluir um controle de linha hPSC que você sabe que é pluripotente, como WA09 (também conhecido como H9). Desta forma, você tem um controle positivo que você pode usar para determinar se a injecção ou a cirurgia foi falha.
- Lentamente injectar as hPSCs (20-30 uL) para o centro da cápsula testículo longe de qualquer vasos sanguíneos principais, parando se a cápsula testicular começa a inchar.
- Remover a agulha lentamente para evitar o refluxo das células.
- Usando uma pinça, transferir os testículos e costas tecido adiposo à sua posição original no abdómen.
- Fechar o peritônio com 2 ou 3 suturas reabsorvíveis e feche a pele com autoclips.
- O mouse deve ser mantido quente até ele se recupera e dado algum tipo de analgésico (ver o que é aceito em seu viveiro) após a cirurgia duas vezes ao dia por 1-2 dias.
Note-se que nem o anestésico nem o analgésico com interferir com o desenvolvimento do tumor. - Monitorar ªanimais e para o crescimento do tumor por 6-12 semanas. Muito raramente, os tumores podem crescer a 5 mm de tamanho antes de 6 semanas após a injecção, assim, é importante para monitorar os animais. Se isso acontecer, os animais devem ser sacrificados e os tumores tratados e analisados como de costume.
- Uma vez que o tumor é palpável e atinge aproximadamente 5 mm de tamanho, anestesiar o rato e sacrificá-lo de acordo com procedimentos aceitos protocolos animais.
- Remover tumor e documento nesse sentido - tamanho medida, fotografia, pesar.
- Corte tumor em pedaços pequenos e fixar em solução de paraformaldeído 4%. Armazenar em paraformaldeído a 4% até amostras são enviadas para um patologista para seccionamento de coloração, e análise.
2. Resultados representativos:
Quando este protocolo é feita como descrito ea linha de células injectadas é pluripotentes, uma palpável, visualmente óbvia do tumor, deverá formar dentro de 12 semanas, no máximo. Para estabelecidas linhas hPSC como WA09, que se costuma vertumores em 6 semanas. Para as linhas de IPSC, não é incomum para ver tumores dentro de 8-10 semanas. É muito importante para injectar ratinhos com uma linha que é conhecido por ser pluripotentes, como um controlo positivo, a fim de ter a certeza de que o procedimento foi realizado correctamente. Tumores costumam olhar muito heterogênea e têm muitos cistos em anexo (Figura 1). Análise das amostras de tumor por um patologista deveria mostrar tecidos diferenciados a partir de todas as três camadas germinais (Figura 2).
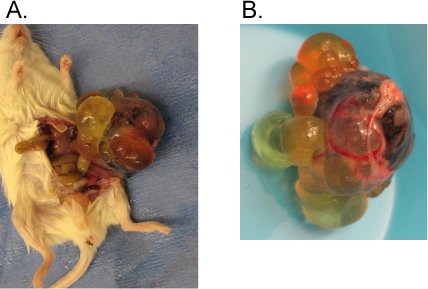
Figura 1. Teratoma hPSC típica derivado na cápsula testículo.
Seguindo o protocolo descrito, um milhão de WA09 células foram injectadas na cápsula testículos de um rato imune comprometida. Seis semanas mais tarde um teratoma foi observada. A) Teratoma puxado do rato. B) Feche acima do retrato do teratoma. Observe as estruturas de heterogeneidade e cisto.

Figura 2. Hematoxilina e Eosina seções do teratoma mostram tecidos de cada camada germinativa.
Após a fixação, o teratoma foi seccionado e corado com hematoxilina e eosina. Análise por um patologista revelou a presença de células de cada uma das 3 camadas germinais.
Discussão
O método aqui apresentado fornece um altamente confiáveis, simples meios de geração de teratomas de hPSCs na cápsula testicular. Existem vários parâmetros críticos nesta técnica. Em particular, é importante para injectar linhas celulares hPSC que são conhecidos por serem pluripotentes como controlo. Outros parâmetros importantes incluem o intervalo de tempo entre a injecção ea observação do tumor. Para linhas de células como WA09, teratomas deve ser observado em 6-8 semanas. Para novas linhas de IPSC, descobrimos que muitas vezes são necessárias 10 semanas. Outra preocupação é o número de células injectadas. Nós injetar um milhão de células, mas o teste pode ser feito facilmente com poucas células. Além disso, o meio de injecção é importante. Nós descobrimos que os melhores resultados quando as células são injectadas numa mistura 1:1 de matrigel e DMEM/F-12, em oposição a PBS ou DMEM/F-12.
Divulgações
Não há conflitos de interesse declarados.
Agradecimentos
Este trabalho foi financiado por doações CIRM # TR-1250, RT1-01108, e CL1-00502.
Materiais
| Name | Company | Catalog Number | Comments |
| Nome do reagente | Companhia | Número de catálogo | |
| Accutase | Invitrogen | A1110501 | |
| DMEM/F-12 | Invitrogen | 113300-032 | |
| Matrigel | BD Biosciences | 354277 |
Referências
- Bradley, A., Evans, M., Kaufman, M. H., Robertson, E. Formation of germ-line chimaeras from embryo-derived teratocarcinoma cell lines. Nature. 309, 255-255 (1984).
- Evans, M. J., Kaufman, M. H. Establishment in culture of pluripotential cells from mouse embryos. Nature. 292, 154 (1981).
- Martin, G. R. Isolation of a pluripotent cell line from early mouse embryos cultured in medium conditioned by teratocarcinoma stem cells. Proc. Natl. Acad. Sci. U. S. A. 78, 7634-7634 (1981).
- Downing, G. J., Battey, J. F. Technical assessment of the first 20 years of research using mouse embryonic stem cell lines. Stem Cells. 22, 1168-1168 (2004).
- Thomson, J. A. Embryonic stem cell lines derived from human blastocysts. Science. 282, 1145-1145 (1998).
- Reubinoff, B. E. Embryonic stem cell lines from human blastocysts: somatic differentiation in vitro. Nat Biotechnol. 18, (2000).
- Muller, F. J., Goldmann, J., Loser, P., Loring, J. F. A call to standardize teratoma assays used to define human pluripotent cell lines. Cell Stem Cell. 6, 412-412 (2010).
- Brivanlou, A. H. Stem cells. Setting standards for human embryonic stem cells. Science. 300, 913-913 (2003).
- Lensch, M. W., Schlaeger, T. M., Zon, L. I., Daley, G. Q. Teratoma formation assays with human embryonic stem cells: a rationale for one type of human-animal chimera. Cell Stem Cell. 1, 253-25 (2007).
- Gertow, K. Organized development from human embryonic stem cells after injection into immunodeficient mice. Stem. Cells. Dev. 13, 421-421 (2004).
- Gertow, K. Isolation of human embryonic stem cell-derived teratomas for the assessment of pluripotency. Curr Protoc Stem Cell Biol. Chapter 1, Unit1B 4-Unit1B 4 (2007).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados