Method Article
Estimulação do nervo vago como uma ferramenta de neuroestimulação adjuvante na depressão tratamento-resistente
Neste Artigo
Resumo
Estimulação do nervo do vagus (VNS) foi mostrada para ser eficaz como um tratamento adjuvante para a depressão tratamento-resistente (TRD). VNS conduz a efeitos antidepressivos e antisuicidal e melhorias de qualidade de vida. Este protocolo oferece um passo-a-passo guia para gerenciar e ajustar um estimulador de nervo vago para o tratamento eficiente de TRD.
Resumo
Estimulação do nervo do vagus (VNS) é uma terapia de neuroestimulação aprovados. O objetivo do método é tratar pacientes com depressão resistente a terapia (TRD). VNS exibe efeitos antidepressivos e estabilizadores. Este método é particularmente útil como um tratamento a longo prazo, em que até dois terços dos pacientes respondem. O estimulador de nervo vago é posicionado sobre o nervo vago esquerdo durante um procedimento cirúrgico e é ativado telemetrically por uma varinha conectada a um dispositivo computadorizado portátil. O médico pode realizar vários ajustes do estimulador de nervo vago durante visitas em exercício (por exemplo, modificando a frequência de estimulação de intensidade ou estimulação) para alcançar a máximos efeitos terapêuticos com baixos efeitos colaterais. Configuração do dispositivo, geralmente, leva vários meses. Efeitos colaterais típicos incluem infecção da ferida, temporária salivação, tosse, paralisia de cordas vocais, bradicardia ou assistolia mesmo. O paciente pode parar o VNS colocando um ímã sobre o gerador. O atual protocolo descreve a entrega dos métodos para ajustar os parâmetros de ajuste para conseguir as melhores taxas de remissão em pacientes com TRD e ferramenta de estimulação específica.
Introdução
Principais doenças depressivas (MDD) é frequentemente recorrentes ou doença psiquiátrica crônica com alta prevalência de1,2 e é caracterizada por alterações de afeto e humor. De extrema importância é a associação de MDD com altas taxas de suicídio e mortalidade3,4,5,6. Estratégias de tratamento farmacológico incluem inibição de recaptação de neurotransmissores monoamina [por exemplo, o tratamento com inibidores seletivos da recaptação da serotonina (SSRIs) e inibidores da recaptação de serotonina-noradrenalina (ISRNs)], aumento do lítio, ou aumento dos antipsicóticos atípicos estratégias7,8. Além do tratamento farmacológico, abordagens psicoterapêuticas e suplementares estratégias não-invasivas são usadas para tratar o MDD8,9,10. Estratégias alternativas como terapia baseada em luz, exercício, acupuntura e ioga também têm sido utilizadas com sucesso no tratamento de MDD8,9,11,12; embora, estas não são métodos aprovados. No entanto, até 30-50% de todos os pacientes com MDD não atingir remissão com opções de tratamento disponíveis atualmente13. Este subtipo de MDD é chamado depressão resistente a terapia (TRD)14,15,16. TRD é definida como a falha de dois ensaios sucessivos do tratamento antidepressivo, administrado em uma dose apropriada e para um suficiente duração17,18,19.
A alta taxa de TRD representa um desafio na gestão global de pacientes com MDD13; assim, terapias inovadoras complemento para TRD são urgentemente necessárias. Neuroestimulação ferramentas tais como a eletroconvulsoterapia (ECT), estimulação transcraniana de corrente contínua (tDCS), estimulação magnética transcraniana repetitiva (rTMS), estimulação cerebral profunda (DBS), terapia magnética apreensão (MST), eletroterapia craniana ( CES), e a estimulação do nervo do vagus (VNS) são ferramentas clinicamente disponíveis e promissoras no arsenal psiquiátrica para pacientes com TRD20. VNS é particularmente útil em TRD e exibe o antidepressivo e estabilizar os efeitos de humor. Durante o tratamento a longo prazo (> 12 meses), até a dois terços dos pacientes têm respondido favoravelmente21,22,23. A associação americana de psiquiatria recomenda o uso de VNS como uma opção de tratamento após tratamento quatro falhas22.
Neste estudo, nós esboçamos um protocolo para os clínicos, descrevendo como usar e configurar o instrumento VNS para o tratamento contínuo de TRD. Notas adicionais sobre componentes de hardware estão incluídas para ajudar os leitores a escolher o produto que melhor se adapte às necessidades do paciente.
Protocolo
O protocolo seguinte fornece um manual passo a passo para usar o VNS no tratamento contínuo de TRD. O protocolo baseia-se principalmente nas experiências e recomendações dos autores dos diferentes centros psiquiátricos na Alemanha. O protocolo segue as diretrizes do Comitê de ética de pesquisa humana da nossa instituição.
1. pré-operatório exame
Nota: Antes de executar etapas pré-operatória, os pacientes devem ser avaliados para conformidade contínua e vontade de participar regular (e provavelmente irregular) controle e ajuste de visitas após a implantação. Em particular, os aspectos de conformidade após implantação exigem consideração cuidadosa.
-
Contra-indicações
- Antes da implantação, exclua contra-indicações para a terapia VNS como suicídio agudo, dependência de substância e difícil de tratar e documentada não-conformidade ou não-adesão durante tratamentos psiquiátricos e/ou somáticos anteriores.
Nota: Transtorno bipolar e sintomas depressivos psicóticos não são contra-indicações para a terapia VNS.
- Antes da implantação, exclua contra-indicações para a terapia VNS como suicídio agudo, dependência de substância e difícil de tratar e documentada não-conformidade ou não-adesão durante tratamentos psiquiátricos e/ou somáticos anteriores.
-
Exame neurocirúrgico
- Após a indicação positiva psiquiátrica e avaliação, consulte os probandos avaliação cirúrgica para determinar as contra-indicações do ponto de vista cirúrgica e, em seguida, avaliar a elegibilidade para anestesia geral.
2. ato cirúrgico
-
Implantação
- Administre anestesia geral endo-traqueal para o paciente, usando as técnicas padrão. Use o propofol (4-12 mg/kg/h iv) para anestesia geral. Adicionar um medicamento analgésico (por exemplo, remifentanyl em 1 µ g/kg/min iv) e um relaxante muscular (por exemplo, rocurônio em 0,6 mg/kg iv).
- Posicione o paciente em decúbito dorsal na mesa de operação. Rode a cabeça ligeiramente para a direita. Prepare o lado esquerdo do pescoço para implantação de chumbo supraclavicular e uma abordagem infraclavicular ou axilar para o gerador.
- Use um agente específico para preparação da pele para evitar infecção cirúrgica de lado. Esfregue a pele com uma base aquosa Iodofor como povidone-iodo (PVP-eu).
- Realizar uma incisão axilar, seguindo uma linha de pele. Após hemostasia, disse sem rodeios a gordura subcutânea para liberar a fáscia grande peitoral e formam um espaço para o gerador.
- Fazer uma incisão oblíqua na pele de 4 cm aproximadamente a meio caminho entre a mastoide e a clavícula, com a borda medial do músculo esternocleidomastoideo no centro. Em seguida, dividir o músculo platisma e dissecar a fáscia cervical.
- Palpe a artéria carótida para identificar com segurança o compartimento correto neuro-vasculares. Depois de abrir a camada profunda da fáscia cervical, retraia cuidadosamente a artéria carótida e a veia jugular interna. O nervo vago pode ser encontrado entre e abaixo os vasos.
Nota: Neste ponto, nós geralmente continue o procedimento com microscópios de funcionamento. -
Disse o nervo vago longitudinalmente por aproximadamente 4 a 5 cm, poupando todos os ramos e cuidadosamente evitando danos para o vasa nervorum.
- Trazer a liderança no lugar de infra - a supra-clavicular usando o dispositivo tunneller, permitindo a implantação.
- Cuidadosamente enrole a corda de âncora inferior do VNS chumbo em torno do aspecto caudal do nervo vago e, em seguida, fixar os eletrodos de contato de positivos e negativos no nervo. Introduza o pino do conector do gerador infraclavicularly.
- Após o teste (veja abaixo), fixe o chumbo com as cordas, facilitando um "loop de reposição". Isso permite que o paciente a mover a cabeça sem tethering a sonda. Sutura do gerador para a fáscia do músculo grande peitoral.
Nota: É importante colocar os eletrodos inferiores aos ramos do nervo vago para evitar cardíacos efeitos colaterais cardíacos.
-
Teste de chumbo intra-operatória
Nota: É necessário primeiro realizar um teste no intra-operatório (chumbo), que deve excluir os efeitos colaterais mais comuns e graves. Mais notavelmente, assistolia pode ocorrer quando o VNS é ativado no intra-operatório.- Ensaios in situ
- Conecte a varinha programação do VNS, mantendo a esterilidade no intraoperatório in situ. Realizar testes de chumbo com um mínimo de 10 segundos de estimulação de 0,5 m a 1,0 mA e 25 Hz. Se não há efeitos colaterais cardíacos graves ocorrerem, proceda ao teste de impedância.
- Ensaios in situ
-
Interpretação de testes de impedância intra-operatória
- Verifique a impedância durante os testes no local do dispositivo. Verifica repetidamente.
Nota: Impedâncias de altas (> 1.700 – 2.000 Ω) indicam mau contacto entre os eléctrodos helicoidais e o nervo. Durante esta fase, o anestesiologista deve estar preparado para a ocorrência de bradicardia ou assistolia mesmo. Impedância é testada por um período máximo de cinco segundos, com saída de corrente de 2,00-3,00 mA e deve estar abaixo dos 100 Ω.
- Verifique a impedância durante os testes no local do dispositivo. Verifica repetidamente.
-
Os eletrodos de fixação após a implantação
- Use um tunneller para posicionar o papel de principal estimulador, passando-o do bolso torácico subcutâneo para a incisão cervical.
- O fio do túnel e finalmente, fixe as voltas ao redor do nervo para reduzir a probabilidade de desalojar o eletrodo.
-
Os procedimentos operacionais de acabamento
- Crie uma curva de alívio de tensão para fornecer folga durante os movimentos do pescoço.
- Fixe o eletrodo por davante suturas para suportes de cabeça de silicone na fáscia cervical profunda e perto do músculo esternocleidomastoideo.
- Consertar a bateria para o eletrodo de chumbo e ancorá-lo com suturas na fáscia. Feche as incisões por técnicas padrão.
3. pós-cirúrgicos e dosagem
-
Quitação
- Descarregue o paciente um dia após a cirurgia, após um raio-x para garantir posicionamento regular do dispositivo.
-
VNS dosagem
- Começar a regular VNS dosagem 2 semanas após a implantação usando as configurações recomendadas de estimulação (1.5 – 3.0 mA; 500 µs pulso largura; 20-30 Hz; 30 s na, 5 min fora), que deve ser alcançada gradualmente com 0,25 – 0,5 mA aumenta por semana.
- Começa a dosagem (recomendado) a 0,25 intervalos de mA conforme necessário e aumento acima de 2,00-3,00 mA. A maioria dos pacientes (> 90%) exigirá a dosagem não superior a 2.00 mA.
-
Dosagem em caso de persistência de sintomas depressivos
- Defina o tempo de ligar/desligar a 30 s em/5 min fora.
- Fim de dosagem quando uma resposta a VNS é alcançado, após um máximo de 9 – 12 meses.
-
Dosagem de alternativas em casos de resposta parcial ou de não-resposta
- Em casos de resposta parcial ou de não-resposta, como uma alternativa para aumentar a corrente de saída (mA), mudar a frequência do sinal (Hz) tuning (normalmente, diminuindo de 30 para 20 Hz) ou reduzir o tempo de folga para 3 min.
-
Dosagem nos casos de efeitos colaterais
- Se ocorrer efeitos secundários (principalmente laryngopharyngeal disfunção como rouquidão, dispneia e tosse), que tendem a ser transitórios e directamente associado à estimulação do nervo laríngeo inferior (recorrente), reduzir o máximo mA afinação (normalmente não inferior a 0,75 mA) e/ou alterar o tempo de ligar/desligar.
Nota: Uma visão geral de adicional do protocolo é fornecida na tabela 2.
- Se ocorrer efeitos secundários (principalmente laryngopharyngeal disfunção como rouquidão, dispneia e tosse), que tendem a ser transitórios e directamente associado à estimulação do nervo laríngeo inferior (recorrente), reduzir o máximo mA afinação (normalmente não inferior a 0,75 mA) e/ou alterar o tempo de ligar/desligar.
Resultados
As medições de resultados de eficácia VNS geralmente incluem um declínio em sintomas depressivos, medidos pelo observador-Pontuação: escalas e/ou instrumentos de avaliação Self avaliado [por exemplo, a escala de classificação de depressão de Hamilton, a classificação de depressão de Montgomery-Åsberg Escala, ou o inventário de depressão de Beck (BDI)]6.
O primeiro julgamento que sistematicamente examinadas VNS em pacientes com episódios depressivos major foi conduzido por Rush et al.24, que usou o VNS como uma estratégia de aumento com uma combinação de 10 semanas de tratamento VNS juntamente com a medicação normal dos pacientes . O placar de escala de classificação de depressão de Hamilton de item de base média 28 foi 38.0. Quarenta por cento dos pacientes responderam favoravelmente, enquanto 17% apresentaram remissão24. Sackheim et al.25 combinado a coorte de estudo inicial com um adicional de 30 pacientes que foram monitoradas por doze semanas. Os autores observaram uma taxa de resposta de 30% e uma taxa de remissão de 15%. Schlaepfer e colegas examinaram os efeitos antidepressivos de VNS em um estudo multicêntrico Europeu aberto, descontrolado. Taxas de resposta e remissão foram 37% e 17%, respectivamente,26. Nomeadamente, no acompanhamento a longo prazo, um aumento nas taxas de resposta e remissão tanto poderia ser observado de27,de23,(Figura 1)28. Em um estudo multicêntrico, controlado por Souza, nenhuma diferença significativa entre os grupos ativos e sham observou-se29. No entanto, os autores só realizaram dez semanas de VNS ativo ou sham. Novamente, observações com remissão mais elevado e taxas de resposta sugerem que o tratamento de VNS tem um efeito benéfico sobre tempo30,31. O registro TRD seguido o curso clínico e prognóstico para TRD pacientes tratados com e sem adjuvante VNS22. No estudo observacional de depressão unipolar ou bipolar, os resultados de 500 pacientes com VNS e 300 com tratamento como de costume foram comparados os pacientes (TAU). Os sujeitos foram autorizados a escolher entre VNS e TAU no momento da triagem. Resultados do registro indicam que o grupo VNS adjuvante tinha melhor os resultados clínicos que o grupo TAU. O ano 5 cumulativo (67,6% em comparação com 40,9%) taxa de resposta e taxa de remissão (43,3% em comparação com 25,7%) foram significativamente maiores no VNS + TAU grupo do que no TAU somente grupo (Figura 2 e Figura 3)22. Além disso, os achados na literatura sugerem que tentativas de suicídio diminuiu, níveis reduzidos de ideação suicida e menos hospitalizações devido a depressão em pacientes com VNS do que naqueles com a mesma severidade de doença, mas quem está a tomar medicamentos 22,32.
A seguir, apresentamos três casos clínicos para destacar os benefícios potenciais, bem como eventuais dificuldades de fornecer terapia de VNS para pacientes com TRD.
Uma mulher de 53 anos com uma história de 20 anos de TRD foi encaminhada para nosso escritório. O tratamento incluiu ensaios ineficazes de antidepressivos tricíclicos, inibidores da recaptação da serotonina, inibidores da recaptação da serotonina-noradrenalina e tratamento adjuvante com agentes antipsicóticos e ansiolíticos. Ela também recebeu uma série de ECT. Embora o suicídio inicialmente remidos, ficou deprimido e ainda mais necessário ECT. ECT foi continuado, mas seu humor melhorou era instável e não resultou em uma diminuição significativa dos medicamentos antidepressivos. Suas características psicopatológicas incluíam sentimentos de inutilidade, baixa auto-estima e falta de energia e motivação diária. Curso de episódios depressivos major resistente ao tratamento do paciente fez de um candidato para a terapia VNS. A paciente foi submetida a implante de dispositivo de terapia VNS por um neurocirurgião durante um procedimento de 1,5 h. O VNS foi verificado para a funcionalidade de inserção. Estimulação foi reativada durante uma visita do escritório dentro de várias semanas. Naquela época, o paciente recebeu adicionalmente sertralina (200 mg/dia). Durante a primeira visita de estimulação, o estimulador de nervo vago foi ajustado para 1,00 mA, 25 Hz e 30 s na/5 min fora. Durante a segunda visita do escritório, a dosagem foi aumentada para 1,50 mA e vários 0,25 mA aumentos foram realizados. O paciente não relataram efeitos colaterais. No prazo de três meses, a corrente tinha sido titulada até uma saída de 1,5 mA, com uma frequência de sinal padrão de 30 Hz, largura de 500 µs e tempo de sinal de 30 s na/5 min fora do pulso. No entanto, naquele tempo, o paciente experimentou apenas pequenas melhorias no humor e qualidade de vida. O BDI mostrou uma ligeira redução da depressão. A corrente de saída foi fixado em 2,25 mA, e durante as duas semanas seguintes, observou-se uma melhoria. Em seguida, adicionado de lítio na dose de 900 mg/dia para os medicamentos dela e diminuiu o VNS fora tempo de 2 min. Durante os próximos três meses, o paciente descrito uma melhora de seu humor e os níveis de energia. Sua pontuação de soma BDI mostrou uma remissão (ou seja,, o paciente já não satisfazia os critérios para depressão maior). Felizmente, ela não tinha experiência eventos adversos ou efeitos colaterais. A medicação foi reduzida a sertralina (100 mg/dia). Talvez use a melhoria mais significativa desde que o ajuste do dispositivo foi a redução da medicação. O paciente é mantido na terapia do antidepressivo com sertralina e lítio. As configurações de dispositivo não foram alteradas novamente. Após o ajuste bem sucedida do estimulador de nervo vago, o paciente participa agora cada seis meses para controle de visitas.
Um paciente cronicamente deprimido de 58 anos de idade foi encaminhada para nosso escritório. Ela tinha experimentado episódios depressivos em curso desde os 15 anos de idade, que requerem vários cursos de ECT. Com cada recaída de depressão grave, ela apresentou de forma característica, ou seja, com períodos de ausência de resposta emocional, apatia, um rosto inexpressivo e olhos esbugalhados. Quando pressionado, ela não se importaria por si mesma, resultando em ingestão oral pobre e perda de peso rápida. Ela também socialmente desacoplado do povo e se recusou a tomar medicação. Ela recebeu várias sessões de ECT de emergência e mostrou uma boa resposta. Durante a última sessão de ECT, o paciente novamente mostrou melhora acentuada. Sua pontuação de BDI foi 46 antes ECT e 18 depois. No entanto, ela se recusou a submeter-se a manutenção ECT. Ela relatou experimentando severa perda de memória e cefaleia após o ECT. O longo e excelente resposta paciente a ECT em termos de efeitos do antidepressivo fez de um candidato para a terapia VNS22. A paciente foi submetida a implante de dispositivo de terapia VNS. O VNS foi verificado para a funcionalidade quando ele foi inserido. Estimulação foi reativada durante um escritório visite mais tarde naquele mês. No momento da iniciação do VNS, a paciente recebeu citalopram (30 mg/dia) e Mirtazapina (60 mg/dia). Durante esta visita, o estimulador de nervo vago foi ajustado para 1,00 mA. No prazo de cinco meses, a corrente tinha sido titulada até uma saída de 2 mA, frequência de sinal padrão de 25 Hz, largura de pulso de 250 µs e tempo de sinal de 30 s na/5 min fora. Seis meses após a implantação do dispositivo VNS, o paciente estava tomando antidepressivos diversos, incluindo o lítio e citalopram. O dispositivo foi implantado há 13 anos. Desde então, os sintomas depressivos do paciente permaneceram estáveis. Ela relatou que o bem-estar subjetivo e sem efeitos colaterais de VNS.
Um homem de 62 anos de idade foi encaminhado para o nosso escritório com uma história de 40 anos de TRD. Devido a gravidade da doença, ele tinha sido um paciente em hospitais psiquiátricos e tinha feito várias tentativas de suicídio graves. Seus sintomas depressivos incluíam humor melancólico, anedonia, perda de apetite com perda de peso consecutivos, diminuição da energia, desespero, delírio niilista e intenções suicidas. Somáticas comorbidades consistiam de hipotireoidismo controlado e controlado epilepsia. A primeira apreensão ocorreu após um traumatismo fechado quando ele tinha 49 anos de idade. O paciente teve sobre as apreensões de média de 3 por ano (tônico-clônica) entre os 49º e 53th aniversários. Ao longo dos anos anteriores, a paciente tinha recebido tratamentos com diferentes combinações de 2 – 5 antidepressivos (por exemplo, citalopram, paroxetina, Fluvoxamina, imipramina, amitriptilina e venlafaxina estendido lançamento) sem remessa completa. Remessa também falhou com ensaios de aumento de antidepressivo com olanzapina, aripiprazol e lítio. Ele também tinha 19 cursos de ECT (bilateral e unilateral) durante o período de 1980 a 2005. O efeito de ECT foi principalmente curta duração, como não foi observado nenhum benefício sustentado ou a longo prazo da ECT. Foi então submetido a uma implantação com um dispositivo VNS para TRD em 2010. Anteriormente, os medicamentos prescritos (ou seja,, duloxetine, quetiapina, lítio e Topiramato) foram alterados. O estimulador de nervo vago foi verificado para a funcionalidade no momento da inserção. Estimulação foi reativada durante um escritório visite mais tarde naquele mês. Durante essa visita, o estimulador de nervo vago foi ajustado para 1,75 mA. Na segunda visita em exercício, a dosagem foi aumentada para 2,00 mA. O paciente não relatou nenhum efeito colateral. Dentro de 14 semanas, a corrente tinha sido titulada até 2,5 mA com uma frequência de sinal padrão de 30 Hz, largura de pulso 500 µs e tempo de sinal de 30 s na/5 min fora. No entanto, durante uma visita em exercício, o paciente relatou uma sensação de globus incomum e rouquidão. Sintomas depressivos claramente melhoraram. O placar de BDI antes da implantação foi 46, mas só 15 no pós-implantação de 14 semanas. Por causa do efeito antidepressivo notável de VNS neste paciente, fizemos apenas pequenas alterações para a configuração VNS. Além disso, o paciente não teve convulsões após a implantação do dispositivo VNS. Durante as seguintes três visitas, que ocorreu ao longo de 2 semanas, nós adaptado a saída de 2 mA e sinal de frequência de 40 Hz e adoptou um extraordinário tempo de 8 min. Com esta configuração, ocorreram efeitos colaterais leves, mas o efeito antidepressivo persistiu. Em conformidade com os desejos do paciente, nós não alterou as configurações do dispositivo.
Estes três pacientes, bem como os outros pacientes recebendo VNS, foram preparados conforme necessário para que necessidades individuais foram abordadas dentro os primeiros seis meses após a implantação do dispositivo. Após os primeiros 6 meses, consultas de acompanhamento devem ser agendadas após 9, 12 e 24 meses, ou quando for necessário um ajuste de dosagem ou dispositivo de manutenção. A instalação deverá ser adaptada a Psicopatologia do paciente, compatibilidade, exame psicológico, somático estatuto (incluindo história de efeitos colaterais), laboratoriais, ECG e (se necessário) os resultados de imagem.
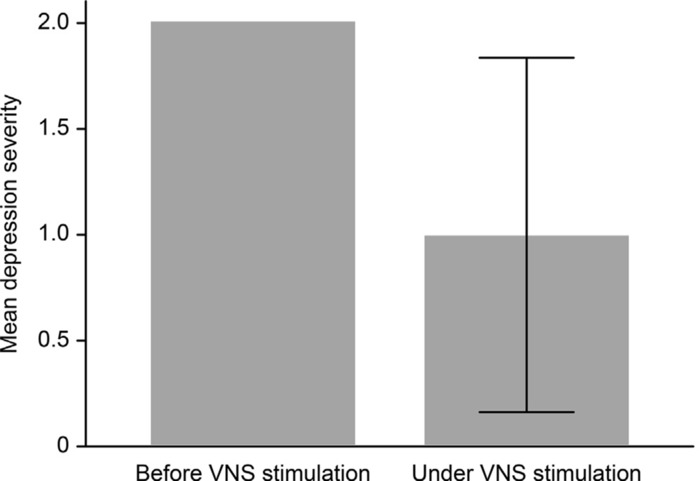
Figura 1: desenvolvimento de severidade da depressão (p < 0,001) sob tratamento de VNS em comparação com a linha de base (antes da estimulação VNS). A severidade da depressão é codificada como: 0 = sem depressão, 1 = depressão leve, 2 = depressão moderada e 3 = depressão severa. Tratamento variou entre 200 e 3 meses (média 104,9 meses). Esta figura foi modificada de Muller et al (2017)23 com permissão. O tamanho da amostra foi 18 (6 fêmea, macho 12; média de idade de 54). Escores brutos de escala de classificação de depressão de Hamilton foram traduzidos para uma classificação ordinal da gravidade da depressão. Diferenças na severidade da depressão (pré e pós-tratamento) foram comparadas usando uma amostra emparelhadas t-teste. Coeficiente de correlação produto-momento de Pearson foi computado para avaliar a relação entre os parâmetros de estimulação VNS e gravidade da depressão. Clique aqui para ver uma versão maior desta figura.
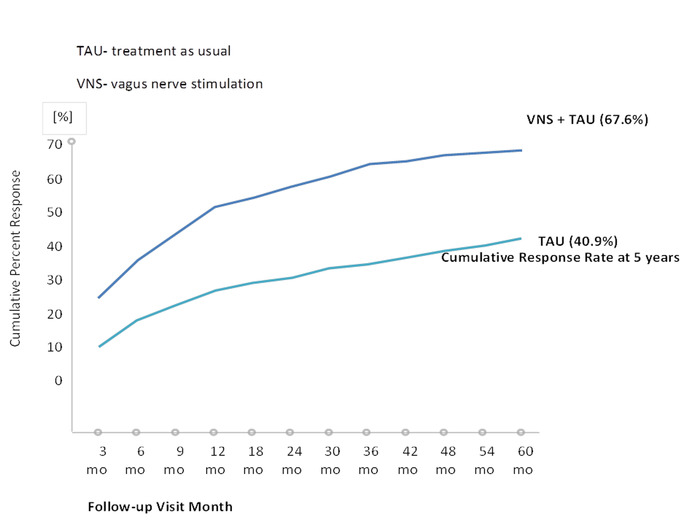
Figura 2: taxa de resposta pela primeira vez depois de 5 anos com base em Montgomery-Åsberg depressão Rating escala (MADRS). Esta figura foi modificada com a permissão de Aguiar et al.22. Um total de 765 pacientes (489 no grupo VNS) e 276 no grupo TAU foi incluído nas análises de eficácia. Clique aqui para ver uma versão maior desta figura.
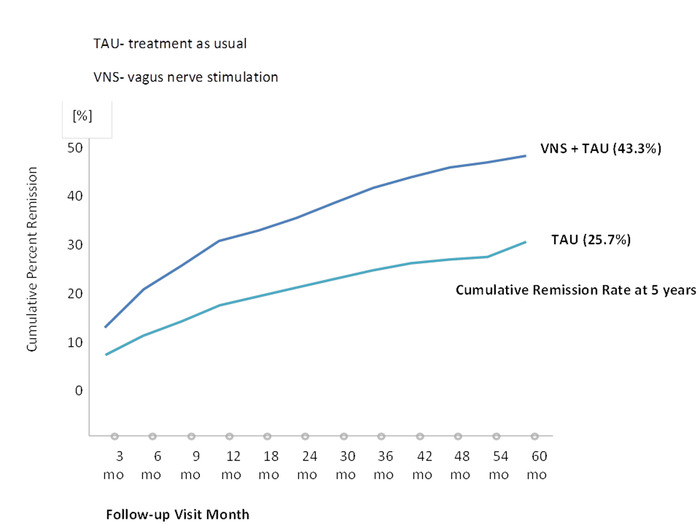
Figura 3: taxa de remissão pela primeira vez baseia o MADRS (≤ 9). Esta figura foi modificada com a permissão de22. Um total de 765 pacientes (489 no grupo VNS) e 276 no grupo TAU foi incluído nas análises de eficácia. Clique aqui para ver uma versão maior desta figura.
| Evento adverso, n (%) | Ano 1 (N = 700) | Ano 2 (N = 344) |
| Alteração de voz | 485 (69.29) | 179 (52.03) |
| Dispneia | 211 (30.14) | 71 (20.64) |
| Dor | 199 (28.43) | 41 (11,92) |
| Aumento da tosse | 185 (26.43) | 47 (13,66) |
| Dor da incisão | 181 (25.86) | 15 (4.36) |
| Parestesia | 159 (22.71) | 39 (11.34) |
| Dor de cabeça | 153 (21,86) | 29 (8,43) |
| Dor de garganta | 139 (19,86) | 55 (15,99) |
| Faringite | 122 (17.43) | 25 (7,27) |
| Depressão | 121 (17.29) | 46 (13.37) |
| Disfagia | 115 (16.43) | 32 (9.30) |
| Reação do local da incisão | 113 (16.14) | 15 (4.36) |
| Náuseas | 107 (15.29) | 12 (3,49) |
| Dor de dispositivo-site | 98 (14,00) | 11 (3.20) |
| Hipertonia | 92 (13,14) | 31 (9,01) |
| Reação de dispositivo-site | 82 (11,71) | 27 (7.85) |
| Insônia | 75 (10,71) | 22 (6,40) |
Tabela 1: [N (%)] efeitos adversos relataram durante os primeiros e segundo anos sobre tratamento de VNS. Esta tabela foi modificada com a permissão de Berry et al.33.
| Parâmetro | Unidades | Gama | Intervalo alvo | Dose terapêutica máxima | Nota |
| Corrente de saída | Miliampère (mA) | 0 – 3,50 | 1.0-2.0 | 2.5 | Stepwise aumentar após a primeira dosagem teste (teste de chumbo), 0,25 cada duas semanas (se tolerado) |
| Frequência do sinal | Hertz (Hz) | 1 – 30 | 20 | 20-30 | Modulação de faixa 20-30 Hz (para o modo de ação antidepressiva) |
| Largura de pulso | Microssegundos (µs) | 130 – 1000 | 250 | 500 | |
| Sinal do tempo | Segundos (s) | 7 – 60 | 30 | 60 | Diminuir quando ocorrem efeitos colaterais |
| Sinal Off-tempo | Minutos (min) | 0,2 – 180 | 5 | 180 | Aumentar quando ocorrem efeitos colaterais |
Tabela 2: Dosagem de recomendação para VNS. Estimulação do modo normal: estimulação 24h/dia e 7 dias por semana. Dosagem é otimizado para o efeito terapêutico e/ou a tolerabilidade.
Discussão
VNS é uma ferramenta de neuroestimulação para depressão crônica e TRD em pacientes com 18 anos ou mais, que não respondem a outros tratamentos de antidepressivo. VNS foi aprovado para uso na União Europeia e os Estados Unidos22. VNS foi mostrado para ser eficaz como um tratamento adjuvante no TRD22; Além disso, tem efeitos antisuicidal e melhora a qualidade de vida22.
Neste artigo, apresentamos um protocolo e informações adicionais para ajudar os médicos a implementar corretamente VNS em pacientes com TRD. A psiquiatra tratar é responsável para a dosagem ideal do estimulador de nervo vago e por considerar todos os aspectos da terapia, incluindo a segurança, tolerabilidade e eficácia de VNS em pacientes com TRD.
VNS requer um gerador de pulso implantável, que é cirurgicamente inserido sob a pele do peito, conforme descrito no protocolo. O gerador de pulso de terapia VNS para tratamento de depressão é colocado por via subcutânea na parede do peito esquerdo. Recomenda-se cuidado padrão ferida durante a primeira semana após o procedimento34,35. A estimulação repetida do nervo vago envia impulsos do sistema nervoso periférico, onde o eletrodo é colocado no cérebro. O elétrodo negativo gera potenciais de ação que viajam afferently através de fibras sensoriais, enquanto efferently itinerante de potenciais de ação são bloqueados principalmente pelo eletrodo positivo. Potenciais de ação desbloqueados podem causar efeitos colaterais. Uma distância de aproximadamente oito milímetros entre os eletrodos positivos e negativos é recomendada a36.
Não é aconselhável para usar o nervo vago direito devido ao risco de bradicardia grave e arritmias. Em contraste, sem tais efeitos colaterais foram relatados quando utilizou-se o nervo vago esquerdo; no entanto, vários pacientes tiveram implantes lado direito com bons resultados. Implantação cirúrgica é realizada por meio de uma pequena cirurgia (principalmente neurocirúrgicos)37,38. As complicações mais frequentes agudas de implante do estimulador de nervo vago incluem temporária salivação, tosse, paralisia das cordas vocais e fraqueza facial inferior. Bradicardia ocorre raramente, e assistolia ocorre muito raramente. O risco de infecção no local de VNS pode ser aproximado para ser entre 1.1 e 3,9%36.
Em matéria de efeitos adversos psiquiátricos, a taxa de mudança induzida por estimulação para mania ou hipomania em julgamentos de VNS foi baixa (ou seja, < 0,01% em um ano), e esses sintomas diminuíram depois de modificar os parâmetros de estimulação29. Efeitos colaterais são geralmente completamente reversível37,39. Eventos adversos relatados durante os primeiros e segundo anos na terapia de VNS estão sumarizados na tabela 133.
Durante a cirurgia, o estimulador de nervo vago é regularmente ligado a 0,5 mA para verificar se o dispositivo está funcionando corretamente e evitar efeitos colaterais como assistolia. Depois que tiver sido verificada a funcionalidade, o dispositivo é desligado novamente. Pelo menos duas semanas (dependendo os potenciais efeitos colaterais de tuning o VNS) depois que o dispositivo tem sido implantado, o estimulador de nervo vago é novamente ligado. Estimulação do modo normal é aplicada 24 h por dia.
A amplitude de estimulação é otimizada em relação o efeito terapêutico e/ou a tolerabilidade. O dispositivo é ativado telemetrically por um tubo conectado a um dispositivo computadorizado portátil durante as visitas do Conselho psiquiátricas. Em geral, a dose (ou seja,, a amplitude) é definido como um nível em que o paciente pode tolerar (ver quadro 2). Ajuste dos parâmetros de tratamento, incluindo a corrente de saída, frequência do sinal, largura de pulso, o sinal na hora e sinal fora de tempo, não invasiva é realizada usando a interface externa. Importante, o paciente pode parar a estimulação VNS colocando um ímã sobre o gerador. Depois que o ímã é removido, o gerador reinicia em modo normal de estimulação. A corrente de saída do modo normal pode ser aumentada para uma amplitude terapêutica tão rapidamente quanto tolerável. Visitas mais frequentes (aproximadamente 1 a 2 visitas por semana), no início da estimulação são recomendadas. Normalmente, a estimulação é aumentada pela 0,25 mA por visitar. No entanto, 0,25 múltiplos aumentos de mA podem ser feitos em uma única visita para atingir a faixa terapêutica mais rapidamente. No entanto, é essencial para garantir a tolerância paciente antes de fazer ajustes adicionais. A amplitude terapêutica é geralmente entre 1,0 e 2,0 mA. Em alguns pacientes, é necessário usar correntes de saída superiores para receber eficácia adicional. O efeito de VNS baseia-se em distintos mecanismos e está relacionado com a anatomia do nervo vago.
O nervo vago tem conexões anatômicas, incluindo aqueles para os solitários de tractus do núcleo, locus coeruleus, núcleos da Rafe, amígdala, hipotálamo e de córtex orbitofrontal40. VNS pode aumentar a atividade metabólica no núcleo principal serotonina e noradrenalina-produção, resultando em concentrações do neurotransmissor aumentada nos CSF41,42. Assim, o modo de ação do VNS funciona de forma análoga para a maioria dos antidepressivos.
Estudos de neuroimagem têm demonstrado que a atividade no tálamo e no córtex de pacientes deprimidos é alterada pela terapia VNS. Atividade mudou nos córtices pré-frontal ventromedial e orbitais também tem sido gravado43,44. Vários estudos de imagiologia sugeriram que a terapia de VNS está associada com diminuição da atividade metabólica no hemisfério direito e aumento da atividade metabólico no hemisfério esquerdo, atenuando assim o desequilíbrio Hemisférico em pacientes depressivos40 ,,45,46,47. Vagais afferents expressar receptores de IL-1 β que transmitem sinais inflamatórios no hipotálamo, levando a uma liberação de hormônios adreno-corticotrophin de hipófise. Esta via também estimula a liberação de glicocorticoides pelas glândulas supra-renais, através de uma diminuição de processos inflamatórios periféricos. No loop reflexo vaso-vagal-inflamatória, vagais afferents ativar eferentes vagais, que liberam a acetilcolina (ACh) na extremidade distal do nervo vago, inibindo a liberação de citocinas pró-inflamatórias como o TNFa48. Em resumo, os efeitos do antidepressivo de curto e médio prazo de VNS podem estar relacionados com o aumento da disponibilidade de serotonina e noradrenalina, semelhante ao mecanismo de medicação antidepressiva49. VNS a longo prazo tem efeitos diferentes de VNS a curto prazo. Efeitos a longo prazo do antidepressivo de VNS podem estar relacionados à redução do desequilíbrio inter-hemisféricas associado com depressão (i. e., inibição do lado direito e lado esquerdo ativação)45. Além disso, VNS pode reduzir a inflamação que contribui para a depressão50, embora nem todos os mecanismos de ação de VNS são completamente compreendidos ainda. Os efeitos são pensados para ser gradual e agindo com latência; por conseguinte, VNS não geralmente é indicado para o alívio dos sintomas depressivos agudos32.
Acima de 60% dos pacientes com TRD mostram redução em seus sintomas depressivos22,23,,49,51,52. Acompanhamento a longo prazo também indica menos tentativas de suicídio e menores níveis de razão suicida e pensamentos. Também documentados estão menos hospitalizações em pacientes tratados com VNS além da farmacoterapia em comparação com pacientes com o mesmo nível de severidade de sintomas de depressão que estavam apenas a tomar medicamentos22,29, 53.
Efeitos de prevenção de antidepressivo e recaída ainda podem ser observados após um acompanhamento de longo prazo de 5 anos22,23. Recentemente, em uma grande amostra de pacientes com TRD, Aaronson e colegas mostraram significativamente maiores taxas de resposta cumulativa de 5 anos e taxas de remissão significativamente maiores em pacientes tratados com VNS em comparação aos pacientes que foram apenas TAU22. O grupo melhor resposto consistiu de pacientes com um histórico de boas respostas para ECT antes de receber VNS22. O número necessário para tratar (NNT) para VNS varia de 4 a 10. Dado o elevado nível de resistência de tratamento nesta população de pacientes, o NNT permanece clinicamente significativa32.
Portanto, os resultados a longo prazo de VNS são distintamente promissoras, sugerindo que VNS pode ser particularmente útil para pacientes com depressão crônica, para quem a resistência de tratamento é um desafio20. Assim, depois de aproximadamente 3 a 6 meses da terapia de VNS, os resultados do tratamento podem ser esperados.
A definição comum de TRD é falha de tratamento pelo menos dois antidepressivos17,18,19. No entanto, a maioria dos doentes com TRD tratados com VNS submeteram-se mais de dois ensaios terapêuticos da medicação antidepressiva antes de implantação de dispositivo22. Por exemplo, no estudo longitudinal de Aaranson et al (2017)22, pacientes que foram tratados com VNS não conseguiu uma média de 8 tratamentos. Os resultados sugerem que VNS também pode ser particularmente útil em Estados muito mais pesados de TRD. Terapia de VNS antidepressive baseia-se principalmente sobre modificações para a corrente de saída e a frequência do sinal. Alterar as configurações de on/off parâmetros tempo geralmente leva a uma redução nos efeitos colaterais.
Semelhante à TRD, VNS foi avaliado para a sua utilização possível para outras doenças psiquiátricas, como bipolar transtorno depressivo maior, doença de Alzheimer, esquizofrenia, transtorno obsessivo-compulsivo, transtorno do pânico, transtorno de estresse pós-traumático, resistente ao tratamento transtorno bipolar de ciclagem rápida, fibromialgia e síndrome de Prader-Willi54. A eficácia de VNS para transtornos afetivos tem sido claramente demonstrado20,22,23,,54; no entanto, para outras condições psiquiátricas, não ainda há relatos de nenhum efeito ou apenas dados preliminares sobre eficácia54. Assim, nenhuma conclusão final sobre a eficácia de VNS nestas indicações psiquiátricas pode ser feito atualmente. No entanto, pode haver potencial para futuras abordagens terapêuticas54. Além disso, VNS não é só no arsenal psiquiátrica, como é um método comum de tratamento para epilepsia tratamento-refratário55. Em pacientes com epilepsia, os parâmetros de estimulação do estimulador de nervo vago são semelhantes às configurações em pacientes com TRD.
Inicialmente, a melhora de humor em pacientes de epilepsia com VNS levou à conclusão de que VNS pode também ser útil em transtornos afetivos32. VNS também foi avaliado para o tratamento de zumbido56de doenças inflamatórias intestinais57, insuficiência cardíaca,58, artrite reumatoide,59e muitas outras condições. Embora dados preliminares são promissores, futuras avaliações são necessárias para a compreensão dos mecanismos possíveis e potencial terapêutico em diversas condições clínicas e doenças.
No entanto, aproximadamente um terço dos pacientes com TRD não respondem adequadamente à VNS23. Além disso, os efeitos colaterais acima referida de VNS pode limitar sua ação terapêutica32. No entanto, em caso de resposta insuficiente ou intolerável de efeitos colaterais, os médicos podem modificar a configuração do estimulador do nervo vago. Ajuste fino do estimulador de nervo vago oferece várias possibilidades para a geração de respostas desejáveis para diferentes condições médicas. Perspectivas futuras para melhorar a eficácia VNS e reduzir os efeitos colaterais, como inclusive aumentando a vida útil da bateria, encurtando o tempo de resposta, estimulação nervosa transcutânea e identificação de fatores prognósticos para respostas valiosas, deveriam ser mais investigada.
Divulgações
Sebastian Moeller recebeu uma bolsa de pesquisa da LivaNova, Inc. Christian Heinen recebeu honorário do palestrante da LivaNova, Inc. Bettina H. Bewernick recebeu honorário do palestrante da LivaNova, Inc. e foi membro de um Conselho consultará da LivaNova, Inc. Merve Aydin, Alexandra Philomena Lam, Teja W. Grömer, Caroline Lücke e Alexandra Philipsen têm sem interesses concorrentes. Helge H.O. Müller serviu como um membro do Conselho Consultivo da LivaNova, Inc. e recebeu compensação do orador da LivaNova, Inc.
Agradecimentos
Este estudo foi suportado financeiramente pela LivaNova, Inc.
Materiais
| Name | Company | Catalog Number | Comments |
| VNS Therapy AspireSR Model 106 Generator | LivaNova Inc. | Primary DI Number: 05425025750061 | Implantable Pulse Generator |
| VNS Therapy Programming Wand Model 2000 | LivaNova Inc. | Primary DI Number: 05425025750177 | Programming Wand |
| VNS Therapy Demipulse Model 103 Generator | LivaNova Inc. | Primary DI Number: 05425025750030 | Implantable Pulse Generator |
| Cyberonics Tunneler Model 402 | LivaNova Inc. | Primary DI Number: 05425025750238 | Tunneler |
| VNS Therapy Model 502 Accessory Pack | LivaNova Inc. | Primary DI Number: 05425025750245 | VNS Therapy Accessory Pack |
| VNS Therapy Model 302 Lead | LivaNova Inc. | Primary DI Number: 05425025750108 | Implantable Bipolar Lead |
| Propofol | Merck | CAS Number: 2078-54-8 | [(CH3)2CH]2C6H3OH |
| Remifentanyl | Merck | CAS Number: 132539-07-2 | C20H28N2O5 · HCl |
| Rocoronium bromide | Merck | CAS Number: 119302-91-9 | C32H53BrN2O4 |
Referências
- Beaucage, C., Cardinal, L., Kavanagh, M., Aube, D. Major depression in primary care and clinical impacts of treatment strategies: a literature review. Sante Mentale au Quebec. 34 (1), 77-100 (2009).
- Maske, U. E., et al. Current major depressive syndrome measured with the Patient Health Questionnaire-9 (PHQ-9) and the Composite International Diagnostic Interview (CIDI): results from a cross-sectional population-based study of adults in Germany. BMC Psychiatry. 15 (77), (2015).
- Tesio, V., et al. Screening of depression in cardiology: a study on 617 cardiovascular patients. International Journal of Cardiology. 245, 49-51 (2017).
- Slepecky, M., et al. Which psychological, psychophysiological, and anthropometric factors are connected with life events, depression, and quality of life in patients with cardiovascular disease. Neuropsychiatric Disease and Treatment. 13, 2093-2104 (2017).
- Lasserre, A. M., et al. Prospective associations of depression subtypes with cardio-metabolic risk factors in the general population. Moecular Psychiatry. 22 (7), 1026-1034 (2017).
- Vandeleur, C. L., et al. Prevalence and correlates of DSM-5 major depressive and related disorders in the community. Psychiatry Research. 250 (50-58), 1023 (2017).
- Crismon, M. L., et al. The Texas Medication Algorithm Project: report of the Texas Consensus Conference Panel on Medication Treatment of Major Depressive Disorder. Journal of Clinical Psychiatry. 60 (3), 142-156 (1999).
- Negt, P., et al. The treatment of chronic depression with cognitive behavioral analysis system of psychotherapy: a systematic review and meta-analysis of randomized-controlled clinical trials. Brain and Behavior. 6 (8), e00486 (2016).
- Harter, M., et al. Psychotherapy of depressive disorders: Evidence in chronic depression and comorbidities. Nervenarzt. 89 (3), 252-262 (2018).
- Thase, M. E., et al. Cognitive therapy versus medication in augmentation and switch strategies as second-step treatments: a STAR D report. American Journal of Psychiatry. 164 (5), 739-752 (2007).
- Smith, C. A., Armour, M., Lee, M. S., Wang, L. Q., Hay, P. J. Acupuncture for depression. The Cochrane Database of Systematic Reviews. 3, (2018).
- Zhao, X., Ma, J., Wu, S., Chi, I., Bai, Z. Light therapy for older patients with non-seasonal depression: A systematic review and meta-analysis. Journal of Affective Disorders. 232, 291-299 (2018).
- Schlaepfer, T. E., et al. The hidden third: improving outcome in treatment-resistant depression. Journal of Psychopharmacology. 26 (5), 587-602 (2012).
- Rush, A. J., et al. Report by the ACNP Task Force on response and remission in major depressive disorder. Neuropsychopharmacology. 31 (9), 1841-1853 (2006).
- Rush, A. J., et al. Acute and longer-term outcomes in depressed outpatients requiring one or several treatment steps: a STAR*D report. American Journal of Psychiatry. 163 (11), 1905-1917 (2006).
- Mojtabai, R. Nonremission and time to remission among remitters in major depressive disorder: revisiting STAR*D. Depression and Anxiety. , (2017).
- Bschor, T. Therapy-resistant depression. Expert Review of Neurotherapeutics. 10 (1), 77-86 (2010).
- Holtzmann, J., et al. How to define treatment-resistant depression?. La Presse Médicale. 45 (3), (2016).
- Wiles, N., et al. Clinical effectiveness and cost-effectiveness of cognitive behavioural therapy as an adjunct to pharmacotherapy for treatment-resistant depression in primary care: the CoBalT randomised controlled trial. Health Technology Assessment. 18 (31), 1-167 (2014).
- Muller, H. H. O., et al. Vagus Nerve Stimulation (VNS) and Other Augmentation Strategies for Therapy-Resistant Depression (TRD): Review of the Evidence and Clinical Advice for Use. Frontiers in Neuroscience. 12, 239 (2018).
- Carreno, F. R., Frazer, A. Vagal Nerve Stimulation for Treatment-Resistant Depression. Neurotherapeutics. 14 (3), 716-727 (2017).
- Aaronson, S. T., et al. A 5-Year Observational Study of Patients With Treatment-Resistant Depression Treated With Vagus Nerve Stimulation or Treatment as Usual: Comparison of Response, Remission, and Suicidality. American Journal of Psychiatry. 174 (7), 640-648 (2017).
- Muller, H. H. O., Lucke, C., Moeller, S., Philipsen, A., Sperling, W. Efficacy and long-term tuning parameters of vagus nerve stimulation in long-term treated depressive patients. Journal of Clinical Neuroscience. 44, 340-341 (2017).
- Rush, A. J., et al. Vagus nerve stimulation (VNS) for treatment-resistant depressions: a multicenter study. Biological Psychiatry. 47 (4), 276-286 (2000).
- Sackeim, H. A., et al. Vagus nerve stimulation (VNS) for treatment-resistant depression: efficacy, side effects, and predictors of outcome. Neuropsychopharmacology. 25 (5), 713-728 (2001).
- Schlaepfer, T. E., et al. Vagus nerve stimulation for depression: efficacy and safety in a European study. Psychological Medicine. 38 (5), 651-661 (2008).
- Nahas, Z., et al. Two-year outcome of vagus nerve stimulation (VNS) for treatment of major depressive episodes. Journal of Clinical Psychiatry. 66 (9), 1097-1104 (2005).
- Bajbouj, M., et al. Two-year outcome of vagus nerve stimulation in treatment-resistant depression. Journal of Clinical Psychopharmacol. 30 (3), 273-281 (2010).
- Rush, A. J., et al. Vagus nerve stimulation for treatment-resistant depression: a randomized, controlled acute phase trial. Biological Psychiatry. 58 (5), 347-354 (2005).
- Rush, A. J., et al. Effects of 12 months of vagus nerve stimulation in treatment-resistant depression: a naturalistic study. Biological Psychiatry. 58 (5), 355-363 (2005).
- Nierenberg, A. A., Alpert, J. E., Gardner-Schuster, E. E., Seay, S., Mischoulon, D. Vagus nerve stimulation: 2-year outcomes for bipolar versus unipolar treatment-resistant depression. Biological Psychiatry. 64 (6), 455-460 (2008).
- Cusin, C., Dougherty, D. D. Somatic therapies for treatment-resistant depression: ECT, TMS, VNS, DBS. Biology of Mood & Anxiety Disorders. 2, 14 (2012).
- Berry, S. M., et al. A patient-level meta-analysis of studies evaluating vagus nerve stimulation therapy for treatment-resistant depression. Medical Devices (Auckland, N.Z.). 6, 17-35 (2013).
- Giordano, F., Zicca, A., Barba, C., Guerrini, R., Genitori, L. Vagus nerve stimulation: Surgical technique of implantation and revision and related morbidity. Epilepsia. 58 (Suppl 1), 85-90 (2017).
- Al Omari, A. I., et al. The vagal nerve stimulation outcome, and laryngeal effect: Otolaryngologists roles and perspective. American Journal of Otolaryngology. 38 (4), 408-413 (2017).
- Morris, G. L., et al. Evidence-based guideline update: vagus nerve stimulation for the treatment of epilepsy: report of the Guideline Development Subcommittee of the American Academy of Neurology. Neurology. 81 (16), 1453-1459 (2013).
- Elliott, R. E., et al. Efficacy of vagus nerve stimulation over time: review of 65 consecutive patients with treatment-resistant epilepsy treated with VNS > 10 years. Epilepsy & Behavior. 20 (3), 478-483 (2011).
- Ng, W. H., Donner, E., Go, C., Abou-Hamden, A., Rutka, J. T. Revision of vagal nerve stimulation (VNS) electrodes: review and report on use of ultra-sharp monopolar tip. Child's Nervous System. 26 (8), 1081-1084 (2010).
- Schneider, U. C., Bohlmann, K., Vajkoczy, P., Straub, H. B. Implantation of a new Vagus Nerve Stimulation (VNS) Therapy(R) generator, AspireSR(R): considerations and recommendations during implantation and replacement surgery--comparison to a traditional system. Acta Neurochirurgica (Wien). 157 (4), 721-728 (2015).
- Pardo, J. V., et al. Chronic vagus nerve stimulation for treatment-resistant depression decreases resting ventromedial prefrontal glucose metabolism. Neuroimage. 42 (2), 879-889 (2008).
- Roosevelt, R. W., Smith, D. C., Clough, R. W., Jensen, R. A., Browning, R. A. Increased extracellular concentrations of norepinephrine in cortex and hippocampus following vagus nerve stimulation in the rat. Brain Resesarch. 1119 (1), 124-132 (2006).
- Hassert, D. L., Miyashita, T., Williams, C. L. The effects of peripheral vagal nerve stimulation at a memory-modulating intensity on norepinephrine output in the basolateral amygdala. Behavioral Neuroscience. 118 (1), 79-88 (2004).
- Muller, H. H., Reulbach, U., Maler, J. M., Kornhuber, J., Sperling, W. Facilitative effects of VNS on the motor threshold: implications for its antidepressive mode of action?. Journal of Neural Transmission (Vienna). 120 (10), 1507-1510 (2013).
- Chae, J. H., et al. A review of functional neuroimaging studies of vagus nerve stimulation (VNS). Journal of Psychiatric Research. 37 (6), 443-455 (2003).
- Conway, C. R., et al. Association of cerebral metabolic activity changes with vagus nerve stimulation antidepressant response in treatment-resistant depression. Brain Stimulation. 6 (5), 788-797 (2013).
- Kosel, M., Brockmann, H., Frick, C., Zobel, A., Schlaepfer, T. E. Chronic vagus nerve stimulation for treatment-resistant depression increases regional cerebral blood flow in the dorsolateral prefrontal cortex. Psychiatry Research. 191 (3), 153-159 (2011).
- Nahas, Z., et al. Serial vagus nerve stimulation functional MRI in treatment-resistant depression. Neuropsychopharmacology. 32 (8), 1649-1660 (2007).
- Bonaz, B., Sinniger, V., Pellissier, S. Anti-inflammatory properties of the vagus nerve: potential therapeutic implications of vagus nerve stimulation. Journal of Physiology. 594 (20), 5781-5790 (2016).
- Furmaga, H., Shah, A., Frazer, A. Serotonergic and noradrenergic pathways are required for the anxiolytic-like and antidepressant-like behavioral effects of repeated vagal nerve stimulation in rats. Biological Psychiatry. 70 (10), 937-945 (2011).
- Corcoran, C., Connor, T. J., O'Keane, V., Garland, M. R. The effects of vagus nerve stimulation on pro- and anti-inflammatory cytokines in humans: a preliminary report. Neuroimmunomodulation. 12 (5), 307-309 (2005).
- George, M. S., et al. A one-year comparison of vagus nerve stimulation with treatment as usual for treatment-resistant depression. Biological Psychiatry. 58 (5), 364-373 (2005).
- Shen, H., Fuchino, Y., Miyamoto, D., Nomura, H., Matsuki, N. Vagus nerve stimulation enhances perforant path-CA3 synaptic transmission via the activation of beta-adrenergic receptors and the locus coeruleus. International Journal of Neuropsychopharmacology. 15 (4), 523-530 (2012).
- Burke, M. J., Husain, M. M. Concomitant use of vagus nerve stimulation and electroconvulsive therapy for treatment-resistant depression. The Journal of ECT. 22 (3), 218-222 (2006).
- Cimpianu, C. L., Strube, W., Falkai, P., Palm, U., Hasan, A. Vagus nerve stimulation in psychiatry: a systematic review of the available evidence. Journal of Neural Transmission (Vienna). 124 (1), 145-158 (2017).
- Oliveira, T., Francisco, A. N., Demartini, Z. J., Stebel, S. L. The role of vagus nerve stimulation in refractory epilepsy. Arquivos de Neuro-Psiquiatria. 75 (9), 657-666 (2017).
- Peter, N., Kleinjung, T. Neuromodulation for tinnitus treatment: an overview of invasive and non-invasive techniques. The Journal of Zhejiang University Science B: Biomedicine & Biotechnology. 12 (10), (2018).
- Breit, S., Kupferberg, A., Rogler, G., Hasler, G. Vagus Nerve as Modulator of the Brain-Gut Axis in Psychiatric and Inflammatory Disorders. Frontiers in Psychiatry. 9, 44 (2018).
- Devgun, J., Jobanputra, Y. B., Arustamyan, M., Chait, R., Ghumman, W. Devices and interventions for the prevention of adverse outcomes of tachycardia on heart failure. Heart Failure Reviews. 12 (10), (2018).
- Koopman, F. A., van Maanen, M. A., Vervoordeldonk, M. J., Tak, P. P. Balancing the autonomic nervous system to reduce inflammation in rheumatoid arthritis. Journal of Internal Medicine. 282 (1), 64-75 (2017).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados