Method Article
Твердофазные Submonomer Синтез Peptoid полимеров и их самосборки в Высоко-упорядоченные нанолистов
В этой статье
Резюме
Простой и общий ручной метод синтеза peptoid с участием основного оборудования и коммерчески доступных реагентов изложил, что позволяет peptoids легко синтезируется в большинстве лабораторий. Синтез, очистка и характеристика амфифильных 36mer peptoid описана, а также ее самоорганизации в сильно упорядоченное нанолистов.
Аннотация
Peptoids это новый класс биомиметических, не естественный, последовательности конкретных гетерополимеры, которые сопротивляются протеолиза, обладают мощной биологической активностью, и сложите в высшие наноструктур порядке. Структурно аналогичные пептиды, peptoids являются поли N-замещенных Glycines, где боковых цепей присоединены к азота, а не альфа-углерод. Их простота синтеза и структурное разнообразие позволяет тестировать основные принципы проектирования ездить заново проектирования и конструирования новых биологически-активных и наноструктурных материалов.
Здесь простой ручной peptoid синтеза протокол, который позволяет представлены синтеза длинных polypeptoids цепи (до 50mers) в превосходном урожайности. Только основное оборудование, простые методы (например, жидкий передача, фильтрация) и коммерчески доступных реагентов требуется, что делает доступным peptoids Помимо инструментария многих исследователей. Peptoid позвоночник выращивается одного мономера, в то время, VИ. А. submonomer метод, который состоит из двухступенчатого цикла мономера: ацилирование и перемещений. Во-первых, бромуксусной кислоты активируются в месте с N, N-диизопропилкарбодиимида acylates смолы связаны вторичный амин. Во-вторых, нуклеофильного замещения метила к первичного амина следует ввести боковой цепи. Двухступенчатый цикл повторяется до желаемой длины цепи будет достигнута. Эффективность ввода этого двухступенчатого цикла обычно превышает 98% и дает возможность синтеза peptoids в течение 50 остатков. Высоко настраиваемый, точный и химически разнообразной последовательности могут быть достигнуты с submonomer метод также сотни имеющихся в наличии первичных аминов могут быть непосредственно включены.
Peptoids становятся универсальным материалом для биомиметических nanobioscience исследований, поскольку их синтетических гибкости, надежности, и заказ на атомном уровне. Складывания одной цепи, амфифильные, информацияТион богатых polypeptoid в очень упорядоченной нанолисты недавно была продемонстрирована. Это peptoid является 36-Мер, который состоит всего из трех различных коммерчески доступных мономеров: гидрофобных, катионные и анионные. Гидрофобных боковых цепей фенилэтил похоронены в нанолисты ядро, тогда как ионные амина и карбоксильные боковые цепи согласования на гидрофильные лица. Peptoid нанолистов служить потенциальной платформой для мембранных миметиков, белок миметиков, устройство производства, и датчиков. Методы peptoid синтеза, лист образования, и микроскопии изображений описаны и обеспечивают простой способ обеспечения будущих конструкций нанолисты peptoid.
протокол
1. Твердофазный Submonomer Синтез Polypeptoids
Твердофазный синтез (СПС) является широко распространенным методом, используемым для синтеза последовательности конкретных биополимеров поэтапно, непосредственно на инертном твердом поддержки, таких как полимерные смолы шарик. Высокие связи урожайности и легкости избыток реагента удаление являются основными преимуществами СПС. После реакции сочетания, чтобы смола, избытка реагентов просто слить и бисером моют быть готовы к следующему шагу реакции. После окончательной реакции синтеза, полнометражный олигомеров расщепляются из смолы и гомогенный материал может быть дополнительно изучены. Здесь, мы адаптируем процедуры SPS для генерации последовательности конкретных полимеров peptoid.
- Установка: Все шаги руководства синтеза peptoid может быть осуществлена в одноразовой, полипропилен (PP) пористым картридж или пористым реакционный сосуд стеклом оснащена 3-х ходовой кран. Выполнение всех операций в вытяжном шкафу. Для инкубации в гСудно девушка или пластиковый картридж, подключить одну руку для подачи азота, чтобы мягко пузырь решение для надлежащего смешивания. Кроме того, для реакции инкубации в одноразовый картридж, печать обоих концах картриджа с крышками и поставьте на роторном шейкере. Для слива реакционной смеси или моет, подключиться к дому с помощью вакуумного отходов ловушку. Судно должно быть пористым с грубыми фритты. Siliconize стеклянный сосуд, чтобы избежать реакции бусин от прилипания к стенкам стеклянного сосуда. Приготовить раствор 5% дихлордиметилсиланом в дихлорэтане (объем / объем). Заполните чистый и сухой реакционный сосуд доверху силицирования решение, дайте постоять 30 минут, затем процедить. Вымойте судно сразу с DCE, а затем один раз с метанолом. Силицирования решение может быть повторно использованы, поэтому она должна быть сохранена. Либо воздух сухой или стряхнуть излишки раствора и выпекать изделия из стекла до высыхания после удаления краном. Холодный реактор перед добавлением смолы.
- Добавить 100 мг (0,06 ммоль) Ринк повторно амидГрех пористым реакционного сосуда. Swell смолы, добавив 2 мл диметилформамида (DMF). Перемешивают при встряхивании или восходящей течение 10 минут. Слейте раствор вакуум, чтобы изолировать увеличилось смолы.
- Добавьте 1 мл 20% 4-метилпиперидин в DMF (о / о), чтобы deprotect Fmoc группы. Перемешивают в течение 2 минут и процедить. Повторите с 12 минутной инкубации.
- Промыть смолы, добавив 2 мл DMF, агитируют за 15 секунд, и осушения. Повторить 3 раза.
- Bromoacetylation: Добавить 1 мл 0,6 М бромуксусной кислоты (0,6 ммоль) в ДМФА и 86 мкл N, N-диизопропилкарбодиимида (0,93 эквивалента, 0,56 ммоль). Инкубируйте с нежным пузырящийся в течение 30 минут, затем процедить и полоскать 2 мл DMF (повторите 4 раза).
- Водоизмещение: Добавьте 1 мл 1-2 М амина в N-метилпирролидон. Инкубируйте с восходящей на 30-120 минут, затем процедить и ополоснуть DMF (4x 2 мл).
- Продолжайте расти peptoid цепочке повторяя submonomer цикла, шаги 1,5 (bromoacetylation) и 1,6 (displacemenт).
- После окончательного перемещения не будет сделано, промыть 2 мл DMF (повторите 4 раза), затем 2 мл дихлорметана (повторите 3 раза). Кап и хранить реакционного сосуда до раскола.
- Пауза в синтезе (необязательно): Для паузы во время peptoid синтеза, закончить перемещение реакции и перейдите к шагу 1.8. Чтобы продолжать расти peptoid цепи, перезагрузите синтеза путем повторного отек сухой смолы (шаг 1.2) и повторяя submonomer цикла (шаг 1,5 и 1,6). Смолы можно высушить и хранить после любого перемещения, за исключением второго перемещения, поскольку смолы peptoid сопряженных могут образовывать циклические побочного продукта diketopiperazine.
- Для нескольких одновременных синтеза, твердофазной экстракции вакуумном коллекторе Рекомендуется для обеспечения максимальной эффективности. Peptoid синтез может быть автоматизирован с помощью правильно методов программирования в коммерчески доступных пептидные синтезаторы, такие как Aapptec Apex 396, CEM Свободы микроволновых синтезаторов и протеина Техноизвинение Инк Прелюдия синтезатора.
2. Расщепление и боковой цепи Снятие защиты
- Перенесите все сухого смолы 20 мл флакон стеклянный сцинтилляции.
- Рабочий внутри капота и используя специальные средства защиты, добавляют 4 мл трифторуксусной кислоты (ТФК) расщепления коктейль 1 (например, 95% водн. TFA, см. обсуждение), чтобы флакон сцинтилляционных стекла и крышка плотно. Встряхните в течение 10 минут до 2 часов при комнатной температуре (см. обсуждение).
- Сбор решение TFA расщепления путем фильтрации через смолу одноразовые, ПП пористым картридж в новый, предварительно взвешенные 20 мл флакон стеклянный сцинтилляции. Одноразовые, ПП пипетку удобно для передачи решений расщепления коктейль.
- Добавьте 1 мл свежего коктейль расщепления для полоскания смолы и собирать любые остаточные peptoid. Повторите 2 раза.
- Evaporate TFA путем продувки струей азота или с помощью Biotage V10 испарителя.
- Растворяться сырой нефти в 6 млацетонитрила / воды 1:1 (объем / объем) для высокоэффективной жидкостной хроматографии. Замораживание и lyophilize. Повторить.
- Запись вес сырого продукта. Магазин в виде сухого порошка при температуре -20 ° C
- Испытание расщепления (по желанию): тест расщепления на 0,5% смолы могут быть выполнены, чтобы быстро определить, чистоты и массы синтезированного peptoid и будет ли правильным условия расщепления были выбраны. Испытание раскол особенно полезны для контроля за ходом синтеза.
3. Характеристика и очистка Polypeptoid
- Благодаря сочетанию аналитической ВЭЖХ, электрораспылением LC-MS, и / или MALDI-TOF, определять чистоту сырой продукт и будет ли желаемый молекулярной массой присутствует.
- Подготовка ~ 5-10 мг / мл раствора сухую peptoid порошка в воде с минимальной ацетонитрил, сколько необходимо для растворимости. Фильтры прозрачный раствор сырой peptoid продукт с 0,45 мкм фильтр шприца, чтобы удалить пыль и частицы.
- Аналитический HПЛК и электрораспылением LC-MS: Подготовка ~ 20 мкг / мл сырой решение peptoid. Фильтр 200 мкл с 0,45 мкм фильтр и вводят 20 мкл.
- MALDI: Смешайте 1 мкл ~ 20 мг / мл peptoid с 1 мкл матрицы. Spot 1 мкл на тарелку MALDI и дайте высохнуть на воздухе. Матрица и приобретение режим зависит от образца (рис. 5).
- Purify сырой peptoid смеси с обратной фазой приготовительный высокоэффективной жидкостной хроматографии. Выберите градиент и столбец (С4 или С18), основанный на гидрофобность polypeptoid. Комбинат очищенные фракции, заморозить, а lyophilize, в результате чего пушистый белый порошок. Запись вес конечного продукта.
- Формирование HCl соли (по желанию): растворяться лиофилизированного порошка в 100 мМ HCl (aq.) с минимальным ацетонитрила. Трансфер в предварительно взвешенные стеклянные флаконы. Замораживание и повторное lyophilize. Повторите 2 раза. Reweigh, чтобы определить массу peptoid порошок.
4. Peptoid Формирование нанолисты
В этом разделе деприписывает протокола для формирования листов из одной цепи, последовательность конкретных, амфифильных 36-Мер peptoid (рис. 1). После peptoid нить синтезируется, очищенный и лиофилизированный как описано выше, в результате белый порошок растворяется в ДМСО, чтобы сделать 2 мМ маточного раствора.
- Подготовка 500 мкл 20 мкМ peptoid решение в лист буфера образование (10 мМ Трис-HCl, 100 мМ NaCl, рН 8,0, в воде) в 1 флакон стеклянный драм. Во-первых, добавить 445 мкл Milli-Q воды, 50 мкл 10х буфера формирование листа, и вихревые перемешать. Затем добавить 5 мкл 2 мМ маточного раствора peptoid и мягко вихревые решения. Крышка стекла флакона.
- Листы образуются нежные агитации разбавленного водного раствора peptoid. Медленно наклоняя стеклянный пузырек из горизонтального положения в вертикальное положение результатов в листах. Нежный встряхивания также дает листы, однако, листы, как правило, меньше и с меньшим количеством прямых краев. Более тщательный анализ механизма формирования листа reporteг отдельно. 2
- Для многих высококачественных листов, вращать стеклянные флаконы вокруг горизонтальной оси медленно (<1 RPM) в течение одного-трех дней. Соответствующие технические ресурсы RKVSD Rotamix трубки ротатор или индивидуальные рокер Для выполнения этой непрерывно.
- Диализ нанолистов (необязательно): В некоторых приложениях может оказаться необходимым, чтобы удалить любые свободные peptoid цепи или буферы / соли. Замочите Float-а-Lyzer 100 кДа мембраны в нужном буфере в течение 15 минут. Нагрузка 500 мкл решение лист peptoid в образец камеры. Замочите в 500 мл желаемого буфера, помешивая магнитной мешалкой со скоростью 60 оборотов в минуту. Разрешить диализа листов проводили в течение 4 часов. Каждый час, обмен со свежим запасом буферного раствора.
5. Флуоресцентной микроскопии в нанолистов
- Флуоресценция образы нанолистов были обследованы с Нилом Красный, экологически чувствительных красителей которых интенсивность флуоресценции возрастает, когда он локализован в гидрophobic среды (рис. 2).
- Добавить 1 мкл 100 мкМ Нила Красной до 100 мкл нанолисты решение для получения конечной концентрации 1 мкМ Нила Red.
- Сделать 1% агарозном решение в горячей воде и влить в пластиковых чашках Петри. Обеспечить решение агарозном является приблизительно 1 / 8 дюйма и позволяют решение для охлаждения спокойно на плоской поверхности. После множества агарозы, используйте лопаточку, чтобы вырезать и передачи 1 см х 1 см до квадратов стекло.
- Для сбора листов в одной плоскости, пятно 1 мкл лист решение на кусок агарозы. Разрешить агарозы, чтобы поглотить буфера в течение 2 минут, оставив листы на поверхности. Изображение в течение 15 минут, в противном случае агарозном начнет деформироваться из-за обезвоживания.
- Чтобы создать образ листы в растворе, нагрузка 15 мкл в 20 мм диаметром 0,12 мм прокладку на стекле. Крышка с покровным стеклом. Если листы просто зажат между предметным стеклом и покровным без прокладки, много листов шбуду сдвига и казалось бы, незначительные испарения вызовут листы постоянно двигаться.
- Изображение листы под epifluorescence освещения (например, Olympus IX81 инвертированный микроскоп снабжен Андор iXonEM + EMCCD спектры с красным фильтром Техас).
6. Сканирующей электронной микроскопии (SEM) из нанолистов
- Плазменного травления силиконовой подложке (по желанию): кремниевые чипы плазме травление, чтобы помочь в адсорбции листов. Место кремниевых чипов в вакуумной камере чистой плазмы (например, Harrick Плазменные Cleaner / Стерилизатор PDC-32G). Насос до 200 мторр и установить РФ катушку 18W (высокая настройка для PDC-32G). Etch в течение 2 минут.
- Оставьте 20 мкл peptoid решение лист на плазму обработанной кремниевой подложке. Разрешить сидеть в течение 3 минут. Удалите излишки раствора с кончика Ким-салфетки. Внесите 20 мкл воды на поверхности и удаления избытка раствора снова, чтобы удалить буфер и солей. Повторить 4 раза.
- Кроме того, наберитеyze peptoid решения лист с водой, чтобы удалить буфер и соль. Оставьте 20 мкл диализу решение лист на плазменных обработанные кремниевые подложки. Воздух сухой образец.
- Изображение листа с SEM (например, Zeiss Близнецы Ультра-55 Аналитическая электронного микроскопа, сканирование) с В-линза детектора и на энергии пучка от 1 кВ и 5 кВ (рис. 3).
7. Безопасность Примечания:
- Диметилформамид и Дихлорметан разумно возможные канцерогены.
- N, N-диизопропилкарбодиимида, 4-methylpiperdine и бромуксусной кислоты опасны для кожи, глаз и дыхательных путей. Они должны использоваться в капюшоне с осторожностью. Это может быть токсичен при вдыхании или через кожу, а также воздействие может привести к сенсибилизации. Пустые контейнеры содержат остатки продукта (жидкость / пар) и должны быть тщательно промыты перед снятием их с капюшоном.
- ТФК является сильной кислотой, и весьма разрушительными для верхних дыхательных путей, глаз икожи. ТФК является также летучих держать концентрированных растворов ТФК в капоте во все времена, чтобы избежать повреждения дыхательных. Используйте соответствующие средства индивидуальной защиты, и осторожность при обращении с решениями ТФК. Изменение перчатки быстро, если они вступают в контакт с ТФК, и сразу же очистить любые разливы.
8. Представитель Результаты:
В этом разделе описываются синтез, характеристика и очистки последовательности конкретных 36-Мер цепи peptoid, которая складывается в весьма приказал нанолисты 3 (рис. 1).
Блок заряда peptoid H-[Nae-NPE] 9 - [NCE-NPE] 9-NH 2 был синтезирован по 100 мг смолы Ринк амида. 2 М раствор амина был использован для всех перемещений реакций, которые проводились в течение 60 минут остатки 1-18 и 120 минут для остатков 19-36. трет-бутил бета-аланин HCl был преобразован в свободное основание (см. обсуждение), тогда как фенилэтиламина и ВОС-этилендиамин оба были использованы directly. Смолу расщепляют 95% TFA, 2,5% triispropylsilane, 2,5% воды в течение 2 часов. TFA выпаривали, а в результате вязкого масла (~ 180 мг) был вновь растворяют в 6 мл ацетонитрила: вода 1:1 (объем / объем). Продукт чистоты (рис. 4) и наличие массы продукта была подтверждена из аналитической ОФ-ВЭЖХ (30-80% ацетонитрила в воде градиент, каждая из которых содержит 0,1% (объем / объем) ТФК, в 1 мл / мин в течение 30 минут при 60 ° С с C18, 5 мкм, 50 х 2 мм колонка) и MALDI (рис. 5).
Очистка с обращенной фазой ВЭЖХ на колонке Vydac C18 (10 мкм, 22 мм х 250 мм) исходили, используя градиент 30-60% ацетонитрила в воде с 0,1% TFA в течение 60 минут при 10 мл / мин. Колонка была загружена с 60 мг неочищенного продукта для каждого хроматографического перспективе. Очищенные фракции были объединены на основе чистоты от аналитической ОФ-ВЭЖХ (рис. 4) и лиофилизировали с выходом ~ 80 мг пушистый белый порошок.
Очищенная блока заряда peptoid молекулярноговес был подтвержден MALDI. 1 мкл 100 мкМ очищенной peptoid в ацетонитриле: вода 1:1 (объем / объем) смешивали с 1 мкл матрицы (5 мг / мл α-циано-4-гидроксикоричных кислоты в ацетонитриле: водой 1:1 об / об и 0,1% ТФУ) и 1 мкл был замечен на тарелке MALDI. После того как образец сушат на воздухе, он был помещен в прикладной Biosystem / MDS 4800 Sciex MALDI TOF / TOF анализатор. Сбора и обработки мод линейной низкой массы. Расчетный вес был введен в целевой массы для автоматической настройки для времени задержки. Интенсивности лазерного излучения был установлен в 3400. Наблюдаемой массы, 4981,2, спички близко к расчетной массой 4981,74.
Лиофилизированный очищенный порошок растворяется в ДМСО, чтобы сделать 2 мМ маточного раствора, которое можно хранить при температуре 4 ° С. Листы были подготовлены вышеупомянутого протокола и полученную с использованием флуоресценции оптической микроскопии и SEM (рис. 2 и 3). Разнообразие форм с функцией размеры до 300 мкм наблюдается, а notabLy, прямые края занимают видное место.
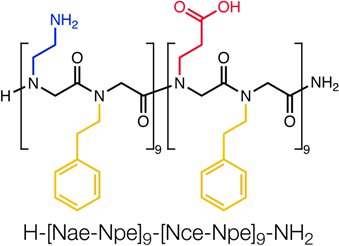
Рисунок 1 Последовательность блока заряда peptoid H-[Nae-NPE] 9 -. [NCE-NPE] 9-NH 2. Одноцепочечные, блок заряда, амфифильных polypeptoid 36-Мер самостоятельно собирает в высоко упорядоченной, двумерные нанолистов 3. Рассчитывается молекулярная масса составляет 4981,74.

Рисунок 2. Флуоресценция изображений микроскопии peptoid нанолистов. Листы были сформированы из 20 мкМ peptoid решение в 10 мМ Tris, 100 мМ NaCl, рН 8,0. Листы были обследованы на агарозном с 1 мкм Нила Red. Шкала бары 100 мкм.

Рисунок 3. Сканирование изображений электронной микроскопиииз peptoid нанолистов. Листы были сформированы из 20 мкМ peptoid решение в 10 мМ Tris, 100 мМ NaCl, рН 8,0. Шкала баров 5 мкм.

Рисунок 4 Аналитическая обращенно-фазовой высокоэффективной жидкостной хроматографии следов H-[Nae-NPE] 9 -. [NCE-NPE] 9-NH 2. Сырой и очищенной аналитической ВЭЖХ следа (30-80% градиент в 1 мл / мин в течение 30 мин при 60 ° С с C18, 5 мкм, 50 х 2 мм колонка) неочищенного и очищенного блока заряда peptoid H-[ Нае-NPE] 9 - [NCE-NPE] 9-NH 2 показано.
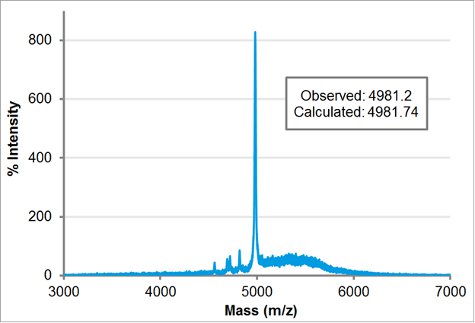
Рисунок 5 MALDI-TOF масс-спектроскопии следов H-[Nae-NPE] 9 -. [NCE-NPE] 9-NH 2. Наблюдаемой массы, 4981,2, хорошо согласуется с расчетной массой 4981,74.
Обсуждение
Приложения и значение
Этот протокол описывает простой и эффективный метод синтеза и peptoid водных самосборки peptoids в нанолистов. Большинство лабораторий, которые легко способны синтезировать peptoids потому недорогих материалов, базовые знания и простой методы используются 4. Кроме того, самосборка ультра-тонкий, высоко упорядоченная нанолистов просто требует повторных наклона флакона разбавленного водного раствора peptoid 2. Peptoids являются перспективными материалами для биомедицинских исследований и нанонауки, потому что они прочные и гибкие, но синтетически последовательности конкретных и тонкой настройке 5. Peptoids показали биологическую активность (6,7 терапия, диагностика 8, внутриклеточной доставки 9-10) и складывающиеся в иерархические наноструктур 3, 11-14. Из-за своей модульной синтеза, комбинаторной peptoid LiBrОвен 15-19 легко могут быть синтезированы и обследование на широкий ряд мероприятий, или свойствам. В частности, нанолистов служить потенциальной платформой для двумерного отображения лесов, мембранные миметиков, биологических датчиков, белок миметиков и устройств производства. С практически неисчерпаемы различных последовательностей возможно, царство peptoid исследования быстро расширяется.
Переменные в твердой фазе submonomer синтез polypeptoids
Из-за способности, чтобы выбрать из невероятно большой и разнообразный алфавита мономеров 20, submonomer метод нуждается в случайных модификаций для случаев, когда повышение эффективности связи каждый шаг улучшит общий выход продукта. Включение незащищенных боковых цепей гетероциклических требует использования хлоруксусной кислоты вместо бромуксусной кислоты 21. Увеличенное время перемещения и вышеамин концентрации, как правило, заняты примерно через 20 муфты долго peptoid последовательности или менее нуклеофильного аминов. Отопление реакционного сосуда до 35 ° C, с помощью водяной рубашкой реакционного сосуда, помогает управлять реакцией. Для особо энергонезависимой амины, такие как изопропиламин, необходимо соблюдать осторожность, чтобы избежать испарения.
Амины в виде соли соляной кислоты, такие как трет-бутил-бета-аланин HCl, должны быть свободны основе до их представления смещение реакции. Это может быть достигнуто путем растворения или приостановления амина в DCM (~ 5 г amine/25 мл DCM), а также нейтрализации эквимолярных решения водный раствор гидроксида натрия в делительную воронку. Слоя DCM собирается и водный слой промывают дополнительным DCM. Объединенные слои DCM сушат над сульфатом натрия и фильтруют в предварительно взвешенные круглодонную колбу. Удаление растворителя на роторном испарителе, получая масло, и записывать вес изделия.
Даринаг расщепления шаг, TFA коктейль расщепление и расщепление время зависит от количества и разнообразия защитных групп используются. Руководящие принципы для расщепления коктейли похожи на традиционные пептид снятия защиты расколы 1. Как правило, 10 минут инкубации требуются для последовательности без защитных групп или последовательности с несколькими сильно кислых лабильной защитных групп (например, ВОС, тритил). Два часа инкубации рекомендуется для последовательностей с более сложной защиты групп (например, трет-бутиловый эфир, МТР, PBF) или последовательности с большим количеством защитных групп для обеспечения полного снятия защиты каждой цепи. Сырая peptoid продукты обычно растворяют в ацетонитриле: вода 1:1 (объем / объем), но выше пропорции ацетонитриле являются общими с боковых цепей с высокой общей гидрофобности.
Раскрытие информации
Нам нечего раскрывать.
Благодарности
Авторы хотели бы поблагодарить Byoung-Чул Ли, Филип Чой и Самуил Хо за ценную помощь. Эта работа проводилась в молекулярной Литейное при Национальной лаборатории Лоренса Беркли, который проводится при поддержке Управления науки, Управление основной энергии наук, из Министерства энергетики США по контракту № DE-AC02-05CH11231 и сокращению военной угрозы Агентство по контракту No: IACRO-B0845281.
Материалы
| Name | Company | Catalog Number | Comments |
| Название реагента | Компания | Номер по каталогу | Комментарии |
| Диметилформамид | EMD | ЭМ-DX1726P-1 | 99 +% |
| N-метилпирролидон | BDH | BDH1141-4LP | 99% |
| Бромуксусной кислоты | Acros Organics | 200000-106 | 99% |
| 4-метилпиперидин | Sigma Aldrich | M73206 | 96% |
| N, N-диизопропилкарбодиимида | Chem-Импэкс | 001100 | 99,5% |
| Дихлорметан | EMD | EMD-DX0835 | ACS класса |
| Ацетонитрил | EMD | ЭМ-AX0145P-1 | 99,8% |
| Трифторуксусной кислоты | Sigma Aldrich | T6508 | 99% |
| Triisopropylsilane | Sigma Aldrich | 233781 -10G | Для расщепления TFA |
| 1,2-дихлорэтан | JT Baker | JTH076-33 | Для силицирования судов стекла реакции |
| Фенэтиламина | Sigma Aldrich | 407 267-100мл | > 99,5% гидрофобных боковых цепей амин |
| Вос-этилендиамин | CNH Технологии | C-1112 | Катионные боковой цепи амина |
| трет-бутил бета-аланин HCl | Chem-Impex Международной | 04407 | Анионные боковой цепи амина |
| α-циано-4-гидроксикоричных кислоты | Sigma Aldrich | C8982-10X10MG | Для MALDI матрицы |
| Нил Красный | Sigma Aldrich | 19123-10мг | Для флуоресценции |
| Дихлордиметилсиланом | Sigma Aldrich | 80430-500G-F | Для силицирования судов стекла реакции |
| Одноразовые ПП пористым корзинухребет | Прикладные Цветоделение | 2416 | 6 мл полипропиленовый картридж 20 мм ПЭ фритта |
| Одноразовые 3-х полосная Luer адаптер | Коул Parmer | 31200-80 | Кран для одноразовых судна реакции синтеза руководстве |
| Luer Lock кольцо | Коул Parmer | 45503-19 | ¼ "установки для одноразовых ручной реактор синтеза |
| Фитинги Луер | Коул Parmer | 45500-20 | ¼ "установки для одноразовых ручной реактор синтеза |
| Одноразовые ПП пипец | VWR | 16001-194 | Для TFA переводов |
| Луер блокировки пластиковый шприц | Национальный научный | S7515-5 | 6 мл шприцев |
| 1 драм стеклянный пузырек | VWR | 66011-041 | С фенольным литой колпачок с поливинил-лайнер столкнулся целлюлозы |
| 20 мл сцинтиллясцинтилляционных флаконе | VWR | 66022-060 | С прикрепленными ПП колпачок и лайнер целлюлозно фольги |
| Безопасные-Seal клей Spacer | Invitrogen | S-24736 | Для флуоресценции |
| Стекло слайды | Электронная микроскопия наук | 63411 | Для флуоресценции |
| Обложка скольжения | VWR | 48366-067 | Для флуоресценции |
| 4 "Кремниевая пластина | Тед Пелла | 16007 | Предварительно в кости в 5x7 мм чипы |
| 0,45 фильтр | VWR, Acrodisc | 28143-924 | Для высокоэффективной жидкостной хроматографии. ПТФЭ мембрана |
| Агароза | BD | 212272 | Для флуоресценции |
| SPE вакуумном коллекторе | Sigma Aldrich | 57044 | Пример SPE вакуумную |
| Пористым стеклянный сосуд | Ace стекла | 6402-12 | Пористость Cфритта |
| Плазменные Cleaner / стерилизатор | Harrick плазменных | PDC-32G | Пример плазмы очиститель для подготовки кремниевых чипов для SEM |
Ссылки
- King, D. S., Fields, C. G., Fields, G. B. A cleavage method which minimizes side reactions following Fmoc solid phase peptide synthesis. Int. J. Pept. Pro. Res. 36, 255-266 (1990).
- Sanii, B., Kudirka, R., Cho, A., Venkateswaran, N., Oliver, G. K., Olson, A. M., Tran, H., Harada, R. M., Tan, L., Zuckermann, R. N. Shaken, not stirred: Collapsing a peptoid monolayer to produce free-floating, stable nanosheets. J. Am. Chem. Soc. , (2011).
- Kudirka, R., Tran, H., Sanii, B., Nam, K. T., Choi, P. H., Venkateswaran, N., Chen, R., Whitelam, S., Zuckermann, R. N. Folding of a single-chain, information-rich polypeptoid sequence into a highly-ordered nanosheet. Bioploymers: Peptide Science. 96, 586-595 (2011).
- Utku, Y., Rohatgi, A., Yoo, B., Zuckermann, R., Pohl, N., Kirshenbaum, K. Rapid multistep synthesis of a bioactive peptidomimetic oligomer for the undergraduate laboratory. J. Chem. Ed. 87, 637-639 (2010).
- Fowler, S. A., Blackwell, H. E. Structure-function relationships in peptoids: Recent advances toward deciphering the structural requirements for biological function. Org. Biomol. Chem. 7, 1508-1524 (2009).
- Zuckermann, R. N., Kodadek, T. Peptoids as potential therapeutics. Curr. Op. Mol. Ther. 11, 299-307 (2009).
- Chongsiriwatana, N. P., Patch, J. A., Czyzewski, A. M., Dohm, M. T., Ivankin, A., Gidalevitz, D., Zuckermann, R. N., Barron, A. E. Peptoids that mimic the structure, function and mechanism of helical antimicrobial peptides. , 105-2794 (2008).
- Yam, A. Y., Wang, X., Gao, C., Connolly, M. D., Zuckermann, R. N., Bleua, T., Halla, J., Fedynyshyn, J., Allauzen, S., Peretz, D., Salisbury, C. M. A Universal method for detection of amyloidogenic misfolded proteins. Biochem. 50, 4322-4329 (2011).
- Huang, C. -Y., Uno, T., Murphy, J. E., Lee, S., Hamer, J. D., Escobedo, J. A., Cohen, F. E., Radhakrishnan, R., Dwarki, V., Zuckermann, R. N. Lipitoids - novel cationic lipids for cellular delivery of plasmid DNA in vitro. Chem. Biol. 5, 345-354 (1998).
- Schroeder, T., Niemeier, N., Afonin, S., Ulrich, A. S., Krug, H. F., Bräse, S. Peptoidic amino- and guanidinium-carrier systems: Targeted drug delivery into the cell cytosol or the nucleus. J. Med. Chem. 51, 376-379 (2008).
- Murnen, H. K., Rosales, A. M., Jaworski, J. N., Segalman, R. A., Zuckermann, R. N. Hierarchical self-assembly of a biomimetic diblock copolypeptoid into homochiral super helices. J. Am. Chem. Soc. 132, 16112-16119 (2010).
- Nam, K. T., Shelby, S. A., Marciel, A. B., Choi, P. H., Chen, R., Tan, L., Chu, T. K. Free-floating ultra-thin two-dimensional crystals from sequence-specific peptoid polymers. Nature. Mater. 9, 454-460 (2010).
- Burkoth, T. S., Beausoleil, E., Kaur, S., Tang, D., Cohen, F. E., Zuckermann, R. N. Toward the synthesis of artificial proteins: The Discovery of an amphiphilic helical peptoid assembly. Chemistry & Biology. 9, 647-654 (2002).
- Murphy, J. E., Uno, T., Hamer, J. D., Cohen, F. E., Dwarki, V., Zuckermann, R. N. A Combinatorial approach to the discovery of efficient cationic peptoid reagents for gene delivery. Proc. Natl. Acad. Sci. U. S. A. 95, 1517-1522 (1998).
- Mora, P. uig, Masip, I. sabel, Cortés, N. uria, Marquina, R. egina, Merino, R. amón, Merino, J. esús, Carbonell, T. eresa, Mingarro, I. smael, Messeguer, A. ngel, Pérez-Payá, E. nrique Identification from a positional scanning peptoid library of in vivo active compounds that neutralize bacterial endotoxins. J. Med. Chem. 48, 1265-1268 (2005).
- Zuckermann, R. N. Discovery of nanomolar ligands for 7-transmembrane G-protein coupled receptors from a diverse (N-substituted)glycine peptoid Library. J. Med. Chem. 37, 2678-2685 (1994).
- Alluri, P., Liu, B., Yu, P., Xiao, X., Kodadek, T. Isolation and characterization of coactivator-binding peptoids from a combinatorial library. Moleular Biosystems. 2, 568-579 (2006).
- Figliozzi, G. M., Goldsmith, R., Ng, S., Banville, S. C., Zuckermann, R. N. Synthesis of N-(substituted)glycine peptoid libraries. Methods Enzymol. 267, 437-447 (1996).
- Culf, A. S., Ouellette, R. J. Solid-phase synthesis of N-substituted glycine oligomers (α peptoids) and derivatives. Molecules. 15, 5282-5335 (2010).
- Burkoth, T. S., Fafarman, A. T., Charych, D. H., Connolly, M. D., Zuckermann, R. N. Incorporation of unprotected heterocyclic side chains into peptoid oligomers via solid-phase submonomer synthesis. J. Am. Chem. Soc. 125, 8841-8845 (2003).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены