Method Article
Свободные радикалы в химической биологии: от химического поведения в биомаркеров развития
В этой статье
Резюме
Радикальные основе биомиметических химии была применена к наращиванию библиотеки, необходимые для биомаркеров развития.
Аннотация
Участие свободных радикалов в науках о жизни постоянно растет с течением времени и был подключен к ряду физиологических и патологических процессов. Эта тема включает в себя различные научные области, простирающиеся от физической, биологической и биоорганической химии с биологией и медициной, с приложениями к улучшению качества жизни, здоровья и старения. Многопрофильная навыки, необходимые для полного расследования многих аспектах радикальные процессы в биологической среде и химических знаний играет решающую роль в открытии основных процессов и механизмов. Мы разработали подход химической биологии возможность подключения свободных радикалов химической активности с биологическими процессами, предоставление информации о механистической путей и продукты. Суть этого подхода заключается в разработке биомиметических модели для изучения поведения биомолекул (липидов, нуклеиновых кислот и белков) в водных системах, получение понимание реакции путей, а такжес создания молекулярно библиотек свободных радикалов продуктов реакции. Этот контекст может быть успешно использован для биомаркеров открытие и примеры приведены с двумя классами соединений: моно-транс-изомеров эфиров холестерина, который синтезируется и используется в качестве ссылки для обнаружения в плазме крови человека, и пуриновых 5 ',8-цикло-2 '-дезоксирибонуклеозиды, подготовлены и использованы в качестве ссылки в протокол для обнаружения таких повреждений в ДНК образцов, после ионизирующего излучения или полученные из разных заболеваний.
Введение
Реакционная способность свободных радикалов показал свою огромную важность для многих биологических явлений, в том числе старение и воспаление. В настоящее время она становится все более и более очевидно, что разъяснение каждого химического шаг, участвующих в этой реактивности необходима для того, чтобы понять основные механизмы и предусматривают эффективные стратегии для управления свободными радикалами и ремонта повреждений. Вклад от химических исследований является основополагающим, но прямого исследования в биологической среде может быть трудно, так как наложение различных процессов усложняет и возмущает изучение результатов и соответствующие выводы. Таким образом, стратегия моделирования свободно-радикальных реакций в биологически связанной условиях стало важным шагом в исследовании химических механизмов в биологии.
В последнее десятилетие наша группа разработала модели свободно-радикальных процессов в рамках биомиметических условиях. В частности, мы Envisaged биологически значимых преобразований ненасыщенных жирных кислот, нуклеозидов, и серосодержащих аминокислот и положить их в треке быть оценены и утверждены в качестве биомаркеров состояния здоровья. 1-4
Наш общий подход состоит из трех модулей:
- Органический синтез, который обеспечивает доступ к соответствующим образом изменены биомолекул. Синтетических план может быть также разработан с целью имитации свободно-радикальных процессов, происходящих в биологической среде, таким образом, условия применения способны имитировать биологические процессы интерес, который является принцип биомиметических радикальной химии. В биомиметических модели реакционной средой является вода или гетерогенной среде в связи с сосуществованием гидрофильных и гидрофобных отсеков. Преимущество работы с биомиметических модели является наличие упрощенной среде с известной реакцией партнеров, где реактивность и продуктов могут быть рассмотрены более подробно, возможно, открытиепути романа химических веществ. С этого шага механистической и кинетические информация может быть получена;
- Очистка, анализа и характеристика продукции, обеспечивая структурную и химическую информацию модифицированных биомолекул в целях организации молекулярно библиотек и облегчение recognition.in более сложные биологические среды. Протоколы устанавливаются также с учетом решения сложных смесей соединений, таких как полученные из биологических образцов;
- Биомаркеров развития с использованием биологических образцов, полученных либо в пробирке эксперименты на клеточных культурах, так и в естественных условиях исследования животных и людей. Протоколов, разработанных в биомиметических моделей затем наносят на комплексном анализе образцов, предусмотреть свободный радикальных преобразований в различных условиях. Молекулярная библиотеки разработан синтез имеют огромную помощь открытий науки о жизни. Информация, собранная на свободные радикальные преобразования GIVэлектронной возможность выяснить, ремонт и стратегии профилактики. Базы данных результаты могут быть использованы для тщательной оценки многофакторного анализа биомаркеров значения, а также возможных сопутствующих факторов.
Мы выбрали два класса соответствующие биомаркеры в аккредитации такого подхода: эфиров холестерина и пуриновых 5 ',8-цикло-2 "-дезоксирибонуклеозиды.
протокол
1. Синтез моно-транс-изомеров эфиров холестерина
- Растворите эфиров холестерина (линолеат или арахидоната эфира холестерина) в 2-пропанол (15 мм). Для лучшего растворения, образцы обрабатывали ультразвуком в течение 15 мин в атмосфере аргона.
- Передача решения кварца фотохимического реактора, добавьте 2-меркаптоэтанол в 2-пропанол (для достижения 7 мМ концентрации от 2 M раствор тиоловых). Флеш реакционной смеси с аргоном в течение 20 минут для того, чтобы устранить присутствие кислорода в растворе.
- Облучения реакционной смеси с помощью УФ-света с помощью 5.5W низкого давления ртутных ламп на 22 ± 2 ° С в течение 4 мин. Монитор аналитической Ag-TLC (серебристо-тонкослойной хроматографии) для доказательства формирования моно-транс эфиров холестерина (см. рисунок 1 для химических формул). Окрашивание TLC осуществляется путем заливки плиты в церия аммония молибдата (CAM) решения, а пятна появляются на отоплениепластину. Quench реакция на ранней стадии, с тем чтобы восстановить исходный материал, который может быть повторно использован для выполнения других раундах изомеризации, получение увеличение общей урожайности.
- Сбор в реакционную смесь в круглодонную колбу, стиральные устройства с несколькими мл 2-пропанола. Удалите растворитель и очистить моно-транс-изомеров эфиров холестерина на Ag-TLC, как описано в литературе. 5 Использование гексан-диэтиловый эфир (9:1 об / об) в качестве элюента для моно-транс-изомеров линолеат холестерина, в то время как использование гексана -диэтиловый эфир уксусной кислоты (9:1:0,1 об / об) для моно-транс-изомеров арахидоната холестерина.
2. Выделение доли эфиров холестерина из сыворотки крови человека
- Развести 1 мл сыворотки крови человека (полученный путем центрифугирования крови) с 1 мл рассола и залить раствор в делительную воронку под струю аргона для того, чтобы избежать артефактов (например, аддукты окисления). Добавить 10 мл хлороформ-метанол (2: 1 о / о) трижды. Встряхните делительную воронку очень медленно для того, чтобы ограничить образование эмульсии в связи с наличием альбумина.
- Вымойте органические слои один раз солевым раствором (10 мл), затем собирают в колбу в токе аргона, сушат над безводным сульфатом натрия. Удалить летучих роторном испарителе с получением желтого масла (общей липидной фракции плазмы).
- Возьмите сырую с 1 мл хлороформ-метанол (2:1 об / об), нагрузка на препаративной ТСХ в потоке аргона и использовать смесь гексан-диэтиловый эфир (9:1 об / об) в качестве элюента . Соскоблите кремнезема часть, содержащую холестерина фракции эфира и налить в сосуд. Тогда, извлекать диоксид кремния (3 × 5 мл) смесью хлороформ-метанол (2:1 об / об), собирать органические слои и удаления растворителя после испарения с получением чистого доля эфиров холестерина (обычно ~ 1,5 мг).
- Держите эфиров холестерина в темном флаконе покрыта алюминиевой фольгой в атмосфере аргона и хранить при температуре -20 ° C. Холестерил электроннойбеспризорных чувствительны к свету и кислороду.
3. Характеристика Mono-транс эфиров холестерина по спектроскопии комбинационного рассеяния
- Извлечение эфиров холестерина из сыворотки крови человека (≥ 0,7 мг), как описано в разделе 2, растворяют в небольшом количестве четыреххлористого углерода (≤ 10 мкл) и поместить в пузырек. CCl 4 выбран в качестве растворителя, потому что его сигнал КР не пересекается с областью интересов холестерина анализ эфира.
- Перенесите решение держатель образца через одноразовые пипетки стекла, затем осторожно удалите растворитель медленном потоке аргона. После равномерного маслянистая пленка образуется на внутренней стенке держателя образца, установите его в прибор для измерения.
- Преобразованию Фурье спектр КРС эфиров холестерина напрямую получить на липидный экстракт без каких-либо производных реакции. Мощность лазера на образец <100 мВт, чтобы избежать повреждения образца. Общее количество сканированийДля каждого спектра ≥ 800, чтобы минимизировать фоновый шум.
- 1,700-1,630 см -1 диапазоне спектра комбинационного рассеяния анализируются, поскольку она отражает вклад от С = С двойной связи в молекуле (C = C режим растяжения). Кривой анализ проводится в этом регионе, что позволяет отличительной наложенных взносов цис-и транс двойных связей в жирных алкильной цепи и двойной связи в кольце B холестерина (см. Рисунок 2).
- Чтобы соответствовать правильно колебательных полос, некоторые параметры должны быть фиксированными или ограничены в разумных пределах. Профили компонента пика описывается как линейная комбинация лоренцевой и гауссовой функции, в то время как половина высоты полосы лучше всего определяется процедура оптимизации компьютера. Количество и расположение компонентов пики, полученные с использованием четвертой производной спектра, которая позволяет обнаружить и некоторые слабые полосы компонента. Поскольку сигналшум которая ухудшается при дифференцировании сигнала может препятствовать использованию четвертой производной, разгладил четвертой производных с тринадцатилетней точки Савицкого-Голея функции, имеют преимущество, таким образом, правильный компромисс между разрешающей способностью и отношение сигнал-шум получается . Лучший кривой получены при минимально возможных значений с 2.
- Наличие транс-изомеров раскрывается компонента на 1671 ± 1 см -1, в дополнение к, по крайней мере, два компонента, немного сместился в сторону более низких частот, в связи с цепи жирной кислоты и холестерин, С = С двойной связи. Представитель спектра комбинационного рассеяния плазменных эфира холестерина показано на рисунке 9. На вставке сравнении с конкретным регионом холестерина линолеат и моно-транс холестерина линолевой кислоты изомеров показано на рисунке.
4. Дериватизация в Метиловые эфиры жирных кислот (FAME) и анализ с помощью газовой хроматографии
- Растворятьсяэфиров холестерина (~ 1,5 мг) с 0,5 мл 1 М раствора гидроксида натрия в бензол-метанол (2:3 об / об) и место в темном флаконе покрыта алюминиевой фольгой в атмосфере аргона.
- Оставьте смесь перемешивают при комнатной температуре и монитора с помощью тонкослойной хроматографии с использованием смеси гексан-диэтиловый эфир (9:1 об / об) в качестве элюента. Время реакции обычно составляет 30 минут, но тщательный мониторинг реакции не требуется. В самом деле, когда соответствующие метиловые эфиры образуются, реакция должна быть гасится для того, чтобы избежать образования деградации и побочных продуктов. ТСХ количественного формирования метиловых эфиров.
- Quench реакционной смеси добавляют 1 мл солевого раствора и извлечения метиловых эфиров н-гексаном (3 × 2 мл). Сбор органических слоев в пробирку и растворитель удаляют на роторном испарителе с получением фракции метиловый эфир, который затем используется для анализа GC без дополнительной очистки.
- Растворите метиловых эфиров в минимальном количестве н-гексана (обычно 1 мг в 50 мкл) и ввести в ГК оснащена 60 м × 0,25 мм × 0,25 мкм (50%-цианопропил)-methylpolysiloxane колонки. Используйте детектор ионизации пламени (FID) со следующей программой печи: температура начала при 165 ° C, удерживайте в течение 3 мин, а затем увеличение на 1 ° С / мин до 195 ° C, удерживайте в течение 40 мин, затем второй на 10 ° C / мин до 240 ° C, и удерживайте в течение 10 мин. Режим постоянного давления (29 фунтов на квадратный дюйм) выбран. Гелий или водород может использоваться в качестве газа-носителя. Метиловых эфиров идентифицируются по сравнению с временами удерживания подлинных образцов. Рисунке 10 показано представитель GC анализа FAME полученных из плазмы эфиров холестерина.
5. Синтез (5'R) - и (5'S) -5 ',8-цикло-2 "-дезоксиаденозин
- Растворите 33 мг 8-бром-2'-дезоксиаденозина (8-Br-Дадо) в ацетонитриле (100 мл) для того, чтобы достигать 1 мм концентрации. Регулирование потока газа (Ar или N2) в фотореактора и заполнить APPARatus с решением 8-Br-Дадо.
- Подготовка перегородки с соответствующим размером для ввода фотореактора и передать иглу подключен к линии инертного газа через центр его. Закройте системы с перегородкой. Промойте инертного газа в течение 30 мин.
- Облучения УФ-светом использованием 125W среднего давления ртутных ламп на 22 ± 2 ° С в течение 15 мин, собирают раствор в 250 мл колбу. Вымойте фотореактора с 10 мл ацетонитрила и собирать промывные в той же колбе.
- Quench сырой реакционной смеси 1 М NH 4 OH решения и испарения растворителя в ротационном испарителе.
- Выполнить высокоэффективной жидкостной хроматографический анализ (ВЭЖХ-УФ) с аналитической колонке (см. приборный отсек) при известных условиях, и сравнить профиль со ссылкой соединений.
- Выполнить высокоэффективной жидкостной хроматографический анализ (ВЭЖХ-УФ) с аналитической колонке (см. приборный отсек) с помощью следующей зольвентиляционные отверстия и градиентов: 2 мМ формиата аммония в качестве растворителя и ацетонитрила в качестве растворителя B. Установить расход на 1 мл / мин, а градиент от 0% растворителя B до 0,3% растворителя B должны быть достигнуты в 2,2 мин. Тогда 0,8% растворителя B в в 4,0 мин, затем 1% растворителя B в 4,8 мин. Оставайтесь на 1% растворителя B в течение 9 минут, а затем перейти к 8% растворителя B в 6 мин. После перехода на 10% растворителя B в 4 минуты и 30% растворителя B в течение 5 мин и остается на уровне 30% растворителя В других 5 мин. Сбор хроматографических пиков, соответствующих двум диастереомерных продуктов в двух разных флаконах.
- Измерить абсорбцию из двух собранных фракций в УФ-спектрофотометр и рассчитать точную концентрацию на основе Ламбер-Бера (A = εlC, где это поглощение, ε коэффициент вымирания и л длина ячейки). Используйте ε коэффициент экстинкции 2'-дезоксиаденозина (Дадо) (15400 М -1 см -1 при 260 нм).
6. Синтез (5'R) -D (5'S) -5 ',8-цикло-2 "-дезоксигуанозина
- Растворите 35 мг 8-бром-2'-дезоксигуанозина (8-Br-dGuo) и 30 мг йодида натрия (NaI) в дистиллированной воде (100 мл), чтобы достичь 1 мм и 2 мМ концентрации, соответственно. Регулирование инертного газа (Ar или N 2) поток связан с фотореактора и заполнить фотореактора с реакцией решение.
- Degass реакционной смеси, как описано в процедуре 5 (стадия б).
- Облучения УФ-светом использованием 125W среднего давления ртутных ламп на 22 ± 2 ° С в течение 30 мин, собирают раствор в 250 мл колбу. Вымойте фотореактора с 10 мл воды и сбора промывных в той же колбе.
- Quench сырой реакционной смеси 1 М NH 4 OH решения и испарения растворителя в вакууме.
- Выполнить анализ, как описано в процедуре 5 (шаги е в г). Используйте ε коэффициент экстинкции 2'-дезоксигуанозина (dGuo) (11700 М -1 см -1 при 260 нм).
7. Синтез Изотопный Маркированный пуринов (5'R) - и (5'S) -5 ',8-cyclonucleosides
- Подготовьте 2 мл 1 мМ водного раствора (дистиллированная вода) 15 N изотопного помечены пуриновых нуклеозидов ([15N 5] Dado или [15N 5] dGuo) в стеклянный флакон (4 мл) с крышкой перегородки.
- Подключите флакон с крышкой перегородки и подключиться к газопроводу (N 2 O для насыщения раствора) через иглу в перегородке, которая достигает дна флакона. Еще одна короткая игла в перегородке крышки работает выхода газа.
- Промойте решение с N 2 O в течение 30 мин. Поток газа регулируется, чтобы быть очень низкой.
- Выход иглы сначала вынимают и после 1 'длинный следует, чтобы иметь небольшое давление внутри флакона.
- Положите раствор в аппарате гамма-радиолиза в течение 8 часов (расчет на основе дозы ок. 4,5 Гр / мин).
- После реакции утолить нефть с 1 M NH 4 OH решение.
- Выполнить высокоэффективной жидкостной хроматографический анализ (ВЭЖХ-УФ) при известных условиях, 6 и сравнить хроматограмме со стандартными ссылками.
8. Гамма радиолиза водных растворов ДНК
- Подготовить 1 мл 0,5 мг / мл раствора (дистиллированная вода) ДНК зобной железы теленка и положить в стеклянный флакон (2 мл) с крышкой перегородки.
- Degass реакции, как описано в процедуре 7 (шаги BD).
- Положите раствор в аппарате гамма-радиолиза в течение 30 минут (расчет на основе дозу / скорость ок. 4,5 Гр / мин).
9. Ферментативного расщепления ДНК
- Для трубки Эппендорф, содержащие 80 мкг ДНК, добавить 8 U нуклеазы P1, 0,01 U фосфодиэстеразы II, 20 нмоль EHNA в 20 мкл 300 мМ ацетата натрия (рН 5,6) и 10 мМ хлорида цинка. Выдержите эту смесь при температуре 37 ° С в течение 48 часов.
- Затем добавьте смесь из 8 U щелочной фосфатазы, 0,02 U из phosphodiesterasE I, в 40 мкл 0,5 М Трис-HCl буфером (рН 8,9) в смеси пищеварения. Образец инкубируют при 37 ° С в течение 2 часов.
- Смесь нейтрализуют добавлением 10% муравьиной кислоты.
- Передача образца Amicon Ultra-0,5 центробежный фильтр устройства (отсечка 3 кДа), добавить 200 мкл тридистиллированную H 2 O. Поместите Ultra-фильтр в ротора центрифуги при 14000 х г в течение 15 мин. Затем отделить Ультра фильтрующее устройство от микроцентрифужных трубку. Lyophilize фермент-бесплатное решение в микроцентрифуге трубку.
10. Образец ДНК Опреснение до анализа
- Выполнить высокоэффективной жидкостной хроматографический анализ (ВЭЖХ-УФ) с аналитической колонке (см. приборный отсек) после известных условиях 6.
- Растворить лиофилизированный расщепленной ДНК в 20 мкл H 2 O и вводят в ВЭЖХ-УФ.
- Соберите образец в пробирку после солью элюирования (первых минут) и непосредственно перед элюирования тиме первый нуклеозидов (5'R-cdGuo), до конца хроматографического программы.
- Образец лиофилизировали и resolubilized в 20 мкл воды.
11. LC-MS/MS Количественный анализ
- Подготовка HPLC-MS/MS (тройной квадрупольный) перед началом анализа загрузки аналитического метода и метода детектор MS (ESI) 6.
- Добавить 1 мкл изотопного меченых соединений смеси в образец, полученный в процедуре 7.
- Inject 20 мкл шипами расщепленной ДНК раствор в дистиллированной воде.
- Полученные данные хроматографического разработаны на основе предыдущей калибровки со ссылкой соединений. Представитель ВЭЖХ запустить содержащие аденозина и гуанозина 2'-дезоксирибонуклеозиды и их окислительное и цикло производными показано на рисунке 11.
Результаты
Процесс изомеризации была описана в частности, для эфиров холестерина получая моно-транс-изомеров линолевой и арахидоновой кислоты показано на рисунке 1 в качестве первых продуктов этой атаки, которые могут возникнуть в условиях свободных радикалов напряжения в биологической среде 5.
На рисунке 3 химический механизм, участвующих в цис-транс-изомеризации двойной связью показано на рисунке. Радикальное указания источника в общем виде, чтобы позволить себе S-центре радикалов. В описанных протоколов радикальная источник ультрафиолетового света, который может сломать homolitically SH настоящее связи в молекуле тиола RSH.
На рисунке 4 показаны три шага протокола для синтеза модифицированных класс липидов и их обнаружение в плазме крови человека: синтез представляет собой биомиметических свободных радикалов процесса, а также предоставляет в одном сосуде удобный вход в геометрическойrical изомеры, без каких-либо загрязнений позиционных изомеров с последующей очисткой и изоляцией протоколов.
Некоторые аналитические методики могут быть использованы для высокочувствительного обнаружения транс-изомеров содержание и характеристика моно-транс библиотеки эфиров холестерина. В частности, спектроскопии комбинационного рассеяния света может быть осуществлена непосредственно на холестерина фракции эфир без производных (см. Рисунок 2 и Рисунок 9).
Второй пример касается пуринов 5 ',8-цикло-2 "-дезоксирибонуклеозиды, которые являются повреждения ДНК созданные атаки свободных радикалов на должность C5' сахарной части и последующее образование ковалентной связи между сахаром и базы фрагментами. Четыре структур могут быть произведены, то есть 5 ',8-цикло-2 "-дезоксиаденозин и 5' ,8-цикло-2"-дезоксигуанозина, как существующие в 5'R и 5'S диастереомерные формы (рис. 5). На рисунке 6 тОн механизма реакции показано, что включает в себя фотолиза 8-bromopurine производных от 5 до получения соответствующего C8 радикальных 6, который абстрагируется внутримолекулярно атома водорода от позиции C5 'выборочно предоставляя 2'-deoxyadenosin-5-ил радикальных 7. Радикальные 7 подвергается циклизации с константой скорости в диапазоне 10 5 -10 6 с -1, 2 с последующим окислением гетероароматических радикальных 8 до получения окончательных продуктов 9. Реакция гидроксильных радикалов, порожденных радиолиза воды, с 2'-дезоксиаденозина и 2'-дезоксигуанозина (10) был обнаружен ок. 10% водорода абстракции от позиции C5 '7.
Наша химическая биология подход к библиотекам пуриновых 5 ',8-цикло-2 "-дезоксирибонуклеозиды (в том числе меченых соединений) показано на рисунке 7, с идентификацией этих поражений в олигонуклеотидов, а также в образцах ДНК, полученных из ваrious источников, таких как, например, обрабатывают в условиях ионизирующего излучения, как имитировать радикальных условиях стресса.
На рисунке 8 типового оборудования фотореактора показано. Устройство позволяет при облучении соединений, растворенных в соответствующем растворителе. Она состоит из: а) реакционной камеры оборудованы входом для инертных газов (на дне) и два входа для выхода газа и для того реагентов; II) внутренние камеры, содержащей соответствующие ртутная лампа подключена к системе охлаждения и электрической энергии, которая вставляется в реакционную камеру через стекло сустава.
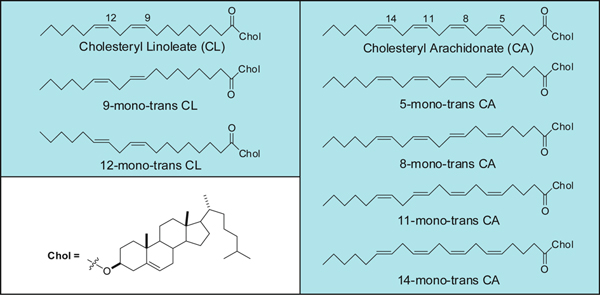
Рисунок 1. Моно-транс-изомеров холестерина линолеат и арахидоната.
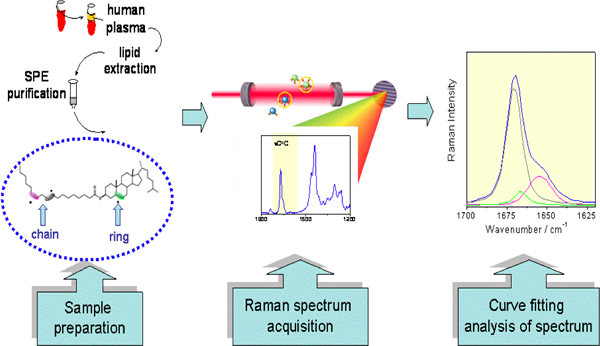
Рисунок 2. Эфиров холестерина в сыворотке крови человека и прямой анализ моно-транс-изомеров по спектроскопии комбинационного рассеяния.
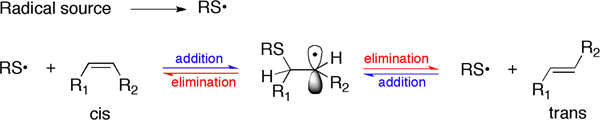
Рисунок 3. Кроме того, ликвидация процесс, который приводит к цис-транс-изомеризация двойных связей по тиильных радикалов.
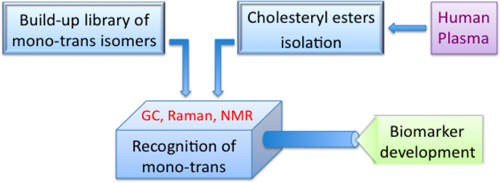
Рисунок 4. Три шага протокола для развития моно-транс эфиров холестерина в качестве биомаркеров свободных радикалов стресс.

Рисунок 5. Четыре пуриновых 5 ',8-цикло-2 "-дезоксирибонуклеозид диастереоизомеров. Нажмите, чтобы увеличить показатель .
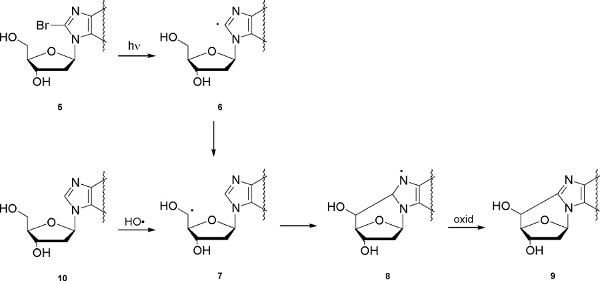
Рисунок 6. Генерация C5 'радикалов, либо путем фотолиза 5 или реакции 10 с HO • радикалы, и механизм пуриновых 5' ,8-цикло-2 "дезоксирибонуклеозид образования. Нажмите, чтобы увеличить показатель .
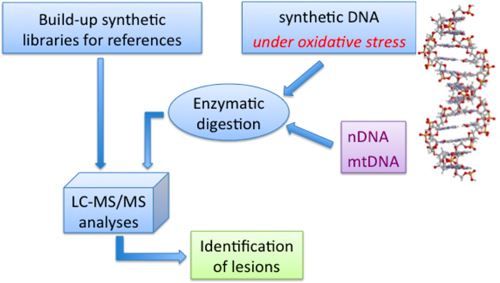
Рисунок 7. Протокол Fили идентификации некоторых радикальных основе повреждений ДНК, мтДНК: митохондриальная ДНК, нДНК: ядерная ДНК.

Рисунок 8. Фотохимический реактор.
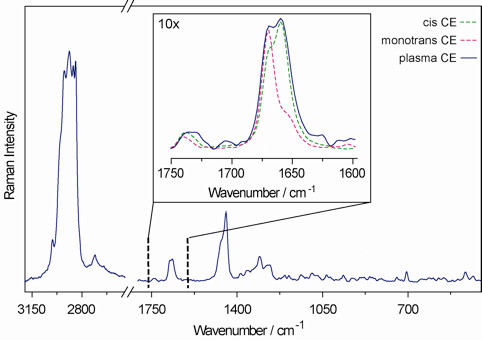
Рисунок 9. Представитель спектра комбинационного рассеяния плазменных эфира холестерина. На вставке сравнении с конкретным регионом холестерина и холестерина линолеат моно-транс-изомеров линолевой кислоты.
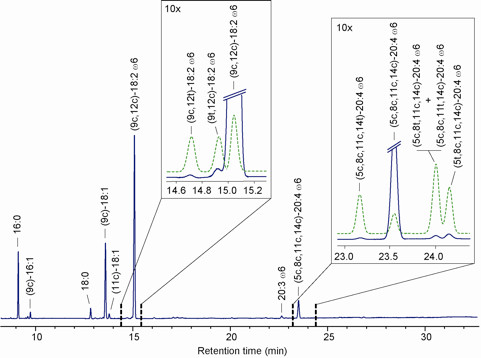
Рисунок 10. Представитель GC анализа FAME получены из плазмы эфиров холестерина.
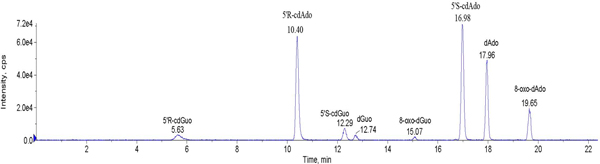
<сильная> Рисунок 11. Представитель ВЭЖХ запустить содержащие 2'-дезоксиаденозина и 2'deoxyguanosine вместе с их окислительной и пуриновых 5 ',8-цикло-2 "-дезоксирибо нуклеозидов. Нажмите, чтобы увеличить показатель .
Обсуждение
Преобразование естественных СНГ ненасыщенных жирных кислот в геометрической транс-изомеров является преобразование связано с производством радикальных напряжения в биологической среде. Сотовые мембранных липидов, которые содержат жирные кислоты, являются соответствующие биологические мишени для радикального стресса и мы сначала изучили эндогенных цис-транс-изомеризации фосфолипидов в клеточных культурах, животных и людей оценке аналитической протоколов в каждом конкретном случае. 8-10 Мы показали, что эта трансформация может происходить с помощью различных S-содержащих соединений, в том числе тиолы, тиоэфиры и дисульфиды, которые под разными радикальными условиях стресса способны генерировать тиильных радикалов, т.е. изомеризации агента (рис. 3). В примере, приведенном в данной статье основное внимание уделяется классу эфиров холестерина, которые представляют собой известную долю липидов плазмы, собственно, участвующих в метаболизме липопротеина. Эфирную связь между жирными кислотами и чоlesterol в синтезируются передачи жирных кислот с позиции 2 из глицерина фрагмент фосфатидилхолина на холестерин, шаг катализируется ферментом ацил холестерина лецитин трансферазы (LCAT). Таким образом, плазма эфиров холестерина строго связаны с мембранной оборот липидов, и содержат относительно высокий процент полиненасыщенных жирных кислот (ПНЖК) обычно присутствует в фосфатидилхолины, то есть линолевая и арахидоновая кислоты. Липопротеинов формировании участвует в сердечно-сосудистых и метаболических заболеваний. Реакционной способности природных эфиров холестерина со свободными радикалами может произойти в двойных связей линолеат и арахидоната остатки, которые могут быть преобразованы в соответствующие транс-геометрические изомеры (см. рисунок 1 для структур). Характеристика транс холестерина содержание эфира в биологических образцах интересно биомаркеров развития. Косвенная методика состоит из преобразований cholesteryл эфиров изолирован от плазмы в соответствующие метиловые эфиры жирных кислот (FAME) и разделения по протоколам газовой хроматографии. В этом случае калибровки стандартные ссылки цис-и транс метиловых эфиров жирных кислот осуществляется для того, чтобы позволить количественного транс содержание в образцах. На основании аналитического исследования, проведенные на холестерина библиотеки эфир, мы предложили применить также метод, основанный на спектроскопии комбинационного рассеяния света, что может быть осуществлено непосредственно на холестерина фракции эфира изолирован от плазмы, без дальнейших производных в соответствующие FAME (см. рис 2 и 9). Стоит отметить, что до сих пор ни одного успешного методы описаны в отдельном цис-и транс-изомеры жирных кислот, содержащих липиды ВЭЖХ, так как вместо описывается гидроперекисей эфира холестерина. До сих пор косвенным методом газовой хроматографии-прежнему является наилучшим доступным методом до сих пор. По этому методу первые количественные evaluвиях работа моно-транс содержания, полученных от эфиров холестерина изолированных из плазмы здоровых испытуемых не было. Использование пламени ионизационный детектор (ПИД) предел обнаружения удовлетворительное (частей на миллиард) и наномолярных количества соединений были обнаружены. 5. С различными системами обнаружения этот предел может быть даже снижена. Влияние ионизирующего излучения на эфиров холестерина является вопросом дальнейших исследований, будь то линейный отклик получается по отношению к принятой дозы.
В качестве второго примера мы выбрали модифицированных нуклеозидов, которые могут быть получены повреждения свободными радикалами ДНК. Гидроксильных радикалов (HO •), как известно, наиболее вредных активных форм кислорода (ROS) по их способности вызывать химические изменения в ДНК. Один или несколько очагов могут возникнуть на ДНК, что в эукариотических клетках находится в ядре и митохондриях. Выявление и измерение основных классов генерируются окислительные повреждения ДНК требует approprИАТЭ молекулярные библиотеки для того, чтобы создать аналитическую протоколов. Мы сосредоточили наши интересы на самых маленьких тандеме поражений, которые являются пуриновые 5 ',8-цикло-2 "-дезоксирибонуклеозиды, имеющие дополнительные ковалентная связь между базой и сахаров создан свободных радикалов. Соединения 5 ',8-цикло-2 "-дезоксиаденозин и 5' ,8-цикло-2"-дезоксигуанозина существующих в 5'R и 5'S диастереомерные формы (рис. 5). Их потенциал, чтобы стать свободными радикалами маркеров стресса вопрос фундаментальных исследований. 2 Действительно, если ДНК подвергается HO • радикальной абстракции водорода из положения C5 'сахарной является одним из возможных событий, приведших к образованию этих тандеме поражений. Пурин 5 ',8-cyclonucleosides может быть измерена как сумма диастереомеры по HPLC-MS/MS в ферментативно расщепляют γ-облученных образцов ДНК от 1 до 12 поражениях / 10 6 нуклеозидов / Гр собирается форме отсутствии кислорода к физиологическому уровню кислорода яп тканей, диастереомерные отношение 5'R / 5 бытия ~ 4 и ~ 3 для 5 ',8-cdAdo и 5' ,8-cdGuo, соответственно (рис. 11) 11. Стоит отметить, что отношения между дозой облучения и 5 ',8-cdAdo и 5' ,8-cdAdo поражения обнаружены в клеточной ДНК далека от понимания. Единственный эксперимент, основанный на 2kGy облучения сообщили в экспериментальном не может считаться убедительным 11. Дальнейшие эксперименты такого рода и аналитического количественного из четырех поражений необходимы для определения таких отношений. Обнаружение этих поражений и более популярным окислительных превращений (например, 8-оксо-2'-дезоксигуанозина, 8-oxodGuo) являются вопросом интенсивные исследования, подтверждающие важность и поражений во время окислительного метаболизма. 6,13 использованием высокоэффективной жидкостной хроматографии -MS/MS (тройной квадрупольный) имеет предел обнаружения близко к 30fmol для всех четырех поражениях. Последние усовершенствования утверждал, что достичь пределов обнаружения attomol уровней прибора произвоССВ. На основе самых последних литературе, 6 аналитические процедуры должны включать надлежащую очистку образца и обогащение в целях удовлетворения пределы обнаружения MS / MS / MS (ионной ловушки) или MS / MS (тройной квадрупольный), используемых в нашем случае.
Bio-вдохновил синтетических процедур соединений 1-4 были разработаны, начиная с 8-bromopurine производных под или фотолиза. 7,12 Эти процедуры предусматривают радикальных реакций каскада, который имитирует механизм повреждения ДНК формирования 5 ',8-cdAdo и 5' ,8-cdGuo поражений. С биологической точки зрения, было установлено, что эти повреждения накапливаются с возрастом в тканях-специфическим образом (печень> почки> мозг), что свидетельствует о механизмах репарации ДНК недостаточно для сохранения генетического материала из этих поражений 13. Действительно, эксцизионной репарации нуклеотидов (НКО) является единственным путем в настоящее время определены для ремонта этих повреждений 2.
Эти два классаэс-соединений показаны на рисунках 1 и 5 не являются коммерчески доступные на данный момент, однако к синтетической стратегии описаны в литературе не было бы трудно подготовить эти соединения для коммерческого использования.
Междисциплинарный подход, предоставляемый исследования химической биологии не только имеет огромное значение в выявлении новых механизмов, происходящих в биологической среде, но и дает основной вклад в открытие биомаркеров и диагностических средств, в конечном счете, чего новинка в сфере здравоохранения и стратегии профилактики 14. химические вклад необходим для успешного развития молекулярной медицины, создания интегрированных платформ и панелей для метаболического профилирования которая, как ожидается, позволит оптимально рационализации разработки мер вмешательства, либо терапевтические и питательные, что снижает неопределенность и неудач, когда они могут быть предсказуемым.
Раскрытие информации
Нет конфликта интересов объявлены.
Благодарности
Финансовая поддержка со стороны Ministero dell'Istruzione, dell'Universita делла Ricerca (PRIN-2009K3RH7N_002) и Мари Кюри Intra-Европейского Содружества (CYCLOGUO-298555), а также спонсорство COST Action CM0603 на "Свободные радикалы в химической биологии и COST Action CM1201 на "Biomimetic Радикальная химия" с благодарностью.
Материалы
| Name | Company | Catalog Number | Comments |
| MATERIALS | |||
| Cholesteryl linoleate ≥98% | Sigma-Aldrich | C0289-100 mg | |
| Cholesteryl arachidonate≥95% | Sigma-Aldrich | C8753-25mg | |
| 2-mercapt–thanol | Sigma-Aldrich | M6250-100 ml | |
| 2-propanol | Sigma-Aldrich | 34965-1L | |
| Methanol 215 SpS | Romil | H409-2,5 L | |
| Ethanol | Sigma-Aldrich | 02860-2.5L | |
| Chloroform SpS | Romil | H135 2,5 L | |
| n-Hexane 95% SpS | Romil | H389 2,5 L | |
| Acetonitrile 230 SpS | Romil | H047 2,5 L | |
| Dichloromethane SpS | Romil | H2022,5 L | |
| Carbon tetrachloride | Sigma-Aldrich | 107344-1L | |
| Sodium iodide | Sigma-Aldrich | 383112-100G | |
| Sodium hydrogen carbonate | Carlo Erba | 478536-500 g | |
| Diethyl ether | Sigma-Aldrich | 309966-1L | |
| NaCl | Sigma-Aldrich | S7653-5KG | |
| NaOH solid | Sigma-Aldrich | 221465-25G | |
| NH4OH sol. 28%-30% | Sigma-Aldrich | 221228-1L-A | |
| Acetic acid | Sigma-Aldrich | 320099-500ML | |
| Ammonium Cerium(IV)sulfate dihydride | Sigma-Aldrich | 221759-100G | |
| Ammonium Molybdate tetrahydrate | Sigma-Aldrich | A7302-100G | |
| Sulfuric Acid 95%-98% | Sigma-Aldrich | 320501-1L | |
| Silver Nitrate | Sigma-Aldrich | 209139-25G | |
| Sodium sulfate anhydrous | Sigma-Aldrich | 238597-500G | |
| Nuclease P-I from penicillium citrinum | Sigma-Aldrich | N8630-1VL | |
| Phosphodiesterase II type I-sa | Sigma-Aldrich | P9041-10UN | |
| Erythro-9-(2-hydroxy-3-nonyl)adenine, hc | Sigma-Aldrich | E114-25MG | |
| Phosphatase alkaline type VII-t from*bov | Sigma-Aldrich | P6774-1KU | |
| Phosphodiesterase I type VI | Sigma-Aldrich | P3134-100MG | |
| Deoxyribonuclease II type IV from*porcin | Sigma-Aldrich | D4138-20KU | |
| Trizma(r) base, biotechnology performanc ce | Sigma-Aldrich | T6066-100G | |
| EDTA | Sigma-Aldrich | E1644-100G | |
| Succinic acid bioxtra | Sigma-Aldrich | S3674-250G | |
| Calcium chloride | Sigma-Aldrich | C5670-100G | |
| Formic acid, 98 % | Sigma-Aldrich | 06440-100ML | |
| Amicon Ultra-0.5 Centrifugal Filter Unit with Ultracel-3 membrane | Millipore | UFC500324 | |
| 8-Bromo-2'-deoxyguanosine | Berry Associates | PR3290-1 g | |
| 8-Bromo-2'-deoxyadenosine | Berry Associates | PR3300-1 g | |
| Sodium iodide | Sigma-Aldrich | 383112-100G | |
| Sodium hydrogen carbonate | Carlo Erba | 478536-500 g | |
| 2'-deoxyguanosine:H2O (U-15N5, 96-98%) | Cambridge Isotope Laboratories, Inc | CILNLM-3899-CA-0.1 | |
| 2'-deoxyadenosine (U-15N5, 98%) 95%+ CHEMICAL PURITY | Cambridge Isotope Laboratories, Inc | CILNLM-3895-0.1 | |
| Nitrous oxide (N2O) | Air Liquide | ||
| Deoxyribonucleic acid from calf thymus | Sigma Aldrich | D4522-5MG | |
| EQUIPMENT | |||
| 60Co-Gammacell | AECL- Canada | 220 | |
| Immersion well reaction medium pressure 125 watts | Photochemical reactors ltd | Model 3010 | |
| Evaporating flask 250 ml | Heidolph | P/N NS 29/32 514-72000-00 | |
| Luna 5 μm C18(2) 100 Å, LC Column 250 x 4.6 mm | Phenomenex | 00A-4252-E0 | |
| Alltima C8 Column 250 x 10 mm 5 μm | Grace | 88081 | Semipreparative |
| SecurityGuard Kit | Phenomenex | KJ0-4282 | Analytical holder kit and accessories |
| Holder for 10.0 mm ID cartridges | Phenomenex | AJ0-7220 | Semipreparative holder |
| 10.0 mm ID cartridges | Phenomenex | AJ0-7221 | |
| High-performance liquid chromatography (HPLC) | Agilent | 1100 | |
| LC/MS/MS | Applied Biosystems | 4000QTRAP System | |
| Tandem mass ESI spectrometer | (Bruker Daltonics) | Esquire 3000 plus | |
| Vial 2-4 ml | SUPELCO | Cod 27516 | |
| Vial 4 ml | SUPELCO | Cod 27517 | |
Ссылки
- Ferreri, C., Chatgilialoglu, C. Membrane lipidomics and the geometry of unsaturated fatty acids: from biomimetic models to biological consequences. Methods Molecular Biology. 579, 391-412 (2009).
- Chatgilialoglu, C., Ferreri, C., Terzidis, M. A. Purine 5',8-cyclonucleoside lesions: chemistry and biology. Chemical Society Reviews. 40 (3), 1368-1382 (2011).
- Chatgilialoglu, C., Ferreri, C., et al. Radiation-induced reductive modifications of sulfur-containing amino acids within peptides and proteins. Journal of Proteomics. 74 (11), 2264-2273 (2011).
- Chatgilialoglu, C., Ferreri, C. Trans lipids: the free radical path. Accounts Chemical Research. 38 (6), 441-448 (2005).
- Melchiorre, M., Torreggiani, A., Chatgilialoglu, C., Ferreri, C. Lipid markers of geometrical radical stress: synthesis of mono-trans cholesteryl esters isomers and detection in human plasma. Journal of the American Chemical Society. 133 (38), 15184-15190 (2011).
- Wang, J., Yuan, B., Guerrero, C., Bahde, R., Gupta, S., Wang, Y. Quantification of Oxidative DNA Lesions in Tissues of Long-Evans Cinnamon Rats by Capillary High-Performance Liquid Chromatography-Tandem Mass Spectrometry Coupled with Stable Isotope-Dilution Method. Analytical Chemistry. 83 (6), 2201-2209 (2011).
- Boussicault, F., Kaloudis, P., Caminal, C., Mulazzani, Q. G., Chatgilialoglu, C. The fate of C5' radicals of purine nucleosides under oxidative conditions. Journal of the American Chemical Society. 130 (26), 8377-8385 (2008).
- Ferreri, C., Kratzsch, S., Brede, O., Marciniak, B., Chatgilialoglu, C. Trans lipids formation induced by thiols in human monocytic leukemia cells. Free Radicals Biology & Medicine. 38 (9), 1180-1187 (2005).
- Zambonin, L., Ferreri, C., et al. Occurrence of trans fatty acids in rats fed a trans-free diet: a free radical-mediated formation. Free Radicals Biology & Medicine. 40 (9), 1549-1556 (2006).
- Puca, A. A., Andrew, P., et al. Fatty acids profile of erythrocyte membranes as possible biomarker of longevity. Rejuvenation Research. 11 (1), 63-72 (2008).
- Belmadoui, N., Boussicault, F., et al. Radiation-induced formation of purine 5',8-cyclonucleosides in isolated and cellular DNA: high stereospecificity and modulating effect of oxygen. Organic & Biomolecular Chemistry. 8 (14), 3211-3219 (2010).
- Chatgilialoglu, C., Bazzanini, R., Jimenez, L. B., Miranda, M. A. (5'S)- and (5'R)-5',8-cyclo-2'-deoxyguanosine: mechanistic insights on the 2'-deoxyguanosin-5'-yl radical cyclization. Chemical Research in Toxicology. 20 (12), 1820-1824 (2007).
- Wang, J., Clauson, C. L., Robbins, P. D., Niedernhofer, L. J., Wang, Y. The oxidative DNA lesions 8,5'-cyclopurines accumulate with aging in a tissue-specific manner. Aging Cell. 11 (4), 714-716 (2012).
- Ferreri, C., Chatgilialoglu, C. The role of fatty acid-based functional lipidomics in the development of molecular diagnostic tools. Expert Review of Molecular Diagnostics. 12 (7), 767-780 (2012).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены