Method Article
Radicais Livres em Biologia Química: de comportamento químico para o Desenvolvimento de biomarcadores
Neste Artigo
Resumo
Radical baseado em química biomimética tem sido aplicado para a construção de bibliotecas, necessários para o desenvolvimento de biomarcadores.
Resumo
O envolvimento dos radicais livres em ciências da vida tem aumentado constantemente ao longo do tempo e tem sido ligado a vários processos fisiológicos e patológicos. Este assunto abrange diversas áreas científicas, abrangendo desde a química, física, biológica e bioorganic para a biologia e medicina, com aplicações para a melhoria da qualidade de vida, saúde e envelhecimento. Competências multidisciplinares são necessários para a investigação completa das várias facetas do processo radicais no ambiente biológico e químico conhecimento desempenha um papel crucial em revelar processos básicos e mecanismos. Nós desenvolvemos uma abordagem de biologia química capaz de se conectar a reatividade química de radicais livres com processos biológicos, fornecendo informações sobre as rotas mecanísticas e produtos. O núcleo da presente abordagem é a concepção de modelos biomiméticos para estudar o comportamento de biomoléculas (lípidos, ácidos nucleicos e proteínas) em sistemas aquosos, obtendo insights da reacção das vias, bem como ums construção de bibliotecas moleculares dos produtos livres de reação radical. Neste contexto, pode ser utilizada com sucesso para a descoberta de biomarcadores e exemplos são fornecidos com duas classes de compostos: mono-trans isómeros de ésteres de colesterol, que são sintetizados e utilizados como referência para a detecção em plasma humano, e de purinas 5 ',8-ciclo-2 '-desoxiribonucleósidos, preparados e utilizados como referência no protocolo para a detecção de lesões em amostras de DNA, depois de radiações ionizantes ou obtidos a partir de diferentes condições de saúde.
Introdução
A reatividade de radicais livres revelou sua enorme importância para muitos eventos biológicos, incluindo o envelhecimento e inflamação. Hoje em dia, é cada vez mais evidente que a clarificação de cada passo químico envolvido nesta reactividade é necessário, de forma a compreender os mecanismos subjacentes e estratégias prevêem eficazes para o controlo de radicais livres e de reparação dos danos. A contribuição dos estudos químicos é fundamental, mas o estudo direto no ambiente biológico pode ser difícil, uma vez que a sobreposição de diferentes processos complica e perturba a análise dos resultados e as conclusões relacionadas. Assim, a estratégia de modelação reacções de radicais livres em condições biologicamente relacionados tornou-se um passo fundamental na investigação de mecanismos químicos em biologia.
Na última década, o nosso grupo desenvolveu modelos de processos do radical livre sob condições biomiméticos. Em particular, PTvisaged transformações biologicamente relevantes de ácidos graxos insaturados, nucleosídeos e enxofre contendo aminoácidos e colocá-los no caminho certo para ser avaliado e validado como biomarcadores do estado de saúde 1-4.
Nossa abordagem geral consiste de três módulos:
- Síntese orgânica, que permite o acesso a biomoléculas modificadas adequadamente. O plano de síntese pode também ser concebido de forma a simular os processos de radicais livres que ocorrem no ambiente biológico, assim, a aplicação de condições capazes de simular o processo biológico de interesse, que é o princípio da química biomimética radical. Em modelos biomiméticos o meio de reacção é água ou um meio heterogéneo devido à coexistência de compartimentos hidrófilos e hidrófobos. A vantagem de trabalhar com modelos biomiméticos é ter um ambiente simplificado de reação com parceiros conhecidos, em que a reatividade e os produtos podem ser examinados com mais detalhes, possivelmente descobrindoquímicos novas vias. A partir deste passo informações mecanicista e cinética podem ser obtidas;
- Análise, purificação e caracterização dos produtos, proporcionando informação estrutural e química das biomoléculas modificadas, a fim de organizar bibliotecas moleculares e facilitar recognition.in o ambiente mais complexo biológico. Os protocolos são estabelecidos tendo em vista também a resolução de misturas complexas de compostos, tais como aqueles derivados a partir de espécimes biológicos;
- Desenvolvimento biomarcador utilizando amostras biológicas derivadas quer por experiências in vitro utilizando culturas de células e em estudos in vivo, a partir de animais e seres humanos. Os protocolos desenvolvidos em modelos biomiméticos são então aplicados à análise de amostras complexas, prever as transformações de radicais livres sob condições diferentes. Bibliotecas moleculares desenvolvidos por síntese são de grande ajuda para as descobertas das ciências da vida. A informação recolhida sobre os radicais livres transformações give a oportunidade de descobrir estratégias de reparação e prevenção. Bases de dados dos resultados pode ser utilizado para uma avaliação cuidadosa por análise multivariada do significado de biomarcadores, bem como possíveis factores associados.
Nós escolhemos duas classes de biomarcadores para acreditar nesta abordagem: ésteres de colesterilo e de purinas 5 ',8-ciclo-2'-desoxiribonucleósidos.
Protocolo
1. Síntese de Mono-trans de ésteres de colesterilo
- Dissolver os ésteres de colesterilo (linoleato de colesterilo ou araquidonato éster) em 2-propanol (15 mM). Para uma melhor solubilização, as amostras foram sonicadas durante 15 min sob atmosfera de árgon.
- Transferir a solução para um reactor de quartzo fotoquímica, adicionar 2-mercaptoetanol em 2-propanol (a concentração atingir 7 mM, a partir de uma solução-mãe 2 M de tiol). Lavar a mistura de reacção com árgon, durante 20 min, a fim de eliminar a presença de oxigénio na solução.
- Irradiar a mistura reaccional através de luz UV usando uma lâmpada de mercúrio de baixa pressão de 5,5 W a 22 ± 2 ° C durante 4 min. Monitor analítico Ag-TLC (cromatografia de prata fina camada) a evidência da formação de ésteres de colesterilo mono-trans (veja a Figura 1 para as fórmulas químicas). A coloração de TLC é levada a cabo, vertendo a placa na solução de molibdato de amónio e cério (CAM), e as manchas aparecem no aquecimentoa placa. Extingue-se a reacção numa fase inicial, a fim de recuperar o material de partida, que pode ser reutilizado para executar outras rondas de isomerização, a obtenção de um aumento do rendimento global.
- Recolher a mistura reaccional num balão de fundo redondo, lavando o aparelho com alguns ml de 2-propanol. Remover o solvente e purifica-se os isómeros trans de mono-ésteres de colesterilo por TLC-Ag, como descrito na literatura. 5 Utilização de hexano-éter dietílico (9:1 v / v) como eluente para mono-trans linoleato de colesterilo isómeros, ao passo que o uso de hexano -dietil éter-ácido acético (9:1:0,1 v / v) para mono-trans de colesterilo do ácido araquidônico.
2. Isolamento da fracção éster de colesterol a partir de soro humano
- Diluir 1 ml de soro humano (obtido por centrifugação do sangue) com 1 ml de salmoura e verter a solução para um funil de separação e sob uma corrente de árgon, a fim de evitar artefactos (por exemplo, aductos de oxidação). Adicionar 10 ml de clorofórmio-metanol (2: 1 v / v) três vezes. Agitar o funil de separação muito lentamente, a fim de limitar a formação da emulsão devido à presença de albumina.
- Lavar as camadas orgânicas uma vez com salmoura (10 ml), em seguida, recolher em um balão de Erlenmeyer sob um fluxo de árgon, seca-se sobre sulfato de sódio anidro. Remover os voláteis por evaporação rotativa para proporcionar um óleo amarelo (fracção de lípido total de plasma).
- Tome-se o produto em bruto com 1 mL de clorofórmio-metanol (2:1 v / v), para uma carga de TLC preparativa sob uma corrente de árgon, e utilização de uma mistura de hexano-éter dietílico (9:1 v / v) como eluente . Raspar a porção de sílica que contém a fracção de ésteres de colesterilo e despeje em um frasco. Em seguida, extrair de sílica (3 × 5 ml) com clorofórmio-metanol (2:1 v / v), as camadas orgânicas recolher e remover o solvente para se obter, após a evaporação da fracção pura de ésteres de colesterilo (normalmente a ~ 1,5 mg).
- Mantenha ésteres de colesterol num frasco escuro coberto por folha de alumínio sob atmosfera de árgon e armazenar a -20 ° C. Colesterol esters são sensíveis à luz e ao oxigênio.
3. Caracterização de Mono-trans ésteres de colesterilo por Espectroscopia Raman
- Extrair ésteres de colesterol a partir do soro humano (≥ 0,7 mg), tal como descrito na secção 2, dissolve-se numa pequena quantidade de tetracloreto de carbono (≤ ul 10) e colocar num frasco. CCl 4 é seleccionado como solvente porque o seu sinal de Raman não se sobrepõe com a região de interesse de análise de ésteres de colesterilo.
- Transferir a solução para o porta-amostras por meio de uma pipeta de vidro descartável, em seguida, cuidadosamente remover o solvente por meio de uma corrente lenta de árgon. Uma vez que um filme uniforme oleosa é formada na parede interna do recipiente de amostra, colocar este último dentro do instrumento de medição.
- Transformada de Fourier do espectro de Raman de ésteres de colesterilo é obtido directamente sobre os extractos de lípidos, sem qualquer reacção de derivatização. A potência do laser sobre a amostra for <100 mW, para evitar danos amostra. O número total de verificaçõespara cada espectro é ≥ 800 para minimizar o ruído de fundo.
- A gama de 1,700-1,630 centímetros -1 do espectro Raman é analisado uma vez que reflecte a contribuição dos C = C ligações duplas presentes na molécula (C = C que se estende de modo). A análise da curva de ajuste é realizado nesta região, permitindo assim a distinção das contribuições sobrepostas de cis e trans de ligações duplas na cadeia de alquilo gordo e dupla ligação no anel B de colesterol (ver a Figura 2).
- Para ajustar corretamente as bandas vibracionais, alguns parâmetros devem ser fixados ou constrangido dentro de limites razoáveis. Os perfis de pico de componentes são descritos como uma combinação linear de Lorentz e funções gaussianas, enquanto que as larguras de banda de meia altura são melhor determinado pela rotina de optimização computador. O número e a posição dos picos de componentes são obtidos utilizando o espectro de quarto derivado, que permitem a detecção de componentes também algumas bandas fracas. Uma vez que o sinala taxa de ruído que se deteriora na diferenciação do sinal pode impedir a utilização do derivado de quarto, alisou quarto derivados com um 13-point função Savitsky-Golay, são de vantagem, portanto, um certo compromisso entre a resolução e relação sinal-ruído é obtida . Encaixe melhor curva são obtidos em menores possíveis c dois valores.
- A presença de isómeros trans é revelado pelo componente em 1671 ± 1 cm-1, para além de, pelo menos, os dois componentes, ligeiramente deslocado para frequências mais baixas, devido à cadeia de ácido gordo e de colesterol C = C ligações duplas. Espectro de Raman representativo do éster de colesterilo no plasma é mostrado na Figura 9. Na inserção da comparação de uma região específica de colesterol linoleato e mono-trans isómeros ácido linoleico colesteril é mostrado.
4. A derivatização de ésteres metílicos de ácidos gordos (FAME) e análise por cromatografia gasosa acoplada
- Dissolverésteres de colesterilo (~ 1,5 mg) com 0,5 ml de uma solução 1 M de hidróxido de sódio em benzeno-metanol (2:3 v / v) e colocar num frasco escuro coberto por folha de alumínio sob atmosfera de árgon.
- Deixar a mistura em agitação à temperatura ambiente e do monitor por TLC utilizando uma mistura de hexano-éter dietílico (9:1 v / v) como eluente. O tempo de reacção é geralmente de 30 minutos, mas um controlo cuidadoso da reacção é necessária. De facto, uma vez que os ésteres metílicos correspondentes são formados, a reacção deve ser arrefecida, a fim de evitar a formação de produtos de degradação e de lado. A TLC mostrou que a formação quantitativa dos ésteres metílicos.
- Extingue-se a mistura de reacção por adição de 1 ml de salmoura e extrai-se os ésteres metílicos com n-hexano (3 x 2 ml). Recolher as camadas orgânicas para um frasco e remover o solvente por evaporação rotativa para dar a fracção de éster de metilo, que é então utilizado para a análise de GC sem purificação adicional.
- Dissolver os ésteres de metilo em uma quantidade mínima de n-hexano (normalmente 1 mg em 50 ul) e injectar no GC equipado com uma altura de 60 m × 0,25 mm × 0,25 ^ m (50%-cianopropil)-metilpolissiloxano de coluna. Utilizar um detector de ionização de chama (FID) com o programa de forno seguintes: temperatura inicial de 165 ° C, parado durante 3 min, seguido por um aumento de 1 ° C / min até 195 ° C, manter durante 40 min, seguido por um segundo um aumento de 10 ° C / min até 240 ° C, e manter durante 10 min. Um modo de pressão constante (29 psi) é escolhido. Hélio ou o hidrogénio, pode ser utilizado como gás de transporte. Os ésteres metílicos são identificados por comparação com os tempos de retenção de amostras autênticas. Figura 10 mostra uma análise representativa de GC FAME obtidos a partir de ésteres de colesterilo no plasma.
5. Síntese de (5'R) - e (5'S) -5 ', 8-ciclo-2'-desoxiadenosina
- Dissolver 33 mg de 8-bromo-2'-desoxiadenosina (8-Br-dado) em acetonitrilo (100 ml), a fim de chegar a uma concentração de mM. Regular o fluxo de gás (Ar ou N2) na fotorreator e encher o appaRatus com a solução de 8-Br-Dado.
- Preparar um septo com o tamanho apropriado para a entrada fotorreator e passar uma agulha ligada à linha de gás inerte através do centro do mesmo. Fechar o sistema com o septo. Lave o gás inerte durante 30 min.
- Irradiar com luz UV utilizando uma lâmpada de mercúrio de média pressão de 125 W a 22 ± 2 ° C durante 15 minutos, recolher a solução para um balão de 250 ml de fundo redondo. Lava-se a foto-reactor, com 10 ml de acetonitrilo e recolher líquido de lavagem no mesmo balão.
- Extingue-se a mistura reaccional em bruto com 1 M de solução de NH OH 4 e evapora-se o solvente no evaporador rotativo.
- Executar alto desempenho de análise de cromatografia líquida (CLAE-UV) com coluna analítica (ver secção instrumentação), sob condições conhecidas, e comparar o perfil com compostos de referência.
- Executar alto desempenho análise por cromatografia líquida (HPLC-UV) com uma coluna analítica (ver secção instrumentação) usando o seguinte solrespiradouros e gradientes: 2 mM de formiato de amónio como solvente A e acetonitrilo como solvente B. Definir a taxa de fluxo de 1 ml / min e o gradiente de 0% de solvente B a 0,3% do solvente B a ser alcançado em 2,2 min. Então B 0,8% em solvente em 4,0 min, em seguida, 1% de solvente B em 4,8 min. Permanecem em 1% de solvente B durante 9 min e, em seguida, passar a 8% de solvente B em 6 min. Depois de passar para 10% do solvente B em 4 min e a 30% de solvente B em 5 min e manter a 30% de solvente b para 5 min outro. Recolher os picos cromatográficos correspondem aos dois produtos diastereoméricos em dois frascos diferentes.
- Medir as absorvâncias das duas fracções recolhidas no espectrofotómetro de UV e calcula a concentração exacta com base na lei de Beer-Lamber (A εlC =, em que A é a absorvância, ε o coeficiente de extinção e l o comprimento da célula). Use a ε coeficiente de extinção da 2'-desoxiadenosina (Dado) (15.400 M -1 cm -1 a 260 nm).
6. Síntese de (5'R) - umd (5'S) -5 ', 8-ciclo-2'-desoxiguanosina
- Dissolver 35 mg de 8-bromo-2'-desoxiguanosina (8-Br-dGuo) e 30 mg de iodeto de sódio (NaI), em água destilada (100 ml) de modo a atingir a concentração 1 mM e 2 mM, respectivamente. Regular o fluxo de gás inerte (Ar ou N2) conectado ao fotorreator e encher o fotorreator com a solução de reacção.
- Degass da mistura de reacção como descrito no procedimento 5 (etapa b).
- Irradiar com luz UV utilizando uma lâmpada de mercúrio de média pressão de 125 W a 22 ± 2 ° C durante 30 minutos, recolher a solução para um balão de 250 ml de fundo redondo. Lava-se a foto-reactor, com 10 ml de água e recolher líquido de lavagem no mesmo balão.
- Extingue-se a mistura reaccional em bruto com 1 M de solução de NH OH 4 e evapora-se o solvente sob vácuo.
- Realizar análise conforme descrito no Procedimento 5 (passos E a G). Use a ε coeficiente de extinção da 2'-desoxiguanosina (dGuo) (11.700 M -1 cm -1 a 260 nm).
7. Síntese de purina Labeled isotópica (5'R) - e (5'S) -5 ',8-cyclonucleosides
- Preparar 2 ml de 1 mM de solução aquosa (água destilada) dos 15 N isotópica nucleósidos de purina marcados ([15N 5] Dado ou [15N 5] dGuo) num frasco de vidro (4 ml), com uma tampa de septo.
- Ligue o frasco com a tampa de septo e conectar-se a linha de gás (N 2 O para a saturação da solução) através de uma agulha no septo que atinge o fundo do frasco. Outra pequena agulha no septo tampa funciona como a saída de gás.
- Lavar a solução com N 2 O durante 30 min. O caudal de gás é regulado para ser muito baixa.
- A agulha de saída é primeiro retirada e depois de 1 'a um tempo decorre, a fim de ter uma pequena pressão no interior do frasco.
- Colocar a solução no aparelho da radiólise gama de 8 horas (com base no cálculo de uma taxa de dose de ca. 4,5 Gy / min).
- Depois de temperar a reacção em bruto com 1 M de NH 4 OH solução.
- Executar alto desempenho análise por cromatografia líquida (HPLC-UV), sob condições conhecidas, 6 e comparar o cromatograma com as referências padrão.
8. Radiólise gama de soluções de DNA aquosas
- Prepare 1 ml de 0,5 mg / ml de solução (água destilada) de ADN de timo de vitelo e colocado em um frasco de vidro (2 ml), com uma tampa de septo.
- Degass a reacção conforme descrito no Procedimento 7 (passos bd).
- Colocar a solução no aparelho da radiólise gama de 30 min (com base no cálculo de dose / taxa de ca. 4,5 Gy / min).
9. Digestão enzimática de DNA
- Para um tubo de Eppendorf contendo 80 ug de ADN, adicionar 8 U de nuclease P1, 0,01 U de fosfodiesterase II, 20 nmol de EHNA em 20 ul de acetato de sódio 300 mM (pH 5,6) e 10 mM de cloreto de zinco. Incubar a mistura a 37 ° C durante 48 horas.
- De seguida, adicionar uma mistura de 8 U de fosfatase alcalina, 0,02 U de phosphodiesterase I, em 40 ul de 0,5 M de tampão Tris-HCl (pH 8,9) para a digestão mistura. A amostra é incubada a 37 ° C durante 2 horas.
- A mistura é neutralizada pela adição de 10% de ácido fórmico.
- Transferir a amostra para um Ultra-0.5 Amicon dispositivo centrífugo de filtro (corte de 3 kDa), adiciona-se 200 ul de H 2 O. tridistilled Coloque a Ultra-filtro para o rotor de centrífuga a 14.000 xg durante 15 min. Em seguida, separar o dispositivo Ultra filtro do tubo de microcentrífuga. Liofilizar a solução de enzima livre no tubo de microcentrífuga.
10. Dessalinização DNA da amostra antes da análise
- Executar alto desempenho de análise de cromatografia líquida (CLAE-UV) com coluna analítica (ver secção instrumentação), seguindo as condições conhecidas. 6
- Dissolve-se o DNA digerido liofilizado em 20 ul de H2O e injectar no HPLC-UV.
- Coletar a amostra em um frasco após a eluição de sal (primeiros minutos) e à direita antes do tim eluiçãoe do nucleósido primeiro (5'R-cdGuo), até ao final do programa cromatográfica.
- A amostra é liofilizada e ressolubilizado em 20 ul de água.
11. Análise Quantitativa LC-MS/MS
- Preparar os HPLC-MS/MS (quadrupolo triplo) antes de iniciar a análise, carregando o método analítico e do método para o detector de MS (ESI) 6.
- Adicionar 1 ul da mistura isotópica de compostos marcados na amostra preparada no Procedimento 7.
- Injectar 20 ul da solução de DNA digerido com cravos em água destilada.
- Os dados cromatográficos obtidos são elaboradas a partir de calibração com compostos de referência anterior. A HPLC representativo executar contendo adenosina e guanosina 2 '-desoxiribonucleósidos e seus derivados oxidativos e cyclo é mostrado na Figura 11.
Resultados
O processo de isomerização foi descrito em particular para os ésteres de colesterilo que proporcionem as mono-isómeros trans de ácidos linoleico e araquidónico, mostrados na Figura 1, tal como os primeiros produtos deste ataque, que podem ocorrer em condições de stress de radicais livres no meio biológico. 5
Na Figura 3, o mecanismo de química envolvida na ligação a isomerização cis-trans dupla é mostrado. A fonte radical é indicado de forma genérica para pagar S centradas radicais. Nos protocolos descritos a fonte de radical é a luz UV, que é capaz de quebrar a ligação presente homolitically SH na molécula de tiol RSH.
A Figura 4 resume os três passos de protocolo para a síntese da classe de lípidos modificados e sua detecção no plasma humano: a síntese representa um processo livre biomimética radical e também fornece uma entrada de uma panela conveniente para o Geometisómeros rical, sem qualquer contaminação por isómeros posicionais seguido de protocolos de purificação e isolamento.
Várias metodologias de análise pode ser aplicado para uma detecção de alta sensibilidade do teor de isómero trans e caracterização da biblioteca de éster mono-trans colesterilo. Em particular, a espectroscopia de Raman pode ser realizada directamente sobre a fracção de éster de colesterol sem derivação (ver Figura 2 e Figura 9).
O segundo exemplo refere-purina 5 ',8-ciclo-2'-desoxiribonucleósidos, que são lesões do ADN criadas pelo ataque de radicais livres na posição C5 'da porção açúcar e subsequente formação de uma ligação covalente entre o açúcar e a base porções. Quatro estruturas podem ser produzidas, ou seja, 5 ', 8-ciclo-2'-desoxiadenosina e 5 ', 8-ciclo-2'-desoxiguanosina, ambos existentes nos 5'R e 5'S formas diastereoméricas (Figura 5). Na Figura 6 tele mecanismo de reacção é mostrado, que envolve a fotólise de 8-bromopurina derivados 5 para dar os correspondentes radical C8 6, que abstrai intramolecularmente um átomo de hidrogénio a partir da posição C5 'selectivamente para se obter o 7-2'-5'-deoxyadenosin ilo. 7 radical sofre ciclização com uma velocidade constante no intervalo de 10 5 -10 6 s-1, 2, seguido de oxidação do radical heteroaromático de 8 para dar os produtos finais 9. A reacção dos radicais hidroxilo, gerado por radiólise da água, com 2'-desoxiadenosina 2'-desoxiguanosina e (10) foi encontrada para ocorrer ca. 10% por abstração de hidrogênio a partir da posição C5 ". 7
A nossa abordagem biologia química para as bibliotecas de purina 5 ',8-ciclo-2'-desoxiribonucleósidos (incluindo compostos marcados) é ilustrada na Figura 7, com a identificação dessas lesões nos oligonucleótidos, bem como em amostras de DNA obtidas a partir de various fontes, tais como, por exemplo, tratada sob condições de radiação ionizante, como mímica das condições de stress radicais.
Na figura 8 um equipamento fotorreator típico é mostrado. O dispositivo permite a irradiação de compostos dissolvidos no solvente apropriado. É constituída por: i) a câmara de reacção equipado com a entrada para o gás inerte (na parte inferior) e duas entradas para a saída do gás e para a adição de reagentes, ii) uma câmara interna que contém a lâmpada de mercúrio ligado a um adequado sistema de refrigeração e de energia eléctrica, que é inserido para dentro da câmara de reacção através de uma junta de vidro.
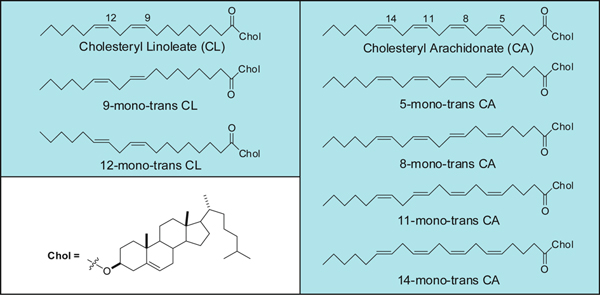
Figura 1. Mono-trans de colesterilo e linoleato de araquidonato.
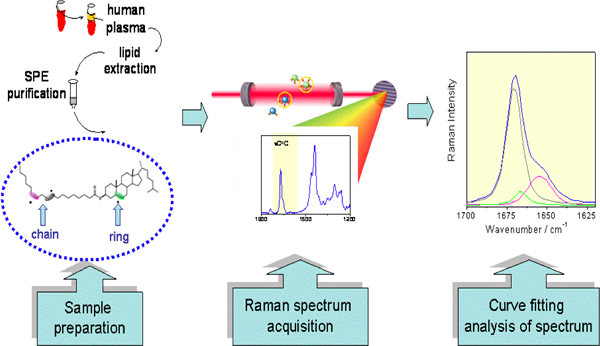
Figura 2. Ésteres de colesterol na análise de soro e humana direta para mono-trans por espectroscopia Raman.
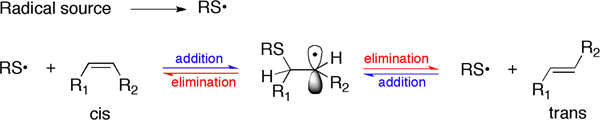
Figura 3. O processo de adição-eliminação, que leva à isomerização cis-trans de ligações duplas por radicais thiyl.
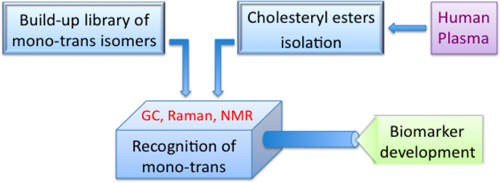
Figura 4. Três passos para o desenvolvimento do protocolo de ésteres mono-trans colesterol como biomarcador de estresse dos radicais livres.

Figura 5. A purina quatro 5 ',8-ciclo-2'-desoxiribonucleósidos diastereoisómeros. Clique aqui para ver maior figura .
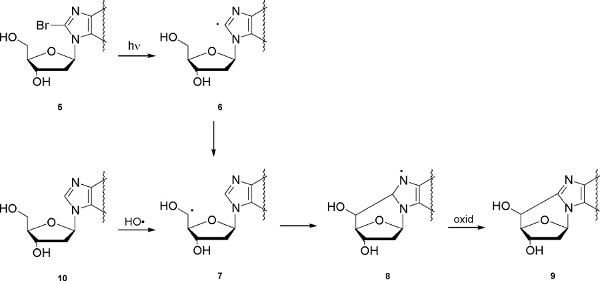
Figura 6. Geração de C5 'radicais, ou por fotólise de 5 ou de 10 por reacção com os radicais HO •, e o mecanismo de purina 5' ,8-ciclo-2 'formação desoxinbonucleosido. para ver figura maior .
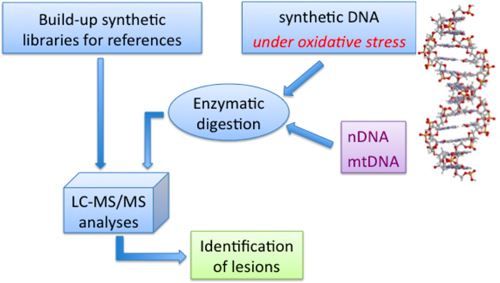
Figura 7. Protocolo fou a identificação de algumas lesões radical à base de ADN; mtDNA: DNA mitocondrial, nDNA: DNA nuclear.

Figura 8. Reator fotoquímico.
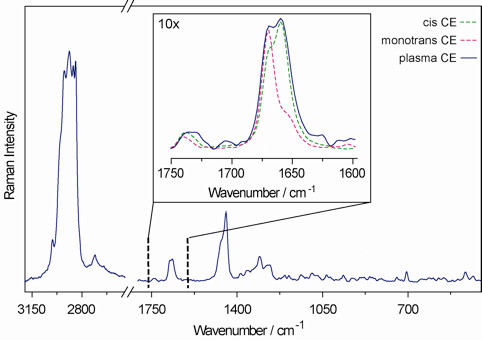
Figura 9. Espectro de Raman representativo de plasma de ésteres de colesterilo. Na comparação da inserção de uma região específica de colesteril com o linoleato de colesterilo e mono-trans de ácido linoleico.
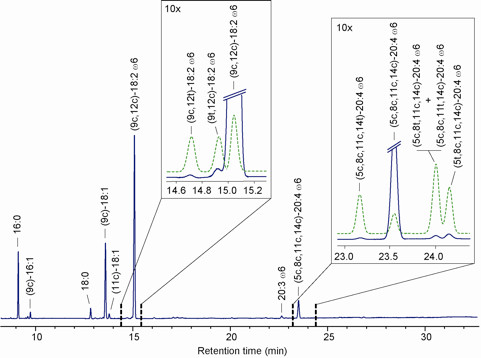
Figura 10. Representante análise GC de FAME obtida a partir de ésteres de colesterilo no plasma.
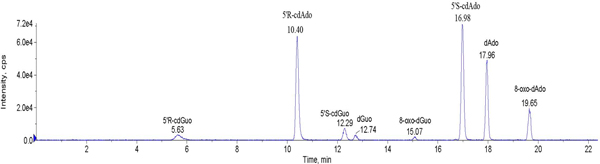
Figura 11. Representante HPLC executar contendo 2'-desoxiadenosina e 2'desoxiguanosina juntamente com a sua oxidativo e purina 5 ',8-ciclo-2'-Deoxyribo nucleosídeos. Clique aqui para ver maior figura .
Discussão
A conversão de ocorrência natural de ácidos gordos insaturados cis para trans isómeros geométricos é uma transformação relacionada com a produção de stress radical no ambiente biológico. Lipidos da membrana celular, que contêm os ácidos gordos, é um alvo relevante para o stress biológico e radical que primeiro estudou a endógeno isomerização cis-trans fosfolípidos em culturas de células, animais e seres humanos que avaliam protocolos analíticos em cada caso. 8-10 Foi demonstrado que esta transformação pode ocorrer através de uma variedade de compostos contendo S, incluindo tióis, tioéteres e dissulfetos, que, sob diferentes condições de stress radicais são capazes de gerar radicais thiyl, ou seja, o agente de isomerização (Figura 3). O exemplo mostrado no artigo centra-se na classe de ésteres de colesterilo, que representam uma fracção muito conhecido de lípidos no plasma, estritamente envolvido no metabolismo das lipoproteínas. A ligação éster entre os ácidos gordos e chorol é biossintetizado pela transferência de ácidos gordos a partir da posição 2 da porção de glicerol de fosfatidil de colesterol, um passo catalisado pela enzima acil lecitina colesterol transferase (LCAT). Por isso, os ésteres de colesterol no plasma são estritamente relacionado com o volume de negócios lipídica da membrana, e contêm proporções relativamente elevadas dos ácidos gordos poli-insaturados (PUFA), tipicamente presentes em fosfatidilcolinas, isto é, linoleico e os ácidos araquidónico. Formação de lipoproteínas está envolvido em doenças cardiovasculares e metabólicas. A reactividade de ésteres de colesterilo naturais com os radicais livres podem ocorrer nas ligações duplas de linoleato e resíduos de ácido araquidônico, que podem ser transformados nos correspondentes isómeros geométricos trans (ver Figura 1 para as estruturas). Caracterização do teor de éster de colesterilo trans em amostras biológicas é interessante para o desenvolvimento de biomarcadores. Uma metodologia indirecta consiste na transformação de cholesteryésteres de l, isolada de plasma para os correspondentes ésteres metílicos de ácidos gordos (FAME) e separação por protocolos cromatográficos de gás. Neste caso, a calibração das referências normalizadas de cis e trans de ésteres metílicos de ácidos gordos é executada, a fim de permitir a quantificação do teor de trans nas amostras. Com base nos estudos analíticos realizados sobre a biblioteca de éster de colesterilo, propôs-se aplicar também um método baseado na espectroscopia de Raman, que pode ser realizada directamente sobre a fracção de ésteres de colesterilo, isolada de plasma, sem derivatização após a FAME correspondente (ver Figuras 2 e 9). É interessante notar que até agora não existem métodos de sucesso são descritos para cis separado e isômeros trans de ácidos graxos contendo lipídios por HPLC, em vez como descrito por hidroperóxidos de éster de colesterol. Até agora, o método de cromatografia de gás indireta ainda é o melhor método disponível até agora. Por este método o primeiro quantitativa avação do conteúdo mono-trans a partir de ésteres de colesterol derivado isolado a partir de plasma de indivíduos saudáveis foram fornecidas. Usando Detector de Ionização de Chama (FID) do limite de detectabilidade é satisfatório (ppb) e as quantidades nanomolares dos compostos foram detectados. 5. Com sistemas de detecção de diferentes este limite pode ser ainda reduzido. O efeito da radiação ionizante em ésteres de colesterol é matéria de estudos adicionais, se uma resposta linear é obtido em relação à dose aplicada.
Como um segundo exemplo, escolhemos nucleósidos modificados que podem ser produzidos por radicais livres danos de DNA. Os radicais hidroxilo (HO •) são conhecidos por serem os mais prejudiciais Espécies reactivas de oxigénio (ROS) para a sua capacidade para causar modificações químicas de DNA. Lesões simples ou múltiplas podem ocorrer no DNA, que, em células eucarióticas está localizado no núcleo e as mitocôndrias. Identificação e medição das principais classes de oxidativos danos gerados ao DNA requerem o adequado doiate bibliotecas moleculares, a fim de definir os protocolos analíticos. Focamos nosso interesse sobre as lesões mais pequenas em tandem, os quais são purinas 5 ',8-ciclo-2'-desoxiribonucleósidos, tendo uma ligação covalente adicional entre a base e as porções de açúcar criadas pelo ataque de radicais livres. Os compostos são 5 ',8-ciclo-2'-desoxiadenosina e 5 ', 8-ciclo-2'-desoxiguanosina existente nos 5'R e 5'S formas diastereoméricas (Figura 5). O seu potencial para se tornar marcador de stress de radicais livres é a matéria de investigação fundamental. 2 Com efeito, quando o DNA é exposto a HO • abstração radical hidrogénio a partir da posição C5 'do açúcar é um dos possíveis eventos que conduzem à formação destas lesões em tandem. Purina 5 ',8-cyclonucleosides pode ser medido como a soma de diastereómeros por HPLC-MS/MS enzimaticamente digeridas em amostras irradiadas γ ADN variando 1-12 lesões / 10 6 nucleósidos / Gy indo ausência forma de oxigénio ao nível fisiológico de oxigénio Eutecidos n, a proporção diastereomérica 5'R / 5'S sendo ~ ~ 4 e 3 para 5 ',8-cdAdo e 5' ,8-cdGuo, respectivamente (Figura 11). 11 É interessante notar que a relação entre a dose de radiação e 5 ',8-cdAdo e 5' ,8-cdAdo lesões detectadas no ADN celular está longe de serem compreendidos. O experimento único baseado irradiação 2kGy relatado na experimental não podem ser considerados conclusivos. 11 Outras experiências deste tipo e quantificação do método dos quatro lesões são necessários para definir tais relações. A detecção destas lesões e as transformações oxidativas mais populares (tais como 8-oxo-2 '-desoxiguanosina, 8-oxodGuo) são assunto de investigações intensas, evidenciando a importância de ambas as lesões durante o metabolismo oxidativo. 6,13 O uso de HPLC -MS/MS (quadrupolo triplo) tem um limite de detecção de cerca de 30fmol para todos os quatro lesões. Melhorias últimos são requeridas para alcançar limites de detecção dos níveis attomol pela produ instrumentoRCEs. Com base na literatura recente, 6 procedimentos analíticos têm de incluir a limpeza adequada da amostra e o enriquecimento, a fim de satisfazer os limites de detecção da MS / MS / MS (armadilha de iões) ou da MS / MS (quadrupolo triplo) usado no nosso caso.
Bio-inspirados procedimentos de síntese de compostos 1-4 foram desenvolvidas a partir da 8-bromopurina derivados segundo ou fotólise. 7,12 Estes procedimentos envolvem a reacção em cascata radical que imita o mecanismo de dano do ADN de formação de 5 ',8-cdAdo e 5' ,8-cdGuo lesões. A partir de perspectivas biológicas, verificou-se que estas lesões se acumulam com o envelhecimento de um modo específico do tecido (fígado> rim cérebro>), fornecendo a evidência de que os mecanismos de reparação de ADN são inadequadas para preservar o material genético a partir de tais lesões. 13 Com efeito, a reparação de excisão de nucleótidos (NER) é o único caminho actualmente identificados para a reparação das lesões. 2
A classe doises de compostos mostrados nas Figuras 1 e 5 não estão comercialmente disponíveis no momento, no entanto, por as estratégias de síntese descritos na literatura, não seria difícil de preparar estes compostos para uso comercial.
A abordagem multidisciplinar fornecida por estudos de biologia química não só tem um enorme valor para a identificação de novos mecanismos que ocorrem no ambiente biológico, mas também dá um contributo fundamental para a descoberta de biomarcadores e diagnóstico, em última análise, trazendo novidade em cuidados de saúde e estratégias de prevenção. 14 A contribuição química é necessária para um bom desenvolvimento da medicina molecular, criando plataformas integradas e painéis para perfis metabólicos, que se prevê venham a permitir uma óptima racionalização do desenho da intervenção, quer terapêutica e nutricional, reduzir as incertezas e falhas quando podem ser previsíveis.
Divulgações
Não há conflitos de interesse declarados.
Agradecimentos
O apoio financeiro da dell'Istruzione Ministero, della Ricerca dell'Universita (PRIN-2009K3RH7N_002) e Marie Curie Fellowship intra-europeu (CYCLOGUO-298555), bem como o patrocínio da Acção COST CM0603 em "Radicais Livres em Biologia Química e Acção COST CM1201 em "Química Biomimetic Radical" Agradecemos imensamente.
Materiais
| Name | Company | Catalog Number | Comments |
| MATERIALS | |||
| Cholesteryl linoleate ≥98% | Sigma-Aldrich | C0289-100 mg | |
| Cholesteryl arachidonate≥95% | Sigma-Aldrich | C8753-25mg | |
| 2-mercapt–thanol | Sigma-Aldrich | M6250-100 ml | |
| 2-propanol | Sigma-Aldrich | 34965-1L | |
| Methanol 215 SpS | Romil | H409-2,5 L | |
| Ethanol | Sigma-Aldrich | 02860-2.5L | |
| Chloroform SpS | Romil | H135 2,5 L | |
| n-Hexane 95% SpS | Romil | H389 2,5 L | |
| Acetonitrile 230 SpS | Romil | H047 2,5 L | |
| Dichloromethane SpS | Romil | H2022,5 L | |
| Carbon tetrachloride | Sigma-Aldrich | 107344-1L | |
| Sodium iodide | Sigma-Aldrich | 383112-100G | |
| Sodium hydrogen carbonate | Carlo Erba | 478536-500 g | |
| Diethyl ether | Sigma-Aldrich | 309966-1L | |
| NaCl | Sigma-Aldrich | S7653-5KG | |
| NaOH solid | Sigma-Aldrich | 221465-25G | |
| NH4OH sol. 28%-30% | Sigma-Aldrich | 221228-1L-A | |
| Acetic acid | Sigma-Aldrich | 320099-500ML | |
| Ammonium Cerium(IV)sulfate dihydride | Sigma-Aldrich | 221759-100G | |
| Ammonium Molybdate tetrahydrate | Sigma-Aldrich | A7302-100G | |
| Sulfuric Acid 95%-98% | Sigma-Aldrich | 320501-1L | |
| Silver Nitrate | Sigma-Aldrich | 209139-25G | |
| Sodium sulfate anhydrous | Sigma-Aldrich | 238597-500G | |
| Nuclease P-I from penicillium citrinum | Sigma-Aldrich | N8630-1VL | |
| Phosphodiesterase II type I-sa | Sigma-Aldrich | P9041-10UN | |
| Erythro-9-(2-hydroxy-3-nonyl)adenine, hc | Sigma-Aldrich | E114-25MG | |
| Phosphatase alkaline type VII-t from*bov | Sigma-Aldrich | P6774-1KU | |
| Phosphodiesterase I type VI | Sigma-Aldrich | P3134-100MG | |
| Deoxyribonuclease II type IV from*porcin | Sigma-Aldrich | D4138-20KU | |
| Trizma(r) base, biotechnology performanc ce | Sigma-Aldrich | T6066-100G | |
| EDTA | Sigma-Aldrich | E1644-100G | |
| Succinic acid bioxtra | Sigma-Aldrich | S3674-250G | |
| Calcium chloride | Sigma-Aldrich | C5670-100G | |
| Formic acid, 98 % | Sigma-Aldrich | 06440-100ML | |
| Amicon Ultra-0.5 Centrifugal Filter Unit with Ultracel-3 membrane | Millipore | UFC500324 | |
| 8-Bromo-2'-deoxyguanosine | Berry Associates | PR3290-1 g | |
| 8-Bromo-2'-deoxyadenosine | Berry Associates | PR3300-1 g | |
| Sodium iodide | Sigma-Aldrich | 383112-100G | |
| Sodium hydrogen carbonate | Carlo Erba | 478536-500 g | |
| 2'-deoxyguanosine:H2O (U-15N5, 96-98%) | Cambridge Isotope Laboratories, Inc | CILNLM-3899-CA-0.1 | |
| 2'-deoxyadenosine (U-15N5, 98%) 95%+ CHEMICAL PURITY | Cambridge Isotope Laboratories, Inc | CILNLM-3895-0.1 | |
| Nitrous oxide (N2O) | Air Liquide | ||
| Deoxyribonucleic acid from calf thymus | Sigma Aldrich | D4522-5MG | |
| EQUIPMENT | |||
| 60Co-Gammacell | AECL- Canada | 220 | |
| Immersion well reaction medium pressure 125 watts | Photochemical reactors ltd | Model 3010 | |
| Evaporating flask 250 ml | Heidolph | P/N NS 29/32 514-72000-00 | |
| Luna 5 μm C18(2) 100 Å, LC Column 250 x 4.6 mm | Phenomenex | 00A-4252-E0 | |
| Alltima C8 Column 250 x 10 mm 5 μm | Grace | 88081 | Semipreparative |
| SecurityGuard Kit | Phenomenex | KJ0-4282 | Analytical holder kit and accessories |
| Holder for 10.0 mm ID cartridges | Phenomenex | AJ0-7220 | Semipreparative holder |
| 10.0 mm ID cartridges | Phenomenex | AJ0-7221 | |
| High-performance liquid chromatography (HPLC) | Agilent | 1100 | |
| LC/MS/MS | Applied Biosystems | 4000QTRAP System | |
| Tandem mass ESI spectrometer | (Bruker Daltonics) | Esquire 3000 plus | |
| Vial 2-4 ml | SUPELCO | Cod 27516 | |
| Vial 4 ml | SUPELCO | Cod 27517 | |
Referências
- Ferreri, C., Chatgilialoglu, C. Membrane lipidomics and the geometry of unsaturated fatty acids: from biomimetic models to biological consequences. Methods Molecular Biology. 579, 391-412 (2009).
- Chatgilialoglu, C., Ferreri, C., Terzidis, M. A. Purine 5',8-cyclonucleoside lesions: chemistry and biology. Chemical Society Reviews. 40 (3), 1368-1382 (2011).
- Chatgilialoglu, C., Ferreri, C., et al. Radiation-induced reductive modifications of sulfur-containing amino acids within peptides and proteins. Journal of Proteomics. 74 (11), 2264-2273 (2011).
- Chatgilialoglu, C., Ferreri, C. Trans lipids: the free radical path. Accounts Chemical Research. 38 (6), 441-448 (2005).
- Melchiorre, M., Torreggiani, A., Chatgilialoglu, C., Ferreri, C. Lipid markers of geometrical radical stress: synthesis of mono-trans cholesteryl esters isomers and detection in human plasma. Journal of the American Chemical Society. 133 (38), 15184-15190 (2011).
- Wang, J., Yuan, B., Guerrero, C., Bahde, R., Gupta, S., Wang, Y. Quantification of Oxidative DNA Lesions in Tissues of Long-Evans Cinnamon Rats by Capillary High-Performance Liquid Chromatography-Tandem Mass Spectrometry Coupled with Stable Isotope-Dilution Method. Analytical Chemistry. 83 (6), 2201-2209 (2011).
- Boussicault, F., Kaloudis, P., Caminal, C., Mulazzani, Q. G., Chatgilialoglu, C. The fate of C5' radicals of purine nucleosides under oxidative conditions. Journal of the American Chemical Society. 130 (26), 8377-8385 (2008).
- Ferreri, C., Kratzsch, S., Brede, O., Marciniak, B., Chatgilialoglu, C. Trans lipids formation induced by thiols in human monocytic leukemia cells. Free Radicals Biology & Medicine. 38 (9), 1180-1187 (2005).
- Zambonin, L., Ferreri, C., et al. Occurrence of trans fatty acids in rats fed a trans-free diet: a free radical-mediated formation. Free Radicals Biology & Medicine. 40 (9), 1549-1556 (2006).
- Puca, A. A., Andrew, P., et al. Fatty acids profile of erythrocyte membranes as possible biomarker of longevity. Rejuvenation Research. 11 (1), 63-72 (2008).
- Belmadoui, N., Boussicault, F., et al. Radiation-induced formation of purine 5',8-cyclonucleosides in isolated and cellular DNA: high stereospecificity and modulating effect of oxygen. Organic & Biomolecular Chemistry. 8 (14), 3211-3219 (2010).
- Chatgilialoglu, C., Bazzanini, R., Jimenez, L. B., Miranda, M. A. (5'S)- and (5'R)-5',8-cyclo-2'-deoxyguanosine: mechanistic insights on the 2'-deoxyguanosin-5'-yl radical cyclization. Chemical Research in Toxicology. 20 (12), 1820-1824 (2007).
- Wang, J., Clauson, C. L., Robbins, P. D., Niedernhofer, L. J., Wang, Y. The oxidative DNA lesions 8,5'-cyclopurines accumulate with aging in a tissue-specific manner. Aging Cell. 11 (4), 714-716 (2012).
- Ferreri, C., Chatgilialoglu, C. The role of fatty acid-based functional lipidomics in the development of molecular diagnostic tools. Expert Review of Molecular Diagnostics. 12 (7), 767-780 (2012).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoExplore Mais Artigos
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados