Method Article
Миелин олигодендроцитов гликопротеин (МОГ
В этой статье
Резюме
Экспериментальный аутоиммунный энцефаломиелит (ЕАЕ) является признанным животной модели рассеянного склероза. C57BL / 6 мышей иммунизируют миелина олигодендроцитов гликопротеина (MOG) пептида 35-55 (MOG 35-55), в результате чего восходящей периферического паралича, вызванного аутореактивных иммунных клеток в центральной нервной системе. Будут обсуждаться Протоколы для индукции заболевания и мониторинга.
Аннотация
Рассеянный склероз является хроническим расстройством нейрогенный демиелинизирующих центральной нервной системы с сильным нейродегенеративного компонента. Хотя точная этиология заболевания пока неясно, аутореактивные Т-лимфоциты, как полагают, играют центральную роль в его патофизиологии. MS терапия эффективна только частично до сих пор и научно-исследовательских работ и впредь расширять наши знания о патофизиологии этого заболевания и разработать новые стратегии лечения. Экспериментальный аутоиммунный энцефаломиелит (ЕАЕ) является наиболее распространенным животная модель для MS обмена множество клинических и патофизиологических особенностей. Существует широкий разнообразие моделей EAE, которые отражают различные клинические, иммунологические и гистологические аспекты человека MS. Активно-индуцированной ЕАЕ у мышей является самым простым индуцибельный модель с надежными и воспроизводимых результатов. Она особенно подходит для исследования воздействия наркотиков или конкретных генов с помощью трансгенных мышей, зараженных аутоиммунным neuroinflammation. Таким образом, мышей иммунизируют с ЦНС гомогенатах или пептиды миелиновых белков. Из-за низкой иммуногенной потенциала этих пептидов, используют сильные адъюванты. ЕАЕ восприимчивость и фенотип зависит от выбранного антигена и деформации грызунов. C57BL / 6, являются обычно используется штамм для трансгенной конструкции мыши и отвечать числе в миелиновой олигодендроцитов гликопротеина (MOG). Иммуногенный эпитоп MOG 35-55 суспендируют в полном адъюванте Фрейнда (CFA) до иммунизации и коклюшного токсина применяется в день иммунизации и через два дня. Мыши разработать "классический" самоограниченный монофазный EAE с возрастанию вялый паралич в 9-14 дней после иммунизации. Мыши оцениваются ежедневно, используя клиническую систему подсчета очков для 25-50 дней. Обсуждаются Специальные условия для ухода взятия животных с EAE, а также потенциальных применений и ограничений этой модели.
Введение
Рассеянный склероз (РС) представляет собой хроническое воспалительное заболевание демиелинизирующих центральной нервной системы, в которой разрушение олигодендроцитов и нейронов приводит к гетерогенных и накопления клинических симптомов. MS рассматривается в качестве прототипического аутоиммунных расстройств центральной нервной системы (ЦНС) и модели на животных были разработаны, чтобы пролить свет на его сложного патогенеза. Кроме того, в настоящее время методы лечения эффективны лишь частично и целевой основном воспалительный фазу заболевания в то время как нейродегенеративное компонент, вероятно, основная задача для будущих терапевтических подходов 1,2.
Хотя точная этиология заболевания пока неясно, аутоиммунной реакции против эпитопов на миелиновой оболочки аксонов в ЦНС, как предполагается, провоцировать возникновение болезни. Нарушение регуляции иммунной системы, генетической уязвимости и факторов окружающей среды (например, инфекции, витамин D), как полагают,влияние центральные аспекты патофизиологических механизмов МС.
Три различные типы моделей животных в настоящее время создана для исследования патологических форм РС: Вирусные модели, как мышиный вирус энцефаломиелита Theiler в (TMEV), модели, вызванные токсичных веществ, таких как cuprizone и, наконец, различные варианты экспериментального аутоиммунного энцефаломиелита (ЕАЕ) 3, 4. Хотя все они имитируют черты MS, они сильно отличаются друг в основных патологических функций, таких как вовлечение адаптивной иммунной системы. ЕАЕ является наиболее распространенным животная модель, как это особенно полезно исследовать нейровоспалительных пути и часто служит "доказательством правильности принципа" модели для эффективности новых стратегий лечения 5,6. EAE могут быть индуцированы в различных животных (например, мышей, крыс, miniswine, морских свинок, кур, или приматов). Однако, мыши стали наиболее широко использовать виды, которые по крайней мере частично из-зана расширение репертуара сложной трансгенных или нокаутом мышей 7.
Патофизиология EAE основан на реакции иммунной системы против мозгоспецифических антигенов. Эта реакция вызывает воспаление и разрушение несущих конструкций антиген, в результате неврологических и патологических особенностей, которые сопоставимых тем, которые наблюдаются у больных с МС. Три различных подхода можно выделить: Активно-индуцированной ЕАЕ (aEAE; активная иммунизация), пассивно передается ЕАЕ (pEAE; передача энцефалитогенных клеток от иммунизированных животных), а в последнее спонтанные модели ЕАЕ мыши (SEAE), которые позволяют изучение аутоиммунных механизмы без экзогенного манипуляции. Самый простой индуцибельный модель aEAE у мышей, дающих в быстрых и надежных результатов. Эта модель считается "золотым стандартом" в neuroimmunological животных моделях многими исследователями в области 8.
Для индукции aEAE, животноеиммунизируют подкожной инъекции эмульсии, состоящей из выбранного антигена и завершить адьюванте Фрейнда (CFA) в сопровождении внутрибрюшинного введения коклюшного токсина в день иммунизации и через два дня. Следовательно, миелин-специфические Т-лимфоциты являются активированными на периферии и мигрируют в ЦНС через гематоэнцефалический барьер. После вступления в ЦНС, Т-клетки активируются местными и проникают антиген-представляющих клеток, приводящих к последующей воспалительные каскады, участия других клеток, таких как моноциты или макрофаги и в конечном итоге в демиелинизации и аксонов гибели клеток 9. В зависимости от протокола иммунизации и комбинации линии мышей (например C57BL / 6, SJL / J, Biozzi) и антиген (например, миелин олигодендроцитов гликопротеин (MOG), основной белок миелина (МВР), миелин протеолипид белок (PLP)), болезнь Конечно можно взять острый, хронический прогрессивный или рецидивирующее течение смягчая болезнь.
мыши C57BL / 6 стали наиболее часто используемый штамм для строительства трансгенных мышей и растущее множество нокаутом или трансгенных мышей доступно. Мы здесь описывать протокол для иммунизации мышей C57BL / 6 с MOG 35-55 пептида 10, что приводит к однофазной EAE с первым симптомов после 9-14 дней, максимум болезни около 3-5 дней после начала заболевания и медленное и частичное восстановление симптомов в течение ближайших 10-20 дней. Как иммуногенный потенциал только MOG 35-55 пептида не является достаточным, чтобы вызвать заболевание, адъюванты, такие как CFA являются необходимыми. Предполагается, что компоненты CFA активировать мононуклеарных фагоцитов индуцировать фагоцитоз этих молекул и секрецию цитокинов. Это приводит к продлению присутствии антигенов и более эффективной транспортировке их к лимфатической системы. Индукции ЕАЕ способствует применению коклюшного токсина (СТ), который среди прочего было предложено, чтобы модулироватьгематоэнцефалический барьер и сама 11 иммунологическая реактивность. После индукции заболевания, особое внимание должны быть приняты для ежедневного оценки мышей для симптомов заболевания.
протокол
1. Общие комментарии для экспериментов мыши
- Все эксперименты на мышах должны выполняться в соответствии с руководящими принципами соответствующей институциональной уходу и использованию животных комитета.
- Держите мышей под свободных от патогенов условиях и дать им возможность иметь доступ к пище и воде вволю. Примечание: Важно использовать возрасту и полу соответствием мышей в экспериментальных группах, потому что восприимчивость к болезни может варьироваться от возраста и пола.
- В зависимости от выбранных условий эксперимента, иммунизированных Sham контрольная группа может рассматриваться где MOG 35-55 пептид заменен либо PBS без антигена или nonencephalitogenic пептида.
- Пожалуйста, обратите внимание методологические аспекты Перед началом экспериментов (см. также ниже). Мы рекомендуем привлечь одну или две ослепленные наблюдателей для EAE скоринга.
2. Подготовка MOG 35-55 эмульсии
- 200 мкл соотношении МО 1:01G 35-55 Раствор пептида и CFA следует вводить в каждой мыши. Существует некоторая потеря вязкой эмульсии при подготовке и инъекционных наркотиков. Таким образом, подготовить 1,5-2x в нужном количестве. Рассчитать общий объем эмульсии и разделить на 2 при необходимых количеств как MOG 35-55 раствора пептида и CFA.
- Развести лиофилизированный MOG 35-55 в DDH 2 O в конечной концентрации 2 мг / мл. Мы обычно используем 200 мкг MOG 35-55 пептида на мыши. Это количество содержится в 100 мкл исходного раствора. Раствор пептида следует хранить при температуре -20 ° С.
- Поместите содержание 1 флакон усохшего микобактерий туберкулеза H37Ra (100 мг) в ступке.
- Участок с помощью ступки и пестика с получением тонкого порошка.
- Добавьте 10 мл адъювантов неполном адъюванте Фрейнда с получением исходного раствора 10 мг / мл CFA, которые можно хранить при температуре 4 ° С.
- До иммунизации, развести CFA исходный раствор остроумиеч IFA в конечной концентрации 2 мг / мл. Тщательно перемешать перед каждым использованием, чтобы ресуспендировать порошковый материал и рассмотреть некоторые потери громкости вязкого раствора во время экспериментальных препаратов.
- Смешать 1:1 с MOG 35-55 раствора пептида до конечной концентрации 1 мг / мл не будет достигнута.
ВНИМАНИЕ: Тепло-убил микобактерии туберкулеза стимулирует врожденный иммунный ответ. Избегайте вдыхания, проглатывания и контакта с кожей и глазами.
- Предварительного охлаждения решения на льду.
- Составление 1 мл 2 мг / мл CFA и 1 мл 2 мг / мл MOG 35-55 раствора на две 2 мл шприцы. Рассчитать количество шприцев, необходимых в соответствии с количеством иммунизированных животных.
ВНИМАНИЕ: Строго избежать сшивания при подготовке вспомогательного как это может вызвать гранулемы или вызвать аутоиммунные реакции. - Используйте 27 г канюли для решения MOG 35-55 и 20 г канюли для CFA. Избегайте воздушных пузырьков и подключить оба шприцы с наHREE-ходового клапана.
- Отправить эмульсии из одного шприца в другой и тщательно перемешать в течение не менее 10 мин, как хороший эмульгирования является важным шагом. Рядом-закрыть трехстороннюю-клапан для поддержки эмульсии. Решение должно быть белым, жесткая и вязкая без разделения фаз.
- Эмульсия может храниться в течение нескольких дней до иммунизации. Подождите не менее 30 минут после приготовления эмульсий для наблюдения, являются ли они стабильными. До иммунизации, обратить решение к одной из двух шприцев и подключить 27 г канюли.
- Составление 1 мл 2 мг / мл CFA и 1 мл 2 мг / мл MOG 35-55 раствора на две 2 мл шприцы. Рассчитать количество шприцев, необходимых в соответствии с количеством иммунизированных животных.
3. Подготовка Токсин коклюша
- Различные количества токсина коклюша можно найти в литературе, который также зависит от пути введения (например, внутривенно или интраперитонеально). Наша лаборатория использует 400 нг коклюшного токсина в 200 мкл PBS внутрибрюшинно в день иммунизации и через два дня. ВНИМАНИЕ: Токсин коклюша имеет много биологических эффектов. Избегайте вдыхания, проглатывания и контакта с кожей и глазами.
- Развести 50 мкг коклюшного токсина в 500 мкл DDH 2 O в течение 100 мкг / мл исходного раствора. Хранить при 4 ° С.
- Развести 1:50 ЗФР. 200 мкл теперь содержат 400 нг PBS. Подготовьте необходимое количество шприцев и рассмотреть дополнительный избыток объем ~ 100 мкл для каждого втулке иглы.
4. Животных иммунизации
- Пожалуйста, обратитесь к институциональной уходу и использованию животных комитета конкретных критериев, необходимых краткосрочных эвтаназии. В нашей лаборатории использует краткое наркотизации с изофлуран, тогда как другие протоколы, такие как инъекции кетамина / ксилазина или halothan также может быть возможным. Подождите анестезии и использовать переднюю ногу носок щепотку, чтобы оценить уровень анестезии.
- Убедитесь в том, что иммунизация осуществляется опытного человека, чтобы минимизировать стресс для животных и для обеспечения оптимальной иммунизации.
- Введите 100 мкл антипоколения / CFA эмульсия подкожно в двух разных местах на каждой задней фланге. Убедитесь, что луковичные массовые формы под кожей, которые должны сохраняться в течение всего эксперимента.
- Введите 200 мкл коклюшного токсина intraperitonelly.
- Убедитесь, что отдельные мыши могут быть легко идентифицированы для ежедневного оценки, например, цветовой маркировки, основание хвоста.
- Администрирование вторую дозу токсина коклюша на после иммунизации двое суток.
5. ЕАЕ Мониторинг
- Вес и клиническая оценка должна быть оценена в день. Наступление EAE обычно коррелирует с потерей веса, который может быть использован в качестве индикатора активности заболевания. Пожалуйста, обратитесь к институциональной ухода за животными и использовать комитет предопределить критерии, когда отдельные мыши должны быть выведены из экспериментов. Это следует учитывать при потери веса превышает 20% от исходной массы тела или при тяжелых клинических признаков (ЕАЕ забить 7 или хуже) происходит. Пожалуйста, обратитесь к репроспективных руководящие принципы соответствующей институциональной уходу и использованию животных комитета разрешенных максимальных баллов.
- Когда мыши имеют клинические симптомы EAE, важно обеспечить, чтобы бутылки с водой все же может быть достигнута и, что пища помещается на полу клетки.
- Различные симптомы скоринга могут быть использованы. В нашей лаборатории устанавливается шкала 0-10.
| Класс | Клиническая знак | Комментарий |
| 0 | Нет клинические признаки | Нормальная походка, хвост движется и может быть поднята, хвост обтекает круглый объект, если мышь проводится в основании хвоста |
| 1 | Частично хромать хвост | Нормальная походка, кончик хвоста отвисает |
| 2 | Парализованный хвост | Нормальная походка, хвост свисает |
| 3 | Задней конечности парезы, несогласованные движения | Нескоординированное походка, хвост хромает, задние конечности реагировать на ущемление |
| 4 | Один задних конечностей парализована | Нескоординированное походка с одной задней конечности увлечения, хвост хромает, один задних конечностей не отвечает ущипнуть |
| 5 | Обе задние конечности парализованы | Нескоординированное походка с обеих задних конечностей, тянущих, хвост хромает, обе задние конечности не реагируют на ущипнуть |
| 6 | Задние конечности парализованы, слабость в передних конечностей | Нескоординированное походка с передними конечностями бороться, чтобы вытащить тело, передние конечности рефлекс после сжимать, хвост хромает |
| 7 | Задние конечности парализованы, один передних конечностей парализована | Мышь не может двигаться, один передних конечностей реагирует на палец щепотку, хвост хромает |
| 8 | Задние конечности парализованы обе передние конечности парализованы | Мышь не может двигаться, как передние конечности не реагируют на носок крайнем случае, хвост хромает |
| 9 | Умирающий | Нет движения, изменения дыхания |
| 10 | Смерть |
Таблица 1. Клиническая система подсчета очков.
Результаты
После иммунизации мышей должны быть оценены в день в течение изменений в весе и клинических симптомов. Болезнь начала, как правило, коррелирует со снижением веса, которые могут начать за 1-2 дня до могут видеть симптомы EAE. Клинические признаки EAE обычно начинаются в день 9 и 14 после иммунизации. Как поражения преимущественно локализуется в спинном мозге в MOG-EAE в C57BL / 6 мышей, они обычно развиваются преимущественно моторные симптомы в каудальнее ростральной узором. Примерный фото из иммунизированной мыши с симптомами EAE (оценка 6) изображена на рисунке 1а. Некоторые атипичные симптомы EAE также может иметь место, например, переходящего в аксиально-роторный образом, сгорбившись появление или повышенной чувствительности, которые не отражены в классической EAE оценка приведены в таблице 1. Как моторные симптомы являются основной характеристикой в этой модели, это оценка дает нам хорошим показателем тяжести заболевания. Различные системы мониторинга (например, счет 0 -5 или 0-6) и более сложные композитные оценки, оценивающих разные дефициты были также опубликованы. Пожалуйста, обратите внимание, что мыши с тяжелыми симптомами должны быть выведены из эксперимента в соответствии с соответствующей институциональной уходу и использованию животных комитета. Мыши показать как правило, частичное восстановление симптомов в течение ближайших 10-20 дней. Представитель течение заболевания изображен на рисунке 1b. Существуют различные моменты времени в течение ЭАЭ, которые представляют интерес для оценки параметров исхода. Некоторые типичные анализы, которые часто могут быть найдены, описаны очень кратко. В максимума заболеваний, мыши могут быть оценены для продукции цитокинов или пролиферации после повторной стимуляции изолированных клеток иммунной системы с MOG 35-55 пептида в пробирке (MOG напомним анализа). Иммунные клетки также могут быть выделены из мозга и спинного мозга мышей с ЕАЕ симптомов и дальнейшей обработке, например, с помощью проточной цитометрии. Гистологический анализ срезов спинного мозга может быть выполнена при заболевании мaximum для поражения нагрузки и демиелинизации, в более позднее время в то время как указывает маркеры для нейродегенерацией и гибели нейронов может представлять интерес.
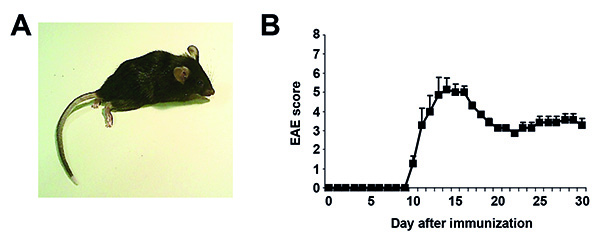
Рисунок 1. Результаты представитель EAE. А. Представитель картина иммунизированного C57BL / 6 мыши с симптомами EAE (ЭАЭ забить 6). Болезнь Конечно Б. Представитель после иммунизации в течение 30 дней. Данные представлены в виде среднего и стандартного ошибка среднего (п = 5). Нажмите здесь, чтобы увеличить изображение .
Обсуждение
Множество различных моделей EAE с активными протоколов иммунизации была описана в последние десятилетия. В то время как модели крысы не были широко использованы до недавнего времени, мыши теперь самая популярная модель организм для исследований EAE. Такое развитие событий является среди прочего в связи с широким и постоянно растущим репертуара доступных трансгенных мышей. Иммунизация мышей C57BL / 6 с MOG 35-55 пептида является одним из самых распространенных моделей EAE и может рассматриваться в качестве надежного, воспроизводимого и животной модели также в использовании. Во многих neuroimmunological лабораторий, МНГ 35-55 индуцированной ЕАЕ устанавливается как модель выбора в то время как другие модели ЕАЕ используются для более конкретных экспериментальных вопросов.
Критическая точка рассмотреть является планирование экспериментальных установок для того, чтобы EAE эксперименты проводятся методологически правильно. Для внутренней валидности, ослепленный забил симптомов заболевания рекомендуется. Экспериментальныйтальные группы должны быть возрастное, вес-и секс-соответствуют и мышей следует случайным образом распределены по группам лечения. Эксперименты всегда должны быть выполнены в соответствии с правилами защиты животных. Исследования EAE часто недостаточна и не принимать во внимание статистические ошибки типа II. Таким образом, до экспериментов, расчетов размера выборки должны быть выполнены. Необходимые размеры групп зависит от ожидаемого размера эффект. Консультация эксперта для статистического анализа можно было бы считать, прежде чем начать EAE эксперименты.
Некоторые ограничения протокола нужно иметь в виду,. Самое главное, интерпретации данных aEAE скомпрометирована режиме иммунизации с использованием адъюванта и коклюшного токсина, которые имеют как дополнительное воздействие на иммунологической реакции. Кроме того, следует учитывать, что модель MOG 35-55 EAE показывает главным образом клетки CD4 + T приводом иммунологическую реакцию. CD8 + Т-клетки и В-клетки играютменее заметную роль и альтернативные протоколы следует учитывать при решении этих типов клеток. Ожидаемая течение заболевания острый, монофазные и самоограниченными. В качестве альтернативы, ремиттирующим течение заболевания также может быть достигнуто в альтернативных моделей EAE. Еще одним важным ограничением протокола определенный уклон в сторону иммунологическим компонентом патофизиологии MS. В последние годы, она становится все более ясно, что МС имеет сильную нейродегенеративного компонент. Смерть олигодендроцитов и нейронов приводит к прогрессивному накоплению неврологического дефицита. Следует принимать во внимание, что модель EAE могут быть не полностью подходят для решения вопросов, связанных эксперимента нейродегенеративных механизмы аутоиммунного воспаления. Альтернативные модели животных с акцентом на патологией ЦНС могут быть рассмотрены - например, cuprizone модели, которая ставит под угрозу токсичных демиелинизацию без участия периферической иммунной системы.
Описанный протокол можно рассматривать как основной neuroimmunological экспериментальной модели и могут быть изменены для других приложений. Экспериментальная процедура, описанная выше, может быть легко применены к другим протоколам EAE путем изменения штаммов мышей или тип и количество белка (например, использовать PLP 139-151 пептид и мышей SJL для ремиттирующего EAE заболевания курс, который особенно подходит для оценки терапевтического воздействие на рецидивов). Описанный протокол также может быть использован для проведения экспериментов приемный переноса (пассивный EAE). В этой модели C57BL / 6 мышей, иммунизированных MOG 35-55 пептида и CFA, как описано выше. В противоположность этому, коклюшный токсин не требуется. После 7-15 дней, селезенки или лимфоузлов изолированы и иммунные клетки повторно стимулировали в пробирке с MOG 35-55 пептида и различных цитокинов предварительного передать в новую группу мышей C57BL/6se. Эти мыши-получатели развивать EAE на несколько дней раньше, чем на класSical иммунизации. условия в искусственных условиях можно варьировать для специфических иммунологических вопросов (например, поляризацию в T H 1 или T H 17 клеток).
Иногда, низкий уровень заболеваемости или слабые симптомы могут быть экспериментальная задача. Некоторые рекомендации для устранения неполадок являются:
- Тяжесть заболевания можно варьировать с различными количествами пептида / мышь.
- Концентрация Оптимальное CFA может варьировать от 1-5 мг / мл. Рассмотрим титрования CFA при установлении эксперименты. Пожалуйста, обратитесь к соответствующим рекомендациям соответствующей институциональной уходу и использованию животных комитета допустимых концентрациях КФА столько Правила запрещают концентрации CFA, превышающие 2 мг / мл.
- Различные способы описаны для приготовления эмульсии. Альтернативные методы, такие как вортексе в течение 1 часа или ультразвуком можно было бы считать, если бедный эмульгирование рассматривается как Possibле источник ошибки.
- Возраст, пол, время года и условий окружающей среды в учреждении животных являются важными факторами, которые влияют на EAE восприимчивость. Следует обеспечить, чтобы условия сравнимы между независимых экспериментов.
Как описано выше, упомянутый протокол может быть использован в качестве начальной точки для приемных экспериментов EAE. Эта модель особенно подходит для разделения периферийные и ЦНС эффекты генетического фенотипа (например, путем передачи энцефалитогенных нокаутом клетки в мышей-реципиентов дикого типа) и для специфических иммунологических вопросов, как фенотип переданных клеток может быть полностью описана. Новейшая разработка в области исследований EAE в последние годы являются клеточных рецепторов трансгенные мыши T. Эти мыши появляются симптомы EAE спонтанно, без внешнего воздействия обойти проблему адъювантной прививки. Тем не менее, эта модель требует большого количества животных для breediнг обеспечить достаточные размеры групп. Оценка мышей с требуется скрещивание до EAE экспериментов в отличие от aEAE. Как каждая мышь развивается симптомы заболевания в другой день, оценка новых веществ может быть довольно сложным. Таким образом, значение классического aEAE для neuroimmunological остается без ответа.
Раскрытие информации
Авторы заявляют каких конкурирующих финансовых интересов.
Благодарности
Эта работа была поддержана Междисциплинарного Центра клинических исследований (IZKF) Мюнстер (SEED 03/12, СО).
Материалы
| Name | Company | Catalog Number | Comments |
| Female C57BL/6 mice, age 10-12 weeks, ~20 g weight | e.g. Jackson Laboratory, Charles River | ||
| MOG35-55 (MEVGWYRSPFSRVVHLYRNGK) | e.g. Pepceuticals Ltd | Store at -20 °C | |
| Incomplete Freund’s adjuvant (IFA) | e.g. Sigma-Aldrich Co. | F5506 | Store at 4 °C |
| Syringes, 1 ml with 26 G 3/8 in needle | e.g. Becton Dickinson & Co. | 309625 | |
| Syringes, 2 ml | e.g. B. Braun | 7389 | |
| Needles, 25 G 5/8 in and 30 G 1/2 in | e.g. Becton Dickinson & Co., | 305122, 305106 | |
| Three way valve | e.g. B. Braun | 16494 C | |
| Pertussis toxin, lyophilized in buffer | Enzo Life Sciences Inc. | BML-G100 | Store at 4 °C |
| M. tuberculosis H37 RA | BD Difco | 231141 | Store at 4 °C |
Ссылки
- McFarland, H. F., Martin, R. Multiple sclerosis: a complicated picture of autoimmunity. Nat. Immunol. 8, 913-919 (2007).
- Wiendl, H. Neuroinflammation: the world is not enough. Curr. Opin. Neurol. 25, 302-305 (2012).
- vander Star, B. J., et al. In vitro and in vivo models of multiple sclerosis. CNS Neurol. Disord. Drug Targets. 11, 570-588 (2012).
- Pachner, A. R. Experimental models of multiple sclerosis. Curr. Opin. Neurol. 24, 291-299 (2011).
- Bittner, S., et al. The TASK1 channel inhibitor A293 shows efficacy in a mouse model of multiple sclerosis. Exp. Neurol. 238, 149-155 (2012).
- Handel, A. E., Lincoln, M. R., Ramagopalan, S. V. Of mice and men: experimental autoimmune encephalitis and multiple sclerosis. Eur. J. Clin. Invest. 41, 1254-1258 (2011).
- Krishnamoorthy, G., Wekerle, H. EAE: an immunologist's magic eye. Eur. J. Immunol. 39, 2031-2035 (2009).
- Stromnes, I. M., Goverman, J. M. Active induction of experimental allergic encephalomyelitis. Nat. Protoc. 1, 1810-1819 (2006).
- Fletcher, J. M., Lalor, S. J., Sweeney, C. M., Tubridy, N., Mills, K. H. T cells in multiple sclerosis and experimental autoimmune encephalomyelitis. Clin. Exp. Immunol. 162, 1-11 (2010).
- Mendel, I., Kerlero de Rosbo, N., Ben-Nun, A. A myelin oligodendrocyte glycoprotein peptide induces typical chronic experimental autoimmune encephalomyelitis in H-2b mice: fine specificity and T cell receptor V beta expression of encephalitogenic T cells. Eur. J. Immunol. 25, 1951-1959 (1995).
- Hofstetter, H. H., Shive, C. L., Forsthuber, T. G. Pertussis toxin modulates the immune response to neuroantigens injected in incomplete Freund's adjuvant: induction of Th1 cells and experimental autoimmune encephalomyelitis in the presence of high frequencies of Th2 cells. J. Immunol. 169, 117-125 (2002).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены